CASO CLÍNICO
Paciente femenina de 40 años de edad, con diagnóstico de insuficiencia renal crónica desde 1995, secundaria a preeclampsia severa que ameritó tratamiento con hemodiálisis. En enero de 2004 se realizó trasplante renal de donador vivo relacionado (hermano), pero tuvo rechazo, infecciones urinarias de repetición y estenosis de anastomosis ureterovesical, por lo que continuó con terapia sustitutiva, con tres sesiones por semana. Su padecimiento inició con dolor torácico generalizado que inicialmente cedía a la administración de analgésicos y posteriormente se agregó dolor intenso en la cadera de predominio del lado izquierdo, irradiado hacia la pierna, que progresivamente la llevó a incapacidad para la deambulación y uso de silla de ruedas en el transcurso de dos años, durante este tiempo fue tratada con múltiples analgésicos no esteroides, calcio oral, calcitriol y alendronato, sin respuesta clínica ni alivio del dolor. En su evaluación a la exploración física destacó peso de 50 kg, talla de 1.52 m (previa de 1.57 m), dolor intenso a la movilización de la pierna izquierda y en la pelvis e hipotrofia muscular. En los análisis de laboratorio se obtuvieron los siguientes resultados: leucocitos 4.84 mm3, hemoglobina 10.3 g/ dL, hematócrito 30.6%, plaquetas 175,000 mm3, glucosa 97 mg/dL, BUN 64 mg/dL, urea 136.96 mg/dL, creatinina 8.0 mg/dL, ácido úrico 5.9 mg/dL, sodio 136 mmol/L, potasio 5.2 mmol/L, calcio sérico 8.6 mg/dL, fósforo sérico 5.3 mg/ dL, albúmina 3.8 g/dL, concentraciones de 25-hidroxivitamina D 16 ng/mL, fosfatasa alcalina 1,246 UI/L y paratohormona intacta (PTH intacta) 2,600 pg/mL (Cuadro 1). La radiografía de tórax evidenció prominencias óseas a nivel de los arcos costales y en la pelvis una lesión en el lado izquierdo, heterogénea e irregular, así como disminución importante del estado de mineralización ósea, por lo que se realizó estudio complementario con tomografía computada que reportó una lesión lítica, expansiva, con adelgazamiento de la cortical de 87x43 mm en el isquión izquierdo, así como múltiples lesiones líticas en los arcos costales 6 y 8 del lado derecho y 5, 7 y 10 del lado izquierdo (Figuras 1 y 2).
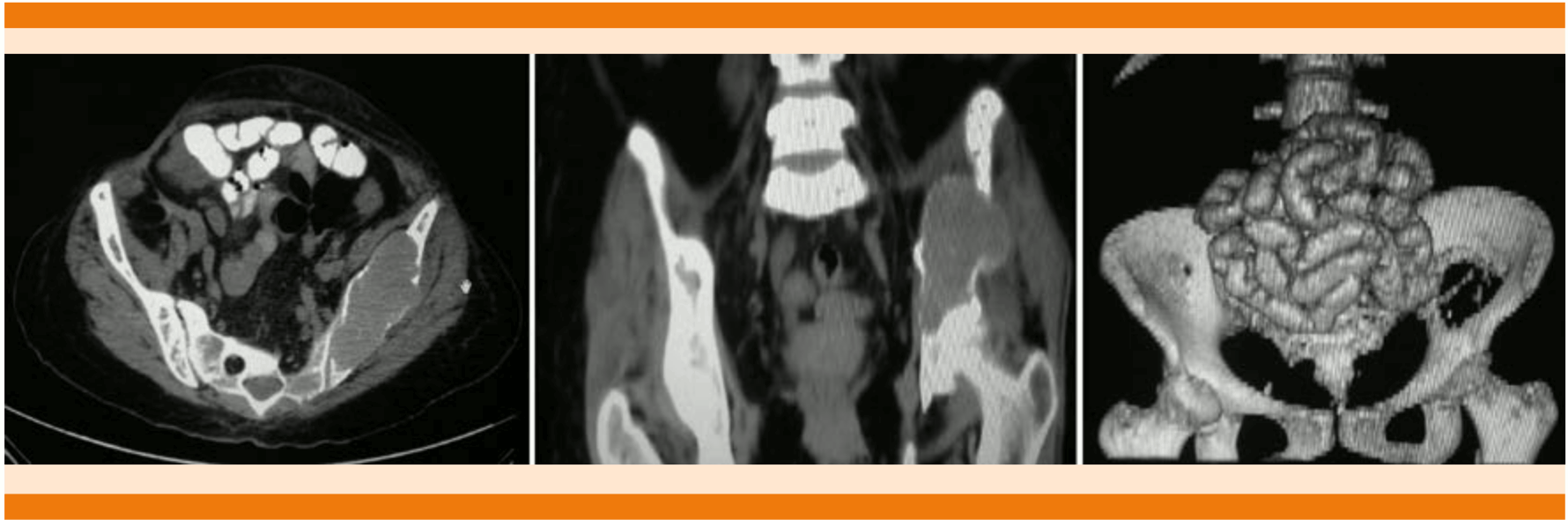
Figura 1 Lesión lítica de 87x43 mm, con adelgazamiento de la cortical en el isquion del lado izquierdo.
La biopsia de la lesión en la pelvis reportó células gigantes osteoclásticas de distribución irregular con depósitos de hemosiderina compatible con tumor pardo (Figura 3). La paciente rechazó tratamiento quirúrgico (paratiroidectomía subtotal) por lo que se inició manejo médico con cinacalcet, 30 mg/día durante un mes, y posteriormente se incrementó la dosis a 60 mg/día, calcio 500 mg/12 horas, vitamina D 2,000 U/día y calcitriol 0.25 mg/día. A los cuatro meses de iniciado el tratamiento, la paciente tenía mejoría clínica respecto a la intensidad del dolor y descenso en las concentraciones de PTH intacta a 503 pg/ mL y fosfatasa alcalina a 224 UI/L. En la actualidad la paciente continúa en hemodiálisis, con tratamiento médico y se encuentra nuevamente en protocolo de trasplante renal de donador cadavérico.
DISCUSIÓN
El hiperparatiroidismo secundario es producido por cambios en el metabolismo óseo y mineral debido al deterioro progresivo de la función renal; la disminución en la producción renal de 1-25 hidroxivitamina D (forma activa), concentraciones elevadas del factor fibroblástico 23 y la hiperfosfatemia favorecen la hiperplasia de las glándulas paratiroides aumentando la síntesis y secreción de PTH intacta.1
Los tumores pardos son lesiones óseas benignas con incidencia de 1.5 a 1.7% en pacientes con enfermedad renal crónica, debido al remodelado óseo acelerado, secundario a concentraciones persistentemente elevadas de PTH intacta, las localizaciones más frecuentes son las costillas, las clavículas, la pelvis y la mandíbula.2 En términos histológicos, están formados por microhemorragias, macrófagos y células gigantes multinucleadas del tipo osteoclástico en un estroma fibrovascular, predominan los depósitos de hemosiderina que le confieren el color pardo.3
El diagnóstico de hiperparatiroidismo secundario en pacientes con insuficiencia renal terminal se realiza por sospecha clínica y al demostrar cambios bioquímicos, como hipocalcemia o normocalcemia, hiperfosfatemia y elevación de las concentraciones de PTH intacta (>350 pg/mL).4 Debido a que la enfermedad resulta de la hiperplasia de las glándulas paratiroides, la sensibilidad y especificidad de los estudios de imagen preoperatorios, como el ultrasonido de cuello y el gammagrama paratiroideo, son bajas respecto a la localización de adenomas paratiroideos en hiperparatiroidismo primario.5 La sensibilidad en la detección de hiperplasia paratiroidea del gammagrama es de 32 a 81%, con media de 43%.6 Un estudio detectó 32 de 60 paratiroides hiperplásicas con gammagrama con sestamibi en un grupo de pacientes con insuficiencia renal crónica y la detección de lesiones hiperplásicas por ultrasonido y tomografía fue inferior a la detección con gammagrama, por lo que los pacientes con hiperparatiroidismo secundario a insuficiencia renal crónica que son aptos para someterse a cirugía ameritan la exploración de cuello y paratiroidectomía subtotal o total.7
El tratamiento depende de la severidad de las lesiones óseas, está dirigido a corregir el hiperparatiroidismo secundario, mediante la normalización de las concentraciones de calcio, fósforo, PTH intacta y marcadores de resorción ósea, con análogos de la vitamina D, suplementos de calcio, quelantes de fósforo y calcimiméticos.8
El cinacalcet es un agente calcimimético aprobado por la Dirección de Alimentos y Fármacos desde 2003 en el tratamiento de hiperparatiroidismo secundario y recientemente contra cáncer de paratiroides y en algunos casos de hiperparatiroidismo primario; actúa modificando la función de las células principales del receptor de sensor de calcio a nivel de las glándulas paratiroideas disminuyendo la secreción de PTH intacta para normalizar las concentraciones séricas de calcio y fósforo.9 La dosis inicial es de 30 mg/día con incremento cada dos a cuatro semanas hasta una dosis máxima de 180 mg/día, sus efectos secundarios más comunes son en el aparato gastrointestinal, como náusea y vómito, pero el efecto más importante es la hipocalcemia, por lo que deben vigilarse las cifras de calcio sérico y evitar su administración si se tienen concentraciones de calcio sérico menores a 8.0 mg/dL. Existe disponibilidad del fármaco en México, pero su costo es elevado. Un estudio con distribución al azar en un grupo de 371 pacientes en hemodiálisis con hiperparatiroidismo secundario descontrolado demostró que la administración de cinacalcet a dosis de 30 a 180 mg al día, disminuyó en 43% las concentraciones de PTH intacta y se obtuvo mejoría del producto calcio-fósforo en comparación con placebo a las 26 semanas de seguimiento.10
En casos muy severos o resistentes al tratamiento médico, es necesaria la paratiroidectomía subtotal (resección de 3½ glándulas) o paratiroi-dectomía total (resección de cuatro glándulas con o sin autotrasplante de remanente paratiroideo en el antebrazo); la disminución de 50% de las concentraciones de PTH intacta intraoperatoria respecto a las concentraciones basales sugiere éxito quirúrgico. Es importante la vigilancia posoperatoria de las concentraciones de calcio por riesgo de síndrome de hueso hambriento (estado de remineralización ósea acelerada), por lo que el tratamiento con calcio, calcitriol y análogos de la vitamina D ayuda a prevenir la hipocalcemia. El riesgo de recurrencias después de la cirugía es variable y las causas principales son hiperplasia del remanente paratiroideo, mala técnica quirúrgica o glándulas ectópicas. Entre las indicaciones absolutas de tratamiento quirúrgico de hiperparatiroidismo secundario están la falla e intolerancia al tratamiento médico, elevación persistente de PTH intacta mayor a 800 pg/mL, enfermedad ósea severa, producto calcio-fósforo mayor a 70 y calcifilaxis.11
CONCLUSIÓN
La aparición de tumores pardos es una complica ción relativamente infrecuente y es el resultado de una manifestación ósea grave de hiperparatiroidismo descontrolado.12 El tratamiento efectivo médico o quirúrgico puede producir la regresión de los tumores y recuperación paulatina del estado de mineralización ósea.











 text new page (beta)
text new page (beta)





