El cempasúchil (Tagetes erecta) es una planta anual de la familia de las Asteraceae, originaria de México. Las flores son fuente de pigmentos amarillo-naranjas de carotenoides; especialmente de xantófilas, tales como la luteína (Deineka et al., 2007). Además de pigmentos, el cempasúchil también produce metabolitos con actividad antioxidante, hepatoprotectiva y nematocida (Gopi et al., 2012) y peculiarmente se usa como adorno en los rituales del Día de los muertos en México (Brandes, 1998).
Debido a la importancia del cempasúchil como fuente de metabolitos secundarios y componente del patrimonio cultural mexicano, se requiere información sobre los patógenos microbiales para definir estrategias de protección a los cultivos y prevenir pérdidas económicas, sobre todo para productores de pequeña escala. Las plántulas de cempasúchil cultivadas en el campo son susceptibles a Damping-off causado por el patógeno fúngico Ceratobasidium sp. (Saroj et al., 2013). A diferencia del Damping-off, las enfermedades causadas por bacterias podrían no impedir la producción de flores si emergen en las etapas tardías del desarrollo de la planta, y la comercialización de plantas enfermas contribuye a la propagación de la enfermedad. La marchitez bacterial causada por Pseudomonas solanacearum, así como las manchas foliares causadas por Pseudomonas syringae pv. tagetis están entre las enfermedades bacteriales más dañinas para el cempasúchil (Horst, 2013). P. syringae pv. tagetis fue reportada por primera vez como Pseudomonas tagetis (Hellmers, 1955) y causa clorosis apical en girasol (Helianthus annuus) y en la alcachofa de Jerusalén (Ambrosia tuberosa) (Gulya et al., 1982; Shane y Baumer, 1984). Además de sus efectos perjudiciales, este patógeno tiene el potencial de ser usado como agente de biocontrol, ya que causa clorosis y necrosis al ser inoculado en hierbas tales como el cardo de Canadá (Cirsium arvense) (Gronwald et al., 2002) y en la ambrosia arvense Ambrosia grayi (Sheikh et al., 2001). La clorosis quizá sea producida por la tagetitoxina, un inhibidor de la polimerasa de ARN plastidial (Mathews y Durbin, 1990).
Una nueva cepa bacterial que se asemeja a Pseudomonas syringae llamada LF2012 inicialmente fue aislada por el Dr. Leopoldo Fucikovsky+ (Colegio de Posgraduados) de plantas de cempasúchil enfermas. Se inocularon 1x108 CFU mL-1 por aspersión en tres plantas para demostrar los postulados de Koch. Después de la inoculación, las plantas se mantuvieron en una cámara de crecimiento bajo condiciones controladas de luz (aproximadamente 300 µmoles m-2s-1), temperatura (27 °C), fotoperiodos (16 h luz/8 h oscuridad) y humedad relativa (75%). Este experimento se repitió tres veces. En este conjunto de experimentos se usó P. syringae pv. tomato DC3000 como referencia del agente causal de enfermedades en Arabidopsis y tomate, y se incluyó a P. syringae pv. syringae 61 como una cepa sin huésped, ya que no causa enfermedad en la especie vegetal estudiada.
La clorosis, acompañada de un halo necrótico, se volvió visible cinco días después de su inoculación en las tres plantas examinadas en cada experimento (Figura 1). Las bacterias fueron re-aisladas de la planta enferma, lo que confirma que esta cepa es patogénica hacia el cempasúchil. Se realizaron ensayos de rango de huéspedes en plantas partenecientes a cinco familias diferentes, incluyendo Asteraceae, Amaranthaceae, Brassicaceae, Poaceae y Solanaceae (Valenzuela-Soto et al., 2015). Otras cepas fitopatogénicas fueron incluidas como testigos. Los resultados se encuentran resumidos en el Cuadro 1. LF2012 solo causó síntomas en plantas de cempasúchil, pero no así en otras plantas, incluyendo girasol (H. annuus) “flor pequeña” que también pertenece a Asteraceae, y ha sido reportada como huésped de P. syringae pv. tagetis (Rhodehamel y Durbin, 1985). Se realizaron ensayos con tres cultivares diferentes de girasol y en cualquier caso LF2012 no causó enfermedades en girasol, por lo que descartamos la posibilidad de nombrar la cepa como P. syringae pv. tagetis.

Figura 1 Síntomas de la enfermedad de manchas foliares en cempasúchil (Tagetes erecta) causada por P. syringae LF2012 (LF2012) cinco días después de inocular con aspersor. Las plantas con tratamientos simulados fueron rociadas con un amortiguador de fosfato (simulacro). Las plantas se mantuvieron bajo un fotoperiodo (16 h luz/8 hoscuridad), con luz de aproximadamente 300 μmoles m-2s-1, 28 °C y una humedad relativa de 75%.
Cuadro 1 Determinación del rango de huésped de Pseudomonas syringae LF2012. Los ensayos se realizaron al rociar una inoculación de suspensión bacterial (1x108 CFU mL-1) y se roció un amortiguador de fosfato como simulacro. P. syringae pv. tomato DC3000 se usó como cepa virulenta de A. thaliana y S. lycopersicum. P. syringae pv. syringae 61 se usó como testigo sin huésped.
| Experimental host | LF2012 | P. s. pv. tomato DC3000 | P. s. pv. syringae 61 | Mock | |
|---|---|---|---|---|---|
| Asteraceae | Tagetes erecta | + | - | - | - |
| Helianthus annuus “small flower” | - | - | - | - | |
| Brassicaceae | Brassica oleracea cv. Grandeur | - | - | - | - |
| Arabidopsis thaliana Col-0 | - | + | - | - | |
| Amaranthaceae | Amaranthus hypochondriacus | - | - | - | - |
| Amaranthus hybridus | - | - | - | - | |
| Poaceae | Zea mays cv A188 | - | - | - | - |
| Sorghum bicolor | - | - | - | - | |
| Solanaceae | Solanum lycopersicum cv. Río Fuego | - | + | - | - |
| Nicotiana tabacum cv. Xanthi | - | + | - | - |
Estos resultados sugieren que LH2012 es un patógeno adaptado causante de enfermedades en cempasúchil, pero es no adaptado para el acceso a las demás especies vegetales. Los patógenos no adaptados no causan una reacción cuando son inoculados con aspersión porque no acceden hacia adentro de la planta. Sin embargo, si el patógeno es forzado a invadir la mesófila, será percibido por la planta como un agente de riesgo y se inducirá una fuerte respuesta de defensa. La detección de moléculas derivadas de patógenos dispara la resistencia del no-huésped, que suele caracterizarse por una respuesta hipersensible o la muerte celular en el sitio de infiltración que restringe la propagación del patógeno (Lee et al., 2017). Para confirmar que LH2012 tiene características de patógeno no adaptado hacia otras especies, se realizaron infiltraciones de 1x108 CFU mL-1 de LH2012 en hojas de tabaco. LF2012 causó puntos semejantes a una reacción de hipersensibilidad (RH) (Figura 2). Como se esperaba para esta reacción, se limitó al sitio de infiltración, sin importar el tiempo de incubación de las plantas. Este resultado sugiere que se reconoce a LH2012 como un patógeno en una planta no huésped cuando se inocula directamente en la mesófila.

Figura 2 P. syringae LF2012 causa una respuesta similar al RH en hojas infiltradas de tabaco (Nicotiana tabacum) (LF2012). Las plantas testigo fueron infiltradas con amortiguador de fosfato (simula ción). Las plantas en maceras se matuvieron bajo condiciones controladas de luz, temperatura y humedad. Las fotografías de las plantas fueron tomadas 5 días después de infiltrarse.
El perfil metabólico se llevó a cabo con la prueba BIOLOG como una primera aproximación para identificar a las especies de LF2012. LF2012 se inoculó en el medio de crecimiento universal Biolog y se incubó a 28 °C. Los datos fueron obtenidos y analizados con el software de datos MicroLog versión 4.2. El perfil se relaciona con patovares de P. syringae. Asimismo, el uso de myo-inositol, D-sorbitol, D-manosa, D-fructosa, α-D-glucosa, sacarosa, L-fucose y maltosa como fuentes de carbono fueron similares a las fuentes reportadas para P. syringae pv. tagetis (Rhodehamel y Durbin, 1985). La identificación como P. syringae pv. tagetis no fue posible, ya que el perfil metabólico de este patovar no está incluido en la base de datos disponible.
La secuencia del gen ARNr 16S es ampliamente usado como un gen codificado y es usado en la construcción de relaciones filogenéticas dentro de las procariotas. Específicamente, en Pseudomonas ha sido útil para redistribuir algunas especies de Pseudomonas en otros géneros (Mulet et al., 2010). El género de Pseudomonas se divide en dos linajes: aeruginosa y fluorescens. Pseudomonas syringae se clasifica en el linaje de fluorescens y siete genomoespecies (Gs) dentro de P. syringae son discernibles por análisis filogenético (Marcelletti y Scortichini, 2014).
El gen ARNr 16S de LF2012 se amplificó y clonó con los siguientes procedimientos experimentales reportados anteriormente por nuestro grupo de trabajo (Valenzuela-Soto et al., 2015). El plásmido purificado fue sujeto a una secuenciación capilar en un Analizador de ADN ABI PRISM 3700 (Applied Biosystems) usando el promotor T7 y los oligonucleótidos en reversa M13 que coinciden con las secuencias flanqueantes de pCR-XL-TOPO (Invitrogen). La secuencia fue depositada en el GenBank bajo el número de Acceso KP796138.1. La secuencia de ARNr 16S de LF2012 y las secuencias correspondientes de las cepas representativas de ambos linajes de Pseudomonas fueron alineadas con el algoritmo ClustalW. Una vez alineados, se creó un árbol filogenético con el método de unión de vecinos. Ambos procedimientos bioinformáticos fueron llevados a cabo en MEGA6 (Tamura et al., 2013). El árbol filogenético muestra que la secuencia de ARNr 16S de LF2012 está agrupada en el linaje de fluorescens y tiene una estrecha relación con las genomoespecies Gs3, Gs6, Gs8, Gs9 (Figura 3). Las secuencias del linaje de aeruginosa están claramente separadas de fluorescens. Las genomoespecies con relación estrecha con LF2012 pertenecen al grupo P. syringae (Mulet et al., 2010). La secuencia de referencia de P. syringae pv. tagetis usada en el presente análisis (AB001449.1) está agrupada con otras cepas fitopatogénicas, pero P. syringae LF2012 está excluido de este subárbol. El árbol también muestra que LF2012 tiene menos relación con otros linajes de especies fluorescens tales como P. putida y P. savastanoi. Por lo tanto, clasificamos a esta cepa como Pseudomonas syringae LF2012. Se requiere analizar otros marcadores para determinar la relación con P. syringae pv. tagetis o secuencias de cepas de referencias para las genomoespecies 7, tales como P. syringae pv. helianthi, que hasta ahora es insuficiente.
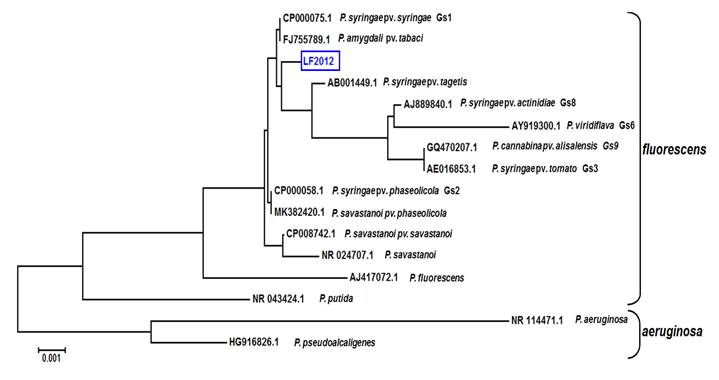
Figura 3 Árbol filogenético que muestra la relación del Pseudomonas syringae LF2012 aislado de plantas de cempasúchil con un subconjunto de cepas y especies de relación cercana. El número de acceso de cada secuencia usada está indicado en la rama antes del nombre.
Se llevó a cabo un perfil de macrorestricción al digerir el ADN genómico de LF2012 y nuestras cepas testigo con I-CeuI. Los productos de restricción fueron separados por electroforesis en gel de campo pulsado (PFGE, por sus siglas en inglés) (Figura 4). El patrón de restricción de LF2012 (línea A, Figura 4) fue como el perfil de P. syringae pv. syringae 61 del Gs1 (línea B, Figura 4), pero no se detectaron fragmentos comunes entre LF2012 y P. syringae pv. glycinea (línea C, Figura 4), miembro del grupo amygdali dentro del linaje de fluorescens (Gomila et al., 2017). Las diferencias y semejanzas en estos patrones de restricción respaldan la clasificación de la cepa como P. syringae LF2012.
En conclusión, los resultados obtenidos en el presente estudio para el perfil bioquímico y el análisis molecular permitieron identificar a esta bacteria como Pseudomonas syringae LF2012, un patógeno que causa síntomas de la enfermedad de manchas foliares en el cempasúchil. Es avirulenta en otra planta Asteraceae y plantas de otras familias, y dispara reacciones semejantes a HR en hojas de tabaco infiltradas. La secuenciación de genoma completo de esta nueva cepa permitirá determinar la clasificación precisa que ayuda en métodos moleculares de patógenos de cempasúchil y en la identificación de factores de virulencia que ilustran la base molecular de la enfermedad. Debido a la relación con P. syringae pv. tagetis, su potencial como biocontrol de malezas puede ser explorado.
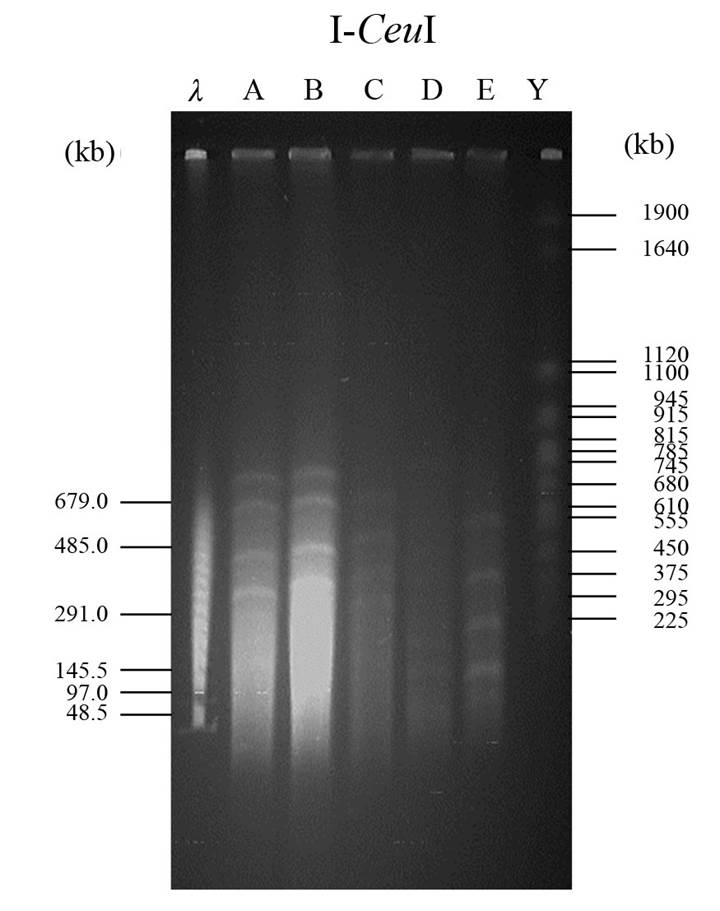
Figura 4 Perfiles de macrorestricción de Electroforesis en gel de campo Pulsado (PFGE) producidos por P. syringae LF2012 y otras bacterias fitopatógenas. El ADN cromosómico DNA fue digerido con la endonucleasa de corte raro I-CeuI y luego separado con PFGE. (λ) Marcador de tamaño de escalera Lambda. Patrones de PFGE de: (A) Pseudomonas syringae pv. tagetis LF2012; (B) P. syringae pv. syringae 61; (C) P. syringae pv. glycinea PG4180; (D) P. syringae pv. tomato DC3000; (E) Pectobacterium cacticidum FHLGJ22 y (Y) cromosoma de Saccharomyces cerevisiae YPH80; (kb) tamaños en kilo pares de base.











 text in
text in 


