Alternaria tenuissima (Nees & T. Nees: Fr.) Wilshire es un hongo que causa pérdidas en la producción de cultivos como en manzano (Malus x domestica Borkh.), peral (Pyrus communis L.), brócoli (Brassica oleracea var. italica), entre otros, agudizándose el problema por la producción de toxinas (Jones y Aldwinckle, 2002; Fraire-Cordero et al., 2010; Agamy et al., 2013). Alternaria es un género ampliamente distribuido en zonas agrícolas y cuenta con especies saprofitas, endofíticas y fitopatógenas. Asimismo, como producto de su actividad, se han identificado alrededor de 70 metabolitos secundarios tóxicos para las plantas y algunos pueden afectar la salud humana relacionándose en casos de alergias y cáncer de esófago (Pavón-Moreno et al., 2012; Woudenberg et al., 2015).
Tradicionalmente, para prevenir y controlar la invasión de los hongos fitopatógenos en la agricultura se han utilizado fungicidas sintéticos (Campbell y López-Ortíz, 2014). Los más utilizados contra Alternaria son el azoxystrobin, difenoconazol, mancozeb, tebuconazole, entre otros (Malandrakis et al., 2015; Savitha y Ajithkumar, 2016). Sin embargo, estos fungicidas causan efectos adversos al ambiente y a la salud humana. Por lo que es necesario la búsqueda de alternativas amigables con el entorno para el control de hongos fitopatógenos (Blair et al., 2015).
Algunos compuestos de fuentes botánicas tienen potencial de ser usados para el control de fitopatógenos en cultivos de interés agrícola. Considerando que se han descrito alrededor de 374,000 especies de plantas, existe un amplio campo de oportunidad para el desarrollo de antifúngicos a partir de extractos de estas plantas (Cowan, 1999; Christenhusz y Byng, 2016). Entre los compuestos de las plantas con capacidad antifúngica destacan los aceites esenciales (Isman et al., 2011). Algunos de los cuales han mostrado capacidad antifúngica tales como los extractos a base de té de limón (Cymbopogon citratus (D.S.) Stapf.), eucalipto (Eucalyptus spp.), canela (Cinnamomum verum L.), clavo (Syzygium aromaticum L.), entre otros (Calo et al., 2015). El ajo (Allium sativum L.) contiene aceite esencial compuesto por aromáticos como el dialil disulfuro, dialil trisulfuro y otros compuestos azufrados con actividad antimicrobiana con potencial para ser utilizados en el control de hongos (Casella et al., 2013; Kocić-Tanackov et al., 2012). El objetivo del estudio fue evaluar la actividad antifúngica in vitro del aceite esencial de ajo contra de A. tenuissima.
El estudio se realizó en los laboratorios del Centro de Investigación en Alimentación y Desarrollo, AC unidad Culiacán. La cepa de A. tenuissima fue proporcionada por el Departamento de Investigación y Posgrado en Alimentos de la Universidad de Sonora, previamente identificada por Quintana-Obregón et al. (2013), se reactivó y creció en medio papa dextrosa agar (PDA) a 25 °C con fotoperiodos de 12 h luz-oscuridad por siete días. Posteriormente, suspensiones de esporas con una solución de Tween® 20 al 0.1% (v/v) fueron preparadas y finalmente se determinó la concentración mediante un hematocitómetro (cámara de Neubauer, BRAND ® Alemania).
El aceite esencial de ajo utilizado fue grado analítico (Sigma-Aldrich® lote MKBB8390V). La identificación de volátiles del aceite se realizó mediante un cromatógrafo de gases GC-7890B (Agilent Technology®, EUA), acoplado a un detector selectivo de masas Agilent 240 (CG-MS) con un sistema de ionización eléctrico de 70 eV. La columna capilar utilizada fue DB-5 (50 m*0.25 mm) (J&C Scientific, Agilent Technologies®, Pennsylvania, EUA) y se acondicionó a 60 °C por 10 min. La temperatura se incrementó (20 °C/min) hasta 180 °C por 2 min y finalmente (4 °C/min) hasta 250 °C por 4.5 min. Gas acarreador helio fue utilizado a un flujo de 2 mL min-1. Las temperaturas de la cámara de ionización y de la línea de transferencia fueron de 220 y 280 ºC, respectivamente. Los constituyentes se identificaron por comparación de índices de retención lineales con base a una mezcla de n-alcanos y tiempos de retención de los espectros obtenidos con la base de datos NIST 98 (National Institute of Standard and Technology, Maryland, EUA).
Crecimiento Radial. El PDA con Tween® 80 (1% v/v) se esterilizó por 15 min a 15 psi, se enfrió a 45 °C y se mezcló con aceite esencial de ajo a diferentes concentraciones (0, 10, 100, 500, 1,000 y 10,000 ppm). Adicionalmente, se preparó PDA sin Tween® 80 bajo las mismas condiciones, pero sin mezclarlo con aceite esencial de ajo, cada mezcla se depositó a razón de 15 mL en cajas de Petri de 50 mm de diámetro. Posteriormente, con una pipeta Pasteur de vidrio esterilizada se realizó una perforación de 6 mm en el centro del medio de cultivo solidificado y se inoculó con 25 µl de la suspensión de esporas (105 esporas) de A. tenuissima. Finalmente, los cultivos se incubaron a 25 °C con fotoperiodos de 12 h luz-oscuridad y se midió el radio de la colonia fúngica cada 24 h hasta que cubrió el 95% del testigo (PDA sin Tween® 80) tomado como referencia. Las concentraciones mínimas inhibitoria (CMI) y media inhibitoria (CI50) se determinaron a las 120 h post-inoculación del hongo mediante análisis Probit con el programa estadístico NCSS 2000 (Number Cruncher Statistical Systems, Utah, EUA).
Producción de biomasa. Las cajas de Petri con las concentraciones de aceite previamente descritas se inocularon con 25 µL de la suspensión de esporas (105 esporas) de A. tenuissima en la parte central distribuyéndolas por medio de la técnica de difusión en superficie y se mantuvieron bajo las mismas condiciones descritas anteriormente. A las 120 h se cuantificó el peso seco de las colonias que crecieron en el medio de cultivo para lo cual el micelio se separó de la caja de Petri y se trasfirió a un vaso de precipitado con 50 mL de agua destilada, se esterilizó y se separó el micelio con papel filtro Whatman® # 2. El papel filtro junto con el micelio se secó en una estufa de convección de aire a 105 °C por 2 h y se enfrió en un desecador. El peso seco se expresó en mg caja-1 (Larralde-Corona et al., 1997; López-Insunza et al., 1997).
Germinación de esporas. Se evaluó el efecto de la CI50 y CMI del aceite esencial obtenidas por análisis Probit contra las esporas de A. tenuissima. Para ello, se distribuyeron 25 μL de la suspensión de esporas (105 esporas) sobre la superficie del medio de cultivo en la caja de Petri en testigos y tratamientos con aceite esencial. Las cajas de Petri se incubaron a 25 °C con fotoperiodo de 12 h luz-oscuridad hasta un tiempo máximo de 24 h. Se tomaron muestras aleatorias cada 4 h y se contó el número de esporas germinadas y no germinadas de un total de 200 esporas bajo un microscopio óptico. Se consideró como una espora germinada cuando la longitud del tubo germinativo fue de al menos el 50% de la longitud de la espora sin germinar (Dantigny et al., 2006).
Diseño experimental y análisis estadístico. En el experimento se utilizó un diseño completamente al azar donde los tratamientos fueron: PDA, PDA-Tween® 80 (testigos) y concentraciones de aceite esencial de ajo en PDA-Tween® 80 (10, 100, 250, 500 y 1,000 ppm). Los siete tratamientos se evaluaron contra A. tenuissima donde la unidad experimental fue una caja de Petri. Las variables respuesta fueron crecimiento radial y producción de biomasa. Las CI50 y CMI se evaluaron en la etapa de germinación de esporas. Todos los experimentos se realizaron por triplicado. Los datos fueron analizados utilizando el programa estadístico JMP versión 5.0 (SAS, 2002) para el análisis de varianza (ANVA) y las medias de los tratamientos se separaron por la prueba de Tukey (p≤0.05).
En el Cuadro 1 se muestran los principales componentes volátiles tentativos del extracto de ajo obtenidos por CG-MS con proporciones relativas ≥1%. Predominan compuestos con azufre en su estructura, entre los que destacan el dialil sulfuro y dialil disulfuro, los cuales son derivados de la actividad de la enzima alinasa al ser liberada por rompimiento del tejido durante la extracción de aceite (Kocić-Tanackov et al., 2012).
Cuadro 1 Principales compuestos del aceite esencial de ajo identificados por reconocimiento estructural mediante CG-MSx.
| Tiempo de Retención (min) | Identificación | Cantidad Relativa (%) |
| 6.867 | Dialil sulfuro | 20.33 |
| 8.885 | 1,3-Ditiano | 6.1 |
| 11.205 | Ciclopentano, 1-acetil-1,2-epoxi | 2.51 |
| 12.144 | [1,3] Ditiano-2-ona | 1.15 |
| 13.784 | Dialil disulfuro | 23.64 |
| 14.038 | 2-etileden [1,3] ditiano | 3.54 |
| 14.6893 | Hidroxiperóxido, 1,4-dioxan-2-il | 6.89 |
| 15.314 | 3-Vinil-1, 2-dithiacyclohex-4-ene | 2.02 |
| 19.526 | Cyclopenteno, 3-metil-3-(trimethylsily) acetil- | 1.94 |
x Con proporciones relativas ≥ 1%.
El crecimiento radial de A. tenuissima en el tratamiento con medio PDA solo cubrió el 95% de la caja de Petri a las 120 h alcanzando un radio de 22 mm. Entre los tratamientos PDA y PDA-Tween® 80 no hubo diferencias significativas en su crecimiento radial a las 120 h. El aceite esencial logró una disminución significativa del crecimiento radial de A. tenuissima con concentraciones iguales o superiores a 250 ppm logrando a 1,000 ppm una inhibición del 100% con respecto al testigo PDA-Tween® 80 (Cuadro 2).
Cuadro 2 Efecto antifúngico de aceite esencial de ajo a diferentes concentraciones sobre la producción de biomasa de Alternaria tenuissima a las 120 h.
| Aceite esencial de ajo (ppm) | Crecimiento radial (mm) ±DE | Biomasa (mg caja-1) ±DE |
| 0 (PDA) | 22±0.0ax | 161.13±11.60cx |
| 0 (PDA-Tween® 80) | 22±0.0a | 522.60±83.01b |
| 10 | 22±0.0a | 692.35±16.47a |
| 100 | 20±2.17a | 148.10±19.74cd |
| 250 | 9.67±0.76b | 101.00±1.13cde |
| 500 | 2.83±0.56c | 68.03±1.86e |
| 1000 | 0±0.0d | 72.10±7.23de |
xLetras distintas entre columnas indican diferencias estadísticas de acuerdo con la prueba de Tukey (p≤0.05). Valores promedio de al menos tres replicas
En la producción de biomasa, el medio PDA-Tween® 80 con 10 ppm de aceite esencial mostró un incremento significativo con respecto al PDA solo. Sin embargo, al incrementar la concentración de aceite esencial a 500 y 1,000 ppm hubo diferencias significativas con respecto a los testigos, evidenciándose inhibición sobre el crecimiento de A. tenuissima a estas concentraciones, siendo la inhibición de producción de biomasa de 86.20% a 1,000 ppm de aceite con respecto al testigo PDA-Tween® 80 (Cuadro 2). El incremento en biomasa en medio de cultivo con Tween® 80 a 10 ppm pudo deberse a la interacción entre el Tween® 80 y el aceite esencial. Se ha reportado que el Tween® 80 puede incrementar la permeabilidad celular favoreciendo la absorción de nutrientes, en Aspergillus fumigatus se ha sugerido que el compuesto es utilizado como fuente de carbono (Inouye et al., 2001; Taoka et al., 2011). Al ser mayor la concentración de Tween® 80 con respecto al aceite esencial (10 ppm) la superficie de contacto del micelio es competida por el Tween® 80 disminuyendo la actividad antifúngica del aceite solo (Inouye et al., 2001). Al incrementar la concentración de aceite esencial (500 y 1,000 ppm) la interacción de aceite-micelio se incrementa favoreciendo su bioactividad, evidenciado por la disminución significativa de biomasa a las 500 y 1,000 ppm con respecto al testigo PDA-Tween® 80 (Cuadro 2).
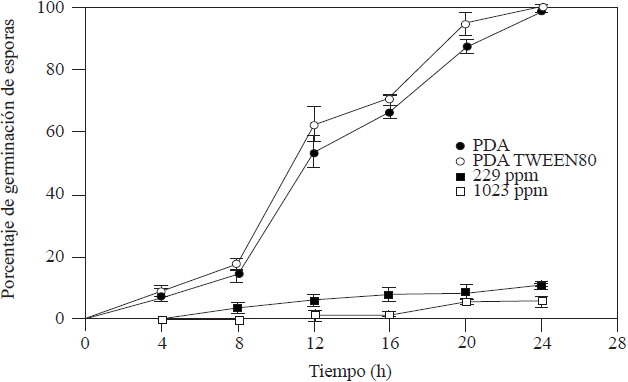
A partir del crecimiento radial se obtuvo la CI50 y CMI de 229 ppm y 1,023 ppm, respectivamente. La cinética de germinación de esporas de A. tenussima expuestas a las CI50 y CMI de aceite esencial de ajo (Figura 1) mostró diferencias significativas con respecto a los medios testigo (PDA y PDA-Tween® 80) con inhibiciones de germinación de esporas del 88.89 y 94.17% para CI50 y CMI, respectivamente. De acuerdo con Inouye et al. (2001) la capacidad inhibitoria de los compuestos volátiles de aceites esenciales se destaca por afectar tres etapas del desarrollo fúngico, la germinación de esporas, micelio vegetativo y micelio reproductor. Este efecto del aceite esencial de ajo ha sido reportado en etapas de crecimiento de Aspergillus versicolor y Penicillium funiculosum (Kocić-Tanackov et al. 2012; Li et al., 2014). Al evaluar la CMI del aceite esencial contra A. tenuissima se observó un efecto fungistático. Es posible que el aceite esencial del ajo interactúe con la membrana celular y al disminuir su concentración a través del tiempo por la volatilidad de sus componentes la interacción disminuye y el hongo regulariza su metabolismo. Tian et al. (2012) encontraron alteraciones en la membrana celular de Aspergillus flavus, particularmente ergosterol al ser tratadas con eneldo (Anethum graveolens). El mecanismo de acción antimicrobiana de los compuestos azufrados se ha asociado la interacción con proteínas con grupos sulfhídricos de la célula y a los enlaces disulfuro que puedan formarse (El-Sayed et al., 2017), es posible que la inhibición en A. tenuissima se deba a este tipo de interacciones químicas. No obstante, son necesarios estudios adicionales para elucidar mecanismos de interacción del aceite esencial de ajo sobre el crecimiento in vitro de A. tenuissima.











 text in
text in