Antecedentes
De acuerdo con el Instituto Nacional de Alergia y Enfermedades Infecciosas y la Academia Europea de Alergia e Inmunología Clínica, la alergia alimentaria se define como una “reacción adversa hacia determinados alimentos, que surge de una respuesta inmune específica, ya sea mediada por inmunoglobulina (Ig) E, por células o por ambos”.1,2,3 Sin embargo, en este trabajo solo nos enfocaremos a las mediadas por IgE, que se agrupan dentro de las reacciones de hipersensibilidad tipo I de acuerdo con la clasificación de Gell y Coombs.
La prevalencia de esta patología ha tenido un crecimiento acelerado durante las últimas décadas, sobre todo en las regiones más industrializadas. La Organización Mundial de Alergia ha declarado que 2.5 % de la población en general padece algún tipo de alergia alimentaria, aunque los valores pueden variar de 1 a 10 % dependiendo de la forma como se diagnostica, la metodología de estudio, la variación geográfica y la edad, entre otros factores.4 Sin embargo, la población infantil es la que resulta más afectada, con una prevalencia de 6 a 8 %. Aun cuando esta patología no resulta mortal en la mayoría de los casos, genera una morbilidad considerable3 y disminuye la calidad de vida de quien la padece, además de ocasionar costos importantes al sistema de salud y a las familias de los pacientes.5,6,7
Alérgenos alimentarios
Los alérgenos alimentarios son proteínas o glucoproteínas de 5 a 100 kDa de peso molecular con capacidad de unirse específicamente a la IgE,8 que llegan intactas o prácticamente sin digerir a la células presentadoras de antígenos y que en una persona atópica ven favorecida su capacidad inmunogénica.9 Numerosos estudios sobre las alergias alimentarias se enfocan en un grupo particular de alérgenos denominados “los grandes ocho”, alérgenos que en Norteamérica causan alrededor de 90 % de las alergias a alimentos e incluye los productos más alergénicos: leche, huevo, pescado, marisco, nueces, cacahuate, trigo y soya.10
Aunque el término anterior se ha mantenido vigente, las modificaciones a nivel mundial en la regulación de estos alérgenos, así como en las estadísticas de su alergenicidad han dado paso al uso de otros términos en el contexto de las alergias alimentarias (Cuadro 1). De tal forma, se denomina trofoalérgeno a todo aquel alérgeno capaz de entrar por el sistema digestivo al organismo, lo cual podría incluir algunos aditivos y fármacos,11,12,13 aunque comúnmente se limita a alérgenos alimentarios. Además de “los grandes ocho”, más de 160 alimentos han sido documentados como alérgenos menos frecuentes,14 si bien se sabe que cualquier alimento puede ser potencialmente alergénico y provocar hipersensibilidad mediada por mecanismos inmunológicos.1,15,16
Cuadro 1 Antígenos capaces de desencadenar alergia alimentaria
| Denominación | Características particulares en alergia alimentaria | Principales alérgenos |
| “Los grandes ocho” | Antígenos altamente alergénicos para 90 % de la población estadounidense |
Leche, huevo, pescado, marisco, nueces, cacahuate, trigo y soya10 |
| Trofoalérgeno | Cualquier antígeno de ingreso por vía gastrointestinal | Leche, huevo, pescado, marisco, nueces, cacahuate, trigo, soya, manzana, aguacate, plátano, cocoa, papa, fresa, entre otros10,14 |
| Alérgenos sensibles a la digestión |
Antígenos que suelen degradarse en cavidad oral, no resisten la digestión ni la proteólisis. Originan el síndrome de alergia oral |
Papa (Solt t 1), apio (Api g 1), piña (Ana 1), cacahuate (Ara h 5), cereza (Pru av 4), entre otros18 |
| Aeroalérgenos | Antígenos de ingreso por vía aérea (inhalación). Tras
sensibilizar al individuo pueden ocasionar reacciones cruzadas con diversos alérgenos alimentarios |
Polen de abedul, de ambrosía, de artemisa, de ciprés, de cedro, de maíz, de girasol y látex, entre otros20 |
| Panalérgenos | Familia de proteínas relacionadas, ampliamente distribuidas
en la naturaleza y que comparten estructura tridimensional o regiones con secuencias altamente conservadas. Responsables de muchas reacciones cruzadas entre pólenes y alérgenos alimentarios |
Profilinas como las del polen de abedul (Bet v 1 y Bet v 2), proteínas de transferencia de lípidos no específicas como las de la ambrosía (Amb 6), kiwi (Act 10) y látex (Hev b 12), entre otros23 |
En el intento de discernir qué proteínas tienen más probabilidad de ser alergénicas, se realizó un análisis in silico en el que se buscó la relación entre la homología estructural de proteínas causantes de alergia con proteínas humanas y su capacidad para generar alergias. Se encontró que todas las proteínas con homología humana menor o igual a 54 % en su secuencia eran alergénicas; mientras que aquellas con homología mayor a 63 % raramente lo eran.17 Estos datos resultan útiles para la identificación y el estudio continuo de los alérgenos más importantes en la actualidad.
Existen alérgenos “sensibles a la digestión”, que, a diferencia de los mencionados, no resisten la digestión enzimática o proteólisis ácida, por lo que rápidamente son disueltos y degradados en la boca. Dichos alérgenos generan ligeras reacciones de inicio súbito: picor, edema en los labios, la lengua, el paladar o la faringe; manifestaciones localizadas exclusivamente en la cavidad oral, mediadas por IgE y conocidas como síndrome de alergia oral.18,19 Esta condición, también puede ser provocada por reacción cruzada. El término “reacción cruzada” implica que los anticuerpos generados contra un alérgeno específico puedan unirse a otros estructuralmente relacionados, aún si el individuo no fue sensibilizado a ese segundo alérgeno, lo que aumenta considerablemente el número de alimentos contra los que se puede desencadenar una reacción alérgica.
Los aeroalérgenos, como el polen de numerosos árboles o el látex, se han reportado como causantes de reacciones cruzadas con diversos alérgenos alimentarios.20,21 Solo por mencionar un ejemplo, personas con alergia al polen de abedul presentan reacción cruzada con frutas de la familia de las rosáceas como la manzana, la pera, el durazno o la almendra, entre otras.18 Incluso, las especias utilizadas para mejorar el sabor de los alimentos son capaces de provocar este tipo de reacciones. Moléculas homólogas a Bet v 1, principal alérgeno del polen del abedul, se han detectado en la familia botánica de las apiáceas, que incluye el apio, la zanahoria y muchas otras especias populares como el comino, el anís y el hinojo.22
En general, los alérgenos que comparten regiones de secuencias altamente conservadas con homologías superiores a 70 % o estructuras tridimensionales, lo que facilita su unión a IgE previamente producidas, reciben el nombre de “panalérgenos”.23
Factores de riesgo
La predisposición a presentar alergia alimentaria se ha relacionado, como en otros tipos de alergias, a factores genéticos. En un estudio de asociación de genoma completo en niños de ascendencia europea con alergias alimentarias bien definidas y en sus padres, se encontraron loci específicos para la alergia al cacahuate en la región de los genes de HLA-DR y HLA-DQ.24
Otro estudio de asociación de epigenoma completo en el que se midió metilación de ADN en 485 512 loci en 106 niños con alergia a leche de vaca y 76 niños sanos mostró una metilación alterada del ADN en genes relacionados con las respuestas de los linfocitos T cooperadores (Th)1/Th2, como IL1RL1, IL5RA, ATAT4, IL4 y CCL18; así como en otros genes regulados por interleucina (IL)-4 (NDFIP2) e IL-13 (EVL).25 No obstante, el aumento dramático en la incidencia de esta enfermedad ha permitido asociar este incremento con diversos factores ambientales: el tipo de dieta, el procesamiento de los alimentos, el consumo de conservadores o de aditivos y el uso de antibióticos u otros medicamentos.26,27,28 Sin embargo, ha sido hasta las últimas décadas cuando se ha comprendido algunos de los mecanismos que favorecen la predisposición de padecer alergia alimentaria. En la actualidad se sabe que entre estos mecanismos se incluyen elementos moleculares y celulares,29 mismos que llevan al rompimiento de los factores homeostáticos de la tolerancia antigénica a proteínas alimentarias, lo que resulta tanto en alergia alimentaria mediada como no mediada por IgE y que se explicarán en detalle en el siguiente apartado.30
Conforme transcurre el tiempo, los pacientes pediátricos con historial de atopia son susceptibles de desarrollar diversas patologías alérgicas, denominadas en conjunto “marcha atópica”. La marcha atópica consiste en una progresión de afecciones alérgicas que tienen factores predisponentes genéticos y ambientales comunes y que comparten las características inmunológicas de generar IgE específica, la activación de granulocitos y la aparición de determinados signos, como la producción excesiva de moco y edema.
Es importante destacar que la presencia de una condición alérgica aumenta el riesgo de desarrollar otras, característica adicional de la marcha atópica.31 Los primeros síntomas que aparecen son gastrointestinales o eccematosos, pudiendo continuar en edades posteriores con alergias respiratorias como la rinitis atópica o el asma.1 A partir de un estudio de cohorte en retrospectiva del Hospital Infantil de Filadelfia se encontró que la alergia alimentaria, particularmente al cacahuate, la leche y el huevo, aumenta el riesgo de desarrollar alergia respiratoria, y que este riesgo se incrementa aún más cuando se trata de alergias a varios alimentos.32 Cabe mencionar, que la alergia alimentaria también puede dar inicio en la etapa adulta dependiendo de factores dietarios y genéticos específicos de cada persona.33
Uno de los factores de riesgo más importante para la presentación de esta patología es el consumo de alimentos alergénicos por la madre durante el embarazo.34 Asociado a esto, mediante pruebas in situ se ha descrito que al perfundir placentas obtenidas tras el parto o cesárea con ovoalbúmina (OVA), β-lactoglobulina o el aeroalérgeno Bet v 1, se detectan niveles bajos de estos alérgenos en el efluente fetal placentario.35 Además, se ha demostrado la presencia de alérgenos ingeridos por la madre en la leche materna.36
Las anteriores observaciones sugieren vías de primer contacto del infante con el alérgeno, que bajo condiciones adecuadas podrían generar la sensibilización y originar síntomas alérgicos tras el contacto vía oral con ese alimento. Sin embargo, los resultados relacionados con la lactancia son controversiales, pues algunos grupos de investigación sugieren que la ingesta de los alérgenos presentes en la leche materna induce tolerancia a los mismos. En este sentido, Metcalfe et al. han asociado la ingesta materna de huevo durante la lactancia con el incremento de OVA en la leche materna y el aumento de los niveles séricos de IgG4 alérgeno-específica en el lactante. Curiosamente, estos resultados no correlacionaron con los niveles de IgE, aunque se observó que algunos lactantes de madres con una baja ingesta de huevo presentaron IgE específica a OVA.37 Los resultados anteriores podrían sugerir que el contacto con cantidades elevadas de alérgenos durante la lactancia podría ser un factor inductor de tolerancia; sin embargo, la presencia de niveles bajos de alérgenos en la leche materna podría ser un factor inductor de inmunización alérgica.
Asimismo, desde hace varias décadas se sabe que otros factores ambientales, como la exposición microbiana, modifican el riesgo de sensibilización alérgica, tal como lo explica la hipótesis de la higiene o la hipótesis de la microbiota.38,39 Diversos estudios en modelos murinos libres de gérmenes revelan que la ausencia de microbiota aumenta la predisposición a desarrollar alergia alimentaria. Particularmente en un modelo de tolerancia oral a OVA en ratones libres de gérmenes se observó que quedó abolida la producción de IgG2a e interferón-γ, mientras que se incrementaron los niveles de IL-4; además cuando se reconstituye la microbiota con Bifidobacterium infantis se restablece la tolerancia oral alérgeno-específica.40
A pesar de las numerosas evidencias que señalan que en el infante disminuye su probabilidad de desarrollar alergia alimentaria tras el contacto con diversos microorganismos, es necesario realizar más investigaciones que lo sustenten. Diferentes estudios epidemiológicos muestran resultados controversiales en infantes nacidos por canal de parto o cesárea, en niños que reciben cuidados comunitarios o los que estuvieron expuestos a procesos infecciosos como sarampión, hepatitis, rubeola o tosferina.41,42
Por último, se ha reportado que la prescripción de antibióticos durante los primeros años de vida aumenta la posibilidad de diagnóstico de alergia alimentaria.43,44 Lo anterior, en conjunto con la edad del paciente, pone en relieve la importancia de la microbiota propia del organismo en el mantenimiento de las respuestas normales a antígenos cotidianos como los de la dieta.
Sistema inmune de la mucosa intestinal y tolerancia antigénica
El intestino es uno de los órganos que presenta mayor contacto con agentes externos, incluidos los alimentos y un gran número de microorganismos benéficos para nuestra salud, razón por la cual, en este órgano predomina un perfil tolerogénico del sistema inmune, sin dejar de desempeñar un papel protector. El intestino se encuentra recubierto por un epitelio en monocapa compuesto por diferentes poblaciones celulares, cada una de ellas desempeña un papel importante en el establecimiento de la homeostasis e integridad de la barrera intestinal: los enterocitos encargados de la absorción de nutrientes, las células madre que permiten la regeneración del tejido, las células de Paneth secretoras de péptidos antimicrobianos, las células caliciformes productoras de moco, las células M (importantes en la transcitosis de los antígenos), las células en cepillo o caveoladas (descritas como elementos conectores funcionales entre el compartimento hematopoyético y el epitelial durante la respuesta inmune frente a los parásitos) y las células enteroendocrinas encargadas de la secreción de hormonas.45,46,47
Un papel importante en esta gran barrera física que forma el epitelio intestinal lo desempeñan diversas proteínas que forman parte de las uniones estrechas, como las claudinas y las ocludinas; de las uniones adherentes, como las caderinas y las cateninas; y de los desmosomas, como la desmogleína.46,47 Todas ellas impiden el paso paracelular de la mayoría de los agentes externos a través de la barrera epitelial.48
El mecanismo de transporte de los agentes externos se realiza transcelularmente por transcitosis a través de las células M; por endocitosis mediada por los enterocitos, a través de exosomas derivados de los linfocitos intraepiteliales; por el receptor para la fracción cristalizable de la IgA, que permite el retrotransporte de inmunocomplejos;46 o por muestreo directo de los macrófagos o las células dendríticas a través de proyecciones membranosas emitidas hacia la luz de la mucosa intestinal.49
Los mecanismos anteriores permiten la interacción de los elementos presentes en el lumen intestinal con las células especializadas de la respuesta inmune ubicadas en la lámina propia, por debajo de la barrera epitelial. Dichas células incluyen células dendríticas, macrófagos, linfocitos intraepiteliales, linfocitos T reguladores (Treg), linfocitos Th, linfocitos B y células plasmáticas, ya sea formando parte de tejido linfoide anatómicamente estructurado, como las placas de Peyer y los ganglios linfáticos mesentéricos, o simplemente distribuidas a lo largo de la lámina propia.50
La comunicación entre el lumen intestinal y las células especializadas de la lámina propia es la base del establecimiento de la homeostasis intestinal. Los ratones libres de gérmenes presentan una menor cantidad de macrófagos en la lámina propia,51 lo que refleja la importancia de la microbiota en la distribución de estas células en el intestino. En la lámina propia de ratones, los macrófagos M1, junto con las células epiteliales, son fuentes importantes de la proteína quimiotáctica de monocitos-1, quimiocina que recluta macrófagos M2. Esta subpoblación M2 produce una gran cantidad de IL-10 en respuesta a bacterias comensales y desempeña un papel esencial en el mantenimiento de la homeostasis,52 mediante la diferenciación de los linfocitos a células Treg Foxp3+ dependientes del factor transformante del crecimiento (TGF)-β y ácido retinoico y la modulación de la expresión de IL-17,53 citocina proinflamatoria asociada a enfermedades alérgicas.54 Además, en la mucosa intestinal se han descrito dos principales poblaciones de células presentadoras de antígeno; cada una de ellas contribuye de diferente manera al desarrollo de la tolerancia intestinal.55
En modelos murinos se ha identificado una población de células dendríticas CD103+ que tiene la capacidad de capturar antígenos de la lámina propia, migrar a los ganglios linfáticos mesentéricos y presentárselos a los linfocitos T, con lo que contribuye a la inducción de células Treg Foxp3+ dependientes de TGF-β y ácido retinoico,56,57,58 que presentan tropismo intestinal a través de los receptores CCR9 y α4β7. La otra población la constituyen las células dendríticas y los macrófagos CX3CR1+, que se acumulan en la lámina propia tras la colonización microbiana. También residen en el epitelio intestinal, donde emiten proyecciones membranosas hacia el lumen, lo que les permite muestrear antígenos luminales. Dichas células tienen por naturaleza una alta actividad fagocítica y generan tolerancia intestinal ayudando a la expansión de las células Treg.55
Las células Treg Foxp3+ desarrollan un papel clave en el establecimiento y mantenimiento de la tolerancia intestinal; se ha detectado la presencia de células Treg tímicas y Treg inducidas por antígeno (iTreg).55 Mediante ensayos de manipulación genética del locus Foxp3 se ha demostrado que ratones deficientes en secuencias conservadas no codificadoras de dicho locus desarrollan inflamación intestinal dependiente de células B, con anticuerpos contra antígenos alimentarios e intestinales, niveles elevados de IgE e IgA y una acumulación de células TCD4+ Gata3+ productoras de IL-4, IL-5 e IL-13, con lo que se demuestra el papel crucial de las células iTreg en la tolerancia oral hacia antígenos luminales y en el control de la respuesta alérgica, así como la importancia de sesgar la respuesta inmune mucosa hacia un programa Treg Foxp3+ para generar torelancia.55,59 Particularmente, en la mucosa intestinal murina se detecta una mayor presencia de células Treg NRP-1− Helios- Foxp3+, consideradas células iTreg en tejido periférico.57 Esta subpoblación de células iTreg realiza su actividad supresora principalmente mediante IL-10 y CTLA-4.60 Así, una pérdida de la función de los linfocitos iTreg induce la activación de los linfocitos Th2,61 favoreciendo el desarrollo de inflamación alérgica.
La producción de IL-10 y TGF-β por diferentes poblaciones celulares intestinales es de gran importancia en la inducción de tolerancia. Ambas participan en el mantenimiento de la población de células Foxp3+ y en su función, así como en evitar respuesta de células T inflamatorias intestinales. Además, la IL-10 inhibe la expresión de moléculas coestimuladoras en los macrófagos. Cualquier fallo en la producción de estas citocinas o en sus vías de señalización resulta en pérdida de tolerancia intestinal.55
Adicionalmente, la microbiota desempeña un papel importante en la regulación de la homeostasis intestinal. Diversos grupos de investigación han trabajado en modelos murinos libres de gérmenes y han demostrado un menor número de linfocitos intraepiteliales62 y de células plasmáticas secretoras de IgA,63 así como centros germinales más pequeños dentro de las placas de Peyer de los animales.64 Específicamente, se ha demostrado que el polisacárido A producido por bacterias como Bacteroides fragilis, promueve la diferenciación de células T CD4+ a células iTreg en ratones libres de gérmenes,65 solo por mencionar algunos ejemplos. Mientras exista una adecuada cantidad de organismos simbiontes que contribuyan al metabolismo de las partículas alimentarias que ingresen al microambiente y pueda prevalecer una adecuada comunicación con las células del hospedero, el entorno tolerogénico podrá mantenerse.66
Sensibilización a alérgenos alimentarios
Como ocurre en otras enfermedades alérgicas, la alergia alimentaria no presenta manifestaciones clínicas en la fase de sensibilización. En su desarrollo intervienen numerosos factores y está generada por la entrada inicial del alérgeno y su interacción con células del sistema inmune para producir anticuerpos IgE específicos.67,68,69 Particularmente en la alergia alimentaria se han observado distintas vías y mecanismos de sensibilización.
La relación entre alergia cutánea y alimentaria nos lleva a retomar la antigua hipótesis de la “exposición alergénica dual”,70 la cual postula que la sensibilización alimentaria puede ocurrir por dosis pequeñas del alérgeno que ingresa al organismo por vía cutánea, favoreciendo la respuesta Th2 y la producción de IgE; mientras que el consumo oral de altas dosis del alérgeno induce tolerancia mediada por un perfil Th1.71 En los primeros años de vida, uno de los signos de alergia alimentaria son las reacciones cutáneas como urticaria o eccema, por lo que se cree importante el estudio de esta relación.
Un estudio prospectivo de cohorte en población pediátrica australiana con eccema demostró que estos infantes son cinco veces más proclives al desarrollo de alergia alimentaria dependiente de IgE que los niños que no lo presentan.72 Un trabajo realizado en niños y adolescentes muestra que mutaciones con pérdida de función en el gen de la filagrina, asociada con anormalidades en la función de barrera cutánea, incrementa el riesgo de desarrollar alergia alimentaria en la infancia tardía y adolescencia, lo que sugiere que alteraciones en este gen vincula la sensibilización cutánea con las alergias alimentarias.73 Sin embargo, la presencia de dermatitis atópica en niños de uno a tres meses los hace más susceptibles a ser sensibilizados a antígenos alimentarios, independientemente de las mutaciones de la filagrina, además de encontrarse una asociación importante entre la sensibilización alimentaria y la severidad de la dermatitis.74 Asimismo, un análisis transversal en adultos reveló que el historial de dermatitis atópica, pero no la presencia de mutaciones en filagrina, se asocia de nuevo a la sensibilización a alérgenos alimentarios y aeroalérgenos.75 En conjunto, estos resultados sugieren que la sensibilización alimentaria puede ocurrir a través de una barrera cutánea alterada.
Por otro lado, diversas investigaciones en pacientes que han presentado reacciones de alergia alimentaria ante la primera ingesta del alérgeno, pero que tuvieron contacto previo con el mismo alérgeno por vía aérea, evidencian la factibilidad de sensibilización a alimentos por vía respiratoria.76,77 Asimismo, diversos reportes de casos han dejado evidencia de la aparición inmediata de signos graves a alérgenos alimentarios como papa,78 leche79 y arroz80 después de su inhalación. Los mecanismos exactos de esta relación entre sensibilización a trofoalérgenos y aeroalérgenos no se han podido discernir. No obstante, reportes de casos, como el de un hombre de 38 años de edad alérgico al moho quien desarrolló anafilaxia alimentaria al consumir champiñones y tras demostrarse la reactividad cruzada entre algunas enzimas del hongo comestible y los aeroalérgenos del moho,81 explican la “reacción cruzada” entre alérgenos inhalados y alimentarios como un mecanismo claro de sensibilización en la alergia alimentaria.
Muchos trabajos señalan que la alteración en la permeabilidad intestinal es clave en la sensibilización a trofoalérgenos (Figura 1-1). En los últimos años se ha resaltado el papel que juegan los receptores activados por proteasas (PAR) en el incremento de la permeabilidad intestinal. La familia de los receptores PAR es altamente expresada en un gran número de células. Particularmente, PAR-2 se ha identificado en células epiteliales de la mucosa intestinal.82 Este receptor puede ser activado por diversas proteasas como la enzima digestiva tripsina,83 la triptasa de mastocitos84 o alérgenos con actividad proteasa.82 Ensayos in vitro con células epiteliales de colon de la línea celular T84 en co-cultivo con la línea celular de mastocitos humanos HMC1 o estimulados por agonistas de PAR-2, mostraron que sustancias liberadas por los mastocitos desgranulados o la activación directa de estos receptores incrementan la permeabilidad de la monocapa de colonocitos por una reorganización de F-actina y de uniones estrechas.84 Estos reportes infieren que la activación de PAR-2 pudiera participar en la sensibilización a los trofoalérgenos asociados al incremento en la permeabilidad de la mucosa intestinal.
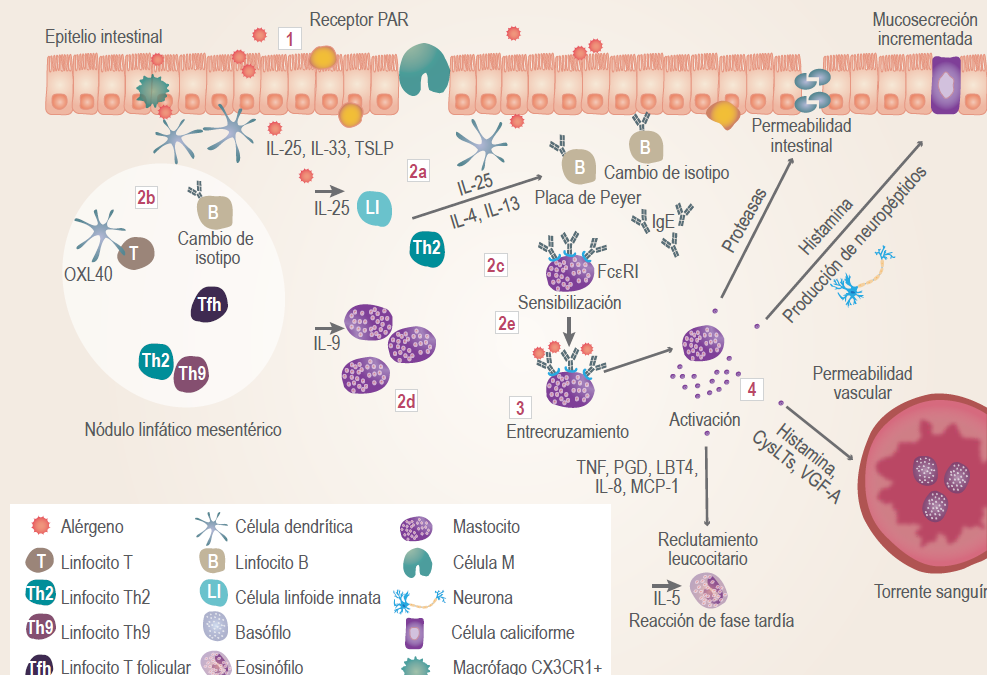
Figura 1 Microambiente intestinal en alergia alimentaria. 1) Captación del alérgeno. La captación del antígeno alimentario por células CX3CR1+ o por las prolongaciones de células dendríticas, así como la estimulación de receptores tipo PAR, dan lugar a la secreción de citocinas por células epiteliales. 2) Sensibilización. Estas citocinas (2a) inician la polarización y maduración de células dendríticas en nódulo linfático, capacitándolas para procesar el antígeno y presentarlo a linfocitos T para su diferenciación a células Th2, Th9 y T foliculares (2b). Las subpoblaciones Th2, Th9 y T foliculares, junto con otras células del microambiente intestinal, producen citocinas que contribuyen a la maduración y cambio de isotipo del linfocito B para la producción de IgE (2c). La expansión mastocitaria en mucosa intestinal (en gran medida originada por la IL-9) hace posible que en el intestino exista gran cantidad de mastocitos (2d). La IgE se une a su receptor de alta afinidad (FcεRI) de la superficie de los mastocitos, quedando la célula sensibilizada (2e). 3) En siguientes exposiciones al alérgeno, el entrecruzamiento de los complejos FcεRI-IgE activa numerosas cascadas de fosforilación y cambios en concentraciones de calcio intracelular de los mastocitos que dan lugar a la activación celular y liberación de mediadores vasoactivos. 4) Aparecen las manifestaciones fisiológicas en respuesta a la activación de mastocitos por el alérgeno. Los efectos más importantes generados por los mediadores liberados incluyen la mucosecreción incrementada por acción de neuropéptidos sobre la célula caliciforme; el incremento de la permeabilidad intestinal por efectos sobre uniones estrechas; vasodilatación que permite que el alérgeno entre a la sangre y se una a basófilos ya sensibilizados y genere un incremento en los efectos sistémicos por la liberación de más mediadores vasoactivos; y por último, el reclutamiento de numerosos leucocitos que van a causar la reacción de fase tardía, perpetuar el proceso inflamatorio y el daño tisular, agravando las manifestaciones de la patología.
Después del ingreso del alérgeno por alguna de las vías mencionadas, aunado a fallas en los factores tolerogénicos o prevalencia de factores predisponentes de alergia alimentaria en el organismo, se inician los mecanismos de sensibilización alérgica (Figura 1-2). Ciertos alérgenos son capaces por sí solos de estimular respuestas asociadas al perfil alérgico, en el cual hay predominio de linfocitos Th2. En un modelo murino de sensibilización cutánea se demostró que el extracto de cacahuate aplicado en piel sana puede modificar per se el fenotipo de las células dendríticas, dependiente de ST2 (receptor de IL-33) y, finalmente, inducir un perfil Th2 en los linfocitos y la síntesis de IgE anti Ara h 1 y Ara h 2, principales alérgenos del cacahuate.85 En relación con esto, se sabe que in vitro, Ara h 1 se une al receptor DC-SIGN de las células dendríticas derivadas de monocitos, detonando el desarrollo de un perfil Th2.86
A la par de los anteriores hallazgos se ha demostrado que en las células dendríticas el lipopolisacárido puede estimular la expresión de Jagged 1, mientras que la prostaglandina E2 o la toxina del cólera incrementan la expresión de Jagged 2.87 Ambas moléculas son ligandos de Notch, vía de activación de los linfocitos Th2.88 La señalización mediada por Notch promueve la activación de GATA3,89 que en conjunto inician con la síntesis de IL-4, mejorando así la activación de STAT6 y fortaleciendo la respuesta Th2.90 Además, como consecuencia de daño o inflamación, las células del epitelio intestinal producen linfopoyetina estromal tímica (TSLP), IL-25 o IL-33 (Figura 1-2a).
En ratones deficientes en receptores de TSLP, IL-25, IL-33 y con alergia alimentaria a la proteína de cacahuate se mostró que la secreción de estas citocinas propicia un perfil Th2 mediante la activación de las células dendríticas, las células linfoides innatas y los basófilos, entre otras. Este efecto estuvo mediado por el aumento en la expresión de OX40L, principalmente en las células dendríticas.91 La interacción OX40-OX40L promueve la supervivencia y la expansión de los linfocitos T efectores y antagoniza o inhibe a las células Treg (Figura 1-2b).92 La investigación de Han et al. en un modelo de alergia en ratones deficientes en el receptor ST2 generó suficiente evidencia que señala a la IL-33 como principal inductor del desarrollo de la marcha atópica, de la severidad de las manifestaciones alérgicas y de la inducción de la respuesta Th2, aunque no establece el mecanismo mediante el cual actúa.93
Los linfocitos Th2 se convierten en fuente importante de IL-4 e IL-13, citocinas que, junto a diversas moléculas coestimuladoras, contribuirán a la maduración, recombinación génica y cambio de isotipo del linfocito B para la producción de IgE alérgeno-específica (Figura 1-2c).94 Este cambio de isotipo queda demostrado al analizar biopsias de mucosa cecal de pacientes con alergia alimentaria, en las que los niveles de ARNm de IL-4 y de los transcritos en la línea germinal de la región constante de la IgE fueron superiores a los de los individuos sanos.95
Además de esas citocinas, cada vez se hace más evidente la participación de la IL-9 en el desarrollo de la alergia (Figura 1-2d). La IL-9 es producida por diversas células, entre ellas los linfocitos Th2 y los Treg. Particularmente, los linfocitos Th2 en presencia de TGF-β potencian la producción de IL-9 y el surgimiento de una nueva subpoblación celular de linfocitos TCD4+, los linfocitos Th9.96 En modelos murinos de alergia alimentaria se han identificado mastocitos de mucosa intestinal productores de IL-9 e IL-13 en respuesta a IL-33. Esta población celular se asocia a la perpetuación de la respuesta anafiláctica y a la severidad de los síntomas alérgicos.97
Más aún, la IL-9 se propone como posible biomarcador para tamizar a los pacientes alérgicos de los individuos con tolerancia natural, conforme a un estudio clínico en el que se evaluó un panel de citocinas y quimiocinas de células mononucleares de sangre periférica de pacientes alérgicos y de pacientes tolerantes al cacahuate, generadas en respuesta al alérgeno. Se observó que las respuestas Th2/Th9 predominaban en los pacientes alérgicos, siendo la producción y expresión génica de IL-9 el marcador que aumentó más significativamente en los pacientes de una manera alérgeno-específica, incremento que se correlacionó con la expresión génica de la IL-33.98
Se ha reportado que la concentración de IgE sérica en individuos sanos suele ser mucho más baja que la de otras inmunoglobulinas como la IgG: la primera es de aproximadamente 150 ng/mL, mientras que la de IgG llega a 10 mg/mL.99 Se conoce menos acerca de los niveles de IgE en la lámina propia. Sin embargo, existe evidencia suficiente que revela la presencia de células plasmáticas IgE+ que secretan el anticuerpo y que provocan incremento en los niveles de Ig en heces100 y jugos gástricos101 de personas alérgicas. La IgE recién producida se une al receptor de alta afinidad de la fracción cristalizable ε (FcεRI), expresado en la superficie de mastocitos y basófilos, quedando las células y el individuo sensibilizados (Figura 1-2e). Además, la IgE interacciona con los receptores de Fcε de baja afinidad (FcεRII o CD23) presentes en la membrana de los linfocitos B, las células T, las células de Langerhans, los macrófagos, los monocitos e, incluso, en las células epiteliales intestinales.102 A su vez, la activación de CD23 por IgE incrementa la expresión de CD23 en las células epiteliales intestinales, mejorando el transporte de los complejos inmunes alérgeno-IgE a la lámina propia.103
Manifestaciones de alergia alimentaria y mediadores inmunológicos involucrados
Tras la sensibilización, cuando el alérgeno es ingerido y entra en contacto con el microambiente intestinal del individuo, una cascada de eventos desencadena los mecanismos inmunes característicos de la alergia alimentaria en el tracto gastrointestinal o a nivel sistémico.104 En los humanos se ha demostrado que generalmente comienza con manifestaciones cutáneas seguidas de las gastrointestinales.105 Al unirse al complejo IgE-FcεRI en los mastocitos o basófilos, el alérgeno provoca una cascada de fosforilaciones de tirosina en múltiples moléculas de señalización intracelular, que culmina con la activación celular y liberación de mediadores inflamatorios (Figura 1-3). El FcεRI carece de actividad tirosinacinasa, pero está asociado con Lyn, una tirosinacinasa de la familia Src cuya actividad es clave para la fosforilación de los motivos de activación de inmunorreceptores basados en tirosina (ITAM, immunoreceptor tyrosine activation motif) presentes en el receptor.
Una vez fosforilados, los residuos de los ITAM unen una variedad de proteínas clave para la continuidad de la señal. La tirosinacinasa Syk es una de ellas, que al desempeñar un papel central en la activación de la célula se ha convertido en un blanco terapéutico en las enfermedades en las que su activación es fundamental en la respuesta inmune subyacente.106 La señalización intracelular iniciada por Lyn y Syk es amplificada a través de moléculas adaptadoras que reclutan otras proteínas que participan en la regulación de los niveles intracelulares de calcio, teniendo como resultado la activación de la célula.107
Tras este segundo contacto con el alérgeno, los basófilos y los mastocitos activados serán importantes en la manifestación de la patología. Los mastocitos son las células clave en este proceso debido a su amplia distribución por el tejido conectivo y mucoso de todo el organismo, su larga vida media superior a seis meses y su capacidad proliferarse después de su maduración.108,109,110 En los humanos se clasifican dependiendo del contenido de proteasas; los mastocitos que contienen solo triptasa residen principalmente en la mucosa gástrica y alveolar y los que contienen solo quimasa o triptasaquimasa predominan en la piel y submucosa intestinal.111
Además de las proteasas, los mastocitos producen una gran cantidad de mediadores inflamatorios, clasificados como preformados y de nueva síntesis. Los primeros están contenidos en sus gránulos y tras la activación de la célula son rápidamente liberados; se incluyen aminas vasoactivas como la histamina y la serotonina, proteasas y citocinas como el factor de necrosis tumoral (TNF)-α. Por otro lado, los de nueva síntesis incluyen a los mediadores lipídicos derivados del ácido araquidónico, como las prostaglandinas, los leucotrienos y el factor activador de plaquetas (PAF), lo cuales son producidos en cuestión de minutos, así como una gran variedad de citocinas, quimiocinas, factores de crecimiento y neuropéptidos, los cuales son sintetizados varias horas después.112
Diversos modelos murinos han permitido identificar a los mediadores relacionados con la fisiopatología de la alergia alimentaria. La serotonina, el PAF,113 la proteasa de mastocito-1114 y, en menor grado, la histamina,115 están relacionados con el incremento de la permeabilidad vascular, edema, hipermotilidad intestinal y la secreción de líquidos por células del recubrimiento intestinal (Figura 1-4). Estos mediadores ocasionan manifestaciones intestinales, de intensidad variable como diarrea, náusea, vómito o dolor abdominal, o signos en la cavidad oral como hormigueo, comezón o edema comunes del síndrome de alergia oral,116,117,118) que constituyen la fase temprana de la anafilaxia. Los mediadores de nueva síntesis están generalmente relacionados con la fase tardía de la anafilaxia alimentaria, en la que se evidencia un reclutamiento de células inflamatorias a los tejidos afectados. El TNF-α es vital en el reclutamiento de los mastocitos y la IL-9 incrementa la acumulación tisular de los mastocitos en modelos murinos,119,120 amplificando la respuesta inmune asociada a la patología. Además, la IL-33 participa en el mantenimiento del perfil Th2.91,93 Los leucocitos reclutados incluyen los basófilos, linfocitos T, neutrófilos, monocitos, macrófagos y eosinófilos.121 Todas estas células perpetúan el proceso inflamatorio mediante la producción de citocinas y otros mediadores citotóxicos capaces de producir más daño tisular o manifestaciones del proceso anafiláctico.122
Tal como se acaba de explicar, los mecanismos fisiopatológicos determinantes de las respuestas aberrantes frente a los alérgenos alimentarios son los inmunológicos. Sin embargo, los mediadores liberados por las células del sistema inmune activan neuronas sensoriales que pueden mediar reacciones como prurito, broncoconstricción o motilidad intestinal.123
La activación de los mastocitos de la mucosa intestinal en cobayos por alérgenos llevó a la liberación de histamina, lo que finalmente inhibió la síntesis de acetilcolina y noradrenalina a través del receptor inhibidor de la histamina H3R presente en las neuronas parasimpáticas y simpáticas.124,125 Por su parte, el péptido intestinal vasoactivo, un neuropéptido secretado por las neuronas aferentes primarias intrínsecas, participa en la relajación del músculo liso intestinal y pudiera hacerlo también en las interacciones neuroinmunes de la alergia alimentaria, ya que puede ser reconocido por células de la respuesta inmune.126
Tratamiento
Indiscutiblemente, el tratamiento más simple y efectivo en la alergia alimentaria es la dieta de eliminación, la cual debe individualizarse y ofrecer alternativas para garantizar el aporte de nutrimentos del alimento por evitar (como leche o huevo, alimentos altamente proteicos), además de instruir al paciente para el análisis del etiquetado nutricional de los alimentos.127,128 Sin embargo, pueden ocurrir el consumo accidental del alérgeno, por lo que es necesario disponer de tratamientos alternativos. El tratamiento de rescate en las reacciones alérgicas agudas sigue siendo el uso de antihistamínicos y glucocorticoides para las reacciones localizadas, y epinefrina autoinyectable para las sistémicas.129 Sin embargo, cada vez más estudios se centran en buscar opciones dirigidas a inducir tolerancia a los alérgenos o modular los mecanismos inmunológicos causantes de la enfermedad.
El uso de los antihistamínicos (antagonistas de receptores de las histaminas H1 y H2) constituye un tratamiento sintomático que bloquea el receptor específico correspondiente, inhibiendo los efectos de la histamina liberada y disminuyendo la urticaria y el prurito ocasionados por el consumo de algún alérgeno alimentario. Debe considerarse que su efecto suele ser más lento que el de otros medicamentos utilizados en esta condición alérgica.130,131
Por otro lado, los glucocorticoides no suelen utilizarse durante la fase aguda de la alergia alimentaria, ya que su efecto es lento y su efectividad no ha sido demostrada en estudios controlados con placebo en anafilaxia secundaria a alérgenos alimentarios. Sin embargo, su utilidad en otros padecimientos alérgicos como la rinitis o el asma en fases no agudas de la enfermedad deriva de sus funciones antiinflamatorias mediante la inhibición de factores de transcripción como NF-κB y AP-1 (que pueden ser activados por citocinas proinflamatorias) y la regulación de muchos genes sobreexpresados durante el proceso alérgico.132 Con base en su mecanismo de acción, su uso podría prevenir las reacciones tardías de la alergia a los alimentos.
Finalmente, la epinefrina es una opción de rápido efecto, indicada sobre todo en los cuadros de anafilaxia. Es un agonista del sistema adrenérgico y su acción recae sobre la disminución del edema de mucosas e inducción de broncodilatación, vasoconstricción y efectos musculares y cardiacos específicos (actividad cronotropa/ionotropa positiva).133,134
Leonard Noon fue el primer científico en notar que luego de administrar extractos de pólenes en concentraciones crecientes a individuos con rinitis alérgica, las manifestaciones de la patología desaparecían. En su artículo “Prophylactic inoculation against hay fever”, publicado en The Lancet, Noon demostró que la sensibilidad al alérgeno se reduce solo con la dosis y la frecuencia correctas, de lo contrario se ocasiona la exacerbación del problema.135 Lo anterior originó uno de los principales y más frecuentes tratamientos de la alergia alimentaria: la inmunoterapia desensibilizante.
Diversos trabajos de investigación han permitido comprender algunos de los mecanismos efectores de dicho tratamiento: existe una desviación del perfil Th2 al Th1, cambio de isotipo de anticuerpos IgE a IgG4 o IgA e incremento de la actividad de los linfocitos Treg, entre otros. Sin embargo, se necesitan más estudios que permitan diseñar protocolos más efectivos e inocuos para el paciente, adaptados a las diferentes variantes de la inmunoterapia: oral, sublingual o epicutánea.136
Un tratamiento altamente efectivo aprobado por la Food and Drug Administration (FDA) en el asma alérgica ha sido el omalizumab, un anticuerpo monoclonal humanizado anti-IgE que evita la unión de la IgE a sus receptores de baja y alta afinidad, disminuye la expresión de los mismos, la presentación de los alérgenos por las células dendríticas, así como la liberación de los mediadores de los mastocitos y basófilos, principalmente.137 En los últimos años, este tratamiento se ha estudiado en la alergia alimentaria y se ha observado mejoría en la tolerancia a mayores cantidades de alérgeno;138,139 aunque, se han obtenido mejores resultados cuando se combina con la inmunoterapia desensibilizante.140
Como se mencionó, los microorganismos desempeñan un papel importante en la inducción de la tolerancia en la mucosa intestinal, lo que plantea el uso potencial de probióticos como tratamiento profiláctico o terapéutico en las alergias alimentarias. Aunque el efecto benéfico de los probióticos ha sido probado en otros padecimientos alérgicos, es importante realizar estudios que demuestren su eficacia en las alergias a los alimentos mediadas por IgE.
En general, los probióticos pueden ejercer efectos inmunorreguladores en numerosos puntos del proceso alérgico, modulando la acción de células presentadoras de antígeno y de linfocitos B y favoreciendo el sesgo del perfil regulador en el microambiente mucoso intestinal, además de incidir directamente en el mantenimiento de una barrera intestinal intacta.141) Se ha reportado que la administración oral de Bifidobacterium infantis en un modelo murino de alergia a OVA origina sobrerregulación de los géneros Coprococcus y Rikenlla, logrando a su vez disminuir los síntomas, los niveles de IgE e IgG1 séricas alérgeno-específicas, así como la producción de IL-4, IL-5 e IL-13 por los esplenocitos en respuesta a la OVA.142
En otro modelo murino de alergia a la OVA, la administración oral de Lactococcus lactis NCC 2287 redujo las manifestaciones alérgicas mediante la disminución en los niveles de citocinas del perfil Th2, principalmente IL-13 y eotaxina-1.143 Además, la coadministación de Lactobacillus rhamnosus con el alérgeno por inmunoterapia oral, potencia la tolerancia inducida en niños alérgicos.144
Debido a la importancia de las citocinas en el desencadenamiento de las alergias alimentarias, otra opción propuesta es el uso de anticuerpos anticitocinas. Se ha sugerido que el uso de anticuerpos que bloquean algunas citocinas clave del perfil alérgico, como IL-4 e IL-13, mejora algunos estados alérgicos como el asma o la dermatitis atópica; los anticuerpos son más efectivos al utilizarlos contra varias citocinas simultáneamente, debido a los mecanismos redundantes entre estas.145 Aun cuando las mismas citocinas están presentes en la fisiopatología alérgica alimentaria, hay que demostrar su eficacia en este contexto. Uno de los anticuerpos más prometedores y que se encuentra en ensayos clínicos de fase 2 controlado con placebo es el anticuerpo monoclonal etokimab, dirigido contra la IL-33, debido a la importancia de esta citocina en el desarrollo de la patología.146,147
Por último, entre los tratamientos más novedosos se encuentra la exposición a los alérgenos mediante vacunas de ADN, que busca desviar la respuesta inmune hacia el perfil Th1. Algunas de estas vacunas se encuentran en la fase 1 de su estudio clínico.148,149
Conclusiones
La alergia alimentaria es una patología compleja con numerosos factores idiosincráticos que la hacen difícil de abordar. Durante las últimas décadas, su incidencia se ha incrementado y, aunque en la mayoría de los casos no resulta mortal, disminuye la calidad de vida del paciente y ocasiona costos importantes al sistema de salud y a las familias. El entendimiento de las características alergénicas de algunos alimentos y de los mecanismos inmunológicos que subyacen a la fisiopatología de la alergia alimentaria es crucial para el desarrollo de estrategias terapéuticas. El objetivo de las nuevas terapias debe centrarse en limitar el daño orgánico y reinstaurar un estado de tolerancia inmunológica en el individuo, de forma que se logre un mayor control de la enfermedad y de su sintomatología, evitando así el uso de tratamientos de emergencia.











 nueva página del texto (beta)
nueva página del texto (beta)



