Introducción
La respuesta inflamatoria es un proceso altamente regulado que integra una compleja red de señales que implican comunicación celular. Dicha comunicación involucra la secreción y la subsecuente detección, mediada por receptores específicos, de distintas biomoléculas como citocinas, quimiocinas e, incluso, distintos tipos de metabolitos. En este sentido, se reconoce la existencia de comunicación intercelular, tanto unidireccional como bidireccional, entre leucocitos y células no inmunológicas durante el inicio, el mantenimiento y la resolución del proceso inflamatorio.1 La mayoría de las interacciones entre células del sistema inmunológico que no involucran el contacto directo se dan gracias a citocinas liberadas en respuesta a diferentes estímulos; sin embargo, evidencias recientes demuestran la existencia de un tipo distinto de comunicación intercelular mediado por exosomas; un subtipo de vesículas extracelulares (EV) capaces de regular procesos inflamatorios.
De forma general, las EV son clasificadas de acuerdo con su tamaño y su origen: las EV que se forman y desprenden directamente de la membrana plasmática se nombran como ectosomas; los exosomas difieren de estas vesículas debido a que se derivan de procesos de invaginación de membranas endosomales para formar cuerpos multivesiculares que se fusionarán posteriormente con la membrana plasmática.2 Las vesículas así liberadas poseen un tamaño de 30 a 150 nm y se componen de una bicapa con composición lipídica distintiva, diversas proteínas tanto transmembranales como citoplasmáticas, así como diferentes clases de RNA, incluyendo mRNA, lncRNA y miRNA (Figura 1).3,4,5,6,7 Algunas proteínas altamente enriquecidas en exosomas son empleadas como marcadores para identificar a estas vesículas, algunos ejemplos incluyen a Hsp70 o las tetraspaninas CD9, CD63 y CD81. Las células emplean a estas nanovesículas como medio de comunicación con células adyacentes o muy distantes entre sí; las moléculas presentes en la superficie de las EV les permiten el reconocimiento de células blanco. Estas vesículas son capaces de inducir procesos de señalización a través de interacciones ligando-receptor, pueden ser internalizadas mediante endofagocitosis o pueden incluso fusionarse directamente con la membrana plasmática de las células blanco, liberando su contenido en el citoplasma de las mismas.7
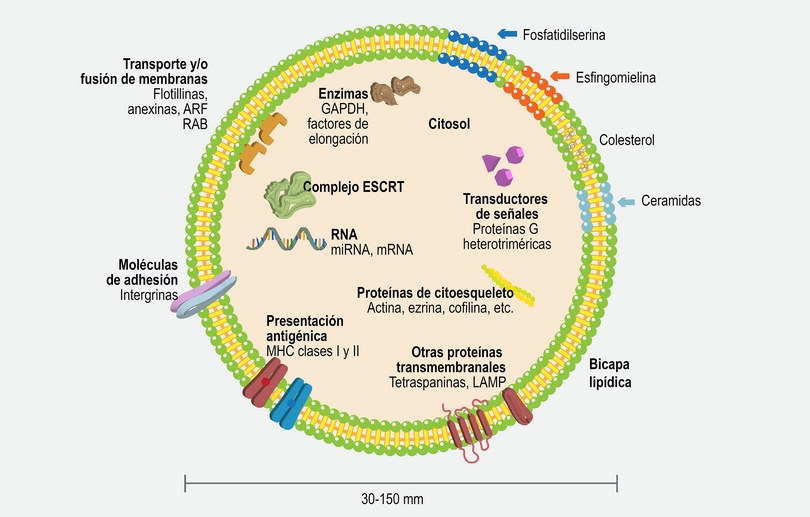
Figura 1 Características y composición de los exosomas. Los exosomas se componen por una bicapa lipídica enriquecida en diversos lípidos, así como diferentes proteínas transmembranales embebidas en dicha estructura. En su interior, estas microvesículas contienen diversas proteínas típicamente citosólicas derivadas de la célula de procedencia con funciones enzimáticas, implicadas en transducción de señales, adhesión, presentación de antígenos o coestimulación y proteínas propias de la génesis exosomal. De igual forma, dicho contenido exosomal incluye usualmente diversos tipos de RNA, incluyendo RNA mensajero (mRNA) así como microRNA (miRNA) y RNA largos no codificantes (lncRNA).
Los efectos biológicos generados tras la captación de exosomas por parte de las células blanco dependen en gran medida de la naturaleza de las células generadoras de exosomas.8,9 El contenido exosomal varía dependiendo de la fuente y las condiciones fisiológicas de las células que liberan estas nanovesículas: cambios debidos a infección, inflamación o transformación como en el caso de células tumorales e, incluso, cambios inducidos por la presencia de fármacos, pueden influenciar y alterar la composición de los exosomas. Sin embargo, es claro que no todo el contenido de la célula generadora de exosomas se halla presente en estas EV, lo cual sugiere que el proceso de “carga” de las moléculas exosomales se encuentra bien regulado y que puede ser alterado por diversas señales. La variabilidad en las moléculas que presentan los exosomas explica las múltiples consecuencias funcionales que su captación puede ejercer sobre las células blanco, así como su utilidad como biomarcadores. A pesar de que el papel homeostático de los exosomas sigue en discusión, se reconoce su importancia en condiciones patológicas, ejerciendo funciones protectoras durante el desarrollo de diversas enfermedades.10 Para el caso de las células del sistema inmunológico, múltiples funciones de estas EV se han descrito en estudios con células presentadoras de antígeno como macrófagos y células dendríticas (DC).
Función inmunorreguladora de los exosomas
Funcionalmente, el sistema inmunológico puede dividirse en respuesta inmune innata y adaptativa. La respuesta innata se halla evolutivamente conservada y está presente en todos los organismos multicelulares, mientras que la respuesta adaptativa es exclusiva de vertebrados.11 La activación del sistema inmune innato se encuentra controlada por un número limitado de receptores capaces de reconocer patrones moleculares asociados a patógenos (PAMP) o a daño celular (DAMP).12 Estos receptores de reconocimiento de patrón, como los receptores tipo Toll (TLR), se encuentran codificados en línea germinal.
En el caso de la inmunidad adaptativa, los receptores de antígeno, más allá de esta propiedad, se caracterizan por ser el resultado de procesos de recombinación y mutación somática,13 lo cual resulta en un amplio repertorio de este tipo de receptores presentes en las células más características de este tipo de inmunidad; los linfocitos, tanto T como B. Los linfocitos B pueden reconocer antígenos de forma nativa, mientras que las células T utilizan el proceso de presentación antigénica para el reconocimiento de los mismos. Las DC, los macrófagos y los propios linfocitos B son células presentadoras de antígeno (APC). Las APC son capaces de internalizar antígenos, procesarlos (degradarlos hasta péptidos en el caso de proteínas) y montarlos sobre moléculas del complejo principal de histocompatibilidad, tanto de clase I (MHC-I) como de clase II (MHC-II), para su presentación a linfocitos T naïve CD8+ y CD4+, respectivamente, desencadenando su activación.14
Los exosomas desempeñan un papel crucial al desplegar complejos MHC-péptido funcionales en su superficie para modular respuestas antígeno específicas de linfocitos T CD4+ y CD8+.15,16 Esta presentación puede ejercerse de forma directa u ocurrir en forma de presentación cruzada. En la presentación directa, los complejos MHC-péptido sobre los exosomas se unen y entrecruzan directamente con receptores antígeno-específicos de células T (TCR). En el caso de la presentación cruzada, las APC captan antígenos acarreados por exosomas y tras un procesamiento adicional de los mismos, son presentados a células T. La presentación cruzada también puede ocurrir cuando complejos MHC-péptido son transferidos por fusión exosomal a las membranas de DC y posteriormente presentados a linfocitos T.15
Función inmunorreguladora del RNA exosomal
Los análisis de secuenciación de nueva generación de material genético proveniente de exosomas aislados de muestras de plasma humano demuestran la presencia de una amplia variedad de especies de RNA en estas nanovesículas circulantes.17 Dichas variantes incluyen RNA mensajeros y RNA reguladores tales como microRNA (miRNA) y RNA no-codificantes largos.3,18,20
Los estudios de secuenciación de RNA de macrófagos (en reposo comparados con células activadas) demuestran que la inflamación altera importantemente el transcriptoma de dichas células.21 De forma interesante, estudios del mismo tipo llevados a cabo comparando RNA exosomal derivado de macrófagos naïve y estimulados con lipopolisacárido (LPS) indican también alteraciones en el transcriptoma exosomal inducidas por la inflamación. En este sentido, el análisis de vías de señalización implicadas en este proceso muestra cambios significativos, específicamente en aquellas relacionadas con la señalización vía TLR y con la activación de NF-kB, en donde se observan cambios entre los mRNA exosomales de las células naïve comparados con sus correspondientes en células estimuladas con LPS.22 Adicionalmente, se ha reportado que los miRNA miR-21 y miR-29a, secretados por células tumorales, pueden fungir como ligandos de TLR7 y TLR8 en leucocitos, promoviendo así la activación de NF-kB y la secreción de citocinas proinflamatorias.23
Los avances actuales respecto a la secuenciación de RNA (RNAseq) muestran que los miRNA son abundantes en los exosomas.2,5 También se ha descrito que el repertorio de miRNA en exosomas es distinto a aquel que despliegan las células de las que derivan estas nanovesículas. De forma interesante, análisis recientes sugieren que los miRNA son incorporados dentro de exosomas de forma regulada y selectiva.24,25 En este sentido, se han identificado varios procesos y proteínas que median la selección e incorporación de estos RNA en exosomas; algunos de ellos incluyen:
La implicación de la esfingomielinasa neural 2 (nSMase2), que se observa tras inducir la sobreexpresión de nSMase2 en células epiteliales mamarias. En este caso, se detecta un incremento en la producción de exosomas y en los niveles de miRNA exosomales secretados. De forma opuesta, la inhibición de la expresión de esta proteína correlaciona con la reducción en el número de miRNA exosomales.26
La contribución de las ribonucleoproteínas heterogéneas nucleares sumoiladas (hnRNP) y motivos específicos de los miRNA. Se reconoce que hnRNPA2B1 es capaz de reconocer el motivo GGAG en la secuencia de miRNA, lo que se asocia con la incorporación de estos últimos en exosomas.27 Un número elevado de repetidos de dicho motivo se halla presente en los miRNA que se encuentran enriquecidos comúnmente en exosomas, como es el caso de los producidos por células T.27
El papel de la secuencia 3' de los miRNA. Algunos estudios han implicado que las adenilaciones y las uridilaciones en el extremo 3' de los miRNA contribuyen directamente a la regulación de la incorporación de estos elementos en exosomas, con lo cual se sugiere la existencia de alguna señal (motivo), aún no identificada en esta región de estos RNA, que controle dicho proceso.28
La participación del complejo de silenciamiento inducido por miRNA (miRISC). Los miRNA son capaces de interactuar con las proteínas AGO2 y GW182 para conformar el complejo miRISC. Este último ha sido detectado colocalizando con cuerpos multivesiculares existiendo una correlación entre la expresión de AGO2 y la incorporación de miRNA en exosomas; de esta forma, se ha observado que la inhibición en la expresión de AGO2 disminuye la abundancia y la diversidad de miRNA secretados en nanovesículas.29,30
Por otra parte, en la actualidad se reconoce que distintos miRNA son transferidos entre células del sistema inmunológico con consecuencias funcionales que implican generalmente, la regulación de las respuestas inflamatorias. De forma interesante, se ha observado que la transferencia de miRNA entre células T y APC, mediada a través de exosomas, se ve favorecida tras la formación de una sinapsis inmunológica funcional.31
En cuanto a la regulación de la inflamación; diversos miRNA “responsivos” a lipopolisacárido (LPS) poseen múltiples genes “blanco” validados que codifican para proteínas involucradas en señalización vía receptores acoplados a proteínas G, destacando receptores de quimiocinas, señalización vía TLR y en la vía de señalización ejercida por TGF-β. En un estudio donde se determinaron los perfiles de miRNA presentes en exosomas purificados de dos líneas de APC distintas: RAW 264.7 (macrófagos de ratón) y THP-1 (línea monocítica humana), tanto en reposo como tras estimularlas con LPS, se demostró la variabilidad interespecie en el contenido de estas moléculas en microvesículas respecto al tipo celular y al estado fisiológico celular.22
Igualmente, la estimulación con LPS en las células RAW 264.7 modifica de forma significativa las proporciones de RNA no codificantes presentes en exosomas; la presencia y el incremento de pre-miRNA y snoRNA (RNA nucleolares pequeños) en estas condiciones nos indica que las células receptoras de estos exosomas podrían ser susceptibles de modificaciones epigenéticas temporales que regulen la expresión de genes inflamatorios blanco.32 El influjo de pre-miRNA asociados con eventos inflamatorios en células estimuladas con LPS probablemente se asocia con la necesidad de una respuesta rápida durante la inflamación más que una regulación a nivel transcripcional dentro del núcleo. Los miRNA maduros en este caso pueden mediar la regulación fina en estos procesos al alterar los niveles de mRNA de proteínas asociadas con el fenómeno inflamatorio de forma inmediata. En paralelo, los pre-miRNA que se incorporen representan un segundo evento de regulación que se iniciará posteriormente, después del procesamiento final de estas moléculas. En este sentido, los exosomas poseen la ventaja de mediar la incorporación de proteínas maduras y RNA reguladores ya listos (preformados) para actuar de forma inmediata al interior de la célula receptora.22
Más allá de los miRNA y otros ácidos nucleicos ya mencionados, existen evidencias de la regulación mediada por fragmentos pequeños de mRNA. En cuanto a exosomas, se ha verificado la existencia de estos fragmentos enriquecidos en las regiones no traducidas 3' (3'UTR) de diversos mensajeros completos cargados en estas microvesículas.33 Estas regiones 3'UTR poseen propiedades reguladoras ya que permiten la interacción de proteínas de unión a RNA que modulan la estabilidad y la eficiencia traduccional de los mensajeros. Dichas regiones también poseen múltiples secuencias blanco para miRNA que guían la asociación del complejo de silenciamiento inducido por RNA (RISC) y que media a su vez, eventos de degradación de los mensajeros y posterior represión traduccional.33
Función inmunorreguladora de las proteínas exosomales
Dentro del proteoma de exosomas se han logrado identificar proteínas citoplásmicas, nucleares, endosomales y membranales.34,35,36 Dentro de estas destacan moléculas típicamente asociadas con tránsito vesicular (Rab GTPasas, SNARE, flotillina y anexinas), proteínas involucradas en la biogénesis exosomal (miembros del complejo ESCRT, ALIX, TSG101, etcétera), tetraspaninas (CD9, CD63, CD81, etcétera), proteínas de choque térmico (HSP70, HSP90, etcétera) y moléculas de histocompatibilidad, tanto de clase I como de clase II.37 Cabe resaltar que los exosomas funcionan importantemente como acarreadores de mediadores solubles tales como las citocinas, una función particularmente relevante para la comunicación intercelular en el sistema inmunológico.38
La mayoría de los estudios con exosomas y su efecto en el sistema inmunológico han sido llevados a cabo en el contexto del cáncer y la autoinmunidad; dentro de estos, se ha prestado mayor atención a la regulación de dichos procesos por parte del sistema inmune adaptativo, aunque recientemente se han empezado a generar datos que apuntan a la participación de los exosomas regulando respuestas inmunes innatas.
Inmunidad innata
Las DC producen exosomas de forma constitutiva; dichas nanovesículas han sido implicadas por algunos estudios en la activación de la respuesta inmune innata (Figura 2). Tanto los exosomas de DC inmaduras (iDC) como aquellos de DC maduras (mDC) contienen en su superficie diversas proteínas pertenecientes a la familia del factor de necrosis tumoral (TNF), incluyendo por ejemplo a TNFα, TRAIL y FasL, mismas que se ha reportado pueden unirse a receptores presentes en células NK para favorecer su actividad citotóxica.2 En este sentido, es interesante resaltar que la actividad de dichas células NK se ve favorecida cuando son estimuladas con exosomas liberados a partir de mDC activadas.39

Figura 2 Los exosomas generados por APC modulan las respuestas inmunológicas innatas y adaptativas. Exosomas derivados de DC maduras (mDC) pueden proveer estimulación antigénica a linfocitos T, así como inducir respuestas de tipo innato en diversas células del sistema inmunológico y de otros tipos, promoviendo una respuesta proinflamatoria. En contraparte, lo exosomas liberados por DC inmaduras (iDC) poseen una naturaleza inmunosupresora, siendo capaces de inducir apoptosis en células T efectoras o promover la activación de células con fenotipo regulador (Treg). M0, monocito; NK, célula natural-killer; DP, presentación antigénica directa; CP, presentación antigénica cruzada o cross-presentation; CD, cross-dressing; CIA, artritis inducida por colágeno; DT4, hipersensibilidad tipo 4.
De forma análoga, otras proteínas presentes en exosomas pueden fungir como ligandos de receptores de células NK, tal es el caso de BAT3, que se puede unir a NKp30 para generar activación celular.40 En otro contexto, las DC activadas con lipopolisacárido (LPS) liberan vesículas extracelulares capaces de estimular la secreción de quimiocinas como IL-8 o RANTES por parte de células epiteliales, un fenómeno relevante durante la patogénesis de afecciones tales como la sepsis. Así también se ha demostrado la actividad de TLR presentes en exosomas provenientes de células estimuladas con LPS en la polarización de macrofagos distales M1 y el aumento de la expresión de genes proinflamatorios (CCL3, IL1B, TNF) y la generación de un estado refractario en la célula distal a través del aumento de TOLLIP.41
Inmunidad adaptativa
La presencia y abundancia de antígenos del complejo principal de histocompatibilidad, tanto de clase I como de clase II (MHC-I y MHC-II), así como de moléculas de coestimulación para células T, en la superficie de los exosomas derivados de DC, macrófagos y linfocitos B representan evidencia de su papel en los mecanismos de presentación antigénica de dichas células. En este sentido, se han propuesto tres posibles mecanismos mediante los cuales los exosomas liberados por APC son capaces de estimular la activación de linfocitos T:
Presentación cruzada (cross-presentation): los exosomas secretados por una APC dada, que contienen proteínas/péptidos antigénicos, son capturados por APC bystander que posteriormente procesan y presentan estos antígenos valiéndose de sus moléculas de histocompatibilidad MHC-I y MHC-II endógenas (Figura 2), generando la activación de células T específicas.42,43
Captación exosomal/fusión de membranas (cross-dressing): las APC captan exosomas de otras APC conteniendo complejos MHC-péptido (Figura 2); dichos complejos son incorporados en la membrana de las células receptoras capacitándolas para la presentación a las células CD4+ o CD8+ antígeno-específicas.44,45 Ambos mecanismos requieren la captura de exosomas libres por parte de las APC, en consecuencia, se reconoce la existencia y participación de diversos receptores y moléculas de adhesión en este fenómeno dentro de los cuales se incluyen diversas tetraspaninas, ICAM1, MFG-E8 y fosfatidilserina por mencionar algunos ejemplos.46,47,48 Estas moléculas facilitan la interacción de los exosomas con las APC (y otros tipos celulares) receptoras, tal es el caso de MFG-E8 que interactúa con las integrinas αvβ3 y αvβ5 (ambas con expresión constitutiva en macrófagos y DC humanas), así como con fosfatidilserina.46,47
Activación directa de linfocitos T por exosomas: debido a su contenido de moléculas MHC-I y MHC-II, así como proteínas de coestimulación, se reconoce que los exosomas derivados de APC, particularmente aquellos secretados por DC, tienen el potencial de activar directamente linfocitos T CD4+ o CD8+ (Figura 2).45,49,50 A pesar de que este mecanismo de estimulación se ha observado principalmente con células T de memoria o células T previamente activadas,51,52 existen evidencias de que los exosomas pueden activar células T naïve de forma directa. Como se mencionó anteriormente, dicho fenómeno de activación requiere la presencia de moléculas de adhesión y de coestimulación en las vesículas, ejemplos de ello son ICAM1 y B7 respectivamente.53
Ejemplos de este papel directo de los exosomas en la activación linfocitaria son estudios que han empleado APC “sintéticas” secretoras de exosomas (transfectadas con MHC-I determinados) capaces de inducir la actividad de células T CD8+ de ratón en un modelo in vitro,53 así como la estimulación directa de linfocitos T CD8+ derivados de PBMC humanas en presencia de exosomas que contienen complejos MHC I-péptido en un modelo de infección viral.48
Es importante mencionar que a pesar de que esta estimulación directa se ha demostrado con estos modelos, existen evidencias de que la actividad estimulatoria de estas vesículas es de entre 10 a 20 veces menos eficiente con respecto a la presentación antigénica ejercida por una APC completa,54,55 sugiriendo que la interacción directa exosoma-célula T no necesariamente representa un mecanismo principal de activación de células T naïve in vivo.
Independientemente del mecanismo de presentación antigénica por parte de los exosomas, la capacidad para estimular células T puede depender del estado de activación de la APC generadora de dichas nanovesículas. Como es de suponer, los exosomas generados por DC maduras poseen mayor cantidad de MHC clase II, ICAM1 y moléculas de coestimulación respecto a los producidos por DC inmaduras,48 un fenotipo que se relaciona con una mayor capacidad activadora. En contraste, los exosomas derivados de DC inmaduras han sido asociados con la generación de anergia en células T, así como la promoción de la activación de células T reguladoras (Treg), por lo que dichas nanovesículas emergen entonces como un posible tratamiento en ciertas enfermedades, particularmente aquellas con un componente autoinmune.56,57
Potencial terapéutico de los exosomas
En años recientes, el uso de DC con fines inmunoterapéuticos para el cáncer y diversas enfermedades con algún componente inflamatorio se ha extendido, sin embargo, la factibilidad de los tratamientos basados en este enfoque se ha visto comprometida debido a las dificultades intrínsecas derivadas del uso de dichas células. En el presente escenario, los exosomas de DC adquieren relevancia debido a su facilidad relativa de manipularse y adaptarse a los procesos regulados de manufactura y almacenaje a largo plazo requeridos o deseados. Adicionalmente, la administración de exosomas reduce enormente los riesgos y complicaciones potenciales derivados de la introducción de células exógenas (o propias pero manipuladas ex vivo) a un individuo dado.11
Existen evidencias claras de la utilidad de exosomas de DC para el tratamiento de cáncer; se ha reportado que los exosomas derivados de DC aisladas de tumores son capaces de inducir la activación de linfocitos T citotóxicos específicos contra el tumor in vivo y que, además, la simple inyección de estas vesículas en el sujeto enfermo resulta en la disminución del crecimento tumoral o la completa erradicación del mismo en un modelo murino.58 Así, es evidente que los exosomas, al igual que las DC de las que provienen, mantienen su capacidad de presentar antígenos asociados com tumores para activar respuestas específicas dirigidas contra aquellas células que poseen estos antígenos.59,60
Actualmente algunos estudios han demostrado la factibilidad de la producción a gran escala de exosomas derivados de DC, confirmando, además, su perfil de seguridad adecuado durante su administración a pacientes.61 En un ensayo clínico que incluyó pacientes con un estadio avanzado de melanoma, se demostró que tras la administración de una primera generación de exosomas de DC, dichos individuos mostraron un incremento relevante en las respuestas de células NK, no así las que involucran células T específicas.61 La inmunogenicidad limitada de las mencionadas nanovesículas llevó al desarrollo de una segunda generación de exosomas derivados de DC, en este caso obtenidos a partir de células tratadas con INF-γ, que expresan niveles mayores de CD40, CD80, CD86 e ICAM1 respecto a los exosomas de DC inmaduras, características que, como se ha mencionado, favorecen la inmunogenicidad de estas estructuras.62 Con este precepto, se desarrolló un ensayo clínico fase II, incluyendo pacientes con carcinoma pulmonar de células no pequeñas (NSCLC) no operable. Exosomas de DC tratadas con IFN-γ cargados con antígenos derivados de este tipo de tumor en complejo con moléculas de MHC-I y MHC-II fueron usados a manera de inmunoterapéutico de mantenimiento después de una quimioterapia de inducción. A pesar de las expectativas de generar actividad antitumoral por parte de células T, este ensayo solo pudo corroborar la exacerbación de la respuesta citotóxica por parte de células NK contra este tipo de tumores.63
Los exosomas derivados de APC también han demostrado ejercer un efecto inmunosupresor en distintos modelos de enfermedad inflamatoria, incluyendo la artritis reumatoide.57 En la artritis inducida por colágeno se ha observado una mejoría en la enfermedad tras la administración de DC transducidas para expresar IL-10 o tratadas con IL-10 recombinante murina.64,65
Con esto en mente, se han desarrollado enfoques para la obtención de exosomas derivados de DC que sobreexpresan esta citocina y otras moléculas como IL-4, FasL y la enzima indoleamina 2,3 dioxigenasa (IDO). La administración sistémica de estos exosomas IL-10+ en un modelo de artritis inducida por carragenina en ratones demostró efectividad al frenar la progresión de la enfermedad; un efecto que no pudo ser reproducido en el mismo estudio tras la administración de IL-10 recombinante murina.66 De la misma forma, al generar DC con sobreexpresión de IL-4 se observó la capacidad de estas células para reducir la inflamación en el mismo modelo de artritis inducida en ratón. Al igual que en el caso anterior, los exosomas derivados de estas DC demostraron su efectividad al reducir la incidencia y severidad de la enfermedad inducida tras su administración sistémica, además de que se les atribuyó una mayor eficiencia respecto a dosis repetidas de IL-4 recombinante.64 Consecuencias similares se observaron en el mismo tipo de modelo tras la administración de exosomas derivados de células con sobreexpresión de FasL.65 Por último, para el caso de los exosomas que sobreexpresan IDO, se ha reportado que los mismos son capaces de reducir inflamación, inhibir la activación de células T y suprimir las respuestas de estas últimas células contra auto y aloantígenos.67
Por otra parte, los exosomas, y particularmente su contenido, pueden ser empleados como biomarcadores para enfermedades inflamatorias. La presencia de exosomas en diversos fluidos corporales, una composición rica en proteínas, diversos RNA y lípidos característicos, así como la plasticidad mostrada por su contenido en respuesta a diversos estímulos hacen de estas vesículas un elemento biomarcador de alteraciones en el estado de salud de un individuo. La utilidad potencial de estas vesículas como fuente de biomarcadores en enfermedades inflamatorias se refleja en los datos mostrados en el Cuadro 1.
Cuadro 1 Exosomas como biomarcadores en enfermedades inflamatorias
| Enfermedad | Fuente de exosomas | Biomarcadores | Referencias |
|---|---|---|---|
| Artritis reumatoide | Suero y líquido sinovial | Proteínas citrulinadas y Hotair | 68, 69 |
| Lupus eritematoso generalizado | Orina | Bajos niveles de miR-26a y 29c, altos niveles de miR-146a | 70, 71, 72 |
| Síndrome de Sjögren | Saliva | miR-let7b, miR-let7c, miR-128, entre otros. | 73 |
| Enfermedad intestinal inflamatoria | Suero | Anexina A1 | 74 |
| Hepatitis alcohólica | Plasma y suero | miR-192 y miR-30a | 75 |
Conclusiones
Actualmente existe un enorme interés en dilucidar el papel de los exosomas, tanto en condiciones fisiológicas normales como en el caso de diversas enfermedades. Como se ha descrito, estas nanovesículas resultan de especial interés como potenciales acarreadores terapéuticos de diversas moléculas inmunomoduladoras, debido a que poseen diversas ventajas sobre otros enfoques tales como el empleo de vectores genéticos o liposomas. En este sentido, los exosomas pueden actuar como “nanoacarreadores” naturales membranosos y no tóxicos de diversas biomacromoléculas, particularmente útiles en contextos autólogos. Por otra parte, el contenido de estas estructuras ha sido estudiado ampliamente con miras a su empleo como biomarcadores útiles en el diagnóstico temprano de diversas enfermedades, debido a la naturaleza no invasiva de la su obtención. Debido a estas razones, el estudio y comprensión de la biología exosomal adquiere relevancia en la futura implementación de estrategias para hacer de la “medicina de precisión” una realidad aplicable a diversas enfermedades.











 nueva página del texto (beta)
nueva página del texto (beta)


