Introducción
Ectasia vascular antral gástrica
La ectasia vascular antral gástrica o GAVE (por sus siglas en inglés Gastric Antral Vascular Ectasia, es un tipo de malformación vascular de tipo capilar localizada predominantemente en antro gástrico. Endoscópicamente se caracterizada por lesiones rojas y angiomatosas. Es un proceso patológico gástrico, que generalmente presenta pérdida crónica de sangre, hemorragia digestiva y anemia por deficiencia de hierro. GAVE fue descrito por primera vez por Rider et al. en 19531,2, sin embargo, no fue reconocido hasta el advenimiento de la endoscopia moderna, con Jabbari, et al. en 1984, donde se describió una serie de casos de 3 pacientes con características clásicas endoscópicas de GAVE con líneas de mucosa eritematosa longitudinal. El termino de “estómago en sandía” se utilizó por el aspecto rayado2,3.
Epidemiologia, Etiopatogenia y condiciones asociadas
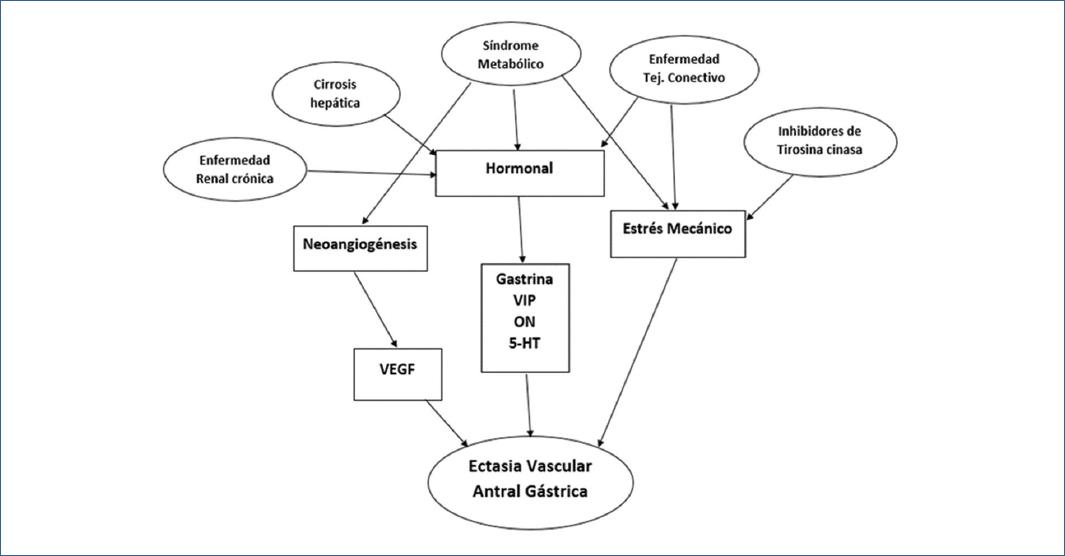
GAVE se cree que es una enfermedad adquirida según sus hallazgos histopatológicos4. Representa el 4% de todas las hemorragias gastrointestinales superiores no variceales, y hasta 62% de los pacientes afectados se vuelven dependientes de la transfusión1-3,5. La prevalencia es poco conocida pero se estima de 0.2-2%. Tiene predominio en mujeres entre la sexta y octava década de la vida. Tiene una asociación clara con múltiples enfermedades incluyendo enfermedad del tejido conectivo, enfermedad hepática, cardiopatía isquémica, trasplante de médula ósea6, y componentes del síndrome metabólico, no tiene asociación con hipertensión portal7,8. Dentro de su etiopatogenia se considera estrés mecánico como mecanismo patogénico en el molinillo antral de alta presión y se ha visto un mecanismo patogénico similar en la intususcepción intestinal, además que múltiples enfermedades metabólicas tienen alteración en la motilidad9-11, lo que favorece aún más este mecanismo. También se ha observado un mecanismo hormonal con aumento de gastrina, glucagón y óxido nítrico, así como aumento de péptido intestinal vasoactivo12. Además GAVE y los pólipos hiperplásicos comparten características histológicas similares, así como una asociación clínica con gastritis autoinmune y niveles elevados de gastrina, lo que sugiere un mecanismo compartido13. Tiene una asociación clara con enfermedad autoinmune principalmente enfermedades del tejido conectivo representando del 14,8 al 62% de todos los pacientes con este diagnóstico15. El tratamiento exitoso con ciclofosfamida y esteroides en pacientes con esclerodermia difusa y GAVE refractaria, sugiere que la fisiopatología sugiere un proceso inmunomediado16. Se ha observado en varios estudios el uso de inhibidores de tirosina quinasa (específicamente imatinib y dasatinib) para el tratamiento de procesos neoplásicos y la asociación con GAVE17-19. En los últimos informes, ha habido mayor evidencia de asociaciones entre GAVE y diversas características del síndrome metabólico. Estas asociaciones incluyen obesidad, diabetes, NASH, hipertensión arterial e hiperlipidemia1-3. Los modelos actuales favorecen su surgimiento de un estado proinflamatorio, protrombótico y estrés oxidativo (1,20,21). Esto conduce a un estado hipóxico relativo y un aumento posterior del VEGF, promoviendo la proliferación vascular1,21,22. Se han reportado tres casos en la literatura de GAVE refractarios a APC que fueron tratados exitosamente con talidomida, un potente agente anti-VEGF (23). La etiopatogenia propuesta para GAVE se observa en la figura 1.
Apariencia endoscópica de GAVE
Desde su descripción original se han descrito tres fenotipos endoscópicamente reconocidos, que también pueden presentarse en combinación. Estos fenotipos incluyen: (1) la apariencia endoscópica de “sandía” rayada “clásica”, que puede ser elevada o plana; (2) una distribución antral difusa de angiodisplasias dispersas, ocasionalmente denominado patrón de “panal”; y (3) una variante nodular también conocida como gastropatía antral nodular1,3. Además de la enfermedad antral, GAVE también puede manifestarse con un parche en el cardias proximal.
Diagnóstico histológico de GAVE
El diagnóstico histológico de GAVE se confirma por la presencia de vasos mucosos anormalmente dilatados con trombos de fibrina, proliferación de células fusiformes e hiperplasia fibromuscular en la lámina propia1,3,4. Además, la evaluación histológica puede producir falsos negativos de un muestreo inadecuado y puede requerir tinciones especiales para microtrombos (CD61) para confirmar el diagnóstico5. Además la histología no puede distinguir GAVE nodular de pólipos hiperplásicos; por lo que se puede diagnosticar erróneamente GAVE como un pólipo hiperplásico5.
Tratamientos endoscópicos de GAVE
El tratamiento con Argón plasma coagulación
La coagulación con argón plasma (por sus siglas APC) es un método térmico de no contacto que utiliza gas argón para suministrar plasma de energía térmica uniformemente distribuida a un campo de tejido adyacente a la sonda con una profundidad de penetración de 2-3 mm. APC ha sido el tratamiento endoscópico de elección para GAVE desde su introducción. En general, los pacientes tienen eficacia del 90-100%, sin embargo con una tasa de recurrencia de 49.7% después de 1 año, 35.5% después de 2 años y 35.5% después de 3 años3,24-27.
Ligadura con banda endoscópica (LBE)
La eficacia de LBE se ha informado en 70-85% de los casos3,28,29. Recientemente se ha publicado un ensayo controlado aleatorio de LBE versus APC para GAVE29, con 88 pacientes (todos cirróticos) que fueron incluidos y aleatorizados para recibir tratamiento endoscópico cada 2 semanas. Ambos grupos tuvieron un aumento significativo en los niveles de hemoglobina, pero sin diferencias entre ellos. En el grupo LBE, el 13.6% de los pacientes tuvieron eventos adversos, y en el grupo APC, el 20.5%29.
Ablación por radiofrecuencia (ARF)
En 2008 se publicó un ensayo piloto de ARF para el tratamiento de GAVE con el catéter de ablación HALO90 que incluía a 6 pacientes. La tasa de éxito clínico general osciló entre 67 y 86%. Las complicaciones fueron leves; sin embargo, hay un informe reciente de un paciente que experimentó bacteriemia y sepsis después del tratamiento con ARF para GAVE30,31.
Coagulación con láser YAG
En un estudio retrospectivo a largo plazo de 2003, 24 pacientes con GAVE fueron tratados con láser Nd: YAG durante un período de 18 años con una mediana de seguimiento de 55 meses (rango 9-127) después del último procedimiento. Veinte pacientes experimentaron resolución de sangrado y permanecieron libres de transfusiones durante una mediana de 16 meses. Un tratamiento más profundo también aumenta el riesgo de perforación, que ocurrió en 1/24 sujetos en este estudio, además de alto costo asociado1,32.
Crioterapia
Kantsevoy, et al. demostró el éxito de la crioterapia en pacientes con hemorragia gastrointestinal refractaria secundaria a GAVE. De los 7 pacientes tratados con GAVE, 5 (77%) dejaron de sangrar con hallazgos normales de la mucosa a los 6 meses después del tratamiento (33). Otro estudio se centró en 12 pacientes con GAVE y anemia por deficiencia de hierro, y demostró que Cinco pacientes mostraron una respuesta parcial, con Hemoglobina estable y un número reducido de transfusiones1,33.
Sonda térmica / escleroterapia / resección mucosa
A fines de la década de 1980, un estudio mostró la eficacia de la terapia con sonda térmica con 8/10 pacientes que ya no requirieron transfusiones después del tratamientos34. También en estudios pequeños retrospectivos se ha visto eficacia en escleroterapia, pero hay pocos estudios que respalden esta modalidad. La resección endoscópica de la mucosa (REM) se ha utilizado como una nueva modalidad endoscópica para el tratamiento de GAVE en algunos informes de casos1,35.
Argón plasma hibrido (Hybrid-APC)
Reciente se ha desarrollado una nueva técnica “Hybrid-APC” que combina la inyección submucosa con solución salina isotónica y posterior aplicación de APC convencional, el principal fundamento fue conducir a una tasa menor de complicaciones, especialmente en la formación de estenosis por daño tisular y ulceración profunda, las primeras aplicaciones han sido estudiadas en esófago de barrett, y vasos de neoformación, un método que se ha aplicado en modelos animales36.
En un estudio con modelos ex vivo se observó que con la técnica estándar de APC la capa submucosa es dañada térmicamente en más de la mitad de las aplicaciones que utilizan 50W y en todos los casos utilizando 70 W. Además, la capa muscular se vio dañada en la técnica estándar de APC y no con Hybrid-APC. Por lo tanto, se puede suponer que Hybrid-APC puede conducir a una menor tasa de formación de estenosis durante la aplicación de argón plasma36.
En el estudio de Manner et al. Publicado en el 2014 en modelos ex -vivo (porcinos), utilizaron un gastroscopio olimpus, y un sistema generador de APC VIO 300D, este sistema fue utilizado tanto para APC convencional e Hybrid-APC. Fue un estudio aleatorizado en modelos porcinos, con el objetivo de comparar la profundidad de las lesiones del tejido esofágico entre ambos métodos. En los pacientes con APC convencional a 50 Watts tuvo una profundidad de 937 micras Vs Hybrid-APC 477 micras. Cuando se comparó a 70 watts, APC tuvo una profundidad de 1.096 micras Vs 468 micras para Hybrid-APC. El daño de la submucosa se observó 66% y 100% en el grupo APC a 50 y 70 watts, en comparación con el grupo de Hybrid-APC se observó daño a la submucosa en el 33% y 16% a 50 y 70 watts respectivamente. El daño a la capa muscular en el grupo APC fue de 16% y 50% cuando se administró a 50 y 70 watts respectivamente. Los autores concluyen que Hybrid-APC reduce la profundidad de la coagulación hasta un 50% comparado con argón plasma convencional, por lo consiguiente podría tener una menor tasas de complicaciones y estenosis de esofágica durante su aplicación clínica37.
Gong E, et al. evaluaron los efectos de APC en tejido de estómago humano: un estudio con modelos ex vivo. Su trabajo se realizó en 10 estómagos resecados posterior a una gastrectomía total y se compararon los efectos de potencia del APC (40, 60 Y 80 Watts y duración 5, 0, 15, 20 y 25 segundos). Realizaron 2 grupos; el grupo de la inyección submucosa con solución salina vs grupo control sin inyección de la submucosa. Su objetivo era evaluar la necrosis de la mucosa completa sin dañar la capa muscular propia. Se concluyó en este estudio que en el grupo de la inyección de la submucosa, la lesión del tejido por APC se limita a la submucosa incluso cuando se utilizó potencia alta (80-100 watts) comparado al grupo control sin inyección de la submucosa donde el daño a la capa muscular aumentó a medida que se usaba mayor potencia y/o mayor duración38-40.
Tratamiento quirúrgico: Antrectomía
La antrectomía a menudo se considera para pacientes cuya enfermedad consiste en malformaciones vasculares más extensas, que son refractarias a las terapias médicas o endoscópicas. La morbilidad y mortalidad del procedimiento son mayores que los beneficios, y la antrectomía laparoscópica ha intentado disminuir el riesgo involucrado con un enfoque menos invasivo41.
Tratamiento médico
Se han propuesto muchas terapias médicas como una alternativa no invasiva para el tratamiento de la hemorragia relacionada con GAVE. Las terapias, como la ciclofosfamida, el estrógeno, la progesterona, los corticosteroides, el ácido tranexámico, la octreótida, la ciproheptadina y la talidomida, han mostrado resultados positivos en informes de casos y pequeños ensayos clínicos, pero no han demostrado una eficacia suficiente para funcionar como alternativas a las modalidades endoscópicas. Recientemente se ha estudiado la eficacia de talidomida como una alternativa en pacientes que no responden a terapia endoscópica y ha mostrado resultados alentadores, sin embargo faltan más estudios para comprobar su eficacia y seguridad1,3,23,42.
Justificación
Las ectasias vasculares antrales gástricas (GAVE) son malformaciones vasculares de etiología desconocida. Es un motivo frecuente de realización de endoscopia. Actualmente el tratamiento endoscópico con Argón plasma coagulación es una de las terapias consideradas de primera línea, sin embargo se reporta una tasa de complicaciones hasta del 20%, y la refractariedad a uno o dos años es alta hasta 40-60%, siendo el siguiente escalón terapéutico la antrectomía con alta morbilidad y mortalidad. Por lo anterior, se requiere un tratamiento con mejores tasas de éxito a corto-mediano plazo.
Dentro de la exploración de nuevas alternativas de tratamiento se encuentra el argón plasma coagulación hibrido (Hybrid-APC), una técnica endoscópica que emplea inyección de la submucosa con solución salina más aplicación de APC convencional en busca de disminuir el número de complicaciones reportadas para los pacientes, disminuir el número de hospitalizaciones, la necesidad de hemotransfusiones, así como disminuir el número de sesiones endoscópicas y mejorar la eficacia a mediano-largo plazo. Por lo cual consideramos que se trata de una técnica que por el beneficio que brinda, y la potencial aplicabilidad en nuestra población afectada por esta enfermedad, podría ser una opción de tratamiento en este grupo de pacientes.
Planteamiento del problema
Las ectasias vasculares antrales gástricas (GAVE) son una causa importante de hemorragia gastrointestinal aguda, y representa la principal causa de hemorragia gastrointestinal oculta con anemia por déficit de hierro que puede ser leve hasta severa que compromete el estado hemodinámico y bienestar de los pacientes que la padecen. Además, estos pacientes requieren hospitalizaciones frecuentes, y múltiples transfusiones sanguíneas periódicas por niveles de hemoglobina bajos como consecuencia, aumentado los costos de salud y el riesgo de enfermedad de transmisión por hemoderivados. Actualmente el tratamiento endoscópico con Argón plasma coagulación (APC) es una de las terapias consideradas de primera línea, sin embargo hay una gran proporción de pacientes que no responden a dicha terapia y se requiere tratamiento adicional incluso antrectomía.
Dentro de las alternativas terapéuticas, se encuentra el tratamiento de APC con inyección submucosa de solución salina (Hybrid-APC) en pacientes en los que ya se utilizó la terapia endoscópica con APC y fueron refractarios a tratamiento, y cuyos resultados iniciales han demostrado seguridad y eficacia mayor al 80% en este grupo de pacientes. Por lo cual, la exploración de este procedimiento para ser aplicado en nuestros pacientes afectados por esta patología es factible, ya que con esto se podrá mejorar las alterativas de tratamiento en pacientes considerados refractarios a otros tratamientos endoscópicos.
El presente estudio se realiza con el objetivo de evaluar la seguridad y eficacia de Hybrid-APC en pacientes considerados refractarios a tratamiento con APC convencional, con la finalidad de obtener una terapia segura y eficaz, capaz de disminuir el riesgo de hemorragia y complicaciones que comprometan la vida del paciente con GAVE, disminuir el número de sesiones endoscópicas y complicaciones derivadas del procedimiento endoscópico, obtener mejoría en las cifras de hemoglobina y el número de transfusiones, con un menor costo para hospitales en servicios de salud, y disminuir el riesgo de complicaciones.
Pregunta de investigación
¿El tratamiento endoscópico con Hybrid-APC es eficaz y seguro en pacientes con GAVE considerados refractarios a terapia con APC?
Objetivos
Objetivo general
Evaluar la Eficacia y seguridad de Hybrid-APC en pacientes con Ectasias vasculares antrales refractarios a APC.
Objetivos específicos
Determinar la frecuencia de manifestaciones clínicas en los pacientes con GAVE refractario
Evaluar el comportamiento bioquímico en los niveles de hemoglobina antes y después del tratamiento endoscópico
Evaluar la frecuencia de eventos adversos presentados durante o después del tratamiento
Determinar si existe disminución de lesiones, en 1 o más grados endoscópicos de GAVE posterior al tratamiento endoscópico.
Evaluar el éxito clínico y endoscópico alcanzado posterior a la terapia endoscópica
Determinar si existe diferencia entre el número de transfusiones antes y después de tratamiento endoscópico
Material y métodos
Pacientes, material y métodos
Universo del estudio
Pacientes con el diagnostico de Ectasias vasculares Antrales (GAVE), que se consideraron refractarios a terapia endoscópica convencional (definido por más de 3 sesiones de argón plasma convencional (APC) o dos sesiones de ligadura previas) que hayan sido tratados con argón plasma hibrido (Hybrid-APC) y que se encuentren en seguimiento en el Departamento de Endoscopia Gastrointestinal del Hospital de Especialidades del Centro Médico Nacional s. XXI, entre enero 2018 y enero 2020.
Lugar de desarrollo
El estudio se realizó en el servicio de endoscopia gastrointestinal del Hospital de Especialidades UMAE CMN s XXI, en los pacientes con GAVE refractarios a terapia endoscópica convencional (APC) y fueron tratados con Hybrid-APC.
Criterios de inclusión
- Hombres y mujeres mayores de 18 años.
- Pacientes con diagnóstico de GAVE considerados refractarios a tratamiento endoscópico con APC >3 sesiones o >2 sesiones de ligadura endoscópico.
- Pacientes que acepten el procedimiento endoscópico con hybrid-APC.
- Pacientes que acepten el estudio y firmen consentimiento informado
Criterios de exclusión
- Pacientes con otra alteración endoscópica diferente a GAVE
- Pacientes que cuenten con diagnóstico de GAVE y no cumplan criterios de refractariedad a terapia endoscópica con APC
- Pacientes asintomáticos sin evidencia de síndrome anémico o requerimiento de terapia transfusional previo al tratamiento con Hybrid-APC
- Aquellos pacientes que no acepten el procedimiento y no firmen el consentimiento informado
- Embarazadas
Variables y escalas de medición
Se documentaron las características clínicas de los pacientes, que incluyen: Edad, género, enfermedad concomitante, síntoma: melena, hematemesis, síndrome anémico, dolor abdominal, grado endoscópico de GAVE: Grado 1, 2, o 3. Localización de la lesión: Antro, cuerpo, fondo, todo el estómago, patrón endoscópico de GAVE: puntiforme, granular, lineal. Estancia intrahospitalaria, transfusiones, Eventos adversos: dolor abdominal, diarrea, fiebre, ulcera gástrica de alto o bajo riesgo, estenosis de antro.
Definición de variables
Variable independiente: edad, género, manifestación clínica de GAVE, patrón endoscópico de GAVE; grado de afectación endoscópica de GAVE. Eventos adversos
Métodos de recolección de datos:
Se registraron los parámetros clínicos, bioquímicos, y endoscópicos de todos los pacientes con diagnóstico de GAVE tratados con >3 sesiones de APC considerados refractarios y que fueron tratados con Hybrid-APC en el servicio de endoscópica del Hospital de Especialidades “Dr. Bernardo Sepúlveda Gutiérrez” del Centro Médico Nacional siglo XXI en una base de datos física y electrónica y además se contó con un expediente médico por cada paciente, los cuales solo fueron manejados por el personal médico incluido en el protocolo, todo esto además de su expediente normal del hospital. Aquí se recolectaron todos los datos previos al procedimiento, durante el procedimiento endoscópico y posterior al procedimiento (Anexo 1).
Descripción general del estudio
I. Equipo utilizado
- Se utilizó endoscopio Fujinon modelo EG-590W con equipo de 9.3 mm de diámetro y canal de trabajo de 2.8 mm, con cap blando y recto, asociado unidad electroquirúrgica ERBE VIO 300D asociado a equipo ERBEJET para irritación endoscópica. El equipo que se utilizó para el estudio fue otorgado por los servicios médicos integrales (VITALMEX) contratados por el Instituto Mexicano del Seguro Social de nuestra unidad. No se contó con patrocinio por farmacéuticas o fabricante relacionado a los equipos aquí utilizados.
II. Técnica de aplicación de argón plasma híbrido
Se programó a los pacientes que cumplieron con criterios de inclusión, posterior a la autorización y firma del consentimiento informado. se realizó procedimiento endoscópico superior, bajo sedación, realizando endoscopia alta con el equipo endoscópico. Se revisó de forma inicial la presencia de ectasias vasculares y/o la presencia de hemorragia activa en capa y en base a los hallazgos clínicos, bioquímicos y endoscópicos evaluados previamente al procedimiento. Se procedió a la aplicación de argón plasma a través del sistema electroquirúrgico combinado con un sistema de inyección de agua (ERBE-Jet) y una sonda flexible “Hybrid-APC”, en modo pulsado de APC con efecto 2, de 80-100 watts con un flujo constante de 1.5 lt/min; para inyección de submucosa se utilizó solución salina al 0.9% de 250cc + 10 ml de solución de Azul de metileno al 1% para lograr el levantamiento submucoso (almohadilla) entre 4-6 mm. La sonda de “Hybrid-APC” se aplicó a 2 mm de la pared gástrica. Durante el procedimiento se evaluó el porcentaje de lesiones gástricas por GAVE, clasificando como Grado I (un porcentaje de afección gástrica por GAVE <30%), grado II (de 30-70%), y grado III (>70%).
III. Procedimiento
1. PREPROCEDIMIENTO:
Se realizó la evaluación previa al procedimiento donde se incluyó una historia clínica completa, los datos de acentuaron en una base de datos electrónica y física. Se recabaron los datos clínicos y bioquímicos de cada paciente, así como los resultados de los estudios que se incluyeron el cuestionario de síntomas, la primera endoscopia previa al procedimiento. Para el procedimiento los pacientes acudieron al servicio de endoscopia en forma ambulatoria, con ayuno de 8 horas, se revisaron estudios preoperatorios y riesgo quirúrgico para valorar la seguridad durante el procedimiento.
2. POSTPROCEDIMIENTO
Posteriormente al procedimiento, el paciente se hospitalizó por 24 horas en esta unidad, se realizó una revisión clínica, así como laboratorios generales para detección temprana complicaciones. Se manejo con ayuno por 4-6 horas, posteriormente dieta líquida/blanda por 24 horas y reposo el día del procedimiento, se dio manejo con analgésicos y antieméticos en caso necesario. La terapia adyuvante posterior al procedimiento incluyó: Inhibidor de bomba de protones doble dosis en base al proceso de necrosis, ulceración y cicatrización documentados posterior a la aplicación de argón plasma, para reducir el tamaño de la úlcera y favorecer al proceso de cicatrización, como se ha reportado en pacientes post aplicación de argón plasma en GAVE. 24 horas después al descartar complicaciones, los pacientes se dieron de alta a domicilio, con vigilancia estrecha de posibles complicaciones, con dieta blanda por 24 horas posteriores al procedimiento.
La primera evaluación posterior se realizó 1 mes y se aplicó cuestionario de síntomas, BHC, así como realización de endoscopia superior de control para valorar el porcentaje (%) de aumento de las cifras de hemoglobina, así como el porcentaje de mejoría endoscópica de las lesiones vasculares clasificándolo como grado I si posterior al procedimiento endoscópico presentaba lesiones <30%, grado II (lesiones entre 30 y 70%), y grado III (>70%). La segunda revisión se realizó a los 2 meses evaluando los parámetros del primer mes postratamiento. La tercera revisión a los 3 meses y la cuarta revisión a los 6 meses. La sexta revisión a 1 año posterior al inicio del primer tratamiento.
Todos los datos obtenidos se documentaron en el expediente físico, y en expediente electrónico previamente comentados, así como en el expediente del hospital.
Análisis estadístico
Se consideró un universo de pacientes con GAVE refractarios a tratamiento endoscópico previo (con más de 3 sesiones) que fueron tratados con terapia endoscópica con Hybrid-APC y se les realizó seguimiento de acuerdo a síntomas clínicos, parámetros bioquímicos, y estudios endoscópicos, en el Departamento de Endoscopia Gastrointestinal del Centro Médico Nacional Siglo XXI.
Las variables cuantitativas se representan con medidas de tendencia central según su distribución; con Media y desviación estándar para distribución normal, mediana y rangos intercuartílicos para las variables de libre distribución y las variables nominales y cualitativas con proporciones
Se utilizó análisis estadístico bivariado: T de Student para variables cuantitativas de distribución normal relacionadas (demostrar diferencia entre dos grupos), las variables cualitativas dicotómicas se analizarán con Chi2 para demostrar diferencia entre 2 grupos.
Se utilizó el programa de análisis estadístico Excel 2016, y el programa de análisis estadístico SPSS v. 22.
Consideraciones éticas
El protocolo fue evaluado por el comité local de investigación del hospital y está sujeto a las normas específicas para este tipo de estudios: reglamento de la Ley General de Salud en materia de investigación para la Salud y con la Declaración de Helsinki, así como a las normas e instructivos institucionales en materia de investigación científica. Todos los pacientes y sus representantes legalmente autorizados proporcionaron el consentimiento informado por escrito con las firmas correspondientes previa explicación amplia en que consiste el procedimiento, así como también de los riesgos y beneficios.
Se contó con válvula de seguridad ante cualquier eventualidad o complicaciones durante el procedimiento: los pacientes fueron tratados en nuestro hospital, para esto existió un contacto directo con los servicios de admisión continua, gastroenterología, medicina interna, cirugía general, terapia intensiva o cualquier otro servicio necesario en caso de presentarse algún tipo de complicación. Cabe mencionar, que este procedimiento ha demostrado ser seguro y eficaz. Sin embargo, en caso de presentarse algún evento adverso posterior, los pacientes tuvieron contacto con los investigadores y pudieron acudir a cualquier hora al servicio de admisión continua del hospital donde se evaluaron por el servicio de gastroenterología las 24 h enterado de los participantes en este estudio y se brindó la atención necesaria.
Se cuidó la confidencialidad de los participantes para el manejo de los datos en informes, tesis y/o publicaciones que deriven de este proyecto de investigación. Para la protección de identidad, cada paciente se identificó por su número de afiliación y una numeración consecutiva según la fecha de ingreso al estudio. El manejo de los datos fue de uso exclusivo por los investigadores participantes.
Si el paciente no aceptó participar en el protocolo se otorgó la misma atención que normalmente se realiza en estos casos por parte del instituto.
Recursos, financiamiento y factibilidad
Recursos humanos
Médicos
- Dr. Oscar Víctor Hernández Mondragón: Jefe de Servicio del departamento de Endoscopia Gastrointestinal, Médico gastroenterólogo y especialista en endoscopía especializada, así como en modelos biológicos, adscrito al servicio de endoscopia del Hospital de Especialidades UMAE CMN Siglo XXI.
- Dr. Omar Michel Solórzano Pineda, Médico especialista en Cirugía general, cirugía laparoscópica avanzada y Endoscopia Gastrointestinal adscrito al servicio de endoscopía del Servicio de Endoscopía del Hospital de Especialidades UMAE CMN Siglo XXI
- Dra. María del Rosario Domínguez García: Médico especialista en Gastroenterología cursando adiestramiento endoscópico gastrointestinal adscrito al servicio de endoscopia del Hospital de Especialidades UMAE CMN Siglo XXI.
Recursos físicos
Instalaciones del servicio de endoscopia del Hospital de Especialidades “Dr. Bernardo Sepúlveda Gutiérrez”, Centro Médico Nacional Siglo XXI, unidad de Endoscopia.
Pacientes
Todos los pacientes incluidos son derechohabientes del IMSS y que acudieron de cualquiera de los 3 niveles de atención, con diagnóstico de GAVE refractario a terapia previa con Argon plasma convencional, y que se encontraban en evaluación y tratamiento por parte de los servicios de cirugía general, gastroenterología o medicina interna. Se realizó una apertura de expediente en nuestra unidad para su atención integral.
Recursos Materiales
Papelería diversa
Sistema de trabajo y equipos del servicio de endoscopía. El equipo de endoscopia es un equipo otorgado por parte de los servicios integrales con los que cuenta el hospital por lo cual no hubo necesidad de solicitar otro tipo de equipamiento especial.
Se utilizó una computadora que forma parte del servicio de endoscopia y donde se integraron las bases de datos de los pacientes de este protocolo.
Máquina de anestesia y monitoreo continuo durante el procedimiento: electrocardiograma, tensión arterial no invasiva, oximetría de pulso, por el servicio de Anestesiología.
Factibilidad
El estudio es factible en nuestra unidad debido a que somos un centro de referencia, contamos con todos los recursos necesarios para llevar acabo cualquier tipo de procedimiento con los cuidados necesarios y el control adecuado para cualquier procedimiento terapéutico.
Resultados
Se reclutaron un total de 12 pacientes con diagnóstico de GAVE que previamente fueron tratados con más de 3 sesiones de APC y considerados refractarios, en el departamento de Endoscopia Gastrointestinal del Hospital de Especialidades del Centro Médico Nacional siglo XXI de enero 2018 a enero 2020, que cumplieron los criterios de inclusión y que fueron tratados con Hybrid-APC. Las características basales de la población se encuentran en la tabla 1 (Anexos).
El índice de masa corporal fue de 26.4 (±41), las comorbilidades fueron cirrosis hepática en 3 pacientes (25%), Diabetes mellitus en 4 pacientes (33.3%), hipertensión arterial en 10 pacientes (83.3%), EPOC e hipertensión pulmonar en 4 pacientes (33.3%),y enfermedad renal crónica en 6 pacientes (±1.7). La media del valor de hemoglobina sérica al diagnóstico fue de 6.4 (±1.7), el patrón endoscópico de GAVE más frecuente fue lineal o longitudinal con 8 pacientes (66.7%), seguido de patrón mixto puntiforme y lineal en 2 pacientes (16.7%), el patrón puntiforme se observó en 1 paciente ( 8.3%), y el patrón nodular en 1 paciente (8.3%), la distribución de ectasia vascular fue más frecuente en antro en 8 pacientes (66.7%), seguida de fondo y antro en 2 pacientes (16.7) y todo el estómago en 2 pacientes (16.7%), la manifestación clínica se presentó con melena en 3 pacientes (25%), síndrome anémico en 1 paciente (8.3%), y melena más síndrome anémico en 8 pacientes (66.7%), siendo esta ultima la presentación clínica más frecuente. El porcentaje de afectación gástrica previo a la sesión de Hybrid-APC fue grado III (con afectación más del 70%) en 5 pacientes (41.7%) y grado II (afectación del 30-70%) en 7 pacientes (58.3%), y ningún paciente presento Grado I (afectación <30%) previo al procedimiento con hybrid-APC. El número de transfusiones previas fue de 7 paquetes globulares (±28), las sesiones previas de APC fueron de 4.5 (± 10), el promedio de sesiones previas de Hybrid-APC fue de 1 (±1), y el tiempo de seguimiento en meses fue de 12 (±18).
Al comparar la hemoglobina inicial previo a la sesión del Hybrid APC con media de 6.4 gr/dl, y la disminución del valor de hemoglobina 4 semanas posterior al procedimiento con media de 9.2 gr/dl, se obtuvo una diferencia estadísticamente significativa de -2.8 gr/dl (p=0.000). Al comparar el valor de hemoglobina de la semana 8 con media de 9.8 gr/dl, y el valor a la semana 12 postratamiento (media de 10.4 gr/dl), se obtuvo una diferencia estadísticamente significativa (p=0.45), y al comparar el valor de hemoglobina de la semana 24 y 48 no se encontró diferencia significativa. Los resultados se muestran en la tabla 2 de anexos.
Al comparar el porcentaje de afección de lesiones gástricas de acuerdo a los grados establecidos (grado I: <30%, grado II: 30-70%, y grado III > 70%) antes y después de la sesión de Hybrid-APC, un 33% de pacientes tuvieron disminución de 2 puntos en la endoscopia, y un 50% tuvieron disminución 1 punto. Un total de 9 pacientes (75%) finalizaron con grado I (afección endoscópica <30%), y 3 pacientes (25%) con grado II, ningún paciente presentó lesiones de grado III (>70%) posterior a la sesión de Hybrid-APC. Los resultados se muestran en la tabla 3 y 4 de anexos.
Al comparar el requerimiento de transfusiones antes y después del tratamiento endoscópico de Hybrid-APC, se obtuvo diferencia significativa con p=0.001 (IC 5.041-16.125), Los resultados se muestran en la tabla 5 de anexos.
Al evaluar el éxito técnico definido por la disminución de uno o mas grados endoscópicos, observamos que éxito técnico en 9 pacientes (75), y el éxito clínico (definido por ausencia de datos clínicos síndrome anémico en 3 meses postratamiento, aumento o Mantenimiento de los niveles de HB en el tiempo de seguimiento sin la necesidad de transfusiones o hierro) se presentó en 9 pacientes (75%), obteniendo criterios de respuesta Clínica y endoscópica en el 75% de pacientes. Los resultados se muestran en la tabla 6 de anexos.
Se reportó como efecto adversó más frecuente dolor abdominal en 4 pacientes (33.3%), úlcera de bajo riesgo Forrest III en 2 pacientes (16.7%), estenosis simple sin requerimiento de manejo endoscópico en 1 paciente (8.3), y un paciente (8.3%) durante el seguimiento posterior a la sesión de hybrid-APC presentó hemorragia gastrointestinal documentándose ulcera Forrest IIa, realizándose tratamiento endoscópico con terapia térmica y adrenalina, sin complicaciones posteriores. No se observaron eventos adversos mayores durante el tiempo de seguimiento. Los resultados se muestran en la tabla 7 de anexos.
Discusión
Nuestro estudio es uno de los pocos estudios y de los primeros en valorar la seguridad y eficacia de Hybrid-APC en pacientes considerados refractarios a la terapia con APC. Existen múltiples estudios que evalúan la terapia con APC en pacientes con GAVE, pero existen pocos estudios que evalúan terapia con Hybrid-APC en pacientes con GAVE, y no existe ningún estudio que evalúe Hybrid-APC en pacientes refractarios a tratamiento endoscópico con terapias previas de APC. Este estudio se realizó con el objetivo de evaluar la seguridad y eficacia de Hybrid-APC en pacientes considerados refractarios a la terapia con APC, y demostramos que pacientes aun considerándolos refractarios a una terapia convencional endoscópica, pueden beneficiarse de la terapia de Hybrid-APC con menor número de sesiones (en promedio 1-2 sesiones), logrando criterios de respuesta con éxito técnico y éxito clínico mayor al 75%, presentando seguridad para el paciente con menor número de eventos adversos (8.3% de estenosis en Hybrid-APC vs 12-20% en APC convencional) y menores sesiones endoscópicas (1-2 sesiones en Hybrid-APC comparadas con promedio de 4-5 de APC). Nuestro estudio muestra buenos resultados en pacientes refractarios a tratamiento endoscópico, ya que el éxito técnico y éxito clínico se presentó en 75% de pacientes refractarios. La mayoría de estudios reflejan en otros tratamientos una eficacia de 90-100% para APC, y del 75-86% en ligadura con banda endoscópica y radiofrecuencia, sin embargo, estos resultados se presentaron en pacientes vírgenes de tratamiento, y no en pacientes refractarios. Con los datos anteriores se logrará exponer a los pacientes con GAVE a un número menor de procedimientos endoscópicos, y menor número de complicaciones derivadas del procedimiento endoscópico y de sedación. Además el realizar Hybrid-APC mejoraran los niveles de hemoglobina en el paciente hasta 4 gramos desde el diagnostico hasta 12 semanas postratamiento, lo cual disminuirá el riesgo de descompensación hemodinámica en estos, y la necesidad de transfusiones (hasta 10 concentrados eritrocitarios en promedio). Por los beneficios y las diferencias a favor de Hybrid-APC este podría compararse como primera opción endoscópica vs APC solo, sin embargo se necesitan estudios prospectivos con mayor número de muestra para corroborar estos datos. En nuestro estudio un paciente presentó hemorragia gastrointestinal con ulcera con vaso visible (Forrest IIA) posterior a la terapia con Hybrid-APC requiriendo doble terapia endoscópica con adrenalina y 2 paquetes globulares, sin presentar complicaciones posteriores. Un paciente de este estudio falleció posterior a cumplir el tiempo de seguimiento, por causa diferente a hemorragia o GAVE (complicaciones por fractura de cadera).
Nuestro estudio tiene varias limitaciones, el tamaño de muestra muy pequeño es la limitación más importante, además debido a la baja prevalencia de la enfermedad se realizó muestreo probabilístico por conveniencia. Sin embargo, el estudio se desarrolla en un centro de referencia nacional con experiencia en endoscopia terapéutica, lo cual refleja la prevalencia de la enfermedad en el país. Este trabajo contribuye a corroborar y reforzar el conocimiento que se tiene en la literatura mundial.











 nueva página del texto (beta)
nueva página del texto (beta)