Introducción
En los últimos años se ha intensificado la búsqueda de métodos para reducir el sangrado y los requerimientos de transfusiones sanguíneas en las cirugías de Ortopedia y Traumatología, especialmente durante artroplastías de cadera y rodilla, cirugía de columna y de trauma.1 Estos procedimientos quirúrgicos se asocian con sangrado importante, entre otras complicaciones. Cabe recalcar que pacientes con anemia aguda por hemorragia intra- o postoperatoria pueden requerir de transfusiones sanguíneas, lo cual es un predictor independiente de morbilidad.1 Asimismo, la transfusión de sangre alogénica no sólo es costosa, sino que conlleva el riesgo de hemólisis, reacciones anafilácticas, transmisión de infecciones (virus de hepatitis, virus de la inmunodeficiencia humana, citomegalovirus, entre otros), así como un aumento en la estancia hospitalaria y utilización de recursos.1 Por esto mismo, recientemente se han investigado agentes farmacológicos que minimicen el sangrado mediante la inhibición de la degradación del coágulo sanguíneo. Los tres principales agentes antifibrinolíticos que han sido investigados son el ácido aminocaproico, aprotinina y el ácido tranexámico (ATX).1,2,3
Características y mecanismo de acción del ATX
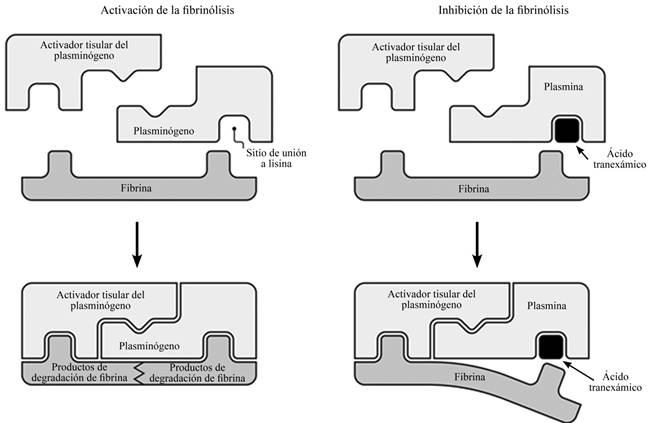
El ATX (ácido trans-4-(aminometil)-ciclohexanocarboxílico) es un agente antifibrinolítico desarrollado en Japón en 1962 por Utako Okamoto con el objetivo de disminuir las muertes postparto causadas por hemorragias.1 El ATX es un análogo sintético de la lisina que inhibe competitiva y reversiblemente la conversión del plasminógeno en plasmina1,4 (Figura 1). Además, en concentraciones altas, el ATX bloquea de manera no competitiva la plasmina, inhibiendo así la disolución y degradación de coágulos de fibrina.5 Por otro lado, se ha demostrado que el ATX tiene propiedades antiinflamatorias, lo que constituye un mecanismo secundario en la reducción de la mortalidad secundaria a hemorragia.1
La farmacocinética del ATX indica que su pico de concentración es a los 60 minutos postadministración por vía intravenosa, con una vida media de aproximadamente dos horas y 90% de excreción a las 24 horas, por vía renal, mientras que sus efectos antifibrinolíticos tienen una duración de 8 a 17 horas posteriores a la administración.1,5,6 El ATX tiene la capacidad de atravesar la barrera placentaria, es excretada por la leche materna y aparece rápidamente en los fluidos sinoviales. Sin embargo, la farmacocinética en algunos tipos de pacientes (por ejemplo, aquéllos que fueron sometidos a cirugía o politraumatizados) puede diferir. El ATX es de seis a 10 veces más potente que el ácido aminocaproico.6 La manera clínica de medir el efecto antifibrinolítico del ATX es mediante la reducción del dímero D en sangre.2
La primera indicación del ATX fue autorizada por la Food and Drug Administration (FDA) en 1986 para la administración intravenosa en el tratamiento del sangrado durante procedimientos dentales en pacientes con hemofilia.2,5 Posteriormente en 2009 la FDA aprobó la administración por vía oral del ATX para el control de la metrorragia.6 El uso del ATX en trauma ha ganado considerable atención en los últimos años debido a que la hemorragia es la principal causa de muerte prevenible en esta población, resultando en que la Organización Mundial de la Salud agregara al ATX a su lista de medicamentos esenciales en 2011 después de que se comprobó que éste reduce significativamente la mortalidad secundaria a hemorragia.1
El ATX se encuentra contraindicado en pacientes con hipersensibilidad al mismo, aquéllos con trombosis u oclusiones vasculares agudas, historia de eventos tromboembólicas, hematuria macroscópica, insuficiencia renal y hemorragia subaracnoidea6 (Tabla 1). Se han reportado convulsiones en casos que han recibido altas dosis del ATX, lo cual se cree que se debe a alteraciones en el flujo sanguíneo cerebral y a variaciones en los neurotransmisores.6
Tabla 1: Contraindicaciones del uso del ácido tranexámico.6
| • Enfermedad arterial coronaria |
| • Insuficiencia renal (creatinina sérica > 200 mmol/L, depuración de creatinina < 50 mL/min, uso de diálisis) |
| • Historia de reacciones alérgicas al uso del ácido tranexámico |
| • Coagulación intravascular diseminada |
| • Evento tromboembólico activo |
| • Uso de anticoagulantes |
| • Historia de un evento tromboembólico < 1 año previo al procedimiento quirúrgico (infarto agudo al miocardio, evento vascular cerebral, trombosis venosa profunda, tromboembolia pulmonar) |
Para aplicaciones ortopédicas, el ATX se ha utilizado efectivamente por vía intravenosa, intraarticular, tópica y oral. La dosis intravenosa más utilizada es la administración de 10 mg/kg en bolo seguido de una infusión de 1 mg/kg/h.2,7
Una de las limitantes que ha tenido el ATX para su aplicación clínica es el de su seguridad. Debido a que el ATX es un antifibrinolítico, podría existir un riesgo teórico de formación de trombosis vasculares; sin embargo, múltiples estudios han demostrado que no existe un mayor riesgo de desarrollar trombos o émbolos después de la administración de ATX. Asimismo, no se ha demostrado que el ATX aumente el riesgo de insuficiencia renal, cardíaca, eventos cerebrovasculares ni la mortalidad intrahospitalaria.1 Varios meta-análisis han reiterado la seguridad del uso de ATX, demostrando que no existe un aumento en las tasas de trombosis venosa profunda, tromboembolia pulmonar, tiempo de tromboplastina parcial activado o tiempo de protrombina.1 Sí se ha demostrado un mayor riesgo de presentar náusea, diarrea y reacciones ortostáticas.2 Sólo existen reportes de casos de trombosis cerebrovascular, trombosis arterial y oclusión de injerto coronario.2
Dosis, vía y tiempo de administración
La dosis óptima y el tiempo de administración no se han estandarizado. Sin embargo, la dosis más frecuentemente utilizada por vía intravenosa es de 10-15 mg/kg previo a la incisión o inflado del torniquete para la artroplastía total de rodilla. Se repite otra dosis previa al cierre de la herida o al desinflado del torniquete. Se ha reportado que la dosis intravenosa de 2 gramos tiene la mejor eficacia y perfil de seguridad para artroplastía total de rodilla.8 También en artroplastía de rodilla se han utilizado dosis intraarticulares de 250 mg a 2 gramos y por vía tópica de 1-3 gramos mezclados con solución salina. Para los casos de trauma, la dosis típica por vía intravenosa es de 1 gramo administrado durante 10 minutos seguido de una infusión de 1 gramo en las próximas ocho horas.1 Otra alternativa que se ha estudiado ha sido la combinación de vías de administración. Liu y colaboradores demostraron en su estudio que la combinación de ATX por vía intravenosa y tópica reduce la pérdida sanguínea total en comparación con la administración únicamente por vía intravenosa en pacientes sometidos a artroplastía de cadera.9,10
Un metaanálisis realizado en pacientes sometidos a artroplastía de rodilla comparó la administración de ATX previo a la incisión contra su administración posterior a la misma, observándose que una dosis previa a la incisión disminuye el riesgo de sangrado. Sin embargo, no se observó una diferencia significativa sobre la pérdida sanguínea. Existen inconsistencias sobre el tiempo de administración del ATX; sin embargo, se recomienda la administración previa a la incisión, ya que no se han observado beneficios de la administración posterior a la misma.11,12
Todas las vías de administración han mostrado utilidad para la disminución del sangrado, por lo que en general es la preferencia del cirujano la que decide la vía de administración.11 La Tabla 2 muestra los diferentes protocolos de administración del ATX en las distintas aplicaciones dentro de la Ortopedia y Traumatología.
Tabla 2: Protocolos de administración del ATX en Ortopedia y Traumatología.
| Procedimiento quirúrgico | Dosis vía oral | Dosis vía intravenosa | Dosis vía tópica |
|---|---|---|---|
| Artroplastía de cadera | 1.95 gramos 2 horas previo a la cirugía(17) | 1 gramo previo a la incisión(17) | 10 mililitros de ATX al 5%, 1/3 administrados intramuscular e intracapsular y 2/3 administrados intraarticular posterior al cierre de la fascia(8) |
| 1 gramo 2 horas previas a la cirugía, seguido de 1 dosis a las 6 horas y otra a las 12 horas postoperatorias(8) | Infusión de 15 mg/kg en 100 ml de solución salina 0.9% administrados en el preoperatorio inmediato(8) | ||
| Artroplastía de Rodilla | 1 gramo 1 hora previo a la cirugía, seguido de 1 gramo cada 6 horas por las siguientes 18 horas (3 dosis postoperatorias)(8) | 1 gramo previo a la incisión quirúrgica + 1 gramo durante el cierre(20,27) | 3 gramos diluidos en 100 mililitros de solución salina al 0.9%(20) |
| 1 gramo 2 horas previas a la cirugía, seguido de 1 gramo a las 6 y 12 horas postoperatorias(8) | 10-15 mg/kg en 100 mililitros de solución salina al 0.9% durante la inducción anestésica + 1 dosis igual 3 horas posterior a la primera dosis(26) | 2 gramos diluidos en 75 mililitros de solución salina 0.9% aplicados durante 5 minutos durante inflado del torniquete(8) | |
| 1 gramo diluido en 50 mililitros de solución salina al 0.9% previo al cierre de la herida(8) | |||
| Cirugía de Columna | 1.95 gramos 2 horas previas a la cirugía(8) | 10 mg/kg preoperatorio + una infusión de 1 mg/kg/h durante el tiempo quirúrgico(33) | 3 gramos diluidos en 100 ml de solución salina 0.9%(8) |
| 1 gramo previo a la incisión y 1 gramo previo al cierre de la herida(8) | 1 gramo diluido en 100 ml de solución salina 0.9% colocado en la herida quirúrgica durante 5 minutos(8) | ||
| 2 gramos (adultos) o 30 mg/kg (pediátrico) en bolo, seguido de una infusión intraoperatoria de 100 mg/hora (adultos) o 1 mg/kg/hora (pediátrico)(8) | |||
| Trauma | No aplica | En las primeras 8 horas del trauma: 1 bolo de 1 gramo durante 10 minutos + infusión de 1 gramo para 8 horas(1,5,6) | No aplica |
Artroplastía de cadera: es un procedimiento que se asocia a hemorragia importante; la pérdida sanguínea promedio durante una artroplastía primaria varía de 700 a 2,000 ml, con una tasa de transfusión de 16 a 37%.9 Varios estudios han demostrado de manera consistente que la administración de ATX reduce los requerimientos de transfusión sanguínea en pacientes sometidos a una artroplastía total de cadera sin importar los niveles preoperatorios de hemoglobina.1,4,11,13 Estos hallazgos son independientes de la dosis, momento de administración, tipo de anestesia o tipo de prótesis (cementada o no cementada), asimismo, también se ha evidenciado una reducción significativa en el sangrado trans- y postoperatorio, drenaje postoperatorio y costos.11,12,14,15
El ATX también ha demostrado utilidad para disminuir el sangrado durante las artroplastías de revisión.4 Se estima que la pérdida sanguínea intraoperatoria durante una revisión de artroplastía total de cadera puede llegar hasta los 2,000 ml y que aproximadamente 45% de los pacientes requerirán ser transfundidos.2,16 En un estudio realizado por Peck y colaboradores se administró una dosis preoperatoria de 20 mg/kg de ATX. Estos autores subdividen a los casos sometidos a revisión de artroplastía total de cadera en los siguientes grupos: revisión mayor (revisión de todos los componentes protésicos), revisión aislada del componente femoral, revisión aislada del componente acetabular y revisión aislada de la cabeza femoral y liner. El ATX demostró disminuir la hemorragia intraoperatoria, disminuir la necesidad de transfusión perioperatoria en todos los pacientes sin importar el componente protésico revisado y mejorar los valores de hemoglobina postoperatoria. De la misma manera, en el estudio no se observó un aumento en las complicaciones tromboembólicas.16
Otro estudio señala que la administración tópica de ATX ha demostrado disminuir el sangrado, requerimientos de transfusión sanguínea, drenaje postoperatorio y disminución en las cifras de hemoglobina, sin aumentar el riesgo de trombosis venosa profunda y tromboembolia pulmonar.1
La administración de ATX por vía oral para la disminución de sangrado en pacientes sometidos a artroplastía total de cadera ha sido estudiada por Kayupov y colaboradores. En este estudio, los autores aleatorizaron la administración de 1.95 gramos dos horas previas a la cirugía de ATX por vía oral o 1 gramo por vía intravenosa en bolo previo a la incisión en pacientes sometidos a artroplastía total de cadera, observaron una disminución similar en los niveles de hemoglobina y sangrado así como la necesidad de transfusión sanguínea en ambos grupos. Sin embargo, la administración por vía oral de ATX tuvo un menor costo, por lo que recomiendan esta vía para la administración del ATX en casos sometidos a artroplastía total de cadera.17
Existen estudios que se han interesado en evaluar el resultado de la aplicación de ATX durante la artroplastía de cadera indicada para fracturas. Farrow y su grupo realizaron un meta-análisis en el que observaron que el ATX reduce en 12% la necesidad de transfusión sanguínea postoperatoria. Los autores observaron que el ATX no se asoció con un mayor riesgo de eventos tromboembólicos postoperatorios.18 Jennings estudió la utilidad del ATX en sujetos con fractura de cadera que serán sometidos a hemiartroplastía y demostró que es una herramienta segura, efectiva y costo-efectiva para la reducción del sangrado y de la necesidad de transfusión, sin aumentar la mortalidad. El ATX es especialmente útil en esta población, ya que por lo general se trata de ancianos, los cuales son más susceptibles a padecer anemia sintomática y transfusiones postoperatorias. La utilidad del ATX también ha sido comprobada en pacientes con fractura de fémur.1
Artroplastía de rodilla: la pérdida sanguínea promedio en una artroplastía total de rodilla va desde 300 ml a 1 litro, lo que resulta en anemia y en una alta probabilidad de transfusión sanguínea.19,20 Lo anterior queda en evidencia al apreciar que las tasas de transfusión posterior a una artroplastía de rodilla, ya sea primaria o de revisión, varían desde 63 a 95% con una tasa de transfusión de 93% en caso de artroplastía bilateral de rodilla.4,19,21
El uso del ATX en pacientes sometidos a artroplastía de rodilla se recomienda particularmente en aquéllos con un riesgo elevado de transfusión, con niveles de hemoglobina menores a 13 g/dl o en casos donde se espere sangrado importante, como en cirugías bilaterales.19
Se ha observado que el uso del ATX durante la artroplastía de rodilla reduce de manera importante el sangrado, los requerimientos de transfusión y el uso de drenaje postoperatorio.11 Como se mencionó previamente, se ha demostrado que la administración tópica es igual de efectiva que la administración intravenosa con una menor absorción sistémica.1,20 Alshryda y colaboradores observaron una disminución en la pérdida sanguínea de 591 ml después de la administración de ATX en pacientes sometidos a artroplastía total de rodilla primaria, así como una reducción significativa de pacientes que requirieron transfusión sanguínea.22,23
Huang y su equipo en una interesante investigación compararon el uso del ATX contra el torniquete en pacientes sometidos a artroplastía total de rodilla, los autores compararon tres grupos de pacientes: grupo A, al cual se le administraron múltiples dosis de ATX intravenoso y tópico además del uso del torniquete transoperatorio; grupo B, el cual fue igual que el grupo A pero sin el torniquete; y el grupo C, en el cual se utilizó únicamente torniquete sin la administración de ATX. La cantidad de pérdida sanguínea transoperatoria fue similar en los tres grupos. No se observó una diferencia estadísticamente significativa entre los grupos A y B con respecto a pérdida sanguínea total, volumen de drenaje, pérdida sanguínea intraoperatoria, tasa de transfusión o cambio máximo en la hemoglobina. Sin embargo, se observaron más beneficios en el grupo B en comparación con los grupos A y C: menor edema postoperatorio, menores niveles de biomarcadores inflamatorios (proteína C reactiva e interleucina 6), menor escala visual análoga y puntajes de dolor, mayor rango de movilidad con el alta hospitalaria y mejor satisfacción del paciente. No hubo diferencias estadísticamente significativas entre los tres grupos con respecto a trombosis venosa profunda o tromboembolia pulmonar. En los grupos en que se utilizó el torniquete se observó mayor secreción de la herida. De acuerdo a esto se puede concluir que el uso del ATX es superior al torniquete durante una artroplastía total de rodilla debido a que resultó en mejor función temprana de la rodilla y en mejor satisfacción del caso.24 Se recomienda no utilizar torniquete debido al efecto paradójico que sucede al retirarlo secundario a la activación de la fibrinólisis, lo que provocaría una coagulopatía en la extremidad.25,26
Dobarganes-Barlow y colaboradores publicaron que la administración de ATX a una dosis de 1 gramo intravenoso al terminar el bloqueo epidural y 1 gramo intravenoso diez minutos previos al retirar el torniquete reducen el sangrado pre-, trans- y postquirúrgico global, así como el descenso en la hemoglobina y la necesidad de transfusión postoperatoria, aunque estos resultados no fueron estadísticamente significativos.27,28 Se ha demostrado también el beneficio del ATX para disminuir el sangrado y la necesidad de transfusión en revisiones de artroplastía total de rodilla.4
Cirugía de columna
En algunos tipos de cirugía de columna pediátrica y de adultos puede existir un sangrado significativo atribuido a la duración larga del procedimiento, tamaño de la herida quirúrgica y sangrado proveniente del hueso esponjoso. Varios estudios han demostrado la utilidad del ATX para la reducción del sangrado en cirugía de columna, sin aumentar el riesgo de complicaciones. Un estudio encontró una reducción de 33% en la tasa de transfusiones gracias a la administración del ATX.1,29
El ATX es especialmente útil en la población pediátrica sometida a cirugía para corrección de escoliosis, donde se ha demostrado una reducción en el sangrado y requerimientos de transfusiones. En cirugía de columna en adultos, se ha demostrado recientemente que el ATX reduce la pérdida sanguínea en 49% y las transfusiones en 80%, en comparación con los controles.2
Varios estudios han fortalecido estas aseveraciones. Por un lado Yang y colaboradores demostraron una reducción en la pérdida sanguínea postoperatoria de 389 ml después de la administración de ATX en cirugía pediátrica para corrección de escoliosis.30 Otro estudio aleatorizado de pacientes con escoliosis idiopática del adolescente encontró que el ATX redujo significativamente la pérdida sanguínea en comparación con la solución salina; sin embargo, no observaron una reducción significativa de la tasa de transfusiones.6
En la laminoplastía cervical se ha observado una disminución en la pérdida sanguínea de 264 ml después de la administración intravenosa de ATX a una dosis de 15 mg/kg, sin observar un mayor riesgo de eventos tromboembólicos.31
En 2015 se realizó un metaanálisis de 11 estudios controlados aleatorizados en el cuál se administró ATX a 644 pacientes sometidos a cirugía de columna. Los autores determinaron que el ATX disminuyó la pérdida sanguínea intraoperatoria, postoperatoria y total en un promedio de 219 ml, 119 ml y 202 ml, respectivamente. Además, también notaron una disminución en la necesidad de transfusión sanguínea, sin observar un mayor riesgo de eventos tromboembólicos.29
Pong y colaboradores en 2018 realizaron un estudio en adultos sometidos a cirugías para corrección de deformidades de la columna, en el que a un grupo de pacientes no se les administró ATX y a otro grupo se le administró un bolo preoperatorio de ATX intravenoso de 10 mg/kg seguido de una infusión intravenosa preoperatoria de 1 mg/kg/hora. La pérdida sanguínea estimada fue significativamente menor en el grupo al que se le administró el ATX (932 ± 539 ml) en comparación con el grupo control (1,800 ± 1,029 ml). La tasa de transfusiones sanguíneas también fue significativamente menor en el grupo al que se le administró el ATX (1.5 ± 1.6 vs 4.0 ± 2.1 paquetes globulares). De la misma manera, los valores de dímero D fueron significativamente menores en el grupo del ATX (3.3 ± 3.2 vs 8.3 ± 5.02 mg/ml). El consumo de fibrinógeno también disminuyó de 98.4 ± 42.6 mg/dl en el grupo control a 60.6 ± 35.1 mg/dl en el grupo del ATX.32
Trauma
Los resultados alentadores en el uso de ATX en cirugía ortopédica electiva llevaron a la investigación sobre su uso en cirugía de trauma con el objetivo de reducir los requerimientos de transfusión sanguínea, así como la mortalidad secundaria a hemorragias. Uno de los estudios sobre el uso de ATX en trauma es el Clinical Randomization of an Antifibrinolytic in Significant Hemorrhage (CRASH-2).33 Este estudio controlado aleatorizado internacional evaluó el efecto del ATX en más de 20,211 pacientes que sufrieron trauma penetrante o contuso en 274 hospitales en 40 países, se aleatorizó la administración de ATX o placebo; el principal desenlace fue muerte a las cuatro semanas posteriores al traumatismo. A los casos que llegaron al hospital dentro de las primeras ocho horas del trauma se les administró 1 gramo de ATX en bolo intravenoso durante 10 minutos seguido de una infusión de 1 gramo intravenoso en ocho horas. El grupo que recibió ATX tuvo menos muertes por hemorragia sin un aumento en la formación de coágulos, además de que hubo una disminución en la mortalidad de 14.5%. Los eventos tromboembólicos fueron similares en ambos grupos; sin embargo, los pacientes a los que se les administró el ATX dentro de la primera hora del trauma tuvieron los mayores beneficios. Los autores concluyeron que el uso de ATX es seguro y eficaz y que debe ser administrado lo antes posible a los pacientes que hayan sufrido un trauma.1,5,6
Otro estudio ha demostrado que el ATX tuvo el mayor beneficio de sobrevivencia en los pacientes que se presentaron con una presión sistólica por debajo de 75 mmHg y que fueron tratados prontamente después de sufrir las lesiones, especialmente en aquéllos que lo recibieron dentro de la primera hora después del trauma. Interesantemente, aquéllos que recibieron el ATX después de tres horas tuvieron un aumento en la mortalidad.1,34
Otra investigación demostrando el uso del ATX en trauma fue el Military Application of Tranexamic Acid in Trauma Emergency Resuscitation (MATTERs) en el cual se incluyeron 896 soldados que requerían transfusiones sanguíneas masivas por heridas traumáticas. Se observó una disminución en la mortalidad, una mayor supervivencia y menor coagulopatía en los pacientes a quienes se les administró ATX. En contraste con el estudio CRASH-2, el estudio MATTERs reportó un aumento en el riesgo de eventos tromboembólicos. Sin embargo, se piensa que este hallazgo fue debido a que los pacientes a los que se les administró el ATX tenían lesiones más severas.6,35 Asimismo, se ha demostrado que el uso de ATX en trauma es costo-efectivo y disminuye la estancia hospitalaria.
Gausden y su grupo publicaron en 2017 un metaanálisis en el que evaluó la eficacia del ATX en sujetos que requirieron cirugía traumatológica. Los autores evaluaron estudios que involucraron casos con fracturas del cuello femoral, fracturas intertrocantéricas, de calcáneo, de acetábulo y pacientes con fracturas de la diáfisis femoral. El efecto máximo del ATX en disminuir el sangrado fue dentro de las primeras 24 horas posteriores a la administración del medicamento. Los autores no observaron diferencia entre la administración tópica versus la intravenosa para la reducción de la transfusión sanguínea. Es importante señalar que los autores no observaron un mayor riesgo de eventos tromboembólicos sintomáticos en los pacientes a los que se les administró el ATX.36
ATX y eventos cardiovasculares
Una de las principales razones por las que muchos médicos no quieren o tienen aprehensión al momento de utilizar ATX, es por la creencia de que este aumenta el riesgo de desarrollar eventos cardiovasculares.
Varios estudios han investigado si el ATX aumenta el riesgo de presentar eventos cardiovasculares, tromboembólicos o aumentar el riesgo de muerte y ningún estudio hasta la fecha ha encontrado que el ATX tenga efectos perjudiciales sobre el riesgo de desarrollar eventos cardiovasculares o muerte en pacientes con bajo riesgo.11,21 En un estudio realizado por Poeran en 872,416 pacientes de 510 hospitales en Estados Unidos sometidos a artroplastía de cadera o rodilla a los que se les administró ATX, los autores observaron una disminución de 60% en cuanto a transfusiones sanguíneas autólogas y alogénicas. Asimismo, los casos que recibieron ATX tuvieron menos complicaciones tromboembólicas, complicaciones en general, necesidad de ventilación mecánica y admisión a una unidad de cuidados intensivos. De la misma manera, el costo de la estancia hospitalaria fue menor en los pacientes que recibieron ATX.37,38,39.40,41
Es de interés resaltar que en una investigación realizada por Dastrup y colaboradores se encontró que los pacientes expuestos al ATX tuvieron un riesgo significativamente reducido de trombosis arterial y de mortalidad.42 Poeran y su grupo reportaron que la tasa de admisión a la unidad de terapia intensiva disminuyó significativamente de 7.5 a 3.1% con el uso del ATX.37
Los efectos cardiovasculares del ATX en pacientes con alto riesgo, como los pacientes con antecedentes de un evento vascular cerebral, enfermedad coronaria, trombosis venosa profunda, tromboembolia pulmonar o condiciones protrombóticas como deficiencia del factor V de Leiden o síndrome antifosfolípidos, no se conocen con exactitud debido a que estos pacientes generalmente son excluidos de los estudios. Un estudio evaluó el uso del ATX en pacientes de alto riesgo sometidos a artroplastía total de rodilla o cadera primarias, con un American Society of Anesthesiologists (ASA) score de III o IV. No se observó que los pacientes con alto riesgo quirúrgico tuvieran un riesgo aumentado de desarrollar una trombosis venosa profunda sintomática a los 30 días de la cirugía.4
Efectos secundarios del ATX
La administración tópica de ATX en el sistema nervioso central de animales ha demostrado causar convulsiones de una manera dosis dependiente. En humanos, la inyección accidental intratecal de ATX también ha causado convulsiones. En algunos pacientes pueden ocurrir alteraciones gastrointestinales como náusea, vómito o diarrea, visión borrosa, vértigo, cefalea, reacciones ortostáticas y reacciones alérgicas cutáneas.4,5),(8,43 Con el uso de ATX no se han observado diferencias estadísticamente significativas en el tiempo de protrombina, índice normalizado de referencia, tiempo parcial de tromboplastina, fibrinógeno y dímero D.8
Conclusiones
El ATX es efectivo dentro de la Ortopedia y Traumatología para la disminución del sangrado peri- y postoperatorio y para la disminución de la necesidad de transfusiones de sangre alogénica en las artroplastías de rodilla y cadera, ya sean primarias o de revisión, en la cirugía de columna y en trauma.
Asimismo, se ha demostrado que el ATX no aumenta el riesgo de desarrollar eventos tromboembólicos en pacientes sanos, por lo que su uso es seguro.
Hasta la fecha, no se tiene un acuerdo universal sobre la vía de administración ni la dosis más eficaz, por lo que más estudios son necesarios para estandarizar esta información.
Con la evidencia aquí presentada, se espera que los cirujanos ortopedistas tengan la información más actual acerca del ATX, incluyendo sus aplicaciones en distintas subespecialidades de la Ortopedia y Traumatología, las contraindicaciones y los efectos adversos para que pueda ser adoptado en sus prácticas médicas y para que el ATX tenga una mayor disponibilidad en los hospitales.











 nueva página del texto (beta)
nueva página del texto (beta)