Servicios Personalizados
Revista
Articulo
Indicadores
Links relacionados
Compartir
Revista mexicana de biodiversidad
versión On-line ISSN 2007-8706versión impresa ISSN 1870-3453
Rev. Mex. Biodiv. vol.85 no.4 México dic. 2014
https://doi.org/10.7550/rmb.43457
Ecología
Composición, estructura y diversidad de la comunidad arbórea del bosque tropical caducifolio en Tziritzícuaro, Depresión del Balsas, Michoacán, México
Composition, structure and diversity of Tziritzícuaro tropical dry forest tree community, Balsas Watershed, Michoacán, Mexico
Moisés Méndez-Toribio*, Juan Martínez-Cruz, Jorge Cortés-Flores, Francisco Javier Rendón-Sandoval y Guillermo Ibarra-Manríquez
1 Centro de Investigaciones en Ecosistemas, Universidad Nacional Autónoma de México. Antigua carretera a Pátzcuaro 8701, Col. San José de la Huerta, 58190 Morelia, Michoacán, México. * mendeztm@comunidad.unam.mx
Recibido: 23 noviembre 2013
Aceptado: 17 julio 2014
Resumen
Se describe la composición, estructura y diversidad de los árboles del bosque tropical caducifolio en Tziritzícuaro, municipio de La Huacana, en la Depresión del Balsas, Michoacán. Se censaron todos los árboles enraizados dentro de 36 parcelas de 100 m2 (0.36 ha) con un diámetro a la altura del pecho (DAP) ≥ 1 cm. Se registraron 78 especies, incluidas en 50 géneros y 24 familias. La familia Fabaceae fue la más importante respecto a su número de especies (24), géneros (14) e individuos (274). En total se registraron 1 013 individuos y 2 313 tallos. Los valores promedio del área basal, cobertura y altura fueron de 0.18 m2, 310 m2 y 5 m, respectivamente. El número promedio de especies por parcela fue 10, mientras que el valor medio del índice α de Fisher= 8. El bosque tropical caducifolio estudiado comparte características similares a comunidades análogas situadas en otras partes de México y del neotrópico, lo que permite ratificar patrones previamente detectados en la composición, estructura y diversidad de este tipo de vegetación.
Palabras clave: árboles, diversidad alfa, Fabaceae, valor de importancia relativa.
Abstract
We characterized the composition, structure and diversity of tropical dry forest trees at Tziritzícuaro, municipality of La Huacana, in the Depresión del Balsas, Michoacán. We sampled all trees that were rooted inside 36 plots of 100 m2 (0.36 ha) with a diameter at breast height (DBH) ≥ 1 cm. A total of 78 species, including 50 genera and 24 families were recorded. Fabaceae was the most important family respect to the number of species (24), genera (14) and individuals (274). It was recorded a total of 1 013 individuals and 2 313 stems. Basal area, cover and height average were of 0.18 m2, 310 m2 and 5 m, respectively. The average of species richness was of 10 species, with a mean value of Fisher α= 8. The tropical dry forest studied shares comparable characteristics to similar communities located in other parts of Mexico and the Neotropics, this enable to confirm patterns previously detected in the composition, structure and diversity of this vegetation type.
Key words: trees, alpha diversity, Fabaceae, importance value.
Introducción
La vegetación localizada en las regiones tropicales estacionalmente secas es heterogénea y está influida por una compleja historia ambiental y biogeográfica (Pérez-García et al., 2012). Los autores anteriormente citados indican que dentro de este tipo de vegetación el bosque tropical caducifolio (Rzedowski, 1978) es el mejor representado en México, aunque sus límites geográficos no son fáciles de circunscribir. En el país se han llevado a cabo distintos estudios para documentar su estructura y diversidad, resaltando por su amplitud espacial el de Trejo y Dirzo (2002), quienes caracterizaron 20 localidades con bosque tropical caducifolio (BTC) a lo largo de su área distribución. A una escala más regional, se cuenta con estudios similares para las penínsulas de Baja California y Yucatán, y los estados de Chiapas, Guerrero, Jalisco, Oaxaca, Sonora y Veracruz (Lott et al., 1987; Rico-Gray et al., 1988; Martínez-Yrízar et al., 1996, 2000; Balvanera et al., 2002; Segura et al., 2002; White y Hood, 2004; Pérez-García y Meave, 2004; Gallardo-Cruz et al., 2005; Durán et al., 2006; Pineda-García et al., 2007; Lebrija-Trejos et al., 2010, 2011; Rocha-Loredo et al., 2010; Almazán-Núñez et al., 2012; Martínez-Cruz et al., 2013; Dzib-Castillo et al., 2014). La información disponible en los estudios previamente mencionados permite resaltar algunas tendencias del BTC de México: 1) las familias Burseraceae, Euphorbiaceae, Rubiaceae, y en especial Fabaceae, son importantes en cuanto al número de especies o individuos; 2) la predominancia de los árboles sobre las lianas es evidente, aunque su variación es considerable entre sitios; 3) el área basal presenta una marcada oscilación, con intervalos entre 10.5 y 78.8 m2 ha-1; 4) el número total de especies también es muy fluctuante, con valores de riqueza extremos de 22 a 97 especies en 0.1 ha (plantas ≥ 2.5 cm DAP) y 5) presenta una diversidad beta alta.
Este tipo de vegetación se localiza en 6 provincias biogeográficas de México, las cuales se distribuyen, principalmente, en ambas vertientes del país (Rzedowski, 1978; Lott y Atkinson, 2006). Una excepción a lo anterior es la Provincia de la Depresión del Balsas, ya que se registra hacia la parte continental, abarcando aproximadamente 112 320 km2. En esta provincia la vegetación con mayor extensión es el BTC (Rzedowski, 1978; Morrone, 2005), el cual se caracteriza por presentar un notable porcentaje de biota endémica (Rzedowski, 1991; Rodríguez-Jiménez et al., 2005; Lott y Atkinson, 2006; Ceballos et al., 2010).
En general, la mayoría de los estudios realizados en el BTC en esta provincia han tenido como objetivo su descripción fisonómica y florística (Miranda, 1947; Miranda y Hernández-X, 1963; Rzedowski, 1978). Dentro de las publicaciones con un enfoque cuantitativo se puede mencionar la de Trejo y Dirzo (2002), quienes por medio del censo de los árboles y lianas > de 1 cm DAP, en unidades de muestreo de 0.1 ha, incluyen 4 sitios de la Depresión del Balsas (Cañón del Zopilote, Guerrero; Cerro Tuxpan e Infiernillo, Michoacán y El Limón, Morelos). El número de especies en estas localidades osciló entre 76 y 115 especies, con valores del índice de Shannon de 3.64 a 4.09. Posteriormente, Pineda-García et al. (2007) realizaron 4 muestreos similares en El Tarimo, Guerrero, donde encontraron un menor número de especies (43-55) y una similitud alta entre sitios (índice de Jaccard de 0.40 a 0.58). En un estudio más reciente, Martínez-Cruz et al. (2013) censaron 3 sitios en el municipio de Francisco J. Múgica, Michoacán y, aunque su categoría diamétrica mínima fue de individuos ≥ a 2.5 cm, sus resultados fueron similares a los cuantificados en El Tarimo (38 a 45 especies e índice de similitud de Sorensen entre 0.41 y 0.57).
Considerando la superficie de la Provincia de la Depresión del Balsas, la importante variación observada en los atributos comunitarios del BTC en México, la amplia extensión de éste en la Depresión del Balsas, así como el limitado número de contribuciones enfocadas a estimar parámetros cuantitativos de este tipo de vegetación dentro de los límites de esta provincia, el presente estudio tiene como objetivo principal aportar una caracterización de la composición, estructura y diversidad del componente arbóreo de un BTC de la Depresión del Balsas, en el estado de Michoacán (Fig. 1). En particular, se desea determinar el grado de similitud de este bosque con respecto a otras regiones previamente estudiadas en México y en el continente americano, ya que debido a la composición florística distintiva de la Provincia Biogeográfica de la Depresión del Balsas, se podrían esperar respuestas particulares de las especies que afecten los atributos de estructura y diversidad a nivel comunitario.
Materiales y métodos
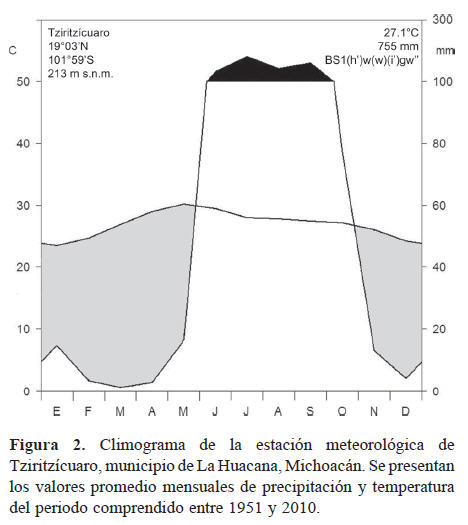
Área de estudio y sitios de muestreo. La zona de trabajo se localiza en el ejido de Tziritzícuaro, en la Provincia Morfotectónica de la sierra Madre del Sur, Subprovincia de la Depresión del Balsas, en la cuenca hidrológica del río Balsas, cuya altitud oscila entre 200 y 1 000 m (Ferrusquía-Villafranca, 1993). Entre los sistemas geomorfológicos más importantes que se presentan en la región se encuentran los lomeríos, el valle de laderas tendidas con lomeríos y meseta lávica, así como el de la sierra con cañadas y mesetas (Ferrusquía-Villafranca, 1993; Nava et al., 1998). De acuerdo con la clasificación de Köppen, modificada por García (2004), el clima del área de estudio es seco cálido con régimen de lluvias de verano, isoterma intertropical y con canícula [BS1(h')w(w)(i)gw"]. La temperatura media anual es de 27.1° C y mayo es el mes que muestra la mayor temperatura (30.2° C); la precipitación total anual es de 755.4 mm, de los cuales el 80% se concentra entre los meses de junio a septiembre, con una marcada estación seca que va de octubre a mayo (Fig. 2). El tipo de vegetación presente en el área corresponde al bosque tropical caducifolio (Rzedowski, 1978) o selva baja caducifolia (Miranda y Hernández-X., 1963), que generalmente se asienta sobre litosoles de textura media (Inifap y Conabio, 1995). El uso predominante de la vegetación en la zona es la crianza extensiva de ganado y la extracción de madera (Conanp, 2006).
Como una estrategia para incluir la mayor heterogeneidad florística y ambiental posible, los datos de la vegetación fueron registrados en 36 parcelas de 100 m2 (10×10 m), distribuidas en las partes bajas, medias y altas de 3 macizos montañosos (La Araña, El Ortigo y El Tukuy), cuya altitud oscila entre 380 y 780 m. Las parcelas se establecieron en las laderas norte y sur, en sitios sin evidencia aparente de disturbio, aunque en el área la recolección de leña y el libre pastoreo de ganado, principalmente vacuno, son actividades frecuentes. En cada una de las unidades de muestreo se registraron todas las plantas arbóreas, incluyendo cactus arborescentes, que estuvieran enraizadas dentro de la parcela y con un diámetro a la altura del pecho (DAP) ≥ 1 cm. Cada una de las plantas registradas fue identificada taxonómicamente y se midió su altura total, 2 diámetros de cobertura, lado mayor de la copa y el perpendicular a éste, así como el número y diámetro de sus tallos.
Análisis de estructura y diversidad. Se realizaron análisis de estas variables a nivel de parcela (36 de 0.01 ha) y para 0.1 ha, esto último con el objeto de contrastar estos atributos con trabajos similares que usaron esta superficie como área de muestreo. Para ello, de las 36 parcelas censadas se eligieron 10 al azar, sin reemplazo, obteniendo los valores de los atributos comunitarios de interés para las categorías diamétricas ≥ 1 y ≥ 2.5 cm. Con respecto a la estructura se calcularon las siguientes variables: densidad, porcentaje de individuos policaules, cobertura, área basal, DAP y altura. De acuerdo con los procedimientos descritos por Mueller-Dombois y Ellenberg (1974), se calculó el valor de importancia de cada especie, usando los valores relativos de frecuencia, densidad y área basal (Apéndice). Asimismo, como primera medida de diversidad de la comunidad se obtuvo la riqueza de especies local (S) y se calcularon los siguientes índices (ver Magurran, 2004 para las fórmulas de éstos): i) el de dominancia de Simpson (D); ii) el de diversidad de Shannon (H'), usando el logaritmo natural para calcularlo; iii) el de equidad de H' y iv) el α de Fisher. Para este último, se usó el programa Paleontological Statistics (Hammer, 2012).
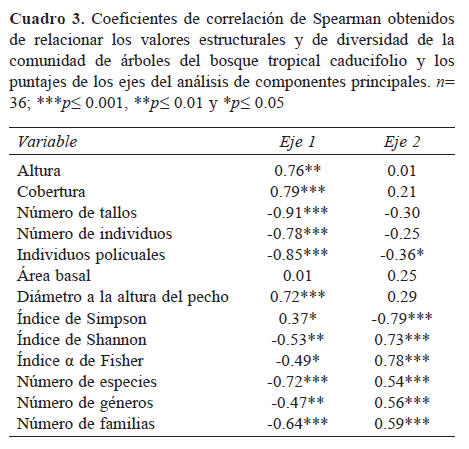
Variación de los atributos comunitarios. Para analizar la variación en la estructura y diversidad taxonómica entre las parcelas, se realizó un análisis de componentes principales (PCA) que incluyó variables de estructura (altura promedio por parcela, promedio de la cobertura, número de tallos, número de individuos, porcentaje de individuos policaules, área basal total y promedio del diámetro a la altura del pecho), de diversidad (índices de Simpson, Shannon y de α de Fisher), así como el número de familias, géneros y especies. Se realizaron correlaciones de Spearman para determinar el grado de asociación de las variables de respuesta a los ejes del PCA que mayor porcentaje de variación explicaron. Se consideró como significativa la prueba a un nivel de α≤ 0.05.
Resultados
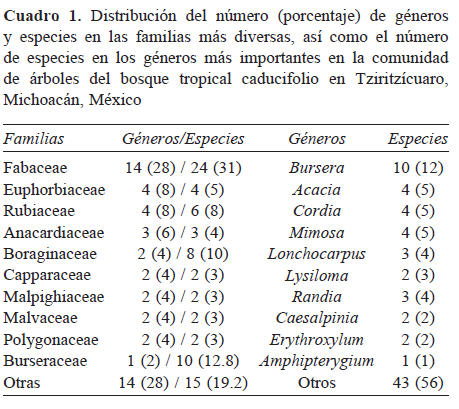
Composición florística. En los 3 sitios censados se registraron 78 especies, incluidas en 50 géneros y 24 familias de Magnoliophyta (Apéndice). El Cuadro 1 muestra que el 67% de la riqueza total de especies registradas pertenecen a Fabaceae (24), Burseraceae (10), Boraginaceae (8), Rubiaceae (6) y Euphorbiaceae (4). La primera de estas familias también presenta el mayor número de géneros (14), seguida de Euphorbiaceae y Rubiaceae (ambas con 4), aunque el más diverso pertenece a Burseraceae (Bursera, 10 spp.). La riqueza a nivel de familia se relaciona claramente con la abundancia de sus individuos, ya que Fabaceae (274 individuos), Rubiaceae (178), Euphorbiaceae (143), Boraginaceae (89) y Burseraceae (86) representan el 76% del total registrado. Con respecto a este último atributo, los géneros que destacan son Randia (145 individuos), Euphorbia (92), Bursera (86), Cordia (85) y Acacia (82), que en conjunto engloban el 48% del total.
Estructura. Se registraron 1 013 individuos y 2 313 tallos en las 36 parcelas de 100 m2. Ninguna especie estuvo presente en todas las parcelas, y las de mayor frecuencia fueron Cordia elaeagnoides, Randia nelsonii, Apoplanesia paniculata y Euphorbia schlechtendalii (26, 22, 19 y 18 parcelas, respectivamente). Un total de 52 especies (66%) aparecieron en menos de 5 parcelas y 26 (33%) se registraron solamente en una. La densidad promedio fue de 28, con una desviación estándar (DE) de ±10 individuos, con valores entre 7 y 56 (Cuadro 2). Las 5 especies más abundantes fueron R. nelsonii, E. schlechtendalii, C. elaeagnoides, Acacia picachensis y Handroanthus impetiginosus (Apéndice). Con respecto al número de tallos, el promedio fue de 64±33 tallos (mínimo 17, máximo 189). El promedio del porcentaje de individuos policaules fue 54±17% y fue la variable estructural que presentó el menor coeficiente de variación (32%), con un intervalo que osciló de 17 al 100% (Cuadro 2). En cuanto al número de tallos nuevamente destacó R. nelsonii, seguida por C. elaeagnoides, A. paniculata, E. schlechtendalii y Bursera coyucensis.
El promedio de la cobertura para el total de parcelas fue de 310±154 m2. El valor mínimo fue de 124 m2 y el máximo de 1 003 m2 (Cuadro 2). Esta variable fue la que mostró el mayor coeficiente de variación (50%) y se caracterizó porque los individuos con DAP entre 5 a 9.9 cm presentaron los valores más altos de cobertura (Fig. 3A). Las 5 especies que se destacaron, en cuanto a sus valores de cobertura fueron (Apéndice): C. elaeagnoides (1 608 m2), Lysiloma microphylla (956 m2), A. picachensis (799 m2), Acacia cochliacantha (725 m2) y R. nelsonii (722 m2).
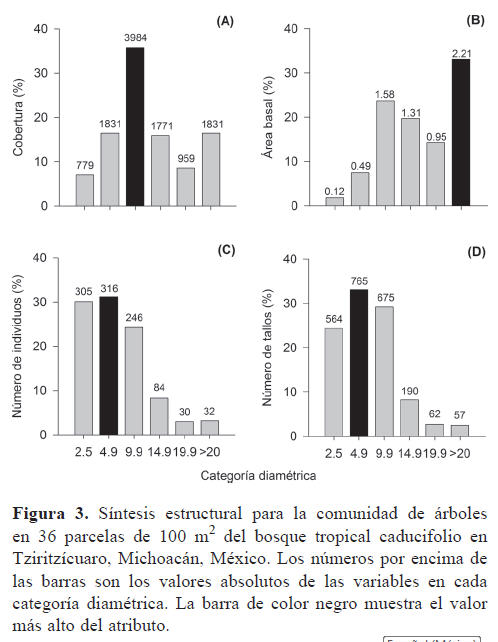
El promedio del área basal fue de 0.18±0.08 m2, con el valor más bajo de 0.06 m2 y el mayor de 0.44 m2 (Cuadro 2). Los individuos con un diámetro ≥ 20 cm son los que tuvieron el mayor aporte al valor total de área basal (33%; Fig. 3B). Un total de 10 especies contribuyeron con más del 60% del área basal (Apéndice), destacando C. elaeagnoides (18.6%), Cyrtocarpa procera (8.2%), L. microphylla (7.9%), A. paniculata (6.7%) y Cochlospermum vitifolium (4.2%). El promedio del DAP fue de 5.1±1.4 cm y el intervalo osciló entre 2.9 y 7.7 cm (Cuadro 2). Los individuos y los tallos de 1 a 4.9 cm representan el 61 y 54% del total registrado, respectivamente (Figs. 3C, D). Las especies con los valores promedio de DAP más sobresalientes fueron C. vitifolium (42±5.8), Pterocarpus orbiculatus (24±0), Stenocereus queretaroensis (22±6.7) y Bursera heteresthes (17±5.6).
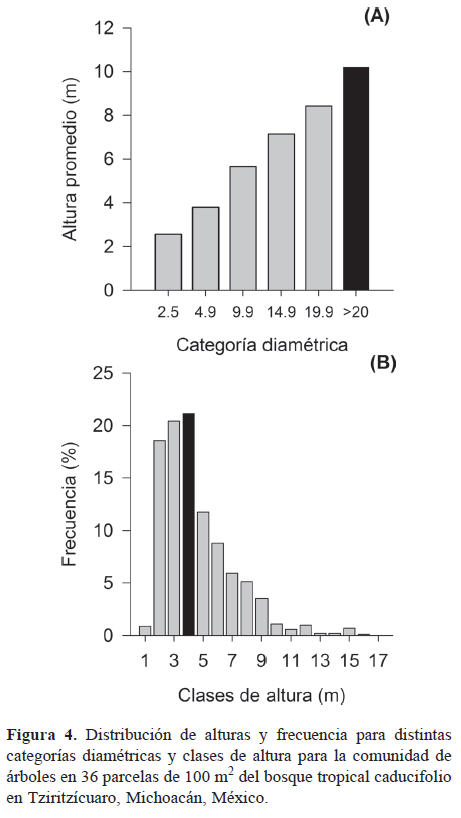
La altura promedio en el total de parcelas muestreadas fue de 4.6±0.9 m, con un intervalo de 2.9 a 6.8 m (Cuadro 2). Las plantas con un diámetro ≥ 20 cm presentaron la mayor altura promedio, mientras que la frecuencia más alta se presenta en los individuos de 4 m (Fig. 4). La especie con mayor estatura fue H. impetiginosus (16 m), mientras que 3 alcanzaron una altura de 15 m (C. vitifolium, C. elaeagnoides y L. microphylla). Los resultados de los valores de importancia relativa (VIR) muestran que las 5 especies estructuralmente más importantes en orden decreciente fueron (Apéndice): C. elaeagnoides (33.45), R. nelsonii (23.22), E. schlechtendalii (16.34), A. paniculata (15.85) y L. microphylla (15.01).
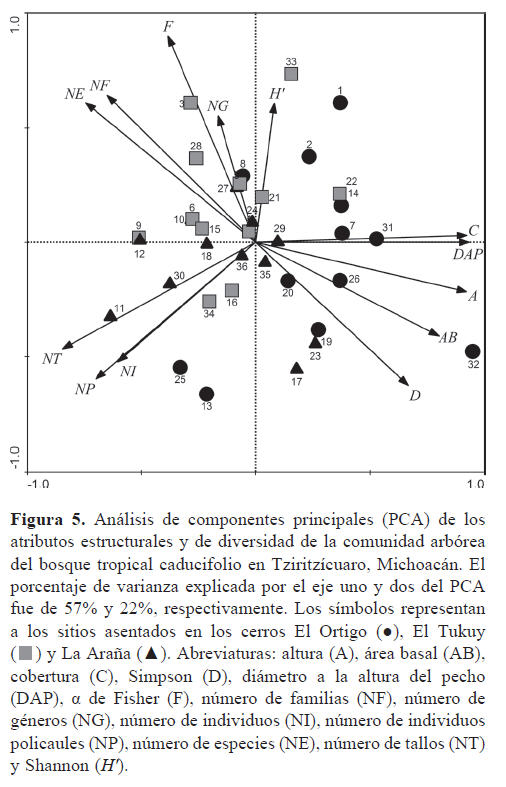
El análisis multivariado indica que el 85% de la variación en los datos es explicada por los 2 primeros ejes (eje 1, 56%; eje 2, 29%). Con la excepción del área basal, las variables estructurales se relacionan significativamente con el eje 1 del PCA, mientras que, en general, las variables de diversidad están asociadas con el eje 2 (Cuadro 3). Las parcelas ubicadas hacia el lado derecho de la figura 5 están principalmente afectadas por las variables estructurales (e. g., cobertura o altura). Por otro lado, las parcelas localizadas a la izquierda del cuadrante superior se caracterizan por tener valores altos en las distintas categorías taxonómicas que presentan y en el índice alfa de Fisher, mientras que en la parte inferior izquierda se presentan aquellas con los valores mayores de abundancia.
Diversidad. La riqueza promedio en las parcelas muestreadas fue de 10±4 especies (intervalo: 2-19 especies). El valor obtenido para el índice de Simpson (0.05) y su promedio (0.18±0.15) muestran un bajo nivel de dominancia dentro de la comunidad, aunque este atributo resultó ampliamente variable entre las unidades de muestreo, lo que concuerda con los valores obtenidos para el índice de equitatividad (Cuadro 2), con un coeficiente de variación de 80%. El valor promedio del índice de Shannon fue de 2±0.5, con valores de 0.41 a 2.69 y un coeficiente de variación del 26%. El índice α de Fisher promedió 7.5±4.9, con una variabilidad alta (67%) y un valor global de 21 (Cuadro 2).
Discusión
Composición florística. En el presente estudio se encontró que la familia con mayor número de especies, géneros e individuos fue Fabaceae (Cuadro 1). Este hallazgo coincide con numerosos estudios desarrollados en los bosques secos de México, Centro y Sudamérica (Lott et al., 1987; Gentry, 1988; Gillespie et al., 2000; Phillips y Miller, 2002; Trejo y Dirzo, 2002; Gallardo-Cruz et al., 2005; Ruiz et al., 2005; Lott y Atkinson, 2006; Pineda-García et al., 2007; Pérez-García et al., 2010; Almazán-Núñez et al., 2012; Martínez-Cruz et al., 2013). De hecho, la revisión de Rzedowski y Calderón de Rzedowski (2013), sobre la flora fanerogámica del BTC, confirma la predominancia indudable de esta familia. Asimismo, en Tziritzícuaro, las familias Burseraceae, Euphorbiaceae y Rubiaceae ocupan posiciones importantes en lo que concierne al número de especies, lo que coincide con lo documentado en estudios previos (Gentry, 1995; Phillips y Miller, 2002; Gallardo-Cruz et al., 2005; Cué-Bär et al., 2006; Sousa, 2010; Almazán-Núñez et al., 2012).
A nivel genérico no sorprende encontrar que el taxón con mayor número de especies en Tziritzícuaro sea Bursera (Cuadro 1), ya que la cuenca del Balsas ha sido reconocida como centro de endemismo y diversificación de este taxón (Rzedowski, 1978, 1991; Becerra, 2005; De-Nova et al., 2012). Cabe destacar que Michoacán y Oaxaca comparten la segunda posición a nivel nacional respecto al número de especies en este género (37), sólo superadas por Guerrero, con 47 especies (Rzedowski et al., 2005). Se postula que la gran diversidad de Bursera se debe en parte a procesos geográficos como el levantamiento de la sierra Madre Occidental y el Eje Neovolcánico Transmexicano, eventos que sucedieron durante los periodos Terciario y Cuaternario (Becerra, 2005; Rzedowski et al., 2005) y que permitieron su radiación, principalmente a lo largo de la vertiente del Pacífico y la cuenca del Balsas. Otros géneros que se destacaron también en este estudio y que han sido clasificados previamente como de amplia distribución en el neotrópico, especialmente en los bosques secos son: Acacia, Caesalpinia, Cordia, Euphorbia, Lonchocarpus, Lysiloma, Mimosa y Randia (Gentry, 1995). Todos estos taxones son mencionados por Rzedowski y Calderón de Rzedowski (2013), entre los que contienen mayor número de especies y que habitan preferencial o exclusivamente en el BTC.
Estructura. Los valores de densidad en 0.1 ha (314 individuos ≥ 1 cm y 202 individuos ≥ 2.5 cm) obtenidos para Tziritzícuaro (Cuadro 4), se ubican dentro de las cifras previamente documentadas para este tipo de vegetación en México (203-583 individuos ≥ 1 cm DAP; Lott et al., 1987; Trejo, 2005) y para otras comunidades del neotrópico seco donde se censaron entre 135 y 520 individuos ≥ 2.5 cm de DAP (Keel et al., 1993; Gentry, 1995; Gillespie et al., 2000; Phillips y Miller, 2002; Pineda-García et al., 2007; Martínez-Cruz et al., 2013). La policaulescencia fue un atributo notable debido a su alta frecuencia, ya que 61.1% de las unidades de muestreo se caracterizaron por tener más del 50% de sus individuos con más de un tallo (Cuadro 2) y lo mismo acontece cuando se compara este porcentaje en un área de 0.1 ha (Cuadro 4). La presencia de árboles con tallos múltiples constituye un rasgo característico de los bosques tropicales secos (Dunphy et al., 2000; Gallardo-Cruz et al., 2005, 2009).
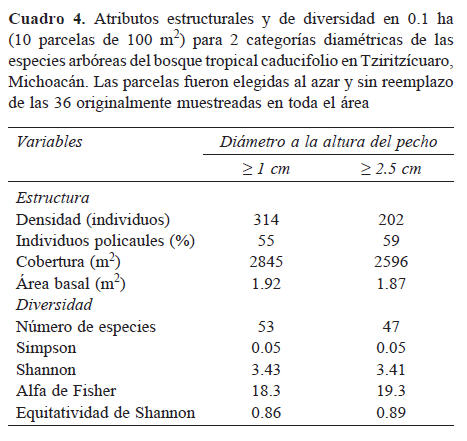
Los valores de cobertura promedio muestran que existe un alto porcentaje (> 300) de superposición de las copas de los árboles en el dosel del BTC estudiado (Cuadro 2), en particular de los individuos con DAP cercanos a los 10 cm (Fig. 3), una situación análoga a lo obtenido para el BTC de Nizanda (Gallardo-Cruz et al., 2005; Pérez-García y Meave, 2004). El área basal promedio para los individuos ≥ 2.5 cm de DAP fue de 1.87 m2 (Cuadro 4), la cual es similar a lo registrado en localidades de Jalisco y Michoacán por Lott et al. (1987) y Martínez-Cruz et al. (2013). Este valor está por debajo del promedio registrado para el neotrópico, que es de 3.2 m2 (Gentry, 1995; Salas-Morales, 2002).
La altura promedio registrada en el área de estudio (4.6 m; Cuadro 2) también resultó parecida a la que se obtuvo en Cerro Verde, Oaxaca (4.1 m, Gallardo-Cruz et al., 2005), pero menor a los 6 y 8 m registrados en distintas localidades de México e islas del Caribe (Kapos, 1986; Murphy y Lugo, 1986; Martínez-Yrízar et al., 1992, 1996; González y Zak, 1996; Salas-Morales, 2002; Segura et al., 2002; Gallardo-Cruz et al., 2005; McLaren et al., 2005; Durán et al., 2006; Álvarez-Yépiz et al., 2008).
El análisis mutivariado muestra que el BTC de Tziritzícuaro presenta una alta variación (> 80%), en cuanto a sus atributos comunitarios de riqueza, estructura y diversidad, pero en términos generales reitera su equivalencia con el BTC localizado a lo largo del neotrópico (Gentry, 1995; Phillips y Miller, 2002; Trejo y Dirzo, 2002; Gallardo-Cruz et al., 2005; Lott y Atkinson, 2006; Pineda-García et al., 2007; Pérez-García et al., 2010; Martínez-Cruz et al., 2013). Esta gran heterogeneidad en los rasgos comunitarios se ha explorado con cierto detalle en diversas regiones del mundo y ha sido relacionado con la variación de factores ambientales (e. g., insolación, temperatura y humedad) que se puede presentar en los paisajes naturales debido a factores geográficos como el relieve y la geomorfología (Gallardo-Cruz et al., 2005; Durán et al., 2006; Warren, 2008, 2010; Flores et al., 2009; Reich et al., 2010; Li et al., 2011). No obstante, este tipo de relaciones aún tienen que ser evaluadas en el área de estudio.
Diversidad. En el submuestreo de 0.1 ha (Cuadro 4) se cuantificaron 53 y 47 especies, tomando en cuenta individuos ≥ 1 y ≥ 2.5 cm de DAP, respectivamente; este contingente florístico incluye para la categoría diamétrica menor 20 familias y 36 géneros, mientras que para la segunda estos taxones registran valores ligeramente menores (18 y 32). Nuevamente la riqueza de las categorías supraespecíficas es casi idéntica a la registrada en varias localidades de México y del neotrópico (Murphy y Lugo, 1986; Gentry, 1995; Trejo y Dirzo, 2002; Pineda-García et al., 2007; Martínez-Cruz et al., 2013). A nivel de especie, el valor obtenido en el BTC de Tziritzícuaro se ubicó dentro del intervalo registrado para este tipo de vegetación en México (Trejo y Dirzo, 2002), aunque por debajo del promedio nacional (74±24 especies). Asimismo, la riqueza es lejana de los valores más altos (> 100 especies) documentados para el BTC del neotrópico (Gentry, 1995) y a nivel mundial (Phillips y Miller, 2002). De hecho, la cifra de este atributo de diversidad se parece más a las obtenidas previamente por Pineda-García et al. (2007), Martínez-Cruz et al. (2013) y a los de otras localidades del país estudiadas por Trejo (2005) (e. g., La Burrera, Baja California; Cerro Zináparo, Michoacán; Jesús María, Nayarit; Calipam, Puebla). Al compararlos con otros sitios localizados en América, los valores de los índices de diversidad (Cuadro 4) siguen tendencias similares a las descritas para el número de especies.
Conclusiones. Los resultados del presente estudio permiten afirmar que la composición, estructura y diversidad del BTC en Tziritzícuaro son comparables con lo detectado para este tipo de vegetación en otras localidades de México y del continente Americano. Estos atributos comunitarios podrían ser mejor entendidos si se analizará la influencia de factores ambientales críticos como la topografía, diferentes tipos de suelo o el efecto del disturbio por actividades agropastoriles (Robert y Marie-Agnès, 2003; Lebrija-Trejos et al., 2010; Eisenlohr et al., 2013). También puede ser pertinente evaluar la variación de atributos funcionales de las especies a lo largo de gradientes ambientales de disponibilidad de humedad, un enfoque de investigación relativamente reciente y promisorio para entender los patrones de estructuración y mantenimiento de la biodiversidad en el BTC (McGill et al., 2006; Li et al., 2011; Pavoine y Bonsall, 2011). El establecimiento de parcelas permanentes, que incluso puedan reflejar diferentes tiempos de disturbio (e. g., Lebrija-Trejos et al., 2010, 2011), serían especialmente valiosas para el desarrollo de este tipo de investigaciones, lo que contribuiría en la conservación del BTC de la Depresión del Balsas, una región prioritaria al respecto a una escala global (Olson y Dinerstein, 2002).
Agradecimientos
El presente estudio forma parte de la investigación doctoral del primer autor y constituye un requisito para la obtención del grado de Doctor en Ciencias del Posgrado en Ciencias Biológicas de la Universidad Nacional Autónoma de México. El primer autor agradece al Conacyt por la beca para desarrollar sus estudios de doctorado. Esta investigación fue apoyada por el Programa de Apoyo a Proyectos de Investigación e Innovación Tecnológica (PAPIIT) de la UNAM, como parte del proyecto IN207512 (Fenología de especies arbóreas del bosque tropical caducifolio en la Depresión del Balsas, Michoacán). Se agradece a Patricio y Jesús Rosas, habitantes de la localidad de Tziritzícuaro, por la asistencia en el trabajo de campo realizado en el presente estudio. A la Ing. Atzimba López-Maldonado, al Ing. Alberto Valencia-García y al MTI. Heberto Ferreira-Medina, por apoyar diversos aspectos técnicos del trabajo de cómputo. La ayuda de la M. en C. Guadalupe Cornejo-Tenorio fue invaluable en la identificación de las plantas censadas y en la elaboración final de las figuras. Los comentarios realizados al documento por 3 árbitros anónimos y por el Dr. Ramón Cuevas-Guzmán contribuyeron a mejorar sustancialmente una versión previa del trabajo.
Literatura citada
Almazán-Núñez, R. C., M. del C. Arizmendi, L. E. Eguiarte y P. Corcuera. 2012. Changes in composition, diversity and structure of woody plants in successional stages of tropical dry forest in southwest Mexico. Revista Mexicana de Biodiversidad 83:1096-1109. [ Links ]
Álvarez-Yépiz, J. C., A. Martínez-Yrízar, A. Bórquez y C. Lindquist. 2008. Variation in vegetation structure and soil properties related to land use history of old-growth and secondary tropical dry forests in northwestern Mexico. Forest Ecology and Management 256:355-366. [ Links ]
Balvanera, P., E. Lott, G. Segura, C. Siebe y A. Islas. 2002. Patterns of β-diversity in a Mexican tropical dry forest. Journal of Vegetation Science 13:145-158. [ Links ]
Becerra, J. X. 2005. Timing the origin and expansion of the Mexican tropical dry forest. Proceedings of the National Academy of Sciences of the United States of America 102:10919-10923. [ Links ]
Ceballos, G., L. Martínez, A. García, E. Espinoza, J. B. Creel y R. Dirzo. 2010. Diversidad, amenazas y áreas prioritarias para la conservación de las selvas secas del Pacífico de México. Fondo de Cultura Económica, México, D. F. 594 p. [ Links ]
Conanp (Comisión Nacional de Áreas Naturales Protegidas). 2006. Estudio previo justificativo para el establecimiento de la Reserva de la Biofera Zicuirán-Infiernillo. Conanp, México, D. F. 59 p. [ Links ]
Cué-Bär, E. M., J. L. Villaseñor, L. Arredondo-Amezcua, G. Cornejo-Tenorio y G. Ibarra-Manríquez. 2006. La flora arbórea de Michoacán, México. Boletin de la Sociedad Botánica de México 78:47-81. [ Links ]
De-Nova, J. A., R. Medina, J. C. Montero, A. Weeks, J. A. Rosell, M. E. Olson, L. E. Eguiarte y S. Magallón. 2012. Insights into the historical construction of species-rich Mesoamerican seasonally dry tropical forests: the diversification of Bursera (Burseraceae, Sapindales). New Phytologist 193:276-287. [ Links ]
Dunphy, B. K., P. G. Murphy y A. E. Lugo. 2000. The tendency for trees to be multiple-stemmed in tropical and subtropical dry forests: studies of Guanica forest, Puerto Rico. Tropical Ecology 41:161-168. [ Links ]
Durán, E., J. A. Meave, E. J. Lott y G. Segura. 2006. Structure and tree diversity patterns at the landscape level in a Mexican tropical deciduous forest. Boletin de la Sociedad Botánica de México 79:43-60. [ Links ]
Dzib-Castillo, B., C. Chanatásig-Vaca y N. A. González-Valdivia. 2014. Estructura y composición en dos comunidades arbóreas de la selva baja caducifolia y mediana subcaducifolia en Campeche, México. Revista Mexicana de Biodiversidad 85:167-178. [ Links ]
Eisenlohr, P. V., L. F. Alves, L. C. Bernacci, M. C. Padgurschi, R. B. Torres, E. M. Prata, F. A. M. Dos Santos, M. A. Assis, E. Ramos y A. L. C. Rochelle. 2013. Disturbances, elevation, topography and spatial proximity drive vegetation patterns along an altitudinal gradient of a top biodiversity hotspot. Biodiversity and Conservation 22:2767-2783. [ Links ]
Ferrusquía-Villafranca, I. 1993. Geology of Mexico: a synopsis. In Biological diversity of Mexico: origins and distribution, T. Ramammorthy, R. Bye, A. Lot y J. Fa (eds.). Oxford University Press, New York. p. 3-107. [ Links ]
Flores, A. N., V. Y. Ivanov, D. Entekhabi y R. L. Bras. 2009. Impact of hillslope-scale organization of topography, soil moisture, soil temperature, and vegetation on modeling surface microwave radiation emission. IEEE Transactions on Geoscience and Remote Sensing 47:2557-2571. [ Links ]
Gallardo-Cruz, J. A., J. A. Meave y E. A. Pérez-García. 2005. Estructura, composición y diversidad de la selva baja caducifolia del Cerro Verde, Nizanda (Oaxaca), México. Boletin de la Sociedad Botánica de México 76:19-35. [ Links ]
Gallardo-Cruz, J. A., E. A. Pérez-García y J. A. Meave. 2009. β-Diversity and vegetation structure as influenced by slope aspect and altitude in a seasonally dry tropical landscape. Landscape Ecology 24:473-482. [ Links ]
García, E. 2004. Modificaciones al sistema de clasificación climática de Köppen. Instituto de Geografía, Universidad Nacional Autónoma de México, México, D. F. 90 p. [ Links ]
Gentry, A. H. 1988. Changes in plant community diversity and floristic composition on environmental and geographical gradients. Annals of the Missouri Botanical Garden 75:1-34. [ Links ]
Gentry, A. H. 1995. Diversity and floristic composition of neotropical dry forests. In Seasonally dry tropical forests, A. H. Gentry, H. A. Mooney y E. Medina (eds.). Cambrige University Press, New York. p. 146-194. [ Links ]
Gillespie, T., A. Grijalva y C. Farris. 2000. Diversity, composition, and structure of tropical dry forests in Central America. Plant Ecology 147:37-47. [ Links ]
González, O. J. y D. R. Zak. 1996. Tropical dry forests of St. Lucia, West Indies: vegetation and soil properties. Biotropica 28:618-626. [ Links ]
Hammer, Ø. 2012. PAST. Paleontological statistics, version 2.17. Reference Manual. 60 p. [ Links ]
Inifap (Instituto Nacional de Investigaciones Forestales y Agropecuarias) y Conabio (Comisión Nacional para el Conocimiento y Uso de la Biodiversidad). 1995. Edafología. http://www.conabio.gob.mx/informacion/gis/; última consulta: 20.XI.2013. [ Links ]
Kapos, V. 1986. Dry limestone forests of Jamaica. In Forests of Jamaica, D. A. Thompson, P. K. Bretting y M. Humphreyss (eds.). The Jamaican Society of Scientists and Technologists, Kingston. p. 49-58. [ Links ]
Keel, S., A. H. Gentry y L. Spinzi. 1993. Using vegetation analysis to facilitate the selection of conservation sites in eastern Paraguay. Conservation Biology 7:66-75. [ Links ]
Lebrija-Trejos, E., J. A. Meave, L. Poorter, E. A. Pérez-García y F. Bongers. 2010. Pathways, mechanisms and predictability of vegetation change during tropical dry forest succession. Perspectives in Plant Ecology, Evolution and Systematics 12:267-275. [ Links ]
Lebrija-Trejos, E., E. A. Pérez-García, J. A. Meave, L. Poorter y F. Bongers. 2011. Environmental changes during secondary succession in a tropical dry forest in Mexico. Journal of Tropical Ecology 27:477-489. [ Links ]
Li, X., Y. Nie, X. Song, R. Zhang y G. Wang. 2011. Patterns of species diversity and functional diversity along the south to north-facing slope gradient in a sub-alpine meadow. Community Ecology 12:179-187. [ Links ]
Lott, E. J., S. H. Bullock y J. A. Solis-Magallanes. 1987. Floristic diversity and structure of upland and arroyo forests of coastal Jalisco. Biotropica 19:228-235. [ Links ]
Lott, E. J. y T. H. Atkinson. 2006, Mexican and Central American seasonally dry tropical forests: Chamela-Cuixmala, Jalisco, as a focal point for comparison. In Plant diversity, biogeography, and conservation, R. T. Pennington, G. P. Lewis y J. A. Ratters (eds.). Taylor and Francis, Boca Raton. p. 315-342. [ Links ]
Magurran, A. E. 2004. Measuring biological diversity. Blackwell, Oxford. 256 p. [ Links ]
Martínez-Cruz, J. M., M. Méndez-Toribio, J. Cortés-Flores, P. Coba y G. Ibarra-Manríquez. 2013. Estructura y diversidad de los bosques estacionales desaparecidos por la construcción de la presa Gral. Francisco J. Múgica, en la Depresión del Balsas, Michoacán, México. Revista Mexicana de Biodiversidad 84:1216-1234. [ Links ]
Martínez-Yrízar, A., J. Sarukhán, A. Pérez-Jiménez, E. Rincón, J. M. Maass, A. Solis-Magallanes y L. Cervantes. 1992. Above-ground phytomass of a tropical deciduous forest on the coast of Jalisco, Mexico. Journal of Tropical Ecology 8:87-96. [ Links ]
Martínez-Yrízar, A., J. M. Maass, L. A. Pérez-Jiménez y J. Sarukhán. 1996. Net primary productivity of a tropical deciduous forest ecosystem in western Mexico. Journal of Tropical Ecology 12:169-175. [ Links ]
Martínez-Yrízar, A., A. Búrquez, M. Maass, R. Robichaux y D. Yetman. 2000. Structure and functioning of tropical deciduous forest in western Mexico. In The tropical deciduous forest of Alamos. Biodiversity of a threatened ecosystem in Mexico, R. H. Robichaux y D. A. Yetmans (eds.). University of Arizona, Tucson. p. 19-35. [ Links ]
McGill, B. J., B. J. Enquist, E. Weiher y M. Westoby. 2006. Rebuilding community ecology from functional traits. Trends in Ecology and Evolution 21:178-185. [ Links ]
McLaren, K. P., M. A. McDonald, J. B. Hall y J. R. Healey. 2005. Predicting species response to disturbance from size class distributions of adults and saplings in a Jamaican tropical dry forest. Plant Ecology 181:69-84. [ Links ]
Miranda, F. 1947. Estudios sobre la vegetación de México. V. Rasgos de la vegetación en la cuenca del río Balsas. Revista de la Sociedad Mexicana de Historia Natural 8:95-114. [ Links ]
Miranda, F. y E. Hernández. 1963. Los tipos de vegetación de México y su clasificación. Boletin de la Sociedad Botánica de México 28:29-179. [ Links ]
Morrone, J. 2005. Hacia una síntesis biogeográfica de México. Revista Mexicana de Biodiversidad 76:207-252. [ Links ]
Mueller-Dombois, D. y H. Ellenberg. 1974. Aims and methods of vegetation ecology. John Wiley and Sons, New York. 547 p. [ Links ]
Murphy, P. G. y A. E. Lugo. 1986. Structure and biomass of a subtropical dry forest in Puerto Rico. Biotropica 18:89-96. [ Links ]
Nava, R., C. Jiménez, M. Sánchez y A. Jiménez. 1998. Listado florístico de la cuenca del río Balsas, México. Polibotánica 9:1-151. [ Links ]
Olson, D. y E. Dinerstein. 2002. The global 2000: priority ecoregions for global conservation. Annals of the Missouri Botanical Garden 89:199-224. [ Links ]
Pavoine, S. y M. B. Bonsall. 2011. Measuring biodiversity to explain community assembly: a unified approach. Biological Reviews 86:792-812. [ Links ]
Pérez-García, E. A. y J. A. Meave. 2004. Heterogeneity of xerophytic vegetation of limestone outcrops in a tropical deciduous forest region in southern México. Plant Ecology 175:147-163. [ Links ]
Pérez-García, E. A., J. A. Meave, J. L. Villaseñor, J. A. Gallardo-Cruz y E. E. Lebrija-Trejos 2010. Vegetation heterogeneity and life-strategy diversity in the flora of the heterogeneous landscape of Nizanda, Oaxaca, Mexico. Folia Geobotanica 45:143-161. [ Links ]
Pérez-García, E. A., J. A. Meave y S. R. S. Cevallos-Ferriz. 2012. Flora and vegetation of the seasonally dry tropics in Mexico: origin and biogeographical implications. Acta Botanica Mexicana 100:149-193. [ Links ]
Phillips, O. y J. S. Miller. 2002. Global patterns of plant diversity: Alwyn H. Gentry's forest transect data set. Monographs in Systematic Botany from the Missouri Botanical Garden 89:1-319. [ Links ]
Pineda-García, F., L. Arredondo-Amezcua y G. Ibarra-Manríquez. 2007. Riqueza y diversidad de especies leñosas del bosque tropical caducifolio El Tarimo, cuenca del Balsas, Guerrero. Revista Mexicana de Biodiversidad 78:129-139. [ Links ]
Reich, R., C. Bonham, C. Aguirre-Bravo y M. Chazaro-Basañeza. 2010. Patterns of tree species richness in Jalisco, Mexico: relation to topography, climate and forest structure. Plant Ecology 210:67-84. [ Links ]
Rico-Gray, V., J. García-Franco, A. Puch y P. Sima. 1988. Composition and structure of a tropical dry forest in Yucatán, Mexico. International Journal of Ecology and Environmental Sciences 14:21-29. [ Links ]
Robert, A. y M. Marie-Agnès. 2003. Topographic variation and stand heterogeneity in a wet evergreen forest of India. Journal of Tropical Ecology 19:697-707. [ Links ]
Rocha-Loredo, A. G., N. Ramírez-Marcial y M. González-Espinosa. 2010. Riqueza y diversidad de árboles del bosque tropical caducifolio en la Depresión Central de Chiapas. Boletín de la Sociedad Botánica de México 87:89-113. [ Links ]
Rodríguez-Jiménez, C., R. Fernández-Nava, M. L. Arreguín-Sánchez y A. Rodríguez-Jiménez. 2005. Plantas vasculares endémicas de la cuenca del río Balsas, México. Polibotánica 20:73-99. [ Links ]
Ruiz, J., M. C. Fandino y R. L. Chazdon. 2005. Vegetation structure, composition, and species richness across a 56-year chronosequence of dry tropical forest on Providencia Island, Colombia. Biotropica 37:520-530. [ Links ]
Rzedowski, J. 1978. Vegetación de México. Limusa, México, D. F. 432 p. [ Links ]
Rzedowski, J. 1991. Diversidad y orígenes de la flora fanerogámica de México. Acta Botanica Mexicana 14:3-21. [ Links ]
Rzedowski, J., R. Medina-Lemos y G. Calderón-de Rzedowski. 2005. Inventario del conocimiento taxonómico, así como de la diversidad y del endemismo regionales de las especies mexicanas de Bursera (Burseraceae). Acta Botanica Mexicana 70:85-111. [ Links ]
Rzedowski, J. y G. Calderón-de Rzedowski. 2013. Datos para la apreciación de la flora fanerogámica del bosque tropical caducifolio de México. Acta Botanica Mexicana 102:1-23. [ Links ]
Salas-Morales, S. H. 2002. Relaciones entre la heterogeneidad ambiental y la variabilidad estructural de las selvas tropicales secas de la costa de Oaxaca, México. Tesis, Fac. de Ciencias, Universidad Nacional Autónoma de México. México, D. F. 101 p. [ Links ]
Segura, G., P. Balvanera, E. Durán y A. Pérez. 2002. Tree community structure and stem mortality along a water availability gradient in a Mexican tropical dry forest. Plant Ecology 169:259-271. [ Links ]
Sousa, M. 2010. Centros de endemismo: las leguminosas. In Diversidad, amenazas y áreas prioritarias para la conservación de las selvas secas del Pacífico de México, G. Ceballos, L. Martínez, A. García, E. Espinoza, J. Bezaury y R. Dirzo (eds.). Fondo de Cultura Económica, México, D. F. p. 77-91. [ Links ]
Trejo, I. 2005, Análisis de la diversidad de la selva baja caducifolia en México. In Sobre diversidad biológica: el significado de las diversidades alfa, beta y gamma, G. Halffter Salas, J. Soberon, P. Koleff y A. Melic (eds.). m3m-Monografías Tercer milenio, Sociedad Entomológica Aragonesa, Zaragoza/Conabio/Grupo Diversitas-México/ Conacyt, México, D. F. p. 111-122. [ Links ]
Trejo, I. y R. Dirzo. 2002. Floristic diversity of Mexican seasonally dry tropical forests. Biodiversity and Conservation 11:2063-2084. [ Links ]
Warren, R. J. 2008. Mechanisms driving understory evergreen herb distributions across slope aspects: as derived from landscape position. Plant Ecology 198:297-308. [ Links ]
Warren, R. J. 2010. An experimental test of well-described vegetation patterns across slope aspects using woodland herb transplants and manipulated abiotic drivers. New Phytologist 185:1038-1049. [ Links ]
White, D. A. y C. S. Hood. 2004. Vegetation patterns and environmental gradients in tropical dry forests of the northern Yucatan peninsula. Journal of Vegetation Science 15:151-160. [ Links ]














