Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Boletín médico del Hospital Infantil de México
versión impresa ISSN 1665-1146
Bol. Med. Hosp. Infant. Mex. vol.65 no.6 México nov./dic. 2008
Aspectos clínicos
El papel actual del tratamiento quirúrgico. ¿Puede la cirugía curar enfermedades metabólicas?
Present role of surgical treatment. Can surgery cure metabolic diseases?
Federico López, Miguel F. Herrera
Departamento de Cirugía, Instituto Nacional de la Nutrición Salvador Zubirán, México, D. F., México.
Solicitud de sobretiros:
Dr. Miguel F. Herrera, Departamento de Cirugía,
Instituto Nacional de la Nutrición Salvador Zubirán,
Vasco de Quiroga Núm. 15, Deleg. Tlalpan,
CP. 14000, México, D. F., México.
Fecha de recepción: 08-09-2008.
Fecha de aprobación: 09-10-2008.
Resumen
La epidemia global coloca a la obesidad como un problema de salud serio tanto en niños como en adultos. Es bien conocido el hecho de que la obesidad incrementa el riesgo de padecer diversas enfermedades, dentro de las que destacan la diabetes mellitus tipo 2 y el síndrome metabólico. La prevalencia de este síndrome en la población de obesos en edad pediátrica es de 4-2% y llega a ser hasta de 50% en los adolescentes con obesidad extrema. La cirugía bariátrica permite una pérdida durable de hasta 75 % del exceso de peso y también es una herramienta efectiva para mejorar varios aspectos del síndrome metabólico. El impacto de la cirugía bariátrica sobre las diversas comorbilidades es dramático. Se ha demostrado mejoría o resolución de la diabetes en 72 a 76% de los pacientes, destacando el hecho de que dicha mejoría se presenta incluso antes de que ocurra una pérdida importante de peso. Probablemente la cirugía bariátrica impacte directamente el eje entero-insular. Se investiga la conveniencia de realizar cirugía bariátrica en pacientes con diabetes mellitus a pesar de que su índice de masa corporal (IMC) sea menor a 35 kg/m2. El tratamiento de la obesidad mórbida mediante cirugía se ha extendido a la población de adolescentes en un afán de prevenir complicaciones y se han diseñado recomendaciones específicas.
Palabras clave: Cirugía bariátrica, síndrome metabólico; obesidad.
Abstract
There has been a dramatic increase in the prevalence of obesity worldwide in both children and adults. It is well known that obesity leads to an increased risk of complications such as type 2 diabetes and the metabolic syndrome. The prevalence of this syndrome in the obese population of children is 4.2% and it increases up to 50% in morbidly obese adolescents. Bariatric surgery has shown a long lasting excess weight loss of 75%, and a positive impact in the resolution or improvement of many metabolic syndrome parameters. Type 2 diabetes is controlled in 72 to 76% of patients after surgery and it has been recognized that improvement occurs even before a significant weight loss is achieved. An effect on the entero-insular axis has been proposed as a mechanism for metabolic control. Based on the dramatic impact of bariatric surgery on the metabolic syndrome, some authors have proposed to perform bariatric surgery in patients with type 2 diabetes and a BMI <35 kg/m2. Indications for bariatric surgery have been extended to adolescents and some specific guidelines have been developed.
Key words: Surgery, bariatric; metabolic disease; obesity.
La epidemiología de la obesidad
La epidemia global de la obesidad constituye un problema médico serio.1 Su prevalencia y gravedad ha aumentado de forma dramática en las últimas tres décadas, tanto en adultos como en niños. La Encuesta Nacional de Salud en México 2000 mostró una prevalencia de sobrepeso en adolescentes de 10 a 19 años de 16.8% en hombres y 22.7% en mujeres, y una prevalencia de obesidad de 9.1% en hombres y 10.6% en mujeres;2 la prevalencia de la obesidad en escolares puede llegar a ser hasta de 38% según el área geográfica estudiada.3 El problema del incremento dramático de la obesidad en niños y adolescentes necesariamente se traducirá en aumento de la prevalencia y gravedad de la obesidad en la siguiente generación de adultos, porque los adolescentes obesos tienen una probabilidad muy elevada de permanecer obesos en la edad adulta.4
En los pacientes obesos, es bien conocido el incremento de riesgo de padecer diabetes mellitus tipo 2 (DM2), intolerancia a la glucosa, hipertensión arterial, dislipidemia, osteoartrosis, apnea del sueño y otras comorbilidades. La asociación entre hipertensión, dislipidemia, obesidad central e intolerancia a la glucosa es conocida como síndrome metabólico. La obesidad en la edad pediátrica provoca daño endotelial progresivo y crónico, que puede condicionar el desarrollo de aterosclerosis. Algunos marcadores de riesgo cardiovascular como lo son la proteína C reactiva, leptina y niveles bajos de adiponectina se han encontrado en esta población;5 por lo tanto, la obesidad es una enfermedad que pone en peligro la vida. Existe una relación dosis-respuesta entre el índice de masa corporal (IMC) durante la juventud y el riesgo de muerte precoz, con una reducción en los años de vida en pacientes con obesidad extrema de 20, 13, 5 y 8 años en hombres afro-americanos, caucásicos, mujeres caucásicas y afroamericanas respectivamente. Es muy importante reconocer que la pérdida de entre 5 y 10% del peso corporal, resulte en mejora importante tanto del riesgo de muerte como de las comorbilidades.6
Síndrome metabólico
El diagnóstico de síndrome metabólico en adultos se basa en lo establecido por el panel del programa educativo nacional de colesterol en el adulto III (NCEP-ATPIII por sus siglas en inglés) así como por la Federación Internacional de Diabetes (IDF). Se requieren tres de las siguientes cinco características para establecer el diagnóstico:1,6
1. Obesidad abdominal con una circunferencia de cintura de más de 102 cm en hombres y 88 cm en mujeres.
2. Concentración de triglicéridos >150 mg/dL.
3. Niveles de colesterol HDL <40 mg/dL en hombres y <50 mg/dL en mujeres.
4. Tensión arterial ≥130/85 mm Hg.
5. Glucosa en ayuno ≥110 mg/dL.
En la población pediátrica no existe una definición formal de síndrome metabólico, pero al utilizar los criterios empleados en adultos, la prevalencia de éste en adolescentes entre 12 y 19 años de edad es de 4.2%.6 Utilizando los criterios de Weiss, cerca de 50% de los adolescentes con obesidad extrema tiene síndrome metabólico.7 Aún existe controversia en la población pediátrica acerca de si esta entidad constituye un riesgo a la salud mayor que la suma de sus partes.6
El síndrome metabólico no es la única consecuencia metabólica de la obesidad. También lo son la apnea del sueño y el síndrome de ovarios poliquísticos. Cada entidad se desarrolla como consecuencia de una interacción pobremente entendida entre predisposición genética, factores adquiridos y ambientales.8
Tratamiento quirúrgico
La cirugía bariátrica permite una pérdida durable hasta de 75% del exceso de peso. También es una herramienta efectiva para mejorar varios aspectos del síndrome metabólico como lo son la hitólerancia a la glucosa, la hipertensión arterial y la dislipidemia. Esta mejoría o corrección generalmente se relaciona con la reducción en la masa de tejido adiposo visceral, sin embargo, procedimientos como la derivación gastroyeyunal o la derivación biliopancreática estimulan la secreción de incretinas por medio de la exposición temprana de los alimentos al íleon. La pérdida de peso lograda por la cirugía disminuye la mortalidad global y reduce el riesgo relativo de muerte de forma importante en comparación con pacientes no tratados (riesgo relativo de 0.11 reportado en un estudio canadiense), lo cual se traduce en una reducción de 89% si se mantiene una pérdida sostenida de peso igual o mayor a 67%.9JC
En el consenso de los Institutos Nacionales de Salud de los Estados Unidos de Norteamérica (EUA) (NIH) acerca de la cirugía gastrointestinal para el tratamiento de la obesidad, se reconoció la importancia de las condiciones comórbidas asociadas a la obesidad y se propuso una disminución en el IMC recomendado para cirugía, con la finalidad de que pacientes con IMC >35 kg/m2, en los que además existe una o más comorbilidades asociadas a la obesidad como lo son la DM2, hipertensión arterial, enfermedad coronaria o apnea obstructiva del sueño, pudieran beneficiarse de este tipo de tratamiento. En un consenso más reciente organizado por la Asociación Americana de Cirugía Bariátrica y Metabólica (ASMBS) se sugirió la liberación en los criterios disminuyendo el umbral de IMC a 30 kg/m2 en presencia de comorbilidades severas.11
Los procedimientos de cirugía bariátrica se dividen en tres variedades: restrictivos, malabsortivos y mixtos. La eficacia y seguridad de cada uno varía importantemente.
Procedimientos restrictivos
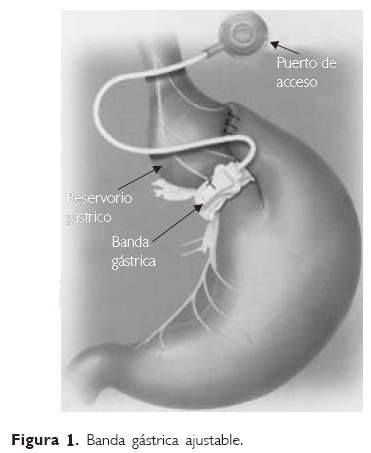
Los procedimientos restrictivos inducen la pérdida de peso por medio de la combinación de un reservorio gástrico pequeño con una desembocadura estrecha limitando la ingesta oral y produciendo saciedad precoz. Entre estos procedimientos se encuentra la gastroplastia vertical con banda (GVB), usada ampliamente en la década de los años ochenta pero prácticamente en desuso en la actualidad; y la banda gástrica ajustable (BGA). Este último procedimiento consiste en una banda de silicon que se coloca envolviendo la porción superior del estómago inmediatamente distal a la unión gastroesofágica, la cual se conecta a un puerto de colocación subcutánea que permite realizar ajustes en la luz del estómago al inyectar mayor o menor cantidad de agua en el interior de la banda (Fig. 1).
Procedimientos malabsortivos
Los procedimientos malabsortivos consiguen la pérdida de peso por medio de la desviación de los nutrientes directamente al íleon terminal; incluyen la realización de una gastrectomía parcial para inducir cierto efecto de saciedad inicial y de una derivación intestinal, realizada de tal forma que el proceso de absorción se lleve a cabo solamente en un segmento de íleon de aproximadamente 50 cm. En la actualidad se realizan dos procedimientos de este tipo: la derivación biliopancreática convencional (DBP) y la acompañada de "switch duodenal" (Fig. 2).

En general, hay pobre aceptación para estos procedimientos tanto por su complejidad técnica, particularmente cuando se elige la técnica laparoscópica para pacientes con un IMC superior a 50 kg/m2, como por la frecuencia elevada de efectos adversos como lo son diarrea, flatulencia, anemia y desmineralización ósea.
Procedimientos mixtos
Los procedimientos mixtos consisten en una combinación de los dos previos, ya que tienen tanto efectos restrictivos como malabsortivos. La derivación gastroyeyunal por laparoscopia (Bypass gástrico en Y de Roux [DGY]) es el prototipo y el procedimiento con mayor aceptación dentro de la cirugía bariátrica (Fig. 3). El efecto mixto de este procedimiento se logra al combinar un reservorio gástrico pequeño, cuyo volumen es aproximadamente de 15 a 30 mL y se construye en lacurvatura menor del estómago y una anastomosis gastroyeyunal en Y de Roux. La longitud habitual del asa alimentaria es entre 70 y 150 cm y la del asa biliopancreática entre 20 y 50 cm. Al añadir longitud al asa alimentaria se incrementa al grado de malabsorción, lo cual repercute en una mayor pérdida ponderal, pero también incrementa el riesgo de anormalidades nutricionales y metabólicas. Aunque el mecanismo de acción de esta operación no está completamente comprendido, se aceptan en general los siguientes efectos:12

1. El reservorio gástrico pequeño con una desembocadura estrecha, permite que el paciente experimente saciedad con una cantidad pequeña de alimento y que ésta perdure por tiempo prolongado.
2. La operación condiciona cierto grado de malabsorción por la separación de los alimentos y de las secreciones biliopancreáticas en aproximadamente la tercera parte de la longitud del intestino. El grado de malabsorción está determinado por la longitud de esta asa común.
3. La derivación impide la ingestión de alimentos ricos en carbohidratos, al favorecer el desarrollo de síndrome de "Dumping". Este síndrome está ocasionado por el paso rápido de azúcares simples y de alimentos con una os-molaridad elevada del reservorio al asa alimentaria, lo que provoca síntomas como diaforesis, taquicardia, náusea, debilidad y mareo, entre otros, dando lugar a una sensación desagradable y trayendo como consecuencia evitar la ingesta de dulces.
4. Existen sin duda diversos mecanismos hormonales secundarios a la derivación en sí. Cummings y col.13 demostraron que los niveles séricos de ghrelina se encuentran disminuidos de forma importante después de la DGY. La ghrelina es una hormona orexigénica secretada principalmente por el estómago y el duodeno que estimula la ingesta calórica. Esta hormona participa en la regulación a largo plazo del peso corporal, por lo que sus niveles se incrementan con la pérdida de peso secundaria a dieta. La DGY reduce la secreción de ghrelina al excluir a las células productoras de la hormona del contacto directo con el alimento, estímulo que regula su secreción en forma habitual.8,9
La pérdida de peso es variable y depende en parte del comportamiento del paciente después de la cirugía. Esta pérdida de peso ocurre principalmente durante los primeros 6 a 12 meses de la operación. Después de este tiempo, el peso tiende a estabilizarse. El apetito, que se encuentra bastante disminuido durante el primer año, tiende a regresar a lo habitual después de este período y por ello es importante que el paciente logre una modificación substancial de sus hábitos en el transcurso de los primeros dos años.
En general, los pacientes pierden entre la mitad y las tres cuartas partes de su exceso de peso. De acuerdo con un meta-análisis de Buchwald y col.,14 el porcentaje promedio de pérdida de exceso de peso con la DGY es de 68.2%.
Por otra parte, Sjostrom y col.,15,16 en su estudio a 10 años, observaron una pérdida de 38% del peso corporal al año de la cirugía. Con el tiempo, los pacientes ganaron una pequeña cantidad de peso manteniendo una pérdida de 25 ± 11% del peso corporal a 10 años. Los resultados de la DGY fueron mejores que los de la BGA, cuya pérdida de peso a 10 años fue de 14 ± 4% y que los de un grupo control con tratamiento médico que incluso ganó entre 1.6 ± 12% de peso.
La DGY se realizó por vía laparoscópica por primera vez en 1994 y desde su inicio, en un ensayo clínico controlado realizado por Nguyen y col.,17 se demostraron los beneficios de este abordaje incluyendo una recuperación más rápida con una estancia hospitalaria más corta, menor alteración de la función pulmonar, menor dolor postoperatorio y una incidencia menor de complicaciones relacionadas a la herida quirúrgica.9
Impacto de la cirugía bariátrica en el control de la DM2 y del síndrome metabólico en pacientes obesos
La cirugía bariátrica ha demostrado ser el método más efectivo para el tratamiento de la obesidad extrema. Diversos procedimientos han demostrado inducir una pérdida significativa de peso a largo plazo y un gran impacto, tanto en el control de las comorbilidades como en la mejoría de la calidad de vida. La cirugía bariátrica puede realizarse en la actualidad con una morbimortalidad muy baja. El impacto de la cirugía bariátrica sobre las comorbilidades es un importante tópico de investigación.9,18,19 Sjostrom y col.,15,16 en un estudio que analizó 4 047 pacientes obesos, de los cuales 2 010 fueron tratados mediante cirugía bariátrica y el resto se utilizó como un grupo control bajo tratamiento médico, demostraron que la pérdida de peso inducida por cirugía, condicionó control de la DM2 en 72% de los pacientes a dos años y en 36%, 10 años después de la intervención. Al comparar los resultados del tratamiento quirúrgico con los del grupo control, encontraron que no solo la pérdida de peso fue significativamente superior, sino que los pacientes intervenidos quirúrgicamente tuvieron también un mejor control de los diversos fenómenos comórbidos incluyendo la DM2.
En el meta-análisis de Buchwald y col.14 se documentó resolución de la DM2 en 76.8% de los casos (95% IC, 70.7-82.9%) y resolución o mejoría de la DM2 en 86%. Al desglosar la resolución de acuerdo con el tipo de cirugía realizada, se observó una resolución de 98.9% con la DBP, de 83.7% con la DGY, de 71% con la GVB y de 47.9% con la BGA.
Se ha visto que la duración de la diabetes es un factor importante en la factibilidad del control glucémico después de la cirugía. Una duración menor de la enfermedad preserva de mejor forma la masa de células β y por ello facilita el control de la diabetes.20 Otros estudios han evaluado y confirmado que la resolución de la DM2 es más factible en pacientes cuya enfermedad se controla con hipoglucemiantes orales, que tiene una duración menor a cinco años y que consiguen una pérdida de peso mayor. Estos factores aplican también en adolescentes.4,6,8 Acorde con el impacto de la cirugía bariátrica sobre el control de la DM2, se ha demostrado que la cirugía bariátrica condiciona resolución de la resistencia a la insulina en alrededor de 96% de los pacientes, a quienes de manera específica se les realiza una DGY.
Un hecho de observación ha sido que el control de la DM2 y la resistencia a la insulina posterior a algunos tipos de cirugía bariátrica se presentan en forma rápida, incluso antes de que ocurra una pérdida importante de peso. Dentro de los mecanismos propuestos para esta mejoría se encuentran los siguientes: durante la fase de ayuno del postoperatorio inmediato se inicia una fase de resolución de la glucotoxicidad inducida por ayuno, que trae consigo una mejoría en la resistencia a la insulina. Conforme pasan los días después de una intervención quirúrgica, se reinicia la vía oral en forma gradual pero los pacientes continúan en un estado de balance energético negativo lo que disminuye la glucotoxicidad y mejora la función de las células (3. La pérdida de peso, junto con el aumento en la actividad física y la disminución en la carga oral de glucosa, condicionan el control de la enfermedad. También se han demostrado cambios en diversos péptidos reguladores de la secreción de insulina.
Se ha propuesto que la cirugía bariátrica impacta de manera importante el eje entero-insular. Existen diversos componentes de mucha importancia en este eje. Las incretinas, dentro de las que destacan el péptido insulinotrópico dependiente de glucosa, también conocido como péptido inhibitorio gástrico (GIP) y el péptido similar al glucagón 1 (GLP-1) son secretagogos de insulina. El GIP es secretado por las células K del duodeno mientras que el GLP-1 es secretado por las células L del íleon terminal y el colon. Juntas, son responsables de 40-50% de la secreción de insulina postprandial y ambas exhiben efectos tróficos sobre las células β. Una de las alteraciones que se ha encontrado en pacientes con DM2 es un defecto en las vías de señalización celular, lo que provoca un efecto atenuado del GIP. Este defecto parece ser secundario a una expresión disminuida del receptor de este péptido (GIPR). Por lo tanto, se cree que en sujetos obesos susceptibles, la estimulación crónica y exagerada del intestino proximal con carbohidratos y grasas, inducen una expresión alterada del GIPR o una alteración en la interacción GIP/GIPR, lo que condiciona los niveles elevados de GIP que se observan en pacientes obesos con DM2. Otra de las incretinas involucradas son el péptido YY (PYY), secretado por las células L, que junto con el GLP-1 funciona como un "freno ileal" al disminuir el vaciamiento gástrico y prolongar el tránsito intestinal. Finalmente la ghrelina, además de su efecto orexigénico, inhibe la secreción de insulina, altera la sensibilidad de la insulina, bloquea la liberación de adiponectinas y estimula la secreción de hormona del crecimiento.8,21,22
De esta forma, los cambios en el eje entero-insular, posterior a un procedimiento mixto o malabsortivo, ocurren por dos mecanismos:
1. La mucosa secretora de la mayor parte del estómago, duodeno y yeyuno del asa biliopancreática excluida, permanece sin estímulo por la ausencia de alimento.
2. La mucosa secretora del íleon terminal se estimula en forma excesiva por la presencia de alimentos digeridos de forma incompleta. Esto provoca una activación incrementada de las células L.
Dichas alteraciones traen consigo cambios en los patrones de secreción de las incretinas como lo son aumento en la secreción de GLP-1 y PYY por las células L y disminución en la secreción de ghrelina, lo que al final incrementa la sensibilidad a la insulina. Otra alteración secundaria a la exclusión de la mucosa del asa biliopancreática de los alimentos consiste en la normalización de los niveles del GIP, lo que trae como consecuencia un incremento en la sensibilidad a la insulina. Estos cambios se presentan de manera precoz, entre la primera y la cuarta semana después de la operación.21-23
En cuanto a la hipertensión arterial, en la mayoría de los estudios se observa que es uno de los fenómenos comórbidos que mejora de manera altamente significativa después de una cirugía bariátrica. En el estudio de Sjostrom y col.15 se observó resolución de la hipertensión en 34% de los pacientes a los dos años, persistente en 19% a 10 años después de la intervención. En el meta-análisis de Buchwald y col.,14 se observó resolución de la hipertensión en 61.7% (95% IC, 55.6-67.8%) de los pacientes intervenidos quirúrgicamente. La resolución por grupos fue de 43.2% con la BGA, de 67.5% con la DGY y de 83.4% con la DBP; y en otro estudio en el que se analizaron más de 1 000 pacientes tratados mediante DGY, se demostró resolución de la hipertensión en 69% de los enfermos dos años después de la cirugía, persistente en 51% en la evaluación a 10 años.24
Finalmente, en lo que se refiere al metabolismo de los lípidos, se sabe que existe repercusión positiva de la cirugía bariátrica en algunos de los parámetros de manera específica. Por ejemplo, en el estudio de Sjostrom y col.,16 se observó resolución de la hipertrigliceridemia en 62% de los pacientes a dos años y de 46% a los 10 años de la intervención así como un incremento en los niveles de colesterol HDL en 76 y 73% de los pacientes a 2 y 10 años de la operación respectivamente. Hubo resolución de la hipercolesterolemia en 22% de los enfermos a dos años, manteniéndose en 21% a 10 años, lo que no tuvo diferencia significativa en comparación con el grupo control de tratamiento médico.
En el meta-análisis de Buchwald y col.,14 se observó mejoría o resolución de la hipertrigliceridemia en 82.4% de los casos (77% con BGA, 91.2% con DGY y 100% con DBP); y de la hipercolesterolemia en 71.3 % de los pacientes (78% con BGA, 94.9% con DGY y 87.2% con DBP).15,24 En el cuadro 1 se resumen algunos de estos datos así como los correspondientes a otros estudios.25,30
Con la finalidad de lograr un mayor impacto de la cirugía sobre el síndrome metabólico, se han realizado algunas modificaciones a los procedimientos quirúrgicos empleados para el control de peso. Un ejemplo es reducir la grasa visceral por medio de omentectomía, ya que en diversos estudios se ha observado que la acumulación de tejido adiposo visceral es un factor de riesgo independiente para el desarrollo de comorbilidades asociadas a la obesidad. Thórne y col.,31 en un estudio de 50 pacientes a quienes se les colocó una BGA, evaluaron los efectos de la omentectomía en 25. Encontraron una pérdida de peso discretamente mayor en el grupo de BGA + omentectomía y en este grupo también existió mejoría del perfil metabólico. En otro estudio realizado en nuestra Institución, se comparó la DGY + omentectomía contra DGY en 22 pacientes. Encontramos que no hubo diferencias significativas entre los grupos, tanto en los parámetros clínicos del síndrome metabólico como en el patrón de las adipocinas. Estos resultados se encuentran en vías de publicación.
Cirugía bariátrica para pacientes con síndrome metabólico o DM2 e IMC menor a 35 kg/m2
Con base en la dramática respuesta del síndrome metabólico en pacientes con obesidad mórbida,18 y el hecho de que los efectos de la operación se observan antes de que exista una pérdida significativa de peso,19 se ha propuesto la conveniencia de tratar quirúrgicamente a pacientes con un IMC menor a 35 kg/m2. En animales de experimentación se ha demostrado que la transposición ileal da lugar a mejoría en la tolerancia a la glucosa sin afectar el peso o la ingesta calórica.32 DePaula y col.19 publicaron los resultados de una gastrectomía en manga asociada a interposición ileal en pacientes con DM2 y obesidad extrema, observando resolución completa de la DM2. Posteriormente, los autores realizaron otro estudio en 39 pacientes con DM2 con IMC <35 kg/m2. Realizaron dos variantes de la técnica; en una, hicieron únicamente interposición ileal asociada a gastrectomía en manga mientras que en la otra agregaron un "switch duodenal" a la interposición ileal. Los procedimientos fueron diseñados para el tratamiento de DM2 al exponer en forma precoz el segmento de íleon interpuesto a los nutrientes, permitiendo con ello un aumento en la secreción de incretinas. La gastrectomía en manga permite lograr una restricción calórica. La variante con "switch duodenal" permite abolir la excesiva estimulación duodenal por los nutrientes logrando un mejor control de los niveles del GIP. Los autores encontraron resolución de la DM2 en 86.9% de los pacientes (definido por un nivel de hemoglobina glucosilada [HbAlc] menor a 7%) y niveles de HbAlc menor de 6% en 47.4%. En cuanto a las otras comorbilidades, se demostró resolución de la HAS en 83.3%, niveles de colesterol LDL <100 mg/dL en 66%, niveles de triglicéridos < 150 mg/dL en 71% y niveles de colesterol HDL >40 mg/dL en 81.2% de los pacientes en un seguimiento promedio de siete meses. La morbilidad del procedimiento fue de 10.3% y la mortalidad de 2.6%.19
Scopinaro y col.18 realizaron DBP a siete pacientes logrando resolución de la DM2, hipercolesterolemia e hipertrigliceridemia en todos los enfermos y resolución de la HAS en seis de ellos en un período de tres años. Cohen y col.33 realizaron DGY a 37 pacientes con IMC <35 (media de 32.5 kg/m2), DM2, HAS y dislipidemia, logrando resolución de la DM2 y la dislipidemia en todos los pacientes así como la resolución de la HAS en todos menos en un paciente, en un período de seguimiento entre 6 y 48 meses.
Cirugía bariátrica en adolescentes
En las guías de los Institutos Nacionales de Salud de los EUA para la cirugía bariátrica, no se incluyeron recomendaciones para los adolescentes obesos, probablemente por el desconocimiento del comportamiento que esta población de pacientes pudiera tener. Dentro de las peculiaridades que dificultan la decisión terapéutica en esta población están:
1. Las comorbilidades asociadas a la obesidad extrema en adolescentes son menos avanzadas que en los adultos.
2. El impacto a largo plazo de la pérdida de peso y la malabsorción en el desarrollo físico en esta población no está completamente caracterizado.
3. Las técnicas quirúrgicas en cirugía bariátrica están evolucionando rápidamente, por lo que se pueden esperar procedimientos menos invasivos y con menor riesgo en el futuro.
4. Los adolescentes pueden tener una susceptibilidad distinta a los efectos nutricionales de un procedimiento mixto o malabsortivo, además de que pueden ser menos aptos en cumplir con las guías nutricionales postoperatorias de por vida.
5. No existen datos en los adolescentes que demuestren que la pérdida de peso inducida por cirugía, mejore la mortalidad temprana que experimentan los individuos con obesidad extrema.
En 2004 la Asociación Americana de Cirugía Pediátrica y la ASMBS crearon recomendaciones específicas para la cirugía bariátrica en adolescentes. Se recomendó realizar cirugía bariátrica en los pacientes adolescentes que cumplieran las siguientes condiciones:
1. Falla a tratamiento médico intenso durante por lo menos seis meses.
2. Tanner IV.
3. Obesidad extrema (IMC >40) con comorbilidades severas u obesidad con IMC >50, incluso sin comorbilidades.
4. Evaluación médica y quirúrgica preoperatoria completa.
5. Capacidad y disposición a seguir las guías nutricionales postoperatorias y acudir a revisiones médicas periódicas.
6. Capacidad suficiente para tomar decisiones y madurez psicológica para entender las implicaciones de la operación y firmar un consentimiento informado.
7. Entorno familiar comprometido y apropiado.
Se reconocieron como contraindicaciones para la cirugía el abuso de sustancias en el año previo, discapacidad médica, psiquiátrica o cognitiva, embarazo, así como incapacidad o indisposición por el paciente o su familia para entender el procedimiento, sus consecuencias médicas o imposibilidad para llevar un seguimiento de por vida.
Se ha sugerido como procedimiento de elección en esta población a la DGY por laparoscopia, ya que ha demostrado una pérdida del exceso de peso de hasta 80% al año, si el paciente cumple con el programa de dieta y ejercicio postoperatorio. Además, la pérdida de peso es durable aunque se sabe que cerca de 15% presentará ganancia de peso en la edad adulta.4,6,34
Referencias
1. Rossi M, Barretto-Ferreira da Silva R, Chaves-Alcántara Jr G, et al. Remission of metabolic syndrome: A study of 140 patients six months after Roux-en-Y gastric bypass. Obes Surg. 2008; 18: 601-6. [ Links ]
2. Marcos-Daccarett NJ, Núñez-Rocha GM, Salinas-Martinez AM, Santos-Ayarzagoitia M, Decanini-Arcaute H. Obesidad como factor de riesgo para trastornos meta-bólicos en adolescentes mexicanos, 2005. Rev Salud Publica. 2007; 9: 180-93. [ Links ]
3. Menchaca-Martín P, Zonana-Nacach A. Obesidad en niños mexicanos de la frontera norte. [Cartas al editor]. Salud Publica Mex. 2006; 48: 1. [ Links ]
4. Xanthakos SA, Daniels SR, Inge TH. Bariatric surgery in adolescents: An update. Adolesc Med Clin. 2006; 17: 589-612. [ Links ]
5. Perichart-Perera O, Balas-Nakash M, Schiffman-Selechnik E, Barbato-Dosal A, Vadillo-Ortega F. Obesity increases metabolic syndrome risk factors in school-aged children from an urban school in Mexico City. J Am Diet Assoc. 2007; 107: 81 -91. [ Links ]
6. Helmrath MA, Brandt ML, Inge TH. Adolescent obesity and bariatric surgery. Surg Clin North Am. 2006; 86: 441-54. [ Links ]
7. Weiss R, Dziura J, Burgert TS, et al. Obesity and the metabolic syndrome in children and adolescents. N Engl J Med. 2004; 350: 2362-74. [ Links ]
8. Folli F, Pontiroli AE, Schwesinger WH. Metabolic aspects of bariatric surgery. Med Clin North Am. 2007; 91: 393-414. [ Links ]
9. Kini S, Herrón DM, Yanagisawa RT. Bariatric surgery for morbid obesity - a cure for metabolic syndrome? Med Clin North Am. 2007; 91:1 255-71. [ Links ]
10. Christou NV, Sampalis JS, Liberman M, et al. Surgery decreases long-term mortality, morbidity, and health care use in morbidly obese patients. Ann Surg. 2004; 240: 416-24. [ Links ]
11. Buchwald H. Consensus Conference Panel. Bariatric surgery for morbid obesity: health implications for patients, health professionals, and third-party payers. J Am Coll Surg. 2005; 200: 593-604. [ Links ]
12. Brolin RE, LaMarca LB, Kenler HA, Cody RP. Malabsorptive gastric bypass in patients with superobesity. J Gastrointest Surg. 2002; 6: 195-205. [ Links ]
13. Cummings DE, Weigle DS, Frayo RS, et al. Plasma ghrelin levels after diet-induced weight loss orgastric bypass surgery. N Engl J Med. 2002; 346: 1623-30. [ Links ]
14. Buchwald H, Avidor Y, Braunwald E, et al. Bariatric surgery: a systematic review and meta-analysis. JAMA. 2004; 292: 1724-37. [ Links ]
15. Sjóstróm L, Lindroos AK, Peltonen M, et al. Lifestyle, diabetes, and cardiovascular risk factors 10 years after bariatric surgery. N Engl J Med. 2004; 351: 2683-93. [ Links ]
16. Sjóstróm L, Narbro K, Sjóstróm CD, et al. Effects of bariatric surgery on mortality in Swedish obese subjects. N Engl J Med. 2007; 357: 741-52. [ Links ]
17. Nguyen NT, Lee SL, Goldman C, et al. Comparison of pulmonary function and postoperative pain after lapa-roscopic versus open gastric bypass: a randomized trial. J Am Coll Surg. 2001; 192: 469-77. [ Links ]
18. Scopinaro N, Papadia F, Marinari G, Camerini G, Adami G. Long-term control of type 2 diabetes mellitus and the other major components of the metabolic syndrome after biliopancreatic diversion in patients with BMI <35 kg/m2. Obes Surg. 2007; 17: 185-92. [ Links ]
19. DePaula AL, Macedo AL, Rassi N, et al. Laparoscopic treatment of type 2 diabetes mellitus for patients with a body mass index less than 35. Surg Endose. 2008; 22: 706-16. [ Links ]
20. Pories WJ, Swanson MS, MacDonald KG, et al. Who would have thought it? An operation proves to be the most effective therapy for adult-onset diabetes mellitus. Ann Surg. 1995; 222: 339-52. [ Links ]
21. Cummings S, Apovian CM, Khaodhiar L. Obesity surgery: Evidence for diabetes prevention/management. J Am Diet Assoc. 2008; 108 (4 Suppl 1): S40-4. [ Links ]
22. Guidone C, Manco M, Valera-Mora E, et al. Mechanisms of recovery from type 2 diabetes after mal-absorptive bariatric surgery. Diabetes. 2006; 55: 2025-31. [ Links ]
23. Rubino F, Gagner M, Gentileschi P, et al. The early effect of the Roux-en-Y gastric bypass on hormones involved in body weight regulation and glucose metabolism. Ann Surg. 2004; 240: 236-42. [ Links ]
24. Kushner RF, Noble CA. Long-term outcome of bariatric surgery: an interim analysis. Mayo Clin Proc. 2006; 81 (10 Suppl): S46-51. [ Links ]
25. Alexandrides TK, Skroubis G, Kalfarentzos F. Resolution of diabetes mellitus and metabolic syndrome following Roux-en-Y gastric bypass and a variant of biliopancreatic diversion in patients with morbid obesity. Obes Surg. 2007; 17: 176-84. [ Links ]
26. Wolf AM, Beisiegel U. The effect of loss of excess weight on the metabolic risk factors after bariatric surgery in morbidly and super-obese patients. Obes Surg. 2007; 17: 910-9. [ Links ]
27. Perry CD, HutterMM, Smith DB, Newhouse JP, McNeil BJ. Survival and changes in comorbidities after bariatric surgery. Ann Surg. 2008; 247: 21 -7. [ Links ]
28. Maggard MA, Shugarman LR, Suttorp M, et al. Meta-analysis: Surgical treatment of obesity. Ann Intern Med. 2005; 142: 547-59. [ Links ]
29. Dixon JB, O'Brien PE. Changes in comorbidities and improvements in quality of life after LAP-BAND placement. Am J Surg. 2002; 184: 51S-4S. [ Links ]
30. Carvalho PS, Moreira CL, Barelli Mda C, et al. Can bariatric surgery cure metabolic syndrome? Arq Bras En-docrinol Metabol. 2007; 51: 79-85. [ Links ]
31. Thórne A, Lonnqvist F, Apelman J, Hellers G, Arner P. A pilot study of long-term effects of a novel obesity treatment: Omentectomy in connection with adjustable gastric banding. Int J Obes Relat Metab Disord. 2002; 26: 193-9. [ Links ]
32. Patriti A, Facchiano E, Annetti C, et al. Early improvement of glucose tolerance after ¡leal transposition in a non-obese type 2 diabetes rat model. Obes Surg. 2005; 15: 1258-64. [ Links ]
33. Cohen R, Pinheiro JS, Correa JL, Schiavon CA. Laparos-copic Roux-en-Y gastric bypass for BMI <35 kg/m2): a tailored approach. Surg Obes Relat Dis. 2006; 2: 401-4. [ Links ]
34. Inge TH, Krebs NF, Garcia VF, et al. Bariatric surgery for severely overweight adolescents: Concerns and recommendations. Pediatrics. 2004; 114: 217-23. [ Links ]














