Servicios Personalizados
Revista
Articulo
Indicadores
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Archivos de cardiología de México
versión On-line ISSN 1665-1731versión impresa ISSN 1405-9940
Arch. Cardiol. Méx. vol.75 supl.1 Ciudad de México ene. 2005
Renasica II
Registro Mexicano de Síndromes Coronarios Agudos
RENASICA II Mexican Registry of Acute Coronary Syndromes
Armando García–Castillo,* Carlos Jerjes–Sánchez,* Pedro Martínez Bermúdez,* José Ramón Azpiri–López,** Alonso Autrey Caballero,*** Carlos Martínez Sánchez,**** Marco Antonio Ramos Corrales,***** Guillermo Llamas,****** Jesús Martínez Sánchez,******* Alfonso J Treviño*
Por los Investigadores del Registro Nacional de Síndromes Coronarios Agudos ll$
* Hospital de Enfermedades Cardiovasculares y del Tórax IMSS 34, Monterrey.
** Hospital Universitario, Monterrey.
*** Hospital de Cardiología Siglo XXI CMN, IMSS México DF.
**** Instituto Nacional de Cardiología "Ignacio Chávez", México DF.
***** Centro Médico "La Raza", México DF.
****** Cardiológica, Ags.
******* Hospital ABC, México DF.
Correspondencia:
Dr. Carlos Jerjes–Sánchez.
Santander 316, Col. Bosques de San Ángel Sector Palmillas,
CP 66290,
San Pedro Garza García, NL,
México.
Correo electrónico: jerjes@infocel.net.mx, jerjes@prodigi.net.mx, armandogd@ prodigi.net.mx
Resumen
Objetivo: El registro pretende establecer en México las características clínicas, identificar abordajes terapéuticos y conocer la evolución hospitalaria en pacientes con síndromes coronarios agudos.
Métodos y resultados: RENASICA II es un registro prospectivo que incluye 8,098 pacientes con diagnóstico final de síndrome coronario agudo. Tres mil quinientos cuarenta y tres tuvieron angina inestable o infarto sin elevación del ST (AI/IMNEST) y 4,555 con infarto con elevación del ST (IMEST). A su ingreso al hospital se identificó dolor torácico típico de isquemia en 78% y 85% respectivamente. Se consideró de alto riesgo al 36% de los pacientes con AI/IMNEST. En la mayoría de los pacientes con IMEST la localización fue anterior y se encontraban en clase KK I. En AI/IMNEST se utilizó aspirina en el 90%, heparina no fraccionada 50%, heparina de bajo peso molecular 45%, nitratos 58%, bloqueadores beta 50% e inhibidores de enzima convertidora en el 54%. En IMEST estos medicamentos se utilizaron en el 88%, 54%, 44%, 66%, 51% y 64% respectivamente. En pacientes con AI/IMNEST se realizó angiografía en el 62%, angioplastía coronaria 30% y cirugía de revascularización 8%. En el grupo con IMEST estos procedimientos se realizaron en el 44%, 27% y 4% respectivamente. En IMEST el 37% recibió terapia fibrinolítica y 15% fueron llevados a angioplastía primaria o facilitada. La mortalidad hospitalaria global del 7%, en AI/IMNEST fue del 4% y en IMEST del 10%.
Conclusión: El más grande registro de síndromes coronarios agudos en Latinoamérica provee información importante sobre el espectro clínico, evolución hospitalaria, calidad de atención e identifica áreas de oportunidad para mejorar la atención médica. El RENASICA II extiende nuestro conocimiento sobre cómo la reperfusión y el tratamiento antitrombótico modifican la evolución y cuáles procesos necesitamos mejorar en la práctica real en México.
Palabras clave: Síndromes coronarios agudos. Infarto agudo del miocardio. Angina inestable. Cardiopatía isquémica aguda.
Summary
Objective: The registry intends to establish the clinical characteristics, identify therapeutic approaches and describe in–hospital outcome of patients with acute coronary syndromes in Mexico.
Methods and results: RENASICA II is a prospective registry that included 8,098 patients with final diagnosis of acute coronary syndromes. Three thousand five hundred and forty three patients had unstable angina or non–ST elevation myocardial infarction (UA/NSTEMI) and 4,555 ST elevation myocardial infarction (STEMI). On admission typical chest pain was identified in 78% and 85% respectively. Non–ST elevation high risk group was identified in 36%. In STEMI group anterior myocardial infarction and Killip class I had higher occurrence. The use of aspirin, unfractionated heparin, low molecular weight heparin, nitrates, beta blockers and ACE inhibitors for patients with UA/NSTEMI were 90%, 50%, 45%, 58%, 50% and 54% respectively, with corresponding rates of 88%, 54%, 44%, 66%, 51% and 64% for STEM I patients. Coronary angiography, angioplasty and coronary bypass surgery were performed in 62%, 30% and 8% in UA/NSTEMI patients respectively with corresponding rates of 44%, 27% and 4% for STEMI group. Among patients with STEMI 37% were under fibrinolytic therapy and 15% received primary or facilitated angioplasty. Overall In–hospital mortality was 7%, 4% for UA/NSTEMI and 10% for STEMI.
Conclusion: The largest registry on ACS in Latin–America provides important and reliable information on complete spectrum, outcome, quality of care, and identifies areas for further improvement of such quality. RENASICA II broadens our knowledge about how reperfusion and antithrombotic approaches modify the outcome and what needs to be improved in the real practice in Mexico.
Key words: Acute coronary syndromes. Acute myocardial infarction. Unstable angina. Acute ischemic heart disease.
Introducción
A nivel mundial los síndromes coronarios agudos (SCA) son una causa importante de morbilidad y mortalidad.1,2 De acuerdo a datos recientes, en el siguiente año más de 6 millones de personas tendrán un infarto agudo del miocardio y su prevalencia aumentará 33%.3,4 Datos epidemiológicos de México, establecen a la cardiopatía isquémica como primera causa de mortalidad en mayores de 60 años, la segunda causa en la población en general, fue responsable de 50,000 muertes en 2003 y contribuyó aproximadamente al 10% de todas las causas de mortalidad.5,6 Avances en el conocimiento de la fisiopatología del SCA permitieron establecer una nueva clasificación de acuerdo a los hallazgos electrocardiográficos del ST7 (con o sin elevación del ST). El manejo del SCA continúa experimentando cambios importantes sobre la base de la evidencia derivada de estudios clínicos bien conducidos y de las guías o lineamientos desarrollados por las sociedades de cardiología.8–11 Aunque se han llevado a cabo excelentes estudios, algunos resultados están abiertos a interpretación, pueden no ser aplicables en todos los ámbitos clínicos y las opciones de tratamiento podrían verse limitadas por la falta de recursos. Todas estas evidencias sugieren la necesidad de identificar indicadores de la buena práctica clínica que reflejen "nuestra práctica real".
Registros de alta calidad pueden ayudar a entender si los conocimientos que derivan de los estudios clínicos se aplican apropiadamente y si los resultados se reproducen en la práctica clínica diaria. En México, el segundo Registro Nacional de Síndromes Coronarios Agudos (RENASICA–II) intenta establecer características clínicas, identificar abordajes terapéuticos, y conocer la evolución hospitalaria con la expectativa de extender los conocimientos derivados del RENASICA I.12
Diseño de RENASICA II
Es un registro prospectivo y observacional de la Sociedad Mexicana de Cardiología diseñado para identificar tendencias de estratificación, diagnóstico y tratamiento mediante el análisis de una población representativa, sin sesgos y con diagnóstico final de SCA secundario a cardiopatía isquémica. La evolución hospitalaria se analizó a través de eventos cardiovasculares mayores adversos (ECMA), que incluyen mortalidad, isquemia recurrente, infarto, reinfarto, choque cardiogénico y evento agudo vascular cerebral.
Centros
Se consideró a investigadores en hospitales de segundo y tercer nivel de atención con conocimientos y experiencia en el diagnóstico, estratificación y el tratamiento de los SCA. Con la finalidad de establecer a una población representativa y evitar una muestra seleccionada, se incluyeron hospitales con diferencias en accesibilidad para realizar cateterismo cardíaco, número de camas de terapia intensiva y en la práctica clínica.
Pacientes
Los pacientes ingresaban al registro si durante la admisión al hospital tenían una alta sospecha clínica de SCA: manifestaciones de isquemia aguda, con o sin cambios en el ECG, con o sin necrosis, y con diagnóstico final de cardiopatía isquémica probada por pruebas invasivas o no invasivas. Los pacientes con síntomas precipitados por anemia, hipertensión, insuficiencia cardíaca, etcétera, no fueron considerados. Al ingreso y al alta hospitalaria el diagnóstico se estandarizó mediante la nomenclatura de SCA con o sin elevación del ST. Todas las decisiones relacionadas con el tratamiento se dejaron a discreción de los médicos tratantes.
Calidad
Para garantizar el control de calidad de los datos, en RENASICA II se aplicaron los criterios de Alpert:12 a) definiciones estandarizadas, y todos los participantes estaban familiarizados con ellas, b) selección cuidadosa del hospital, c) proceso de obtención de los datos del registro aprobado por todos los hospitales, según las políticas locales, d) se reportaron todos los datos obtenidos, e) se centralizaron las formas de reporte de casos originales y los informes enviados por vía electrónica, f) un experto en estadística analizó cuidadosamente todos los datos obtenidos, g) el centro de datos analizó cuidadosamente cada hoja de datos enviada o no por vía electrónica, h) el Investigador Principal y el Comité Directivo mantuvieron el orden administrativo, adjudicaron los desacuerdos y alentaron el sometimiento oportuno de documentos y el análisis de datos. Se realizaron reuniones en donde todos los participantes fueron capacitados para la obtención de datos mediante un manual estandarizado de instrucciones y definiciones. En algunos centros en forma aleatoria se programó una visita clínica de monitoreo de datos clínicos.
Obtención de datos
Cyberworks Inc. desarrolló una forma de reporte de caso electrónica en un ambiente Microsoft SQL (Lenguaje Query Estructurado). Para la recepción de los datos electrónicos, se instaló un servidor Dell en el Centro de Datos Central (Hospital de Enfermedades Cardiovasculares y Tórax) en la ciudad de Monterrey. La base de datos electrónica y la forma de reporte de caso se integró con 300 variables que incluyeron datos demográficos, historia clínica, hallazgos clínicos, datos de laboratorio y ECG, terapia antitrombótica y fibrinolítica, otros tratamientos, riesgo de estratificación, procedimientos invasivos y no invasivos, eventos adversos y evolución hospitalaria. La información de los datos se envió al Centro de Datos Central a través de: a) el sitio en la red www.renasica.com.mx, b) correo electrónico (renasica@prodigy.net.mx), c) disquete o disco compacto (CD), d) Fax, o e) correo convencional.
Análisis estadístico
Pruebas de Chi cuadrada para variables discretas y t de dos colas para variables continuas. Para el análisis de las diferencias, prueba de Chi cuadrada corregida de Yates. Para probar la mediana se usó la prueba de Wilcoxon. Para evaluar el efecto sobre mortalidad entre variable dependientes e independientes se elaboró un modelo de regresión logística. Se estableció como medida de asociación la razón de momios, con un intervalo de confianza (IC) de 95%. Se asumió significancia estadística con un nivel de P < 0.05. Los datos se expresaron en porcentajes, mediana, media y DE. Todos los análisis estadísticos se llevaron a cabo utilizando un paquete estadístico disponible en el comercio (GBSTAT, versión 6.5 de Dynamic Microsystems, Inc.).
Resultados
Entre diciembre de 2002 y noviembre de 2003, ingresaron a RENASICA II 8,600 pacientes con SCA comprobado. Se excluyeron 502, y 8,098 pacientes restantes fueron considerados en el reporte final. De éstos, 3,543 tuvieron angina inestable o infarto del miocardio sin elevación del ST (AI/IMNEST) y 4,555 con infarto del miocardio con elevación del ST (IMEST). En RENASICA II participaron setenta y seis investigadores en sesenta y seis hospitales de segundo y tercer nivel de atención médica. En relación a los hospitales que participaron en el registro, 90% (60 hospitales) tuvieron una participación activa, 48% eran del sistema de salud gubernamental, 39% de la práctica privada y 12% de hospitales universitarios o de otros sistemas de salud. Los hospitales localizados a lo largo del país admitieron al 52% del total de pacientes, y los hospitales de la ciudad de México aceptaron al 48%. El 90% de los pacientes se ingresaron en hospitales del tercer nivel con capacidad para arteriografía coronaria, angioplastía coronaria transluminal percutánea (ACTP) y cirugía de revascularización coronaria (CRVC). La información se envió al Centro de Datos Central mediante forma de reporte de casos escrita en el 55% de los casos, y reporte de caso electrónica en disquete, disco compacto (CD) o correo electrónico en el 45%.
Características demográficas
En ambos grupos, (Tabla I) los pacientes fueron mayores de 60 años, del sexo masculino y por lo menos con un factor mayor histórico de riesgo para aterosclerosis. El rango de edad fue de 21 a 100 años y los pacientes con AI/IMNEST tuvieron una mayor prevalencia de comorbilidad e incidencia de procedimientos de intervención coronaria y cirugía cardiovascular previos en relación con el grupo con IMEST.
Presentación clínica
En el momento de la admisión, la mayoría tuvo dolor torácico típico y estabilidad clínica (Tabla I). Se observó dolor torácico atípico en el 13% de los pacientes con AI/IMNEST y en el 9% de los pacientes con IMEST, no existió historia de dolor de torácico en el 8% y 6%, respectivamente. En ambos grupos el 1% no tuvo síntomas. El grupo sin elevación del ST el 36% se consideró de alto riesgo, 49% con estabilidad clínicay 14% con inestabilidad. En el grupo con IMEST, la mayor incidencia correspondió al infarto de localization anterior de clase 1 de Killip, 17% estuvo en clase II, 5% clase III y 4% clase IV.
Hallazgos electrocardiográficos
Se tomó la información del primer ECG con datos de isquemia aguda tomado previamente o a su ingreso al hospital. De todos los pacientes, (8,098) el 65% tuvo depresión del ST, 45% ondas T negativas, 43% onda Q y 34% elevación del ST. En el grupo con AI/IMNEST de alto riesgo, en el 56% se observaron cambios inespecíficos del ST y ondas T negativas, 26% con desnivel negativo extenso del ST (> 1 mm en > 3 derivaciones subyacentes) y en 18% no se consideró extenso. En la Tabla II se observan otros hallazgos electrocardiográficos como anormalidades del sistema de conducción, arritmias ventriculares y supraventriculares.
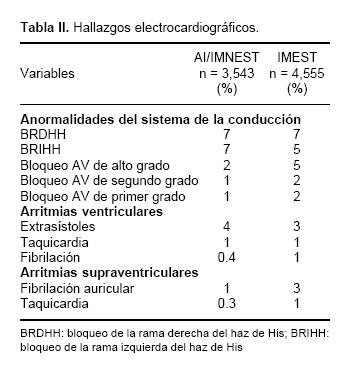
Marcadores bioquímicos
Se obtuvieron determinaciones de la creatinina cinasa total (CK–T) en 3,525 pacientes con AI/ IMNEST (99%). Entre estas determinaciones, 70% eran < 1.5 X, 13% de 1.5 a 3 X, y 17% > 3 X. Se obtuvo la determinación de la creatinina cinasa–MB (CK–MB) en 3,221, (91%) con hallazgos similares, 70% < 1.5 X, 14% 1.5–3 X y 16% > 3X. Sólo se tuvieron determinaciones de troponina disponibles en 712 pacientes (20%) y la troponina I (76%) fue el indicador de micronecrosis más común (245). En el grupo con IMEST se obtuvieron valores de CK–T y CK–MB en 4,512 (99%) y 3,681 (81%) respectivamente. Estos indicadores se comportaron de la siguiente manera > 3 X, (57%y 55%), entre 1.5–3.0 X, (19%y 20%) y < 1.5 X (24%y 25%).
Indicadores de inflamación
Los pacientes con elevación del ST mostraron la mediana más alta de leucocitos, de 10,200 u/L (7,900–12,900 u/L) y linfocitos (3,043 ± 3,265) que el grupo sin elevación del ST, mediana de 8,360 u/L (6,609–10,500 u/L) y linfocitos 2,859 ± 3,604. Se obtuvieron mediciones cualitativas de la proteína C reactiva en el 3% (103) de los pacientes con AI/IMNEST y en el 4% (167) del grupo de IMEST; este prototipo de reactante de fase aguda fue positivo en el 21% y en el 42% de ambos grupos, respectivamente.
Tratamiento farmacológico
Hubo una tendencia ascendente a usar ácido acetilsalicílico, heparina no fraccionada, heparina de bajo peso molecular (HBPM), nitratos, betabloqueadores e inhibidores de la enzima convertidora de la angiotensina. Entre los pacientes bajo tratamiento con HBPM, la enoxaparina fue el agente empleado con mayor frecuencia. Los pacientes que se presentaron con AI/IMNEST tuvieron menos probabilidades de recibir heparina no fraccionada, nitratos, estatinas, inhibidores de la enzima convertidora de la angiotensina y terapia fibrinolítica, pero tenían más probabilidades de recibir clopidogrel, bloqueadores del canal del calcio, intervención coronaria percutánea y CRVC durante la hospitalización de referencia (Tabla I). El uso de ticlopidina y anticoagulación oral fue infrecuente en ambos grupos. En los pacientes con AI/IMNEST e IMEST por complicaciones se utilizaron medicamentos como digoxina, (7% vs 8%) diuréticos, (14% vs 17%) aminas vasoactivas, (7% vs 15%) amiodarona (6% vs 2%) y xilocaína (11% vs 5%).
Terapia de reperfusión
De los 4,555 pacientes con IMEST, 1,685 (37%) recibieron terapia fibrinolítica(TF), el tiempo entre el inicio de los síntomas y la administración fue de < 2 horas en 31%, de 2 a 4 horas en el 36%, de 4 a 6 horas en el 19% y, finalmente, de > 6 horas en el 15%. La estreptoquinasa fue el fibrinolítico que se utilizó con mayor frecuencia (82%), seguido de alteplasa (17%). Tenecteplasa y la reteplasa se usaron sólo en algunos pacientes. Se llevó a cabo ACTP primaria o facilitada en el 15% de los pacientes. El índice global de revascularización durante la hospitalización, ya sea ACTP o CRVC, fue de 30% (1,366 pacientes). En AI/IMNEST, se logró reperfusión farmacológica en 149 pacientes (4%), y el índice de revascularización global (ACTP o CRVC) fue de 39%.
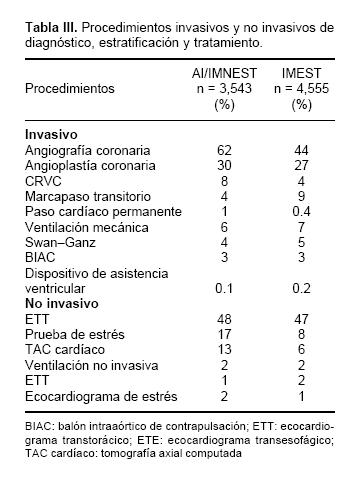
Procedimientos no invasivos e invasivos
Los procedimientos realizados durante la hospitalización se muestran en la Tabla III. Una mayor proporción de pacientes con AI/IMNEST requirió de un diagnóstico invasivo, y también de reperfusión mecánica y quirúrgica. Se obtuvo un alto índice de éxito de la ACTP en 1,087 pacientes con AI/IMNEST (92%) y en 1,234 pacientes con IMEST (85%). Se observó fracaso en 5% y 8%, y se consideró como un procedimiento subóptimo en 3% y 6%, respectivamente. Se empleó la colocación de un stent en el 88% de los pacientes con AI/IMNEST y en el 85% de los pacientes con IMEST. En 3,543 pacientes del grupo con AI/IMNEST, los principales hallazgos angiográficos fueron: enfermedad de la descendente anterior izquierda en el 60%, coronaria derecha en el 49%, circunfleja en el 44%, tronco principal izquierdo en el 9%, y oclusión de injerto venoso en el 3%. En 4,555 pacientes con IMEST, la angiografía coronaria mostró: enfermedad de la descendente anterior izquierda 65%, coronaria derecha 53%, circunfleja 37%, tronco principal izquierdo 5%, y oclusión de injerto venoso en el 1%. Los pacientes con IMEST tuvieron más probabilidades de recibir apoyo respiratorio y soporte cardiovascular invasivo, mientras que en el grupo de AI/IMNEST, requirieron de mayores estudios diagnósticos no invasivos y pruebas de estratificación. Se llevó a cabo un ecocardiograma transtorácico en más del 45% en ambos grupos.
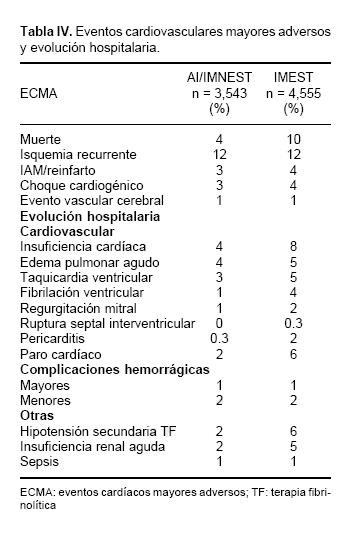
Eventos cardiovasculares adversos y evolución hospitalaria
La mortalidad global en los 8,098 casos de SCA, fue de 7%, y en el grupo con IMEST fue mayor. Entre los pacientes con AI/IMNEST e IMEST se observó un porcentaje similar de otros ECMA hospitalarios (Tabla IV). Los pacientes con IMEST tuvieron mayor disfunción ventricular izquierda grave, arritmias ventriculares, complicaciones mecánicas y paro cardíaco. En lo que respecta a las complicaciones hemorrágicas, no se observaron diferencias en ambos grupos. La hipotensión inducida por terapia fibrinolítica e insuficiencia renal se observó con mayor frecuencia en los pacientes con IMEST (Tabla IV).
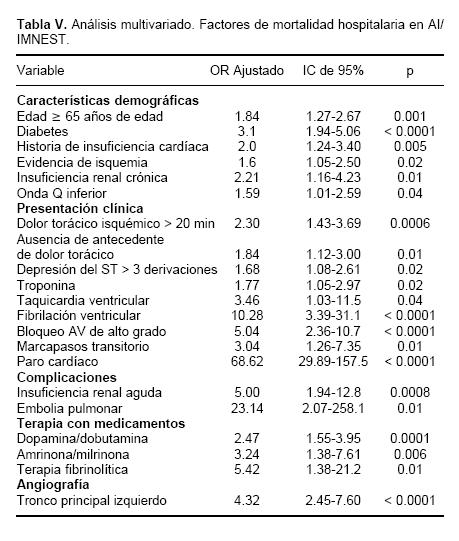
Análisis multivariado en angina inestable e infarto sin elevación del ST (AI/IMNEST)
En las Tablas IV y V se muestra un análisis de regresión logística realizado para evaluar el efecto de las variables independientes sobre la mortalidad, incluyendo un ajuste para factores de confusión potenciales en pacientes con AI/ IMNEST y en pacientes con IMEST. Fueron predictores poderosos de mal pronóstico: estados de disfunción endotelial crónica, función renal inadecuada, dolor torácico de duración prolongada, ausencia de antecedentes de dolor torácico, fibrilación ventricular, anormalidades severas del sistema de la conducción y paro cardíaco. Otras complicaciones en el hospital, como disfunción renal aguda y embolia pulmonar, tuvieron relevancia estadística. La terapia fibrinolítica y los medicamentos empleados en los estados de disfunción ventricular izquierda severa y en las complicaciones arrítmicas tuvieron una relación negativa. El hallazgo angiográfico con mayor relación con mortalidad fue la enfermedad de tronco coronario izquierdo (Tabla IV).
Análisis multivariado en infarto al miocardio con elevación del ST (IMEST)
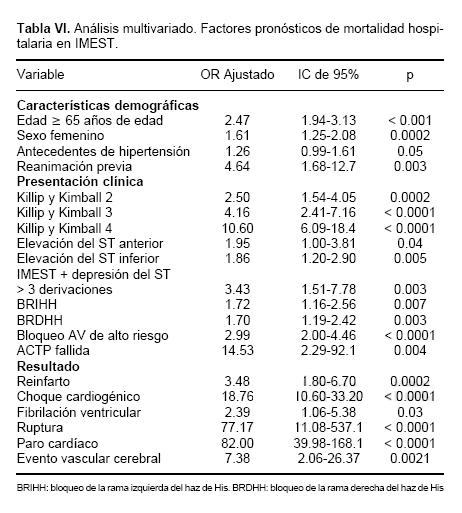
Los predictores más importantes de mortalidad fueron edad avanzada y sexo femenino, así como cualquier grado de disfunción ventricular, miocardio extenso en riesgo, anormalidades graves del sistema de conducción, cualquier complicación hospitalaria relacionada con un nuevo evento isquémico, disfunción ventricular grave (KK III – IV), arritmias ventriculares, complicaciones mecánicas y evento vascular cerebral. El fracaso de la ACTP se relacionó estrechamente con un mal resultado (Tabla VI).
Diagnóstico final
Durante el período del estudio, se admitieron 8,600 pacientes con alto grado de sospecha de SCA clínico. La proporción del diagnóstico inicial entre dolor torácico inespecífico, AI/IMNEST e IMEST se muestra en la Figura 1. La precisión del diagnóstico para AI/IMNEST e IMEST fue de 82% y 89%, respectivamente. Los pacientes con dolor torácico inespecífico inicial tenían IMEST o AI/IMNEST en 16% (Fig. 1).
Discusión
El RENASICA II es el registro más grande del SCA en Latinoamérica, que proporciona información importante y confiable acerca de la calidad de la atención médica. Esta evidencia proporciona conocimientos importantes acerca de los abordajes terapéuticos y la evolución hospitalaria, para ello se establecieron definiciones específicas previamente determinadas a través de los criterios de calidad establecidos para los registros.13 El registro RENASICA II forma parte de un paso importante para identificar evidencia que permita conocer una visión más real de la morbilidad y mortalidad, similitudes y diferencias con registros previos,12,14–18 y en este escenario, que hemos aprendido y que necesitamos mejorar.
El SCA es un término que incluye una constelación de síntomas clínicos secundarios a isquemia aguda. El espectro clínico incluye en un extremo, a la isquemia silenciosa y en el otro, al IMEST, en la parte media de este espectro se posiciona el SCA sin elevación del ST con o sin micronecrosis. Aunque en todos los grupos el evento inicial característico es la ruptura de una placa vulnerable con formación de un trombo, existen diferencias en la evolución a corto y largo plazo.19,20 En el IMEST se ha demostrado mayor mortalidad hospitalaria, mientras que en AI/IMNEST es más frecuente el reinfarto, isquemia recurrente y mortalidad a largo plazo.21 Dado el impacto del SCA en México,5,6,12 el RENASICA II surge como otro vínculo entre los estudios clínicos aleatorios, guías o lincamientos y la práctica clínica diaria22 en un país con ingresos medios.
Lecciones aprendidas de RENASICA I
Este registro que incluyó 4,353 pacientes con SCA con o sin elevación del ST enfatiza las prácticas actuales y los abordajes terapéuticos en la transición de los siglos veinte y veintiuno. El SCA sin elevación de ST fue la causa más común de admisión hospitalaria y se demostró inaccesibilidad en nuestro medio para obtener determinaciones iniciales de troponinas. En el SCA sin elevación del ST fueron indicadores de riesgo edad > 65 años, depresión del ST, macronecrosis y angiográficamente una enfermedad coronaria extensa. La presencia de dolor isquémico típico, disnea y diaforesis tuvieron una relación estrecha con macronecrosis y el diagnóstico final de IMEST. A pesar de que el 90% de los hospitales tenían capacidad para realizar reperfusión farmacológica y/o mecánica, menos de la mitad de los pacientes recibieron este beneficio. En el 70% de los pacientes se empleó un tratamiento antitrombínico y antiplaquetario estándar y en una menor proporción heparina de bajo peso molecular y antagonistas de los receptores de superficie plaquetaria IIb/IIIa. A través del RENASICA I se obtuvo información que podría ayudar a las autoridades de salud mexicanas para que se utilicen mejor los recursos de salud en el futuro próximo del tratamiento de los SCA.12
RENASICA II
Este proyecto ha generado un gran volumen de datos sobre la incidencia y la frecuencia relativa de SCA con o sin elevación del ST como una causa de admisión en el hospital. El infarto con elevación del ST fue la causa más frecuente de hospitalización (56%), seguida de AI/IMNEST (44%). La proporción 1.3:1 de IMEST para AI/ IMNEST es más alta que la reportada en RENASICA I (35% vs 65%)12 y otros registros previos.15,16,18 Una explicación parcial podría ser la facilidad para el acceso a reperfusión mecánica en los hospitales participantes. Otra razón potencial es que la prevalencia global de IMEST asociado con otras comorbilidades (diabetes) aumentó rápidamente. Estos resultados establecen al IMEST como la principal causa de admisión hospitalaria y ponen de relieve el impacto que tiene sobre los recursos del Sistema de Salud Nacional.
Ambos grupos tuvieron una media de estancia hospitalaria de 8.1 días, estos resultados son muy parecidos a lo observado en GRACE (8 días) y ENACT (angina inestable, 8.5 días) y en lo que respecta al infarto del miocardio de acuerdo a la experiencia europea, los tiempos de estancia fueron más cortos.14,16 Sin embargo, estamos muy lejos de la impresionante y dramática reducción de la estancia hospitalaria (4.3 días) observada en el registro NRMI1,2,3 en pacientes llevados a reperfusión farmacológica o mecánica.23 Esto podría atribuirse a un incremento en las estrategias de reperfusión que permiten limitar el tamaño del infarto y la isquemia recurrente, así como a reformas importantes en el Sistema de Salud para implementar rutas críticas y otras medidas de control de calidad para mejorar la eficacia y reducir el costo de la atención hospitalaria. En ambas modalidades de reperfusión no se observó ninguna diferencia en relación con la estancia hospitalaria.23 La base de datos de RENASICA II podría utilizarse para establecer prioridades terapéuticas y estandarizar la atención, lo que permitiría reducir el tiempo de hospitalización.
La mayoría de los datos demográficos fueron muy similares a otras poblaciones de SCA, sin embargo, en RENASICA I12 y II, hasta donde sabemos, la diabetes (50% y 42%) tuvieron la incidencia más elevada jamás reportada en el marco de un registro de SCA.14–18,23 La diabetes, una enfermedad que se está expandiendo rápidamente en la actualidad, es un factor de riesgo importante de morbilidad y mortalidad cardiovasculares, y se asocia con un mal pronóstico después de un infarto del miocardio.24 La diabetes sola o asociada con otros estados de disfunción endotelial crónica e inflamación (pacientes de edad avanzada, tabaquismo, hipertensión, lípidos anormales) podría explicar la elevada incidencia de IMEST en el RENASICA II y a nivel mundial.25 En la AI/IMNEST, la diabetes fue un factor de pronóstico poderoso de la mortalidad hospitalaria.
Considerando que el objetivo principal en RENASICA II no fue evaluar el estado metabólico, no se realizaron pruebas de la glucosa en ayuno, hemoglobina glucosilada Ale o tolerancia a la glucosa oral, no se llevaron a cabo pruebas de la glucosa sanguínea en ayuno, hemoglobina glucosilada Ale o tolerancia a la glucosa oral. De esta forma, los estados de diabetes, deterioro de la tolerancia a la glucosa y resistencia a la insulina podrían subestimarse. Además, no se estableció el índice de obesidad. La elevada incidencia de diabetes subraya marcadamente la importancia de incluir una prueba de diagnóstico para las anormalidades de la glucosa, a fin de mejorar la estratificación del riesgo y el resultado. En cualquier estadio de la enfermedad coronaria es necesario establecer o incrementar estrategias de prevención secundaria y aplicar objetivos aún más estrictos para el control de la tensión arterial, lípidos y obesidad.25
El diagnóstico de SCA con o sin elevación del ST es un proceso clínico que depende de factores de riesgo históricos, características del dolor torácico y de hallazgos del ECG. Los datos de la macronecrosis o la micronecrosis disponibles establecen el diagnóstico final, pero no son necesarios para iniciar la estrategia reperfusión óptima y/o el tratamiento antitrombótico. En el espectro clínico del SCA, el dolor de torácico isquémico típico, las anormalidades del segmento ST y la onda T fueron características clínicas en el momento de la presentación. Se ha observado un perfil clínico similar en varios modelos de riesgo,26,27 el cual confirma los resultados de RENASICA I.12
La angina inestable y el IMNEST son síndromes clínicos estrechamente relacionados, con frecuencia imposibles de distinguir en el momento de la presentación y a menudo implica un diagnóstico temprano y un enfoque terapéutico similar. Considerando que los grupos de alto riesgo tienen una evolución desfavorable, la estratificación de riesgo tiene importancia crucial en la práctica de la medicina contemporánea; en este escenario, las determinaciones de la troponina son una herramienta de diagnóstico importante. Las observaciones de RENASICA I (12%),12 II (20%) y ENACT (36%)16 indican que su disponibilidad sigue siendo muy limitada; sin embargo, entre los indicadores bioquímicos, la troponina fue el único factor de pronóstico de la mortalidad. Se observó una tendencia similar con las mediciones de la proteína C reactiva. Estas observaciones establecen la necesidad de identificar un modelo de riesgo apropiado, adaptado a los países con ingresos medios. Aunque se identificó una tendencia ascendente en el uso de tratamientos antitrombóticos y antiisquémicos estándar,12 RENASICA II enfatiza áreas específicas para mejorar el conocimiento y la práctica actual entre los médicos relacionados con el cuidado del SCA. En la AI/IMNEST, los resultados mostraron que el uso de nitratos, betabloqueadores, heparina no fraccionada y HBPM fue marcadamente más bajo de lo esperado. El alto uso de inhibidores de la ECA (54%) es un tanto sorprendente, dada la falta de evidencia, y es probable que se relacione con comorbilidades.15,16 En el IMEST, el uso de ácido acetilsalicílico, nitratos, inhibidores de la ECA y heparina no fraccionada fue más bajo. Considerando las ventajas farmacológicas de enoxaparina y clopidogrel en el marco del IMEST con o sin la estrategia de reperfusión, su uso puede considerarse apropiado; en los pacientes bajo reperfusión farmacológica, la evidencia final proviene de los estudios TIMI 25 y 28.
En ambos grupos se observó un uso reducido de antagonistas de los receptores de superficie plaquetaria IIb/IIIa (16%). Es probable que esta tendencia sea el reflejo de que se utilizan principalmente como tratamiento adjunto en intervención coronaria percutánea, por los desalentadores resultados de los estudios GUSTO IV28 y V29 o porque no fueron un recurso disponible. En todos los pacientes la proporción en el uso de estatinas (13%) fue más baja que en los registros europeos,15,16 lo cual podría reflejar que los médicos adoptan tendencias terapéuticas sobre la base de sus experiencias personales y rechazan resultados de los estudios contemporáneos. Aunque no hay evidencia firme30 (p = 0.04) que demuestre que las estatinas en la fase aguda de un SCA mejoran la evolución, aún se considera como una interrogante en espera de la respuesta final. Mientras tanto, las estatinas en la enfermedad coronaria han demostrado seguridad y efectividad a largo plazo y en los SCA son seguras y podrían mejorar la disfunción endotelial.30 Además, la mayoría de estos pacientes requieren de una intervención farmacológica y no farmacológica para reducción de lípidos.
En el momento actual, la estrategia de reperfusión es el tratamiento estándar para pacientes con IMEST, en este escenario, tanto la reperfusión mecánica como la farmacológica son alternativas válidas. La proporción de TF disminuyó del RENASICA I (50%) al RENASICA II (37%), una posible explicación podría ser el alto número de hospitales con capacidad para realizar intervención coronaria. Sin embargo, las causas de esto deben analizarse detalladamente, ya que una proporción significativa de pacientes ingresaron en ventana para obtener los beneficios de la reperfusión farmacológica. En el IMNEST, el uso de TF (4%) fue similar a lo reportado por otros registros.1516 Aunque en este grupo la TF fue un factor pronóstico importante de mortalidad hospitalaria, un porcentaje alto de los pacientes tuvo inestabilidad clínica, anormalidades del sistema de la conducción, macronecrosis y disfunción ventricular izquierda. Posiblemente la TF se usó como terapéutica de rescate en centros sin posibilidades para realizar reperfusión mecánica. No se observaron complicaciones hemorrágicas mayores. Aunque el porcentaje de intervención coronaria percutánea fue bajo (15%), estos resultados coinciden con reportes previos.14,16 Considerando la proporción significativa de pacientes con IMEST que no recibieron ninguna estrategia de reperfusión, se requieren nuevas direcciones del Sistema de Salud que permitan mejorar la calidad de la atención médica en este grupo.
En todos los grupos se observaron variaciones entre procedimientos invasivos y no invasivos. En AI/IMNEST fueron sorprendentemente altas la angiografía coronaria y la revascularización percutánea y quirúrgica. Sin embargo, estos resultados no son distintos a evidencias previas14 y reflejan la disponibilidad de especialistas y de equipo apropiado. Se observó una tendencia similar en el diagnóstico no invasivo y en las pruebas de estratificación.
En el IMEST los porcentajes de mortalidad fueron más altos de lo esperado y mayor a lo reportado previamente.14–16,23 Sin embargo, esto no es un hallazgo inesperado ya que una proporción importante de pacientes no tuvieron ninguna facilidad de reperfusión. La disfunción ventricular izquierda fue el ECMA más importante y el factor pronóstico más poderoso de mortalidad, esto podría relacionarse con la baja incidencia de estrategias de reperfusión y con tiempos más prolongados de isquemia. Nuevas direcciones de reperfusión farmacológica, que incluyen TF en bolo, como actualmente sucede en otros países, podrían mejorar la evolución de los pacientes con IMEST. La experiencia de los centros y el tratamiento antitrombótico intensivo temprano (24 horas) podrían explicar la baja incidencia de complicaciones hemorrágicas mayores y arritmias ventriculares. En los SCA sin elevación del ST el porcentaje de mortalidad tuvo una proporción similar a reportes previos.14–16
Los resultados del RENASICAII ponen de relieve los retos para el diagnóstico en pacientes con alta sospecha clínica de un SCA (Fig. 1). En los pacientes con diagnóstico inicial de AI/IMNEST y sospecha de IMEST, el diagnóstico fue correcto en más del 80%. El alto porcentaje de SCA en pacientes con dolor torácico inespecífico, a pesar de la participación de médicos expertos, enfatiza lo limitado de su sensibilidad para el diagnóstico. En este grupo, los clínicos deben ser muy cuidadosos para evitar un egreso temprano.
En este registro una interrogante importante es establecer si los pacientes representan una población general de SCA. Los registros tienen una posibilidad más limitada que los estudios clínicos para asegurar la inclusión consecutiva de pacientes. Por otra parte, los registros recluían pacientes tal como se ven en la práctica clínica diaria y sin estrictos criterios de inclusión que comúnmente se aplican en estudios clínicos controlados. De cualquier manera, el tamaño del registro con 8,098 pacientes y un amplio espectro de SCA, permite asumir que el comportamiento descrito efectivamente representa, al menos, en los hospitales seleccionados una imagen real de la situación clínica actual.
Los datos previamente mencionados demuestran similitudes importantes entre RENASICA I12 y II. Esto apoya la validez de los resultados y refuerza la necesidad adicional de mejorar la atención médica. Sin embargo, existen diferencias importantes que hacen difícil comparar la evolución en grupos específicos. Los datos aquí presentados proporcionan conocimientos importantes acerca de la práctica de la cardiología en distintos ámbitos hospitalarios en México.
Limitaciones
Considerando que no fue un estudio epidemiológico basado en población, pueden haberse introducido algunos sesgos en lo que respecta a: a) la selección de los centros participantes, b) la visita de monitoreo limitada se enfocó en la precisión de la introducción de los datos, c) es posible que no se hayan incluido algunos de los pacientes que fallecieron en la sala de urgencias, d) no hubo un seguimiento a largo plazo, e) una elevada proporción de centros con capacidad para revascularización impide generalizar los resultados a todos los hospitales del país.
Conclusión
El registro más grande de SCA en Latinoamérica provee información importante y confiable sobre el espectro clínico, evolución hospitalaria, calidad de atención, e identifica áreas de oportunidad para la mejora de la atención médica. El RENASICA II amplía nuestro conocimiento sobre cómo la reperfusión y tratamiento antitrombótico modifican la evolución y qué procesos necesitamos mejorar en la práctica real en México.
Investigadores y hospitales participantes:
Alonso Autrey Caballero, Gabriela Borrayo, Hospital de Cardiología Siglo XXI CMN IMSS, México DF; (1,354). Armando García–Castillo, Carlos Jerjes Sánchez–Díaz, Beatriz Maldonado, Armando Astorga, Jorge García; Hospital de Enfermedades Cardiovasculares y del Tórax IMSS, Mty. NL; (1,269). Carlos Martínez Sánchez, Úrsulo Juárez, Héctor González, Instituto Nacional de Cardiología, México DF; (890). Guillermo Llamas Esperón, Hospital Cardiológica Aguascalientes; (519). Marco A. Ramos Corrales, Centro Médico "La Raza", México DF; (455). Jesús Martínez Sánchez, Hospital ABC, México DF; (353). Octavio González Chon, Hospital Médica Sur, México DF; (305). Jorge Cortez Lawrenz, Hospital CIMA, Hermosillo Sonora; (228). Miguel Ángel Luna Calvo, Hospital General de Durango; (218). Eduardo Salazar Weill, Hospital N° 1 IMSS, Tepic; (207). Carlos Martínez Hernández, Hospital Regional Adolfo López Mateos, ISSSTE, México DF; (192). Julio López Cuéllar, Hospital Español, México DF; (156). Berenice López Cuéllar, Hospital del Carmen, Guadalajara; (135). Bernardo R. Encarnación, Centro Médico Nacional "Ruiz Cortines", Veracruz; (125). Marco A. Zúñiga, Centro Médico Nacional Occidente, Guadalajara; (117). Ramiro Flores Ramírez, Hospital Universitario, Monterrey NL; (113). Jorge Carrillo, José Luis Arenas, Hospital Central "Morones Prieto", SLP; (112). Alejandro García Reyes, Hospital Especialidades N° 71, IMSS, Torreón Coahuila; (102). Marco A. Alcocer, Hospital Ángeles, Querétaro; (99). Ismael Hernández Santa María, Hospital Juárez México DF; (94). Carlos Urbano Castillo, Hospital ISSSTE, Guadalajara; (87). Federico Rodríguez Wever, Hospital Ángeles del Pedregal, México DF; (80). Germán A. Gómez Briceño, Hospital General "Manuel Gea González", México DF; (76). José Luis Leyva, Centro Médico del Potosí, SLP; (74). Juan Parcero, Mario Zúñiga, Hospital Excel, Tijuana BCN; (72). José Ramón Azpiri, Hospital Christus–Muguerza, Monterrey NL; (71). Amanda Castelán, Centro Médico Nacional Obregón, Sonora; (70). Manuel Odín de los Ríos, Hospital General Culiacán, Sinaloa; (69). Enrique López Rosas, Centro de Especialidades Médicas, Jalapa Ver; (68). Guillermo Ficker, Sanatorio Español, Torreón; (64). José R. Ocampo, Hospital Santelena, México DF; (59). Samuel Guízar, Raúl Rivas, Hospital PEMEX Picacho, México DF; (59). Sergio Luna, Centro Médico Nacional IMSS, León Guanajuato; (55). Darío Lemarroy, Hospital PEMEX Villahermosa; (51). Alfredo Felipe Hoyos, Hospital Regional IMSS, Cuernavaca; (50). Juan Carlos Núñez Fragoso, Hospital General N° 1 IMSS, Durango; (49). Marco A. Alcocer, Hospital General, Querétaro; (46). Sergio Najar, Efraín Gaxiola, Hospital "Fray Bernardete", Guadalajara; (43). Enrique Gómez Álvarez, Hospital ISSSTE 20 de Noviembre, México DF; (43). Carmen Aurora Limón, Centro Médico Nacional IMSS, Puebla; (41). Julio González Jaramillo, Centro Médico Nacional "El Fénix" IMSS, Mérida Yucatán; (41). Ambrosio Cruz, PEMEX Central Norte, México DF; (39). Alfredo Pérez Gea, Centro Español, Tampico; (34). Hernán Navarrete Alarcón, ISSSTE Zaragoza, México DF; (34). Jorge Durón, HGZ N° 2 IMSS, Saltillo; (30). Miguel Beltrán, Hospital ISSSTECALLI, Tijuana BCN; (32). Jesús Manuel Canale, Hospital General del Estado, Hermosillo; (28). Luis Mario Fuentes, Hospital Star Médica, Morelia Mich; (26). Marcos Ibarra Flores, Hospital "San José" TEC de Monterrey; (21). José Luis Rodríguez, HGZ N° 6, Madero Tamps; (16). Norberto Matadamas, Hospital General, Acapulco; (15). Héctor Barragán Mar, Hospital Metropolitano, México DF; (13). Carlos Hernández Herrera, Hospital Especialidades, Monclova Coah; (9). Hugo Aguilar Castillo, Hospital "Darío Fernández" ISSSTE, México DF; (9). Marco Antonio Susarrey, Hospital Cardiomed, Ensenada BCN; (9). Abel Pavia, Hospital General SSA, México DF; (8). Miguel A. Romo, Hospital "San José", Zacatecas; (8). Demetrio Kosturakis, Arturo Monroy, Hospital CIMA, Chihuahua; (7). José Luis Álvarez Cabrera, Centro Médico Naval, México DF; (7). Adrián Medina Amarilla, Hospital ALMATER, Mexicali BCN; (5).
Agradecimiento
Agradecemos a J. Antonio González–Hermosillo, Presidente de la Sociedad Mexicana de Cardiología 2002–2003. Personal Coordinador de RENASICA II: Mely Colomer, Cristina Gaytán y Cristina Guerrero. Aventis Pharma México: Alfredo Gutiérrez, Xenia Cruz, Lorena Vasto, Miguel Wilson y Leonor Gómez.
Deseamos hacer especial mención a los miembros del Comité Directivo y a todos los investigadores involucrados en el proyecto.
$En el Apéndice aparece una lista completa de los investigadores e instituciones que participan en el registro RENASICA II.
RENASICA es un Registro Nacional de la Sociedad Mexicana de Cardiología, y tuvo un apoyo ilimitado por AVENTIS–PHARMA MÉXICO.
El protocolo, la base de datos, las estadísticas, los resultados, las conclusiones y el reporte final son responsabilidad absoluta del Comité Directivo.
Referencias
1. Howson CP, Reddy KS, Ryan TJ, Bale JR, Editors; Committee on research, development and institutional strengthening for control of cardiovascular diseases in developing countries, Institute of medicine: Control of cardiovascular disease in developing countries: research, development and institutional strengthening. Washington, DC, national Academy Press, 1998. [ Links ]
2. Chockaklingam A, Balaguer–Vintro, Achutti A, de Luna AB, Chalmers J, Farinaro E, et al: The World Heart Federation's white book: impending global pandemic of cardiovascular diseases: challenges and opportunities for the prevention and control of cardiovascular diseases in developing countries and economies in transition. Can J Cardiol 2000; 16:227–229. [ Links ]
3. Fox KAA: An Introduction to the Global Registry of Acute Coronary Events: GRACE. Eur Heart J2000;2 (Suppl F): F21–24. [ Links ]
4. Guillot F, Moulard O: Projected populations of people aged over 50 years, and estimated prevalence of myocardial infarction and ischemic stroke cumulated in 14 countries: Belgium, Canada, Denmark, Finland, France, Germany, Italy, Netherlands, Norway, Spain, Sweden, Switzerland, UK, USA. Circulation 1998; 98(Suppl 1): A1421. [ Links ]
5. Secretaría de Salud. Comunicado de prensa No. 206, 12/Septiembre/2004; http://www.salud.gob. mx/ssa_app/noticias/datos/'2004–09–12–991.html [ Links ]
6. Sistema Nacional de Información para la Salud (SINAIS). Principales causas de mortalidad general, 2002 nacional, http//www.salud.gob.mx/apps/htdocs/estadisticas/mortalidad/mortalidad.html [ Links ]
7. The Joint European Society of Cardiology/American College of Cardiology Committee. Myocardial infarction redefined—A consensus document of the Joint European Society of Cardiology/ American College of Cardiology Committee for the redefinition of myocardial infarction. J Am Coll Cardiol 2000; 36: 959–969. [ Links ]
8. Hamm CW, Bertrand M, Braunwald E: Acute coronary syndrome without ST elevation: implementation of new guidelines. Lancet 2001; 358: 1533–1538. [ Links ]
9. Bertrand ME, Simoons ML, Fox KAA, Wallentin LC, Hamm CW, McFadden, et al: Management of acute coronary syndrome in patients presenting without persistent ST–segment elevation. Eur Heart J 2002; 23: 1809–1840. [ Links ]
10. Braunwald E, Antman EM, Beasley JW, Califf RM, Cheitlin MD, Hochman JS, et al: ACC/AHA Guideline update for the management of patients with unstable angina and non–ST–segment elevation myocardial infarction – 2002. Circulation 2002; 106: 1893–1900. [ Links ]
11. Van de Werf F, Ardissino D, Betriu A, Cokkinos DV, Falk E, Fox KAA, et al: Management of acute myocardial infarction in patients presenting with ST–segment elevation. Eur Heart J 2003; 24: 28–66. [ Links ]
12. Por el Grupo Cooperativo RENASICA. El Registro Nacional de los Síndromes Isquémicos Coronarios Agudos (RENASICA). Sociedad Mexicana de Cardiología. Arch Cardiol Mex 2002; 72: S45–S64. [ Links ]
13. Alpert JS: Are data from clinical registries of any value? Eur Heart J 2000; 21: 1309–1401. [ Links ]
14. Fox KAA. Goodman SG, Klein W, Brieger D, Steg PG, Dabbous O: Management of acute coronary syndromes. Variations in practice and outcome. Findings from the Global Registry of Acute Coronary Events (GRACE). Eur Heart J 2002; 23:1177–1189. [ Links ]
15. Hasdai D, Behar S, Wallentin L, Danchin N, Gitt AK, Boersma E, et al: A prospective survey of the characteristics, treatments and outcomes of patients with acute coronary syndromes in Europe and the Mediterranean basin. (Euro Heart Survey of ACS). Eur Heart J 2002; 23: 1190–1201. [ Links ]
16. Fox KAA, Cokkinos DV, Deckers J, Keil U, Maggioni A, Steg G, on belhaf of the ENACT (European Network for acute coronary treatment investigators): The ENACT study: a pan–European survey of acute coronary syndromes. Eur Heart J 2000; 21: 1440–1449. [ Links ]
17. Wu AH, Parsons L, Every NR, Bates E: Hospital outcomes in patients presenting with congestive heart failure complicating acute myocardial infarction. A report from the Second National Registry of Myocardial Infarction (NRMI–2). J Am Coll Cardiol 2002; 40: 1389–1394. [ Links ]
18. 1994 National Hospital Discharge Survey. Washington, DC; U.S. National Center for Health Statistics, 1995. [ Links ]
19. Zaacks SM, Liebson PR, Calvin JE, Parrillo JE, Klein W: Unstable angina and non–Q wave myocardial infarction: does the clinical diagnosis have therapeutic implications? J Am Coll Cardiol 1999; 33: 107–108. [ Links ]
20. Liebson PR, Klein LW: The non–Q wave myocardial infarction revisited: 10 years later. Prog Cardiovasc Dis 1997; 39: 399–444. [ Links ]
21. Furman MI, Dauerman HL, Goldberg RJ, Yarsbeski J, Lessard D, Gore JM: Twenty–two year (1975 to 1977) trends in the incidence, in–hospital and long–term case fatality rates from initial Q–wave and non–Q–wave myocardial infarction: A multi–hospital, community–wide perspective. J Am Coll Cardiol 2001; 37: 1571–1581. [ Links ]
22. Zeymer U, Senges J: Why do we need prospective registries in patients with acute myocardial infarction? Eur Heart J 2003; 24: 1611–1612. [ Links ]
23. Rogers WJ, Canto JG, Lambrew CT, Tiefenbrum AJ, Kinkaid B, Shoultz DA, et al: Temporal trends in the treatment of over 1.5 million patients with myocardial infarction in the U.S from 1990 through 1999. The National Registry of Myocardial Infarction 1, 2, 3. J Am Coll Cardiol 2000; 36: 2056–263. [ Links ]
24. Bartnika M, Rydén L, Ferraric R, Malmberga K, Pyörälä; K, Simoonse M, et al: on behalf of the Euro Heart Survey Investigators. The prevalence of abnormal glucose regulation in patients with coronary artery disease across Europe. The Euro Heart Survey on diabetes and the heart. Eur Heart J 2004; 25: 1880–1890. [ Links ]
25. Yusuf S, Hawken S, Ounpuu S, Dans T, Avezum A, Lanas F, et al: Effect of potentially modifiable risk factors associated with myocardial infarction in 52 countries (the INTERHEART study): case–control study. Lancet 2004; 364: 937–952. [ Links ]
26. Doukky R, Calvin JE: Risk stratification in patients with unstable angina and non–ST segment elevation myocardial infarction: Evidence–based review. J Invasive Cardiol 2002; 14: 29. 215–220. [ Links ]
27. Calvin JE, Klein LW, VadenBerg B J: Risk stratification in unstable angina: prospective validation of the Braunw aid classification. JAMA 1995; 273: 136–141. [ Links ]
28. Simmons ML: Effect of glycoprotein IIb/IIIa receptor blocker abciximab in patients with acute coronary syndromes without early coronary revascularization. The GUSTO IV ACS randomized trial. Lancet 2001; 357: 1914–1915. [ Links ]
29 GUSTO V Investigators. Reperfusion therapy for acute myocardial infarction with fibrinolytic therapy or combination reduced fibrinolytic therapy and platelet glycoprotein IIb/IIIa inhibitions: the GUSTO Vrandomized trial. Lancet 2001; 357: 1905–1914. [ Links ]
30. Schwartz GG, Olsson AG, Ezekowitz MD, Ganz P, Oliver MF, Waters D, et al: Effects of atorvastatin on early recurrent ischemic events in acute coronary syndromes. The MIRACL study: A randomized controlled trial. JAMA 2001; 285: 1711–1718. [ Links ]














