Introducción
En la literatura podemos encontrar propuestas para apoyar a los estudiantes en el aprendizaje de la química. En algunos artículos (Parolo, Barbieri y Chrobak, 2004; Ramos, 2009) se ha propuesto adoptar un nuevo enfoque instruccional considerando herramientas metacognitivas, los Mapas Conceptual y la V de Gowin, las cuales ayudan a los alumnos en sus procesos de aprendizaje al hacerlos conscientes de los mecanismos que se utilizan para obtener un aprendizaje significativo.
En este documento se propone otra técnica de representación gráfica, el Mapa Híbrido, la cual permite representar la conexión y organización de los objetos químicos y químico-matemáticos, así como advertir la realización de algunos procesos cognitivos, los cuales se encuentran implicados en la resolución de los problemas que se plantean en la clase de química. Se propone al Mapa Híbrido como una ayuda para la enseñanza de la química desde el nivel básico de secundaria, hasta el nivel universitario, por ejemplo, puede ser empleado por el docente en una exposición plenaria con el objeto de presentar, analizar y reflexionar con los alumnos sobre cuáles son las estrategias que los expertos emplean cuando resuelven una situación química problematizada. El Mapa Híbrido también puede ser empleado como objeto de reflexión de la práctica docente, previo a la intervención en el aula, con la intención de identificar los conocimientos previos necesarios, los aprendizajes que se quieren desarrollar y a partir de ellos anticipar las posibles dificultades que se podrían presentar cuando los estudiantes se enfrentan a la tarea de resolver un problema químico.
Un aspecto importante de nuestra propuesta es el sustento teórico desarrollado para la técnica del Mapa Híbrido, el cual consiste en una extensión a la química escolar de algunos elementos teóricos del Enfoque Ontosemiótico (EOS) de la Matemática Educativa. La interpretación ontosemiótica del Mapa Híbrido permite describir la resolución de un problema químico en términos de un sistema de prácticas en donde participa un conjunto de objetos químicos y químico-matemáticos, así como algunos procesos cognitivos. Lo anterior proporciona al docente y al investigador en didáctica de la química, de una herramienta para el análisis de la actividad químico-matemática. Cabe señalar que el Mapa Híbrido ha sido interpretado desde algunos elementos del EOS (Moreno, 2017; Moreno, Torres, Zúñiga, 2019) así como desde extensiones de dichos elementos a la física escolar (Moreno, Angulo y Reducindo, 2018; Moreno, Zúñiga y Tovar, 2018; Moreno, Aguilar, Angulo y Ramírez, 2019).
Para mostrar la viabilidad de nuestra propuesta, se presenta la reconstrucción, representación y análisis de la actividad químico-matemática mediante el Mapa Híbrido del sistema de prácticas implicado en la resolución de dos problemas químicos que se discuten como ejemplos de problemas resueltos en el libro de texto de química Chang (2010). Mediante estos ejemplos se pretende delinear también una metodología para la construcción del Mapa Híbrido en el contexto de la química escolar.
2. Marco teórico
En esta sección se describe en un primer momento los elementos del EOS que fueron extendidos a la química y posteriormente, apoyados en la noción de objeto proveniente del Interaccionismo Simbólico (Blumer, 1969) se describe la extensión teórica, la cual será empleada para interpretar la técnica del Mapa Híbrido.
2.1. Algunos elementos teóricos del EOS
En el EOS (Godino, Batanero y Font, 2007) se argumenta que cuando un sujeto, novato o experto, resuelve un problema matemático éste lleva a cabo un sistema de prácticas (la práctica, entendida como todo lo que hace el sujeto para resolver el sub-problema) que le permiten desarrollar la resolución del problema apoyado en un conjunto de objetos matemáticos: situación problematizada, lenguaje, conceptos, propiedades, procedimiento y argumentos.
En el sistema de prácticas el sujeto también realiza procesos sobre los objetos matemáticos, algunos de estos son: idealización, por ejemplo, cuando al observar un trazo curvo en forma de “U” sobre el pizarrón piensa en una parábola; materialización, inverso a la idealización, cuando piensa en la ecuación de una recta con pendiente “1” que corta el eje ordenado en “−4” y escribe la expresión “y = x − 4”; particularización, cuando a partir de una expresión general como “ax2 + bx + c = 0” aborda un caso concreto como “2x2 − 5x + 8 = 0”; generalización, inverso a la particularización, cuando al derivar “y = 2x2” obtiene “y’ = 2 ∙ 2x2-1= 4x” y puede advertir la regla general “y’ = a ∙ nxn - 1” para derivar funciones de tipo “y = axn”; significación, cuando relaciona dos objetos matemáticos y a uno de ellos, como significante, le asigna o lo hace corresponder con el otro objeto pensado como el significado, por ejemplo, cuando al concepto de derivada “D” o de integral “I” se relaciona o se significa con la propiedad de linealidad, T(aA) = aT(A) y T(aA + bB) = aT(A) + bT(B); representación, inverso de la significación, cuando a un objeto matemático se la asigna un significante. Los dos últimos procesos pueden ser pensados en términos de una relación funcional o relación de significación llamada función semiótica, la cual relaciona a dos objetos matemáticos, uno el significante y el otro el significado.
2.2. Una extensión del EOS a la química escolar
La extensión a la química escolar de los elementos del EOS parte de la idea de que, en la resolución de problemas químicos, teóricos o experimentales, participan objetos de tipo químico y de tipo químico-matemático, éstos últimos pensados en términos de funciones semióticas las cuales permiten establecer relaciones de significación entre algunos objetos químicos y los objetos matemáticos primarios. Los objetos químicos son pensados como idealizaciones o abstracciones de la experiencia perceptual o de las mediciones que realiza el sujeto, novato o experto, en el laboratorio de química. A continuación, se describe la tipología de objetos químicos y objetos químico-matemáticos propuestos:
(i) Situaciones químicas problematizadas donde no se busca cuantificar, por ejemplo, las demostraciones experimentales recreativas tales como la del arcoíris químico, donde se emplean indicadores para la enseñanza del concepto de reacción. Situación químico-matemática problematizada, se trata de los fenómenos químicos que son objeto de estudio cuantitativo en la química, por ejemplo, los gramos de soluto que se requieren para preparar cierta cantidad de disolución de concentración conocida. Situación química o químico-matemática se nombrará con el nombre genérico problema.
(ii) Lenguaje químico, por ejemplo, fotografías, como la de la Figura 1(i) que muestra que la densidad del agua es más baja en estado sólido que en estado líquido en comparación con la del benceno, el cual, en estado sólido, se va al fondo al ser más denso que en su estado líquido; representaciones pictóricas de procedimientos químicos, por ejemplo, en la Figura 1(ii) se muestra la preparación de una disolución de molaridad conocida donde en (a) se agrega agua a un soluto sólido en un matraz volumétrico, luego en (b) se disuelve el sólido en el matraz y en (c) se agrega agua hasta el aforo, por lo que una vez conocidos el volumen de la disolución y la cantidad de soluto disuelto en ella, se puede calcular la molaridad de la disolución preparada. Se trata de lenguaje que no tiene un trasfondo matemático pero que interviene en la actividad químico-matemática.
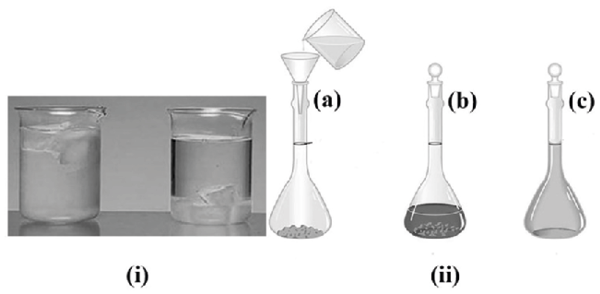
Figura 1 (i) Fotografía del agua y el benceno, (ii) preparación de una disolución. Fuente: (Chang, 2010, p. 148, 471).
También se tiene un lenguaje químico-matemático, y se refiere a las fórmulas condensadas, a las estructuras de Lewis, a las fórmulas estructurales o a los modelos de esferas y barras, a las ecuaciones químicas, a las gráficas, entre otras formas de representación. Considerando las características de índice, símbolo e ícono (Peirce, 1987), se argumenta que éstas se encuentran presentes en las ecuaciones químicas, por ejemplo, en la ecuación 2NO(g) + O2 → 2NO2(g), los signos 2NO, O2, 2NO2, +, → son símbolos debido a la relación convencional que guardan con el objeto (molécula, reacción, sentido de la reacción), lo convencional puede verse en la historia de la química, a través de la propuesta de Dalton, cuando se representaba al carbono, el hidrógeno y oxígeno mediante los pictogramas “●”, “ʘ” y “Ο”, respectivamente. Son índices ya que los coeficientes, subíndices numéricos y el signo “(g)” denotan la proporción cuantitativa de las sustancias y el estado de agregación, y también es un ícono, por la semejanza que guarda la ecuación química con la reacción.
(iii) Concepto químico (CQ), los cuales no se matematizan, por ejemplo: ácido, que se puede definir como una sustancia que produce iones de hidrógeno en solución acuosa; base, definida como una sustancia que produce iones de hidróxido en solución acuosa; entre otros. También se tiene el concepto químico-matemático (CQM), que se enuncian mediante definiciones que se pueden matematizar directamente, por ejemplo, los conceptos de: número atómico “Z”, definido como el número de protones en el núcleo de un átomo; número de oxidación de un elemento en un compuesto binario iónico sencillo que es el número de electrones que gana o pierde un átomo de ese elemento cuando forma el compuesto; mol, entendida como la cantidad de sustancia que contiene el número de Avogadro de partículas; por mencionar algunos.
(iv) Propiedad química, no matematizada, se enuncian a través de enunciados no matemáticos, como el enunciado de que el papel tornasol azul cambia a rojo cuando éste entra en contacto con una sustancia ácida. Propiedad químico-matemática (PQM), se refiere a enunciados asociados a conceptos químico-matemáticos, por ejemplo, en relación con el concepto de número de oxidación, un enunciado químico-matemático podría ser la regla del octeto de Lewis expresado como “un átomo diferente del hidrógeno tiende a formar enlaces hasta que se rodea de ocho electrones de valencia” (Chang, 2010, p. 375).
(v) Procedimiento químico, tiene que ver con las técnicas experimentales de laboratorio y se relaciona con el objeto procedimiento químico-matemático mediante el establecimiento de funciones semióticas. Por ejemplo, el procedimiento de valoración, que consiste en agregar una disolución patrón a otra disolución de concentración desconocida hasta completar la reacción entre ambas disoluciones, que permite calcular (procedimiento químico-matemático) la concentración de la disolución desconocida a partir del volumen de la disolución desconocida y del volumen y concentración de la disolución patrón. Procedimiento químico-matemático (PrQM), se refiere a las técnicas de cálculo o algoritmos tales como el balanceo de ecuaciones que resulta de gran importancia para cualquier estudio cuantitativo en una reacción química.
(vi) Argumentos químicos, intervienen en los procedimientos químicos experimentales y justifican los pasos que se siguen. Argumentos químico-matemáticos, se refieren a enunciados que permiten justificar o validar los procedimientos químico-matemáticos.
A partir de la tipología anterior argumentamos que, en el contexto de la química escolar, cuando un sujeto (aprendiz o experto) resuelve una situación química o situación químico-matemática problematizada, éste lleva a cabo un conjunto de prácticas donde intervienen tanto objetos químicos como objetos químico-matemáticos. Las prácticas son organizadas por el sujeto en un sistema de prácticas que le permiten resolver la situación problematizada inicial.
Considerando la relación entre objetos químicos y objetos matemáticos argumentamos que el sujeto realiza ciertos procesos cognitivos, por ejemplo, idealización, cuando un sujeto al observar una representación pictórica como la de la Figura 1(ii) en (a) desmaterializa y piensa en un soluto contenido en un matraz, o bien, cuando en el punto en la estructura de Lewis de un compuesto es desmaterializado y pensado como un electrón; particularización, cuando el concepto químico-matemático de molalidad
3. Construcción e interpretación del Mapa Híbrido químico
Una manera de describir la construcción e interpretación ontosemiótica del Mapa Híbrido puede ser a partir de un ejemplo. La construcción del mapa requiere de la recopilación de la producción oral y escrita realizada por el sujeto al resolver el problema. La producción oral puede obtenerse al solicitar al sujeto resolver el problema en voz alta, esto para conocer las propiedades, argumentos, conceptos e interpretaciones que fueron pensados por el sujeto y que no fueron materializados de forma escrita. La producción y el mapa correspondiente se nombrarán epistémicos si corresponde a un experto (profesor) y cognitivos si corresponde a un estudiante.
Una vez que se tiene la producción del sujeto, el siguiente paso es transcribir la producción. Cabe señalar que, en el caso epistémico, como transcripción también se puede tomar lo que presenta el autor de algún libro de texto. En este trabajo se describe cómo construir e interpretar el Mapa Hibrido a partir de lo que presenta el libro de Chang (2010) en dos ejemplos que describen la resolución de problemas relacionados con el concepto de mol y de cantidad de producto obtenido a partir de cierta cantidad de reactivo. La producción de Chang (2010) es complementada por los autores con la finalidad de mostrar cómo puede ser mejorada y presentada en el aula mediante el Mapa Híbrido.
A diferencia de la heurística que se propone para la construcción de los Mapas Conceptuales, la construcción del Mapa Híbrido se apoya en la extensión teórica de los elementos del EOS a la química escolar. A continuación, se presentan los pasos para la construcción del mapa híbrido químico:
(i) Identificar las prácticas que se ponen en juego a partir de la transcripción de la producción oral y escrita de la resolución del problema.
(ii) Identificar los objetos químicos y químico-matemáticos que intervienen en cada práctica. Los conceptos aparecen en forma de símbolos en el registro escrito y otros son señalados verbalmente; argumentos, que se forman a partir de las conexiones entre los conceptos identificados; propiedades, que se presentan mediante la conexión de conceptos o aparecen como expresiones algebraicas; procedimiento, que se observa en el registro escrito.
(iii) Se presentan los nombres de las prácticas en recuadros de manera secuencial, conectados mediante palabras enlace para indicar la manera en que éstas se coordinan.
(iv) Iniciando con la primera práctica, se conectan los conceptos correspondientes mediante palabras enlace según el orden del discurso del sujeto. La conexión de los conceptos lleva a reconstruir los argumentos y las propiedades señaladas. En el caso de las prácticas donde aparece el objeto procedimiento, se requiere conectar dicho objeto con los conceptos, argumentos o propiedades.
(v) Una vez representadas las prácticas y los objetos, se establecen conexiones entre los objetos que no fueron señaladas explícitamente por el sujeto que resolvió el problema.
La construcción del Mapa Híbrido puede realizarse a partir de distintas fuentes, por ejemplo, el docente puede resolver un problema químico que desee discutir en clase y a partir de su producción construir el mapa o bien el docente puede solicitar a un alumno la resolución de algún problema y a partir de la producción del alumno proceder a elaborar el mapa, sin embargo, el análisis de los mapas deberá realizarse a partir de la extensión teórica de los elementos del EOS a la química escolar. El Mapa Híbrido puede construirse mediante el software CmapTools (IHMC, 2021). En la siguiente sección se describe la construcción del mapa mediante los pasos anteriores.
3.1. Una aplicación del Mapa Híbrido en la química escolar
A continuación, se describe la construcción del Mapa Híbrido correspondientes a la resolución de dos problemas que se presentan como ejemplos en el libro de química general de Chang (2010). La primera construcción es un mapa horizontal obtenido a partir de la producción que presenta el autor del libro cuando resuelve un problema que pone en juego el concepto de mol. La segunda construcción es un mapa con orientación vertical donde se aborda el problema de calcular la cantidad de producto que se puede obtener a partir de cierta cantidad de reactivo. Por cuestiones de espacio, en ésta última aplicación solo se presenta el mapa y se describe cómo leerlo. Así mismo, se añadieron las etiquetas CQ, CQM, PQM y PrQM en cada mapa para indicar algunos conceptos químicos, conceptos químico-matemáticos, propiedades químico-matemáticas y procedimientos químico-matemático, respectivamente, presentes en los sistemas de prácticas químico-matemáticos.
Construcción del Mapa Híbrido relacionado con el concepto de mol
El mapa fue elaborado a partir de la producción en el ejemplo 3.2, Figura 2, que resuelve el problema: “El helio (He) es un gas valioso utilizado en la industria, en investigaciones en las que se requiere baja temperatura, en la que los tanques para buceo profundo y para inflar globos. ¿Cuántos moles de átomos de He hay en 6.46 g de He?” (Chang, 2010, p.83).
En la producción se identifican tres prácticas: práctica I, interpretación de la situación-problema; práctica II, determinar el factor de conversión; práctica III, obtener el número de moles, Figura 2. También se identifican 36 objetos químicos y químico-matemáticos, 12 objetos en la práctica I numerados del 1 al 12, 15 objetos en la práctica II numerados del 13 al 27 y 9 objetos en la práctica III numerados del 28 al 36. La construcción del mapa se inicia con la descripción de la situación química y el planteamiento del problema mediante la pregunta focal, ver A en la Figura 3 y, posteriormente, en la parte inferior se escriben los nombres de cada práctica de manera consecutiva de izquierda a derecha, ver I, II y III en la Figura 3.
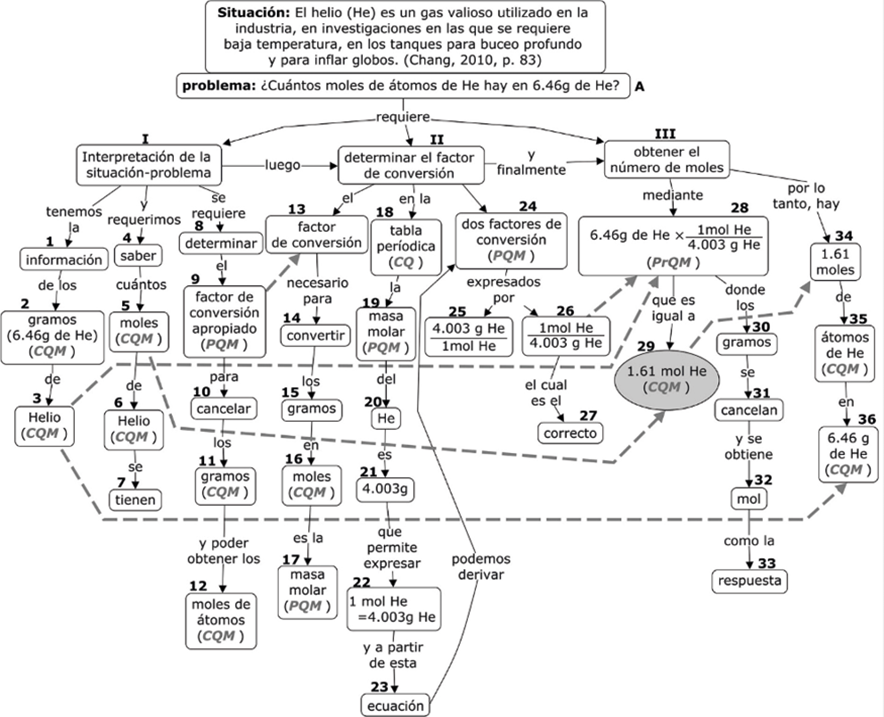
Figura 3 Mapa Híbrido asociado al ejemplo 3.2. Fuente: elaboración propia mediante CmapTools (Moreno, 2020).
Los 12 conceptos en la práctica I permiten enunciar tres argumentos: (i) Tenemos la información de los gramos de helio, donde participan los conceptos 1, 2 y 3 relacionados con el dato de los gramos de helio que proporciona el problema; mediante los conceptos 4, 5, 6 y 7 se identifica el problema a ser resuelto Y requerimos saber cuántos moles de helio hay; y advierte la resolución del problema mediante los conceptos 8, 9, 10, 11 y 12 al señalar Determine el factor de conversión apropiado de manera que cancele los gramos y pueda obtener los moles. Los argumentos anteriores son representados en el mapa híbrido horizontal de la Figura 3 mediante las rutas de lectura 1-2-3, 4-5-6-7 y 8-9-10-11-12. Nótese que para representar ésta última ruta de lectura se modificó, conservando el significado, la producción I de la Figura 2, por lo que en la Figura 3 se agregó la palabra enlace se requiere en la ruta I-8 en lugar del concepto 8 de la Figura 1, asimismo, el concepto moles de átomos indicado con 12 en la Figura 3 se corresponde con el concepto moles numerado con 12 en la Figura 2. En general, es posible realizar el mismo proceso anterior con el resto de las prácticas, también se pueden realizar modificaciones de algunas palabras preservando los significados o el sentido de los argumentos y propiedades.
La práctica II es una particularización de la propiedad químico-matemática general de masa molar. Los objetos 13 a 17 en la Figura 2 son representados mediante la ruta de lectura 13-14-15-16-17 de la Figura 3. Por otra parte, los objetos 18 a 23 de la Figura 2 se representaron en el mapa mediante la ruta 18-19-...-23 en la Figura 3. La propiedad químico-matemática general de masa molar indicado mediante 13-14-15-16-17, que fue particularizado a través de 18-19-...-23, permite establecer una relación que se representa mediante 22-23, Figura 3, y luego advertir dos factores de conversión en 24, por un lado, se tiene el factor 25 y por otro el 26, sin embargo, éste último es el que se considera útil (ver la ruta 26-27) para la resolución del problema.
En la práctica III se representa el procedimiento 28, el cual se explica mediante el argumento 30-31-32-33. El procedimiento conduce al número de moles de He en 29, el cual es validado mediante la tesis III-34-35-36, ver la Figura 3.
Es importante destacar la participación de los CQ, CQM, PQM y PrQM indicados en el mapa, algunos de los cuales fueron particularizados, por ejemplo, el CQM de mol es particularizado al caso del Helio en 4-5-6-7, la PQM de masa molar se particulariza al pasar de 17 (propiedad general) a 19-20 (como propiedad particular acerca del He) y también son particularizados los CQM de átomos y masa en gramos de helio mediante 35 y 36 respectivamente, sin embargo, no se lleva a cabo la particularización del CQ de tabla en periódica en 18. En relación con la PQM de masa molar 19, se resalta el señalamiento explícito de la función semiótica entre el objeto matemático razón y el concepto químico matemático de masa de un mol de He, el cual lleva a plantear 24 y a elegir 26.
A diferencia de la producción de Chang (2010), que hace énfasis en una estrategia y una solución, Figura 2, mediante el Mapa Híbrido se habla de tres prácticas, una de interpretación de la situación-problema, otra referente a la particularización de la propiedad químico-matemática de masa molar al caso del He y una tercera procedimental que le lleva a resolver el problema. La presentación del mapa en la clase podría motivar la discusión respecto al uso de 26 y a la omisión de 25; el docente podría cuestionar a los estudiantes acerca de qué datos tendría que proporcionarse en el problema A, Figura 3, para habilitar el uso del factor de conversión 25.
Construcción del Mapa Híbrido relacionado con la cantidad de productos a partir de reactivos
El Mapa Híbrido de la Figura 4 representa esquemáticamente la resolución del problema: “Los metales alcalinos reaccionan con agua para formar hidrógeno gaseoso y el hidróxido correspondiente. Una reacción común en la que ocurre entre el litio y el agua es 2Li(s) + 2H 2 O(l) → 2LiOH(ac) + H2 (g) ¿Cuántos gramos de Li se necesitan para producir 9.89g de H2?” (Chang, 2010, p.102).
La resolución de la situación-problema, A en la Figura 4, implica la realización de cuatro prácticas: práctica I, interpretación de la situación-problema; práctica II, convertir gramos de H2 a moles de H2; práctica III, convertir moles de H2 a moles de Li; práctica IV, convertir moles de Li a gramos de Li, Figura 4. La figura 4 muestra el mapa con orientación vertical que inicia con la situación problematizada A y, del lado izquierdo, se presentan las prácticas I, II, III y IV de manera descendente, mientras que los objetos de cada práctica se agregan horizontalmente hacia la derecha.
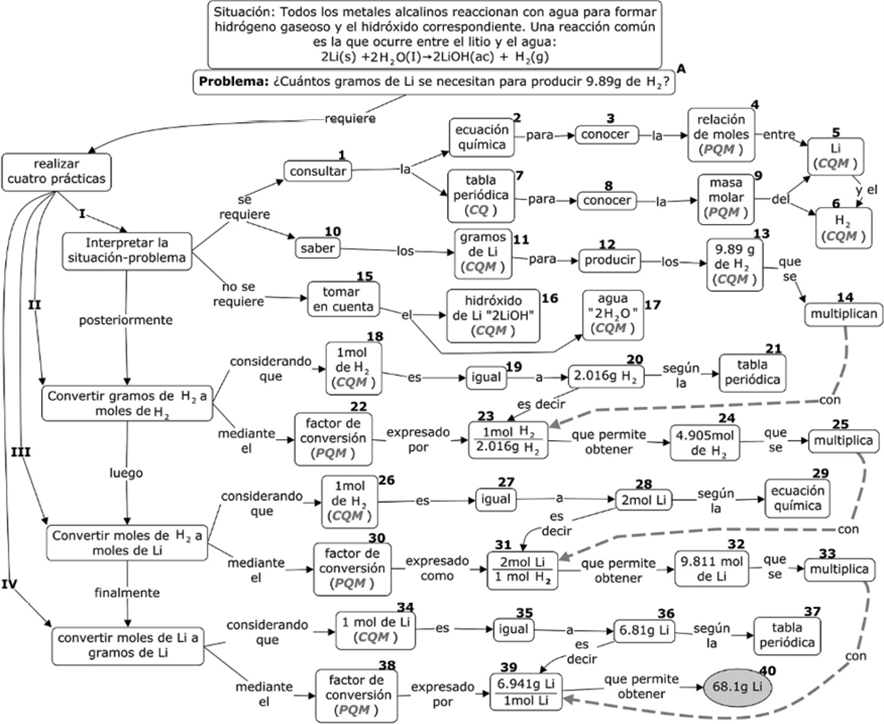
Figura 4 Mapa Híbrido correspondiente al ejemplo 3.14. Fuente: elaboración propia mediante CmapTools (Moreno, 2020).
En la práctica I se argumenta que se requiere indagar la propiedad general de la relación molar en la ecuación química mediante 1-2-3-4-5-6, se argumenta que es necesario considerar la propiedad de masa molar en 1-7-8-9-5 y 6 y se identifica el problema mediante el argumento 10-11-12-13. Esta práctica fue complementada por los autores del presente trabajo mediante el argumento I-15-16 y I17, para fijar la atención únicamente en el Li y en el H2.
La particularización de la propiedad químico-matemática general de masa molar en la práctica I, ruta 1-7-8-9-5 y 6, permite realizar la práctica II. La propiedad general particularizada a través de 18-19-20-21 y que permite establecer el factor de conversión 22-23, el cual permite llevar a cabo el procedimiento 13-14-23-24 para convertir los 9.89g de H2 que proporciona el problema a su cantidad correspondiente en unidades molares en 24.
La realización exitosa de la tercera práctica requiere tomar en cuenta, por un lado, la propiedad general emergente de la relación molar en la reacción 1-2-3-4-5-6 de la práctica I y, por otro lado, el concepto emergente 24 de la práctica II. Mediante la primera, se advierte la propiedad químico-matemática particularizada 26-27-28-29 y a su vez permite establecer la propiedad químico-matemática 30-31. A partir de esta propiedad, se lleva a cabo el procedimiento 24-25-31-32 que conduce a obtener el número de moles de Li requerido, objeto emergente 32.
Por último, en la cuarta práctica se realiza la conversión del objeto emergente 32 de unidades molares a unidades de masa en gramos. Para esto se lleva a cabo la particularización de la propiedad general de masa molar mediante 34-35-36-37, que permite plantear la relación 38-39, para poder llevar a cabo el procedimiento 32-33-39-40, para obtener el resultado 40 en IV.
Es importante hacer referencia a algunos CQ, CQM y PQM señalados en el mapa de la Figura 4, al igual que en el problema anterior, algunos conceptos son particularizados y otros no, por ejemplo, la propiedad general de la relación molar en la reacción indicada mediante 1-2-3-4-5-6 fue particularizada en la práctica III en 26-27-28-29. También se particularizó el concepto químico-matemático general de masa molar 1-7-8-9 en las prácticas II, con 18-19-20-21, y en IV con 34-35-36-37. Esto nos lleva a distinguir el objeto llamado factor de conversión, señalado mediante 22, 30 y 38, al tomar en cuenta la noción de función semiótica. Los objetos 22 y 38 son CQM pues se trata de la función semiótica que relaciona el concepto matemático de razón con el concepto químico-matemático de masa de un mol de sustancia, mientras que 30 es una PQM pues surge de la función semiótica entre el concepto matemático de razón y la propiedad química de la relación molar entre los compuestos que intervienen en la reacción; se trata de factores de conversión que poseen significados distintos.
En los mapas de las Figuras 3 y 4 emergieron objetos en la realización de las prácticas, algunos de los cuales fueron empleados como insumos para la realización de las prácticas subsecuentes, por ejemplo, en la Figura 3, el objeto 26 puede ser considerado como objeto emergente de la práctica II, el cual es empleado en la práctica III en la realización del procedimiento 28. En la Figura 4, el objeto emergente 24 de la práctica II es empleado en el procedimiento 24-25-31-32 en la práctica III para calcular los moles de Li requeridos.
Por otra parte, el objeto procedimiento químico-matemático interviene solo en algunas prácticas de los mapas, por ejemplo, en la primera práctica del mapa de la Figura 3 no se observa el objeto procedimiento pues se trata de una práctica interpretativa, sin embargo, en la primera práctica del mapa de la Figura 4 sí es posible advertir las distintas etapas del procedimiento.
Cabe señalar que los mapas de las Figuras 3 y 4 muestran sistemas de prácticas que pueden catalogarse algorítmicas, pues se presenta una escasa significación de los resultados obtenidos en términos de la situación química planteada. Lo anterior podría llevar a los estudiantes a construir explicaciones y a hacer predicciones diferentes de las que son aceptadas por la ciencia (Galagovsky y Bekerman, 2009).
4. Reflexiones finales
La extensión de algunos elementos del EOS a la química escolar permite interpretar el Mapa Híbrido. La extensión considera que cuando un sujeto resuelve un problema químico, este lo descompone en subproblemas que resuelve mediante prácticas que son coordinadas en un sistema de prácticas que permite la resolución del problema. En el sistema de prácticas se realizan procesos sobre objetos químicos y químico-matemáticos, los primeros de naturaleza material son considerados como idealizaciones de la experiencia perceptual del sujeto en el laboratorio de las mediciones experimentales. Algunos de los objetos químicos idealizados se relacionan mediante funciones semióticas con los objetos matemáticos, dando lugar a los objetos químico-matemáticos.
Los mapas epistémicos construidos a partir de Chang (2010) podrían emplearse para mostrar a los alumnos los objetos intervinientes y sus conexiones, los procesos, las prácticas y su coordinación en el sistema de prácticas. Complementar el mapa resultante al agregar nuevos objetos provenientes de los conocimientos disciplinares y de la experiencia del docente, permitirá adaptar la enseñanza al contexto de los estudiantes, por ejemplo, los conocimientos previos de los alumnos, la consideración de conceptos vistos en la clase pasada, las dificultades de aprendizaje, por mencionar algunos.
En los Mapas Híbridos construidos se identifican aspectos en común, por ejemplo, se puede advertir que la primera práctica es interpretativa, la cual consiste en considerar los datos que proporciona la situación-problema, ya sea un dato numérico que se refiere a la cantidad de cierta sustancia o bien a la ecuación química, también es posible percatarse de la identificación del problema a ser resuelto. La realización de esta primera práctica es crucial para garantizar el éxito al resolver el problema.
También se particularizaron propiedades químico-matemáticas generales. En el primer mapa se particularizó la propiedad de la masa molar para el He, en el segundo mapa se particularizó la propiedad general de que los coeficientes junto a las fórmulas de una ecuación química balanceada indican el número de moles de la sustancia correspondiente. Se enfatiza que señalar o motivar la realización de los procesos en el aula podría ayudar a una mejor comprensión de la resolución de los problemas al identificar los saberes que se ponen en juego.











 nueva página del texto (beta)
nueva página del texto (beta)



