Introducción
El desarrollo articular empieza secundariamente dentro de las condensaciones mesenquimales precoces del hueso cartilaginoso, aproximadamente alrededor de la quinta semana de gestación. Entre la séptima y octava semana aparecen los espacios articulares, así como movimientos de las extremidades, lo cual es esencial para el desarrollo normal.1
La artrogriposis múltiple congénita (AMC) es una enfermedad que se caracteriza por múltiples contracturas articulares, así como debilidad muscular. Habitualmente el diagnóstico es al nacimiento.
El término artrogriposis se deriva de las palabras griegas “arthro” (articulación) y “gryposis” (torcida). Este término incluye un conjunto de enfermedades en la que los niños afectados presentan al menos dos articulaciones rígidas en un mismo miembro, además de la rigidez de músculos de miembros superiores, inferiores y del dorso. Los músculos pueden estar ausentes, reducidos en tamaño o en número, o bien, estar reemplazados por tejido fibroso o grasa.
El grado de afectación varía de un paciente a otro; la deformidad clásica es bilateral y simétrica. Otto utilizó el término miodistrofia congénita en 1841. Stern usó la denominación de artrogriposis múltiple congénita en 1923. Sheldon usó por primera vez la palabra amioplasia congénita en 1992 relacionándola con una supuesta hipoplasia o aplasia muscular. Hall y colaboradores denominaron en 1983 a la amioplasia como la forma de AMC que afecta las cuatro extremidades.2,3
La incidencia de estos desórdenes se estima entre uno por cada 3,000 a 5,000 nacidos vivos.4 La mayoría de los niños afectados presentan al menos una lesión ortopédica que requiere atención médica.5 La forma de artrogriposis más frecuente es la amioplasia, con una incidencia de 1/10,000 nacidos vivos.6
En general, cualquier causa que lleve a la reducción de los movimientos fetales puede guiar a contracturas congénitas y, en casos graves, progresar a deformación. En los últimos 30 años se han identificado diferentes tipos de artrogriposis, así como las posibles causas, incluyendo las genéticas.7 Se han señalado también alteraciones en el desarrollo o funcionamiento de los músculos, del sistema nervioso central (SNC) o nervios periféricos, así como anormalidades neuromusculares de la placa terminal. Asimismo, se ha relacionado a limitación de espacio o restricción de movimiento en útero por oligoamnios, gestaciones múltiples, miomas o malformaciones uterinas. Además, por la exposición a misoprostol, penicilamina, inhibidores de la enzima convertidora de angiotensina (ECA), relajantes musculares. Por último, a enfermedades maternas: distrofia miotónica, miastenia gravis, diabetes mellitus, esclerosis múltiple.8,9
El misoprostol también se ha relacionado con el síndrome Moebius (SM), sugiriendo que tiene un efecto vasoconstrictor, que resulta en isquemia transitoria fetal afectando principalmente los núcleos de los nervios craneales abducens y facial. Asimismo, se ha propuesto que, al producir contracciones uterinas intensas y prolongadas, generaría reducción del flujo sanguíneo en ciertas áreas (por ejemplo: nervios craneales) y la restricción del crecimiento y movimiento fetal adecuado.10
En cuanto a los aspectos clínicos, en los pacientes con amioplasia, el tejido muscular es atrófico, el cual es reemplazado por tejido graso y fibroso. Las cuatro extremidades están involucradas en un patrón simétrico, y los individuos suelen tener inteligencia normal y no presentan malformaciones.11 Típicamente los pacientes se describen con hombros rotados internamente y aducidos, flexión palmar y contracturas de flexión de articulaciones interfalángicas distales, luxación de cadera, contracturas de extensión de rodillas y deformidad en pie equinovaro grave.12
El segundo tipo más común es la artrogriposis distal, una alteración con herencia autosómica dominante, que es un grupo de síndromes principalmente con contracturas articulares distales de las extremidades. Se han descrito al menos 10 tipos diferentes de artrogriposis distal.13,14
Los niños con AMC pueden presentarse con malformaciones congénitas mayores en corazón, pulmones, SNC, aparato digestivo, entre otros. El pronóstico puede ser grave; por ejemplo, cuando se asocia con malformaciones múltiples puede producir muerte intraútero o en el periodo neonatal, por lo general secundario a hipoplasia pulmonar.15 En la forma clásica, el pronóstico está determinado por la limitación funcional que producen las contracturas articulares.16,17
El objetivo de esta comunicación es presentar el caso de un recién nacido (RN) con AMC en quien además se identificó hidrocefalia congénita, pero que tenía antecedente de uso de misoprostol en las primeras etapas de la gestación, como posible factor causal.
Presentación del caso
Recién nacido masculino, hijo de madre de origen Togole-Beninua de 20 años que vivía en la localidad de Kango de la ciudad de Libreville, capital de Gabón, en África. Antecedentes obstétricos: cuatro gestaciones, dos partos, un aborto espontáneo y tiene dos niños vivos; la madre no deseaba el embarazo y trató de abortar con el uso de misoprostol, pero sin lograrlo. Posteriormente, aceptó el embarazo. Recibió atención prenatal por enfermera obstetra (Sage-femme); asistió a algunas consultas y se le administró la vacuna antitetánica.
El parto ocurrió en junio de 2014 en el hospital de Kango, fue eutócico, de presentación cefálica, líquido amniótico claro. La evaluación del Apgar fue de 4/7, con edad gestacional de 37.5 semanas y peso de 1,900 gramos. El personal de asistencia médica decidió trasladarlo al séptimo día de vida al servicio de Neonatología del Hospital Central Universitario de Libreville porque sospechaban que tenía múltiples malformaciones congénitas, y para ofrecer mejores cuidados médicos.
Por las condiciones generales, que se pueden observar en la Figura 1, se solicitan diversos estudios. En ecografía transfontanelar se identificó hidrocefalia congénita; mientras que la ecografía abdominal fue normal. Los especialistas de Ortopedia indican sólo fisioterapia. Por su parte, Neurocirugía sugiere intervención quirúrgica para colocar derivación ventrículo-peritoneal por la hidrocefalia congénita activa.
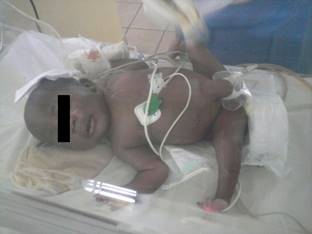
Figura 1: Fotografía tomada en las primeras horas de vida del recién nacido con artrogriposis múltiple, dentro de la incubadora.
Al mes de nacido se realizó derivación ventrículo-peritoneal sin complicaciones. Debido a que continuó con evolución favorable, se egresó para continuar seguimiento de manera ambulatoria por Neurocirugía, Neonatología y Ortopedia. Cabe señalar que no se realizaron estudios genéticos.
Discusión
Según Hall, el término AMC fue acuñado para describir a RN con múltiples contracturas congénitas.18 La artrogriposis describe múltiples contracturas congénitas que son parte de más de 300 enfermedades diferentes.19,20 La etiología subyacente sigue siendo motivo de investigación.17,20
Se conoce que muchas mujeres, especialmente en países con leyes restrictivas para el aborto y con situación económica difícil, intentan terminar un embarazo temprano con misoprostol, aunque debido a la falta de información, lo utilizan en una variedad de formas, tanto de dosis como en etapas del embarazo. El misoprostol es una droga sintética análoga de la prostaglandina I 2, se utiliza en la práctica obstétrica para maduración cervical, aborto médico, evacuación del útero en caso de muerte fetal o embrionaria y en inducción del trabajo de parto. La exposición intraútero puede causar anomalías en el feto, siendo las más frecuentes los defectos en las extremidades con acortamiento o amputación de uno o más dedos, pies en equinovaro y alteraciones de los pares craneales.21 Misoprostol está reconocido como teratógeno, ya que causa constricciones anulares en miembros inferiores, AMC, hidrocefalia, holoprosencefalia, extrofia vesical y síndrome de Moebius.22
En el diagnóstico de contracturas múltiples congénitas o artrogriposis múltiple congénita, deben considerarse muchos más padecimientos que se clasifican según su presentación en:
1. Daño primario de extremidades,23 como en el síndrome de Bruck, con incidencia menor a uno por cada millón de RN. Este padecimiento combina osteogénesis imperfecta y AMC, que se manifiesta con fracturas múltiples y recurrentes, así como con contracturas articulares congénitas con o sin pterigium, escoliosis y osteoporosis. Puede haber escleras azules y, por lo general, tienen dentinogénesis imperfecta o hipoacusia.24
2. Daño musculoesquelético más otra anomalía sistémica,10 como en el síndrome de Larsen, que es una alteración de la formación del tejido conectivo con patrón autosómico dominante y autosómico recesivo, que ocurre en 1:100,000 nacidos. Se caracteriza por la asociación de múltiples dislocaciones articulares (cadera, rodillas y codos), y dismorfias faciales: abombamiento frontal, puente nasal deprimido, hipertelorismo y facies plana; además presentan deformidades en manos y alteraciones espinales.25
También puede haber síndrome de pterigium múltiple tipo Escobar, que se caracteriza por contracturas articulares en grados variables principalmente en cuello y grandes articulaciones. En cuanto a características faciales: facies sin expresión, paladar alto, boca pequeña, retrognatia y paladar hendido.26
3. Daño musculoesquelético más alteraciones del SNC o discapacidad intelectual o letal,23 como en el síndrome de Marden-Walker. Esta es una alteración en el tejido conectivo que incluye dismorfias faciales: facies tipo máscara, blefarofimosis, boca pequeña, micrognatia, paladar alto o hendido, pabellones auriculares de baja implantación. Además, los pacientes tienen múltiples contracturas articulares congénitas, masa muscular disminuida, talla baja, retraso psicomotor severo, así como anomalías renales, cardiovasculares o cerebrales.27
Por todo lo anterior, en los casos con AMC se recomienda la búsqueda etiológica específica, con la finalidad de establecer un consejo genético. Además, se requiere la participación de diversas especialidades para lograr mejorar el pronóstico, tanto de vida como funcional.6,28 En este último punto se debe destacar la importancia de iniciar la intervención ortopédica y la rehabilitación lo más temprano posible. La corrección apropiada de las contracturas requiere tratamiento ortopédico en la mayoría de los casos, lo que es complejo y con alta tasa de recurrencia. En general, estos pacientes requerirán de múltiples cirugías para liberar las contracturas y corregir las deformidades. Los procedimientos ortopédicos incluyen: yesos correctivos en las primeras etapas de la vida, liberaciones o alargamientos tendinosos, corrección del pie equinovaro o talo valgo, entre otros.











 nueva página del texto (beta)
nueva página del texto (beta)


