Antecedentes
El síndrome de Guillain Barré (SGB) es de instauración aguda, afecta al sistema nervioso periférico y puede presentarse en cualquier persona sin importar la edad, sexo o condición social, sin embargo, existe una tendencia en personas mayores de sexo masculino.1 El síndrome se divide en subtipos electrofisiológicos, como la polineuropatía desmielinizante inflamatoria aguda (AIDP, por sus siglas en inglés), neuropatía axonal motora aguda (AMAN, por sus siglas en inglés), neuropatía axonal motora sensitiva aguda (AMSAN, por sus siglas en inglés) y otros subtipos regionales.2,3 Existe también una clasificación clínica: clásica sensoriomotora -la más común-, puramente motora o sensitiva, síndrome de Miller Fisher (MFS, por sus siglas en inglés), paraparética, parálisis facial bilateral con parestesias, encefalitis de tronco encefálico de Bickerstaff y faríngeo cérvico braquial.2 Aunque todavía se desconoce la etiología exacta de este síndrome, se ha asociado con algunas infecciones virales, ya que originan una respuesta inmune del organismo y, a su vez, anticuerpos tipo inmunoglobulina G (IgG), anti gangliósidos monosialicos (GM1) disialicos GD, trisialicos (GT) o tetrasialico (GQ), que atacan las vainas de mielina de los nervios.4,5 Esta afectación de la mielina produce una degeneración axonal y una mala conducción eléctrica a los músculos, la cual en casos severos causa una pérdida axonal extensa y la degeneración de las neuronas motoras.6,7
La clínica del paciente con SGB se caracteriza por la presencia de debilidad muscular simétrica ascendente de predominio distal, que generalmente inicia en miembros inferiores y se extiende a las extremidades superiores, y que incluso puede comprometer los pares craneales, especialmente el séptimo, generando una disminución o ausencia de los reflejos osteotendinosos.1 De igual manera, en el caso de pacientes mayores de 55 años que ingresan con un cuadro severo, el requerimiento de asistencia ventilatoria y la afectación de los pares craneales se asocian a un mal pronóstico.8 El síndrome progresa de dos a cuatro semanas aproximadamente y luego alcanza un nadir o meseta, seguido de una recuperación de cinco a ocho semanas en adelante.1,9 Sin embargo, el tratamiento inadecuado no solo trae consigo una recuperación más lenta, sino que produce secuelas como déficit residual permanente e incluso la muerte, cuando hay compromiso de carácter respiratorio.1,10
El SGB se asocia a infecciones producidas por microorganismos como Campylobacter jejuni, Haemophilus influenzae, Mycoplasma pneumoniae, herpevirus y arbovirus; un 60% de los casos se atribuyen a dichas infecciones.5,11,12 Desde principios del año 2015 hasta el año 2019, en Colombia se presentó un aumento en el número de casos reportados de este síndrome asociados a la infección por virus del zika, reportándose una incidencia de cuatro por 100.000 habitantes.12-15 El SGB es el más frecuente de los síndromes de desmielinización a nivel mundial, con una incidencia de 0,3 a 3 por 100.000 habitantesaño, la cual crece a medida que aumenta la edad.16,17
En Medellín se han realizado dos estudios recientes sobre el SGB. El primero, elaborado durante los años 20012005 en el Hospital San Vicente Fundación, estimó una incidencia de 5 por cada 10.000.000 habitantes e incluyó la descripción de 46 pacientes. El segundo se llevó a cabo en el Instituto Neurológico de Colombia y reportó los casos de 25 pacientes atendidos entre el 2006 y el 2012.18,19 En el presente estudio se identifica a pacientes que desarrollaron SGB y se describen las características clínicas de esta patología, así como los tratamientos de pacientes de tres instituciones especializadas de la ciudad de Medellín.
Métodos
Esta investigación transversal descriptiva identificó las características clínicas y sociodemográficas de pacientes con SGB durante el lapso de 2015 a 2020 según registros del Hospital Alma Máter de Antioquia, el Hospital General de Medellín y el Instituto Neurológico de Colombia, ubicados en la ciudad de Medellín. La población del estudio fue el total de personas diagnosticadas con el código diagnóstico G61.0. Los pacientes con dicho código que eran atendidos por una condición diferente al SGB fueron excluidos.
De acuerdo a la resolución 008430 de 1993 y la evaluación emitida por parte del comité de bioética, el presente estudio se clasifica como sin riesgo. El protocolo fue presentando y aprobado por el comité de ética institucional y los comités de ética y científicos de cada institución, para obtener acceso a la información de las historias clínicas de los pacientes diagnosticados con SGB. Las historias clínicas se evaluaron para determinar si cumplían con los criterios de Brighton, que van desde el nivel 1, el de más alta certeza, hasta el nivel 4, que representa un posible diagnóstico de SGB.
Para el análisis estadístico, los datos recolectados a partir de dichas historias clínicas fueron almacenados en una base de datos de Excel de acuerdo a variables sociodemográficas y clínicas y posteriormente analizados en Jamovi 1.6.16. En el caso de las variables cualitativas, se calcularon las frecuencias absolutas y relativas, y se determinó la distribución de las variables cuantitativas mediante la prueba Shapiro Wilk. Con respecto a las variables que presentaron una distribución normal, se utilizó la media con desviación estándar, y en el caso contrario (distribución no normal) se emplearon medianas y rangos inter-cuartiles. Además, se evaluó la correlación entre el puntaje obtenido en la escala Hughes y los días con ventilación mecánica por medio del coeficiente de correlación de Spearman.
Resultados
En total se identificaron 282 historias clínicas con el código diagnóstico de SGB, de las cuales se excluyeron 162 por presentar un diagnóstico diferente, fuera de las fechas establecidas, o falta de datos asociados con la enfermedad.
En total, 120 historias clínicas fueron analizadas, siendo el sexo masculino ligeramente más frecuente y el rango de edad de 3-85 años (Tabla 1). Los municipios del departamento de Antioquia que registraron un mayor número de historias clínicas con diagnóstico de SGB durante el periodo examinado fueron Medellín (39.81%) y Bello (10.62%). En el año 2015 se registró la mayor cantidad de casos de SGB, mientras que en 2019 y 2020 se presentaron 9 casos por año, lo cual indica una disminución de 80% de los casos (Tabla 1).
Tabla 1 Características sociodemográficas y clínicas al ingreso de pacientes con SGB
| Categorías | n | % |
|---|---|---|
| Femenino/Masculino | 51/69 | 42.5 %/57.5 % |
| Edad (Media / DE) | 50,29 | 20.89 |
| Año de diagnóstico | ||
| 2015 | 46 | 38.33 % |
| 2016 | 32 | 26.67 % |
| 2017 | 12 | 10 % |
| 2018 | 12 | 10 % |
| 2019 | 9 | 7.5 % |
| 2020 | 9 | 7.5 % |
| Antecedentes previos al diagnóstico | ||
| Diarrea | 29 | 24.17 % |
| Infección respiratoria | 37 | 30.83 % |
| Infección viral | 11 | 9.17 % |
| Antecedentes patológicos | ||
| Neuropatías | 6 | 5 % |
| Quirúrgicos | 43 | 35.83 % |
| Traumáticos | 18 | 15 % |
| Hipertensión arterial sistémica | 27 | 22.5 % |
| Diabetes | 12 | 10 % |
| EPOC | 7 | 5.83 % |
| Nota: DE: desviación estándar, EPOC: enfermedad pulmonar obstructiva crónica, SGB: síndrome de Guillain Barré. | ||
En 55% de los casos se encontraron antecedentes de síntomas gastrointestinales y respiratorios en las cuatro semanas previas al inicio de los síntomas, con una predominancia de síntomas respiratorios y diarrea (Tabla 1). El 9.17% de los pacientes refirieron presentar infecciones virales en las últimas cuatro semanas. Se identificaron dos casos de virus zika, uno confirmado y otro con síntomas, pero sin confirmación. También se encontró un caso sin confirmar de chikungunya, un caso sin confirmar de dengue, un caso confirmado del virus de la inmunodeficiencia humana. En cinco casos no se identificó agente causal. Asimismo, se encontró que los antecedentes quirúrgicos y la hipertensión predominan en los pacientes diagnosticados (Tabla 1).
Las características neurológicas son descritas en la Tabla 2. Los pacientes presentaron las siguientes variantes de SGB: AIDP (45.83%), AMSAN (21.67%), AMAN (24.17%) y FMS (7.5%) (Tabla 3). La media del periodo de tiempo desde la aparición de los síntomas hasta la fecha de ingreso al hospital para valoración neurológica es de 12.7 días SD 12.2. El tiempo de estancia hospitalaria osciló entre 1 y 77 días, con una media de 12.3 días SD 7,74. Los puntajes de la escala de Hughes al ingreso se describen en la Tabla 3, los más frecuentes fueron 4 (44.95%) y 3 (29.36%). Los pacientes que tenían un puntaje de 1 o 2 no recibieron terapia con plasmaféresis o inmunoglobulina, en contraste con los pacientes con un puntaje mayor o igual a 3, ya que en estos casos es necesaria una de las dos terapias anteriormente mencionadas como tratamiento del SGB. Un hallazgo muy importante fue la relación directa entre niveles altos de puntuación en la escala de Hughes y el requerimiento de ventilación mecánica, puesto que a medida que la puntuación es mayor, aumenta proporcionalmente la necesidad de ventilación mecánica (rho=0.3941 p<0.001) (Figura 1).
Tabla 2 Características neurológicas y de diagnóstico al ingreso de pacientes con SGB
| Categorías | n | % |
|---|---|---|
| Debilidad en extremidades | ||
| Superiores | 104 | 86.67 % |
| Inferiores | 118 | 97,13 % |
| Hiporreflexia en miembros | ||
| Superiores | 30 | 25 % |
| Inferiores | 38 | 31.67 % |
| Arreflexia en miembros | ||
| Superiores | 53 | 44.17 % |
| Inferiores | 60 | 65.83 % |
| Otras alteraciones | ||
| Parálisis facial | 35 | 17.07 % |
| Afección de otros nervios craneales | 10 | 8.33 % |
| Afección de esfínteres urinario y anal | 9 | 7.5 % |
| Criterios de Brighton | ||
| Debilidad muscular bilateral y flácida en extremidades | 94 | 78.33 % |
| Hiporreflexia o arreflexia en extremidades con debilidad | 74 | 61.67 % |
| Patrón de enfermedad monofásico | 86 | 71.67 % |
| Inicio a nadir de la debilidad: 12h-28 días más meseta subsecuente | 84 | 70 % |
| Disociación albúmino citológica en LCR | 78 | 65.00 % |
| Hallazgos electrofisiológicos consistentes con SGB | 97 | 80.83 % |
| Ausencia de un diagnóstico alternativo identificado de la debilidad | 14 | 11.76 % |
| Nota: LCR: líquido cefalorraquídeo, SGB: síndrome de Guillain Barré. | ||
Tabla 3 Clasificación y evolución de pacientes con SGB
| Categorías | n | % |
|---|---|---|
| Clasificación del SGB | ||
| Polineuropatía desmielinizante inflamatoria aguda | 55 | 45.83% |
| Neuropatía axonal motora sensitiva aguda | 26 | 21,67% |
| Neuropatía axonal motora aguda | 29 | 24,17% |
| Síndrome de Miller Fisher | 9 | 7,5% |
| Escala Hughes | ||
| 1 | 2 | 1.83 % |
| 2 | 15 | 13.76 % |
| 3 | 32 | 29.36 % |
| 4 | 49 | 44.95 % |
| 5 | 11 | 10.09 % |
| Tratamiento | ||
| Inmunoglobulina | 68 | 56.67 % |
| Plasmaféresis | 49 | 40.83 % |
| Seguimiento | ||
| Ventilación mecánica | 17 | 14.17% |
| Defunción | 5 | 4.17% |
| Nota: SGB: síndrome de Guillain Barré. | ||
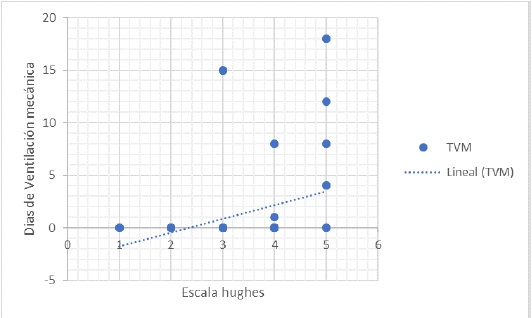
Nota: TVM: tiempo de ventilación mecánica en días.
Figura 1 Correlación positiva entre días con ventilación mecánica y valor obtenido en la escala Hughes
Nota: TVM: tiempo de ventilación mecánica en días.
En relación al tratamiento, a 40.83% de los pacientes se les realizó recambio plasmático en un promedio de cinco sesiones. No se obtuvieron mayores datos de la plasmaféresis, ya que no se especificaban en la historia clínica, sin embargo, se identificó que 3.33% de los pacientes presentaron reacciones adversas a dicho tratamiento. Por otra parte, 56.67% de los pacientes recibieron tratamiento con inmunoglobulina IV, de los cuales, dos recibieron 1gr/kg, 20 recibieron 2 gr/kg y 46 recibieron 400 mg/kg, durante una media de 5 días. Las reacciones adversas a la inmunoglobulina se presentaron en un 4.2% de los casos. El 2.5% de los pacientes no recibieron ningún tratamiento con inmunoglobulina o plasmaféresis y solo estuvieron en observación. Durante el tiempo de estudio fallecieron cinco pacientes (4.17%), 4 mujeres y un hombre, con un promedio de edad de 64 años; las mujeres tenían más de 67 años y el hombre tenía 16 años. El 60% de los pacientes presentaron infecciones respiratorias previas y antecedentes de hipertensión y diabetes. Todos requirieron ventilación mecánica.
Discusión
EL SGB tiene una incidencia a nivel mundial de 0.3 a 3 casos por 100,000 habitantes-año.17 En Colombia, su incidencia anual aumentó 4.4 veces durante los años 2015 y 2016, lo cual estuvo asociado a la infección por virus del zika y otros arbovirus, circunstancia descrita en detalle en algunos departamentos como Norte de Santander y Atlántico.13,15 El departamento de Antioquia no cuenta con información epidemiológica actualizada que permita determinar el efecto de esta epidemia en la presentación del SGB. En este estudio se identificaron 120 casos de SGB en tres instituciones especializadas de Medellín, capital de dicho departamento, durante el periodo de 2015 a 2020. El síndrome se dividió en los subtipos AIDP (45,83%), AMAN (24,17%), AMSAN (21,67%) y SMF (7.5%). Los subtipos que presentaron los pacientes concuerdan con los porcentajes que se describen en la literatura, siendo la AIDP la más frecuente.3,11
El antecedente de síntomas gastrointestinales y respiratorios, principalmente en las cuatro semanas previas al inicio de síntomas neurológicos, se encontró de manera similar a lo reportado en otros estudios.1,3,20 No obstante, en este estudio no se documentó la causa de estos síntomas como infección por virus o bacterias, ya que no es de uso rutinario solicitar pruebas para su identificación.
El SGB es una polineuropatía aguda que se manifiesta con parálisis flácida, arreflexia, y discapacidad motora que empeora en un transcurso de cuatro semanas, causa una respuesta del sistema inmune contra el sistema nervioso periférico y tiene un desenlace muy variable.9,21 En comparación con lo reportado en la literatura médica, se mostró que, en su gran mayoría, los pacientes también presentaron síntomas de debilidad en extremidades, hiporreflexia y arreflexia que progresaban en el trascurso de cuatro semanas.
Este síndrome afecta a pacientes con y sin comorbilidades, principalmente de la tercera edad, y suele representar una gran carga para el entorno familiar del paciente afectado.22-25 El SGB se presenta de forma aguda con un rápido deterioro de la función motriz, y puede generar complicaciones como insuficiencia respiratoria, secuelas neurológicas permanentes e incluso llevar a la muerte, por esto se considera una urgencia neurológica.19,20,23,26 Diversos estudios han mostrado que el SGB no se presenta en un grupo etario en específico sino en varios, ocasionando desde parálisis flácida en extremidades superiores e inferiores hasta la muerte.21,25,27 No obstante, la población más afectada por este síndrome son las personas mayores de 60 años, ya que existe un mal pronóstico de la enfermedad debido a las alteraciones del sistema inmune que se presentan con el proceso de envejecimiento, además de las comorbilidades subyacentes que pueden encontrarse en dicha población.28,29 Además, este pronóstico se puede ver afectado por la progresión rápida de la enfermedad. En los casos cuyo diagnóstico es tardío y, por tanto, el tratamiento no es temprano, hay antecedentes de enfermedad cardiorrespiratoria y el daño axonal es severo.22,25,28
En este estudio no se reportó un aumento de casos según la edad avanzada de los pacientes, como habitualmente se observa en otros estudios, lo cual se debe al incremento en la tasa de infecciones virales en población infantil que pueden ser causa de este síndrome.12,13,30,31 Asimismo, la frecuencia de la enfermedad fue de 20 casos por año con un leve predominio en hombres. Cabe señalar que durante el año 2015 se mostró un aumento significativo en los casos de SGB relacionados a la epidemia de Zika en Colombia; este mismo comportamiento se reportó por infección con otro arbovirus.32,33 Sin embargo, en este estudio solo se encontraron 3 casos de Zika vinculados con el SGB del año 2016, esto es, durante el periodo de epidemia.
Financiamiento
Este proyecto fue financiado por la Corporación Universitaria Remington.
Conflictos de interés
Los autores del presente estudio no tienen conflictos de intereses que declarar.











 nueva página del texto (beta)
nueva página del texto (beta)



