¿Qué sabemos acerca de este problema y qué aporta este estudio?
A pesar de la amplia divulgación y recomendación del uso del MNIO por guías internacionales, existe poca difusión y comprensión por parte de los anestesiólogos sobre técnicas, objetivos, importancia e impacto del manejo anestésico y perioperatorio sobre el mismo.
Este estudio identifica y describe las principales técnicas de MNIO, así como el impacto de los fármacos, variables hemodinámicas, manejo anestésico y perioperatorio sobre el MNIO, fundamental en el conocimiento de todo anestesiólogo.
Introducción
El monitoreo neurofisiológico intraoperatorio (MNIO) permite la identificación de estructuras nerviosas, así como el monitoreo y evaluación en tiempo real de la integridad funcional de corteza cerebral, tronco encefálico, médula espinal (ME), raíces nerviosas y nervios craneales y periféricos, evitando déficits motores y/o sensoriales transitorios o permanentes postoperatorios en procedimientos que ponen en riesgo al sistema nervioso (SN) a través de diversas técnicas neurofisiológicas.1-6 Para garantizar un monitoreo adecuado, es recomendable registrar las formas de onda basales o de referencia y de control.1
Debido a la influencia de la mayoría de los anestésicos sobre las vías inhibitorias,3,7 el conocimiento y la comprensión de las principales técnicas de MNIO y el impacto del manejo anestésico y diversas variables fisiológicas sobre los registros es de vital importancia para el éxito de los resultados.
Metodología
Búsqueda y revisión sistemática y narrativa, en idioma inglés y español, en las bases de datos Medline, Scopus y PubMed, utilizando los términos MeSH: "Monitoreo Neurofisiológico Intraoperatorio”; “Anestesia”; “Neuroanestesia”; “Manejo perioperatorio”; “Cirugía neurológica”; “Complicaciones”; “Seguridad”. Estadística narrativa y recomendaciones basadas en los resultados.
Resultados
El MNIO es una técnica útil para evaluar el estado neurológico del paciente bajo anestesia general.8 Con una historia de más de 30 años, ha sido utilizado para detectar y prevenir lesiones en diversas cirugías intracraneales y de columna.3,9,10 Es efectivo para alertar la posibilidad de lesión de nervios periféricos, predecir riesgo de paraparesia, paraplejía y cuadriplejía (sensibilidad 100%; especificidad 91%); predecir mejoría del nervio facial en cirugía de hemiespasmo facial y guiar la resección de áreas epileptogénicas en cirugía de epilepsia5 Asimismo, se utiliza en cirugía endonasal y resección de tumores de base de cráneo, en identificación y disminución del riesgo de lesión de nervios craneales o estructuras neurovasculares críticas;11-12 prevención de complicaciones isquémicas y déficits neurológicos en manejo endovascular13 o quirúrgico14-15 de aneurismas intracraneales; prevención y predicción de déficits neurológicos perioperatorios en cirugía de fosa posterior,16 aórtica1,17o cirugía de fusión espinal torácica.9 Su uso ha sido mas difundido en cirugía de columna, en la cual, a pesar de resultados favorables, elementos nerviosos pueden dañarse por mecanismos directos (compresión, tracción, laceración sección, avulsión) o indirectos (fenómenos isquémicos por elongación o compresión de la vascularización medular) y generar complicaciones secundarias al tratamiento quirúrgico.18-20
El registro de potenciales evocados (PE) representa la técnica electrofisiológica con mayor capacidad para proporcionar medidas cuantitativas, objetivas y oportunas para la vigilancia de la integridad funcional de ME, raíces nerviosas y adecuación del suministro vascular a estos elementos,4,9,21 ya que permite el reconocimiento de manera rápida y en tiempo real de cambios funcionales en vías motoras, sensitivas y estructuras nerviosas que las conforman (tractos anteriores y cordones posteriores).5,21-22
Evidencia médica sólida de clase I respalda su uso -incluido el registro de potenciales evocados somatosensoriales (PESS) y potenciales evocados motores transcraneales (PEMTc)-, como complemento de diagnóstico confiable, así como método válido para evaluar integridad de ME en entorno perioperatorio de cirugía de columna.23
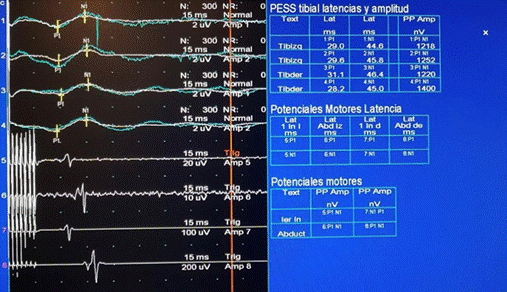
El MNIO multimodal es la combinación de diferentes técnicas neurofisiológicas y es el estándar de oro para prevenir y reducir la incidencia de complicaciones neurológicas postoperatorias24-26 (Figura 1); la combinación de PESS (Figura 2) y PEM (Figura 3) mediante estimulación sensitiva y de la corteza motora evalúa vías de transmisión con el registro de la respuesta evocada (Figura 4), lo que permite sugerir modificaciones durante el procedimiento, detectando, preveniendo y disminuyendo la incidencia de déficit neurológico postoperatorio hasta 60% en cirugía de columna22,26 con beneficio comprobado en corrección de escoliosis;9,27-29 y como componente de rutina en cirugías por deformidades o tumores intramedulares, reduciendo complicaciones y maximizando una resección adecuada.23
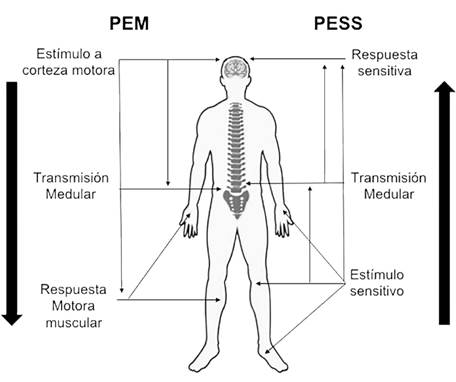
Figura 4 Dirección de la estimulación de las vías de transmisión motoras y sensitivas en Potenciales Evocados Motores y Sensitivos
A pesar del beneficio evidente en la reducción de costos derivados de posibles complicaciones,5 el costo-beneficio en cirugía de fusión cervical anterior se considera controvertido,8,30mientras que en el resto de los procedimientos de columna, debidamente justificada, puede ser una herramienta útil, válida y sensible para detectar daño neurológico en condiciones de alto riesgo o con mielopatía preexistente, especialmente con el uso de MNIO multimodal,4 siempre que se utilice como herramienta diagnóstica y no terapéutica.23
Guías clínicas internacionales actuales recomiendan el MNIO multimodal para evaluar la integridad funcional del SN, ME y raíces nerviosas.1,23,31-32 En México, la Guía de Práctica Clínica para la Implementación del MNIO, establece los niveles de recomendación y grados de evidencia para su práctica.6
Existen al menos ocho métodos para monitorear las funciones de ME y raíces nerviosas espinales durante procedimientos quirúrgicos33
PEME: Potencial evocado registrado en médula espinal posterior a la estimulación de la misma.
PES: Potencial evocado somatosensorial con registro cortical posterior a la estimulación de un nervio periférico.
PESS: Potencial evocado somatosensorial con registro en ME posterior a la estimulación de un nervio periférico.
PEM medular: Estimulación eléctrica o magnética (pulso único) transcraneal en corteza motora y registro de la respuesta (ondas D e I) en ME con electrodo epidural o subdural.
PEM muscular cerebral: Estimulación eléctrica transcraneal (corteza motora) multipulsos (tren de 5-7 estímulos) y registro de respuesta en músculos periféricos.
PEM muscular espinal: Estimulación de ME y registro en músculos periféricos.
Electromiografía continua: registrando en miotomas rostrales y caudales y músculos inervados por raíces motoras que emergen a nivel del procedimiento.
Electromiografía eléctricamente evocada: Identifica estructuras nerviosas, corrobora su integridad, estado de conducción y adecuada colocación de tornillos pediculares. Estimula raíces motoras en el sitio del procedimiento, estructuras óseas circundantes y/o tornillos pediculares.
El monitoreo es específico de acuerdo al área relacionada con el procedimiento, como en el monitoreo del nervio laríngeo recurrente (NLR) en tiroidectomía o cirugías de descompresión/ fijación cervical anterior, en las cuales los electrodos de EMG se adhieren al tubo endotraqueal y se colocan al nivel de los músculos vocal y aritenoides para su monitorización.2
La desaparición completa de PESS se asocia a parálisis de miembros y flacidez,21 el aumento de latencia >10% y/o disminución de la amplitud >50% en PESS y del 50-100% en PEM comparado con el valor basal constituyen "criterios de alarma" indicativos de riesgo de lesiones en la vía sensorial ascendente o motora descendente, respectivamente, que requiere intervención oportuna para evitar daños permanentes.14,21,26 Estos criterios de alarma dependen de una serie de factores como variabilidad de respuesta, tipo de anestesia, posicionamiento y lesión nerviosa,26,34 presencia o ausencia de lesión neurológica preexistente y eventos quirúrgicos, metabólicos y fisiológicos en el momento de la disminución o desaparición, como trauma mecánico o compresivo, o cambios por isquemia, hipoxia, hipotensión, hematocrito <15%, hipotermia <32ºC, hipertermia > 42º C, PaCO2 <20 mmHg, o disminución con PIC >25 mmHg o desaparición con PIC >30 mmHg17,35. La pérdida de señales o decrementos reversibles (<30-40 min) pueden predecir ausencia de nuevos déficits postoperatorios, mientras que decrementos prolongados (>40-60 min) pueden indicar un riesgo de lesión permanente.18-19
En caso de cambios en el MNIO durante la cirugía, se debe compartir la información entre el equipo multidisciplinario y tomar medidas para encontrar y eliminar la causa (NE:1C), ya sea quirúrgica, por falla o desconexión del equipo de neuromonitoreo o anestésica por cambios en variables fisiológicas, por dosis de anestésicos o nivel de hipnosis (NE:1D).1 Una vez identificada la alteración se recomienda que la decisión de continuar el procedimiento sea tomada en conjunto. La mejoría en las señales es un predictor de resultado neurológico favorable, particularmente para la cirugía de descompresión de ME.22
Potenciales evocados somatosensoriales (PESS)
Se utilizaron por primera vez en los años 70´s para vigilar la función de ME en corrección de escoliosis. Después de la estimulación de los nervios mixtos periféricos se registran respuestas en diversos puntos de la vía somatosensitiva (respuestas periféricas, subcorticales y corticales).24,26
Como respuesta electrofisiológica a un estímulo sensitivo del SN, proporcionan información funcional y de localización sobre el sistema somatosensorial; son la modalidad de monitoreo más utilizada.16 Están indicados para cualquier cirugía que ponga en riesgo a la vía propioceptiva y complementa el monitoreo de los PEM.32
La vía aferente inicia con receptores en piel, músculos y tendones, fibras Ia aferentes gruesas mielinizadas de conducción rápida, y las primeras neuronas (unipolares o pseudomonopolares) situadas en el ganglio de la raiz dorsal. Los axones de neuronales viajan en la columna dorsal ipsilateral hasta la unión cervicomedular. En este sitio hacen sinapsis con las segundas neuronas situadas en los núcleos gracil (medial), para piernas, y cuneiforme (lateral), para los brazos.
Los axones de las segundas neuronas cruzan al lado opuesto y posteriormente viajan como lemnisco medial llegando al núcleo ventral posterolateral del tálamo, en donde hacen sinapsis con la tercera neurona, y axones de estas neuronas alcanzan la corteza sensitiva parietal primaria.36 Se realiza el estímulo en un nervio mixto periférico, mediano o cubital (miembros superiores) y tibial o peroneo (miembros inferiores) y se colocan electrodos en sitios específicos del trayecto de la vía somatosensitiva para registrar respuestas eléctricas.
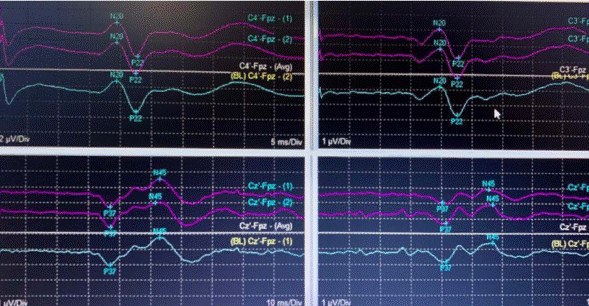
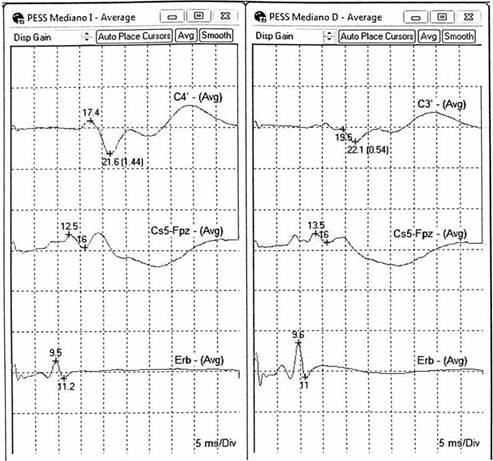
La vía propioceptiva dorsal transmite el tacto discriminativo, vibración y propiocepción, mientras que la vía exteroceptiva anterolateral lleva dolor, sensación de temperatura y tacto superficial. Esta técnica no evalúa el sistema anterolateral porque los axones son más delgados, con umbrales más altos y conducción más lenta y variable. Los nervios estimulados dependerán de la ubicación del sitio quirúrgico.32 La nomenclatura para designar los picos y v alles de las formas de onda de PESS es mediante una letra que representa su polaridad; una desviación ascendente significa polaridad negativa (N), una descendente es positiva (P); también se asigna un número basado en la latencia (tiempo entre el estímulo y presencia de la respuesta), que se mide en milisegundos (ms);17 por su parte, la amplitud representa el número de fibras funcionales -estos dos últimos, amplitud y latencia, se utilizan para demostrar cambios en la actividad neuronal. Los picos denominados N20 y P22 resultan de la estimulación del nervio mediano, de origen talámico y cortical, mientras que para el nervio tibial posterior o del nervio peroneo las respuestas corticales son P37 y N4536 (Figura 5). La lesión intraoperatoria causa una alteración neuronal o axonal aguda que reduce principalmente la amplitud de los PESS con menos efecto en la latencia.
La desmielinización aumenta latencia con menos efecto en amplitud; la amplitud es el principal parámetro a considerar en el monitoreo intraoperatorio.32,36
Las respuestas corticales de PESS del nervio mediano están generados por la corteza somatosensorial primaria irrigada por la arteria cerebral media y son útiles para detectar isquemia asociada al clipaje de aneurisma durante la oclusión temporal de la carótida interna. El nervio tibial se ha utilizado en eventos isquémicos asociados con aneurismas de la arteria cerebral anterior.15 La amplitud de PESS corticales disminuye con FSC regional <20 ml/min/100 g y se pierde completamente con <15 ml/min/100 g.17 Una pérdida abrupta de la respuesta cortical de PESS (<1 min después del clipaje)15 o disminución de amplitud PEM >50% puede predecir disfunción neurológica posoperatoria.14
En cirugía de fosa posterior existe alto riesgo de lesión del tronco cerebral; al respecto, los PESS son útiles para monitorizar la integridad de lemnisco medial.16 En endarterectomías carotídeas es recomendable el uso de electroencefalograma (EEG), PEM y PESS de nervio mediano y tibial para decisiones de puentes arteriales, neuroprotección cerebral intraoperatoria y disminución del riesgo de isquemia cerebral.5
La disminución unilateral de la amplitud en las respuestas de PESS de extremidad superior con o sin deterioro de PEM detecta alteración de conducción del nervio periférico o del plexo braquial en 2 a 3% de las cirugías de escoliosis.27 Procedimientos aórticos descendentes tienen alto riesgo de infarto de ME y paraplejia al interrumpir temporal o permanentemente el flujo sanguíneo; el MNIO detecta isquemia incipiente previo a daño permanente.17
Potenciales evocados motores (PEM)
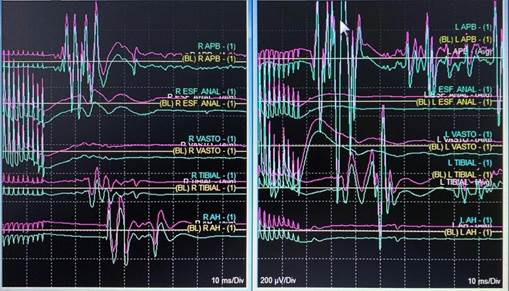
Evaluan integridad funcional de la vía motora, mediante estimulación eléctrica transcraneal y despolarización de neuronas corticoespinales; impulsos descendentes se registran en ME y extremidades 2 (Figura 6).
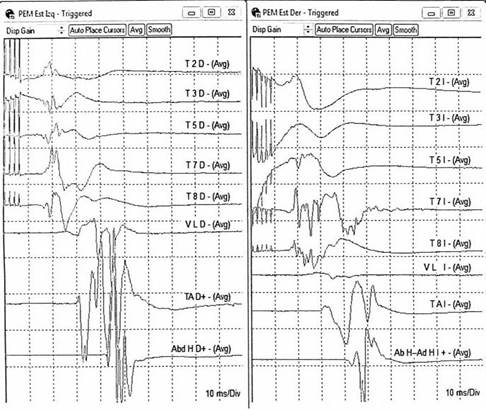
Figura 6 Potenciales Evocados Motores de extremidad inferior, T2, T3, T5, T7, T8, vasto lateral, tibial anterior, abductor del primer dedo
En 1980, Merton y Morton registraron potenciales de acción musculares posterior a la estimulación de corteza motora en humanos de forma transcraneal, impulsando el desarrollo de monitorización de ME.10 Posteriormente, en la década de 1990, se introdujeron los Potenciales Evocados Motores Musculares (PEMm) y Epidurales (PEMe u onda D).24
Pueden ser espinales, neurogénicos y musculares, facilitan una evaluación selectiva y específica de la integridad de la vía motora, desde la corteza hasta las fibras nerviosas periféricas y músculos,24 y permiten detectar la integridad funcional de la vía corticoespinal con alta sensibilidad y especificidad.25 La monitorización del sistema motor puede realizarse por estimulación transcraneal de tren corto (5-7 estímulos) o estímulo único con registro en ME.33 Las lesiones de axones, neuronas o sistemas de apoyo motor, manifiestan un umbral que va desde la reducción de amplitud hasta su desaparición.32
La desaparición de la respuesta de los PEMm no siempre indica déficit motor permanente; la sensibilidad de monitorización de PEM para detectar disminución del flujo sanguíneo cerebral (FSC) en cirugía de aneurisma ya ha sido validada,14 pero su sensibilidad a la agresión isquémica y de compresión médular es alta, por lo que falsos positivos aumentan si el juicio se basa únicamente en este potencial.33
La disminución >50% en amplitud de PEMe (onda D) se correlaciona con déficit motor posoperatorio; variaciones en amplitud de PEMm y PEMe permiten predecir función motora postoperatoria.24
Potenciales evocados de médula espinal
Desarrollados en Japón en los 70´s, consisten en la estimulación de la ME con un electrodo epidural, registrando respuesta proximal o distal, que corresponde a la suma de actividades neuronales originadas en tractos ascendentes y descendentes de neuronas cerca del electrodo de registro.33 La estimulación también puede realizarse cranealmente y registrarse en sentido caudal o viceversa. Debido a las diferentes propiedades de conducción (velocidades) de las vías de la ME, los potenciales registrados toman la forma de dos ondas distintas. Los potenciales registrados son muy robustos y representan actividad combinada de columnas dorsales (CD), tractos corticoespinales y otras vías de médula espinal. Este método se ha abandonado en gran medida, pero conserva valor en neuropatías preexistentes graves, en investigación, o cuando la determinación del grado de conducción es importante.
Electromiografía
Es el registro gráfico en tiempo real de la actividad eléctrica muscular evaluando la integridad de estructuras nerviosas. En el intraoperatorio se utilizan dos variantes con diferente finalidad: EMG contínua y evocada; se colocan dos agujas subdérmicas con 2-3 cm de separación en el músculo inervado por el nervio periférico, nervio craneal o raíz nerviosa involucrados en el procedimiento.
EMG contínua: Se registra la actividad miogénica para evidenciar si una estructura nerviosa está siendo dañada (irritación o lesión al nervio). Se basa en la propiedad del nervio motor de responder a la lesión térmica o mecánica con la consecuente activación de los músculos inervados por dicho nervio.
EMG Evocada: Se utiliza estimulación eléctrica directa o indirecta para identificar una estructura nerviosa, demostrar su integridad y/o estimar el grado de lesión; permite corroborar la adecuada colocación de los tornillos pediculares (TP) por medio de estimulación indirecta de una raíz nerviosa. Cuando el TP está mal colocado, medial o lateralmente o hay fisura del pedículo la coriente eléctrica en la cabeza del TP se propaga y estimula la raíz adyacente obteniendo un potencial de acción compuesto muscular a bajo amperaje. Si el TP esta bien colocado estará rodeado de hueso resistente al paso de corriente, no estimulará a la raíz adyacente y no habrá respuestas. Los valores de seguridad varían dependiendo del segmento de la columna vertebral en el cual se está trabajando.
Potencial de acción del nervio (PAN)
Es una de las técnicas de mayor utilidad en cirugías de nervio periférico, ya que provee información rápida y confiable del status de nervios periféricos durante la cirugía. Es útil para detectar axones de nervios periféricos en regeneración y determinar la acción quirúrgica correspondiente en un procedimiento.
Puede ser registrado con electrodos de estimulación y registro colocados directamente en el nervio. La estimulación se hace con electrodo tripolar que permite concentrar la corriente minimizando su esparcimiento; el registro se realiza con un electrodo bipolar.
Anestésicos y su influencia en el Monitoreo Neurofisiológico Intraoperatorio
La mayoría de los anestésicos ejercen su acción incrementando la acción de vías inhibitorias, disminuyendo actividad neuronal y atenuando las respuestas del MNIO, en especial bloqueadores neuromusculares (BNM) y halogenados inhalados;1,3,7 para el éxito del MNIO, es de vital importancia comprender la influencia de fármacos y otras variables sobre los registros 21, 35,37,38 (Tabla 1).
Tabla 1 Fármacos anestésicos y sus efectos en Potenciales Evocados Somatosensoriales y Potenciales Evocados Motores
| Fármaco | Efecto en PESS | Efecto en PEM |
|---|---|---|
| Propofol(*) | Disminución Menor | Disminución Menor |
| Etomidato | Aumento | Sin efecto |
| Midazolam | Disminución | Sin efecto |
| Ketamina | Aumento | Poco efecto - Disminución |
| Fentanil | Poco efecto - Disminución | Disminución |
| Remifentanil | Poco efecto - Disminución | Poco efecto - Disminución |
| Sufentanil | Poco efecto - Disminución | Disminución |
| Dexmedetomidina | Poco efecto - Disminución | Poco efecto - Disminución |
| Sevoflurano | Disminución mayor | Disminución mayor |
| Desflurano | Disminución mayor | Disminución mayor |
| Rocuronio | Sin efecto | Sin respuesta |
| Succinilcolina | Sin efecto | Sin respuesta |
Los BNM bloquean la transmisión de señales de nervios motores a fibras musculares a nivel de la placa neuromuscular; cuando la vigilancia de la integridad funcional de una estructura nerviosa es por actividad miogénica, es imperativo que el grupo de músculos sea sensible a cambios en el funcionamiento de la raíz, nervio periférico o nervio craneal al ser traccionados o comprimidos, por lo que, con fines de monitoreo, se recomienda no utilizarlos o utilizar BNM de vida media corta y siempre monitorizar su actividad comunicando cualquier decisión con el neurofisiólogo.14
Las benzodiacepinas a dosis de inducción mayores a 30 mcg/kg causan depresión en PESS corticales, subcorticales y periféricos. También tienen efectos depresores en PEM.7 A pesar de no estar contraindicadas, son poco usadas en neurocirugía debido a su impacto en la evaluación postoperatoria.
Los anestésicos halogenados inhalados tienen un impacto signifcativo en MNIO dosis dependiente,1,3 disminuyendo amplitud de PEM e incrementando la posibilidad de falsos positivos,38 PESS corticales también se ven afectados en menor medida por los inhalados.7 El isoflurano causa mayor reducción en amplitud e incremento en latencia dosis-dependiente, seguido de sevoflurano y desflurano. A nivel molecular, causan reducción de la excitabilidad neuronal por efecto en canales de potasio e inhibiendo la activación de motoneuronas inferiores por motoneuronas superiores.7,33
Los opioides causan disminución leve en amplitud y prolongación de latencia de potenciales corticales; su efecto depresor no es comparable con los inhalados, volviéndolos una alternativa útil en MNIO.35
Los coadyuvantes están recomendados para generar singergia, analgesia postanestésica y disminuir dosis de hipnóticos y anestésicos; la lidocaína en perfusión 15-60 mcg/kg/min genera estabilidad hemodinámica, menor necesidad de opioides y analgesia postoperatoria; el sulfato de magnesio 1-5 mg/kg/h es coadyuvante analgésico, brinda estabilidad hemodinámica y menor requerimiento de opioides; la dexmedetomidina tiene poco efecto o disminución de los PE a dosis <0.5 mcg/kg/hr y con adecuada estabilidad en perfusión; se pueden continuar para analgesia en el período postoperatorio en perfusiones continuas solos o asociados por 24-48 horas dependiendo del tipo de cirugía o número de niveles operados. La ketamina incrementa amplitud de PESS y PEM de ME y es una buena alternativa en pacientes con daño neurológico previo35 y se recomienda en cirugía de columna para mejorar el registro de PE, menor uso de opioides, y como analgesia postoperatoria en infusiones de 0.3 mg/kg/hr.
Etomidato y ketamina generan incremento dosis-dependiente en amplitud de PE.7 El etomidato en bolos 0.3 mg/kg incrementa amplitud de PESS corticales, sin cambios en respuestas subcorticales y/o periféricas; en la amplitud de los PEM se observa una ligera disminución, sin cambios en latencia.35
La técnica de elección
Además de la selección del protocolo anestésico para el registro basal y de control, las medidas para mantener constante el nivel de hipnosis y relajación muscular son cruciales para detectar de forma inmediata los cambios en las respuestas de los PE durante o después de la manipulación quirúrgica (NE:1C).1
Tanto el desflurano como el sevofurano disminuyen amplitudes de PESS y PEM y prolongan latencias de PES dosis dependiente; en caso de utilizarlos, se recomienda <0.5-0.6 CAM3,7 y uso de adyuvantes.38 Los bolos de fármacos intravenosos o cambios abruptos en el CAM de halogenados pueden comprometer los registros.
La ATIV con propofol permite mejor registro de los PEM y los PESS (NE:2C);6 la recomendación de la dosis es de 3.0-4.5 mcg/ml CP basada en la hemodinamia y el monitor de profundidad anestésica con EEG procesado o no procesado del paciente; su efecto en latencia es mínimo, lo cual, aunado al perfil farmacocinético que permite perfusiones a concentraciones constantes y menor efecto depresor que los inhalados, lo hacen el hipnótico de elección.1La mayoría de los estudios coinciden en el uso de infusiones o ATIV-TCI con anestésicos intravenosos como propofol como hipnótico, remifentanil TCI sufentanil TCI o ketamina, como anestésico y BNM de acción corta o para intubación, pero no durante la cirugía.4,14,22,26,35
El nivel de hipnosis y relajación muscular debe mantenerse constante; es recomendable el uso de monitores neuromusculares y de profundidad anestésica, idealmente EEG.1
Variables fisiológicas como temperatura, presión arterial, frecuencia cardíaca, concentración de oxígeno en sangre, presión parcial de dióxido de carbono, se deben mantener sin cambios significativos; el neuroanestesiólogo debe asegurar un adecuado posicionamiento del paciente y mantener objetivos claros de hipnosis y homeostasis metabólica y fisiológica, manteniendo adecuada saturación y oxigenación sistémica, hematocrito, normotensión, normotermia y normocapnia, evitando modificaciones que alteren los registros.14
La estimulación de la corteza motora puede provocar movimientos involuntarios de mano, mandíbula y otras partes del cuerpo con el riesgo de automordeduras y otras lesiones. En este sentido, es importante prever y prevenir posibles eventos adversos asociados al MNIO. El consentimiento informado debe incluir no solo los objetivos y métodos de monitoreo, sino también el riesgo de eventos adversos asociados.1
Conclusiones
El MNIO multimodal es un método útil que permite evaluar en tiempo real el estado funcional del sistema motor y sensitivo con el objetivo de prevenir lesiones postoperatorias en procedimientos que ponen en riesgo al sistema nervioso y plantean importantes desafíos para el neuroanestesiólogo.
Es fundamental comprender las bases clínicas de las diferentes técnicas del MNIO e interpretar de forma oportuna alertas y criterios de alarma, esto mediante una estrecha cooperación entre el neurocirujano, neurofisiólogo y neuroanestesiólogo para la toma de decisiones tempranas y la obtención de mejores resultados quirúrgicos.
A su vez, el neuroanestesiólogo debe asegurar un adecuado posicionamiento, estado de profundidad anestésica, estabilidad hemodinámica y de presión de perfusión cerebromedular, evitando modificaciones que alteren los registros.











 nueva página del texto (beta)
nueva página del texto (beta)