Introducción
Se define como aneurisma de aorta abdominal (AAA) a la dilatación anormal, mayor a 1.5 veces el diámetro aórtico esperado o ≥ 30 mm en su diámetro máximo, que involucra las tres capas que la comprenden (íntima, media y adventicia)1,2. La ruptura del AAA es su complicación más grave, se asocia a una mortalidad entre 32-70% y esta puede ascender hasta un 90% si incluimos la mortalidad prehospitalaria2-4. El riesgo de ruptura se asocia directamente con el diámetro máximo del aneurisma; un diámetro máximo entre 50-59 mm alcanza un riesgo de ruptura al año del 9%, superando de manera significativa al riesgo de mortalidad perioperatoria de la reparación endovascular y abierta que es del 1.2 y 4.6% respectivamente, por consiguiente, en pacientes con un diámetro máximo del AAA ≥ 55 mm, con aceptable riesgo quirúrgico, la reparación profiláctica del AAA se considera una intervención segura y eficaz que mejora la sobrevida del paciente a largo plazo5-7.
En las últimas décadas, la reparación endovascular ha desplazado a la reparación abierta como la principal opción de tratamiento, actualmente representa el 85% de todas las reparaciones de AAA realizadas en Norteamérica, se asocia a una menor tasa de mortalidad y morbilidad perioperatoria a 30 días, 1.2 y 11.7% respectivamente, en comparación con la reparación abierta, con una tasa de mortalidad y morbilidad del 4.6 y 26.4% respectivamente6,7. Se asocia con una menor tasa de complicaciones perioperatorias en comparación con la reparación abierta y estas dependen de las características anatómicas del aneurisma y del riesgo quirúrgico de cada paciente. En general, la terapia endovascular se asocia a una tasa de mortalidad perioperatoria por complicaciones cardiopulmonares del 3% a seis meses, en comparación con el 5% en reparación abierta y un riesgo de complicaciones pulmonares del 3.5% con requerimiento de ventilación mecánica posquirúrgica8,9.
Aunque la tasa de éxito técnico inmediato es cercana al 100%, a largo plazo, el comportamiento y sellado de la endoprótesis es un fenómeno dinámico, que varía con el tiempo10. Como resultado, a largo plazo se asocia con un mayor riesgo de complicaciones tardías, reintervención y mortalidad tardía asociada al aneurisma. Las principales complicaciones asociadas a la endoprótesis son: ateroembolia 0.5%, isquemia asociada a oclusión de las extensiones ilíacas 3.5%, usualmente causada por trombosis y/o acodamiento de las extensiones ilíacas (kinking) y endofuga, esta última es la complicación más frecuente con una incidencia del 20% a cinco años y que es la causa del 75-80% de todas las reintervenciones y principal causa de ruptura tardía11-13. El desarrollo de nuevas endoprótesis ha disminuido la tasa de complicaciones asociadas a la endoprótesis y, por ende, ha aumentado la sobrevida libre de reintervención en las últimas décadas, pasando de un 68% a cinco años entre 1998-2008 a un 81% a cinco años en reparaciones realizadas posterior al año 2008; sin embargo, estas complicaciones continúan siendo una causa frecuente de morbilidad y mortalidad14.
Como resultado, es imperativo un seguimiento estricto y seriado de los pacientes sometidos a reparación endovascular de AAA para detectar de manera temprana cualquiera de las complicaciones asociadas a la endoprótesis. La Sociedad Americana de Cirugía Vascular recomienda el seguimiento con angiotomografía computarizada (ATC) de todos los pacientes sometidos a reparación endovascular del aneurisma de aorta abdominal (EVAR) al mes, a los seis meses y posteriormente al año, y repetir cada año hasta completar cinco años. No obstante, esta modalidad de seguimiento conlleva potenciales riesgos por exposición repetida a radiación y un alto riesgo de nefrotoxicidad por contraste yodado2.
Clasificación de las endofugas
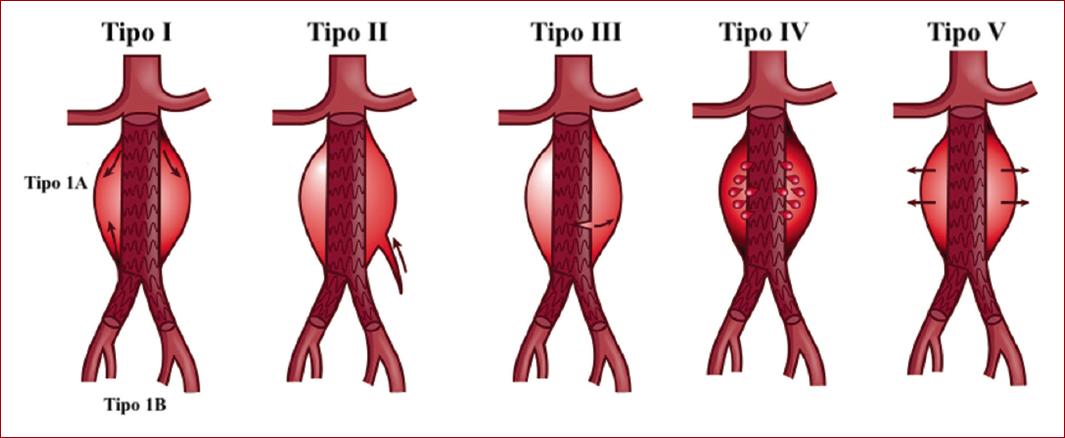
Se define endofuga como la persistencia de flujo sanguíneo por fuera de la endoprótesis aórtica y dentro del saco aneurismático. Es la complicación más frecuente, puede estar presente en un 20-50% de todas las reparaciones endovasculares y la que se asocia a una mayor tasa de reintervenciones15. Las endofuigas se clasifican en cinco tipos diferentes (Fig. 1):
-
- Tipo I. Se define como la persistencia de flujo sanguíneo a través del sitio de fijación de la endoprótesis y la pared arterial. Su incidencia anual es del 8% y representa el 12% de todas las endofugas, con un riesgo de ruptura del 4-7.5% a dos años16. Se subdividen en A o B:
- Tipo II. Se define como el llenado persistente del saco aneurismático, a través de un vaso colateral, como una arteria lumbar o la arteria mesentérica inferior. Es el tipo de endofuga más habitual, con una incidencia aproximada del 34% (18% autolimitadas, 5% persistentes, 11% de novo)17.
- Tipo III. Se define como la presencia de flujo periprostésico a partir de la separación de alguno de los módulos que conforman la endoprótesis o de un defecto en la integridad de la prótesis. Este tipo de endofugas ha experimentado una reducción de hasta el 1% en su prevalencia con el desarrollo de las nuevas generaciones de endoprótesis, sin embargo conllevan un riesgo de ruptura aneurismática del 8-9% y se recomienda su resolución temprana a su identificación18.
- Tipo IV. Se define como el paso de sangre hacia el saco aneurismático debido a la porosidad de la endoprótesis. Su presencia es rara, debido al desarrollo tecnológico de nuevas endoprótesis y no se asocia a ruptura aneurismática16.
La endotensión se define como el crecimiento del saco sin la presencia identificable de una endofuga, su prevalencia es menor del 5% y su riesgo de ruptura a cuatro años es menor del 1%19.
Ultrasonido ecopotenciado
La obtención de imágenes generadas por ultrasonido se basa en la recepción, análisis y la visualización de señales acústicas producidas por la reflexión y retrodispersión del sonido. El método de análisis Doppler permite evaluar la dirección y velocidad del flujo sanguíneo, sin embargo esta modalidad de análisis no permite evaluar la microcirculación o el flujo sanguíneo de muy baja amplitud20. El desarrollo tecnológico de microburbujas ha provisto de nuevas herramientas diagnósticas y conocimientos únicos en la fisiología microvascular que no serían posibles con otras modalidades diagnósticas. Su utilidad como contraste ecográfico se basa principalmente en su compresibilidad. Estas microburbujas se encuentran compuestas de una capa lipídica, rellenas de gas, las cuales sufren oscilaciones volumétricas al ser sometidas a un campo acústico, como consecuencia se comprimen y se expanden en relación con los cambios de presión acústica (Fig. 2). Esta oscilación genera intensas señales acústicas, fenómeno conocido como resonancia acústica. El diámetro de las burbujas varía entre 1 y 10 μm, tamaño similar al de un eritrocito, lo que les permite penetrar en la microvasculatura, el endotelio y el intersticio20,21.
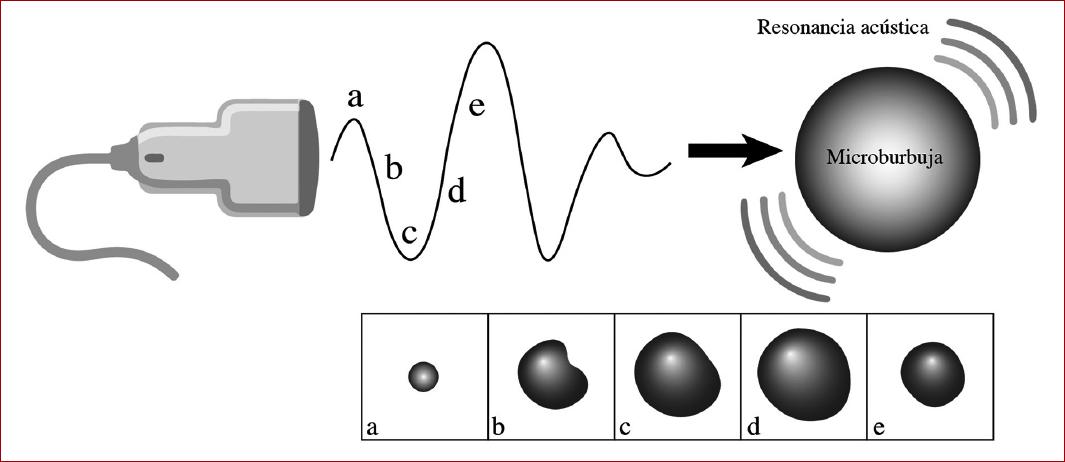
Figura 2 Estimulación acústica sobre una microburbuja sometida a energía ultrasónica, dando como consecuencia un fenómeno de resonancia acústica.
En nuestro medio, contamos con el agente de contraste ecográfico SonoVue (Bracco, Milán, Italia). Está compuesto de microburbujas rellenas de hexafluoruro de azufre con una cubierta de características lipídicas. Su eliminación es pulmonar y no tiene efectos sobre la función renal, los efectos secundarios más comunes son cefalea y náuseas. Las reacciones de hipersensibilidad son extraordinariamente raras, con una incidencia de 1/10,00022. Su aplicación en nuestro medio se enfoca, principalmente, al campo de la ecocardiografía y la caracterización de tumoraciones hepáticas, su uso en el seguimiento de pacientes sometidos a reparación endovascular de AAA es escaso23,24.
Aunque el uso de USC como herramienta auxiliar en el seguimiento de pacientes sometidos a reparación endovascular de AAA se describió desde 1997, no fue sino hasta la última década que contamos con la evidencia suficiente para comparar con mayor exactitud, los resultados del ultrasonido mejorado con contraste (USC) y la ATC para identificar endofugas en el seguimiento de pacientes sometidos a reparación endovascular25.
Una revisión sistemática que incluyó 27 estudios, con un total de 2,217 pacientes, identificó que en pacientes sometidos a EVAR el seguimiento de pacientes con USC demostró ser altamente preciso para la detección de cualquier tipo de endofuga, con una sensibilidad acumulada de 0.94 (intervalo de confianza [IC]: 0.89-0.97) y una especificidad acumulada de 0.93 (IC: 0.89-0.96), con un área bajo la curva de 0.98. En el subanálisis para identificar endofugas tipo I y III, demostró una sensibilidad de 0.97 (IC: 0.8-1.0), especificidad de 1.00 (IC: 0.99-1.00) y un área bajo la curva de 1.0026 (Tabla 1).
Tabla 1 Comparación de sensibilidad y especificidad entre USD, ATC y USC
| Endofuga (general) | Endofuga tipo I | Endofuga tipo II | Endofuga tipo III | |
|---|---|---|---|---|
| Sensibilidad | ||||
| USD | 63% | 72% | 34% | 72% |
| USC | 94% | 97% | 81% | 97% |
| ATC | 88% | 93% | 70% | 93% |
| Especificidad | ||||
| USD | 98% | 97% | 99% | 98% |
| USC | 94% | 97% | 98.9% | 100% |
| ATC | 97% | 96% | 97% | 97% |
ATC: angiotomografía computarizada; USC: ultrasonido mejorado con contraste; USD: ultrasonido Doppler.
Johnsen et al. llevaron a cabo estudio diagnóstico comparativo con 92 pacientes, comparando ATC y USC; este último reporta una sensibilidad del 81.3%, una especificidad acumulada de 98%, con un valor predictivo positivo del 95% y valor predictivo negativo del 95%, así como coeficiente kappa de 0.84 interobservador para identificar endofugas tipo II. En el subanálisis se identificó un aumento de los falsos negativos asociados directamente con el índice de masa corporal (IMC), ya que el 55% de los falsos negativos reportados por el USC se asociaban a un IMC > 29, lo que limitaría su uso en pacientes con obesidad. No obstante, ninguno de los pacientes con resultado falso negativo en USC presentó aumento del diámetro del aneurisma ni requirió una reintervención en el seguimiento, lo que significa que el USC fue altamente efectivo en detectar aquellas endofugas tipo II clínicamente significativas27.
En 2017 Lowe et al. realizaron un estudio comparativo del uso de ATC, USC y USC con reconstrucción en tres dimensiones (USC-3D), en 100 pacientes en seguimiento post-EVAR, sin identificar diferencias significativas entre USC y USC-3D para su identificación, con una sensibilidad del 96%, especificidad 91%, valor predictivo positivo del 90%, valor predictivo negativo del 96% en comparación con la ATC. Con un coeficiente kappa de 0.89 a la aplicación del USC-3D, lo que permitió caracterizar mejor la endofuga28.
El desarrollo de nuevos agentes de contraste ecográfico, así como un mejoramiento en los equipos y el software de sustracción para la obtención de mejores imágenes y una mejoría en la curva de aprendizaje del operador, con al menos 20 estudios de USC, ha mejorado los resultados a favor del USC28.
Actualmente, la ATC es el estudio de elección en la vigilancia y el seguimiento de pacientes post-EVAR, con una sensibilidad del 88% y una especificidad del 97% para la detección de endofugas26,29. Sin embargo, su uso se asocia con un aumento en el riesgo de cáncer inducido por radiación y nefropatía inducida por contraste, situaciones que vale la pena considerar al realizar el seguimiento de estos pacientes30. Otra situación que surge en la identificación de endofugas es la determinación de la dirección del flujo, lo cual resulta relevante, especialmente en las endofugas tipo II, al momento de planear su tratamiento. Estas consideraciones deberán ser tomadas en cuenta al momento de seguir y vigilar a los pacientes post-EVAR (Tabla 2).
Tabla 2 Ventajas y limitaciones del USC
| Ventajas del uso de USC |
|---|
| No radiación |
| Bajo costo |
| No utiliza componentes yodados |
| Análisis del flujo en tiempo real |
| Limitaciones en el uso de USC |
| Pacientes obesos (IMC > 29) |
| Calcificación extensa de la pared |
| Enfisema subcutáneo |
| Gas intestinal |
| Ascitis |
| Abdomen abierto |
USC: ultrasonido mejorado con contraste; IMC: índice de masa corporal.
Protocolo de evaluación por ultrasonido
Pacientes con al menos ocho horas de ayuno de alimentos sólidos, con IMC < 29, así como integridad de la pared abdominal. Se utiliza un equipo ACUSON Sequoia (Siemens, Múnich, Alemania), mediante el uso de un transductor convexo de 2-5 MHz, se lleva a cabo el análisis en escala de grises, Doppler color, Doppler pulsado y ecopotenciado, respectivamente, como se describe a continuación.
Análisis en modo B y escala de grises
- Se evalúa la aorta abdominal, arterias renales, tronco celíaco, arteria mesentérica superior, arteria mesentérica inferior y arterias ilíacas.
- Evaluar y documentar la posición de los sitios de anclaje proximal, distal.
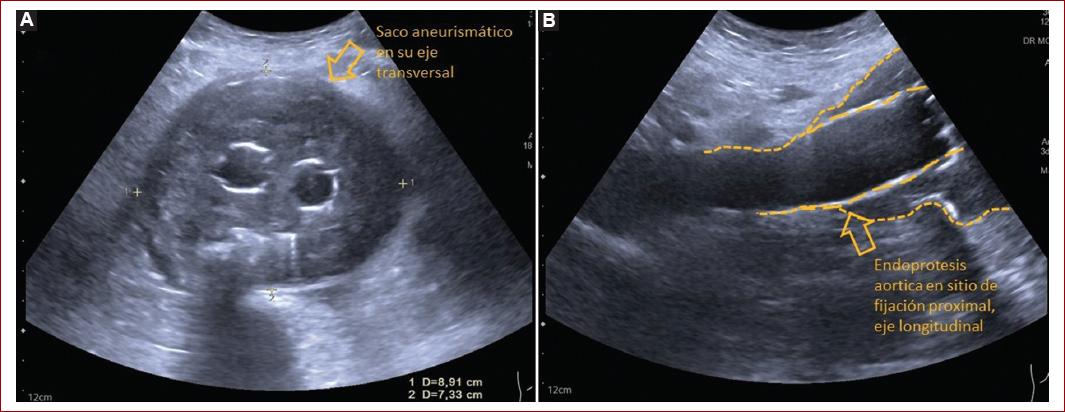
- Evaluación del saco aneurismático en el eje axial y sagital, así como la medición del diámetro máximo del saco. La medición del eje axial se deberá realizar en relación con el eje del aneurisma y no con el eje del cuerpo del paciente (Fig. 3).
Análisis en Doppler color y espectral
- Análisis en color y espectral de la totalidad de la endoprótesis y sus extensiones que demuestre su permeabilidad.
- Búsqueda de flujo turbulento en tortuosidades y/o acodamiento en ramas y extensiones ilíacas.
- Evaluación de los sitios de fijación proximal y distal para identificar la presencia de flujo por fuera de la luz de la endoprótesis, así como de sus extensiones.
- Evaluar la permeabilidad y flujo de las arterias renales, mesentérica superior y tronco celíaco.
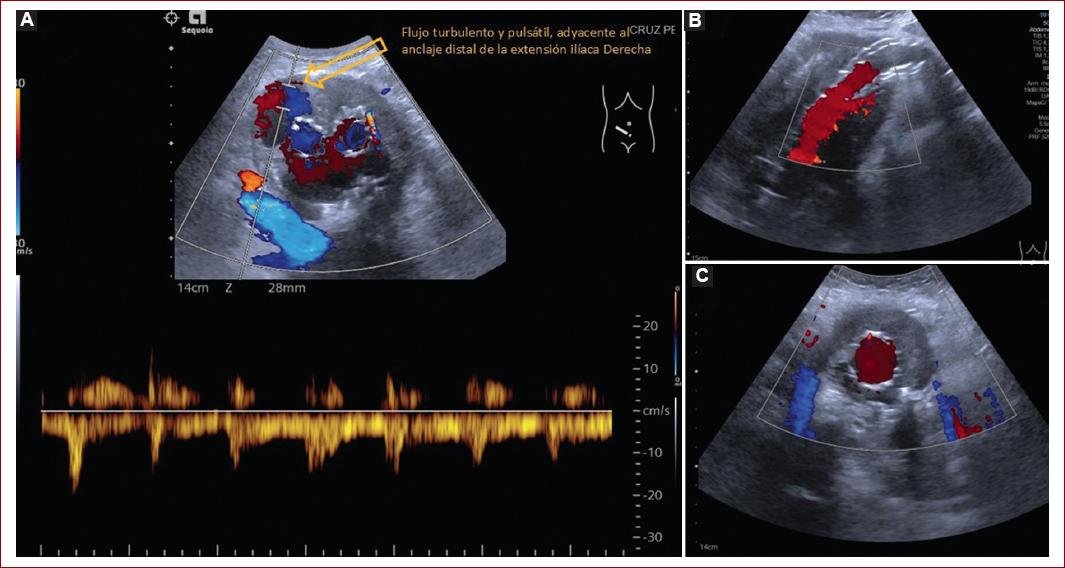
- Evaluar la permeabilidad de las ramas arteriales del saco aneurismático (arterias lumbares, arteria mesentérica inferior), así como la dirección del flujo de cada una de las ramas (Fig. 4).
Análisis con ultrasonido ecopotenciado por contraste de alta definición
- Con el uso de software para adquisición de imágenes con contraste ecográfico VA25 (Siemens, Múnich, Alemania).
- En una vena periférica (cefálica o mediana), con un catéter 18 G, se inyectan 2.5 ml de contraste (SonoVue 8), seguido de un bolo de 20 cc de solución de salina al 0.09%. Se realiza análisis en tiempo real, cronometrado (Fig. 5).
- Se evalúa sitio de anclaje proximal, así como anclaje distal de las extensiones ilíacas.
- El tiempo de aparición de burbujas de contraste en el saco aneurismático, < 10 s es indicativo de endofuga I o III; en cambio, un tiempo > 15 s es indicativo de endofuga tipo II. Respecto a la dirección del flujo: centrípeto es sugestivo de endofuga tipo II, centrífugo es sugestivo de endofuga tipo I o III (Tabla 3).
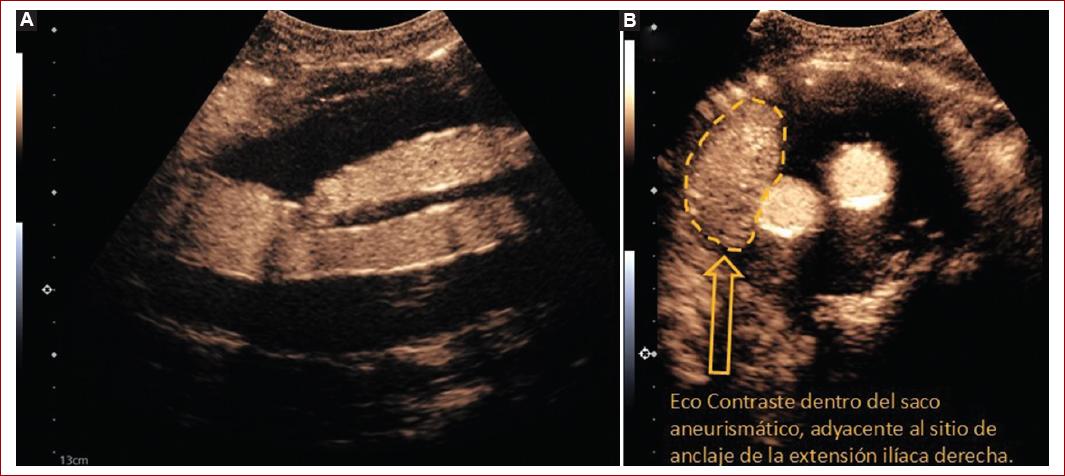
Figura 5 Evaluación de ultrasonido contrastado. A: aplicación de microburbujas, como contraste, el sitio de fijación proximal sin datos de endofugas tempranas ni tardías. B: endofuga tipo IB (flecha amarilla), de realce temprano (< 5 s) adyacente a la extensión ilíaca derecha.
Tabla 3 Características de las endofugas a la aplicación de ultrasonido contrastado
| Tipo de endofuga | Tiempo que tarda en visualizarse la endofuga | Dirección del contraste dentro del saco | Localización de la endofuga |
|---|---|---|---|
| Tipo 1 | Rápida (< 5 s) | Centrífuga | Adyacente al sitio de anclaje con endofuga |
| Tipo 2 | Tardía (> 10 s) | Centrípeta | Anterior: AMI Posterior: Lumbar |
| Tipo 3 | Rápida (< 5 s) | Centrífuga | Sitio de ensamble entre componentes |
AMI: arteria mesentérica inferior. Adaptada de Cruz et al., 202131.
En caso de identificar endofugas, estas se deberán caracterizar según los criterios descritos en la figura 1.
Conclusiones
El uso del ultrasonido mejorado por contraste para el seguimiento de pacientes sometidos a reparación endovascular de AAA se ha popularizado en los últimos años, principalmente en países desarrollados, debido a que ofrece un análisis en tiempo real, rápido, seguro y altamente eficaz en la detección y caracterización de endofugas. Sin olvidar que se trata de un estudio operador dependiente, la mejoría en la tecnología involucrada y con personal capacitado, es posible llevar a cabo un adecuado seguimiento postoperatorio en estos pacientes y presenta una buena concordancia interobservador sin necesidad de requerir una ATC. En prácticamente todas las series, su sensibilidad es mayor del 90% para la detección de cualquier tipo de endofuga, aunque esta se puede ver afectada en pacientes obesos (IMC > 29). En México es necesario llevar a cabo una mayor difusión y entrenamiento en esta modalidad de imagen que nos permitan ofrecer una opción más segura para el seguimiento de los pacientes sometidos a reparación endovascular de aneurisma de aorta.











 nueva página del texto (beta)
nueva página del texto (beta)