Introducción
Desde un punto de vista cibernético, el sistema visual es informacionalmente abierto respecto al entorno, pero desde el punto de vista organizativo es un sistema cerrado de retroalimentación negativa, cualidad que le permite modular y limitar la oscilación1-3.
En condiciones fisiológicas, el integrador cortical modula las frecuencias espaciotemporales de la información visual proveniente de ambos ojos mediante circuitos cortico-corticales reguladores4. La corteza visual primaria ordena y prioriza esta información de acuerdo con las frecuencias espaciotemporales del estímulo eferente, y lo hace en un tiempo relativamente breve, de una manera no bien conocida y difícil de emular in silico5,6. La información es enviada luego hacia la segunda vía visual a través de las vías dorsal y ventral, a fin de determinar el qué es y el dónde están los estímulos visuales7-9, así como para la elaboración de imágenes complejas, como el reconocimiento de rostros10-12. Esto se logra a través de la vía occipito-temporal, que comprende las vías cortas O1-T5 y O2-T6 y las vías ventrales largas O1-T3 y O2-T4, izquierdas y derechas, respectivamente13. La vía ventral derecha, que se dirige de la corteza estriada al lóbulo temporal, forma parte del circuito encargado de la percepción del movimiento13.
Debido a su cercanía y su rica conectividad, la información de la corteza estriada discurre a través de los tractos que transitan de la vía ventral hacia las zonas de la memoria de trabajo adyacentes a los lóbulos temporales, ya que estos poseen un papel fundamental para la identificación de formas13-16.
En la endotropía congénita ocurre algo distinto, debido a que se presenta una discrepancia en la información visual que arriba a V1 a través de las proyecciones geniculocalcarinas procedentes de ambos ojos, de tal manera que en V1 concurren frecuencias temporales idénticas, pero espacialmente distintas, lo que genera un incremento de la oscilación y el ruido visual17-19.
En la endotropía congénita, el integrador cortical falla18,20, en particular en los lóbulos temporales, por lo que las diferencias espaciotemporales pueden no ser moduladas correctamente, lo que altera el proceso perceptual-visual14,15,21.
Es atributo de la corteza cerebral su capacidad para eliminar el ruido, sea este visual o cualquier otro16,22. Se sabe que el ruido puede ser eliminado y amortiguado en casos de paroxismos y epilepsia, o bien mediante estimulación externa23,24, pero al margen de estas eventualidades, la corteza cerebral gestiona la eliminación del ruido25 a través de la atención26, y aunque no es la única estrategia para eliminar el ruido visual16,22,27, de algún modo la atención favorece el desempeño en el aprendizaje y contribuye a procesar y priorizar de manera selectiva lo relevante del entorno, seleccionando y llevando información a las representaciones corticales correspondientes28-30.
El ruido visual puede percibirse, ya sea desde una leve confusión visual hasta diplopía, tal como ocurre en el estrabismo cuando inicia en edades relativamente tardías del desarrollo31.
Los pacientes rehabilitados de ambliopía estrábica pueden exhibir otro tipo de ruido visual que es la interacción de contornos (crowding)32. Se cree que este fenómeno sucede en V1 debido a la interacción espacial en el contorno del estímulo visual; sin embargo, el papel que toman las áreas corticales involucradas aún no es claro33.
De algún modo, la corteza cerebral del paciente con estrabismo congénito es capaz de atenuar o eliminar el ruido visual, ya sea suprimiendo la señal anómala mediante un proceso llamado supresión o bien disminuyendo la prioridad de la información, lo que merma la fidelidad y, con ello, la calidad de la imagen, tal como sucede en la ambliopía estrábica34. En esta última suele ocurrir una perturbación de la frecuencia temporal y, por consiguiente, de la atención visual35.
Los estudios realizados in vitro en corteza cerebral de primates indican que en la ambliopía existe hipofunción en V136, así como una menor tasa metabólica en la corteza estriada ipsilateral del ojo estrábico16.
Respecto a cómo y dónde se elimina el ruido visual, resulta controversial17,37-39 y no existe un acuerdo respecto al sitio en donde ocurre la supresión en la endotropía congénita34,40, y esto a pesar de haber utilizado diferentes técnicas de neuroimagen.
Los estudios realizados con resonancia magnética funcional en adultos con ambliopía estrábica no han logrado demostrar la existencia de supresión interocular de largo alcance en V1, V2 ni V341, mientras que los estudios realizados en primates sobre la representación cortical de las áreas de supresión cortical en la visión binocular sugieren que la eliminación de la diplopía no ocurre en V1, sino en un nivel cortical superior no especificado17.
Entre los métodos neurofuncionales destaca el electroencefalograma cuantitativo (EEGq), el cual permite evaluar la corteza cerebral in vivo42-44. Los datos obtenidos del EEGq pueden procesarse mediante neurometría, una herramienta que permite identificar las variaciones en el tiempo entre las distintas regiones, por lo que al determinar el coeficiente de correlación de Pearson y la covarianza de la transformación de Fourier es posible obtener el valor de la coherencia.
La coherencia estima las semejanzas y diferencias de las señales que discurren entre las interconexiones nerviosas cortas y largas de la corteza cerebral, lo que permite evaluar la relación que existe entre la estructura y la función45. Lo anterior se logra identificando la sincronía que existe entre los distintos grupos neuronales, y con ello se puede entender cómo el cerebro comparte información de su medio interno44,46.
Las alteraciones de la coherencia pueden indicar características funcionales excesivas, deficientes o ambas. Estas alteraciones pueden ser identificadas y localizadas mediante análisis neurométrico en las distintas áreas corticales47.
La hipercoherencia indica que dos o más áreas del cerebro están sobreconectadas y trabajan juntas de manera excesiva, comprometiendo así el rendimiento para procesar la información, mientras que la hipocoherencia muestra que el cerebro no es capaz de conectar áreas corticales de manera eficiente para realizar tareas específicas. Ambas situaciones son patológicas si sobrepasan los parámetros Z normativos establecidos como normales.
Mediante análisis coherencial se estiman las semejanzas y diferencias de las señales que discurren entre las interconexiones nerviosas cortas y largas, tanto intrahemisféricas (cointra) como interhemisféricas (cointer), de la corteza cerebral, así como la sincronía que hay entre los distintos grupos neuronales y cómo el cerebro comparte información entre sus partes44,46,48. Por estas razones, el análisis de las coherencias se ha utilizado para estudiar el comportamiento de la corteza cerebral en pacientes con endotropía congénita49,50, en la que se han identificado alteraciones en la sincronización, hiperactividad, lenificación, paroxismos e incluso epilepsia en áreas precisas de la corteza cerebral44,49.
Debido a que la coherencia permite establecer la relación neurofuncional entre distintas zonas de la corteza cerebral, y conocer así el grado de participación o afectación de estas44,51, se decidió investigar el comportamiento neurofuncional cortical mediante el análisis de las coherencias en niños con endotropía congénita y comparar los resultados con población asintomática, a fin de establecer las diferencias.
Método
Se realizó un estudio de cohorte, prospectivo, comparativo, descriptivo, cuasiexperimental y observacional, en niños oriundos del Estado de Querétaro, México, con endotropía congénita, a quienes se les realizó neurometría a partir del EEGq.
Los criterios de inclusión determinaron que todos los pacientes utilizaran la corrección óptica correcta. El ojo de menor visión debía poseer una agudeza visual corregida de 20/40 o mejor. Ningún paciente podía estar bajo medicación ni presentar enfermedad neurológica conexa. A todos los pacientes se les realizó un examen oftalmológico que incluyó determinación de la agudeza visual, exploración de fondo de ojo, valoración de los reflejos pupilares y segmento anterior, así como pruebas sensoriales y motoras, para diagnosticar y clasificar correctamente el estrabismo52.
A todos los pacientes se les realizó EEGq bajo el sistema internacional 10-20, con 21 canales, con parámetros establecidos en cada época, y se estableció la composición frecuencial de la señal. Los datos obtenidos se agruparon según los rangos frecuenciales definidos por las bandas alfa, beta, delta y theta.
Se obtuvieron registros de 23 parámetros de la actividad eléctrica de cada paciente por medio de las derivaciones mono- y bipolares, y se analizaron los poderes absolutos y relativos, la coherencia (sincronía), la simetría, el gradiente y la potencia de todas las bandas frecuenciales, tanto intra- como interhemisféricas53.
Para fines de esta comunicación, se consideró la coherencia como el valor más significativo. Para determinar el valor de la coherencia, se estimó la correlación de Pearson aplicada a la covarianza de Fourier53-56.
Los valores obtenidos de la muestra fueron sometidos a análisis estadístico multivariado mediante Neurometric Analysis System (NxLink Ltd.). Este software avanzado44,57 permite comparar los valores coherenciales de los pacientes estudiados y los valores Z normativos ajustados a la edad, obtenidos de estudios multicéntricos de población asintomática. El valor Z es igual al valor del paciente (p) menos el promedio normal (Ẋ) sobre la desviación estándar normal (ơ): Z = (p -Ẋ)/ơ.
El valor Z establece entonces la probabilidad de que las mediciones electroencefalográficas de un determinado paciente correspondan o no a la población asintomática. Así, un perfil de EEGq se consideró dentro de los límites normales si menos del 5% de los valores Z alcanzaron cifras mayores de ± 1.96, tanto para anormalidades focales como generalizadas58,59.
El software permitió analizar los valores coherenciales de las 28 vías de cada hemisferio y las 8 vías interhemisféricas de los 63 pacientes. Para fines de esta publicación no se incluyeron los valores normales, esto es, aquellos menores de ± 1.96 Z, por lo que una vez reconocidos los datos patológicos se realizó un análisis estadístico descriptivo para de identificar: 1) la incidencia, es decir, el número de pacientes que presentaron alteraciones en un determinado trayecto; 2) el valor coherencial máximo, tanto positivo (hipercoherencia) como negativo (hipocoherencia); 3) el valor coherencial mínimo, tanto positivo como negativo; 4) el promedio entre el valor más alto y el más bajo; y 5) la suma acumulada, esto es, la cantidad total de eventos que sucedieron en un trayecto determinado en la muestra.
Una vez obtenidos los valores coherenciales, se priorizaron con el fin de identificar las vías intra- e interhemisféricas más afectadas, de acuerdo con la incidencia y la magnitud de la alteración.
Con base en lo anterior, se estimó la conectividad neuronal del grupo y se listaron los hallazgos más destacados en tablas y figuras, para su exposición.
Resultados
Se obtuvieron 23 parámetros de la actividad eléctrica de cada paciente, por medio de las derivaciones mono- y bipolares. A partir de estos parámetros se adquirieron 16,128 valores neurofuncionales: 14,112 intrahemisféricos y 2016 interhemisféricos. Estos valores se procesaron, analizando un total de 80,640 valores coherenciales a partir de los EEGq de 63 pacientes, de los cuales 38 fueron niños y 25 niñas, de 4 a 14 años de edad, que cumplieron los criterios de inclusión.
Al considerar la suma total de los eventos acumulados en cada vía se observó que las vías intrahemisféricas mayormente afectadas fueron aquellas que se dirigieron hacia ambos lóbulos temporales procedentes de sus zonas vecinas. Esto se determinó tanto por la incidencia o número de veces que se presentó la hipocoherencia como por la magnitud de esta (Fig. 1).
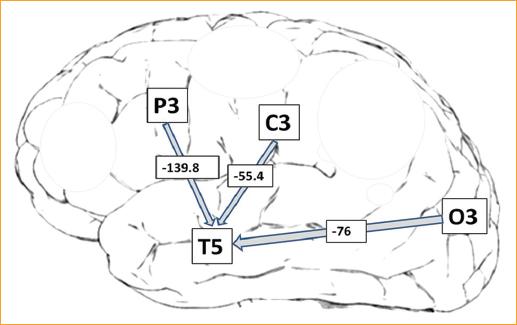
Figura 1 Comportamiento bioeléctrico cortical de los pacientes con estrabismo congénito, determinado a partir del análisis neurométrico. En cajas, con letras, la abreviatura de las zonas contiguas a los lóbulos temporales, con los que mantiene una mala conectividad a partir de una relación de hipocoherencia parieto-temporal izquierda (P3-T5), centro-encefálica izquierda (C3-T5) y occipito-temporal izquierda (O3-T5). En cajas, con números, la suma los valores patológicos para ese trayecto. Las flechas señalan el sentido de la relación hipocoherente entre distintas zonas del cerebro.
Se identificaron dificultades en la conectividad intrahemisférica principalmente en las porciones posteriores del cerebro, desde las regiones centro-encefálicas, parietales y occipitales hacia ambos los lóbulos temporales, siendo el valor máximo de la hipocoherencia de 8.0 para la cointra delta en P4-T6. De las 56 vías intrahemisféricas analizadas, 24 presentaron relaciones hipofuncionantes, especialmente hacia los lóbulos temporales (Fig. 2 y Tabla 1).
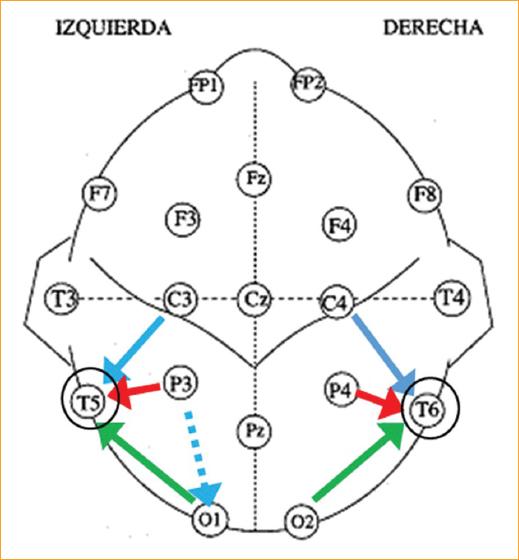
Figura 2 El esquema muestra las alteraciones de la conectividad intrahemisférica más relevantes determinadas en 63 pacientes con estrabismo congénito. Las flechas rojas representan los valores cointer más bajos encontrados en la muestra, en orden de importancia P3-T5 y P4-T6, seguidamente en color azul C4-T6, P3-O1, C3-T5, y finalmente en verde O1-T5 y O2-T6. La onda más alterada fue la delta, la vía más afectada fue la parieto-temporal derecha y los lóbulos con mayor perturbación neurofuncional fueron los temporales.
Tabla 1 Alteraciones de la cointra en el estrabismo congénito. Prevaleció una relación cortical hipofuncional en la mayor parte de las vías intrahemisféricas, principalmente en los trayectos parieto-temporales.
| Incidencia | Porcentaje | Promedio | Zona | Onda |
|---|---|---|---|---|
| 48 | 76.00 | -3.3969 | P4-T6 | Theta |
| 43 | 68.25 | -3.3442 | P4-T6 | Delta |
| 42 | 66.66 | -3.3302 | P3-T5 | Delta |
| 38 | 60.31 | -2.9695 | P4-T6 | Beta |
| 37 | 58.73 | -3.4424 | P3-T5 | Theta |
| 36 | 57.14 | -3.2372 | P4-T6 | Alfa |
| 33 | 52.38 | -3.2703 | P3-T5 | Alfa |
| 32 | 50.79 | -2.7972 | C4-T6 | Theta |
| 31 | 48.43 | -3.0755 | P3-T5 | Beta |
| 31 | 48.43 | -2.7161 | C4-T6 | Delta |
| 28 | 44.44 | -2.49 | C4-T6 | Beta |
| 26 | 41.26 | -2.9446 | P3-O1 | Delta |
| 24 | 38.09 | -2.9488 | P3-O1 | Theta |
| 24 | 38.09 | -3.1071 | O2-T6 | Theta |
| 23 | 36.50 | -3.3043 | O1-T5 | Delta |
| 22 | 34.92 | -2.6077 | C3-T5 | Theta |
| 22 | 34.92 | -2.5182 | C3-T5 | Delta |
| 21 | 33.33 | -2.2995 | O1-T5 | Beta |
| 19 | 30.15 | 3.1479 | O1-T3 | Beta |
Se identificó una relación hipocoherente parieto-occipital izquierda anormal en el 41.2% de la muestra, así como una relación hipocoherente en la mayor parte de las vías intrahemisféricas que llevan información hacia los lóbulos temporales. La hipofunción incluyó las vías parieto-temporales, occipito-temporales y centro-temporales, así como las vías largas intertemporales T5-T6.
Las vías ventrales cortas occipito-temporales derechas O2-T6 e izquierdas O1-T5 mostraron hipocoherencia; esta última fue de -6.93 para alfa hasta +3.06 para beta en el 18.75% de la muestra, mientras que la vía O2-T6 o vía ventral corta derecha presentó una relación hipocoherente de -7.07 para alfa hasta +2.23 para beta en el 16% de la muestra, por lo que la relación de las vías cortas fue hipofuncional.
Al analizar la actividad cointra de las vías ventrales largas occipito-temporales derechas O2-T4 e izquierdas O1-T3 se evidenció un estado hipercoherente, en especial en el trayecto izquierdo O1-T3, con +2.06 para delta hasta +5.76 para theta en el 23% de la muestra. La vía ventral larga derecha mostró -2.23 para delta e hipercoherencia de +4.75 para theta en el 9.5% de la muestra.
El 85.71% de los pacientes presentaron un retraso en la información procedente de distintas áreas del cerebro hacia los lóbulos temporales, incluida la zona T3, con excepción de las vías ventrales largas O1-T3 y O2-T4.
Por su parte, las alteraciones interhemisféricas más destacadas sucedieron al modo de hipocoherencia importante, tanto en las porciones anteriores del cerebro de izquierda a derecha FP1-FP2 como en las porciones temporales de izquierda a derecha T5-T6.
Se observaron relaciones hipofuncionantes interhemisféricas en 36 de los 63 pacientes, siendo las vías más afectadas FP1-FP2, F3-F3 y F7-F8, con marcada hipocoherencia para delta, cuya medida máxima fue de -9.03 en FP1-FP2 (Tabla 2).
Tabla 2 Alteraciones de la cointer en el estrabismo congénito. El análisis coherencial mostró una relación interhemisférica cortical hipofuncional entre las vías fronto-frontales y temporo-temporales.
| Incidencia | Porcentaje | Promedio | Zona | Onda |
|---|---|---|---|---|
| 37 | 58.73 | -3.2714 | FP1-FP2 | Delta |
| 32 | 50.79 | -2.9331 | FP1-FP2 | Theta |
| 23 | 36.5 | -2.3965 | T5-T6 | Delta |
| 22 | 34.92 | -2.5723 | FT-F8 | Delta |
| 20 | 31.74 | -3.007 | F3-F4 | Delta |
| 20 | 31.74 | +3.00 | T3-T4 | Beta |
| 19 | 30.15 | -2.9026 | FP1-FP2 | Alfa |
Discusión
La endotropía congénita es un trastorno neurológico con implicaciones corticales, oftalmológicas, funcionales, cosméticas, psicológicas, educacionales y sociales60. Mediante estudios de neuroimagen se ha descubierto una asociación entre disfunción cortical y estrabismo congénito, pero no se había identificado y mesurado la disfunción en la conectividad cortical, ni se conocían las vías más afectadas, hasta la publicación de un estudio en 201739.
El análisis coherencial develó que los pacientes con endotropía congénita presentan dificultad en la conectividad de las vías cortas y largas, tanto intra- como interhemisféricas, y que estas alteraciones podrían estar relacionadas con la ambliopía, la supresión y la percepción visual.
Los lóbulos occipitales son responsables de la ambliopía, que afecta la primera vía visual y, por tanto, la agudeza visual. El comportamiento de la coherencia occipito-occipital en el presente análisis concuerda con estudios realizados in vitro en corteza cerebral de primates, que indican que en la ambliopía existe hipofunción en V136, así como una menor tasa metabólica en la corteza estriada ipsilateral del ojo estrábico16; sin embargo, solo el 9% de la muestra exhibió una tendencia a la hipofunción occipito-occipital, especialmente para la onda beta, con un rango de -5.01 a +3.51, quizás como una manifestación electroencefalográfica de la ambliopía.
La ambliopía resultó congruente con una conectividad occipito-occipital relativamente normal, quizás porque filogenéticamente la corteza visual primaria está diseñada para recibir y procesar a través de distintos circuitos cortico-corticales aferencias de muy distintas frecuencias espaciotemporales, y no para hacer lo contrario, esto es, para eliminar las imágenes61; de hecho, el 91% de los pacientes presentaron una relación occipito-occipital relativamente normal. Esto resulta relevante porque, si se considera a priori que la corteza estriada es responsable de suprimir la información anómala, se esperaría encontrar una hiperactividad interhemisférica occipito-occipital, pero eso no es lo que sucedió en el presente análisis. Lo anterior coincide con aquellos estudios en los que no se encontraron indicios de que la supresión sea una actividad de la corteza estriada41,62.
Por su parte, el integrador temporal, que corresponde a la segunda vía visual, se sabe que interviene en el proceso de eliminación del ruido visual, así como en la fisiopatogenia del estrabismo congénito15,21.
La conectividad occipito-temporal posee cuatro vías: dos largas y dos cortas, izquierdas y derechas, respectivamente13,63: La vía occipito-temporal comprende las vías cortas O1-T5 y O2-T6 y las vías ventrales largas O1-T3 y O2-T4, izquierdas y derechas, respectivamente13. Estas vías parecen tener un papel determinante en la supresión del ruido visual, ya que se evidenció un estado hiperfuncionante, especialmente en el trayecto izquierdo O1-T3.
La circunvolución temporal inferior, representada en el EEGq como la zona T3, resultó alterada, ya que la actividad cointra de las vías occipito-temporales ventrales largas izquierda y derecha, medida desde O1-T3 y O2-T4, manifestó una hiperfunción importante en el 23% de la muestra. Estas vías se dirigen a la memoria de trabajo, y su inusitada hiperactividad plausiblemente podría estar relacionada con la eliminación del ruido visual15,21.
Se esperaría que el ruido inducido por la falsa proyección manifestara una relación hipercoherente entre los lóbulos occipital y temporal, incluso entre ambos lóbulos occipitales, pero esto no fue lo que se observó. Lo anterior resulta relevante debido a que la literatura dice que la supresión es un proceso cortical activo25; sin embargo, los estudios no han demostrado dónde ocurre.
Todo indica que eliminar el ruido visual es un proceso cortical que requiere la interacción de distintas áreas del cerebro64, y una manera para identificar dónde es precisamente mediante el análisis de las coherencias.
Las relaciones funcionales más afectadas fueron las parieto-temporales. Las vías ventrales largas posteriores P3-T3 y P4-T4, correspondientes al área 38 de Brodmann, manifestaron un desempeño relativamente normal; sin embargo, la conectividad de las vías cortas posteriores P3-T5 y P4-T6, que comprenden tanto el giro medio como el giro inferior, así como las vías occipito-temporales O1-T5 y O2-T6, resultaron con frecuencia afectadas, lo que es de llamar la atención porque a través de estas vías se procesa el reconocimiento de rostros (Fig. 2 y 3).
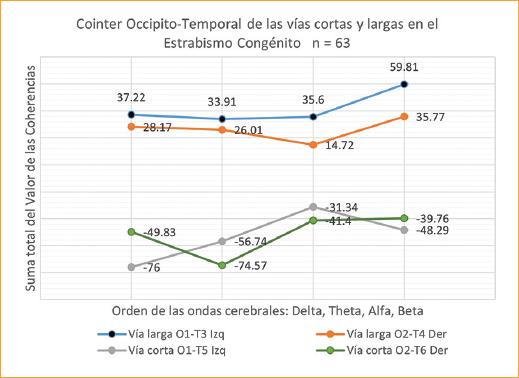
Figura 3 Las vías ventrales largas O1-T3 y O2-T4 son hiperfuncionantes en la endotropía congénita, posiblemente por su participación en la supresión del ruido visual, mientras que las vías ventrales cortas O1-T5 y O2-T6 resultan hipofuncionantes, acorde con dificultades en la percepción visual.
El reconocimiento de rostros es una de las habilidades visuales complejas de aparición más temprana en el ser humano. El estudio mostró que las vías P3-T3 y P4-T4, encargadas de la percepción visual, funcionaron correctamente, mientras que las vías encargadas de la adquisición de nuevas habilidades perceptuales-visuales, esto es, las vías temporales cortas posteriores P3-T5 y P4-T6, resultaron hipofuncionantes en los paciente estrábicos (Fig. 2).
Otro aspecto que llama la atención es que las vías que conducen información hacia los lóbulos temporales, esto es, las vías parieto-temporal, centro-temporal y occipito-temporal izquierdas y derechas, respectivamente, mantuvieron siempre una relación hipocoherente (Fig. 1).
La propia relación intertemporal, esto es, la cointer T3-T4 y T5-T6, mostró signos de hipofunción, y es que la hipofunción de los lóbulos temporales en la endotropía congénita es un signo neurométrico destacado, entre otras consideraciones, no solo por su papel en la elaboración de imágenes complejas, sino porque la zona inferotemporal es el asiento para la clasificación visual de las formas, así como para la facilitación en la utilización de los datos visuales en el aprendizaje y en la memoria visual65 (Tabla 2).
Un porcentaje importante de los pacientes analizados presentaron alteraciones en las vías occipito-temporales O2-T6 y O1-T5, de cuya integridad funcional depende la ejecución de las funciones visuales superiores para la percepción visual66.
La vía parieto-temporal, encargada de llevar la información al lóbulo temporal para la identificación de objetos que se desplazan en el espacio67,68, resultó también afectada, y es plausible afirmar que una deficiente conectividad de este circuito determinaría que los niños con endotropía congénita manifiesten cierta inhabilidad congénita para la percepción visual.
Todo lo anterior permite comprender por qué los niños estrábicos, aunque gocen de una adecuada agudeza visual, deben usar su corrección óptica, llevar terapia visual, tratar su ambliopía y alinear correctamente sus ojos, y que manifiesten problemas perceptuales visuales, especialmente para la ejecución de movimientos sacádicos, la percepción de formas y tamaños, la velocidad de percepción visual y la percepción periférica21,69.
La hipocoherencia cointer más importante se ubicó en las porciones anteriores del cerebro, especialmente en FP1-FP2 para la onda delta en 36 casos y para la onda theta en 32 casos. Resulta notable que la coherencia más baja haya ocurrido en las regiones encargadas de los procesos cognitivos complejos, tales como la memoria de trabajo, la flexibilidad cognitiva y la priorización de la información procedente de todo el cerebro70 (Fig. 1). Lo anterior sugiere que el análisis final del proceso visual podría estar comprometido también en el paciente estrábico, ya que algunas alteraciones en esta circunvalación afectan la representación de características complejas70-72.
El estudio sugiere que, desde un punto de vista neurofuncional, la ambliopía estaría relacionada con una coherencia interhemisférica occipito-occipital O1-O2 normal, así como con una hipofunción temporo-temporal T3-T4 y T5-T6, mientras que la supresión se expresa como hiperfunción en las vías occipito-temporales largas derechas e izquierdas O2-T4 y O1-T3, así como una pobre conectividad interhemisférica FP1-FP2.
Por su parte, la hipofunción de las vías intrahemisféricas temporales cortas posteriores P3-T5 y P4-T6, e interhemisféricas FP1-FP2, podría estar relacionadas con dificultades en la percepción visual.
Las relaciones neurofuncionales aquí señaladas revelan la presencia de cambios neurofuncionales corticales significativos en el comportamiento de las vías de interconexión cortas y largas, intra- e interhemisféricas, contenidas en la sustancia blanca cortical.
Conclusiones
De acuerdo con estos hallazgos, es plausible considerar que tanto la ambliopía como la supresión estrábica son estrategias distintas que concurren en la economía del sistema visual con la finalidad de reducir el ruido visual. Desde esta perspectiva, tanto la ambliopía como la supresión no significan per se una enfermedad, sino que se trata de mecanismos neuroadaptativos consecuentes con la neuroplasticidad cerebral y que contribuyen positivamente a atenuar la dificultad espaciotemporal, la oscilación y el ruido visual que genera la falta de alineamiento ocular, situación que infortunadamente no sucede en los estrabismos de presentación tardía, en cuyo caso la sensación es consciente debido a que el integrador cortical no puede eliminar la falsa proyección.
Es plausible considerar que la información aquí recabada contribuya a comprender mejor la clínica, la fisiopatología y el pronóstico la endotropía congénita, así como ayudar en la toma de decisiones.











 nueva página del texto (beta)
nueva página del texto (beta)


