Introducción
La cirugía de cataratas es la terapia principal para casos sintomáticos. La facoemulsificación (FE) es el procedimiento de elección, principalmente a través de una incisión pequeña1,2. La cirugía de cataratas asistida por láser de femtosegundo (FLACS) es un procedimiento emergente que ayuda en la incisión corneal, la capsulotomía y la fragmentación del cristalino para reducir la cantidad de energía ultrasónica y el tiempo efectivo de FE (TEF)3,4. Hasta la fecha, la FLACS no es significativamente diferente de la cirugía de cataratas con FE en complicaciones intraoperatorias (desgarros de la cápsula anterior y posterior), postoperatorias (edema macular cistoide, elevaciones persistentes de la presión intraocular)5,6 y pérdida de células endoteliales corneales (secundaria a la energía fotodisruptiva)7. No obstante, la FLACS logra una mejor agudeza visual corregida postoperatoria que el abordaje convencional con FE a la semana y a los 6 meses6, pero la agudeza visual no corregida no es significativamente diferente a largo plazo entre los abordajes6.
Los defensores de la FLACS o del abordaje convencional con FE coinciden en que la exposición a la energía ultrasónica provoca una lesión de las células endoteliales corneales que podría complicarse con un daño permanente, incluido el edema persistente que requiere queratoplastia8. Estudios previos en humanos y animales han informado de niveles altos de citocinas proinflamatorias como interleucinas (IL)-1β, IL-6, IL-8, prostaglandina E2 (PgE2) y factor de necrosis tumoral-α en el humor acuoso después del pretratamiento con láser de femtosegundo (FL)9-12. No obstante, los resultados y las condiciones (como el grado de catarata y el equipo) son heterogéneos o evalúan el flare de la cámara anterior con métodos indirectos como la fotometría9,13. Hasta la fecha, según nuestro conocimiento, no existen informes sobre el perfil inflamatorio estandarizado para el fenotipo de catarata, las diferencias interoperatorias y el equipo de FL utilizando muestras de humor acuoso de hispanos. Aquí, evaluamos la respuesta inflamatoria en pacientes con opacidades nucleares (NO3) pretratados con condiciones estándar de FL antes de la FE. Analizamos iniciadores comunes de vías inflamatorias o citocinas previamente investigadas con hallazgos positivos en otros entornos y etnias.
Métodos
Diseño del estudio y población
Realizamos un estudio transversal de 67 ojos de 67 pacientes sometidos a cirugía de cataratas; 34 recibieron pretratamiento con FL. Todos los casos fueron reclutados en la Fundación Hospital Nuestra Señora de la Luz, IAP en la Ciudad de México, y firmaron un formulario de consentimiento informado antes de su inclusión. Pacientes fueron sometidos a un examen oftalmológico completo por oftalmólogos experimentados del segmento anterior (C.P-P.; C.M-V.; A.C-O.). Incluimos pacientes de 60 años o más con catarata nuclear NO3 según el sistema de clasificación de opacidad del cristalino (LOCS) III, sometidos a cirugía de cataratas14. Excluimos los casos tratados con fármacos antiinflamatorios tópicos o sistémicos, con antecedentes de enfermedades sistémicas u oftalmológicas crónicas. Todos los procedimientos y la recopilación de datos siguieron los principios de la Declaración de Helsinki, y todos los datos se manejaron según las directrices de la Ley de Portabilidad y Responsabilidad del Seguro Médico. La junta de revisión institucional local aprobó este estudio (IRB #: CEI-005-20170306).
Pretratamiento con FL
Todos los pacientes recibieron profilaxis antibiótica durante 3 días previo a la cirugía. Para estandarizar las diferencias interoperatorias, un cirujano del segmento anterior con gran experiencia de un centro de capacitación de alta demanda realizó la FE y la FLACS (C.P-P.). Según el protocolo, todos los pacientes recibieron tropicamide al 0,5% tópicamente (Laboratorios Sophia, Ciudad de México, México) y fenilefrina al 5% (Laboratorios Sophia, Ciudad de México, México) 30 minutos antes de la cirugía. La FLACS se realizó utilizando la interfaz LenSx® FL v.2.23 y SoftFit® (Alcon Laboratories, Fort Worth, TX, EE. UU.). Bajo tomografía de coherencia óptica, el FL realizó la capsulotomía anterior (tamaño 5,0 mm, energía de pulso de 7,5 μJ), la fragmentación nuclear (energía de pulso de 10 μJ), las incisiones corneales primaria (tamaño 2,4 mm, 7,5 μJ) y de puerto lateral (tamaño 1 mm, energía de pulso de 4 μJ). Utilizamos los mismos parámetros para la fragmentación nuclear (2 secciones transversales con un tamaño de corte de 5,2 mm y 1 cilindro de corte central con un diámetro de 2,0 mm). Tras el tratamiento con FL, los pacientes fueron trasladados al quirófano. Se permitió un máximo de 15 minutos entre el tratamiento con FL y la toma de muestras de humor acuoso. En el grupo de control de FE, la muestra de humor acuoso se obtuvo a través del puerto accesorio antes de realizar la incisión principal.
Muestreo de humor acuoso
Al inicio de la cirugía, recogimos 5 μL de humor acuoso en condiciones estériles en ambos grupos, a través de la incisión del puerto lateral, realizada con FL o manualmente para la FE, utilizando una aguja de calibre 24. Luego, congelamos y almacenamos inmediatamente todas las muestras a −80°C para su análisis.
Determinación de las concentraciones de PgE2, IL-1β e IL-6 en humor acuoso
Inmediatamente después de la recogida, las muestras de humor acuoso fueron procesadas por investigadores experimentados y ciegos siguiendo un protocolo estandarizado (M.C-R.; A.R-C.). La concentración de PgE2 se determinó mediante un ensayo de inmunoadsorción enzimática (ELISA) competitivo con el Prostaglandin E2 high sensitivity ELISA Kit (Abcam, Cambridge, Reino Unido), bajo un espectrofotómetro a una longitud de onda de 412 nm, según las especificaciones del fabricante. Para IL-1β e IL-6, utilizamos matrices de perlas citométricas (CBA) para mediciones cuantitativas con el BD CBA Human Inflammatory Cytokines Kit (Bioscience, San José, CA, EE. UU.) según las especificaciones del fabricante. Las preparaciones de IL-1β e IL-6 se analizaron con el citómetro de flujo FACSCanto II y el software Flow Cytometric Analysis Program Array v3.0 (Bioscience, San José, CA, EE. UU.).
Análisis estadístico
Comenzamos describiendo la muestra completa utilizando medias y desviaciones estándar para datos continuos y frecuencias relativas para datos categóricos (tabla 1). Luego realizamos análisis estratificados por los grupos de comparación (pretratamiento con FL vs FE) utilizando la prueba t de Student (variables continuas) y las pruebas χ2 (variables categóricas) en SAS v.9.4 (tabla 2). Las variables demográficas o clínicas significativamente asociadas con cualquiera de los grupos en los análisis bivariados al nivel de 0.10 se consideraron para un ajuste adicional mediante regresiones lineales (tabla 3). Para nuestro abordaje de modelado, primero realizamos un análisis bivariado exhaustivo de todas las variables clínicas con el estado del grupo, evaluamos la normalización de variables (transformación logarítmica) y la colinealidad entre citocinas (Fig. S1, material adicional). Luego calculamos la concentración media de citocinas ajustada por covariables con modelos de regresión lineal. Todos estos modelos siguieron: Log (PgE2, IL-1β, IL-6) ~ β1 Grupo (FE 0 vs pretratamiento con FL 1) + Covariables clínicas + ε. Donde β1: representa las diferencias en la concentración media de citocinas ajustada entre la FE y el pretratamiento con FL. También evaluamos la idoneidad de las covariables eliminando del modelo completo de forma escalonada hacia atrás cada variable manteniendo nuestra exposición de interés (FE vs pretratamiento con FL). En cada paso, evaluamos el cambio en los coeficientes restantes del 10% y comparamos las razones de verosimilitud -2 de los modelos completo y reducido con una distribución χ2 para determinar aún más la significación de cada variable independiente politómica para el modelo general. Por último, para producir el modelo más parsimonioso, reevaluamos cada predictor eliminado individualmente en el modelo más reducido siguiendo el mismo proceso descrito anteriormente. Nuestro modelo final se muestra en la tabla 3. Todos nuestros modelos siguieron los supuestos convencionales de regresión lineal.
Tabla 1 Descripción de la muestra (n = 67)
| Característica | n (%)* |
|---|---|
| Grupo de tratamiento, n (%) | |
| Terapia asistida por láser de femtosegundo | 34 (50,8) |
| Terapia convencional | 33 (49,3) |
| Datos demográficos basales | |
| Edad (años), media ± DE | 70,6 ± 8,3a |
| Sexo, n (%) | |
| Masculino | 21 (31,3) |
| Femenino | 46 (68,7) |
| Parámetros bioquímicos | |
| PgE2, media ± DE† | 4,1 ± 2,2b |
| Mediana (RIC) | 91,6 (18,6 - 319,2) |
| Datos ausentes | 1 |
| IL-1β, n (%)‡ | |
| No detectable (0,0) | 47 (92,2) |
| ≥ 0,0 | 4 (7,8) |
| Datos ausentes | 16 |
| IL-6, media ± DE† | 4,5 ± 2,1c |
| Datos ausentes | 16 |
Descripción completa de la muestra. Se muestran las medias y las desviaciones estándar (para los valores transformados logarítmicamente), junto con el tamaño de la muestra y los porcentajes de las columnas.
*Es posible que las cifras no sumen los totales debido a la falta de datos, y es posible que los porcentajes de las columnas no sumen el 100% debido al redondeo.
†Transformado logarítmicamente.
‡Evaluamos los valores distintos de cero como un resultado categórico.
aAsimetría (−0,21), Curtosis (−0,64).
bMedia y desviación estándar de los datos no transformados: 243,5 ± 425,1, fuertemente sesgado a la derecha.
cMedia y desviación estándar de los datos no transformados: 636,2 ± 2284,5, fuertemente sesgado a la derecha. PgE2: prostaglandina E2; IL: interleucina.
Tabla 2 Descripción de la muestra según grupo de tratamiento (n = 67)
| Característica | Femto-asistida (n = 34) (%) | Convencional (n = 33) (%) | p† |
|---|---|---|---|
| Datos demográficos basales | |||
| Edad (años), media ± DE | 70,3 ± 9,2 | 70,8 ± 7,3 | 0,7755 |
| Sexo, n (%) | 0,0541 | ||
| Masculino | 7 (20,6) | 14 (42,4) | |
| Femenino | 27 (79,4) | 19 (57,6) | |
| Parámetros bioquímicos | < 0,0001a | ||
| PgE2, media ± DE† | 5,7 ± 0,9 | 2,6 ± 1,4 | |
| Datos ausentes | 1 | 1,000 | |
| IL-1β, n (%)¶ | |||
| No detectable (0,0) | 25 (92,6) | 22 (91,6) | |
| ≥ 0,0 | 2 (7,4) | 2 (8,3) | |
| Datos ausentes | 7 | 9 | |
| IL-6, media ± DE‡ | 6,1 ± 1,2 | 2,7 ± 1,3 | < 0,0001b |
| IL-6, mediana ± RIC | 5,9 ± 1,4 | 3,0 ± 2,1 | < 0,0001 |
| Datos ausentes | 7 | 9 |
Características estratificadas por grupo de tratamiento (asistido por Femto vs FE convencional). Las diferencias estadísticamente significativas se muestran en negrita y se calcularon con la prueba t de Student (variables continuas) [prueba exacta de Fisher cuando fue apropiado] o la prueba χ2(variable categórica). Cuando fue aplicable, se realizaron métodos no paramétricos (análisis de puntuaciones medianas). *Es posible que las cifras no sumen los totales debido a la falta de datos, y es posible que los porcentajes de las columnas no sumen el 100% debido al redondeo.
†Valor p para la prueba t de Student (variable continua) o la prueba χ2 (variable categórica) [prueba exacta de Fisher cuando fue apropiado]. Cuando fue aplicable, se realizaron métodos no paramétricos (análisis de puntuaciones medianas).
‡Transformado logarítmicamente.
¶Evaluamos los valores distintos de cero como un resultado categórico. En negrita, asociaciones estadísticamente significativas.
aDiferencia de medias entre grupos 3,1 ± 1,2. µdiff (IC 95%): 3,1 (2,5, 3,72).
bDiferencia de medias entre grupos 3,5 ± 1,3. µdiff (IC 95%): 3,5 (2,7, 4,2).
Tabla 3 Niveles medios ajustados de PgE2 e IL-6 (n = 67)
| Característica | β ajustado (EE) | p |
|---|---|---|
| Niveles medios ajustados de PgE2 | ||
| Grupo de tratamiento* | ||
| Terapia asistida por láser femtosegundo | 3,24 (1,57) | < 0.0001 |
| Terapia convencional | Referencia | |
| Datos demográficos basales | ||
| Edad (años) | −0,02 (0,02) | 0,4777 |
| Sexo | ||
| Masculino | Referencia | 0,8360 |
| Femenino | 0,08 (0,40) | |
| Niveles medios ajustados de IL-6 | ||
| Característica | β ajustado (EE) | p |
| Grupo de tratamiento* | ||
| Terapia asistida por láser femtosegundo | 3,40 (0,37) | < 0,0001 |
| Terapia convencional | Referencia | |
| Datos demográficos basales | ||
| Edad (años) | −0,01 (0,02) | 0,9330 |
| Sexo | ||
| Masculino | Referencia | 0,5840 |
| Femenino | 0,22 (0,41) | |
La media geométrica de la concentración de PgE2 en humor acuoso transformada logarítmicamente ajustada con regresión lineal. Nuestras estimaciones son una función de Log (PgE2) ~ Grupo (Incisión manual 0 versus FLACS 1) + edad + ε. Donde β representa la diferencia de medias ajustada por covariables en PgE2 entre grupos. La media geométrica de PgE2 y la media de la concentración de IL-6 en humor acuoso transformada logarítmicamente ajustadas con regresión lineal. Nuestras estimaciones son una función de Log (PgE2) ~ Grupo (Incisión manual 0 versus FLACS 1) + edad + ε. Donde β representa la diferencia de medias ajustada por covariables en PgE2 entre grupos, y Log (IL-6) ~ Grupo (Incisión manual 0 versus FLACS 1) + edad + ε. Donde β representa la diferencia de medias ajustada por covariables en IL-6 entre grupos. En negrita, asociaciones estadísticamente significativas.
*Transformado logarítmicamente.
Resultados
Población del estudio
Analizamos 67 pacientes, la mitad (n = 34) sometidos a FLACS. La descripción completa de nuestra muestra se detalla en la tabla 1. En promedio, nuestra población tenía 70,6 ± 8,3 años y era predominantemente femenina (68,7%). Para todas las citocinas, hubo resultados positivos y detectables. No obstante, en cuatro casos la concentración de IL-1β no fue detectable (tabla 1). Además, para probar si alguna de las características demográficas estaba significativamente asociada con un grupo (FE vs FLACS), realizamos análisis estratificados, representados en la tabla 2. No hubo diferencias significativas en la edad y la proporción de hombres y mujeres entre los grupos de pacientes. Las únicas diferencias significativas entre los grupos fueron las concentraciones de PgE2 e IL-6.
Concentraciones de citocinas entre incisiones manuales y FLACS
En nuestra muestra por CBA, encontramos que los niveles medios no ajustados de IL-6 fueron 2,3 veces más altos en el grupo FL frente al abordaje convencional con FE (Fig. 1) (6,1 ± 1,2 vs 2,7 ± 1,3). Con este método, no pudimos evidenciar ninguna diferencia notable en los niveles de IL-1β entre los grupos (tabla 2). Además, mediante ELISA competitivo, los niveles medios de PgE2 aumentaron significativamente. El grupo FLACS, frente al grupo a tratamiento convencional con FE, tuvo, de media, el doble de expresión de PgE2 (5,7 ± 0,9 vs 2,5 ± 1,4) (tabla 2). Es importante destacar que no hubo correlación entre IL-6 y PgE2, incluso al estratificar por grupo de tratamiento (Fig. S2, material adicional).
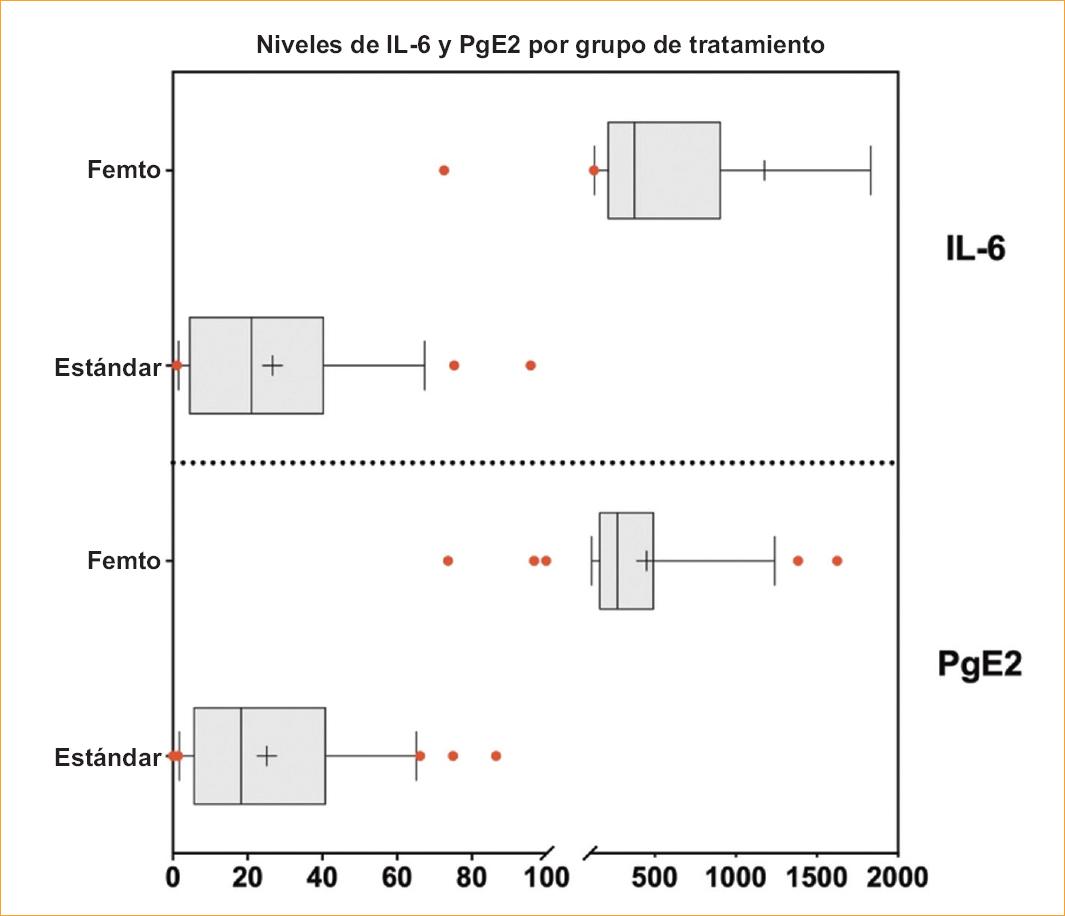
Figura 1 Niveles de interleucinas-6 y prostaglandina E2 por grupo de tratamiento. Diagramas de caja (UNIDADES) transformados logarítmicamente de interleucinas-6 y prostaglandina E2 estratificados por grupo de tratamiento (terapia asistida por láser de femtosegundo frente a terapia convencional). Se muestran la media (+), Q1, la mediana, Q3 y los valores atípicos (en rojo).
Para validar el efecto independiente de FL en los niveles de citocinas, ajustamos nuestros hallazgos mediante modelos lineales. Utilizando la edad y el sexo como constantes, el pretratamiento con FL aumentó significativamente la expresión de PgE2 e IL-6 en el humor acuoso en 3,24 pg/μL y 3,40 pg/μL, respectivamente, en comparación con la FE convencional (β ajustada 3,24, error estándar [EE] 1,57, p = 0,0001) (β ajustada 3,40, EE 0,37, p = 0,0001, respectivamente).
Discusión
Nuestro objetivo fue evaluar mediadores inflamatorios clave en el humor acuoso de pacientes con cataratas nucleares (LOCS III NO3) tratados con FLACS en condiciones estandarizadas (cirujano experimentado del segmento anterior estandarizado, condiciones de FL, fenotipo de catarata). Nuestros resultados sugieren que existe un aumento significativo de PgE2 e IL-6 después de la exposición a FL frente al primer paso del abordaje estándar con FE. Esta regulación positiva ocurrió durante los primeros 15 minutos después de la exposición a FL. En este sentido, los pacientes expuestos a la energía FL podrían tener una ventaja inicial con una respuesta proinflamatoria activada mediada por estas citocinas.
IL-6 y PgE2 son señalizadores conocidos de daño tisular15,16. En el ojo, las prostaglandinas se sintetizan en el cuerpo ciliar y el iris, y se liberan al humor acuoso después de lesiones traumáticasZ17-19. En modelos animales, la inyección intracamerular de PgE2 provoca una elevación significativa del contenido proteico del humor acuoso17. Estos cambios están fuertemente correlacionados con un aumento sostenido de la presión intraocular y la disrupción de la barrera hematoacuosa17,18. La IL-6, por otro lado, es sintetizada por varios tejidos oculares, como las células epiteliales, estromales y endoteliales de la córnea20,21. En el humor acuoso, se informan consistentemente niveles aumentados de IL-6 en patologías inflamatorias de la cámara anterior como la ciclitis heterocrómica de Fuchs o la uveítis por toxoplasma22,23. La IL-6 está principalmente regulada positivamente por la IL-1β24. Curiosamente, en nuestro estudio, los niveles de IL-1β no fueron significativamente diferentes entre los grupos. Es posible que no hayamos detectado la IL-1β, una IL con una vida media de 6 minutos, porque permitimos hasta 15 minutos después del procedimiento FL antes del muestreo25,26. No obstante, podríamos haber observado el efecto aguas abajo respaldado por nuestros resultados significativos en IL-6. Las implicaciones clínicas y las interacciones específicas de las citocinas después del tratamiento con FL en hispanos justifican estudios adicionales.
La importancia de este estudio radica en la inclusión de un solo tipo y grado de catarata y en condiciones estrictamente estandarizadas. Estudios previos han evaluado la respuesta inflamatoria de la cámara anterior, pero han analizado diferentes tecnologías láser o han pretratado con fármacos antiinflamatorios no esteroideos tópicos como profilaxis11,27. A pesar de estas variaciones entre equipos y poblaciones estudiadas, los resultados son consistentes.
El tratamiento con FL podría producir un aumento inicial y rápido de mediadores proinflamatorios. No obstante, otros estudios han informado que el flare de la cámara anterior en el período postoperatorio inmediato es más significativo con el abordaje de incisión manual9,13. El mayor TEF empleado en la cirugía convencional con FE conduce a un daño acumulativo y a la producción de citocinas28,29. En nuestro estudio, estandarizamos el fenotipo de la catarata, el cirujano (diferencias interoperatorias) y el equipo de FL. Nuestros resultados avalan que el tratamiento con FL podría ser ventajoso en escenarios donde se sospecha una catarata hipermadura. Las cataratas duras tienen más probabilidades de aumentar el TEF y la cantidad de energía ultrasónica requerida. En este sentido, un procedimiento automatizado que ahorre tiempo probablemente arrojaría buenos resultados en este escenario. No obstante, el uso indiscriminado de esta herramienta también podría producir efectos no deseados. No obstante, hasta la fecha y en nuestra población, FL es un procedimiento seguro y eficaz.
Conclusiones
La asistencia con láser de femtosegundo en la facoemulsificación aumentó los niveles de IL-6 y PgE2 en el humor acuoso durante los primeros pasos de la cirugía. Saber si esta respuesta inflamatoria afecta el resultado quirúrgico requiere estudios adicionales y específicamente diseñados.
Contribución de los autores
Conceptualización y diseño del trabajo: C. Palacio-Pastrana, A. Robles-Contreras, M. Ceballos-Reyes, V. Lima-Gómez. Adquisición de datos: C. Palacio-Pastrana, C. Mendoza-Velásquez, A. Camacho-Ordóñez. Análisis e interpretación de datos: C. Palacio-Pastrana, A.C. Pérez-Ortiz. Curación de datos: C. Palacio-Pastrana, A.C. Pérez-Ortiz, B. Antonio-Aguirre. Redacción - preparación del borrador original: C. Palacio-Pastrana, A.C. Pérez-Ortiz, B. Antonio-Aguirre. Redacción - revisión y edición: C. Palacio-Pastrana, A.C. Pérez-Ortiz, B. Antonio-Aguirre, V. Lima-Gómez. Aprobación final: C. Palacio-Pastrana, A.C. Pérez-Ortiz, M. Ceballos-Reyes, V. Lima-Gómez. C. Palacio-Pastrana y V. Lima-Gómez aceptan ser responsables de todos los aspectos del trabajo, aseguran que las preguntas relacionadas con la exactitud o integridad de cualquier parte del trabajo fueron investigadas y resueltas de manera adecuada.











 nueva página del texto (beta)
nueva página del texto (beta)


