Introducción
El desarrollo de esta investigación, radica en la importancia que tiene la minimización del consumo de combustibles fósiles dentro de la industria siderúrgica, partiendo del uso de agua industrial amoniacal para la generación electroquímica de hidrógeno (que puede ser aprovechado dentro de la cadena de producción de acero) y a su vez, dar uso a electrodos de desecho que se almacenan, debido a que no son aptos para el proceso de aceración. Por lo tanto, el objetivo general es, como ya se mencionó, la generación electroquímica de hidrógeno partiendo de agua industrial amoniacal, producida en plantas coquizadoras, utilizando electrodos de acería que ya no son aptos para el proceso de fabricación del acero, como ánodo y cátodo respectivamente. De esta manera, la investigación tiene un enfoque ecológico, ya que, además de producir hidrógeno, con la finalidad de utilizarlo en la industria siderúrgica, busca el aprovechamiento de subproductos siderúrgicos.
Para plantear el problema, es importante considerar que en [1], se reporta que el hidrógeno es un buen combustible, capaz de administrar más energía por unidad de masa que cualquier otro combustible conocido, 33.3 kWh por kg frente a los 13.9 kWh del gas natural o también se tiene los 12.4 kWh del petróleo. Así mismo, también el hidrógeno es un combustible limpio a nivel local, que cuando se quema lo único que produce además de energía es básicamente agua en forma de vapor, evitando entre otras cosas, emisiones de CO2 (principal gas del efecto invernadero). Otro aspecto relevante, en el desarrollo de este proyecto, es el aprovechamiento del licor amoniacal generado en la industria, ya que, según lo reporta [2], debido a la creciente preocupación relacionada tanto con el impacto económico como ambiental, se han realizado intensos esfuerzos para proponer y desarrollar un sistema avanzado de producción de amoniaco, que incluye procesos tanto termoquímicos como electroquímicos, en el mismo contexto, de acuerdo con [3], existen diversos métodos de producción de amoniaco, en busca de una tecnología sustentable. Además, cabe mencionar que, según [4] la electrólisis de amoniaco es una forma prometedora de generar hidrógeno y también es importante en términos de impacto ambiental, a fin de eliminar el amoniaco de las aguas residuales, esto ofrece una alternativa rentable y de bajo consumo de energía en comparación con los métodos convencionales, sin embargo, es necesario un mayor estudio tecnoeconómico.
Este documento, muestra una revisión bibliográfica, la descripción de la metodología implementada, el análisis y discusión de resultados obtenidos y las conclusiones más relevantes del trabajo, a fin de ser compartidos con la comunidad científica.
2. Marco teórico
2.1 Combustibles, hidrógeno y amoniaco como elementos en la neutralidad del carbono
2.1.1 Combustibles fósiles y neutralidad de carbono
El ahorro de combustible es un área de interés para todos, sobresalen tres razones para esto, tales como: el uso de combustibles se relaciona directamente con las emisiones de CO2; el uso de combustible se deriva principalmente del petróleo, cuyas reservas se están agotando; la economía de combustible está relacionada con costos de viajes y vehículos, los cuales se han duplicado desde 1970 [5].
Aunado a lo anterior, tal como lo menciona [6], alcanzar la neutralidad de carbono para el año 2050 es un desafío que enfrenta el mundo ante el cambio climático. De acuerdo con [7], el cambio del sistema energético dependiente de combustibles fósiles hacia una energía verde sostenible, proviene de la necesidad de controlar las emisiones de gases de efecto invernadero, a fin de contrarrestar el cambio climático global.
Por lo cual, [8] indica que, el hidrógeno es una pieza clave para la descarbonización en busca de alcanzar los objetivos climáticos. Como portador de energía, es muy útil para almacenar y utilizar energía renovable según lo requiera el usuario final.
Además de lo anterior, en búsqueda de la neutralidad del carbono, se ha reportado que la generación de amoniaco impulsada por hidrógeno, es actualmente la industria líder, además, el hidrógeno se consume en cantidades sustanciales en los sectores químico y de refinería, y en el sector energético, con la gama de sistemas de energía de hidrógeno, la producción, uso y aceptación pública, se prevé que el hidrógeno se convierta en un componente importante en un futuro próximo. En los sectores farmacéutico y metalúrgico el crecimiento del hidrógeno continúa aumentando [9].
2.1.2 El hidrógeno y sus vías de producción
[10] Indica que el hidrógeno rara vez se encuentra de forma natural, por lo que es necesario fabricarlo. [11] Reportaron que desde el siglo XIX, el hombre sabe cómo separar el hidrógeno y el oxígeno que forman el agua aplicando una corriente eléctrica, a este proceso se le conoce como electrólisis y se trata de una tecnología sencilla, que además de limpia ayuda a producir hidrógeno de manera limpia y de gran pureza.
De acuerdo con [8], las vías para la producción de hidrógeno son a partir de materias primas y tecnologías renovables y no renovables; siendo la que utiliza energías renovables la más respetuosa con el ambiente, pero presenta la desventaja de tener tanto pérdida de energía como costos altos. Según [10], actualmente, la mayor parte del hidrógeno se produce utilizando combustibles fósiles, mediante la captura y almacenamiento de carbono, siendo su producto el denominado “hidrógeno azul”, mientras que también se puede utilizar un electrolizador para producir hidrógeno, en donde se divide el agua en hidrógeno y oxígeno, dicho hidrógeno se denomina “hidrógeno verde” ya que es un producto renovable.
Bajo el mismo contexto, [12] indicó que al utilizarse el amoniaco directamente para obtener hidrógeno, se tiene un proceso que es ventajoso, ya que reduce la pérdida del amoniaco así como los problemas asociados con el almacenamiento del hidrógeno, esto resulta importante, ya que, según [13], si el hidrógeno fuera utilizado como un medio de energía en el futuro, se tendría que minimizar la distancia entre la fuente y el suministro, debido a los costos de transporte a través de las tuberías, que tendrían que ser de un acero especial.
[12] Indica también que utilizar amoniaco para generar hidrógeno, ofrece beneficios ambientales, ya que, siendo conservado en el amoniaco, podría utilizarse para generar energía sin emitir gases de efecto invernadero nocivos. Aunado a lo anterior, el autor indica que un electrocatalizador de amoniaco que utiliza un electrolito alcalino, puede funcionar con un 95% menos energía que un electrocatalizador de agua.
Ante la latente necesidad de minimizar las fuentes energéticas a base de carbón, se han desarrollado diversas investigaciones que proveen información relevante respecto al uso del hidrógeno.
[14] Indica que el hidrógeno ofrece una variedad de beneficios como vector de energía limpia, así como que la electrólisis del hidrógeno ha ganado una atención considerable como una opción para la integración a gran escala de energías renovables, no obstante, para utilizar su potencial, es necesario que el hidrógeno se convierta en una parte integral del sistema energético, como fuente de energía.
[15] Indica que utilizar amoniaco como portador de hidrógeno, lo hace un candidato potencial ante los desafíos de almacenamiento y transporte de hidrógeno.
[16] Indica que además de considerarse un combustible libre de emisiones de CO2, el amoniaco es un vector atractivo de hidrógeno y energía debido a la alta densidad de almacenamiento de hidrógeno, además de que es capaz de licuarse fácilmente a temperatura ambiente.
[17] Indica que el amoniaco es uno de los combustibles a base de hidrógeno que tiene muchas cualidades, dándole un papel clave en la transición a una economía basada en el hidrógeno, debido principalmente a que tiene una gran fracción de peso de hidrógeno (17.65%) y una densidad volumétrica de hidrógeno un 45% más alta que el hidrógeno líquido. Los autores también indican que la conversión de amoniaco en hidrógeno es un proceso relativamente simple que utiliza poca energía a bajo costo, cuyo subproducto es nitrógeno, el cual, también es ambientalmente amigable.
2.1.3 Generación de hidrógeno a bajo costo
En relación a la generación de hidrógeno, con procesos de menor costo, se presentan investigaciones como [18], en donde los autores, desarrollaron un estudio sobre la síntesis electroquímica de amoniaco, además de enlistar las ventajas que tiene como combustible verde. Los autores indican que el amoniaco es un combustible libre de carbono muy prometedor ya que es portador de hidrógeno y que sus ventajas le dan un gran potencial incluso como alternativa al hidrógeno, lo cual, respalda el uso de agua amoniacal en esta investigación.
En el trabajo [19], los autores investigaron cuatro técnicas de descomposición de amoniaco: descomposición térmica, reactor de membrana catalítica, descomposición electroquímica y celda de combustible de óxido sólido integrada en un craqueador de amoniaco. Indicando que hace falta una investigación intensiva sobre la generación de hidrógeno partiendo de la descomposición de amoniaco, sin embargo, también indican que la descomposición electroquímica ofrece la posibilidad de producir hidrógeno de alta pureza en condiciones cercanas a las ambientales y con altas tasas de conversión, mostrándose como una alternativa a la descomposición térmica a altas temperaturas.
En la investigación [20], se muestra que, al integrar la remoción de productos electroquímicos con la descomposición térmica del amoniaco, es posible generar hidrógeno a una velocidad sustancialmente mayor que mediante descomposición térmica solamente. Los autores describen que la recuperación del hidrógeno almacenado en el amoniaco, se basa en la generación de medio mol de nitrógeno y 1.5 mol de hidrógeno, la cual, es ligeramente endotérmica y espontánea a partir de temperaturas de 183°C. No obstante, en el mismo trabajo se dice que como alternativa a la descomposición térmica a alta temperatura, la descomposición electroquímica del amoniaco tiene potencial para la producción de hidrógeno de alta pureza, en condiciones cercanas a las ambientales.
Con respecto a la electrólisis alcalina de amoniaco, [21] probaron la eficiencia del proceso, reportando que la temperatura elevada es esencial para la electro-oxidación del amoniaco y para la evolución del hidrógeno, además, los autores probaron que, con el incremento de la densidad de corriente operativa, la pureza del hidrógeno fue aceptable.
En la misma línea de investigación, [22], desarrollaron un análisis en donde se compara el desarrollo de la tecnología y el costo potencial de la descomposición de amoniaco basada en plasma y electrólisis. Sus resultados indican que la descomposición del hidrógeno basada en plasma debe lograr una mejora en la eficiencia energética, mientras que la técnica por electrólisis debe lograr una mayor durabilidad utilizando electrolitos baratos. Además de lo anterior, un estudio desarrollado por [23], describe el uso del amoniaco gas como portador de hidrógeno para su producción, utilizando para la síntesis, materiales mesoporosos preparados en el laboratorio, los autores utilizaron un tubo de acero inoxidable para uso con amoniaco anhidro corrosivo y el rango de temperatura de reacción estudiada fue de 350 a 650°C. Otro estudio desarrollado a temperaturas superiores a 350°C, es el reportado por [24], quienes evaluaron el uso de catalizadores de Ru soportados en nanofibras de alúmina, para la descomposición de amoniaco a fin de generar hidrógeno.
Con respecto al uso de catalizadores para la descomposición de amoniaco, [25] realizaron un estudio de la influencia de las morfologías de los catalizadores (mesoporosos de orden tridimensional, nanotubos y nanocubos) para conocer su relación con el rendimiento para la descomposición de amoniaco, los catalizadores estudiados fueron Co/CeO2-3DOM, Co/CeO2- NC y Co/CeO2-NT, siendo el primero quien aportó los mejores resultados. Aunado a lo anterior, [26] describieron de forma general distintos reactores de descomposición de amoniaco, entre los que destacan, microrreactores, reactores monolíticos, reactores de membrana y reactores electroquímicos. En la parte electroquímica, los autores reportan que la reacción general de la celda para la electrólisis del amoniaco es de 0.06V, lo que corresponde a un 95% menos de la energía para la electrólisis del agua, cuyo voltaje es de 1.223V.
Por otra parte, [27] evaluaron el uso de electrocatalizadores para la electrooxidación de amoniaco, que podrían utilizarse para la generación de hidrógeno de alta pureza y simultáneamente reducir el contenido de amoniaco en aguas residuales. Y [28] presenta una celda electrolítica de amoniaco, para la producción de hidrógeno utilizando un catalizador NiCu/C como catalizador anódico. Los resultados indicaron que el electrolizador puede operar en voltajes bajos para ahorrar energía en la producción de hidrógeno.
Cabe mencionar que de acuerdo con [6], en los últimos años se han realizado una gran cantidad de investigaciones que se relacionan con el amoniaco, mismos que lo colocan como un vector ideal de energía libre de carbono. Además, los autores indican que la síntesis y utilización del amoniaco empleando métodos electroquímicos, han demostrado estar por encima de otras técnicas.
2.2 El carbón como electrodo
[29] Evaluaron el uso de nanotubos de carbón como ánodo para la electrólisis de agua alcalina y lo compararon con un ánodo de grafito; los resultados indican que las propiedades morfológicas de los nanotubos reducen la barrera de energía para la disociación de OH- en oxígeno en el ánodo. Por otro lado, [30] desarrollaron experimentos de electrólisis de agua en un electrodo de tela de carbón utilizando un surfactante catiónico, estudiaron la influencia del surfactante en los dos procesos de electrólisis del agua, es decir en la reacción de hidrógeno y de oxígeno.
Cabe mencionar que según [7], el uso de biomasa para la producción de combustibles de bajas emisiones y fuentes de energía renovables, para producir hidrógeno o amoniaco, es importante debido a la necesidad de descarbonizar las industrias del transporte y generación de energía. Así mismo, [31] demostraron mediante su investigación que es posible producir hidrógeno directamente a partir de celulosa, utilizando un electrodo de carbón mesoporoso como cátodo, además de un ánodo de carbón parcialmente oxigenado. Sus condiciones experimentales incluyen una densidad de corriente de 0.29 A/cm2, obteniendo una eficiencia de corriente aproximada al 100% para la generación de hidrógeno.
2.3 El hidrógeno como agente reductor del hierro
El uso de hidrógeno en la industria siderúrgica, también ha sido de interés de los científicos, por ejemplo, [32] desarrollaron un cálculo de la energía de activación aparente del proceso de reducción de Fe2O3 con hidrógeno. Los autores realizaron una evaluación de la cinética de reducción de nanopolvos de Fe2O3 en una atmósfera de hidrógeno. La energía de activación para el proceso de reducción con hidrógeno de nanopolvos esféricos aglomerados, varía en el rango de 76 a 125kJ/mol. Así mismo, [33] investigaron la termodinámica y cinética de reducción de mineral de hierro con hidrógeno. Luego de su estudio, los autores concluyen que, considerando el efecto de añadir hidrógeno en la distribución de energía, la utilización del gas y la tasa de reducción, el contenido de hidrógeno en el alto horno debe controlarse en el rango de 5 a 10%.
Por otro lado, [34] desarrollaron un estudio en donde se examinó el potencial para la reducción de emisiones de CO2 de los procesos de alto horno empleando hidrógeno (generado mediante la electrólisis de agua) como agente reductor auxiliar, mediante simulación. Sus resultados mostraron que es posible disminuir las emisiones de CO2 utilizando hidrógeno.
3. Metodología
A continuación, se describen los materiales, equipos y procedimientos implementados en esta investigación.
3.1. Materiales y equipos
Equipo utilizado: En el desarrollo de esta investigación se utilizó una celda de acrílico con medidas de 15 cm x 15 cm x 15 cm, (dichas medidas fueron seleccionadas en base al volumen de muestra que se deseaba utilizar), 2 electrodos de grafito de 12.5 cm x 10 cm x 1.5 cm (los electrodos se obtuvieron del área de almacenamiento de electrodos desechados de acería), vaso de precipitado de 10 ml, 1 recipiente grande, probeta graduada de 100 ml, medidor portátil de pH marca HANNA, barras de silicón, abrazaderas, matraz aforado, tornillos de acero inoxidable, papeles filtro, embudos, mangueras, fuente de poder con un output de 0-30 V/0-10 A, bomba hidráulica sumergible de 18 W, balanza analítica, tubo de Venturi el cual fue elaborado con una manguera de – de pulgada, un adaptador de ½ de pulgada y un cople de – de pulgada.
Los reactivos que se utilizaron en las diferentes pruebas fueron: ácido sulfúrico (H2SO4) marca JALMEK (1N); hidróxido de sodio (NaOH) marca JALMEK de una concentración molar de 0.25 M; sulfato cúprico pentahidratado (CuSO₄·5H₂O) marca JALMEK con concentraciones molares de 0.05 y 0.025; sulfato de amonio ((NH4)2SO4) marca JALMEK para la preparación de soluciones sintéticas. Para esta investigación se trabajó con distintas muestras de licor amoniacal que provenían de plantas de producción de coque (coquizadora 1 y 2), cada muestra tomada contenía una concentración distinta en g/L de amoniaco, el cambio de la concentración es dependiente a la producción que esté teniendo la coquizadora, las muestras con las que se trabajó contenían 2.652 g/L de la coquizadora 1, y 0.884 y 1 g/L proveniente de la coquizadora 2.
3.2. Desarrollo de pruebas experimentales
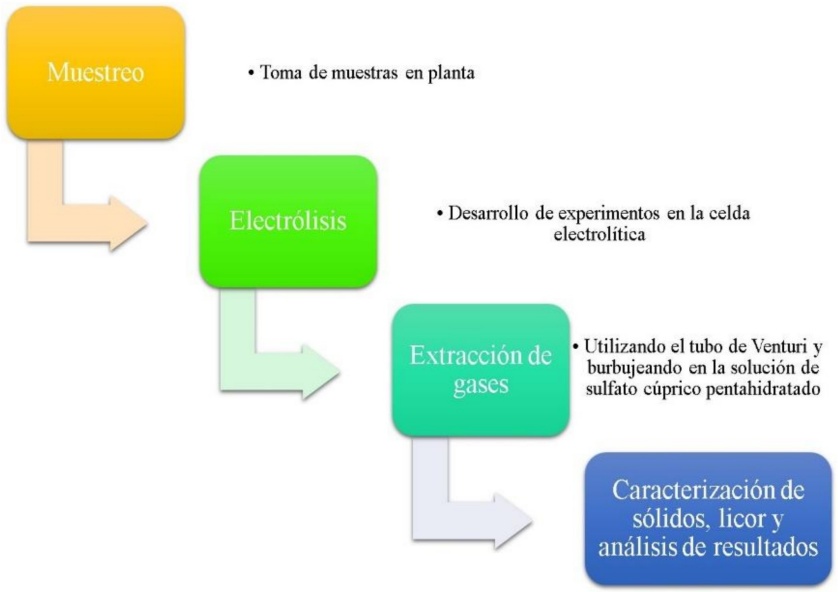
La Figura 1 muestra un diagrama de flujo, que incluye cada etapa del proceso experimental de este proyecto. En la Tabla 1 se presenta la información detallada con las variaciones de tiempo, densidad de corriente y concentración en gramos de amoniaco en el licor. Las electrólisis se realizaron debajo de una campana de extracción de gases, con una fuente de poder que alimenta a la celda, en cuanto al pH del sulfato cúprico pentahidratado y la solución de licor amoniacal se monitoreaban al comienzo y al final de la prueba. En el transcurso de la electrólisis se cerraba la válvula que conecta a la celda y al tubo de Venturi cada 5 minutos y posteriormente se abría otros 5 minutos esto para que se puedan concentrar los gases dentro de la celda y facilitara la extracción. Se trabajó con pruebas variando la densidad de corriente, para analizar el comportamiento y optimizar las condiciones de trabajo del sistema y la cantidad de gramos de hidrógeno obtenidos.
Tabla 1 Lista de pruebas con diferentes cambios de condiciones.
| Muestra | g/L de la muestra | Densidad (A/m2) | Tiempo (min) |
| Electrodo de grafito | |||
| Coquizadora “2” | 1 | 100 | 120 |
| Coquizadora “2” | 1 | 100 | 120 |
| Coquizadora “2” | 1 | 100 | 120 |
| Coquizadora “2” | 1 | 100 | 120 |
| Coquizadora “2” | 1 | 100 | 120 |
| Coquizadora “2” | 0.884 | 100 | 120 |
| Coquizadora “2” | 0.884 | 100 | 30 |
| Coquizadora “2” | 0.884 | 100 | 30 |
| Coquizadora “2” | 0.884 | 75 | 30 |
| Coquizadora “2” | 0.884 | 50 | 30 |
| Coquizadora “2” | 0.884 | 25 | 30 |
| Coquizadora “2” | 0.884 | 150 | 30 |
| Coquizadora “2” | 0.884 | 300 | 30 |
| Coquizadora “2” | 0.884 | 100 | 30 |
| Coquizadora “2” | 0.884 | 100 | 30 |
| Coquizadora “1” | 2.652 | 100 | 30 |
| Coquizadora “1” | 2.652 | 75 | 30 |
| Coquizadora “1” | 2.652 | 300 | 30 |
| Coquizadora “1” | 2.652 | 150 | 30 |
| Sintética | 20 | 100 | 30 |
| Sintética | 20 | 150 | 30 |
| Sintética | 20 | 300 | 30 |
| Sintética | 10 | 100 | 30 |
| Sintética | 10 | 150 | 30 |
| Sintética | 10 | 300 | 30 |
| Sintética | 5 | 100 | 30 |
| Sintética | 5 | 150 | 30 |
| Sintética | 5 | 300 | 30 |
| Electrodo de acero | |||
| Coquizadora | 2.652 | 100 | 30 |
| Coquizadora | 0.884 | 100 | 30 |
| Sintética | 20 | 100 | 30 |
| Sintética | 10 | 100 | 30 |
| Sintética | 5 | 100 | 30 |
3.3 Cuantificación de hidrógeno
Para cuantificar el hidrógeno, la celda estuvo conectada a un tubo de Venturi a fin de succionar los gases generados durante la electrólisis. A su vez, el tubo de Venturi estuvo sumergido en una solución de (CuSO₄·5H₂O) con una molaridad de 0.5. Las bases para intentar caracterizar al gas de esta manera, radican en que el hidrógeno es un reductor y al estar en contacto con el ion cúprico, éste se reduciría formando cobre metálico, de acuerdo a las ecuaciones 1 y 2.
Por estequiometria podrían cuantificarse los gramos de hidrógeno producidos. Todas las pruebas se realizaron bajo las mismas condiciones y el pH del licor amoniacal fue monitoreado antes y después de la realización de electrólisis. Se utilizó el sulfato cúprico para identificar al hidrógeno por su gran poder reductor, al momento en el que se terminaba la prueba la solución de sulfato cúprico pentahidratado (0.5 M) se filtró y posteriormente se le hacía un lavado al recipiente que contenía el sulfato cúprico pentahidratado, a la bomba y el tubo de Venturi esto para que no se perdiera nada del precipitadode Cu, antes y después de hacer el filtrado se pesaban los papeles filtros con el objetivo de poder conocer la cantidad de precipitado de cobre generado al final. Todos los resultados son en gramos y por estequiometria se pueden calcular los gramos de hidrógeno necesarios para precipitar el cobre obtenido. Para realizar la estequiometria se utilizaron las ecuaciones 1 y 2. Al precipitado obtenido se le realizó un estudio con el Microscopio Electrónico de Barrido (MEB) y Difracción de Rayos X (DRX) a fin de caracterizarlo.
3.4 Cuantificación de amoniaco
Las muestras iniciales, y soluciones tratadas, fueron analizadas para determinar la concentración de amoniaco antes y después del experimento, utilizando el método Kjeldahl. [35]. Este método es probablemente uno de los métodos más utilizados para la cuantificación de nitrógeno en compuestos orgánicos siendo una de sus principales aplicaciones la determinación de proteínas en alimentos. Este método consiste en dirigir el sulfato de amonio; posteriormente se agrega un exceso de base fuerte para liberar el amoniaco. Como existen muy pocas sustancias, aparte de las sales amoniaco, que generen compuestos básicos volátiles en las condiciones empleadas de análisis, el método resulta relativamente especifico. El amoniaco liberado se destila siendo recogido en un exceso medido de disolución de ácido y el exceso de este ácido se determina mediante una valoración con una disolución estandarizada de NaOH.
3.5 Caracterización de los sólidos precipitados
Para el análisis microestructural, se utilizó un Microscopio Electrónico de Barrido (MEB) marca JEOL, modelo JSM-6380LV. Para su observación, la muestra fue montada en cinta doble cara de cobre.
Para el análisis por difracción de rayos X (DRX) se utilizó un Difractómetro XPertPro marca Panalytical, realizando un barrido de la muestra de 0 a 110°, los rayos fueron emitidos mediante un tubo de cobalto, con una configuración 2 θ grados. Se empleó el software High Score Plus© para la identificación de fases.
3.6 Elaboración de diagramas termodinámicos
A fin de conocer las especies predominantes en el sistema estudiado, se elaboraron diagramas termodinámicos de Pourbaix utilizando el Software Medusa©. Estos diagramas se construyeron considerando los datos de equilibro contenidos en la base de datos Hydra del Software Medusa© suite [36].
4. Resultados y discusión
Esta parte se divide en cuatro secciones, la primera comprende el análisis para la determinación por estequiometria de hidrógeno generado; la segunda corresponde a los resultados de los experimentos realizados electroquímicamente; la tercera sección presenta el efecto del uso de electrodo de acero y por último, la cuarta al análisis de la disminución de amoniaco en las soluciones tratadas.
4.1 Determinación de hidrógeno mediante la reducción del sulfato cúprico
La Figura 2 muestra una fotografía del aparato experimental utilizado, de lado izquierdo se encuentra la celda electroquímica, mientras que, de lado derecho, se encuentra el recipiente que contiene sulfato cúprico. Es importante notar que la celda electroquímica está conectada a una bomba sumergida en la solución de sulfato cúprico. La conexión de dicha bomba se basa en el acomodo Venturi, que tiene como objetivo la succión de un fluido dentro de un sistema, por lo tanto, su aplicación en este aparato consiste en la succión del gas generado electroquímicamente dentro de la celda (H2). Esta instrumentación fue necesaria debido a la falta de equipamiento para el análisis de los gases generados, sin embargo, al burbujearse dentro del recipiente con un oxidante fuerte, el hidrógeno debería reducirlo. Este planteamiento resultó viable, ya que una vez succionado el gas y al estar en contacto con la solución de sulfato cúprico, se inició la formación de precipitados, que luego de caracterizar química y morfológicamente permitió plantear una ruta de reducción del cobre. La propuesta de reducción del cobre se describe en las ecuaciones 3 y 4, las cuales, permiten pensar que el hidrógeno generado reacciona con el sulfato formando un sulfuro de cobre, por otra parte, este sulfuro también reacciona con el hidrógeno, generando cobre en estado elemental.
Por lo tanto, para analizar la cantidad de hidrógeno que reacciona fue necesario implementar la Ley de Hess. De acuerdo con [37], al aplicar la Ley de Hess es necesario ordenar una serie de reacciones químicas, de tal forma que, cuando se sumen, se cancelen todas las especies excepto los reactivos y productos que aparecen en la reacción global. Por lo tanto, en este trabajo, se aplicó la Ley de Hess a las ecuaciones 3 y 4, haciendo posible obtener la ecuación general del proceso presentada en la ec. 1.
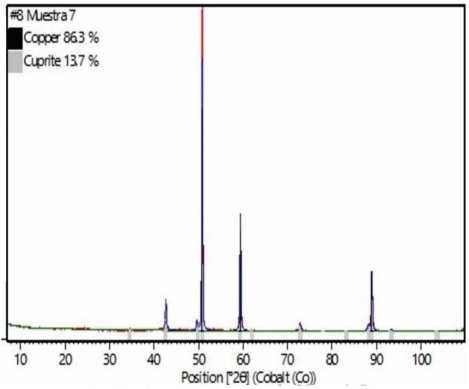
Una vez concluido el experimento, la solución de sulfato cúprico ahora reducido, fue filtrada. A fin de confirmar la teoría estequiométrica, se analizaron los precipitados generados mediante DRX. Los resultados obtenidos se muestran en la Figura 3, en donde es posible observar los resultados de DRX obtenidos, indica no solamente la presencia de cobre metálico, sino también cierto porcentaje de cuprita. Por lo tanto, fue necesario plantear, además, una ruta de oxidación del cobre generado; la generación de la cuprita puede justificarse debido a que el cobre está en presencia de aire y agua, por lo tanto, es factible su oxidación. Por lo que, para continuar con el análisis, se planteó la ec. 2, en donde se muestra que es posible oxidar al cobre generado. Los resultados de DRX indicaron que se obtenía en promedio un 84% de Cu y un 16% Cuprita (Cu2O) en el lavado del recipiente, el tubo de Venturi y la bomba. Y se obtuvo un 65.5% de Cu y un 34.5% de Cu2O directamente en el filtrado. Por lo tanto, considerando la información estequiométrica de las reacciones, y los pesos obtenidos experimentalmente, fue posible calcular los gramos de hidrógeno generados.
4.2 Evaluación del tiempo, densidad de corriente y concentración de las soluciones
En la Tabla 2, se muestran los resultados obtenidos experimentalmente de generación de hidrógeno a partir de las pruebas desarrolladas, variando la densidad de corriente tanto en muestras de licor amoniacal como en las soluciones sintéticas preparadas con diferentes concentraciones, todas estas pruebas fueron realizadas durante media hora de manera continua. Estos resultados fueron la base para la construcción de la gráfica mostrada en la Figura 4 Antes de continuar, debe aclararse que en el caso de la Coquizadora 2, se tomaron dos muestras, por lo que, debido al proceso, la primera muestra tenía una concentración de 1.1 g/L de amoniaco total, mientras que la segunda fue de 0.88 g/L.
Tabla 2 Lista de experimentos donde se muestra concentraciones iniciales de amoniaco, gramos obtenidos de hidrógeno y condiciones experimentales.
| Muestra | g/L de la muestra inicial | Densidad de corriente (A/m2) | Precipitadode Cu (g) | Hidrógeno generado (g) |
| Coquizadora “2” | 1 | 100 | 2.6447 | 2.4529 |
| Coquizadora “2” | 1 | 100 | 2.9634 | 0.8925 |
| Coquizadora “2” | 1 | 100 | 1.8192 | 1.6557 |
| Coquizadora “2” | 1 | 100 | 0.934 | 0.9023 |
| Coquizadora “2” | 1 | 100 | 2.106 | 1.9664 |
| Coquizadora “2” | 0.884 | 100 | 0.587 | 0.5758 |
| Coquizadora “2” | 0.884 | 100 | 0.53 | 0.5189 |
| Coquizadora “2” | 0.884 | 100 | 0.0977 | 0.0959 |
| Coquizadora “2” | 0.884 | 75 | 0.2991 | 0.2906 |
| Coquizadora “2” | 0.884 | 50 | 0.1703 | 0.1637 |
| Coquizadora “2” | 0.884 | 25 | 0.1951 | 0.1882 |
| Coquizadora “2” | 0.884 | 150 | 0.4433 | 0.425 |
| Coquizadora “2” | 0.884 | 300 | 0.5592 | 0.5336 |
| Coquizadora “2” | 0.884 | 100 | 0.3906 | 0.3746 |
| Coquizadora “2” | 0.884 | 100 | 0.14 | 0.1381 |
| Coquizadora “1” | 2.652 | 100 | 1.1803 | 1.13 |
| Coquizadora “1” | 2.652 | 75 | 0.965 | 0.9201 |
| Coquizadora “1” | 2.652 | 300 | 0.656 | 0.6066 |
| Coquizadora “1” | 2.652 | 150 | 0.3019 | 0.2866 |
| Sintética | 20 | 100 | 0.3411 | 0.3247 |
| Sintética | 20 | 150 | 0.361 | 0.343 |
| Sintética | 20 | 300 | 0.4348 | 0.4078 |
| Sintética | 10 | 100 | 0.3495 | 0.3275 |
| Sintética | 10 | 150 | 0.5228 | 0.5006 |
| Sintética | 10 | 300 | 0.4826 | 0.4635 |
| Sintética | 5 | 100 | 0.508 | 0.487 |
| Sintética | 5 | 150 | 0.5038 | 0.4811 |
| Sintética | 5 | 300 | 0.9389 | 0.914 |
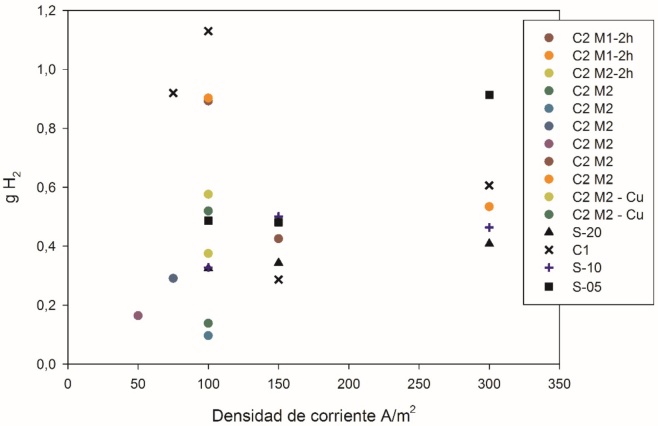
Figura 4 Resultados obtenidos en gramos de hidrógeno generados al variar la densidad de corriente para distintas muestras empleando electrodos de grafito.
Como puede observarse en la Figura 4, se utilizan puntos coloreados para las pruebas realizadas con la muestra de Coquizadora 2, mientras que las de planta 1 se presentan con equis negras. Para analizar dichos resultados, se considera importante iniciar con el análisis del tiempo: primero se realizaron pruebas con tiempo de 2 horas continuas y se realizó una comparativa realizando pruebas a media hora, debido a la mínima diferencia, se determinó que se continuaría trabajando durante media hora de manera continua. En cuanto a la concentración de sulfato cúprico, se realizó una evaluación de la posibilidad de reutilizar la solución, sin embargo, los resultados obtenidos fueron los más bajos (menos de 0.2 g de hidrógeno). Por lo tanto, se decidió que además de trabajar todas las pruebas media hora continua, también se estaría utilizando una solución fresca de sulfato cúprico 0.5 M.
Posteriormente, se trabajó con densidades de corriente diferentes y se observó que a medida que se incrementa la densidad de corriente también se tiene un aumento en la producción del hidrógeno generado, sin embargo, comparando la producción con las densidades de corriente de 150 y 300 A/m2 se determinó que no existe una diferencia muy grande, por lo que se decidió que, para disminuir el consumo energético, podría continuar la experimentación con densidad de corriente de 100 A/m2. Además, con esta densidad de corriente, fue posible obtener las mayores cantidades de hidrógeno generado,por ejemplo, con las muestras de la Coquizadora 1 se pude observar un incremento en la cantidad de hidrógeno generado llegando casi a 1.2 g de hidrógeno a media hora y una densidad de corriente de 100 A/m2, pero a medida en que se aumenta la corriente llega a un punto en el que se pasiva y no se obtiene un incremento considerable.
Además de lo anterior, se observó que la concentración de las soluciones podría influir en losresultados obtenidos, ya que las muestras de Coquizadora 1 y 2 tienen concentraciones de 2.66 y 0.88 g/L respectivamente. Por lo tanto, una vez que se tiene la comparativa de las 2 soluciones, se puede decir que hay una influencia en la concentración de amoniaco en la solución por lo que se decidió trabajar con soluciones sintéticas de diferentes concentraciones.
Las soluciones sintéticas analizadas tuvieron concentraciones de 5, 10 y 20 g/L, con identificación en la Figura 4 de cuadrado, cruz y triángulo respectivamente (S-05, S-10 y S-20). Los resultados indican que, a concentraciones más bajas, se tienen resultados mejores de gramos de hidrógeno obtenidos, esto puede observarse en todas las densidades estudiadas, pero tiene mayor evidencia cuando se trabajó a 300 A/m2.
4.3 Evaluación de electrodo de acero
Una vez definidas las mejores condiciones de trabajo, y la influencia de la concentración inicial de amoniaco en las soluciones, se analizó el sistema utilizando un electrodo de acero como ánodo para la generación de hidrógeno. En la Tabla 3 se muestran los resultados obtenidos experimentalmente al utilizar un electrodo de acero, dichos resultados se muestran gráficamente en la Figura 5, se realizó un análisis de las 5 soluciones utilizando una densidad de corriente de 100A/ m2 y media hora de trabajo.
Tabla 3 Resultados experimentales registrados al utilizar electrodos de acero.
| Muestra | g/L de lamuestra | Densidadde corriente (A/m2) | Precipitadode Cu (g) | Hidrógenogenerado (g) |
| Coquizadora 1 | 2.652 | 100 | 0.631 | 0.5965 |
| Coquizadora 2 | 0.884 | 100 | 0.6012 | 0.5727 |
| Sintética | 20 | 100 | 0.6558 | 0.6262 |
| Sintética | 10 | 100 | 0.6832 | 0.6522 |
| Sintética | 5 | 100 | 0.7193 | 0.6875 |
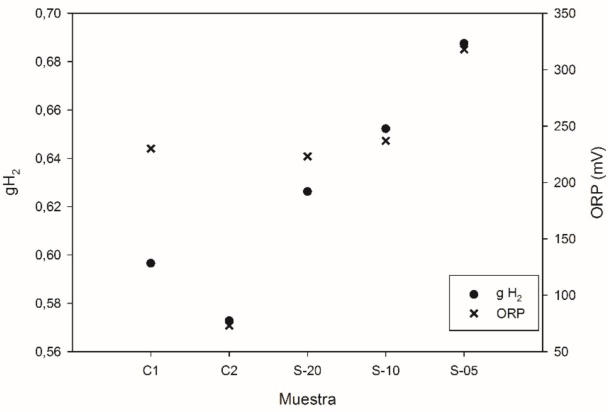
Figura 5 Resultados obtenidos en gramos de hidrógeno generados al variar la densidad de corriente para distintas muestras empleando electrodos de acero.
Los resultados indican que en el caso de la Coquizadora 1 fue posible obtener 0.6 g de hidrógeno mientras que para la Coquizadora 2 fue menos de 0.58 g, lo cual puede deberse a la diferencia en las características de cada muestra. En el caso de dichas soluciones de planta, a medida que el potencial de óxido reducción (ORP) se incrementa, se obtienen mejores resultados de generación de hidrógeno, el mayor efecto se observa con la concentración superior, que corresponde a la muestra de planta 1 con 2.66 g/L de amoniaco, los registros experimentales indican que se tuvo un ORP de 22 mV en esta muestra, mientras que cuando se tuvo una concentración de 0.88 g/L (C2) se reportó menos de 100 mV.
Por otra parte, en las soluciones sintéticas de 5, 10 y 20 g/L de amoniaco, se observa que a medida que se disminuye la concentración de la solución se aumenta la capacidad de obtención de hidrógeno, esto se puede relacionar directamente con el ORP de las soluciones ya que a medida que disminuye la concentración de amoniaco, este valora aumenta.
La explicación a esto radica en que esta muestra de planta está constituida por un mayor número de componentes (los cuales no se pueden mencionar debido a las condiciones de confidencialidad de la empresa). Por lo tanto, esto permite pensar que es posible tratar soluciones con mayores concentraciones de amoniaco de planta y generar hidrógeno en mayores concentraciones que las obtenidas a partir de las soluciones sintéticas.
4.4 Disminución en la concentración de amoniaco contenido en las soluciones tratadas
En la Tabla 4 se presentan los resultados de las soluciones analizadas empleando el método Kjeldahl. Tal como puede observarse, en la mayoría de los casos, se obtuvo una concentración de amoniaco menor al finalizar el experimento que la contenida inicialmente.Con esto, es posible confirmar que el amoniaco contenido en las soluciones pudo descomponerse para la generación de hidrógeno. Antes de continuar con el análisis de esta tabla, es importante aclarar que al final de esta sección, se presenta una explicación termodinámica que corresponde a las soluciones en donde, al finalizar el experimento, se tiene una concentración superior de NH3.
Tabla 4 Resultados de la determinación de amoniaco en soluciones tratadas.
| Muestra | Densidad de corriente (A/m2) | Tiempo (min) | g/L de NH3 inicial | g/L de NH3 final | Resta | g de H generado | g de hidrógeno por NH3 | g de H por H2O |
| Electrodo de grafito | ||||||||
| C 2 | 100 | 120 | 1 | 0.544 | 0.456 | 2.453 | 0.080 | 2.372 |
| C 2 | 100 | 120 | 1 | 0.748 | 0.252 | 0.893 | 0.044 | 0.848 |
| C 2 | 100 | 120 | 0.884 | 0.340 | 0.544 | 0.576 | 0.096 | 0.480 |
| C 2 | 100 | 30 | 0.884 | 0.544 | 0.340 | 0.519 | 0.060 | 0.459 |
| C 2 | 100 | 30 | 0.884 | 0.340 | 0.544 | 0.096 | 0.096 | 0.000 |
| C 2 | 150 | 30 | 0.884 | 0.340 | 0.544 | 0.425 | 0.096 | 0.329 |
| C 2 | 300 | 30 | 0.884 | 0.680 | 0.204 | 0.534 | 0.036 | 0.498 |
| C 2 | 100 | 30 | 0.884 | 0.340 | 0.544 | 0.375 | 0.096 | 0.279 |
| C 2 | 100 | 30 | 0.884 | 0.748 | 0.136 | 0.138 | 0.024 | 0.114 |
| C 1 | 100 | 30 | 2.66 | 1.428 | 1.232 | 1.130 | 0.217 | 0.913 |
| C 1 | 75 | 30 | 2.66 | 1.972 | 0.688 | 0.920 | 0.121 | 0.799 |
| Sintética | 100 | 30 | 20 | 3.740 | 16.260 | 0.325 | 2.868 | -2.544 |
| Sintética | 150 | 30 | 20 | 5.576 | 14.424 | 0.343 | 2.544 | -2.201 |
| Sintética | 300 | 30 | 20 | 3.060 | 16.940 | 0.408 | 2.988 | -2.580 |
| Sintética | 100 | 30 | 10 | 3.876 | 6.124 | 0.328 | 1.080 | -0.753 |
| Sintética | 150 | 30 | 10 | 3.400 | 6.600 | 0.501 | 1.164 | -0.664 |
| Sintética | 300 | 30 | 10 | 2.992 | 7.008 | 0.464 | 1.236 | -0.773 |
| Sintética | 300 | 30 | 5 | 2.856 | 2.144 | 0.914 | 0.378 | 0.536 |
| Electrodo de acero | ||||||||
| C 1 | 100 | 30 | 2.66 | 2.788 | -0.128 | 0.597 | -0.023 | 0.619 |
| C 2 | 100 | 30 | 0.884 | 1.768 | -0.884 | 0.573 | -0.156 | 0.729 |
| Sintética | 100 | 30 | 20 | 7.410 | 12.590 | 0.626 | 2.221 | -1.595 |
| Sintética | 100 | 30 | 10 | 8.160 | 1.840 | 0.652 | 0.325 | 0.328 |
| Sintética | 100 | 30 | 5 | 5.100 | -0.100 | 0.688 | -0.018 | 0.705 |
A partir de los datos mostrados en la Tabla 4, es posible determinar la cantidad en gramos de hidrógeno generados a partir del amoniaco, considerando que la molécula de amoniaco tiene un peso de 17 g/mol, el hidrógeno corresponde a 17.64%. Por lo tanto, si la cantidad de hidrógeno generado menos la cantidad de hidrógeno aportado por la molécula de amoniaco, y se multiplica por 0.1764 se obtiene la cantidad de hidrógeno generado a partir del amoniaco, y al restarlo a los gramos totales de hidrógeno, se obtiene la cantidad obtenida a partir del agua. Dichos datos, también se presentan en la misma tabla.
Para dar una explicación al incremento en la concentración de amoniaco al finalizar el experimento, se hace uso de la termodinámica. En todos los experimentos, se midieron tanto el potencial de hidrógeno (pH) como el potencial de oxidación-reducción (ORP). Lo cual, ha permitido plantear un fenómeno que explique el incremento en la concentración de amoniaco al finalizar el experimento. Para dicha explicación, se considera importante mencionar que el rango de pH en el cual se trabajó estuvo en el rango de 3 a 4.6; y de manera simultánea, se leyó el ORP, cuyos registros indican que se encuentran en un rango entre 0.48 a 0.85V vs SHE.
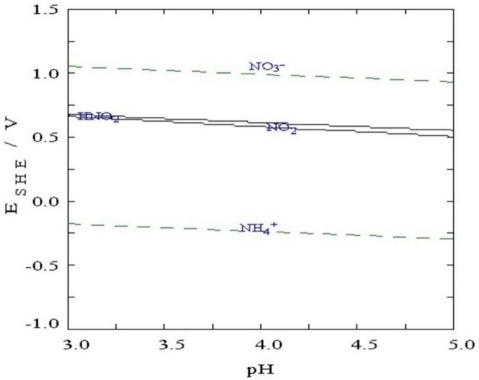
La Figura 6, muestra un diagrama termodinámico que correspondiente al sistema NH3-H2O a temperatura ambiente 0.1M NH3. La línea punteada de la Figura 6, delimita la zona de estabilidad del agua, es decir, bajo las condiciones en las que el agua no puede descomponerse, por encima de la línea punteada está la zona de oxidación, mientras que debajo de ella, está la zona de reducción. Estas líneas definen las condiciones en las cuales el agua no puede descomponerse, además, se muestra que, si se incrementa el potencial de trabajo, se generará oxígeno, debido a que el sistema tiene la capacidad de oxidar al agua, mientras que, si se reduce, debido a las condiciones de trabajo, se estaría generando hidrógeno. Cabe mencionar que debido a que los diagramas están elaborados bajo condiciones de estabilidad óptimas, al analizar los sistemas experimentales, existe cierta variación, no obstante, a medida que las reacciones se acercan a las líneas de equilibrio, tienen más posibilidades de llevarse a cabo.
Los registros experimentales, indican que todas las soluciones tratadas, se encuentran dentro de la zona de estabilidad del agua, esto no quiere decir, que no se pueda generar el hidrógeno, ya que se está aplicando un potencial directo a la celda, y eso obliga la descomposición de la molécula de agua, sin embargo, es más probable que el hidrógeno generado por debajo de la línea de estabilidad pueda continuar estando gaseoso y no combinarse con otros elementos para formar un nuevo compuesto. Esto precisamente, es lo que se piensa que sucede en las soluciones donde se incrementa la concentración de amoniaco, es decir, el hidrógeno producido, podría estarse combinando con el nitrógeno del aire solubilizado y producirse amoniaco en la solución.
La teoría de la generación de amoniaco, a partir del nitrógeno que está en el aire, se sustenta de acuerdo con la ec. 5, la cual, es espontánea a temperatura ambiente, con un valor de energía libre de Gibbs ∆G = -3.922 kCal/mol. Para su viabilidad, se considera que, en la celda completamente cerrada, se tenían 1.3 L de solución y 2.07 L de aire, del cual, el 78% es N2, lo que corresponde a 1.62 L de N2, considerando que 1mol de un gas equivale a 24.4 L, entonces se tendrían 0.06 moles de N2 disponibles para reaccionar con el hidrógeno formado. Por otra parte, si se considera que la solubilidad del N2 en agua es 6.8x10-4 mol/L, entonces existiría la posibilidad de disolver 1.1x10-3 moles de N2. En base a esto, se puede decir que, en el aire contenido en la celda, se tiene el suficiente nitrógeno como para que reaccione con el H2 que se está generando, para formar amoniaco.
5. Conclusiones
Se determinó que las mejores condiciones de trabajo con los electrodos de grafito, es de 100 A/m2, durante 0.5 h, brindando cantidades superiores a 1.1 gr de hidrógeno generados (cuantificados de manera indirecta), utilizando la muestra de Coquizadora 1. En cuanto a la evaluación de los electrodos de acero, al trabajar con soluciones sintéticas, a concentraciones más bajas, se tienen resultados mejores de gramos de hidrógeno, debido a la influencia de la concentración con el ORP de la solución (que se incrementa a medida que la concentración disminuye). Por otra parte, en las muestras de proceso de coquización, a medida que se incrementa la concentración de amoniaco, también aumenta el ORP de la solución, brindando los mejores resultados el hecho de tener una mayor cantidad de amoniaco en la solución. Este comportamiento se justifica al considerar que las soluciones de las plantas contienen un gran número de impurezas, mientras las soluciones sintéticas han sido creadas con reactivos grado analítico y agua bidestilada. Se explicaron los fenómenos involucrados termodinámicamente, justificando el incremento en el contenido de amoniaco, cuando se presentó un aumento en el contenido inicial de este compuesto. Todas las soluciones tratadas, fueron analizadas por el método Kjeldahl, en donde se confirmó la disminución de amoniaco en la mayoría de las soluciones, luego de ser tratadas electroquímicamente. Se determinó indirectamente la masa generada de hidrógeno, así mismo, se validó el uso de la estequiometria, ya que se hicieron cálculos para determinar la cantidad de hidrógeno generado durante el experimento, y, además, para calcular la cantidad obtenida a partir tanto del amonio como del agua. El alcance de esta investigación, corresponde al desarrollo experimental a escala laboratorio, ya que se tuvo la limitante en el análisis in situ de la masa de hidrógeno generado, no obstante, dicha determinación se realizó de manera indirecta mediante un análisis estequiométrico.
Una vez validado el desarrollo experimental a mayor escala, será posible aprovechar el licor amoniacal que se genera en las plantas coquizadoras, para generar hidrógeno, el cual puede ser aprovechado en la misma industria o proceso de producción como combustible ecológico. Para futuras investigaciones, se recomienda la evaluación de la celda electrolítica y las condiciones en una escala mayor, y posteriormente, a escala piloto, a fin de corroborar la aplicabilidad de los resultados.











 nueva página del texto (beta)
nueva página del texto (beta)