Introducción
El arándano azul (Vaccinium corymbosum) es una fruta con alto valor nutricional, bajo contenido calórico, elevado en antioxidantes y con propiedades antiinflamatorias; además de que puede ser consumido tanto en fresco o en sus formas procesadas (Banerjee et al. 2020). Dichos atributos lo convierten en un producto atractivo por su versatilidad y beneficios a la salud humana. Por estos motivos, se ha incrementado la popularidad y demanda de este en la última década; ocasionando así un aumento en la producción y superficie cultivada en diferentes regiones del mundo, incluyendo a México. En el 2022, en nuestro país se registró una producción total de 66,846 t que, al compararlas con las 7,190 t cultivadas en el año 2012, nos indican un aumento importante de casi 10 veces de la producción a nivel nacional en un periodo de 10 años (SIAP 2022).
Las enfermedades fúngicas se encuentran dentro de los principales factores causales de la reducción en la productividad de las plantas. Los géneros más recurrentes son aquellos que afectan el fruto y por lo general se encuentran en la etapa de postcosecha, tal es el caso de Botrytis, Monlinia y Colletorichum (Bell et al. 2021). Sin embargo, también se pueden presentar algunos géneros que afectan otros órganos como las hojas (Septoria y Gloeosporium), causando una reducción en la capacidad fotosintética de la planta y defoliación prematura; o también otros que perjudican las raíces como Phytophthora y Armillaria (Prodorutti et al. 2007). Para el caso específico del arándano, se han registrado pérdidas de hasta un 30% en la producción total debido a dichos fitopatógenos (Scherm y Krewer 2008).
El crecimiento acelerado del cultivo ha dado lugar a una deficiencia en la información disponible sobre los fitopatógenos que afectan su producción en México; sobre todo en la especificidad en la identificación morfológica y molecular a nivel de especie. Dentro de los tipos de bayas cultivadas en México, el arándano presenta el menor número de especies identificadas y reportadas, con un total de 15 especies de hongos fitopatógenos registrados, comparadas con las 45 especies para el cultivo de la fresa (Garay-Serrano et al. 2021). La generación de esta información es importante para poder planear un control eficaz y oportuno de las enfermedades, que se traducirá en un aumento productivo del cultivo y, por lo tanto, mayores ganancias económicas.
El objetivo del presente trabajo consiste en identificar a nivel de especie, de forma morfológica y molecular, los hongos asociados al cultivo del arándano en dos localidades del estado de Michoacán, México. Se hará especial énfasis en los hongos fitopatógenos y su relevancia agrícola, sin excluir a aquellos de vida libre o saprófitos.
Materiales y métodos
Colecta del material
La recolección de las muestras se llevó a cabo en las localidades de Uruapan y Ziricuaretiro en el estado de Michoacán, México. Los predios corresponden a unidades de producción agrícola dedicadas al cultivo de arándano. Se obtuvo una muestra compuesta, formada por varias plantas que presentaron síntomas de enfermedad (necrosis, amarillamiento o coloraciones anormales en las hojas y apariencia raquítica); de las cuales se tomaron muestras de toda la planta (fruto, inflorescencia, hojas, tallo y raíz). Estas fueron depositadas en bolsas de papel encerado para evitar su deshidratación, posteriormente fueron trasladadas al Laboratorio de Toxicología de la Universidad Autónoma Agraria Antonio Narro para su posterior análisis.
Procesamiento de las muestras
Las muestras se lavaron y se cortaron trozos de aproximadamente 1 cm2, para asegurar la uniformidad de las muestras y facilitar el manejo de estas. Posteriormente se desinfectaron por inmersión en una solución de hipoclorito de sodio al 3 % durante un minuto, enseguida se realizó un triple enjuague con agua destilada estéril y se dejaron secar a temperatura ambiente. Consecutivamente, las muestras de tejido se colocaron sobre medio PDA y V8, se incubaron a 25 °C por un periodo de 24 a 72 h. Pasado el tiempo, se verificaron las cajas para confirmar el crecimiento y se realizaron las resiembras pertinentes. Finalmente, se obtuvieron cepas puras por medio de la técnica de punta de hifa.
Identificación y descripción morfológica
La identificación morfológica se llevó a cabo a través de la visualización directa de las estructuras fúngicas. Para ello se incubaron las cepas puras por cuatro semanas para asegurar la presencia de conidios u otras estructuras que facilitaran la identificación. Para su observación al microscopio compuesto se realizaron montajes de micelio sobre portaobjetos teñidos con lactofenol azul de algodón. Para la identificación morfológica inicial a género se emplearon las claves taxonómicas de Barnet y Hunter (1998), posteriormente se emplearon claves y artículos específicos para la identificación a nivel de especie Wang et al. 2017, (Maharachchikumbura et al. 2014, Zhou et al. 2022, Harman y Kubieck 2002, Christensen 1982). La corroboración de la nomenclatura de las especies se realizó en la página Index Fungorum.
Identificación molecular
La extracción de ADN de las cepas purificadas se realizó siguiendo la metodología modificada de Doyle y Doyle (1987). Se tomó micelio con ayuda de un bisturí y se maceró en un mortero con 800 μL de buffer de extracción (Tris-HCL, pH 8.0 - 100mM; EDTA pH 8.5 - 50 mM; NaCl 50 mM y SDS 2 %), se agitó por 30 segundos en el vórtex para asegurar la uniformidad de la muestra. Posteriormente se agregaron 700 μL de cloroformo/alcohol isoamílico (24:1) y se agitó por otros 30 segundos en el vórtex. Se centrifugaron las muestras durante 15 minutos a 12,000 rpm. Se extrajo la fase acuosa y se colocó en un tubo nuevo al que también se le adicionó un volumen equivalente de isopropanol (aproximadamente 500 μL). Dicho tubo se dejó en refrigeración por 15 minutos para después centrifugarlo durante 10 minutos a 12,000 rpm. Terminada la centrifugación se desechó el sobrenadante, la pastilla de ADN se dejó secar a temperatura ambiente sobre papel secante.
Para las amplificaciones por PCR se utilizaron los iniciadores ITS1 (5´-TCCGTAGGTGAACCTGCGG-3´) e ITS4 (5´-TCCTCCGCTTATTGATATGC-3´). Las condiciones de la reacción para la PCR fueron de 1 ciclo de desnaturalización inicial a 94 °C por 5 min., seguido a este fueron 30 ciclos de desnaturalización a 95 °C por 10 segundos, posteriormente se llevaron a cabo 30 ciclos para el alineamiento de los primers a 57 °C por 30 segundos, seguido por 30 ciclos de extensión a 72 °C por 2 minutos y por último un ciclo de extensión final a 72 °C por 5 minutos. La amplificación se visualizó en un gel de agarosa al 1 % mediante electroforesis. Las secuencias de las amplificaciones fueron cotejadas con ayuda de la herramienta BLAST de la base de datos del NCBI para su identificación pertinente. Después de haber confirmado su identidad, las secuencias obtenidas fueron depositadas en el GenBank del NCBI con los números de acceso presentes en la Tabla 1.
Tabla 1 Especies fúngicas descritas en el presente trabajo
| Número de Acceso NCBI | Especie (% similaridad Blast ID) | Parte de la planta | Primer reporte en Vaccinium corymbosum en México |
|---|---|---|---|
| OR652627 | Aspergillus sclerotiorum (100 %) | Hoja y fruto | Sí |
| OR652628 | Trichoderma longibrachiatum (99 %) | Raíz | Sí |
| OR652629 | Stagonosporopsis cucurbitacearum (99 %) | Hoja | Sí |
| OR652630 | Fusarium oxysporum (100 %) | Raíz | Sí |
| OR652631 | Nigrospora sphaerica (100 %) | Hoja | Sí |
| OR652632 | Neopestalotiopsis rosae (100 %) | Tallo | Sí |
| OR652633 | Pestalotiopsis oxyanthi (100 %) | Inflorescencia | Sí |
Resultados y Discusión
Aspergillus sclerotiorum G.A. Huber, Phytopathology 23: 306 (1933)
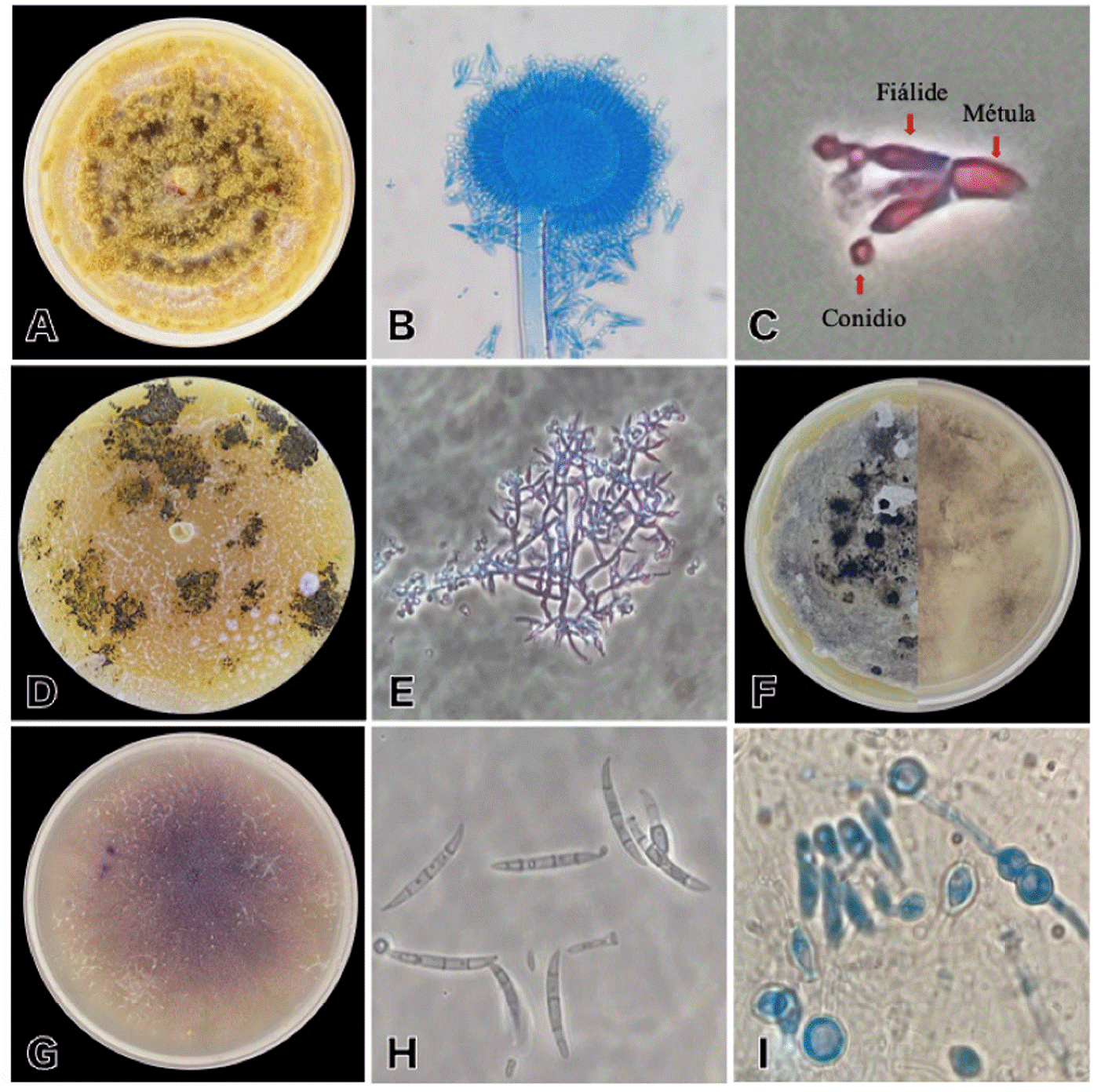
Figura 1 A: Aspergillus sclerotiorum en PDA, acumulación de conidióforos sobre el micelio con apariencia pulverulenta claramente visible. B: cabeza aspergilar biseriada de A. sclerotiorum. C: elementos de una cabeza aspergilar biseriada: métula, fíalide y conidio de A. sclerotiorum. D: Trichoderma longibrachiatum en PDA con manchas de conidióforos color verde oscuro. E: Conidióforos de T. longibrachiatum. F: frente y envés del crecimiento en PDA de Stagonosporopsis cucurbitacearum. G: Fusarium oxysporum en PDA. H: macroconidios de F. oxysporum. I: microconidios y clamidosporas de F. oxysporum.
Crecimiento en PDA con micelio blanco-crema en un inicio, posteriormente el micelio presentó pequeños abultamientos que tomaron una apariencia pulverulenta, con el tiempo el color del micelio cambió a amarillo brillante (Figura 1A); esta característica se debe a la acumulación de conidióforos y conidios sobre el micelio. Conidióforos erguidos, simples, no septados, color amarillo pálido, largos, terminados en un engrosamiento globoso conocido como vesícula aspergilar cuyas dimensiones promedio son de 36.48 x 37.37 μm (n=20); la cabeza aspergilar con dimensiones promedio de 70.03 x 67.46 μm (n=20) (Figura 1B), es bi-seriada, por lo que presenta métulas sobre la cuales se sitúan los esterigmas o fiálides (Figura 1C), las métulas se encuentran radiando de la vesícula o están distribuidas por toda su superficie. Los conidios son unicelulares, globosos a sublgobosos, no elongados, con coloraciones amarillas translúcidas, son lisos a finamente rugosos, se pueden encontrar solitarios o en cadena, se sitúan sobre las fiálides.
Material estudiado: México, Michoacán, municipio de Uruapan, septiembre 22, 2022.
Comentarios: Aislada de hojas y frutos. La morfología concuerda con la reportada en la literatura (Bioresource Collection and Research Center 2023, Christensen 1982). Aspergillus sclerotiorum se encuentra naturalmente en una gran variedad de ecosistemas agrícolas. En sí, la presencia del hongo no representa un peligro para los cultivos, ya que no hay evidencias directas de su fitopatógenicidad; sin embargo, sigue siendo un hongo de interés agropecuario debido a su capacidad productora de micotoxinas y su potencial como agente de control biológico.
En el presente trabajo se reporta por primera vez la presencia de A. sclerotiorum en un cultivo agrícola en México, de forma específica el arándano. Dicho hongo ya ha sido reportado en otras frutas como albaricoque, ciruela, melocotón, uvas, dátiles, higo, manzanas y peras (Aziz y Moussa 2002); el único registro para otras bayas fue hecho por los mismos autores y se trata del cultivo de la fresa. El común denominador de los frutos afectados por A. sclerotiorum es que la mayoría son pertenecientes a la familia Rosaceae, a partir de esto nace la incógnita y posible tópico para futuras investigaciones, que esclarezcan la posibilidad de alguna preferencia del hongo hacia cultivos pertenecientes a dicha familia. La presencia de A. sclerotiorum en frutos de importancia comercial es relevante, debido a su capacidad productora de micotoxinas como ocratoxina A/B, ácido penicílico, xantomegnina, viomelleina y vioxantina (Visagie et al. 2014, Bayman et al. 2002). La contaminación de productos agrícolas con micotoxinas es una seria amenaza para la salud humana debido a que su ingesta resulta en toxicidad aguda y crónica para el ser humano, las micotoxinas pueden poseer propiedades cancerígenas, mutagénicas, teratogénicas y causar hepatotoxicidad, nefrotoxicidad, neurotoxicidad, inmunotoxicidad y dermatotoxicidad (Drusch y Aumann 2005). Debido al riesgo que representan las micotoxinas para la salud humana, entidades como la Organización Mundial de la Salud (OMS) y la Organización de las Naciones Unidas para la Alimentación y Agricultura (FAO) han establecido lineamientos que regulan la presencia y distribución de alimentos con micotoxinas (Navale et al. 2021). Este primer reporte en México representa un posible reto a futuro para los agricultores y comerciantes mexicanos, que tendrán que asegurar la inocuidad alimentaria y cumplir con las regulaciones en lo que concierne a las micotoxinas, para poder comercializar los productos agrícolas en mercados internacionales.
Contrario a los efectos negativos que tiene los metabolitos secundarios de A. sclerotiorum para el ser humano, se han reportado efectos benéficos de dichos metabolitos para la agricultura, como agentes de control biológico. El metabolito mencionado anteriormente, ácido penicílico, fue aislado de A. sclerotiorum y probó tener una alta actividad antifúngica in vitro contra Phytophthora spp. (Kang y Kim 2004). Así mismo, Hadj-Taieb et al. (2019, 2020) reportan antagonismo fúngico de A. sclerotiorum hacia por lo menos 8 especies de hongos fitopatógenos presentes en el cultivo del pistachio. También se ha demostrado su actividad antibacteriana hacia Xanthomonas oryzae pv. oryzae (Jiang et al. 2019); y su actividad entomopatógena ha resultado efectiva contra termitas y mosquitos (Hansen et al. 2016).
Trichoderma longibrachiatum Rifai, Mycol. Pap. 116: 42 (1969)
Conidióforos hialinos, muy ramificados, verticilados; fiálides solitarias o en grupos, son elongadas y lageniformes a casi cilíndricas midiendo en promedio 2.11 x 6.32 μm (n=20) (Figura 1E); afanofiálides o fiálides intercalares presentes en la especie. Conidios (fialosporas) hialinas, unicelulares, redondas a ovoides, que nacen terminalmente en pequeños racimos o individualmente, tamaño promedio de 2.78 x 2.89 μm (n=20). En medio de cultivo PDA T. longibrachiatum presentó pigmentaciones llamativas color amarillo brillante, dichas coloraciones fueron evidentes tanto en el micelio como en el medio de cultivo; posteriormente se hicieron presentes machas color verde (formados por conjuntos de conidios) sobre el mismo (Figura 1D).
Material estudiado: México, Michoacán, municipio de Uruapan, septiembre 22, 2022.
Comentarios: Aislada de la raíz. La morfología observada concuerda con la descrita previamente en la literatura (Harman y Kubieck 2002). Trichoderma longibrachiatum es un hongo saprófito, cosmopolita y de vida libre (Kubicek-Pranz 1998). Ya ha sido reportado en varios cultivos del país como el cacao, maíz y chile; dichos reportes provienen de estudios diversos sobre su papel como antagonista o como promotor vegetal (Allende-Molar et al. 2022). El presente trabajo es el primero que registra la presencia de T. longibrachiatum en el arándano en México; otros estudios similares al presente han sido realizados sobre la comunidad de la rizosfera del arándano en Portugal (Gomes et al. 2023).
Existen varios motivos que pueden dar explicación a la presencia de T. longibrachiatum en las muestras de arándano del presente trabajo, la mayoría de ellas están relacionadas a las diferentes funciones del hongo dentro del agroecosistema. La especie se encuentra frecuentemente en los sustratos agrícolas como descomponedor de materia orgánica debido su capacidad de producir enzimas hidrolizadoras de celulosa (Xie et al. 2014), también es posible encontrarlo como endófito, dentro de las plantas sin ocasionar daño alguno (Samuels 2012). Otra función común de T. longibrachiatum es como agente de control biológico (Sharma y Gothalwal 2017, Poveda 2021), inhibiendo la actividad de otras especies mediante un conjunto de acciones como puede ser antagonismo, parasitismo directo, producción de metabolitos secundarios, entre otros; se ha probado efectivo contra hongos fitopatógenos (Oliveira et al. 2022, Camacho-Luna et al. 2022, Zhang et al. 2018), bacterias (Caracciolo et al. 2023) e incluso se ha reportado su potencial como entomopatógeno (Anwar et al. 2023, Ghosh y Pal 2016, Cisneros-Vázquez et al. 2023). Su presencia en el agroecosistema puede resultar en un beneficio directo para la planta, ya que es un conocido promotor del crecimiento vegetal; mejora los caracteres agronómicos y aumenta la productividad del cultivo (Ruiz-Cisneros et al. 2018, Subramaniam et al. 2022); así mismo, el hongo puede inducir la resistencia sistémica de las plantas ya que durante el proceso de infección se activa la producción de diferentes genes codificadores de proteínas que regulan los procesos y rutas de defensa/estrés de la planta, como lo son la producción de ácido jasmónico, etileno y ácido salicílico (Yuan et al. 2019) o la tolerancia a la sequía (Khoshmanzar et al. 2020). Es posible que T. longibrachiatum estuviera realizando una o varias de las funciones que se mencionaron con anterioridad en los arándanos muestreados.
Stagonosporopsis cucurbitacearum (Fr.) Aveskamp, Gruyter & Verkley, in Aveskamp, Gruyter, Woudenberg, Verkley & Crous, Stud. Mycol. 65: 45 (2010)
El crecimiento de la cepa en PDA presentó una coloración blanquecina del micelio durante los primeros días posteriores a la purificación; al paso del tiempo, el micelio comenzó a tornarse gris oscuro y aparecieron algunas protuberancias y manchas con coloraciones verde oscuro/café; dichas manchas corresponden a cúmulos de conidios (picnidios) sobre el micelio (Figura 1F). De acuerdo con Zhou et al. (2022), se pueden presentar conidios ovales y hialinos con medidas de 4.6-8.7 × 1.2-2.4 µm. Las clamidosporas por lo general son unicelulares, esféricas o ligeramente elípticas con 6.3-15 × 6-11 µm de tamaño, pueden presentarse de forma solitaria o formando cadenas de 4 a 13 unidades.
Material estudiado: México, Michoacán, municipio de Uruapan, septiembre 22, 2022.
Comentarios: Aislada de las hojas. Las observaciones morfológicas y las características del crecimiento en medio de cultivo concuerdan con la descripción de Stagonosporopsis cucurbitacearum (Li et al. 2015, Moumni et al. 2020, Keinath 2013). Stagonosporopsis cucurbitacearum (sin. Didymella bryoniae) es un hongo fitopatógeno que se encuentra afectando principalmente a cucurbitáceas (melón, sandía, calabaza, pepino y luffa) a nivel mundial y se ha reportado prácticamente en todos los continentes (Nuangmek et al. 2018). Puede afectar todos los órganos de las cucurbitáceas, incluyendo tallos, hojas, raíces, semillas y fruto. El patógeno ocasiona la enfermedad conocida como tizón gomoso del tallo (hojas, tallo) o pudrición negra (cuando afecta el fruto); puede encontrarse también en el suelo y en semillas, donde permanecen por largos periodos de tiempo, estas últimas suelen ser una fuente importante de inóculo ya que permite la movilización geográfica del patógeno (Moumni et al. 2019).
En un principio se pensaba que S. cucurbitacearum solo afectaba a miembros de la familia Cucurbitaceae, sin embargo, en años recientes se han hecho reportes que contradicen lo anterior. Entre los nuevos hospederos se encuentran desde plantas herbáceas con usos medicinales en países asiáticos como lo es Ipomoea aquatica (Liu et al. 2017) y Pinellia ternata (Zhou et al. 2022), hasta plantas extensamente comercializadas como el tabaco (Nicotiana tabacum) (Wang et al. 2018); todas las especies anteriores pertenecen a familias taxonómicas diferentes, lo que indica una ampliación en el número y diversidad de hospederos del hongo.
En México el patógeno S. cucurbitacearum, en forma de su sinónimo Didymella bryoniae, ya había sido reportado en el cultivo del chayote (Romero-Velazquez et al. 2015). En el presente trabajo es la primera vez que se hace el registro de S. cucurbitacearum en el cultivo del arándano tanto a nivel nacional como mundial. A pesar de esto, se desconoce si su presencia causa patogénesis alguna en el hospedero, esto da lugar a la posible realización de investigaciones futuras que respondan el planteamiento anterior.
Fusarium oxysporum Schltdl., Fl. berol. (Berlin) 2: 139 (1824)
Micelio aéreo abundante de color blanco en un inicio y tornándose violeta más tarde; la pigmentación del medio es morado o violeta (Figura 1G). Formación de esporodoquios de diferentes formas y tamaños (crecimiento en medio V8), desde globoso a subgloboso, con coloración amarillo oscuro a café pálido o violeta oscuro a casi negro. La esporulación comienza rápido, formando microconidios que no se agrupan en cadenas, tienen de una a dos células, ovaladas a elipsoides (Figura 1I), presentes en el micelio aéreo con una dimensión promedio de 2.41 x 7.51 μm (n=20); los macroconidios se pueden encontrar solitarias y agrupadas en erupciones (i.e. esporodoquios), son moderadamente curveadas, con reducciones en ambos extremos, en algunas ocasiones la célula apical es puntiaguda o en forma de gancho, por lo general tiene de 3 a 5 septos (Figura 1H), con dimensiones promedio de 5.05 x 33.94 μm (n=20); clamidosporas presentes, globosas a subglobosas o alargadas, tanto en micelio aéreo, superficial o sumergido, pueden ser intercalares o terminales, y pueden presentarse de forma solitaria midiendo en promedio 7.19 x 7.44 μm (n=20), en pares o cadenas (Figura 1I).
Material estudiado: México, Michoacán, municipio de Uruapan, septiembre 22, 2022.
Comentarios: Aislada de la raíz. La presente descripción morfológica de Fusarium oxysporum concuerda con la caracterización reportada en la literatura (Leslie y Summerell 2008, Gerlach et al. 1982). Fusarium oxysporum es un hongo fitopatógeno asociado al suelo de los cultivos, puede estar presente en una amplia variedad de hospederos como hortalizas, flores de ornato, maleza, árboles frutales, entre otros (Kant et al. 2011). Dicho patógeno ocasiona la enfermedad conocida como marchitez vascular; debido a su origen en el suelo, el patógeno infecta en un inicio las raíces de las plantas y posteriormente se disemina por el haz vascular, en donde la presencia del micelio ocasiona el bloqueo del mismo; esto último resulta en la imposibilidad de la planta para translocar nutrientes, a consecuencia de esto, comenzarán los síntomas de clorosis, coloraciones rojizas por deficiencia de nutrientes, necrosis marginal, defoliación y el típico marchitamiento ocasionado por la enfermedad (Joshi 2018). El presente patógeno fue aislado de la raíz, la localización del hongo concuerda con la epidemiología y el proceso infeccioso descrito anteriormente; así mismo, la sintomatología presente en la planta de quemadura marginal foliar y coloraciones rojizas debido a la ineficiencia en la toma de nutrientes, concuerdan con la ocasionada por el patógeno. Retomando lo discutido para T. longibrachiatum, la coexistencia de ambos hongos en la rizosfera del arándano en el presente estudio, indican una posible relación antagónica de ambos hongos, en el que T. longibrachiatum ejerce cierto grado de control biológico sobre F. oxysporum y promueve el crecimiento vegetal, como se ha reportado en la literatura (Liu et al. 2023, Sobowale et al. 2022). La presencia de F. oxysporum como fitopatógeno ha sido reportado previamente en el cultivo del arándano en China (Liu et al. 2014) y Chile (Moya-Elizondo et al. 2019); también se ha reportado en Argentina (Pescie et al. 2021), como endófito y sin comprobar su patogencidad. En México, F. oxysporum se ha asociado a otras berries como la zarzamora, fresa y mora (Garay-Serrano et al. 2021); sin embargo, este es el primer reporte que se hace del F. oxysporum afectando al cultivo del arándano en México.
Nigrospora sphaerica (Sacc.) E.W. Mason, Trans. Br. mycol. Soc. 12(2-3): 158 (1927)
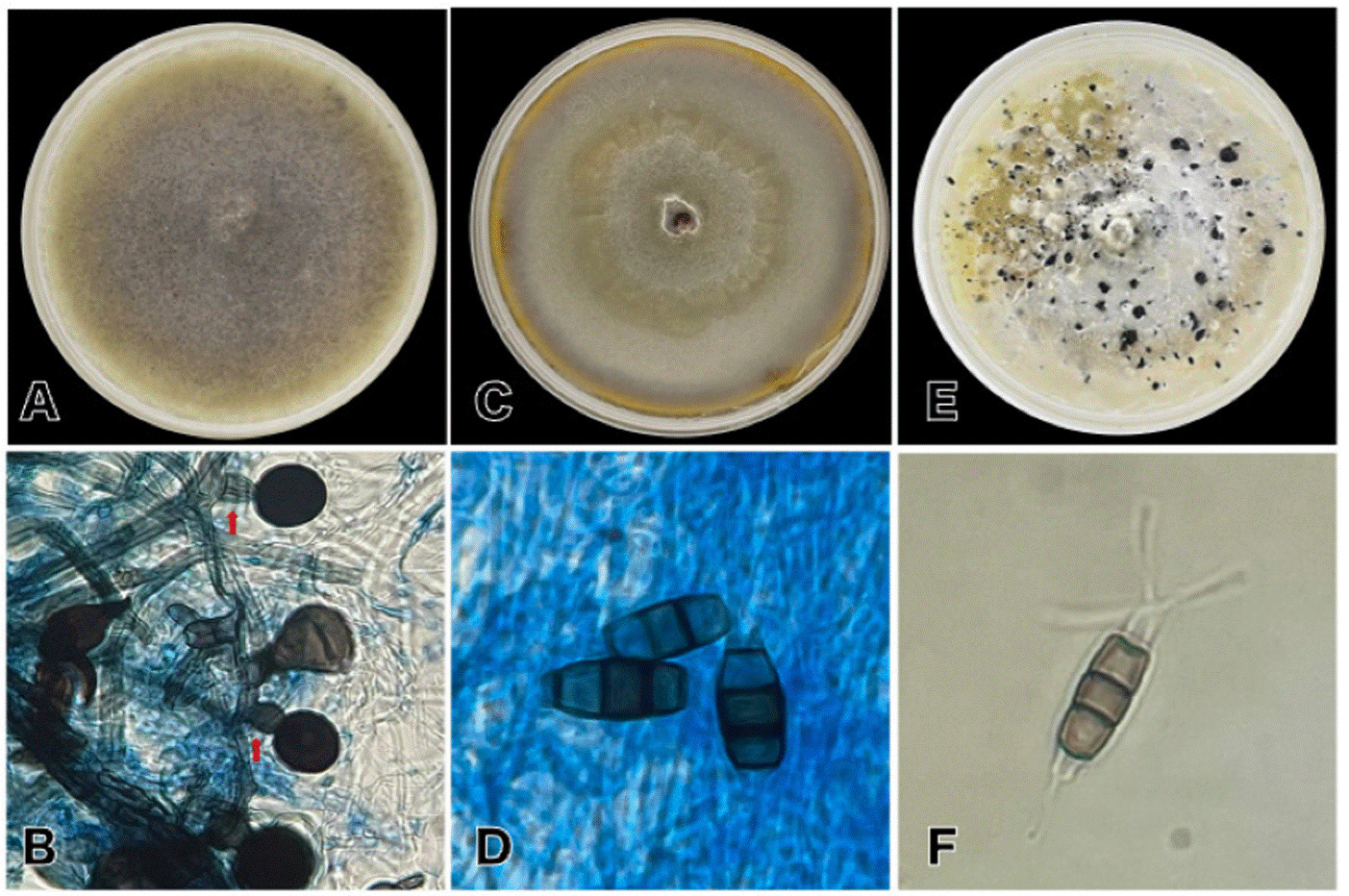
Figura 2 A: Nigrospora sphaerica, crecimiento en PDA. B: conidios y células conidiogénicas (señalada con flechas rojas) de N. sphaerica. C: crecimiento en PDA de Neopestalotiopsis rosae. D: conidios de N. rosae. E: Pestalotiopsis oxyanthi en PDA, acérvulos visibles con apariencia gomosa y color negro brillante. F: conidio de P. oxyanthi, célula basal con un apéndice hialino corto, la célula apical con varios apéndices simples.
Crecimiento del micelio en PDA presentó una coloración blanca en un inicio, posteriormente se presentaron coloraciones cafés sobre el micelio antes blanco (Figura 2A), esto debido a la presencia de conidios en el mismo. Hifas hialinas o café claro, septadas. Conidióforos cortos, rectos o ligeramente curvos, hialinos o con coloraciones café claro, en su mayoría son simples, en el ápice de estos se encuentra una célula conidiogénica hialina o de color café claro (Figura 2B), de forma cilíndrica a subglobosa, con dimensiones promedio de 10.48 x 10.81 μm (n=20), sobre estas se sostienen los conidios (i.e. aleuriosporas) color negro a café oscuro, brillantes, unicelulares, globosas midiendo en promedio de 22.80 x 22.89 μm (n=20).
Material estudiado: México, Michoacán, municipio de Uruapan, septiembre 22, 2022.
Comentarios: Aislada de las hojas. Las características morfológicas coincidieron con la descripción de Nigrospora sphaerica reportada en literatura previa (Zheng et al. 2021). Se ha reportado a Nigrospora oryzae como sinónimo de N. sphaerica (Index Fungorum 2016, Palacio-Bielsa 2010). Sin embargo, en el presente trabajo se discutirá sobre N. sphaerica de forma independiente a N. oryzae, la decisión se tomó con base en los estudios morfológicos y moleculares que afirman lo anterior (Wang et al. 2017, Hao et al. 2020, Abass y Mohammed 2014). Nigrospora sphaerica es un conocido fitopatógeno que afecta una amplia variedad de cultivos de importancia agrícola como el mango (Youssef et al. 2022), cacao (Villanueva et al. 2023), pitahaya (Wang et al. 2022) e incluso a plantas de flor de corte como el crisantemo (Luo et al. 2022); también ha sido reportado, en una sola ocasión, como fitopatógeno en el cultivo del arándano en Argentina (Wright et al. 2008). El hongo afecta comúnmente las partes aéreas de las plantas como las hojas y ramas; las sintomatologías más frecuentes suelen ser la mancha foliar y tizón de las hojas/ ramas. A pesar de la extensa literatura que lo sitúa como fitopatógeno, también se ha reportado como endófito, sin ocasionar daño alguno a las plantas e incluso se reporta su actividad como promotor de crecimiento vegetal mitigando el estrés abiótico de las plantas (Sodhi y Saxena 2023) y como agente de control biológico contra hongos fitopatógenos de raíces (Mmbaga et al. 2018). En México, la presencia de N. sphaerica ha sido reportada únicamente para el cultivo de arroz (Sandoval-Martínez 2022). En el presente estudio se reporta por primera vez a N. sphaerica en el cultivo del arándano en México y el segundo reporte para el arándano a nivel mundial. Queda abierta la posibilidad de futuros estudios para determinar su fitopatogenicidad en el cultivo del arándano en México.
Neopestalotiopsis rosae Maharachch., K.D. Hyde & Crous, in Maharachchikumbura, Hyde, Groenewald, Xu & Crous, Stud. Mycol. 79: 147 (2014)
En un inicio se presentó una coloración blanca del micelio en PDA, posteriormente se comenzaron a percibir tonalidades cafés sobre el mismo, iniciando de forma concéntrica hasta tomar esa apariencia uniformemente, esta coloración se debe a la presencia de conidios (Figura 2C). Los conidióforos son indistintos, reducidos a la presencia de células conidiógenas. Conidios fusoides, elipsoides, rectos a ligeramente curvados, presentando en su mayoría cinco células: una basal, una apical y tres medias, longitud promedio del conidio de 7.31 x 16.77 μm (n=20) (Figura 2D); presenta cuatro septos visiblemente más oscuras que las células medianas; célula basal cónica con base truncada, hialina o con leves coloraciones café translúcido, de paredes finas, en este a menudo se observa un apéndice corto hialino; seguida a esta se encuentran tres células medianas doliformes, café versicolor, la segunda célula desde la base suele ser marrón pálido, de longitud; tercera célula café oscuro, suele ser la más notoria de las cinco; cuarta célula café miel; célula apical, hialina, cilíndrica, de paredes finas y lisas; con 3-5 apéndices apicales tubulares, que no nacen de la cresta apical, sino que cada uno se inserta en un lugar distinto de la mitad superior de la célula.
Material estudiado: México, Michoacán, municipio de Uruapan, septiembre 22, 2022.
Comentarios: Aislada del tallo. La descripción de Neopestalotiopsis rosae concuerda con los registros morfológicos en la literatura (Maharachchikumbura et al. 2014, Essa et al. 2018). Se trata de un hongo fitopatógeno, descrito por primera vez en individuos del género Rosa spp. (Nueva Zelanda) y en Paeonia suffruticosa (USA) (Maharachchikumbura et al. 2014). A pesar de que los primeros reportes del fitopatógeno lo asociaran principalemente con plantas de flor de corte, en la actualidad su asociación más relevante es con el cultivo de la fresa, esto debido a que es principal agente causal de varias enfermedades de importancia económica de dicho cultivo como la pudrición de corona y raíz (Sun et al. 2021, Essa et al. 2018), así como el tizón y mancha foliar, de tallo y de fruto (Wu et al. 2021). También se ha reportado la presencia de dicho patógeno en diferentes cultivos como aguacate (Fiorenza et al. 2022), granada (Xavier et al. 2021), eucalipto (Diogo et al. 2021) y nuez (Gao et al. 2022). Neopestalotiopsis rosae se encuentra reportado como fitopatógeno con alta agresividad en el cultivo del arándano en países como Perú (Rodríguez-Gálvez et al. 2020) y Portugal (Santos et al. 2022). En México N. rosae se ha encontrado causando afecciones en raíces y hojas de cultivos de fresa en el Estado de Michoacán (Rebollar-Alviter et al. 2020). En el presente estudio se reporta por primera vez a N. rosae para el cultivo del arándano en México. La posible proximidad geográfica y la estrecha relación entre el cultivo de la fresa y el arándano (frecuentemente son cultivados en los mismos ciclos de cultivo y en predios cercanos), puede dar explicación a la presencia de dicho patógeno en ambos cultivos en el mismo estado.
Pestalotiopsis oxyanthi (Thüm.) Steyaert, Bull. Jard. bot. État Brux. 19(3): 329 (1949)
Colonias en PDA con micelio abundante, color blanco en los primeros días y posteriormente se torna de color crema. Al paso de las semanas aparecieron secreciones gomosas, color negro brillante, abundantes sobre el micelio, en su mayoría formando manchas circulares o en algunas ocasiones con bordes irregulares, dichas secreciones corresponden a acérvulos (Figura 2E), formados por conglomeraciones de conidios sobre el micelio. Los conidios son en forma fusoide, rectos o levemente curvados; en su mayoría presentan cinco células por conidio, separadas por septos oscuros; las células terminales (basal y apical) son hialinas y cónicas; célula basal con un apéndice hialino corto; la célula apical presenta varios apéndices simples (2-3 en su mayoría, algunos con 5); las tres células medias son de diferentes tonalidades de café, la primera de ellas suele ser más clara (color miel) y las células posteriores son de colores variantes, en su mayoría café claro, ninguna destaca notoriamente (Figura 2F). El tamaño promedio del conidio es de 7.69 x 19.13 μm (n=20); los conidios pueden encontrarse inmersos en el micelio o aglomerarse en acérvulos.
Material estudiado: México, Michoacán, municipio de Uruapan, septiembre 22, 2022.
Comentarios: Aislada de la flor. La descripción del hongo concuerda con la reportada para Pestalotiopsis oxyanthi (Steyaert 1961). A la fecha del presente artículo, no existe una amplia variedad de trabajos que estudien a fondo la relación de P. oxyanthi con cultivos agrícolas o con otros elementos del agroecosistema; entre los reportados, destacan aquellos que señalan su papel como endófito (Zakaria y Wan 2018, Wei et al. 2007); otros cuantos artículos lo posicionan como saprófito descomponedor de materia orgánica (Falcon et al. 1995, Venedikian y Godeas 1996) y solo uno le atribuye actividades como fitopatógeno en la nuez de la india (Anacardium occidentale) (Patsa et al. 2023). A pesar del poco conocimiento de la actividad de P. oxyanthi, el género Pestalotiopsis en sí, ha atraído la atención de la comunidad científica desde hace varios años, y a pesar de que se ha registrado extensamente su actividad como fitopatógeno en varios cultivos (Keith et al. 2006), las principales investigaciones son enfocadas a su capacidad productora de metabolitos secundarios, los cuales tienen una amplia variedad de aplicaciones y usos como antifúngico, antibacterial, nematicida, entre otros (Xu et al. 2010, Wu et al. 2022, Deshmukh et al. 2017).
Para el cultivo del arándano, se ha reportado en varias ocasiones la presencia del género Pestalotipsis, incluso se podría decir que se encuentra con bastante frecuencia en el cultivo, ocasionando enfermedades como cancro, mancha foliar e incluso llegando a causar la muerte de la planta (Araujo et al. 2023, González et al. 2012, Espinoza et al. 2008). En México ya se ha reportado la presencia de Pestalotiopsis spp. afectando al cultivo del arándano en Michoacán (Mondragón-Flores et al. 2012); sin embargo, la identificación de este se realizó únicamente basándose en la morfología (sin confirmación molecular) y a nivel de género. El conocimiento generado en el presente artículo logra complementar la información previamente reportada, confirmando a nivel de especie, tanto morfológica como molecularmente a Pestalotiopsis oxyanthi en el cultivo del arándano en Michoacán, México.











 nueva página del texto (beta)
nueva página del texto (beta)



