ANTECEDENTES
La alergia a la proteína de la leche de la vaca (APVL) es una de las más comunes en alergias alimentarias en infantiles. Esta enfermedad de difícil diagnóstico y tratamiento dado que se utiliza para describir diferentes enfermedades con síntomas variables como urticaria, angioedema, dermatitis atópica, Sibilancia o más comúnmente gástricos como vómitos, regurgitaciones, dolor abdominal.1,2 La complejidad es aún mayor porque la APVL puede ser mediada por inmunoglobulina IgE, no mediada por IgE o una mezcla de ambos, y puede ser similar a los síntomas ocasionados por problemas en la digestión de la leche en particular la lactosa. Una mala digestión de la leche como ocurre frecuentemente con la lactosa resultará en un aumento de líquido en el tracto gastrointestinal, dolor abdominal y diarrea.3–5
La información que existe sobre APVL está dispersa y existen algunos avances que podrían mejorar el abordaje de esta enfermedad tales como el uso de la escalera de las fórmulas, la escalera de la leche, el uso de probióticos y prebióticos y la Inmunoterapia Oral. El objetivo de esta revisión es proporcionar una visión integral y actualizada sobre la alergia a la proteína de la leche de vaca (APLV), lo que incluye mecanismos inmunológicos, diagnóstico, su epidemiología, tratamiento y nuevas investigaciones, con el fin de ofrecer un documento de compilación basado en evidencia para profesionales de la salud y padres de niños afectados por esta condición.
METODOLOGÍA
La presente revisión de literatura se realizó mediante criterios de inclusión y exclusión. Los criterios de inclusión fueron artículos publicados en revistas científicas revisadas por pares, que abordaran la epidemiología, mecanismos inmunológicos, diagnóstico, tratamiento y nuevas investigaciones sobre la alergia a la proteína de la leche de vaca (APLV). Un segundo filtro se basó en incluir publicaciones en los últimos diez años. Se excluyeron las publicaciones no revisadas por pares, estudios con muestras pequeñas o metodologías poco claras, y publicaciones anteriores a 2013, exceptuando documentos históricos o referencias clave.
La búsqueda de información se realizó en las bases: PubMed, Scopus, Scholar y Web of Science. Se emplearon términos de búsqueda y combinaciones clave relacionadas con la APLV, con operadores booleanos (AND, OR, NOT) en la optimización de criterios de búsqueda. La selección de artículos se llevó a cabo mediante la revisión de títulos y resúmenes con el fin de determinar el cumplimiento de los criterios de inclusión. Finalmente, se compiló la información, métricas de importancia, metodología, resultados y hallazgos clave. Se realizó una síntesis cualitativa de los datos para integrar la información de manera coherente y comprensible. Además, se incluyeron estudios recientes y relevantes publicados durante el proceso de revisión para asegurar que la información estuviera actualizada.
Qué es la alergia a la proteína de la leche de vaca (APLV)?
La alergia a la proteína de la leche de vaca (APLV) es una reacción inmunológica que resulta de la ingestión de leche de origen vacuno y una de las alergias más frecuentes en neonatos con una prevalencia que oscila entre el 0.5 al 3% a los 12 meses de vida.5–7 La APLV en niños con factores de riesgo se asocia fuertemente con el consumo proteico mediante fórmulas.8–11 El término alergia alimentaria corresponde a reacciones contra la salud ocasionado por la exposición a un alimento que tiene su origen en una respuesta inmunológica específica y reproducible. Los síntomas asociados a la alergia son variables y comúnmente pueden ser leves como una urticaria, o graves como reacciones anafilácticas severas.12 En el caso de APLV la reacción es producto de los componentes proteicos presentes en la leche. Existen dos tipos de proteínas relacionadas con las reacciones alérgicas, las caseínas, y las proteínas del suero. En particular la α-lactoalbúmina y la β-lactoglobulina presentes en el suero pueden ser responsables de una respuesta inmunológica específica mediada o no por inmunoglobulina E (IgE).5,13 El 54% del APVL tiene su origen en reacciones ocasionados por IgE y 46% por reacciones del sistema inmunológica no relacionadas al mismo.8 Existen dos mecanismos por los cuales se puede tener una reacción adversa al consumo de la leche de vaca. La primera es la alergia alimentaria y la segunda es la intolerancia alimentaria.
ALERGIA ALIMENTARIA
La exposición a un alimento, en este caso proteína de leche, puede disparar el sistema inmunológico de manera específica y reproducible en los casos de una alergia alimentaria. Los síntomas son variables y pueden ser una leve urticaria, o desencadenar una reacción anafiláctica severa.12 La respuesta inmunológica que resulta de una alergia puede ser la actividad de la inmunoglobulina IgE, puede no estar relacionada a las IgE o ser mixta.4 La reacción alérgica mediada por IgE puede desencadenar múltiples síntomas que normalmente ocurren en menos de una hora, las más comunes a nivel cutáneo o de mucosas con la urticaria, angioedema y las más comunes a nivel respiratorio son la rinitis y broncoespasmos, en casos más graves puede llegar a producir anafilaxia.3,5,9,14 La anafilaxia inducida por alergia a los alimentos requiere de atención y cuidado, debido a su rápido inicio en un lapso no mayor de 2 horas y su potencial de llevar a la muerte en ausencia de tratamiento. La APVL corresponde a una alergia alimentaria cuyo origen son las proteínas caseínas, o bien las proteínas del suero en especial la α-lactoalbúmina y la β-lactoglobulina.5,13
Las alergias alimentarias antigénicas ocurren en dos etapas. Una primera fase (transcelular) que ocurre luego de 120 segundos de exposición a algún antígeno. El antígeno que corresponde a un fragmento de la proteína que dispara el sistema inmunológico, se moviliza de manera transcelular mediante receptores de baja afinidad en las células epiteliales y regulada por la interleucina 4. Las IgE se unen al antígeno para protegerlo de la degradación lisosomal. La segunda fase corresponde a la transepitelial y/o paracelular y ocurre alrededor de 30 minutos posteriores a la exposición del antígeno. Esta reacción es dependiente de la activación de los mastocitos. Existen elementos que aumentan la respuesta alergénica en personas susceptibles al aumentar la permeabilidad intestinal tales como el alcohol, fármacos antiinflamatorios no esteroideos y el estrés.15,16
La reacción alérgica mediada por IgE, resultan de la presencia de un antígeno y creación de IgE específicas del antígeno mediada por linfocitos B. Lo anterior dispone de dos etapas una de inducción y una de provocación. La primera etapa no tiene síntomas y consiste en la exposición de un individuo sensible al antígeno, en el caso que nos ocupa de proteína relacionadas a la alimentación. Consecuentemente, los linfocitos B liberan IgE específicas al torrente sanguíneo. Las IgE se unen al antígeno y a los mastocitos tisulares y a los granulocitos basófilos circulantes. En esta segunda etapa sí existen síntomas clínicos de alergia, y ocurre ante la exposición al mismo antígeno. La exposición activa a los basófilos y mastocitos, que habían sido previamente sensibilizados en la primera etapa, desencadena mediadores proinflamatorios (Figura 1).12,17
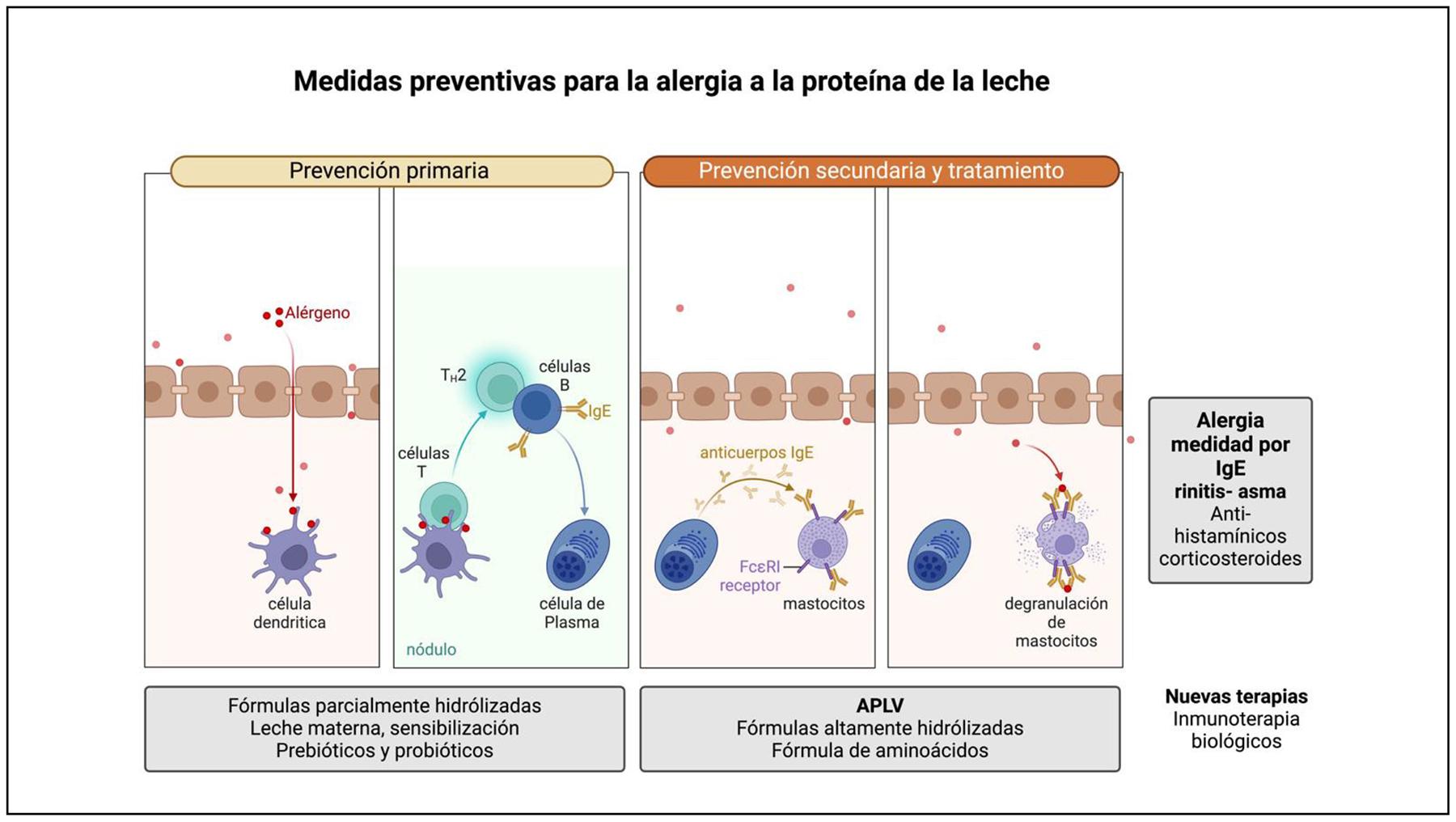
Figura 1. Medidas preventivas para la alergia a la proteína de leche. Adaptado de1,2 Figura creada con BioRender.com.
La leche de bovinos está compuesta por aproximadamente 40 proteínas distintas de las cuales la mitad son potencialmente alergénicas. La caseína representa aproximadamente un 80% de estas proteínas, y el resto está compuesto mayoritariamente por α-lactoalbúmina, β-lactoglobulina y existen otras proteínas pero en mucho menor proporción (Cuadro 1 y 2). Las tres proteínas de mayor relevancia en la alergia mediada por proteína de la leche de vaca son la caseína que es termoestable, eso es que 120 °C por 15 min no altera la antigenicidad; la β-lactoglobulina (BLG) y la α-lacto albumina.7,9,10,18 En particular la BLG está ausente en la leche materna y puede generar reacciones alérgicas aún después de la pasteurización.19 La β-lactoglobulina es una proteína extracelular pequeña que contiene 178aa y un peso de 19,883Da (Figura 2). El identificador como alérgenos en la base de datos del alergoma es 164 y 2739 (164, Bos d 5, 2739, Bos d 5.0101).
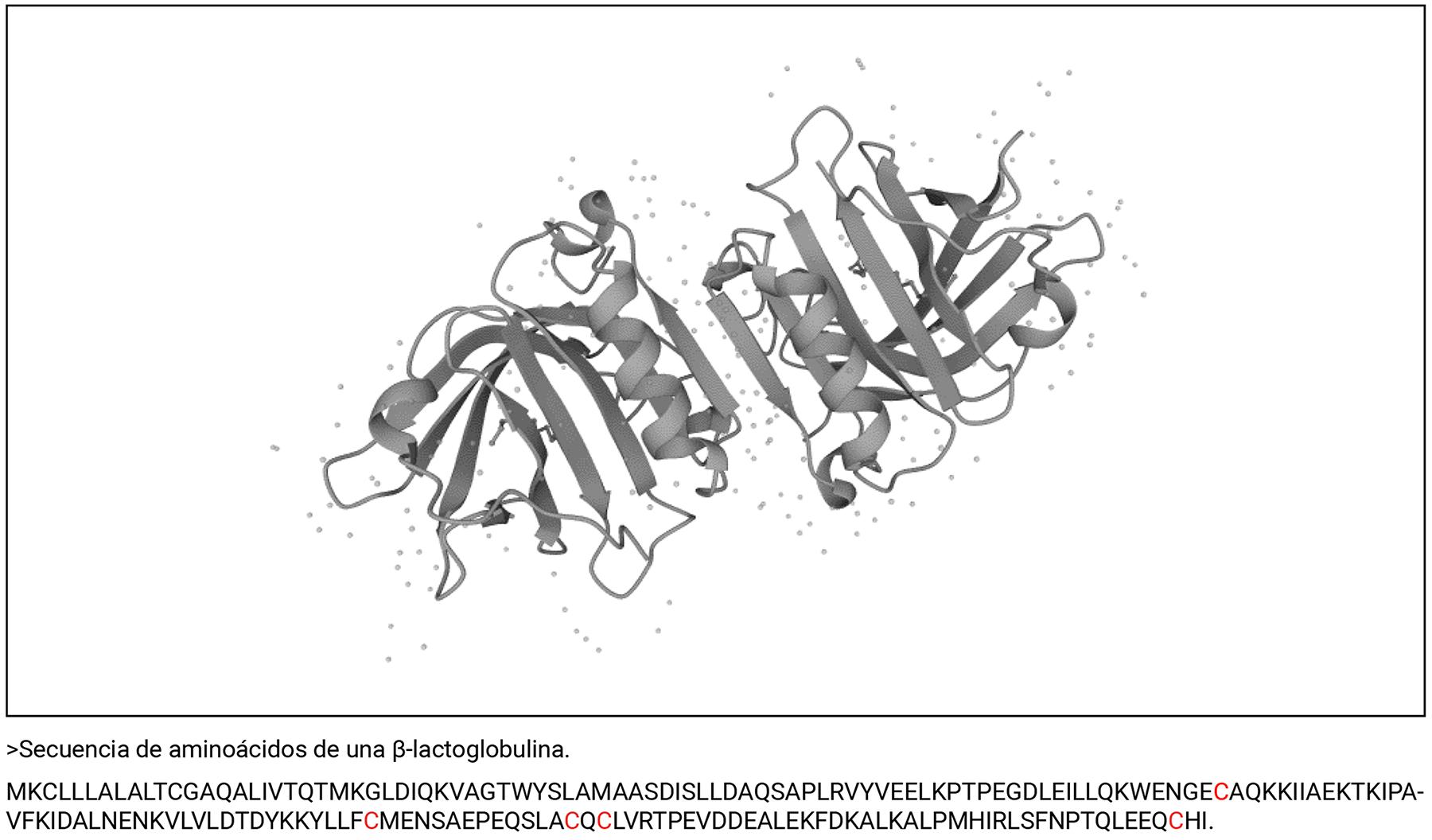
Figura 2. Estructura tridimensional y secuencia de aminoácidos de la β-lactoalbúmina de vaca (Bos taurus) conocida como BGL. Identificador de Uniprot P02754, nótese en rojo los aminoácidos de cisteína con enlaces disulfuro 82-176, 122-135, y 122-137.
Cuadro 1. Alergia a alimentos mediada por IgE, mixta y no mediada por IgE. Adaptado.17
| Mediada por IgE | Mixta | No mediada por IgE |
|---|---|---|
| Inicio< 1 hora, agudo | Inicio > 1 hora, crónico | Inicio > 1 hora, crónico |
| Anafilaxia | Dermatitis atópica | Enterocolitis inducida por proteínas (FPIES) |
| Urticaria y angioedema | Gastroenteropatías | Proctocolitis inducida por proteínas (FPIAP) |
| Síndrome de alergia oral | Esofagitis | Síndrome de Heiner |
| Síndrome gastrointestinal inmediato | Gastritis | Dermatitis alérgica por contacto |
| Rinitis, asma | Enteritis | |
| Anafilaxia por α-Gal | Colitis | |
| Anafilaxia inducida por ejercicio-alimentos |
Cuadro 2. Otras proteínas alergénicas de origen vacuno.
| Fractión | Proteína | Grupo | Allergenicidad | Tamaño KDa | Contenido (%) | Accesión | GI# |
|---|---|---|---|---|---|---|---|
| Caseína (80%) | αs1-caseina | Bos d 9.0101 | Mayor IgE+ basophil+ or SPT+ | 23.6 | 32 | NP_851372.1 | 30794348 |
| αs2-caseina | Bos d 10.0101 | Mayor IgE+ basophil+ or SPT+ | 25.2 | 10 | NP_776953.1 | 27806963 | |
| β-casema | Bos d 11.0101 | Mayor IgE+ basophil+ or SPT+ | 14 | 28 | AAA30431.1 | 162805 | |
| κ-caseína | Bos d 12.0101 | Mayor IgE+ basophil+ or SPT+ | 19 | 20 | NP_776719.1 | 27881412 | |
| Suero (20%) | α-lactoalbúmina | Bos d 4.0101 | Mayor IgE+ basophil+ or SPT+ | 14.2 | 5 | AAA30615.1 | 163283 |
| β-lactoalbúmina | Bos d 5.0101 | Mayor IgE+ basophil+ or SPT+ | 18 | 20 | CAA32835.1 | 520 | |
| Seoralbúmina | Bos d 6.0101 | Menor IgE+ basophil+ or SPT+ | 66 | 1 | AAA51411.1 | 162648 |
La proteína BLG atraviesa las células epiteliales del intestino y son utilizadas por las células presentadoras de antígenos al sistema inmunológico innato tales como los macrófagos y las células dendríticas.19 Estas últimas utilizan endosomas y lisosomas para procesar el alérgeno y procesarlo en péptidos de menor tamaño para presentarlos en la su superficie, donde las células T pueden unirse.20,21 Los síntomas más frecuentes son vómito, regurgitación y diarrea sanguinolentas y los pacientes mejoran con al eliminar el consumo de leche o al usar fórmulas altamente hidrolizadas.22
Algunas de las proteínas de vaca adicionales que pueden ocasionar alergia y relacionadas con la caseína se detallan a continuación en la Cuadro 1 y 2.23 Es importante desatacar la β-lacto albúmina (Bos d 5) a una concentración de 3 a 4 gramos por litro en suero de leche; la α-lactoalbúmina (Bos d 4) que está en una concentración de 1 a 1.5 gramos por litro; las inmunoglobulinas (Bos d 7) de 0.6-1g/L y la albúmina de suero bovino (Bos d 6) 0.1-0.4g/L.9
La alergia alimentaria no mediada por IgE suele ser más lenta y tiene la posibilidad de convertirse en crónica. Los diagnósticos se basan en la presencia de sangre y moco en las heces, el estado del medro, la presencia de diarrea crónica, vómitos, afectación del estado nutricional, rechazo de tomas y si existe alteración del ritmo intestinal.24 A continuación, las tres enfermedades mayoritarias ocasionadas por la alergia a la proteína de la leche no mediada por IgE que son la proctocolitis, la enteropatía y la enterocolitis inducida por proteína de la leche de vaca (FPIES).
En el caso de Proctocolitis inducida por PLV se diagnostica mediante una prueba de provocación una vez que han desaparecido los síntomas. La provocación resulta en un cuadro de sangre en heces pero con coprocultivos negativos. Los síntomas desaparecen alrededor de la cuarta semana de eliminar la exposición y retornan ante una nueva prueba de provocación.24–26
En el caso de enteropatía igualmente se requiere de una prueba de nueva exposición o reintroducción de la PLV una vez desaparecidos los síntomas. La reacción sin embargo es distinta y consiste en el rechazo de las tomas, anorexia, vómitos intermitentes, diarrea, con cuadros que pueden durar dos semanas con o sin fallo de medro. Los síntomas desaparecen aproximadasmente cuatro semanas posterior a eliminar la exposición. El cuadro de diarrea reaparece al reintroducir la exposición de la PLV.24–26
La FPIES se puede presentar en su forma aguda o crónica. En el caso de FPIES aguda existen vómitos en el período de una a cuatro horas después de la exposición, pero con ausencia de los síntomas cutáneos o respiratorios que se presentan cuando la alergia es mediada por IgE. Adicionalmente se pueden presentar episodios subsecuentes de vómitos posterior a la ingestión de la proteína de la leche de vaca; vómitos después de la ingesta de otro alimento; letargia; palidez; puede requerir soporte de líquidos intravenoso; diarrea 5-10h posterior a la exposición, hipotensión, hipotermia (temperatura por debajo de 35°C). En el caso de FPIES crónico grave, igualmente se requiere de una prueba de provocación. Los síntomas son vómitos intermitentes, progresivos y con diarrea que puede contener sangre de manera ocasional, puede tener deshidratación y acidosis metabólica. FPIES tembién puede presentarse como crónico moderada ocasionado por ingestión en menor cantidad de la proteína de la leche, lo que resulta en vómitos intermitentes, sin deshidratación ni acidosis metabólica, y con cuadros de diarrea con escasa ganancia ponderal.24–26
INTOLERANCIA ALIMENTARIA
Este tipo de respuesta puede ser provocada por agentes farmacológicos, preservantes de los alimentos, toxinas contenidas en los alimentos o nutrientes que individuos susceptibles no se pueden digerir. Un ejemplo de este tipo de reacción es la intolerancia a la leche mediada por la lactosa y debido a la ausencia o fallos en la enzima β-galactosidasa (EC.3.2.1.23). La enzima es la encargada de hidrolizar la lactosa en galactosa y glucosa, por lo que su ausencia resulta en una absorción incompleta de lactosa que es utilizada por microorganismos intestinales lo que ocasiona una reacción negativa.3,4
Adicionalmente, existen componentes alimentarios que pueden imitar la respuesta inmunológica ocasionada por la APLV. Por ejemplo, los aditivos alimentarios como el amarillo 5 conocido como tartrazina y los sulfitos que se usan como preservantes que pueden generar una respuesta adversa de mecanismo inmunológico no definido.4,27
Alimentos con potencial alérgeno
La reacción alérgenica dependerá del individuo y la reacción del sistema inmunológico a la exposición de proteínas. Evidentemente la ingestión de alimentos supone la exposición a una gran cantidad de proteínas. Sin embargo, no todas las proteínas tienen el potencial de disparar una respuesta alergénica. Un alimento es cualquier sustancia, ya sea procesada, semi-procesada o cruda que se ingiere. Se deben excluir todas las sustancias que no pueden ser ingeridos como los medicamentos y cosméticos. Ahora bien, algunas proteínas que integran el alimento tienen potencial alergénico, esto es, que disponen de una secuencia de seguidillas de aminoácidos o estructura tridimensional que puede ser reconocidos por el sistema inmunológicos y provocar reacciones típicas de un cuadro de alergia. La mayoría de los alimentos con potencial alérgeno pueden causar reacciones aun después de la cocción o digestión en el estómago y el intestino.7 A esto se le suma la Atopia que son los factores de predisposición genética hacia un alérgeno.
En la industria de los alimentos, los potenciales alérgenos están identificados y deben ser declarados. Es así como el Reglamento (UE) 1169/2011, dispone en el Anexo II, los catorce grupos de alimentos con potencial alérgeno de declaración obligatoria. Esta lista incluye cereales que contengan gluten (trigo, centeno, cebada y avena) o sus variedades híbridas; Crustáceos; Huevos; Pescado; Cacahuetes; Soja; Leche; Frutos de cáscara (almendras, avellanas, nueces, anacardos, pacanas, nueces de Brasil, pistachos, nueces macadamia o nueces de Australia); Apio; Mostaza; Granos de sésamo; Dióxido de azufre y sulfitos (> 10mg/kg o litro); Altramuces; Moluscos.12 Es importante destacar que uno de los principales causantes de alergias alimentarias es el huevo, en Europa, un estudio con 12mil infantes estimó que la alergia al huevo tiene una incidencia media del 1%.28
Tolerancia oral
El término “tolerancia oral” se emplea comúnmente en los siguientes casos que no son excluyentes. El primero es para describir el proceso desarrollado por las células T reguladoras donde se supera la alergia. Lo anterior evidentemente requiere la generación activa de Células T reguladoras específicas de antígenos alimentarios que ocurre ante la inducción al mismo. El segundo ocurre ya sea por terapia o por superación natural, lo que resulta en ausencia de síntomas clínicos después de la ingesta del alimento que ocasionaban la alergia y por tanto existe resolución.
La APVL tiene una resolución mayor al 50% entre los cinco y los diez años, lo mismo ocurre con alergias al huevo con un 50% entre los dos y los nueve años, el trigo con un 50% a los siete años, y la soya con un 45% a los seis años. Por el contrario, existen alergias que persisten y tienen bajas tasas de resolución como la alergia al maní con un veinte por ciento a los cuatro años, la nuez de árbol con tan solo un 10%, mientras que existen alergias persistentes tales como los mariscos.16
La sensibilización a los alérgenos alimentarios puede ocurrir a través del tracto gastrointestinal, la piel y, con menos frecuencia, el tracto respiratorio por lo que es importante verificar la exposición al alérgeno en su manejo para alcanzar la tolerancia.4,11,29 Los factores que influencian la capacidad de tolerar un alérgeno incluyen el microbioma, la insuficiencia de vitamina D, un consumo reducido de ácidos grasos omega 3 poli-insaturados, consumo bajo de antioxidantes, consumo de antiácidos que reducen la digestión de los alérgenos, la obesidad como un estado inflamatorio, así como el momento y exposición a los alimentos. Existe un mayor riesgo a no alcanzar la tolerancia cuando se retrasa la ingesta oral, pero el individuo tiene una exposición ambiental al alérgeno.4,16
Disminución de la exposición al alérgeno.
El ochenta por ciento de las proteínas corresponden a las caseínas y un solo el veinte por ciento se encuentran en el suero de la leche. Los alérgenos más importantes se encuentran en este último a saber la α-lactalbumina (Bosd4), la β-lactoglobulina (Bosd5) y la albúmina de suero bovino (Bosd6) (Cuadro 2).5 Los alimentos cocinados y el uso de matrices como el trigo cocido tienden a mejorar la tolerancia y permitir la ingestión del mismos. En Australia se encontró que un 47% se resuelve a la edad de dos años, en comparación con un 57% de resolución en los niños que tuvieron huevos cocidos, con la tendencia a una mejor resolución en niños con mayor frecuencia de ingestión.30 El microondas puede funcionar para degradar los alérgenos y facilitar la ingesta progresiva del mismo. El microondas es capaz de hidrolizar la β-lactoalbúmina a 200W por 3 minutos, lo que aumenta la hidrólisis y disminuye su inmunoreactividad.9 El uso de matrices como el trigo cocido permitió que un 81% de niños tolerasen la alergia de la leche mediada por IgE.31 Un elemento por considerar sería el uso de presión y en particular el tratamiento enzimático que podría ser efectivo en disminuir la carga antigénica32–34 (Figuras 3 y 4). Alternativamente están emergiendo fórmulas infantiles compuestas de proteínas vegetales como papa, lentejas, quinua, soya y arroz que podrían ser una opción.35
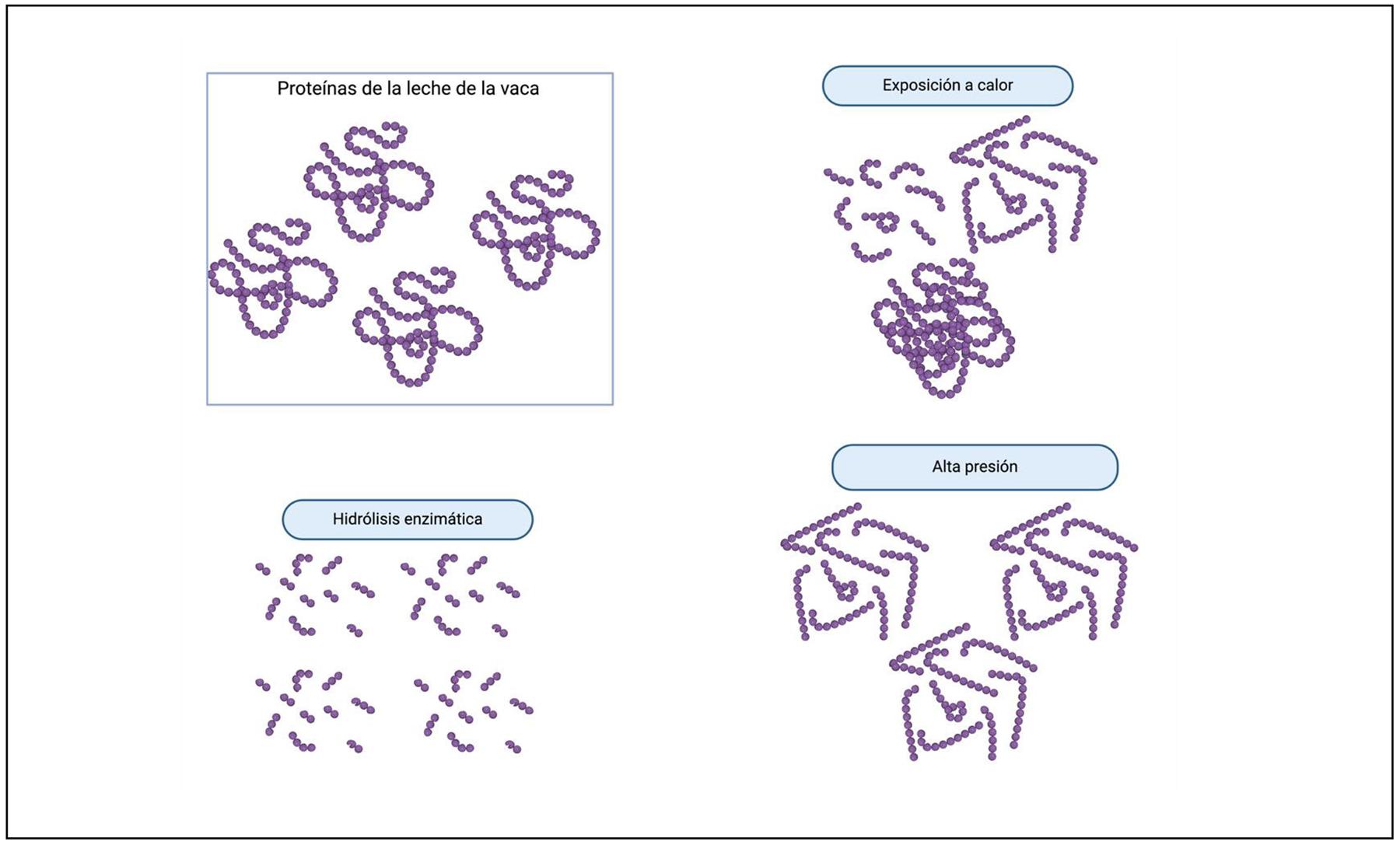
Figura 3. Representación de los cambios en la estructura de proteínas inducidas por tratamientos o procesamiento. Nótese que la hidrólisis enzimática provoca una mayor degradación o proteólisis de las proteínas, destruyendo las estructuras primarias, secundarias, terciarias y cuaternarias, al generar péptidos más pequeños; mientras que los tratamientos térmicos y de presión puede causar la desnaturalización o agregación de proteínas, pero no necesariamente su hidrólisis. Figura creada con BioRender.com.
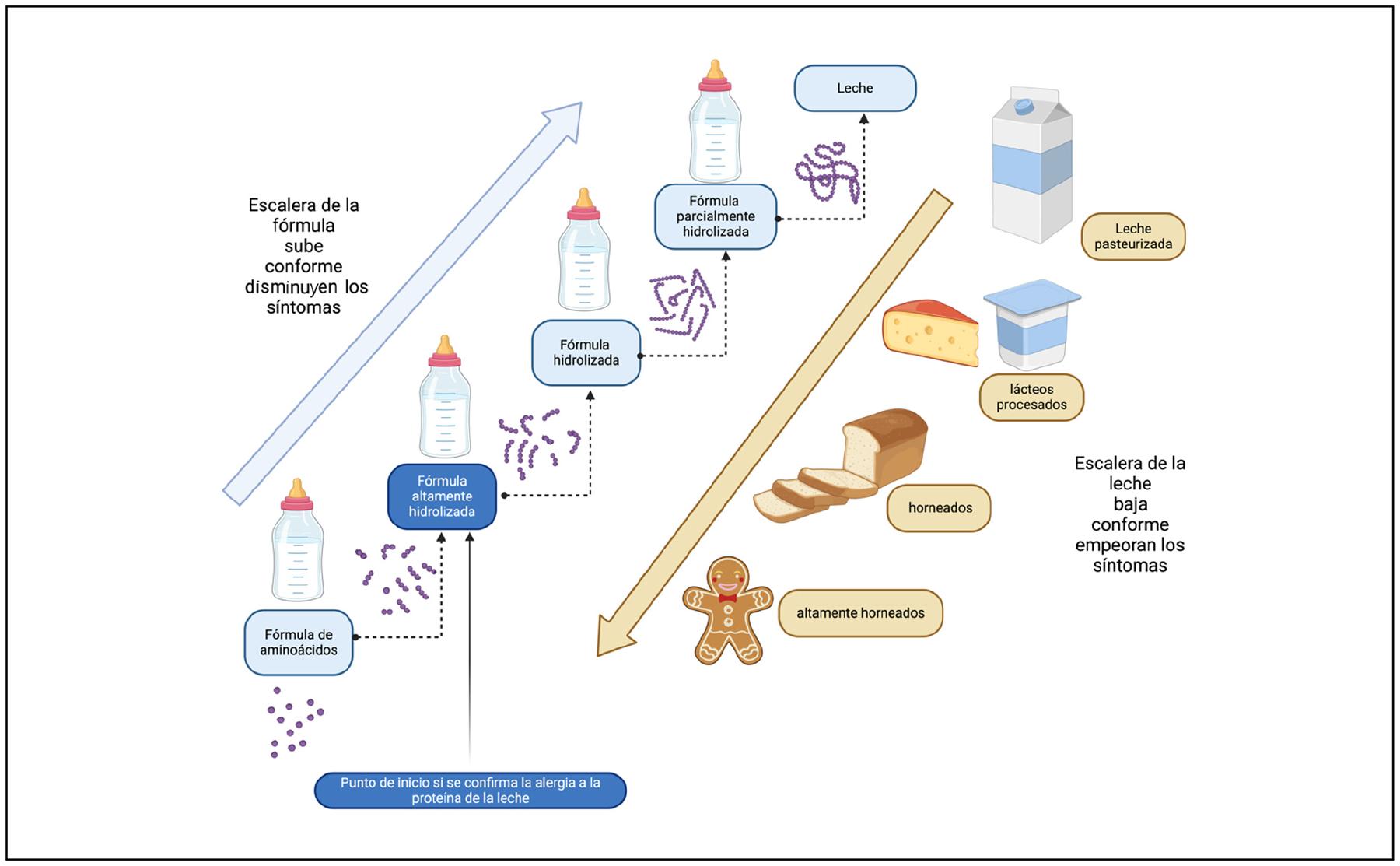
Figura 4. Representación de la escalera del uso de fórmula y escalera de la leche para la introducción de alimentos en alergia a la proteína de la leche. Adaptado de.1 Figura creada con BioRender.com.IgE: inmunoglobulina E, APLV: Alergia a la proteína de la vaca, BLG: β-lactoglobulina, OMS: Organización Mundial de la Salud, FAO: Organización de Agricultura y Alimentos de la Naciones Unidas, BAL: bacterias acidolácticas, GOS: galacto-oligosacáridos (GOS), FOS: fructo-oligosacáridos, 2-FL: 2-fucosil lactosa.
Reacción cruzada.
Los anticuerpos pueden reaccionar al alérgeno original de manera específica y a uno de manera no específica cuya estructura o secuencia es similar. La reacción cruzada es frecuente entre mariscos y nueces. Es posible que exista reacción cruzada con las proteínas de otros bovinos y la PLV, debido a un sitio muy conservado de fosforilación en las proteínas de caseína, sitio que es altamente inmunorreactivo y resistente al calor.9 Esta reacción cruzada ocurre también con proteínas de la soya.10,36 Adicionalmente, es importante aclarar que es común que alergias a otros alimentos como huevo, soya, trigo, pescado ocurran en combinación con APLV por su capacidad alergénica más que por reacción cruzada.
Etiología.
La APVL afecta entre un 0.5 al 3% a los 12 meses de vida, con una prevalencia de un 0.5% en niños alimentados con lactancia materna exclusiva.5,6,8 En América Latina la prevalencia es difícil de establecer debido a que los estudios que se han hecho no han incluido al APVL sino que se enfocan en otros alimentos, sin embargo, se especula un aumento de casos al igual que el resto del mundo.7,13
Epidemiología.
Las estadísticas mundiales indican que existe una prevalencia del 0.5 al 3% durante los primeros 12 meses de vida.4,5 En México se estima la prevalencia en un 1.4% (IC95%:0.9- 2.0%)37 con algunos casos puntuales como Chihuahua con muy baja prevalencia estimada en 0.3%.38 En Brasil varía de un 2,2% en el sur, a 5,4% en el sudeste del país,39 en Argentina al parecer existen datos de baja prevalencia con tan solo 0.3%.40 Los datos sobre alergias alimentarias en otros países de Latinoamérica son escasos, pero se presume un comportamiento similar al mundial fluctuante entre 0,5 al 3%.13,41,42 En Europa se estimaba que era de un 1.3% con un rango de (0.9-2%)43 y existen reportes de incidencias del 0.54%,44 sin embargo, esta frecuencia parece que podría ser mayor según las últimas revisiones que lo estiman en 5.7% (IC95%: 4.4–6.9%).45 En Japón se estima en 2.1%,46 en China se estima que es un 3%, pero es posible que estos datos estén subestimados.47
En Estados Unidos, en una encuesta de 78851 individuos, se presentó una tendencia a la población de estimarse con la enfermedad de 4.7% (IC95%:4.4-4.9%), pero los solamente un 1.9% (IC95%:1.8%–2.1%) cumplían los criterios convincentes.48
Tratamiento.
En general al APLV se confirma al restringir y re-introducir la leche en la dieta. La dieta debe ser de al menos 6 meses de restricción, aunque en pacientes con síntomas graves esta restricción puede extenderse por más tiempo. La APVL no mediada por IgE puede realizarse en casa, a no ser que los síntomas sean muy severos como enterocolitis, diarrea, vómito que lleven a deshidratación y necesidad de hidratación por vía intravenosa. Las pruebas de exposición del alérgeno en piel son una manera de verificar los niveles de IgE.8 La guía latinoamericana para el manejo de la APLV recomienda que se mantenga una dieta de exclusión de leche por 12 meses para la APLV cuando la misma no está mediada por IgE, y hasta 18 meses para la APLV mediada por IgE; lo que varía según la sintomatología del paciente.13,41 Es importante considerar que los niños con APLV tienden a adquirir tolerancia a los 12 años aún sin recibir tratamiento de inmunoterapia oral.49
Guías Médicas para el Abordaje de la APLV
Existen varias guías médicas que proporcionan recomendaciones para el manejo de la APLV (Cuadro 3). En todas las recomendaciones son similares a lo propuesto en la Figura 1, y se resumen en el diagnóstico basado en pruebas de provocación oral y cutáneas; lactancia materna con dieta restrictiva para la madre; el uso de fórmulas hipoalergénicas y el seguimiento y manejo de anafilaxia. La alimentación de la madre como proveedora de leche materna parece tener efectos protectores en el recién nacido en particular las dietas ricas en ácidos grasos polinsaturados de omega-3 EPA y DHA.1
Cuadro 3. Guías Médicas para el Abordaje de la APLV.
| Guía | Organizatión | Año | Recomendaciones clave | Hipervínculo/Cita |
|---|---|---|---|---|
| Guía de Práctica Clínica para el Manejo de la APLV | Instituto Mexicano del Seguro Social (IMSS) | 2011 | Eliminación de la leche de vaca y sus derivados de la dieta. Uso de fórmulas extensamente hidrolizadas o a base de aminoácidos. Dieta de eliminación para madres lactantes. Seguimiento y reevaluación periódica. | IMSS Manejo de la alergia a la proteína de la leche de vaca. México: Instituto Mexicano del Seguro Social, Manejo de la alergia a la proteína de la leche de vaca. 2011. Esta guía puede ser descargada de Internet en: http://www.imss.gob.mx/profesionales/guiasclinicas/Pages/guias.aspx |
| Guía Clínica Alergia a Protema de Leche de Vaca | Subsecretaría de Salud Pública, Chile | 2021 | Diagnóstico basado en pruebas cutáneas y provocación oral. Fomento de la lactancia materna con dieta de eliminación para la madre. Uso de fórmulas hipoalergénicas. Seguimiento y manejo de anafilaxia. | Disponible en https://staging.scai.cl/wp-content/uploads/2024/11/2021-GUIA-CLINICA-APLV-2o-EDICI0N-2021.pdf |
| Documento de Consenso sobre APLV no mediada por IgE | Sociedad Española de Gastroenterología, Hepatología y Nutrición Pediátrica (SEGHNP) | 2018 | Diagnóstico basado en historia clínca y pruebas de eliminación y reintroducción. Uso de fórmulas extensamente hidrolizadas. Manejo de enterocolitis y proctocolitis alérgica. Seguimiento y prevención. | Disponible en https://www.seghnp.org/sites/default/files/2019-02/Doc%20Con-senso%20APLV.pdf |
| Protocolo de Actuación ante la APLV | Servicio de Pediatría, España | 2024 | Evaluación clínica detallada. Eliminación de la leche de vaca y sus derivados de la dieta. Educación a los padres sobre la identificación de alérgenos. Uso de probióticos y prebióticos. | Servicio de Pediatría |
| Consenso sobre el Diagnóstico y Tratamiento de la APLV | Sociedad Latinoamericana de Gastroenterología, Hepatología y Nutrición Pediátrica (SLAGHNP) | 2022 | Diagnóstico basado en pruebas cutáneas y provocación oral. Uso de probióticos y prebióticos. Inmunoterapia oral. Seguimiento y reevaluación periódica. | 65 |
| Guidelines for the Diagnosis and Management of Food Allergy | National Institute of Allergy and Infectious Diseases (NIAID), USA | 2010 | Diagnóstico basado en historia clínica, pruebas cutáneas y niveles de IgE específicos. Uso de fórmulas extensamente hidrolizadas o a base de aminoácidos. Manejo de anafilaxia. Educación a los padres y seguimiento continuo. | NIAID, Disponible en https://asthma-allergy-center.com/wp-content/uploads/FOOD-ALLERGY-NIH-Guide-For-Patients.pdf |
| Food allergy in under 19s: assessment and diagnosis | National Institute for Health and Care Excellence (NICE), UK | 2011 | Diagnóstico basado en historia clínica y pruebas de eliminación y reintroducción. Uso de fómulas extensamente hidrolizadas. Manejo de síntomas gastrointestinales y cutáneos. Educación a los padres y seguimiento continuo. | NICE Disponible en https://www.nice.org.uk/guidance/cg116/resources/food-allergy-in-under-19s-as-sessment-and-diagnosis-pdf-35109392795845 |
| Japanese guidelines for food allergy 2020 | Committee for Japanese Pediatric Guideline for Food Allergy, The Japanese Society of Pediatric Allergy and Clinical Immunologyy, The Japanese Society of Allergology | 2020 | Diagnóstico basado en historia clínica, pruebas cutáneas y niveles de IgE específicos. Uso de fórmulas extensamente hidrolizadas o a base de aminoácidos. Manejo de anafilaxia. Educación a los padres y seguimiento continuo. | 66 |
Consideraciones nutricionales en pacientes con APVL.
El APVL ocasiona una menor ingesta de calcio y lípidos, menor concentración sérica de retinol, betacaroteno, licopeno y 25-hidroxivitamina D.50 Lo anterior significa que es importante proveer suplementos o alimentos ricos en estas necesidades nutricionales.
Indicación de probióticos y prebióticos
Los probióticos y prebióticos representan una estrategia para prevenir y manejar la APLV. Probióticos basados en microorganismos como Lactobacillus rhamnosus y Bifidobacterium bifidum, pueden ser beneficiosos para reducir los síntomas y promover la tolerancia oral.51–53 La Organización Mundial de la Salud (OMS) y la Organización de Agricultura y Alimentos de la Naciones Unidas (FAO) definen a los probióticos como “microorganismos vivos que cuando son consumidos en cantidades adecuadas como parte de los alimentos o suplementos promueven un estado benéfico de salud al huésped”.54 La colonización bacteriana del tubo digestivo inicia posterior al nacimiento y durante los primeros siete días post parto y varía en los primeros meses. El tipo de parto es clave en este desarrollo dado un vaginal provee lactobacilos y bifidobacterias que son microorganismos benéficos en este proceso de colonización. El suplemento de probióticos y prebióticos es además importante dado pacientes con APLV existe una disminución en especies de Firmicutes y un aumento de Bacteroidetes en comparación con pacientes sanos.
A continuación se presentan los datos más relevantes que se encontraron sobre probióticos y prebióticos.
Probióticos. Los microorganismos probióticos utilizados en el consumo humano y pediátrico incluyen las bacterias ácido-lácticas (BAL) lactobacilos como L. rhamnosus GG ATCC53103 y bifidobacterias como Bifidobacterium bifidum, así como cepas bacterianas no patógenas, como Streptococcus, Enterococcus y microorganismos no bacterianos como la levadura no patógena Saccharomyces boulardii cepa CNCM I-745.55 El uso de probióticos es beneficioso para mejorar los síntomas y superar la APLV, uno de los más estudiados es Bifidobacterium bifidum que reduce la respuesta inflamatoria y los niveles séricos de IgE y aumenta los niveles de IgG2, así como Lactobacillus rhamnosus que mostró resultados positivos aún al suplementarse en fórmulas basadas en caseína hidrolizada.56,57 En el caso específico de Bifidobacterium es capaz de modular la inmunidad innata y adaptativa.51 Bifidobacterium bifidum TMC3115 redujo los síntomas de APLV.58 Para mayor información existe una revisión de literatura que presenta el análisis de múltiples estudios sobre el uso de probióticos.53
Prebióticos. Son ingredientes alimentarios que no son digeridos como la inulina y fruto-oligosacaridos pero que estimulan a bacterias beneficiosas como Bifidobacterium. La leche materna contiene alrededor de 200 oligosacáridos (HMO) que ejercen efectos prebióticos y antimicrobianos y explica la presencia incrementada de bifidobacterias en infantes alimentados con leche materna.59 Los más usados para la suplementación alimentaria pediátrica son los galacto-oligosacáridos (GOS) y los fructo-oligosacáridos (FOS) en una relación 90/10, además se usan los oligosacáridos ácidos, la polidextrosa, oligofructuosa e inulina. Uno de los prebióticos con mayor potencial y que está presente en la leche humana como u HMO es el 2-fucosil lactosa (2-FL), que dependiendo del país puede estar presente en formulaciones infantiles de manera comercial.55,60
Respuesta clínica en lactantes con APLV.
El problema de la APVL constituye el diagnóstico en lactantes lo que puede comprometer el crecimiento y desarrollo psicomotor. Desafortunadamente no existen pruebas diagnósticas sensibles ni específicas en los primeros 12 meses post-parto. Lo anterior implica el uso de un diagnóstico basado en excluir el alérgeno para verificar la causa y su reintroducción para determinar si existe o no reacción. El cuadro clínico es variable y puede ser confuso afectando mayoritariamente el tracto digestivo (50%-60%), pero pueden ocurrir también en la piel (50%-60%), y el tracto respiratorio (20%-30%), con grados de intensidad de leve, moderada o grave.
Riesgos.
Esta enfermedad es similar a otras enfermedades crónicas con una fuerte influencia de factores genéticos, ambientales y la interacción de ambos. La prevalencia de APVL puede ser entre 40-60% relacionado a antecedentes familiares y perinatales. Adicionalmente el riesgo de APVL se incrementa según los siguientes factores. Una madre atópica: cinco veces; madre mayor de 30 años: tres veces; nacimiento por cesárea: tres veces; la combinación de madre atópica y cesárea incrementa diez veces el riesgo; tres veces al recibir fórmula a base de PLV; dos veces al haber no recibir lactancia o hacerlo por un corto tiempo.5,9,47
Inmunoterapia oral (ITO)
La inmunoterapia oral (ITO) consiste en proveer pequeñas dosis de manera progresiva del alérgeno, de tal manera que se logre una desensibilización natural y una disminución de los síntomas.
Eficacia y Seguridad
La ITO ha demostrado ser eficaz en la desensibilización de pacientes con APLV, permitiendo que muchos niños toleren la leche dependiente de una constante exposición y terapia. Sin embargo, son comunes los efectos secundarios con presencia de síntomas leves. En algunos casos, pueden ocurrir reacciones alérgicas graves que requieren tratamiento con epinefrina. Esto es particularmente importante para niños un alto IgE para α-lactoalbúmina y caseína parecen tener un mayor riesgo de presentar reacción grave durante la ITO.61
Existen además terapias emergentes con ensayos con clínicos mediados por anticuerpos monoclonales contra los anticuerpos IgE, que complementan la ITO como el duplimab y el omalizumab, y que al parecer muestran mejorías versus el placebo en alergias alimentarias (Ensayo clínico NCT04148352, Ensayo clínico NCT01157117).62–64 Además, una de las estrategias de reintroducción de los alimentos es usar la escalera del uso de las fórmulas hidrolizadas y la escalera de la leche conforme mejoran o empeoran los síntomas (Figura 4).1
CONCLUSIONES
Un diagnóstico preciso y un manejo integral, que incluya la eliminación de alérgenos, lactancia materna, el uso de fórmulas hipoalergénicas, la educación de los padres y el seguimiento continuo, son clave para el tratamiento efectivo de la APLV. La incorporación de probióticos, prebióticos y la inmunoterapia oral puede mejorar aún más los resultados. Para ello, la implementación de guías clínicas actualizadas y basadas en evidencia, como las recomendaciones de la Sociedad Latinoamericana de Gastroenterología, Hepatología y Nutrición Pediátrica (SLAGHNP) y el Instituto Mexicano del Seguro Social (IMSS), puede mejorar significativamente el manejo de la APLV.
Proporcionar una nutrición adecuada y una microbiota intestinal saludable es importante. La leche materna juega un papel clave dado que provee oligosacáridos prebióticos.
El diagnóstico y manejo temprano de la APLV son cruciales para el abordaje correcto del mismo. Para lograr esto son importantes las pruebas de provocación oral y cutáneas, así como fomentar la lactancia materna con dieta restrictiva para la madre.
Lactobacillus rhamnosus y Bifidobacterium bifidum son beneficiosos para reducir la respuesta inflamatoria y promover la tolerancia oral.
La Inmunoterapia Oral (ITO): puede ser útil en lograr la desensibilización de pacientes con APLV, pero existe un riesgo de efectos secundarios.
Es importante mantener una adecuada atención nutricional, que suplemente los requerimientos de calcio y lípidos, retinol, betacaroteno, licopeno y vitamina D.











 nueva página del texto (beta)
nueva página del texto (beta)



