Introducción
La reanimación hídrica intravenosa es una herramienta esencial en el manejo de pacientes hospitalizados en el área de urgencias o áreas críticas. Mientras que en el uso correcto de esta terapia es necesario para asegurar la supervivencia del enfermo en estado de choque, la literatura actual ha demostrado que su uso no está libre de riesgo.
Uno de los conceptos actuales que se ha propuesto es guiar la reanimación hídrica, encontrando el punto exacto donde la reanimación no sea muy poca y ocasione hipovolemia, que lleve al paciente en estado de hipoperfusión, hipoxia y falla orgánica; o a hipervolemia y con ello a una sobrecarga hídrica, edema (cerebral, pulmonar, etcétera), lesión renal y a un incremento en la mortalidad, estancia hospitalaria y costos.1
Se entiende por edema a la acumulación en exceso de líquidos en los tejidos. Dicha acumulación anormal puede ser el resultado de un incremento en la filtración de líquidos afuera del espacio vascular, o una disminución de su eliminación del espacio intersticial por el sistema linfático.2 El desplazamiento de líquidos fuera del espacio intravascular está regulado por la relación que existe entre la presión hidrostática, la presión oncótica y la permeabilidad capilar. Un incremento en la presión hidrostática o en la permeabilidad capilar; o una disminución en la presión oncótica incrementarán el movimiento de fluidos fuera del espacio intravascular.3
El endotelio juega un papel fundamental en la homeóstasis vascular, en el control del tono vascular y en la regulación de la respuesta inmunológica, la inflamación y la angiogénesis. Las células endoteliales presentan una gran versatilidad, ya que deben detectar y adaptarse a las necesidades de sus células vecinas y a microambientes diversos.4 La célula endotelial lleva a cabo una variedad de funciones que son específicas de su localización y, por esta razón, exhibe una considerable heterogeneidad y características que son distintas de cada lecho vascular; sin embargo, una de las funciones más dinámicas es la de barrera selectiva que controla el movimiento de fluidos, iones y otras macromoléculas entre la circulación sanguínea y los tejidos adyacentes, por medio de la regulación de los complejos de unión entre las células endoteliales.5
El propósito de esta revisión es repasar las características del sistema endotelial, el cómo, al llevar a cabo una reanimación hídrica intravenosa, podemos generar una disfunción de dicho sistema y, en consecuencia, la generación de edema.
Sistema endotelial
El endotelio se puede definir como una monocapa que separa los tejidos de la sangre. Las células endoteliales tienen múltiples funciones que son específicas a su localización; sin embargo, su principal función es regular el flujo y la perfusión sistémica a través de cambios en el diámetro y en el tono vascular.6
El endotelio forma la superficie interna de los vasos sanguíneos. Se compone aproximadamente de 1 a 6 × 1013 células, con un peso aproximado de un kilogramo y cubre un área de superficie de cerca 1 a 7 m2 (Figura 1).4
La heterogeneidad estructural del endotelio se observa en los distintos lechos vasculares, ya que en algunos es continuo (cerebro, corazón, etcétera), mientras que en otros es fenestrado (glomérulo renal, glándulas exocrinas y endocrinas, etcétera) y, en otros, discontinuo (sinusoides hepáticas). Las células endoteliales están involucradas en diferentes funciones, que incluyen a todo el endotelio en su conjunto, o que se refieren a órganos o lechos vasculares específicos.7
El endotelio continuo se caracteriza por células endoteliales fuertemente conectadas unas a otras y rodeadas por una membrana basal continua. Las uniones intercelulares están formadas por complejos multiprotéicos, los cuales contienen proteínas transmembranales y citosólicas, que conectan las proteínas de membrana con el citoesqueleto intracelular.8
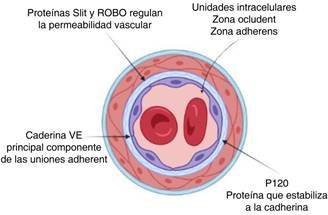
Hay dos subtipos de uniones intercelulares: las uniones apretadas o «zona ocludens» y las uniones adherentes o «zona adherens». En las uniones apretadas las principales proteínas son las claudinas, las ocludinas y las moléculas JAMs. En las uniones adherentes se cuenta sólo una proteína transmembrana, VE-Cadherina9 (Figura 2).
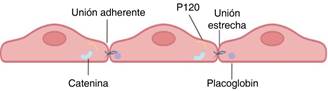
Figura 2: Sistema endotelial caracterizado por células fuertemente conectadas. Uniones intercelulares formadas por complejos multiproteicos, proteínas transmembrana.
En estudio realizado por Nyall R London y colegas, estaban interesados en el papel de una vía de señalización protagonizada por las proteínas Slit y Robo en la regulación de la permeabilidad vascular. Aunque a la proteína Stil y su receptor, Robo, se les implicó en el desarrollo neuronal, los mismos investigadores encontraron que estas unidades también tienen un papel en la angiogénesis. En dicho estudio, se demostró que la Slit recombinante puede atenuar la permeabilidad endotelial provocada por la actividad in vitro de endotoxinas y citoquinas. Este efecto de protección requiere al receptor Robo, y el resultado parece estar mediado por la mayor localización en la membrana celular de una molécula de adhesión, la VE-Cadherina.9
La VE-Cadherina es el principal componente de las uniones adherentes, estrictamente reguladas por complejos de proteínas que se unen a células endoteliales adyacentes y evitan la migración de leucocitos y la fuga vascular. El desplazamiento de la VE-Cadherina de la membrana celular al interior de la célula es suficiente para inducir espacios entre las células endoteliales, conduciendo al aumento de la permeabilidad. Esta eliminación de la VE-Cadherina se previene normalmente mediante otra proteína, la p120-Catenina, que se une y estabiliza la VE-Cadherina de la membrana. Se sabe que los mediadores inflamatorios como el factor de crecimiento vascular endotelial causan la disociación de la p120-Catenina y VE-Cadherina, lo que conlleva la internalización de la VE-Cadherina. El grupo de NR London determinó que la proteína Slit impide esta disociación9 (Figura 3).
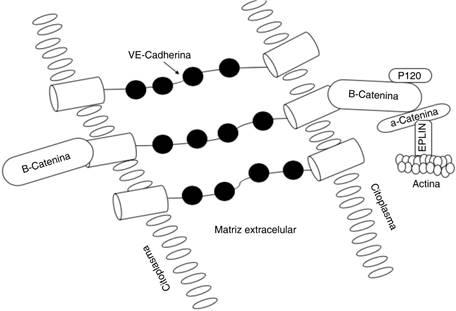
Figura 3: Modelo propuesto de la interacción entre las proteínas que median la adhesión célula-célula. Esta unión se da gracias a la interacción de los dominios extracelulares de las cadherinas, que está reforzada por la unión al citoesqueleto de actina. Esta unión al citoesqueleto mediada por la interacción de b-catenina con el dominio citoplasmático de e-cadherina por un lado y con a-catenina por el otro, a-catenina, a su vez, interactúa con los filamentos de actina a través de EPLIN.
Las células endoteliales cuentan con la presencia de los cuerpos de Weibel-Palade y destaca la presencia de un gran número de vesículas y caveolas a lo largo de la superficie luminal, que son capaces de moverse de la superficie luminal a la superficie basal de la célula.9 Las caveolas juegan un papel importante en la regulación de la señalización y función de las células endoteliales.
Las moléculas de adhesión celular (CAM) se dividen en cuatro subgrupos diferentes: inmunoglobulinas, integrinas, selectinas y cadherinas. Dentro de las inmunoglobulinas existen las moléculas de adhesión intracelular (ICAM-1 e ICAM-2), las cuales participan en la activación y migración de leucocitos a los tejidos. Las integrinas tienen dos subunidades: alfa y beta, y están presentes entre las células endoteliales. Las selectinas son moléculas que interactúan con los leucocitos o con los oligosacáridos. Las selectinas E intervienen cuando las citoquinas inflamatorias están activadas, tomando protagonismo en el rodamiento de los leucocitos. Por su parte, las cadherinas facilitan la unión entre las células o bien en la extravasación de leucocitos (Figura 4).
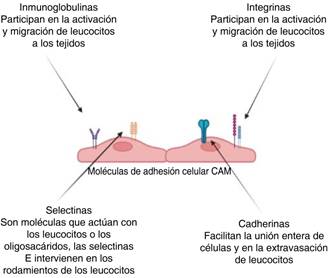
Figura 4: Las moléculas de adhesión celular (CAM) se dividen en 4 subgrupos diferentes: inmunoglobulinas, integrinas, selectinas y cadherinas.
Las células endoteliales producen sustancias con múltiples funciones de crucial importancia. Entre ellas están el óxido nítrico y la prostaciclina, que tiene efecto vasodilatador: la endotelina, el tromboxano A2 y el anión superóxido, con acción vasoconstrictora; el heparán y la trombomodulina con efecto antitrombótico y el activador e inhibidor del plasminógeno tisular con función de regulación de la fibrinólisis, entre otras.10
Glicocálix
Asimismo, el endotelio cuenta con una estructura dinámica, que lo tapiza, rica en carbohidratos dispuestos en red, específicamente proteoglicanos, glucosaminoglicanos y glicoproteínas, llamada glicocálix.11 Su disposición multicapa reducirá el contacto de la célula endotelial con los componentes sanguíneos celulares y macromoléculas.
Dentro de las funciones del glicocálix están la regulación de la permeabilidad vascular a las moléculas y líquidos (agua y solutos), la filtración glomerular, la permeabilidad de macromoléculas (proteínas), hematocrito capilar y flujo sanguíneo capilar, la coagulación vascular, previene la adhesión de plaquetas y leucocitos al endotelio y funciona como barrera de lipoproteínas. Sin embargo, una de sus funciones más importantes es la de modulador entre las fuerzas mecánicas tangenciales del torrente sanguíneo y las células del endotelio vascular.11
El glicocálix es mediador de los cambios de permeabilidad del agua ante las fuerzas de tensión, evitando edema y regulando la filtración de proteínas. Regula la permeabilidad vascular de dos maneras: creando un filtro pasivo sobre las uniones célula-célula y actuando como una plataforma de señalización que regula activamente la integridad de la unión; como filtro molecular, creando una barrera de permeabilidad pasiva al formar un andamio de polímeros en la pared vascular, al que las proteínas del suero se integran12 (Figura 5).
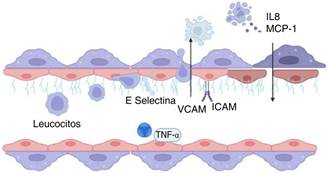
Figura 5: Glicocálix: estructura dinámica que «tapiza» las células endoteliales, compuesta por una red de carbohidratos. Reduciendo el contacto de la célula endotelial con los componentes sanguíneos celulares y macromoléculas. El TNF-alfa promueve la expresión de antígenos de histocompatibilidad canales I y II sobre el endotelio. La migración transendotelial de los monocitos y de los linfocitos está medida por moléculas de adhesión y es favorecida por el TNF-alfa liberado por las células endoteliales, y se ha observado un incremento en la expresión de moléculas de E selectina, ICAM, VCAM, el hecho que se presente un respuesta inflamatoria localizada, favorece la disfunción endotelial. MCP-1 = proteína quimioatrayente de monocitos-1. VCAM = molécula unida a la membrana celular. ICAM = moléculas de adhesión endotelial.
Lesión endotelial y edema
La disfunción endotelial comprende una pérdida del balance entre los factores vasodilatadores y vasoconstrictores derivados del endotelio, donde el estado vasoconstrictor llega a ser dominante, llevando a cambios fisiopatológicos progresivos. Colectivamente, estos cambios endoteliales exhiben características proinflamatorias, prooxidantes, proliferativas, procoagulantes y de adhesión vascular13 (Figura 6).
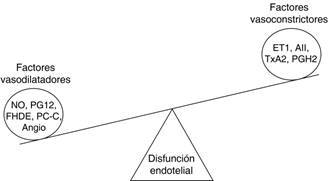
NO = óxido nítrico. PG12 = prostaciclina. FHDE = factor hiperpolarizante dependiente de endotelio. PC-C = péptido natruriético C. ET-1 = endotelina. AII = angiotensina II. TxA2 = tromboxano A2. PGH2 = endoperóxido.
Figura 6: La disfunción endotelial comprende una pérdida del balance entre los factores vasodilatadores y vasoconstrictores derivados del endotelio, donde el estado vasoconstrictor llega a ser dominante, llevando a cambios fisiopatológicos progresivos.
Los mecanismos por los cuales se pueden provocar la lesión endotelial incluyen (Figura 7):
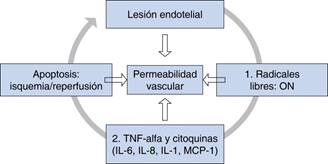
Figura 7: Los mecanismos por los cuales se pueden provocar la lesión endotelial incluyen: lesión por radicales libres y enzimas proteolíticas. TNF-alfa potencia la acción tóxica de los leucocitos polimorfonucleares. Apoptosis. Permeabilidad vascular.
Lesión por radicales libres y enzimas proteolíticas.
TNF-alfa potencia la acción tóxica de los leucocitos polimorfonucleares.
Apoptosis.
Permeabilidad vascular.
1. Lesión por radicales libres y enzimas proteolíticas
La reducción de óxido nítrico no siempre estará asociada a un proceso benéfico de vasodilatación. Cantidades liberadas bajo la acción de la óxido nítrico sintetasa inducible (iNOS) pueden ser lesivas, pues su liberación es traída y al combinarse con el anión superóxido favorecen la producción de peroxinitrito, que actúa como un poderoso oxidante (Figura 8).14
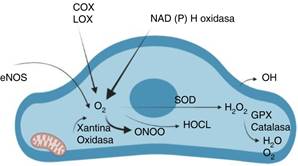
COX = ciclooxigenasa. LOX = lipooxigenasa. NAD = nicotinamida adenina dinucleótido. SOD = superóxido dismutasa. HOCL = ácido hipocloroso.
Figura 8: El óxido nítrico sintetasa al combinarse con especies reactivas de oxígeno producen gran cantidad de especies oxidantes.
Sin embargo, dentro del rubro de la reanimación hídrica en pacientes críticamente enfermos, se ha demostrado que la sobrecarga de sodio, misma que se encuentra en soluciones cristaloides, reduce el grosor del glicocálix, permitiendo que éste penetre en las células endoteliales, lo que resultaría en incremento de la rigidez vascular y en disminución de la liberación de óxido nítrico.15,16
2. El TNF-alfa y las citocinas potencian la acción tóxica de los leucocitos polimorfonucleares
La lesión sobre el endotelio estimula la expresión de moléculas de adhesión que interactúan con los polimorfonucleares y las plaquetas, permitiendo infiltración subendotelial, así como atrapamiento en la microvasculatura, facilitando la vasoconstricción, el edema endotelial y la disminución de la flexibilidad de la membrana celular.14
Se sabe que la mayoría de las actividades del TNF-alfa provoca disfunción en las células endoteliales, mediante la inducción de cambios morfológicos y funcionales, que han sido catalogados como activador endotelial. El TNF-alfa incrementa la permeabilidad del endotelio y la adherencia de leucocitos a esta monocapa a través de la inducción de moléculas de adhesión celular como E-selectina, ICAM-1 y VCAM-1. Activa la quimiotaxis de leucocitos de manera directa o a través de la secreción endotelial de quimiocinas como la IL-8 y la MCP-1, lo que favorece su migración a los sitios de lesión vascular. Por otra parte, el TNF-alfa influye en los eventos inflamatorios vasculares al regular la secreción endotelial de IL-1 e IL-6 e inducir la actividad de la ciclooxigenasa y, por ende, la síntesis de prostaciclinas.14
3. Apoptosis
El daño a los tejidos durante un periodo de disminución de flujo (isquemia total o parcial) puede ser paradójicamente amplificado por la restauración del flujo sanguíneo (reperfusión). Aunque la gravedad de los daños resultantes de la isquemia/reperfusión varía entre los tejidos, es un componente común de este proceso patológico para todos los órganos en la disfunción microvascular. Las células endoteliales sufren un aumento del estrés oxidativo, especialmente las vénulas postcapilares, generando adhesión leucocitaria y aumentando la permeabilidad vascular. Los efectos colaterales de la isquemia/reperfusión alteran de manera directa al glicocálix endotelial y, por lo tanto, la función del mismo.14
4. Permeabilidad vascular
Al modificarse la estructura del glicocálix, conlleva el contacto directo de las sustancias/moléculas con las células endoteliales, lo cual conlleva una remodelación tisular y reclutamiento del sistema inmunológico. La N-alfa-PGP (prolina-glicina-prolina acetilado en porción N terminal) es una matriquina que deriva de la colágena, la cual es capaz de activar la vía de la señalización relacionadas con la permeabilidad vascular de manera selectiva por un mecanismo independiente de citoquinas proinflamatorias.17
In vitro N-alfa-PGP aumenta la fosforilación de la VE-Cadherina y Rac 1 a través del receptor de quimiocinas CXCR2. VE-Cadherina es, como se ha mencionado, la proteína estructural de las uniones intercelulares endoteliales; Rac1 es una proteína G monomérica que, fosforilada, contribuye a la remodelación del citoesqueleto, al emplear una línea de células endoteliales se demostró un incremento en la permeabilidad vascular.17
Conclusiones
Si bien se conoce y se sabe mucho de la estructura del sistema endotelial, tanto de su composición macroscópica, microscópica y molecular, así como del daño endotelial y su génesis en cuanto a la formación de aterogénesis, aún falta conocer mucho sobre la lesión endotelial y la permeabilidad vascular; más allá, por lesión, por sépsis o aterogénesis, falta aún saber a ciencia cierta cómo es que la reanimación causa daño a nivel molecular para generar la permeabilidad vascular. Sin embargo, en este escrito, con la información que se tiene por el momento, se logró explicar que el uso de soluciones cristaloides pueden generar daño a nivel del glicocálix como primer paso y posterior lesión a nivel molecular de las células endoteliales en cuanto a sus uniones, para así facilitar dicha permeabilidad vascular y generar el edema.











 nueva página del texto (beta)
nueva página del texto (beta)