INTRODUCCIÓN: PRIMERO ESCUCHO, LUEGO HABLO
La adquisición del lenguaje articulado ha sido objeto de estudio en diversas disciplinas con un consenso en que el desarrollo de la capacidad de abstracción en el cerebro fue fundamental [Castro et al. 2002; Navarro 2003; P. Lieberman 2007; Benítez 2006].
Además, se reconoce que el surgimiento de rasgos culturales y el proceso lingüístico han contribuido a la modificación de estructuras funcionales presentes en los primates. Este estudio se centra en los aspectos físicos del lenguaje humano, explorando los órganos y estructuras relacionadas con el habla y la percepción auditiva, así como su importancia en la evolución del lenguaje.
El lenguaje humano se caracteriza por cuatro rasgos de diseño (cuadro 1) que abarcan desde su soporte físico hasta la forma en cómo se transmiten los mensajes [Igoa 2010]. Dentro del aspecto físico se analizan los órganos y las estructuras involucradas en el habla (laringe, fosas nasales, lengua), así como las relacionadas con la percepción acústica (conducto auditivo externo y la cóclea).
Cuadro 1. Clasificación de los rasgos de diseño del lenguaje
| Soporte físico | Significante - significado | Funciones | Estructura |
| -Transmisión vocal-auditiva -Emisión multidireccional y recepción direccional | -Arbitrariedad -Desplazamiento -Semántica-Ambigüedad | -Libertad de uso-Predicación -Pluralidad de funciones-Intercambio de roles | -Infinitud discreta-Composición -Recursividad-Doble articulación |
Modificada de Igoa [2010].
Si bien las actividades o comportamientos como el habla no se fosilizan, ciertas estructuras anatómicas a las que podemos acceder en los fósiles, como el hueso hioides o las impresiones del área de Broca o de Wernicke en el cráneo, proporcionan información. La ausencia de soporte anatómico adecuado sugiere la falta de una función biológica concreta [Martínez et al. 2009].
Investigaciones previas Cakir et al. 2002; Aguilera 2007; Quam et al. 2012; 2017] han demostrado una relación entre la capacidad auditiva y la producción de sonidos esenciales para la comunicación, incluso las correlaciones entre la morfología del cráneo y la percepción auditiva.
La función auditiva, esencial para la comunicación, ha evolucionado para adaptarse a las necesidades de supervivencia de cada especie, en cuanto a la captación de un espectro de frecuencias sonoras específicas. Esto implica una variedad de mecanismos de codificación auditiva que comparten diversas especies, incluso mecanismos especializados para codificar sonidos [Del Rio 1989]. De esta manera, el sistema auditivo constituye el brazo aferente de la comunicación y su evolución en los humanos está dirigida hacia la detección de los sonidos del habla [Martínez et al. 2013; Quam et al. 2013].
En los mamíferos, por lo menos en los terrestres, la función del oído es cualitativamente similar, sólo varía en la forma y escala al captar las vibraciones por medio del oído externo, que luego pasan por el oído medio e interno, atravesando la membrana timpánica y los huesecillos, hasta llegar a la cóclea, donde las vibraciones ejercen presión en la ventana oval, que permite el paso del líquido coclear para activar las células pilosas de la membrana basilar y generar potenciales de acción que se transmiten al cerebro. Este proceso permite la percepción de distintos sonidos al ser los receptores sensoriales del oído los encargados de determinar las frecuencias en cada especie y la amplitud del sonido, el cual está determinado por la intensidad de la descarga y el número de neuronas que se activan [Soto et al. 2003; Rosowski 1994].
El análisis de este proceso y su aplicación en diferentes mamíferos ha permitido relacionar directamente las estructuras anatómicas con las frecuencias audibles, conocido como el ancho de banda, que indica las frecuencias mínimas y máximas de un sistema, plasmado en audiogramas.
Por ejemplo, los primates estrepsirrinos muestran una mayor sensibilidad a las frecuencias altas con un límite superior de 60 kHz y rango de mejor audición entre 8 y 16 kHz; mientras que los haplorrinos exhiben una sensibilidad más equilibrada en todo el espectro auditivo, con un límite superior que va de los 40-50 kHz y mayor sensibilidad en frecuencias superiores a los 8 kHz, con excepción de los simios y los humanos.
En todos los primates neotropicales (Platyrrhini) la capacidad auditiva es similar, con un pico de sensibilidad de 1-2 kHz que se va perdiendo hacia los 4 kHz, siendo la máxima sensibilidad de 8-10 kHz, con una disminución paulatina hasta los 16 kHz. En los monos paleotropicales (Catarrhini) las variaciones son mayores, pero existen ciertas generalidades en el ancho de banda, que va desde menos de 60 kHz a 40-50 kHz, con un primer pico de sensibilidad a 1 kHz y un segundo a 8 kHz, así como una pérdida gradual que se intensifica después de los 16 kHz [Quam et al. 2012, 2017].
Los audiogramas de Platirrhini y de Catarrhini tienen forma de ., que sugiere una condición primitiva, sin embargo, este patrón no está presente en algunas especies como: Macaca fuscata, Cercophithecus mitis, Chlorocebus aethiops y Papio cynocephalus.
El valor promedio del ancho de banda, en la especie humana es de 3.8 kHz, mientras que en los chimpancés es de 2.8 kHz y en el caso de algunos especímenes neandertales, de Sima de los Huesos, es de 3.4 kHz con un límite superior de 4.3 kHz, que da lugar a una curva de transmisión de potencia de sonido similar al patrón humano [Martínez et al. 2004; 2013; Quam et al. 2017].
Respecto a los chimpancés, éstos tienen dos picos de mayor sensibilidad audible, el primero alrededor de 1 kHz que, a diferencia de los humanos, se reduce después de los 3 kHz, y el segundo que posteriormente se recupera en los 8 kHz [Martínez et al. 2013]. De igual manera, el tiempo de reacción en chimpancés para discriminar entre las vocales . y . y entre . y . es más largo, por tanto, estas vocales son percibidas de manera similar [Kojima 1990].
Por otra parte, la cadena osicular del oído medio de distintos homínidos evidencia diferencias significativas respecto a Homo sapiens, como un mayor tamaño en la cabeza del martillo y el estribo en Homo neanderthalensis; mientras que en Australopithecus africanus . Paranthropus robustus se mantienen similitudes con los chimpancés. La base del estribo, así como la cóclea en general, son más pequeña en los grandes simios comparados con los humanos modernos, aunque el área coclear no muestra una relación clara con las frecuencias auditivas percibidas y se hipotetiza que estas variaciones reflejan diferencias en tamaño más que en forma [Moggi et al. 2002; Quam et al. 2013; Rosowski 1994].
Por tanto, analizar las estructuras anatómicas asociadas permiten generar hipótesis sobre la plasticidad ontogenética de la organización craneofacial, sobre la influencia de factores epigéneticos, así como de factores internos y externos de las matrices y sobre los patrones de modularidad e integración.
1. MODULARIDAD E INTEGRACIÓN: UNA CORRELACIÓN EDUCATIVA
Las repercusiones de la evolución en los cambios anatómicos del cráneo se dividen en módulos. El concepto de modularidad se refiere al grado de conectividad entre las estructuras anatómicas del cráneo, independientes de manera relativa, pero que interactúan durante los procesos biológicos y forman unidades integradas para producir características fenotípicas particulares [Klingenberg 2008; D. Lieberman 2011]. Los módulos se conforman de centros de tejido blando y espacios que proporcionan soporte funcional, también se conocen como matrices funcionales [Moss et al. 1968].
Se distinguen dos tipos de matrices (cuadro 2): las periósticas que incluyen tejido blando y dientes, y las capsulares que contienen cavidades y órganos como el cerebro y los ojos, divididas en unidades macroesqueletarias y microesqueletarias [Moss et al. 1968; Sardi 2017].
Cuadro 2 Ejemplificación de algunas matrices funcionales y sus componentes menores
| Componente | Matriz funcional |
| Neural anterior | Porción del cerebro (principalmente lóbulos anteriores) relacionada al frontal y la fosa craneal anterior, meninges, líquido céfalorraquídeo, senos frontales. |
| Neural medio | Porción del cerebro (principalmente lóbulos anteriores) relacionada con los parietales, fosa craneal media y parte de la fosa posterior, tallo cerebral, meninges, líquido céfalorraquídeo. |
| Neural posterior | Cerebelo, meninges, líquido céfalorraquídeo. |
| Ótico | Cavidades, conductos, huesecillos, tímpano, ligamentos. |
| Óptico | Globo ocular, músculos orbitarios, nervios ópticos, tejido adiposo, ligamentos. |
| Respiratorio | Cavidad funcional, mucosas respiratorias y olfativas. |
| Masticatorio | Músculos masticatorios (principalmente los músculos masetero y temporal). |
| Alveolar | Dentición, mucosas orales, lengua. |
Modificado de Sardi [2017].
El cuadro muestra que todas las estructuras del cráneo están relacionadas entre sí y participan en más de una función. Los mecanismos de integración permiten que los módulos varíen según el contexto de cada organismo, sean funcionales y puedan adaptarse a las novedades [Klingenberg 2008; Wagner 1990; Camargo-Prada et al. 2017].
En este artículo se analizan dos módulos, el basicráneo y la cara como unidades macroesqueléticas distintas, pero significativamente integradas en los primates [Püschel 2014], con patrones de correspondencia de una cara alargada y estrecha con una base craneal larga, estrecha y plana [Neux 2016; Neux et al. 2018].
Esta clasificación facilita el análisis de los componentes que albergan estructuras anatómicas relacionadas con la transmisión y recepción del lenguaje articulado, localizadas principalmente en estructuras microesqueléticas del basicráneo (paladar, fosas craneales, foramen hipogloso y yugular) y el viscerocráneo (oído y ángulos faciales).
2. METODOLOGÍA
Se utilizaron las imágenes digitales de 31 especímenes adultos, actuales y extintos, pertenecientes a cinco géneros de la familia Hominidae. Australopithecus (n=1), Homo .sapiens n=7, heidelbergensis n=1, neanderthalensisn=1), Pan (n=6), Gorilla (n=5) y Pongo (n=4) . el género Macaca (n=6) de la familia Cercopithecidae, por medio de Tomografías Axiales Computarizadas (TAC).
Los ejemplares del género Homo . Australopithecus .africanus Sts5), se obtuvieron del Archivo Digital de Fósiles Homínidos, del Departamento de Antropología Evolutiva en la Universidad de Viena y del repositorio de Prehistoria y Evolución Humana de la Universidad Nacional Autónoma de México (UNAM), disponibles en la biblioteca “Juan Comas” del Instituto de Investigaciones Antropológicas (IIA).
Los 21 ejemplares de grandes simios se obtuvieron del repositorio digital del Instituto de Investigaciones en Primates de la Universidad de Kioto, Japón (Digital Morphology Museum, kupri).
Mediante morfometría virtual se visualizaron los cortes en 2d y se generó un modelo 3d de cada uno de los cráneos, usando el Software OsiriX Md®v12.0 [Rosset et al. 2004] y realizando 35 medidas (tabla 1): 23 lineales, nueve ángulos y tres áreas, siguiendo la metodología de Bromage [1992], Lieberman y McCarthy [1971] y Quam y colaboradores [2012; 2015; 2017]. Posteriormente, con estos datos también se obtuvieron seis índices.
Tabla 1 Medidas tomadas en las tacs de cráneo
| Medidas | Abreviatura | Definición |
| Longitud | ||
| Superior CAE | LCAEs | Del receso superior al extremo distal del hueso temporal |
| Media CAE | ICAEm | Del centro del meato auditivo al centro de la membrana timpánica |
| Inferior CAE | lcaei | Del surco timpánico al extremo distal del hueso timpánico |
| Ancho proximal CAE | ACAEp | Entre las inserciones de la membrana timpánica |
| Ancho medio CAE | ACAEm | Vertical en el punto medio de la longitud |
| Ancho distal CAE | ACAEd | Del extremo del peñasco temporal al hueso timpánico |
| Basion | LB | De Eb a Ba |
| Total del basicráneo | LBt | Total de LFCA más LFCP |
| Fosa craneal anterior | LFCA | De S a Fc |
| Fosa craneal posterior | LFCP | De S a Ba |
| Segmento vocal horizontal | LSVh | De Pr a Ba |
| Palatina | LP | De Pr a Ef |
| Estafilión-Basión | DEfB | Distancia lineal de Ef a Ba |
| Hormión-Esfenobasión | DHEf | Distancia lineal de H a Eb |
| Neurocráneo | LN | Distancia lineal de N a Op |
| Ancho neurocraneal | AN | Distancia lineal entre E |
| Altura neurocraneal | HN | Distancia lineal de Ba a V |
| Facial | LF | Distancia lineal de Pr a H |
| Ancho facial | AF | Distancia lineal de entre Z |
| Altura facial | HF | Distancia lineal de N a Pr |
| Ótica | LOT | Distancia lineal del margen posteroinferior del hueso timpánico al punto medio interno del petroso |
| Ancho ótico | AOT | Distancia lineal de punto más anterior al más posterior del meato auditivo externo |
| Altura ótica | HOT | Distancia lineal de Au a Po |
| Ángulos | ||
| Base craneal | ABC | Entre los planos de Ba-S y S-Fc |
| Deflexión craneal | DC | De la intersección de los planos N-Ba con Frankfurt |
| Del Plano SN y el Punto Subespinal | SNA | De la intersección de los planos S-N con n-Pr |
| Del Plano SN y el Punto Suprameatal | SNB | De la intersección de los planos S-N con N-Id |
| Facial | ANf | De la intersección de los planos Frankfurt con N-Pg |
| Porción petrosa | APP | Entre el plano trasverso de la superficie petrosa posterior y el plano S-Fc |
| Membrana timpánica | AnT | Entre el plano del receso superior al surco timpánico con el cae en su porción timpánica |
| Ancho distal CAE | AaD | Del extremo distal del hueso timpánico al temporal y la prolongación sobre cae |
| Meato auditivo | AnMA | Del punto orbital medio, al punto medio del meato auditivo a la tuberosidad maxilar |
| Áreas | ||
| Del meato auditivo | AMA | Suma de pixeles representando el meato auditivo |
| Del foramen hipogloso | AH | Suma de pixeles representando el foramen hipogloso |
| Del foramen yugular | AY | Suma de pixeles representando el foramen yugular |
| Índices | ||
| Volumétrico neural | IVN | Raíz cúbica de la longitud por ancho y altura del neurocráneo |
| Volumétrico facial | IVF | Raíz cúbica de la longitud por ancho y altura del viscerocráneo |
| Volumétrico ótico | IVO | Raíz cúbica de la longitud por ancho y altura óticas |
| Neurofacial | INF | IVN entre IVF |
| Tamaño craneal | TCG | IVN más IVF |
| Retropalatino | IRP | LP entre DEtB |
La comparación de individuos con tamaño corporal distinto requirió de medidas análogas para minimizar el error intraobservador, aplicando la prueba de comparación de medidas repetidas; posteriormente se realizó un análisis MANOVA para relacionar varias variables de respuesta y un conjunto común de predictores. Por último, se obtuvieron coeficientes de covarianza y de correlación lineal (Pearson); se realizó un análisis de componentes principales (ACP) para describir conjuntos de datos y describir modelos predictivos. Todos los análisis se realizaron con SPSS (v. 21) y PAST (v. 4.03).
3. UN ANÁLISIS DESDE LA PALEOANTROPOLOGÍA DEL ORIGEN DEL LENGUAJE
En cuanto a las capacidades fonadoras de las especies fósiles, existe un consenso en aceptar que su morfología craneal eran similar a las de los chimpancés [Laitman 1985; Martínez et al. 2009], que se confirma en el presente estudio, de manera específica en las vías aéreas superiores, donde la longitud del segmento vocal horizontal o cavidad oral se encuentra nuevamente dentro del rango de chimpancés, lo cual se ha relacionado con un patrón de incapacidad para producir eficazmente la pronunciación de las vocales /a/, /i/, y /u/ [Lieberman et al. 1971; Martínez et al. 2009].
Este patrón se diferencia en Australopithecus africanus, ya que la longitud de la cavidad oral es intermedia entre Homo sapiens y Pan troglodytes. En el caso de Homo sapiens se encuentra dentro del rango de variación de los macacos, que nos hablaría de la importante reducción de la cavidad oral en los humanos, dentro del grupo Hominini.
En cuanto al índice retropalatino, los resultados confirman la hipótesis de Lieberman y Crelin [1971] de un paladar más corto en proporción a la longitud del espacio retrofaríngeo en grandes simios, dando una diferenciación con Homo sapiens, Australopithecus africanus y Homo heidelbergensis.
especto al ángulo de la base craneal, diversos estudios [Jeffery et al. 2002; Jeffrey 2005] explican la existencia de una relación ontogenética con las vías aéreas superiores (r=0.46, sig. 0.001). La cavidad orofaríngea crece respecto a la nasofaríngea, la línea media de la base del cráneo se retroflexiona entre el segundo y tercer mes de gestación. Moss y colaboradores [1968] explican esta diferencia, debido a que las vías aéreas superiores son influenciadas por el crecimiento de la lengua y el acomodo de la posición del hioides, los cuales en el periodo embrionario y fetal son determinados por el tránsito del líquido amniótico [García 2018].
Por otra parte, algunas investigaciones [Camargo et al. 2017; Quevedo 2017; Sardi 2017] exponen el cambio de las vías aéreas superiores como un efecto de la flexión craneal (ABC); mientras Lieberman [1991] considera que la mandíbula tiene una mayor influencia. Para esta investigación se pudo contrastar una correlación entre el ángulo de la base del cráneo (ABC) y la cavidad oral (LSVH), al obtener correlación pequeña pero significativa (r=0.456, P=0.017).
De acuerdo con la hipótesis de spacial-packing, que implica el crecimiento del cerebro como el factor principal para la modificación de ABC, al crecer el basioccipital y moverse anteroinferiormente el foramen magnum, la base se desvía ventralmente y el hueso petroso se reorienta coronalmente, para poder acomodar un cerebro relativamente mayor [Jeffery et al. 2002]. Esto implicaría que abc se relaciona con el ángulo de la porción petrosa (APP) y ambos con el índice de encefalización relativo (IER). En este caso se encuentra una relación positiva entre ABC y APP (r=0.643, P=0.00), que no muestran correlación con IER, para concluir que el verdadero factor de correlación es el tamaño de la bóveda craneal y no el cerebro directamente
El basioccipital de los humanos tiene una orientación más inclinada relativa a la base craneal anterior, mostrando un grado mayor de flexión, mientras la pirámide petrosa está orientada más coronalmente, como consecuencia muestra una fosa craneal posterior más amplia y profunda en comparación con otros primates. Estos resultados evidencian una disposición menor para la faringe cuando el ángulo es más cerrado.
Respecto a los ángulos faciales se muestra un mayor crecimiento de la mandíbula en el caso de G. gorilla, P. abelii y M. mulatta. Por su parte, Homo heidelbergensis está dentro del rango humano, pero Australopithecus africanus presentan un ángulo menor. En cuanto al prognatismo maxilar, relacionado con el desarrollo mayor del bulbo olfatorio, existe una agrupación de los grandes simios con macaca y una reducción considerable en el grupo Homo. Las últimas dos estructuras de la base del cráneo analizadas son el foramen yugular y el hipogloso. El área del foramen yugular en humanos modernos, coincide con los reportes de Wysocki [2002] de entre 51 a 59 mm2, sin embargo, se ve una diferencia en los macacos de casi el doble de tamaño mayor de la muestra en esta investigación, con el reporte de 7.1 a 7.8 mm2. De manera general, ambos forámenes son mayores en Homo sapiens, que supone un desarrollo diferenciado importante, si se recae en su importancia como canales que contienen el par craneal IX, X y XII, para inervar lengua, hioides, paladar, membrana timpánica y el oído medio [Chávez et al. 2011; Rodríguez et al. 2004; Rivera 2015; Katsuta 1997].
Dicha discrepancia puede deberse a las composiciones morfológicas básicas que presenta el foramen, ya sea dividido o no dividido, cuando se presentan una división el área es más difícil de calcular. En los humanos el porcentaje de división es de 10% en hombres y de 11% en mujeres, con un porcentaje similar presentado en macacos [Wysocki 2002]. En el presente estudio la minoría de los ejemplares presentan un foramen dividido.
Respecto a la capacidad auditiva, Rosowski [1994] evidencia que el oído externo y medio tienen una gran influencia en la forma del audiograma debido a su función selectiva de frecuencia. Otros parámetros que influyen en las frecuencias percibidas por mamíferos terrestres son: 1) el tamaño corporal, 2) distancia entre las orejas, 3) tamaño de la oreja, 4) rigidez de la oreja y 5) la longitud del CAE.
Los mamíferos más grandes son sensibles a frecuencias por debajo de 10 kHz, mientras los más pequeños perciben sonidos superiores a 10 kHz. Relación inversa con la distancia entre las orejas, pares cercanos perciben frecuencias mayores [Heffner y Masterton 1970]. Respecto a la rigidez, entre mayor composición cartilaginosa tenga el oído medio, que se deforma con los movimientos de masticación y de la cabeza, entonces causa una sensibilidad deficiente en la precepción de sonidos de baja frecuencia; mientras que entre mayor sea al área de la membrana timpánica y los huesecillos, se perciben mejores sonidos de bajas frecuencias [Masterton et al. 1969].
En el caso del conducto auditivo externo (CAE), se espera que canales auditivos anchos y cortos tendrán poca audición en frecuencias bajas y los canales angostos captan de mejor manera los sonidos de baja frecuencia [Heffner y Heffner 1990]. Al conjugar ambos factores de longitud y amplitud los CAE (figura 1) se aglomeran en tres grupos, el primero incluye los géneros Homo y Australopithecus africanus; el segundo con macacos, chimpancés y orangutanes; el tercero con los gorilas.
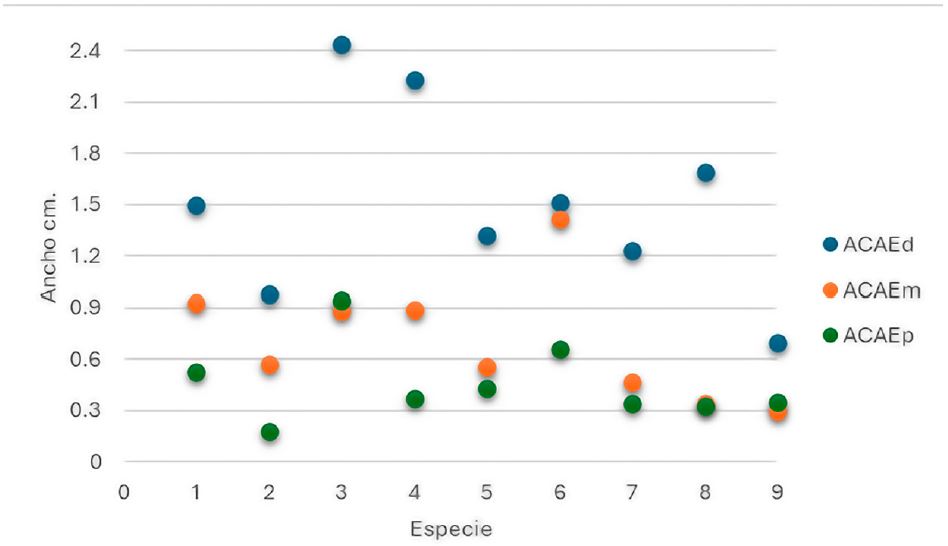
Figura 1. Gráfica de dispersión del ancho del meato auditivo externoLas especies están representadas numéricamente en el eje X: 1) Australopithecus africanus, 2) H. steinheimensis, 3) H. erectus, 4) H. sapiens, 5) P. troglodytes, 6) G. gorilla, 7) P. abelii, 8) P. pygmaeus y 9) M. mulatta.
De igual manera, se debe tener en cuenta que existe una variación de las frecuencias audibles, entre los individuos de una misma especie, con una diferenciación sexual. Reportando, por lo general, las mayores variaciones a frecuencias altas [Heffner y Masterton, 1970]. Este dimorfismo es muy marcado en la muestra de orangutanes de esta investigación.
En cuanto a los ángulos de la membrana timpánica y del ancho distal no se encontró con una referencia previa, pero muestran un ángulo más amplio en la membrana de Homo sapiens, al distinguirlo de los demás grupos. El ángulo del ancho distal muestra en valores más pequeños en Homo sapiens y Homo steinheimensis, seguidos de un grupo de los grandes simios, donde destaca el mismo rango en macacos, por último, los valores más amplios los tiene Australopithecus africanus.
El último rasgo analizado del oído es el índice volumétrico ótico que muestra la cavidad auditiva como una matriz funcional integrada en un módulo relacionado con el crecimiento facial y el craneal.
Respecto al ángulo distal del meato auditivo, Australopithecus africanus está en el rango de los chimpancés, humanos y otros mamíferos [Bromage 1992], que evidencia un rasgo primitivo. Esta variación puede deberse a factores como la altura facial posterior, que indican un cambio temporal tal vez relacionado con la posición de la laringe y faringe en Homininos tempranos, los cuales se encuentran en el rango superior de los chimpancés, posteriormente la condición primitiva de mamíferos reapareció en H. sapiens.
Por último, se realizó una correlación simple de Spearman entre los primeros dos componentes principales del conjunto de medidas relacionadas con el aparato fonador, la audición y el cráneo; dichas correlaciones se expresan por un número real que va de -1 a 1, al existir una correlación fuerte y directa si la covarianza es positiva, los cuales determinan la dependencia que existen entre variables del oído y los módulos del cráneo correspondientes, para obtener correlaciones significativas y positivas entre el CP1 de fonación (LBt) con CP1 del oído (LCAEm); mientras que el CP2 de fonación (ABC) tiene una correlación negativa con la longitud media del CAE y el ancho distal del CAE.
Conclusión
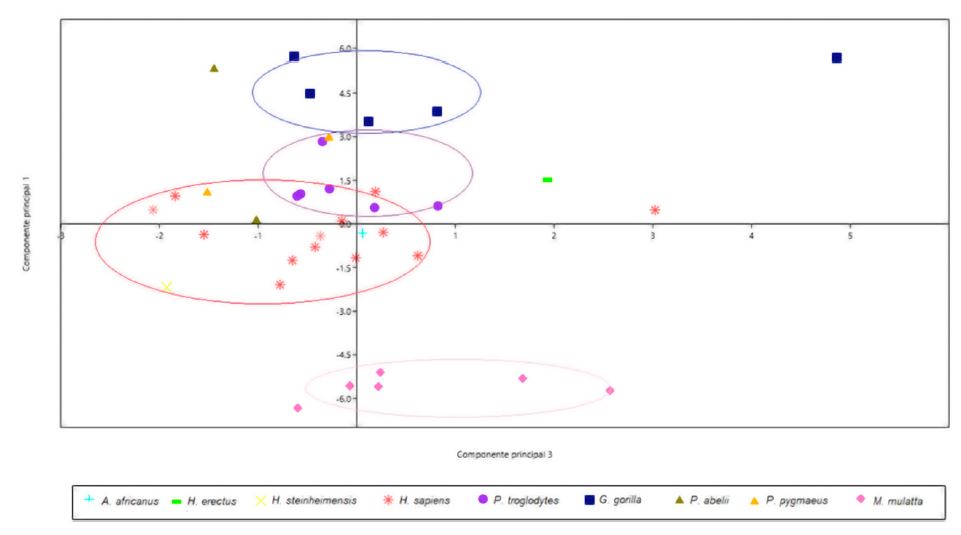
Un análisis de componentes principales, al combinar los rasgos anatómicos analizados, mostró la separación en tres grupos: 1) macacos, 2) grandes simios y 3) el género Homo con Australopithecus africanus (figura 2), confirmando la existencia de una correlación de manera general entre el oído, la base del cráneo y la cavidad bucal; son rasgos adaptativos que, en conjunto, podrían formar un templete que dio paso al desarrollo del lenguaje articulado, también pueden deberse a múltiples factores como el cambio de postura o alimentación, entre otros.
Australopithecus africanus . Homo erectus se agrupan entre chimpancés y humanos o en los rangos de mayor variabilidad del grupo Homo¸ por lo cual sus rasgos en conjunto permiten inferir que no tenían todas las adaptaciones relacionadas con el lenguaje hablado, por tanto, se infiere que carecieron de él, cuando evidencia el caso contrario con Homo heilderbergensis,que se agrupa en los rangos inferiores de los humanos modernos con estructuras anatómicas relacionadas con la fonación y la audición, dando la posibilidad del lenguaje doble articulado.
La separación entre grandes simios y macacos evidencia la anatomía diferencial que limita la producción del habla humana, pero sigue mostrando que en sus determinados géneros existe esta correlación entre el oído y el aparato fonador. Respecto a este grupo, los orangutanes muestran algunas excepciones y cercanía al género Homo, como con los chimpancés, posiblemente debido a una ontogenia convergente de manera evolutiva, respecto a la retención de rasgos juveniles (neotenia) [Caponi 2007; Contreras 2016]. De igual manera, se debe considerar el impacto de las primeras experiencias, por medio de los estímulos sensoriales y la complejidad de los estímulos sociales; por ejemplo, el lazo entre madre y cría [Contreras 2016]; ya que los orangutanes tienen un periodo de crianza de siete años aproximadamente, además de su estructura social de fusión-fisión, requiere una compleja cognición para poder comunicarse [Galdikas 1983]. Por lo cual, ampliar los análisis etológicos de la comunicación en primates se hace necesario para entender las relaciones aquí planteadas.











 nueva página del texto (beta)
nueva página del texto (beta)