Contribución del estudio
Los productos formulados con benzimidazoles no son solubles, por lo que deben de ser administrados en forma de suspensión a dosis altas. Durante décadas se ha estudiado la formulación del compuesto alfa (basado en la solubilidad de los benzimidazoles). Estudios previos han demostrado la actividad fasciolicida del compuesto alfa en ovinos y bovinos con el fin de disminuir el manejo en los animales, así como, para administrar una menor dosis del compuesto activo. En el presente estudio, se evaluó la toxicidad aguda y subaguda del compuesto alfa inyectable en ratas Hsd Han: Wistar, mediante el análisis bioquímico del suero, la hematología y el estudio histomorfológico en la toxicidad subaguda. La información obtenida indicó que no se produjeron cambios importantes en los parámetros analizados, por lo que, con base en la información obtenida, este fármaco tiene un amplio margen de seguridad.
Introducción
Fasciola hepatica es un trematodo zoonótico que afecta a diferentes hospedadores mamíferos, incluido el ser humano.1,2 La fasciolosis es una enfermedad parasitaria importante en medicina veterinaria, porque provoca pérdidas económicas globales en la industria ganadera al disminuir la productividad de la leche, la carne, la lana, el crecimiento de los animales jóvenes y la fertilidad. Se ha de considerar también porque provoca abortos e infecciones bacterianas secundarias, de manera que el costo de los productos se eleva y el manejo de los animales para controlar el parasitismo se dificulta.3,4 La prevalencia de la infección por F. hepatica ha aumentado debido al cambio climático, el aumento del movimiento de animales y el cambio en las prácticas ganaderas. En las granjas, se requieren mejorar las estrategias de control de esta parasitosis para disminuir la resistencia farmacológica por el uso constante de medicamentos.5
El control de este parásito se ha basado en la aplicación de fasciolicidas en el huésped definitivo.6 El control se lleva a cabo entre otros productos por benzimidazoles, como el albendazol; este tiene un amplio espectro de actividad contra trematodos, pero su actividad se restringe al parásito maduro, y requiere dosis altas.7 Otro fármaco es el triclabendazol, muy eficaz contra trematodos adultos y juveniles.8 Por otra parte, debido a que los animales han desarrollado resistencia parasitaria, la eficacia de algunos fármacos químicos como el triclabendazol (TCBZ), el closantel y el clorsulón en el ganado ovino y bovino contra los parásitos inmaduros y adultos ha disminuido.9,10 Sin embargo, desde 1983, cuando se lanzó al mercado el triclabendazol, la industria farmacéutica ha introducido varios fasciolicidas, algunos se importan y son costosos. Por lo que es necesario buscar alternativas sobre el desarrollo de nuevos fármacos para el control de esta importante enfermedad parasitaria.
En México, este trematodo se encuentra principalmente en animales de pastoreo (ovinos y bovinos).11 A principios de los 90, el compuesto Fasciolinip-1 (2-amino-5(6)-cloro-1-metoxicarbonilbenzimidazol), precursor del compuesto alfa, eliminaba las fasciolas de ocho semanas en un número limitado, y las de 12 semanas en un 90.6 % en ovinos.12 Posteriormente, el compuesto alfa (5-cloro-2-(metiltio)-6-(1-naftiloxi)-1H-benzimidazol) mostró alta eficacia contra F. hepatica inmadura y adulta en diferentes infecciones naturales o artificiales en terneros, ovejas y bovinos, similar al del TCBZ.13-15 Al igual que otros benzimidazoles, el compuesto alfa es poco soluble en disolventes acuosos, lo que supone el mayor impedimento para su administración vía intramuscular u otras vías.16
Recientemente (2017), se sintetizó el profármaco hidrosoluble del compuesto alfa mediante la adición de un grupo fosfonooximetilo con el fin de mejorar su solubilidad (13 mg/mL a pH = 7) y disponibilidad por hidrólisis in vivo por fosfatasas alcalinas en diferentes tejidos. Esto favorece la administración parenteral a dosis reducida. Esta sal disódica de fosfato demostró una eficacia del 87.8 % frente a parásitos adultos en ovejas infectadas artificialmente utilizando una dosis intramuscular de 4 mg/kg en comparación con la reportada para el compuesto alfa, que tuvo una eficacia del 86.9 % a una dosis de 15 mg/kg vía oral.17 También recientemente (2017), se ha informado de un nuevo profármaco hidrosoluble del TCBZ. Este profármaco era 88 000 veces más soluble que el TCBZ y presentaba una eficacia cercana al 100 % en ovejas infectadas artificialmente con una dosis intramuscular de 8 mg/kg.18 Sin embargo, para su uso clínico en animales, es necesario realizar estudios de toxicidad para determinar la seguridad de los nuevos profármacos.
Por otro lado, la toxicidad aguda y subaguda se basan en la determinación de la toxicidad tras una única administración y la administración repetida del fármaco. Ambas pruebas consideran los siguientes parámetros: mortalidad, signos de toxicidad, histopatología y cambio de peso de acuerdo con las directrices de la Organización para la Cooperación y el Desarrollo Económico (OCDE). Las guías estipuladas por la OCDE regulan la uniformidad de los ensayos biológicos tanto in vivo como in vitro para distintos fines, garantizando la calidad y la efectividad de los resultados obtenidos a nivel mundial. No obstante, en México no se han realizado estudios de toxicidad de estos nuevos compuestos fasciolicidas. Por lo tanto, el objetivo de este estudio fue evaluar la toxicidad aguda y subaguda del compuesto alfa inyectable en ratas de experimentación, para conocer la seguridad de este compuesto fasciolicida.
Material y métodos
Declaración ética
Los protocolos de experimentación con animales fueron aprobados por el Comité Institucional para el Cuidado y Uso de Animales de Laboratorio (CICUAL) de la Facultad de Química de la UNAM (número FQ/CICUAL/165/16 y FQ/CICUAL/204/17). El estudio siguió las normas nacionales e internacionales de bienestar y cuidado de los animales.
Animales
En los estudios de toxicidad aguda, se utilizaron 18 ratas hembras y en la toxicidad subaguda se utilizaron 24 hembras y 24 machos Hsd Han: WIST, de 8 a 10 semanas de edad, las cuales fueron obtenidas de la empresa ENVIGO-México, (EUA). Todas las ratas fueron identificadas mediante muescas en las orejas y alojadas en cajas de polisulfonato con las siguientes dimensiones: 26.03 × 47.62 × 20.32 cm. Se utilizó cama de viruta de pino, las condiciones ambientales de temperatura, humedad relativa y ciclo de luz/oscuridad fueron de 22 ±2 ºC, 40-60 % y 12/12 h dentro de la Unidad de Experimentación Animal (UNEXA) y en la Unidad de Investigación Preclínica (UNIPREC) de la Facultad de Química, Conjunto E de la Universidad Nacional Autónoma de México (UNAM) de acuerdo con la NOM062-ZOO-1999 de Especificaciones Técnicas para la Producción, Cuidado y Uso de Animales de Laboratorio.
Todas las ratas fueron alimentadas con alimento Harlan Teklad 2018S para ratón/rata y con agua filtrada ad libitum para el estudio de toxicidad aguda y 500 mL cada una durante tres o cuatro días en el caso de toxicidad subaguda mediante un módulo de sanitización automático durante todo el estudio. Las ratas fueron aclimatadas durante cinco días antes del tratamiento, en este periodo se observó su estado de salud, y fueron aleatorizadas para cada grupo experimental. Los protocolos de uso de animales experimentales fueron aprobados por el CICUAL de la Facultad de Química de la UNAM.
Síntesis del compuesto alfa
El compuesto alfa inyectable fue sintetizado en el Departamento de Farmacia de la Facultad de Química, de la Universidad Nacional Autónoma de México de acuerdo con la metodología de Flores-Ramos et al. (2014).17
Estudio de toxicidad aguda
La prueba de toxicidad aguda se llevó a cabo de acuerdo con la Guía de la Organización para la Cooperación y el Desarrollo Económico (OCDE, No. 423). Esta guía recomienda utilizar una serie de dosis superiores a las recomendadas hasta una dosis máxima de 2 000 mg/kg de peso corporal. Aunque la dosis recomendada para este fasciolicida inyectable es de 4 mg/kg de peso corporal en rumiantes,17 se utilizaron seis grupos de tres ratas nulíparas no preñadas. Las dosis utilizadas del compuesto alfa fueron 2 000 (grupo 1), 1 000 (grupo 2), 500 (grupo 3), 100 (grupo 4) y 10 (grupo 5) mg/kg de peso corporal diluidas en agua estéril y fueron inoculadas vía intramuscular. Por último, el grupo 6 (grupo control) fue inoculado vía intramuscular con agua estéril. Se observó a los animales de forma individual durante los primeros 30 minutos después de la inoculación y, después, se les monitoreó periódicamente durante las primeras cuatro horas. Se revisaron a las 24 horas y, luego, diariamente durante 14 días. Se documentó el patrón de comportamiento, los signos de toxicidad (temblores, convulsiones, salivación, diarrea, letargo y coma) y la mortalidad.
Estudio de toxicidad subaguda
Las pruebas de toxicidad subaguda se apegaron al parámetro de 28 días de duración, de acuerdo con la Guidance for Industry Target Animal Safety for Veterinary Pharmaceutical Products (No. 185, Food and Drug Administration, FDA) y la Guía N° 407 de la OCDE. Se utilizaron 24 hembras y 24 machos, ambos géneros de ratas se agruparon en cuatro grupos con seis animales cada uno. Los grupos experimentales fueron tratados vía intramuscular con el compuesto alfa a 8 mg/kg (grupo 1), 24 mg/kg (grupo 2) y 40 mg/kg (grupo 3) de peso corporal los días 0, 7 y 14, respectivamente.
A los animales del grupo control (grupo 4) se les inoculó con agua estéril. Se observaron los parámetros de bienestar (patrón de comportamiento, signos de toxicidad como temblores, convulsiones, salivación, diarrea, letargo, coma y mortalidad) de los animales durante los primeros 30 minutos, y a las 4 y 24 horas después de cada inoculación, luego, diariamente durante los 28 días. Se registró el peso corporal, la ingesta de alimento y el agua de acuerdo con las siguientes ecuaciones:
Análisis bioquímico del suero y estudio hematológico
Se tomaron muestras sanguíneas de cada animal a los 0 y 14 días después del tratamiento en la prueba de toxicidad aguda y, para la prueba de toxicidad subaguda, se tomaron muestras de sangre a los 0, 14 y 28 días, respectivamente. Para ambos estudios se utilizó la misma metodología. Cada muestra de sangre (600 µL) se obtuvo de forma humanitaria a partir de la punción del plexo retrorbital con la ayuda de un tubo capilar, bajo anestesia con isoflurano (5 %) utilizando una máquina de anestesia (VET EQUIP IMPAC6). La muestra fue depositada en dos tubos: con (EDTA) y sin anticoagulante, para los estudios bioquímicos y hematológicos. Se determinaron los parámetros bioquímicos séricos, como la glucosa, el nitrógeno ureico en sangre (NUS), la creatinina, el colesterol total, los triglicéridos, la alanina aminotransferasa (ALT), la aspartato aminotransferasa (AST), la fosfatasa alcalina, las proteínas totales, la urea y la bilirrubina total.
Los parámetros hematológicos, como el hematocrito (HCT), la hemoglobina (HGB), el recuento de eritrocitos (RBC), el volumen corpuscular medio (MCV), la concentración media de hemoglobina corpuscular (MCHC), el recuento de plaquetas (PLT), el recuento de leucocitos (LE), los neutrófilos (NE), los linfocitos (LY), los monocitos (MO) y los eosinófilos (EO), se midieron utilizando un analizador bioquímico automatizado (CS-T240, modelo DIRUI) y un analizador hematológico (S. MBC VET, modelo KONTRO Lab).
Análisis patológico
Después de concluidas las pruebas de toxicidad aguda y subaguda, los animales de cada estudio fueron eutanasiados mediante la exposición de dióxido de carbono (CO2) en una cámara de eutanasia. La muerte de los animales se verificó por la ausencia de signos vitales. Se realizaron las necropsias para observar la presencia o ausencia de cambios en la piel y el músculo (sitio de inoculación). Se recolectaron muestras de cerebro, corazón, pulmón, hígado, bazo, riñón y glándulas suprarrenales de los animales para realizar el examen histopatológico. Previamente, los tejidos se fijaron en solución de formol al 10 % (pH = 7), se deshidrataron y se incluyeron en parafina utilizando un histoquinette y el incluidor de parafina (Leica modelo TP 1020 y Leica EG 1150 H y EG 1150 C). Después, se obtuvieron cortes de 4-6 µm con ayuda de un micrótomo (Leica RM 2125 RTS) y se tiñeron con hematoxilina y eosina (H&E) para ser analizados bajo microscopía óptica.
Análisis estadístico
El análisis estadístico se llevó a cabo con el software SIGMA PLOT 13. El porcentaje de cambio de peso corporal, el consumo de alimentos y la ingesta de agua, así como los parámetros bioquímicos y hematológicos del suero se realizaron mediante la prueba estadística de ANOVA (análisis de varianza) de una vía, la prueba t de Student y la prueba de comparación múltiple de Tukey para las diferentes dosis en los grupos tratados en comparación con el grupo control. Todos los análisis se elaboraron con un nivel de confianza del 95 % (P ≤ 0.05).
Resultados
Toxicidad aguda
En esta prueba de toxicidad del compuesto alfa, no se pudo realizar el análisis estadístico de los parámetros peso y bioquímica sanguínea debido a la mortalidad de dos animales en el grupo inoculado con 2 000 mg/kg y un animal en el grupo de 1 000 mg/kg, ya que como se menciona en la guía, una vez que el animal muere, la prueba refiere que el compuesto es tóxico a la dosis donde se presenta la muerte. Los signos de toxicidad, la patología y el cambio de peso no se realizaron por la falta de estos datos. No se hizo ninguna necropsia en estos animales, pues su muerte se produjo después de 48 h postratamiento durante la noche, y ya había signos de descomposición, además de que se desconoce la hora exacta de la muerte. El análisis histopatológico no mostró cambios aparentes de peso corporal en los demás animales inoculados con las dosis de 2 000 (grupo 1), 1 000 (grupo 2), 500 (grupo 3), 100 (grupo 4) y 10 (grupo 5) mg/kg. Los órganos recolectados como el músculo, el cerebro, el corazón, el pulmón, el hígado, el bazo y las glándulas suprarrenales no tuvieron cambios histomorfológicos aparentes comparados con el grupo control. El tejido renal de los grupos tratados arrojó una morfología celular normal, similar a la del grupo control (Figura 1).
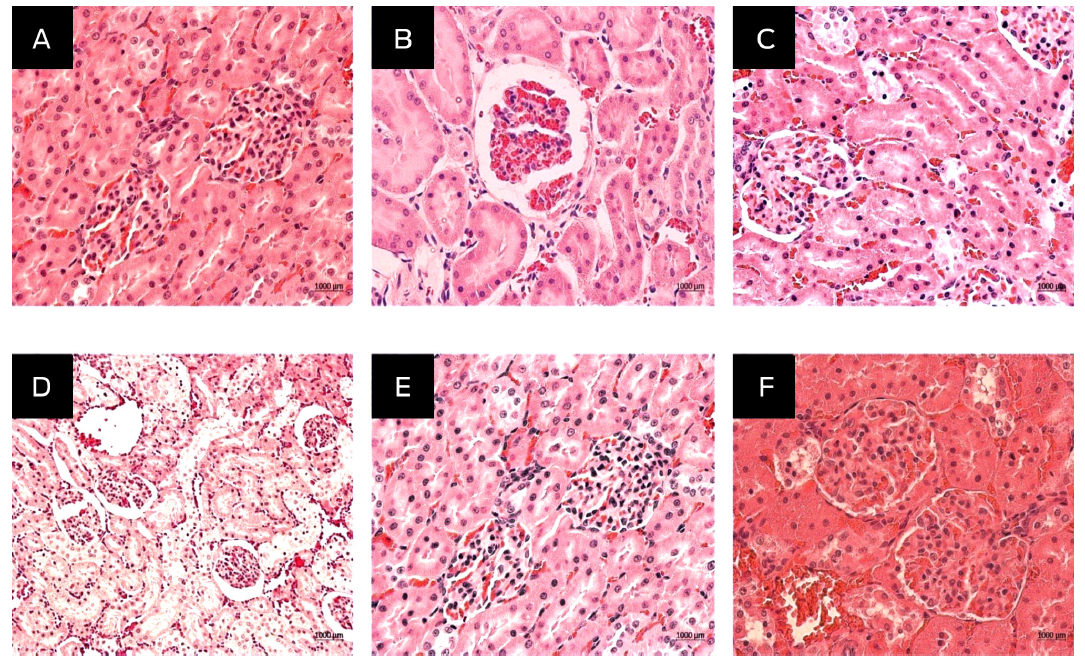
Figura 1 Hallazgo histopatológico en la toxicidad aguda del compuesto alfa inyectable en el riñón de ratas Hsd Han: WIST inoculadas con 2 000 (A), 1 000 (B), 500 (C), 100 (D) y 10 (E) mg/kg de peso corporal de compuesto alfa inyectable y grupo control (F). Las secciones histológicas se tiñeron con H & E y se observaron a 40X.
Toxicidad subaguda
En la Figura 2A, se observó el porcentaje de cambio de peso corporal en ratas hembras Wistar para los grupos dosificados con 8 (grupo 1), 24 (grupo 2), 40 (grupo 3) mg/kg de peso corporal del compuesto alfa y agua inyectable (grupo 4). Se observaron cambios en el porcentaje de peso corporal del grupo 2 (24 mg/kg), aunque no se encontraron diferencias significativas en el peso corporal entre los grupos experimentales (Kruskal-Wallis: Hg.l = 3; 0.05 = 1.9; P = 0.5930)
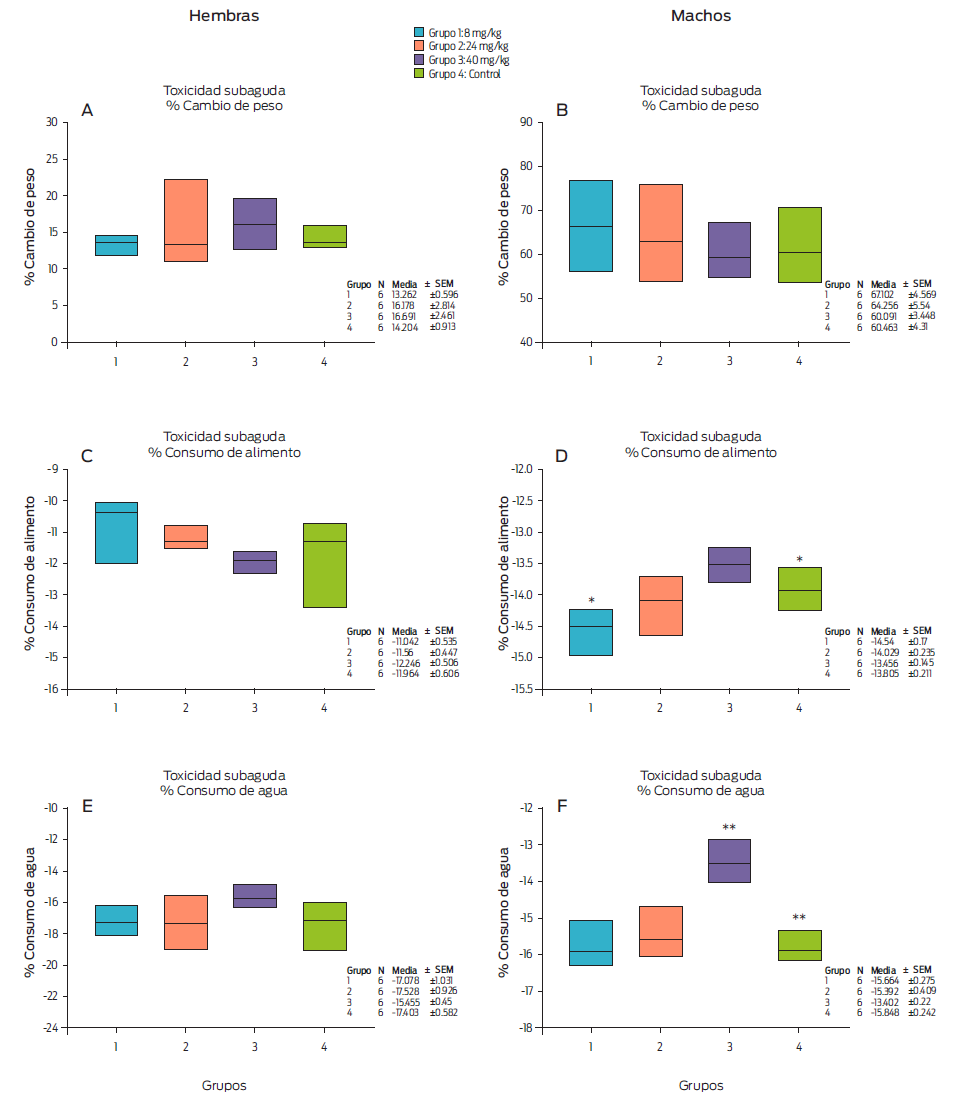
Figura 2 Efecto del compuesto alfa en la toxicidad subaguda de 28 días sobre el porcentaje de peso corporal, el consumo de alimentos y la ingesta de agua de ratas hembras y machos Hsd Han: WISTAR. * Significación estadística (Kruskal-Wallis: Hg.l. = 3; 0.05 = 14.102; P = 0.0030); **Diferencias estadísticas entre los grupos 4 y 3 (P ≤ 0.0010).
En los machos (Figura 2-B), el porcentaje en el peso corporal cambió ligeramente en los grupos 1 (8 mg/kg) y 2 (24 mg/kg), mientras que, no se encontraron diferencias estadísticamente significativas entre los grupos (F = 0.541, P = 0.663).
En las Figuras 2C y D, se muestra el consumo de alimento en el grupo tratado de hembras (seis ratas por grupo) y en el grupo de machos (seis ratas por grupo) en comparación con el grupo control (seis ratas, sin tratamiento). En las hembras, el porcentaje de consumo de alimento se calculó con la siguiente ecuación.
El grupo 4 (agua inyectable) presentó un cambio (Figura 2C), pero no una diferencia estadística con los grupos en tratamiento (Kruskal-Wallis: Hg.l. 3; 0.05 = 7.55; P = 0.0560). Sin embargo, se observó una tendencia similar en el consumo de alimentos entre el 11 y el 12 por ciento.
En los machos (Figura 2D), se observó una diferencia significativa en el grupo 3 (40 mg/kg) en comparación con el grupo 1 (8 mg/kg) (Kruskal-Wallis: Hg.l. = 3; 0.05 = 14.102; P = 0.0030). Asimismo, se hallaron diferencias significativas entre el grupo 1 (8 mg/kg) (P = 0.0170), el grupo 2 (24 mg/kg) (P = 0.4420) y el grupo 3 (40 mg/kg) (P = 0.0650) en comparación con el grupo control (agua inyectable). El análisis estadístico indicó que había una diferencia entre el grupo 1 (8 mg/kg) y el grupo 4 (agua inyectable), teniendo en cuenta que el rango de cambio del porcentaje de consumo de alimentos en todos los grupos era similar (13-14 %).
En la Figura 2E, se observa un incremento en el consumo de alimento, pero no se encontraron diferencias estadísticas entre los grupos en las ratas hembras (P = 0.2370). No obstante, el consumo de agua fue similar en todos los grupos (15-17 %), aunque se observaron diferencias estadísticamente significativas en los machos (Figura 2F). Sí hubo diferencias en el grupo 3 en comparación con los otros grupos (P ˂ 0.001).
Se realizó una prueba de Student para conocer las diferencias estadísticas entre los grupos 3 y 4 (P ≤ 0.001). En los demás grupos no hubo diferencias significativas. Considerar que la ingesta de agua en los grupos 1, 2 y 4 fue alrededor de 15 %, mientras que el grupo 3 la redujo a 13 %. Por lo tanto, el consumo de agua y la comida no afectó al peso corporal en todos los grupos. No se observaron cambios aparentes en los hallazgos histológicos de los músculos y órganos analizados tanto de los animales tratados como del grupo control. En el examen histopatológico, la estructura morfológica del riñón fue normal (Figura 3).
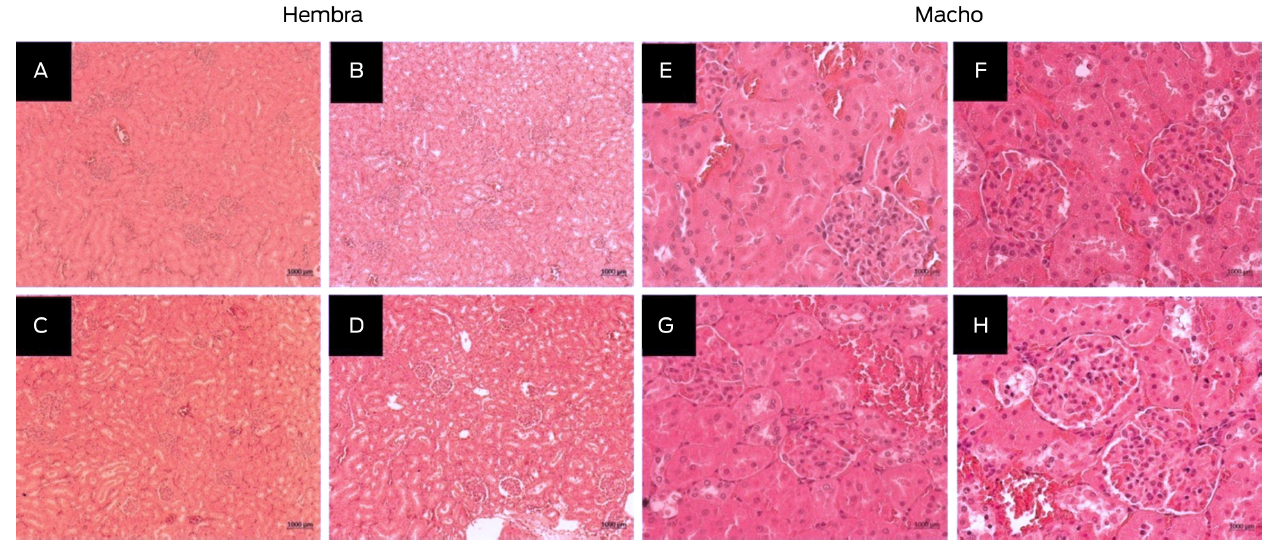
Figura 3 Hallazgo histológico en la toxicidad subaguda del riñón de ratas hembra (A, B, C y D) y ratas macho (E, F, G y H) Hsd Han: WISTAR inoculados con 8 (A, E), 24 (B, F), 40 (C, G) mg/kg por peso corporal del compuesto alfa y el grupo control (D, H; agua inyectable). A los cortes histológicos se les tiñó con H & E y fueron observados a 10X y 40X.
El efecto del tratamiento del compuesto alfa sobre los parámetros bioquímicos del suero se observan en el Cuadro 1. Se encontró una diferencia estadística con el analito de glucosa entre los grupos 1 y 2, comparados con el grupo 3 usando una ANOVA de una vía (P = 0.001) de acuerdo con la siguiente ecuación:
Cuadro 1 Resultados de los parámetros bioquímicos del suero en el estudio de toxicidad subaguda en ratas hembra Hsd Han: WISTAR
| Parámetros | Hembras | |||
| Media ± SEM | ||||
| Grupo 1
(8 mg/kg) |
Grupo 2
(24 mg/kg) |
Grupo 3
(40 mg/kg) |
Grupo 4
(Control) |
|
| Glucosa (mmol/L) | -25.88 ±1.43* | -17.60 ±5.41* | -13.19 ±7.13* | 11.22 ±6.78 |
| NUS (mmol/L) | 17.72 ±7.83 | 17.36 ±9.59 | 17.30 ±6.76 | 1.36 ±4.75 |
| Creatinina (mmol/L) | 2.30 ±3.77 | -0.29 ± 2.2 | 2.55 ±3.64 | -6.70 ±4.49 |
| Colesterol (mmol/L) | -9.85 ±2.54** | 0.68 ±3.77 | 1.55 ±4.49 | 5.92 ±1.94 |
| Triglicéridos (mmol/L) | -39.89 ±10.34 | 12.11 ±13.32 | 11.99 ±23.69 | 37.45 ±24.85 |
| ALT (U/L) | 2.13 ±8.05 | 8.41 ±7.51 | 12.61 ±11.13 | 19.65 ±9.81 |
| AST (U/L) | 0.80 ±7.95 | -8.77 ±11.82 | 20.36 ±11.67 | 9.58 ±15.23 |
| ALP (U/L) | -15.2 ±2.74 | -15.63 ±4.82 | -25.51 ±4.68 | -4.27 ±6.77 |
| Proteínas (mmol/L) | 3.47 ±1.61 | 2.89 ±3.12 | 7.59 ±2.2 | 4.70 ±2.35 |
| Urea (mmol/L) | 20.23 ±7.22 | 18.76 ±9.7 | 16.27 ±6.05 | 1.28 ±5.67 |
| Bilirrubinas (mmol/L) | 35.97 ±25.92 | 12.31 ±14.89 | 71.15 ±30.83 | 16.11 ±12.74 |
NUS= nitrógeno ureico en sangre; ALT= alanina aminotransferasa; AST= aspartato aminotransferasa; ALP= fosfatasa alcalina, grupo tratado con 8 mg/kg (grupo 1); 24 mg/kg (grupo 2); 40 mg/kg (grupo 3) mg/kg por peso corporal; agua inyectable (grupo control); *Diferencia estadística por ANOVA de una vía en glucosa (P = 0.001); **Significancia estadística por ANOVA de una vía en colesterol (P = 0.0220) en ratas hembra.
Para corroborar esta diferencia, la prueba de Tukey mostró una diferencia estadística entre los grupos 1, 2 y 3 en comparación con el grupo 4. Además, el colesterol fue significativo en dos grupos: el 1 y el grupo control, mediante la prueba de Tukey (P = 0.0220). En cambio, en el Cuadro 2, no se halló ninguna diferencia estadística en las ratas macho.
Cuadro 2 Resultados de los parámetros bioquímicos del suero en el estudio de toxicidad subaguda en ratas macho Hsd Han: WISTAR
| Parámetros | Machos | |||
| Media ± SEM | ||||
| Grupo 1
(8 mg/kg) |
Grupo 2
(24 mg/kg) |
Grupo 3
(40 mg/kg) |
Grupo 4
(Control) |
|
| Glucosa (mmol/L) | -6.48 ±3.01 | -12.78 ±4.88 | 5.98 ±8.7 | 2.02 ±5.75 |
| NUS (mmol/L) | 3.99 ±3.19 | 3.7 ±2.25 | 1.32 ±2.18 | -2.41 ±6.36 |
| Creatinina (mmol/L) | 7.06 ±3.9 | 4.77 ±3.98 | 6.26 ±4.12 | 6.81 ±4.06 |
| Colesterol (mmol/L) | -18.10 ±1.99 | -16.31 ±2.32 | -21.46 ±1.84 | -11.72 ±3.76 |
| Triglicéridos (mmol/L) | 29.35 ±10.35 | 48.26 ±14.84 | 47.80 ±18.93 | 73.59 ±24.83 |
| ALT (U/L) | -2.67 ±3.54 | -6.80 ±4.47 | -14.27 ±2.27 | -8.09 ±5.93 |
| AST (U/L) | -17.65 ±3.7 | -7.75 ±10.52 | -14.21 ±3.82 | -10.92 ±5.29 |
| ALP (U/L) | -31.80 ±1.27 | -29.29 ±3.21 | -37.17 ±2.21 | -36.09 ±2.37 |
| Proteínas (mmol/L) | 7.79 ±2.49 | 8.18 ±1.94 | 4.61 ±0.61 | 7.3 ±1.03 |
| Urea (mmol/L) | 4.16 ±4.51 | 3.85 ±2.88 | 1.31 ±1.92 | -2.73 ±5.63 |
| Bilirrubinas (mmol/L) | 13.18 ±7.44 | 11.40 ±15.7 | 23.67 ±17.66 | 15.99 ±7.96 |
NUS= nitrógeno ureico en sangre; ALT= alanina aminotransferasa; AST= aspartato aminotransferasa; ALP= fosfatasa alcalina, grupo tratado con 8 mg/kg (grupo 1); 24 mg/kg (grupo 2); 40 mg/kg (grupo 3) por peso corporal; agua inyectable (grupo control).
En el Cuadro 3, se observan las diferencias estadísticas en los análisis hematológicos de las hembras. Hay cambios en el hematocrito en las ratas hembra en los grupos tratados con 8 mg/kg, 24 mg/kg y 40 mg/kg en comparación con el grupo control, así como en el recuento de plaquetas (grupos: 24 mg/kg y control), lo que muestra una diferencia estadística por medio de una ANOVA de una vía (P = 0.0370), y la prueba de Tukey corroboró esta diferencia (P = 0.0110).
Cuadro 3 Resultados de los parámetros hematológicos en el estudio de toxicidad subaguda en ratas hembras Hsd Han: WISTAR
| Parámetros | Hembras | |||
| Media ± SEM | ||||
| Grupo 1
(8 mg/kg) |
Grupo 2
(24 mg/kg) |
Grupo 3
(40 mg/kg) |
Grupo 4
(control) |
|
| HCT (L/L) | 9.92 ±1.66* | 12.09 ±3* | 8.52 ±0.38* | 1.33 ±1.33 |
| HGB (g/L) | 7.38 ±1.12 | 5.30 ±2.09 | 8.59 ±1.17 | 3.89 ±2.04 |
| RBC (×1012/L) | 19.03 ±5.57 | 26.74 ±6.89 | 24.91 ±4.5 | 21.62 ±2.81 |
| MCV (fL) | -6.65 ±4.23 | -10.54 ±4.59 | -12.82 ±3.08 | -13.57 ±1.28 |
| MCHC (g/L) | -2.49 ±1.07 | 6.143 ±2.28 | 6.02 ±6.04 | -0.57 ±1.55 |
| PL (×109/L) | 57.47 ±27.77 | 75.15 ±25.65* | -23.46 ±14.33 | -3.40 ±15.28 |
| LE (×109/L) | -35.18 ±4.58 | -30.14 ±13.26 | -22.34 ±10.97 | -27.68 ±9.7 |
| NE (×109/L) | 9.91 ±33.59 | -36.27 ±21.75 | -19.98 ±30.04 | -14.96 ±35.14 |
| LY (×109/L) | -37.55 ±5.82 | -29.14 ±12.53 | -20.11 ±13.03 | -25.75 ±10.07 |
| MO (×109/L) | -11.67 ±17.97 | 11.67 ±4.01 | -3.33 ±19.94 | -16.67 ±16.67 |
| EO (×109/L) | -33.33 ±21.08 | -50.0 ±22.36 | -15.0 ±17.08 | -45 ±24.73 |
HCT= hematocrito; HGB= hemoglobina; RBC= conteo de eritrocitos; MCV= volumen medio corpuscular; MCHC= concentración media de hemoglobina corpuscular; PL= conteo de plaquetas; LE= conteo de leucocitos; NE= neutrófilos; LY= linfocitos; MO= monocitos; EO= eosinófilos; *Diferencia estadística por una ANOVA de una vía en HCT (P = 0.0370) y en el conteo de plaquetas (P = 0.0110) en ratas hembra; **Significancia estadística por ANOVA de una vía en RBC (P = 0.0200) y MCV (P = 0.0120) en ratas hembra.
En el Cuadro 4, se ve como el RBC y el MCV fueron significativamente diferentes entre los grupos 1 y 3 en comparación con el grupo control en ratas macho por una ANOVA de una vía (P = 0.0200 y P = 0.0120), además también lo verificó la prueba de Tukey.
Cuadro 4 Resultados de los parámetros hematológicos en el estudio de toxicidad subaguda en ratas macho Hsd Han: WISTAR
| Parámetros | Machos | |||
| Media ± SEM | ||||
| Grupo 1
(8 mg/kg) |
Grupo 2
(24 mg/kg) |
Grupo 3
(40 mg/kg) |
Grupo 4
(control) |
|
| HCT (L/L) | 9.43±1.86 | 10.64±1.57 | 12.38±3.06 | 9.90±1.43 |
| HGB (g/L) | 12.01±1.80 | 14.64±1.40 | 13.95±1.56 | 13.34±1.37 |
| RBC (×1012/L) | 49.85±5.71** | 40.57±4.91 | 50.71±7.59** | 23.61±6.36 |
| MCV (fL) | -27.07±2.60** | -20.75±2.89 | -25.41±2.34** | -9.02±5.93 |
| MCHC (g/L) | 3.19±2.07 | 3.93±1.50 | 1.84±1.89 | 2.94±1.36 |
| PL (×109/L) | 23.53±35.59 | 8.35±11.39 | -15.01±6.34 | -2.27±8.26 |
| LE (×109/L) | -4.53±17.66 | 14.62±20.04 | -25.76±7.20 | -25.51±6.93 |
| NE (×109/L) | 14.07±39.65 | 51.81±26.79 | -2.88±29.65 | -18.36±19.01 |
| LY (×109/L) | -0.70±17.69 | 18.59±22.3 | -26.44±6.74 | -25.57±6.79 |
| MO (×109/L) | -94.44±5.56 | -66.67±21.08 | -46.67±23.90 | -50.0±22.36 |
| EO (×109/L) | -11.67±17.97 | -16.67±16.67 | -33.33±33.33 | -15.0±17.08 |
HCT= hematocrito; HGB= hemoglobina; RBC= conteo de eritrocitos; MCV= volumen medio corpuscular; MCHC= concentración media de hemoglobina corpuscular; PL= conteo de plaquetas; LE= conteo de leucocitos; NE= neutrófilos; LY= linfocitos; MO= monocitos; EO= eosinófilos; **Significancia estadística por ANOVA de una vía en RBC (P = 0.0200) y MCV (P = 0.0120) en ratas macho.
Discusión
En la toxicidad aguda hubo tres muertes, que se presentaron en los grupos 1 (2 000 mg/kg) y 2 (1 000 mg/kg), se produjeron después de 48 h postratamiento. La guía de la OCDE 423 menciona que debido a las muertes, se deberá experimentar para encontrar la dosis letal, debido a que las muertes se presentaron en las dosis más altas, posiblemente la dosis letal se encuentre dentro de las dosis de 2 000 y 1 000 mg/kg. Para la toxicidad subaguda, se decidió utilizar la dosis de 40 mg/kg, que representa 10 veces la dosis recomendada (4 mg/kg).
En el estudio hematológico en la prueba de toxicidad subaguda del compuesto alfa inyectable, cuatro de estos parámetros mostraron diferencias estadísticas (P ˂ 0.01) en comparación con el grupo control. Sin embargo, estos valores están dentro de los valores normales según la literatura. Estas variaciones pueden estar afectadas por las fluctuaciones normales de todos los grupos tratados. Por lo tanto, esto sugiere que el compuesto inyectable alfa no mostró toxicidad en el sistema hematopoyético.Los valores bajos de glucosa y colesterol fueron estadísticamente diferentes en la prueba bioquímica sérica en las hembras, aunque estaban en rangos normales. Otro estudio presentó valores elevados en estos analitos en comparación con el grupo control, aunque estos valores también se encontraban dentro de los valores normales.19,20 En los machos tratados no hubo diferencias en estos analitos.
En el examen histopatológico, las lesiones comunes halladas en la prueba subaguda fueron cambios intersticiales, congestión, hemorragias e infiltración de células inflamatorias.21,22 A pesar de ello, en este estudio de toxicidad aguda no hubo cambios en músculo, cerebro, corazón, pulmón, bazo, hígado, riñón y glándulas suprarrenales. Tampoco cambió la estructura celular, ni en los otros mencionados anteriormente, relacionados con el análisis bioquímico del suero. Finalmente, el compuesto alfa inyectable se perfila como una futura alternativa fasciolicida para el control de la fasciolosis en rumiantes. No obstante, es necesario llevar a cabo estudios adicionales para conocer la dosis letal, corroborar su eficacia en pruebas de gabinete y campo, verificar su tolerancia, el índice de seguridad y el período de retención en rumiantes, a fin de comprobar su verdadero potencial fasciolicida en las especies destino.
Conclusiones
El compuesto alfa inyectable administrado vía intramuscular a ratas Hsd Han: Wistar no produjo cambios importantes en los análisis bioquímicos del suero, la hematología y la estructura histomorfológica en la toxicidad subaguda, al compararlo con los datos señalados en la literatura. La información obtenida sirve como datos preliminares para indicar que el compuesto tiene un amplio margen de seguridad.
Agradecimientos
Los autores desean agradecer a la Unidad de Investigación Preclínica (UNIPREC) por su permiso para utilizar sus instalaciones y a MVZ Lucía Macías Rosales, MC Claudia P. Rico Torres y al Dr. Miguel Ángel Flores Ramos por su excelente apoyo técnico.
Financiamiento
Esta investigación fue financiada por la Universidad Nacional Autónoma de México (www.unam.mx), beca PAPIIT DGAPA-UNAM RT201015, otorgada a F. Ibarra-Velarde. El financiador no tuvo ningún papel en el diseño del estudio, la recopilación y el análisis de datos, la decisión de publicar o la preparación del manuscrito.
Conflicto de interés
Los autores no tienen ningún conflicto de intereses que declarar en relación con esta publicación.
Contribuciones de los autores
Conceptualización: A. Zapata-Arenas, F. Ibarra-Velarde.
Curación de datos: A. Zapata-Arenas, F. Ibarra-Velarde.
Análisis formal: A. Zapata-Arenas, F. Ibarra-Velarde.
Adquisición de fondos: F. Ibarra-Velarde.
Investigación: A. Zapata-Arenas.
Metodología: A. Zapata-Arenas, R. Castillo, J. Ramírez-Lezama, H. Rico-Morales, R. Bustamante-García.
Administración del proyecto: A. Zapata-Arenas, F. Ibarra-Velarde.
Recursos: F. Ibarra-Velarde, I. Gracia-Mora.
Software: R. Bustamante-García.
Supervisión: F. Ibarra-Velarde, I. Gracia-Mora.
Validación: A. Zapata-Arenas.
Visualization: F. Ibarra-Velarde, I. Gracia-Mora.
Redacción-borrador original: A. Zapata-Arenas.
Redacción-revisión y edición: A. Zapata-Arenas, F. Iarra-Velarde, R. Bustamante-García, R. Castillo, H. Rico-Morales.
Redacción-revisión y edición: A. Zapata-Arenas, F. Ibarra-Velarde, R. Bustamante-García, R. Castillo, H. Rico-Morales.











 texto en
texto en 



