Introducción
El grafeno y sus derivados, como el óxido de grafeno (OG), son materiales prometedores para su uso en el área de la salud, especialmente en la odontología (Bonilla-Represa et al., 2020). El OG, derivado de la oxidación del grafeno, se caracteriza por su espesor de aproximadamente 1 nm y longitud de 400-500 mm (Li et al., 2022). Este compuesto anfifílico contiene grupos epoxi, hidroxilo en los grupos basales y ácido carboxílico en los bordes, otorgándole una alta funcionalización y la capacidad de unirse a diferentes tipos de moléculas, especialmente biomoléculas (Lee et al., 2011).
Actualmente, se han hecho estudios sobre el uso del OG sobre la superficie de los implantes de Ti pues cuenta con excelentes propiedades físicas, químicas, es biocompatible, tiene actividad de diferenciación celular y presenta efectos antibacterianos (Srimaneepong et al., 2022; Williams et al., 2023). Se ha demostrado que el OG puede favorecer la proliferación de células troncales, la adhesión celular (Lee et al., 2011) y promover la formación de inserción periodontal con baja citotoxicidad (Kawamoto et al., 2018). Lo cual ha llevado a identificar y desarrollar diferentes formas de deposición de grafeno sobre la superficie de Ti de los implantes dentales, siendo una de las más usadas el dip-coating, técnica de recubrimiento por inmersión o capilaridad, en donde el sustrato se sumerge en una dispersión de OG y, posteriormente, se somete a 180 ºC para su secado y fijación (Tang y Yan, 2017; Inchingolo et al., 2023).
A pesar de que el Ti es el material preferido para los componentes transmucosos debido a su respuesta tisular favorable, un análisis de 11 estudios en una revisión sistemática reveló que, en un periodo de 18 años, la mucositis perimplantaria tenía una incidencia acumulada del 43%, mientras que la perimplantitis alcanzó el 22% (Derks y Tomasi, 2015), por lo tanto, asegurar una sólida y estable integración en la región transmucosa se convierte en un elemento esencial para preservar la salud y la funcionalidad a largo plazo de los implantes dentales (Ivanovski y Lee, 2018).
Aunque el tejido blando perimplantario comparte ciertas similitudes en términos de morfología y estructura con el tejido periodontal natural, existen diferencias sustanciales en varios aspectos. Estas diferencias incluyen la falta de un ligamento periodontal, la ausencia de cemento alrededor de los implantes dentales, la orientación diferencial de las fibras de colágeno, así como variaciones en el sistema inmunológico y la vascularización (Zheng et al., 2021). Estas distinciones ejercen un impacto significativo en el proceso de integración del tejido blando con la superficie del implante.
Con el propósito de afrontar este desafío, han emergido en el mercado pilares estéticos multiposición caracterizados por su diseño innovador, estos componentes han sido concebidos con el objetivo de lograr un sólido sellado biológico y fomentar un entorno adecuado para el tejido perimplantario (Andrukhov et al., 2020).
Se han desarrollado de manera extensa técnicas para modificar y optimizar la superficie de los implantes y pilares con el fin de influir en el comportamiento de los fibroblastos y las células epiteliales, así como en la orientación de las fibras de colágeno (Deng et al., 2022).
Una de estas técnicas es la anodización producida por una superficie que es más lisa, no porosa y nanoestructurada, con propiedades químicas y una topografía diseñada específicamente para estimular la adhesión del tejido blando (Mussano et al., 2018). Estudios recientes in vitro han sugerido el favorecer las superficies anodizadas el crecimiento inicial de fibroblastos y preosteoblastos, así como la adhesión de células epiteliales y fibroblastos (Teng et al., 2018).
El proceso de anodización es una técnica electroquímica en la cual se forma una fina película de óxido de forma controlada, esta capa anódica es una parte integral del metal y puede tener un espesor de hasta 100 micrómetros, convirtiéndola en una medida altamente efectiva en términos de protección. Los pilares con superficies anodizadas y nanoestructuradas no han mostrado un efecto significativo en la colonización bacteriana ni en la actividad proteolítica en comparación con las superficies de Ti mecanizadas convencionales (Hall et al., 2019).
El Ti es el material más utilizado, sin embargo, tiene una superficie relativamente inerte la cual limita su interacción con las células y los tejidos circundantes, por estas razones, se han propuesto diferentes estrategias para modificar la superficie del Ti y mejorar sus características biológicas. Una de las opciones más prometedoras es el uso del OG por su alta resistencia, su mayor solubilidad en agua y su mayor reactividad química (Liu, Y. et al., 2016).
El sellado tisular alrededor de los implantes de Ti se obtiene principalmente por una “adaptación” física de la mucosa perimplantaria, más que por la “integración” biológica alrededor del tejido natural, formando una barrera eficaz para proteger las estructuras subyacentes (Guo et al., 2021).
El sellado biológico alrededor de los aditamentos sobre implantes dentales es importante porque protegen el hueso y el implante de la contaminación bacteriana y la inflamación, ayuda a mantener la estabilidad del nivel óseo perimplantario y a prevenir la pérdida ósea y el fracaso del implante. Este sellado puede verse afectado por varios factores, como el material, la topografía y la química de la superficie del aditamento, el tipo de conexión entre el implante y el aditamento, y la calidad y cantidad de tejido blando perimplantario.
El recubrimiento de superficies de Ti con OG ofrece una serie de beneficios importantes en diversas aplicaciones, desde mejorar la resistencia mecánica y a la corrosión porque el OG forma una capa protectora sobre la superficie del titanio, ayudando a prevenir la corrosión y el desgate, aumentando la vida útil del material (Wan et al., 2022; Liu, J. et al., 2019). Aunado a las propiedades biológicas, como antibacterianas o respuesta celular, las cuales favorecerían su aplicación clínica (Kwak et al., 2022).
Por lo anterior, el objetivo de esta investigación es evaluar el efecto del tratamiento de superficie de aditamentos protésicos de Ti con OG sobre la integración y la estabilidad de las células que conforman los tejidos blandos perimplantarios. Se espera el aumento de la biocompatibilidad y adhesión celular en esta modificación superficial, lo cual se traducirá en una mayor supervivencia y éxito de los implantes dentales.
Materiales y métodos
El óxido de grafeno (OG) fue comprado en Sigma-Aldrich 2mg/mL en dispersión de agua. Lote 763705-25ML.
Muestras:
Se adquirieron por donación de la compañía Nobel Biocare 12 aditamentos protésicos de Ti anodizado On1 Base Xeal™ Conical Connection 1.75 mm. Las 12 muestras de aditamentos protésicos se separaron en 2 grupos: 6 muestras de aditamento protésico de Ti anodizados tratadas con OG (Ti-An-OG) y 6 muestras de aditamentos protésico de Ti anodizados no tratadas con OG (Ti-An).
Recubrimiento:
La superficie de los aditamentos protésicos anodizados se recubrió por medio de inmersión o dip-coating en una disolución de OG en agua durante 4 horas; se retiraron y secaron en un horno a 180 ºC durante 2 horas.
Caracterización:
Se caracterizó la película de OG sobre los aditamentos por medio de microscopía electrónica de barrido usando un microscopio electrónico de barrido de emisión de campo marca JEOL, modelo JSM7800F y resolución de 0.7 nm, usando electrones secundarios para la toma de la muestra y equipado con el detector de rayos X, para el análisis por espectroscopía por dispersión de rayos X-(EDS).
Para confirmar el recubrimiento se hizo un mapeo elemental para identificar la ubicación del carbono en el aditamento, principal constituyente del OG.
Ensayo de viabilidad celular
Se evaluó la adhesión celular por el ensayo WST-1 de los aditamentos protésicos de Ti anodizados con y sin recubrimiento de OG.
Para el estudio se usaron fibroblastos gingivales humanos (ATCC PCS-201-018) y se colocaron a una concentración de 1 × 104 células/ml sobre los aditamentos por triplicado por 24 y 48 horas. Este ensayo se basa en la capacidad de la succinato-tetrazolio reductasa mitocondrial de las células vivas para reducir la sal del WST−1 y producir el compuesto formazán. La concentración de formazán es directamente proporcional al número de células metabólicamente activas. Las células sembradas se incubaron con 400 μL de medio de cultivo fresco y 40 μL del reactivo WST−1 durante 4 horas 37 ºC. Posteriormente, se retiraron 200 μL del sobrenadante, y la absorbancia se midió a 545 nm con un lector de placas (ChroMate, Awareness Technology).
Resultado y discusión
En las imágenes de microscopía electrónica (Figuras 1A, y B), podemos observa el aditamento protésico de titanio anodizado en la Figura 1A, y en la Figura 1B, observar el aditamento protésico de titanio anodizado y recubierto con OG a diferentes amplificaciones.

Fuente: Elaboración de los autores.
Figura 1 A) Aditamento protésico de titanio. B) Aditamento protésico de titanio con una capa de recubrimiento de óxido de grafeno (OG) bajo microscopio electrónico de barrido de sobremesa JCM-6000 a 5 volts
En el aditamento sin recubrimiento se observa una superficie más lisa en comparación con la muestra recubierta donde se observa más rugosa por la presencia del OG.
Entre los diversos métodos disponibles para realizar la deposición de líquidos sobre grandes superficies, dip-coating es uno de los más usados. El método es sencillo y ofrece un excelente control del espesor final, permitiendo un recubrimiento más homogéneo. Las condiciones de procesamiento también pueden adaptarse para la deposición de todo tipo de materiales, incluyendo polímeros, cerámicos, biomoléculas y todo tipo de nanomateriales como en este proyecto en el cual se usó OG (Ceratti et al., 2015).
Los resultados coinciden con otras investigaciones donde lograron recubrir homogéneamente superficies con OG usando la metodología dip-coating (Jeon et al., 2014; Murugesan et al., 2023; Song et al., 2019).
En la Figura 2(A y B) se puede observar, por medio del mapeo elemental, que prácticamente hay presencia de C en toda la superficie y con el análisis de EDS se comprobó la presencia de Ti y C.

Fuente: Elaboración de los autores.
Figura 2 Mapeo elemental y EDS para determinar la presencia de grafeno, los puntos rojos indican la de grafeno y los círculos amarillos señalan las zonas del mapeo sobre la superficie del aditamento.
En la Figura 3A se observan los resultados obtenidos en la evaluación de adhesión celular sobre los aditamentos protésicos anodizados con y sin recubrimiento de OG, resultado estadísticamente significativo en la adhesión celular observando un incremento de esta propiedad en los aditamentos recubiertos con OG, y la Figura 3B muestra una microfotografía de las células adheridas sobre la superficie del aditamento, estos resultados son consistentes con otras publicaciones donde se observó una viabilidad significativa, sin respuesta citotóxica en células troncales derivadas de pulpa dental, de implantes dentales recubiertos con OG (Di Darlo et al., 2020), inclusive en otras superficies recubiertas con OG, se observó un incremento en la viabilidad celular (Park et al., 2022).
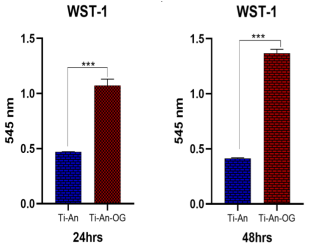
*** p < 0.001.
Fuente: Elaboración de los autores.
Figura 3 Evaluación de la adhesión celular sobre la superficie del aditamento protésico de titanio y sobre el aditamento con óxido de grafeno a los dos tiempos de experimentación, 24 y 48 horas.
Recubrir aditamentos dentales con OG puede ofrecer una serie de beneficios específicos para la odontología y la implantología dental. Desde mejorar su biocompatibilidad, reduciendo el riesgo de rechazo del cuerpo o un proceso inflamatorio (Huang et al., 2022) y promover una mejor integración con el tejido circundante (Kwak et al., 2022).
Al recubrir los aditamentos dentales con OG, se mejora la osteointegración al proporcionar una superficie favorecedora a la adhesión celular y el crecimiento óseo, como se demostró en este estudio, lo cual resulta en una mejor estabilidad y durabilidad del tratamiento.
Aunado a esto, las propiedades antibacterianas del OG ayudarían a prevenir infecciones asociadas con aditamentos dentales e implantes, al reducir la carga bacteriana en la superficie, disminuir el riesgo de complicaciones postoperatorias, y así, aumentar el éxito del tratamiento (Wang et al., 2023; Akshaya et al., 2022).
Los resultados permiten dar una idea del potencial del OG para favorecer la biocompatibilidad, viabilidad celular en superficies recubiertas con ese material, y, en el caso específico de la odontología y los implantes, aumentar la durabilidad y la probabilidad de éxito de los tratamientos (Di Carlo et al., 2020).
Conclusión
Con los resultados obtenidos se puede concluir que se lograron recubrir con éxito las superficies de los pilares de titanio anodizado con óxido de grafeno, demostrado por las imágenes de microscopía electrónica, mapeo elemental y EDS. El recubrimiento favoreció la adhesión celular, lo cual aumentaría la probabilidad de supervivencia de los implantes dentales, logrando una sólida integración de los tejidos blandos en la región transmucosa con los pilares protésicos.











 nueva página del texto (beta)
nueva página del texto (beta)


