Introducción
Los cálculos del conducto biliar suelen ser el resultado de la migración de cálculos biliares de la vesícula biliar al árbol biliar. Entre el 10 y el 20% de los pacientes que cursan con colelitiasis sintomática tienen coledocolitiasis concomitante, con un costo elevado para la salud pública americana; diversos estudios sugieren que cada episodio de coledocolitiasis resulta en un costo aproximado de 9,000 dólares1-3.
La coledocolitiasis es la principal causa de pancreatitis aguda, así como de colangitis, que pueden tener un desenlace incluso mortal en algunos pacientes. La colangiopancreatografía retrógrada endoscópica (CPRE) ha transformado la extracción de cálculos en el conducto biliar, de ser de una operación mayor a un procedimiento mínimamente invasivo2,4.
En este procedimiento se introduce un duodenoscopio por la boca y se avanza gentilmente a la segunda porción del duodeno, donde se encuentra el ámpula. Luego se cánula el árbol biliar a través de la ampolla, con una guía hidrofílica que sirve de férula para la introducción del catéter llamado esfinterotomo, compuesto además por un asa de alambre que brinda tracción y corte para realizar la esfinterotomía del esfínter de Oddi. Posterior al acceso del árbol biliar, se inyecta contraste para obtener una colangiografía, que permite la visualización del lumen biliar. El colangiograma nos muestra la anatomía del árbol biliar, además nos proporciona información de cuerpos alojados dentro del lumen biliar (defectos de llenado) así como la dilatación de este, situación que nos orientaría al diagnóstico de coledocolitiasis.
La piedra angular de la terapia endoscópica de coledocolitiasis es la esfinterotomía, ya que sirve para: extracción de los cálculos y reducción del riesgo de obstrucción por cálculos biliares recurrentes. La limpieza del conducto se puede lograr mediante el uso de un balón de extracción o un dispositivo tipo canasta. Las técnicas adicionales incluyen la litotricia mecánica, extracorpórea por ondas de choque e intraluminal por electrohidráulica o láser. La eliminación de cálculos del conducto biliar por este método se puede lograr con éxito en el 90-95% de los casos4. Sin embargo, también se ha identificado un riesgo significativo de eventos adversos graves potencialmente mortales derivados del procedimiento, alrededor del 6-15%. Las complicaciones más frecuentes son pancreatitis, hemorragia gastrointestinal, perforación e infección asociada al procedimiento2,5,6.
Esto ha generado la necesidad de identificar candidatos apropiados para este procedimiento y de reservar la endoscopia biliar para los pacientes que tienen la mayor probabilidad de cálculos intraductales. La American Society for Gastrointestinal Endoscopy (ASGE) y la Society of American Gastrointestinal and Endoscopic Surgeons (SAGES) en el año 2010 emitieron guías de manejo de los pacientes con sospecha de coledocolitiasis; sin embargo, se descubrió que clasificaban inadecuadamente a los pacientes con perfiles de riesgo más altos, lo que llevó al uso excesivo de CPRE diagnósticas y a la exposición del paciente a complicaciones potencialmente innecesarias5.
La efectividad y rendimiento diagnóstico fue tema de discusión para la falta de apego del personal sanitario hacia estas guías, por tal motivo la ASGE en el año 2019 realizó una revisión y cambios con el objetivo de mejorar la efectividad para predecir el diagnóstico de coledocolitiasis2,7.
Los predictores clínicos se simplificaron en riesgo alto, riesgo moderado y riesgo bajo8. Los nuevos criterios de alto riesgo incluyen: colangitis ascendente, coledocolitiasis en ecografía o tomografía computarizada (TC) abdominal, o bilirrubina total > 4 mg/dl más colédoco dilatado. Para esta estratificación de pacientes se recomienda la CPRE. Riesgo intermedio: bioquímica hepática anormal distinta a la bilirrubina, edad mayor de 55 años y dilatación del conducto colédoco en la imagen. Se recomienda complementación diagnóstica con colangiopancreatografía por resonancia magnética (CPRM)/ultrasonido endoscópico (USE) para este tipo de pacientes. Riesgo bajo: aquellos pacientes sin la presencia de predictores de coledocolitiasis. Se recomienda colecistectomía con o sin colangiografía transoperatoria (CTO)/ultrasonido intraoperatorio2,9 (Fig. 1).

Figura 1 Estratificación de riesgo según la presencia o no de los predictores de coledocolitiasis, así como la estrategia recomendada a seguir por las guías ASGE 2019 (adaptado de Buxbaum JL et al.2). CPRE: colangiopancreatografía retrógrada endoscópica; CPRM: colangiopancreatografía por resonancia magnética; CTO: colangiografía transoperatoria; USE: ultrasonido; USE: ultrasonido endoscópico.
Según la revisión de las guías ASGE 2019, en la categoría de alto riesgo para coledocolitiasis los pacientes tienen la probabilidad del 50% tener un cálculo en el conducto biliar. Para reducir las CPRE de diagnóstico innecesarias, la ASGE establece que solo los pacientes que cumplan con los criterios de alto riesgo procedan a CPRE sin intervenciones complementarias10,11.
En aquellos pacientes con riesgo intermedio se predice coledocolitiasis entre el 10-50%. La ausencia de predictores de riesgo indica una baja probabilidad de coledocolitiasis, menor al 10%. El grupo de pacientes con sospecha de coledocolitiasis de riesgo intermedio son los más propensos a una CPRE innecesaria y su consiguiente exposición al riesgo derivado del procedimiento12.
Se ha demostrado que la ecografía endoscópica y la colangiopancreatografía por resonancia magnética ofrecen una alternativa diagnóstica menos invasiva y riesgosa para este tipo de pacientes4,8. La CPRM tiene una sensibilidad del 85-92% y una especificidad del 93-97%13. En la colecistitis aguda, entidad que va en muchas ocasiones acompañada de coledocolitiasis, la CPRM tiene una sensibilidad del 76.2-85.7% y especificidad del 84.3-92.2%13.
Por su parte, para el USE en múltiples estudios se ha reportado una alta sensibilidad, del 84-98%, una especificidad del 94-100% y un valor predictivo positivo (VPP) y uno negativo (VPN) del 100 y 98%, respectivamente4,14. En una revisión sistemática en la que se evaluó la precisión en el diagnóstico de coledocolitiasis, se describe una sensibilidad del 95 y especificidad del 97% para el USE, y del 93% de sensibilidad y 96% de especificidad para la CPRM. El USE ha propuesto recientemente como el nuevo método de referencia en el diagnóstico de coledocolitiasis. Sin embargo, en comparación con la CPRM, el USE tiene un amplio rango de aplicabilidad, pero una curva de aprendizaje demandante4.
La ASGE establece que se requiere un mínimo de 225 procedimientos de USE para calificar; esta experiencia solo se puede obtener en centros de concentración endoscópica. Por lo tanto, la formación del recurso de la salud con este entrenamiento es un enorme desafío, lo que limita en gran medida la popularidad de la endoscopia ultrasónica15.
En el 2019 se incluyó la TC como método de imagen a la par del ultrasonido abdominal para detectar cálculos de la vía biliar, así como dilatación. La precisión de la guía ASGE para TC fue del 63.98%, con sensibilidad del 79.12% y especificidad del 42.80% en los grupos de alto riesgo, y del 36.02% con sensibilidad del 20.88% y especificidad del 57.20% en el grupo de riesgo intermedio. También se encontró que la precisión de la TC fue mayor que la de la ecografía para detectar coledocolitiasis (78.64 vs. 53.40%), por lo que se sugiere que la elección del método de imagen avanzada de complementación diagnóstica será con base en la disponibilidad16.
Rendimiento general de las directrices ASGE 2019 para la coledocolitiasis
En 2020 se llevó a cabo un estudio de cohorte, retrospectivo, en 744 pacientes; 74 (9.9%) fueron categorizados como de baja probabilidad, 396 (53.2%) como de probabilidad intermedia y 274 como de alta probabilidad (36.8%) según las guías ASGE 2019. En los grupos de probabilidad baja e intermedia, en 318 de 470 pacientes (67.7%) se confirmó la presencia de coledocolitiasis al momento de la CPRE. En el grupo de probabilidad alta, 226 de 274 pacientes (82.5%) presentaron cálculos en el conducto biliar al momento de la CPRE. Se estimó una diferencia del 14.8%, que fue estadísticamente significativa (p < 0.0001).
La sensibilidad y especificidad en este grupo de riesgo fueron del 41.5 y el 76%, respectivamente. El VPP fue 82.5% y el valor predictivo negativo (VPN) del 32.3%17.
Ovalle-Chao et al.11 realizaron un estudio en la población del norte de México. En cuanto al rendimiento general de estas guías, la categoría de riesgo alto tuvo una sensibilidad del 68.75% y una especificidad del 52.08%, un VPP del 79.28% y un VPN del 38.46%, y una exactitud diagnóstica del 64.20%; se corroboró el diagnóstico de coledocolitiasis en el 79.28% de los pacientes de esta categoría de riesgo. Chisholm et al.18 estudiaron una cohorte de 59 pacientes identificados como de alto riesgo según las guías ASGE 2019, de los cuales 34 pacientes realmente tenían coledocolitiasis, lo que reveló una tasa de CPRE negativa del 42.4%.
Hall et al.19 realizaron una revisión retrospectiva de 2,724 pacientes, la especificidad estimada y el VPP de los predictores de alto riesgo demostraron ser del 74 y el 64%, respectivamente. En este estudio se ha reportado una sensibilidad que oscila entre el 59.5 y el 65%, y una especificidad del 60 al 78.9% de las guías ASGE 2019 para el diagnóstico de coledocolitiasis.
Sadeghi et al.20 realizaron un estudio prospectivo de 216 pacientes. Se estimó la sensibilidad y especificidad de las guías predictiva de coledocolitiasis de la ASGE 2019, resultó un 62.31 y 51.85%, respectivamente. Silva-Santisteban et al.21 realizaron un estudio retrospectivo comparando el rendimiento diagnóstico de las herramientas predictoras de coledocolitiasis propuestas por la ASGE 2010, la ASGE 2019 y la Sociedad Europea de Endoscopia Gastrointestinal (ESGE). Se incluyeron en su análisis 359 pacientes, se clasificaron 196 (54.6%) como pacientes con alto riesgo de presentar coledocolitiasis, 153 (42.6%) como de riesgo intermedio y 10 como de riesgo bajo según las guías ASGE 2019. Se confirmó coledocolitiasis por medio de CPRE, USE, CPRM o colangiografía intraoperatoria en el 81.6% (160/196) de los pacientes con alto riesgo, un 40.5% (62/153) en el estrato de riesgo intermedio y un 30% (3/10) en los pacientes con un riesgo bajo.
Tunruttanakul et al.22 en su estudio, en el cual participaron 521 pacientes con sospecha de coledocolitiasis, 12 (2.3%), 146 (28.0%) y 363 (69.7%) pacientes se clasificaron en grupos de riesgo bajo, intermedio y alto respectivamente. Se calculó un VPP del 73.6%. En un estudio realizado en Tailandia, para evaluar su rendimiento diagnóstico de las guías ASGE 2019 en 280 pacientes, la precisión diagnóstica fue del 75% (sensibilidad del 75.47%, especificidad del 73.53%) para los pacientes con criterios de riesgo alto. Respecto al grupo riesgo intermedio, el 25% (sensibilidad del 24.53%, especificidad del 26.47%), el VPP y el VPN fueron 89.89 y 49.02% respectivamente23.
En una evaluación retrospectiva realizada por Steinway et al.10, utilizando las directrices ASGE 2019, en una cohorte de 1,042 pacientes se obtuvo una especificidad del 96.9%, VPP del 89.6% en el grupo de pacientes que cumplían criterios de riesgo alto. La precisión de las directrices de 2019 para la predicción de coledocolitiasis si se presentan criterios de alto riesgo sigue siendo solo del 70.4%, con una especificidad del 79.5%24.
Woo et al.25 realizaron un estudio retrospectivo para evaluar la precisión diagnóstica de los criterios de la ASGE 2019 en población de Corea del sur. Se incluyeron 1,030 pacientes para este estudio, de los cuales 188 (15.4%) se clasificaron como pacientes con riesgo bajo, 905 (74%) como de riesgo intermedio y 130 (10.6%) como de riesgo alto. Se confirmó coledocolitiasis en un 1.1% (2/188) de los pacientes clasificados como de bajo riesgo, con una sensibilidad del 99.3% y una especificidad del 19.7%. En los pacientes clasificados como de riesgo intermedio se confirmó coledocolitiasis en 155 (17.1%), con una sensibilidad del 56% y una especificidad del 20.7%. En el estrato de alto riesgo se confirmó coledocolitiasis en 120 (92%) de los pacientes, con una sensibilidad del 43.3% y una especificidad del 98.9%.
Reclasificar a los pacientes en los diferentes estratos de riesgo
Ramírez-Peña et al.9 realizaron un análisis de los cambios dinámicos en las pruebas de función hepática (definidos como cambios del 30 o 50% en las mediciones entre 24 y 72 h antes de la CPRE) y se documentó que la reclasificación de riesgo con base en estas no eleva la efectividad de predicción de coledocolitiasis, por lo que no se recomienda el seguimiento de los cambios dinámicos de las pruebas de función hepática para reclasificar el riesgo de coledocolitiasis.
Rendimiento de las directrices ASGE 2019 para la coledocolitiasis en pacientes con diagnóstico de colecistitis aguda litiásica concomitante
Reddy et al.26 realizaron un estudio retrospectivo en los pacientes con sospecha de coledocolitiasis, con diagnóstico concomitante de colecistitis aguda litiásica y encontraron que los pacientes con criterios de alto riesgo según las guías de la ASGE 2019 tuvieron una sensibilidad y especificidad del 61.9 y el 83.4%, respectivamente, para predecir la coledocolitiasis.
Comparación de rendimiento diagnóstico de las directrices ASGE/SAGES 2010, ASGE 2019 y ESGE para coledocolitiasis
En una comparación retrospectiva de las guías ASGE 2010 vs. ASGE 2019 se encontró que las características que componen los criterios de alto riesgo de 2019 dan como resultado que menos pacientes se clasifiquen como de alto riesgo, lo que eleva su especificidad alrededor del 76% y disminuye su sensibilidad hasta un 42%. De esta manera, si se hubieran aplicado estas guías se habría reducido el número de pacientes que se sometieron a CPRE27. A raíz de su estudio se demuestra que las guías ASGE de 2019 son más específicas para la detección de coledocolitiasis durante la CPRE en comparación con las pautas de 2010. Sin embargo, aumenta la cantidad de pacientes que se clasifican como de riesgo intermedio y requerirán un estudio de imagen confirmatorio adicional9,17.
La sensibilidad de la herramienta de estratificación de riesgo requiere una interpretación matizada28. En estudios recientes se compara la especificidad y sensibilidad de los criterios propuestos por la ASGE en el año 2019 y los propuestos por la ESGE; los hallazgos indican que los criterios de la ESGE son más específicos22,23,27. Por otro lado, Wangchuk et al.23 encontraron que la variabilidad de rendimiento diagnóstico de estas directrices propuestas por SAGES/ASGE 2010, ASGE 2019 y ESGE fue mínima, por lo tanto es aceptable utilizar cualquiera de estos criterios.
Apego a las directrices ASGE 2019 para la coledocolitiasis
Rashtak et al.29 detectan en su estudio una falta de apego a las guías ASGE 2019 en el 43% de los casos sospechosos de coledocolitiasis para el manejo de los pacientes con sospecha de coledocolitiasis. Se mencionan varias razones que pudieran desencadenar esta falta de apego, como la falta o demora de CPRM o USE.
Controversias del uso de las directrices ASGE 2019 como herramienta de predicción diagnóstica no invasiva
Lograr un equilibrio entre la intervención oportuna y la certeza diagnóstica continúa siendo un reto en los pacientes con sospecha de coledocolitiasis30. Algunos estudios informan una sobrestimación de las guías ASGE 2019 para coledocolitiasis. La precisión de las directrices de 2019 para la predicción de coledocolitiasis si se presentan criterios de alto riesgo sigue siendo solo del 70.4% y, por lo tanto, daría lugar a la realización de CPRE innecesarias en una proporción significativa de pacientes, alrededor del 26.47%20,24.
Método
Estudio observacional de tipo analítico, retrospectivo.
Se recabó el registro de solicitudes para CPRE por sospecha de coledocolitiasis de los pacientes de cualquier sexo, mayores de edad (18 años) del periodo del 1 de enero del 2023 al 31 de diciembre del 2023 en un hospital de segundo nivel en el norte de México. Se analizaron los expedientes clínicos y se clasificó a los pacientes como riesgo alto, riesgo intermedio y riesgo bajo según sus características clínicas, bioquímicas e imagenológicas. Se identificaron los pacientes de alto riesgo a los que se les realizó solicitud de CPRE para medir el porcentaje de aplicación (apego) a las guías.
Posteriormente, se recabaron los reportes de los pacientes en los que se realizó CPRE y si existió confirmación diagnóstica de coledocolitiasis por este medio, de esta forma se puede medir el rendimiento diagnóstico de estas guías en nuestra población.
Se excluyeron pacientes con expediente incompleto y pacientes que hayan generado su alta voluntaria. Se eliminaron del estudio pacientes con otro diagnóstico diferente a coledocolitiasis revelado por la CPRE y pacientes en los que se haya indicado CPRE, pero en su lugar se haya realizado otro abordaje terapéutico (cirugía).
Análisis estadístico
Se utilizó la frecuencia y los porcentajes para describir la aparición de las variables cualitativas. La media y la desviación estándar (DE) de las variables cuantitativas con distribución normal y la moda y percentiles de las variables cuantitativas con distribución no normal. Se calculó la especificidad, sensibilidad, VPP, VPN del grupo de alto riesgo, en el cual se recomienda la realización de CPRE sin algún otro estudio complementario. Derivado de los siguientes valores se calculó la razón de verosimilitud positiva (LR+), la razón de verosimilitud negativa (LR−) y la exactitud global de la prueba. La prueba confirmatoria será la CPRE.
Resultados
Nos apegamos a las guías internacionales STARD 2015 para el reporte de evaluación para la presentación de informes sobre estudios de precisión diagnóstica.
Se encontró registro de 251 solicitudes de CPRE desde el 1 de enero del 2023 al 31 de diciembre del 2023. Se excluyeron las solicitudes que se habían realizado por otro diagnóstico diferente a la sospecha de coledocolitiasis, solicitudes repetidas o aquellas que se hubieran solicitado en pacientes pediátricos. Se registraron 119 solicitudes que se realizaron por sospecha de coledocolitiasis en pacientes adultos. La información obtenida se vacío en una base de datos en Excel, la cual posteriormente fue importada al paquete estadístico SPSS versión 25 para su análisis.
De los 119 pacientes que se incluyeron en el estudio, 89 (74.8%) son mujeres, 30 (25.2%) son hombres. La edad media fue de 45 años y la moda de 29 años. Solo 57 pacientes (47.9%) contaban con criterios de alto riesgo, para realización de CPRE sin otra acción, por lo que se considera que la aplicación de las guías ASGE 2019 por parte de los cirujanos fue de un 47.9% en un inicio (Tabla 1).
Tabla 1 Características sociodemográficas de la muestra
| Sexo | Femenino: 89 (74.8%) | n = 119 |
| Masculino: 30 (25.2%) | ||
| Edad | Media: 45 años (DE: 18.2) | Rango inferior: 19 años Rango superior: 92 años |
| Moda: 29 años | ||
| Grupo de riesgo | Alto: 57 (47.9%) | n = 119 |
| Intermedio: 48 (40.3%) | ||
| Bajo: 14 (11.8%) | ||
| Realización de CPRE | Sí: 97 (81.5%) | n = 119 |
| Pacientes perdidos: 24 (18.4%) | ||
| Confirmación de coledocolitiasis por CPRE | Sí: 62 (63.9%) | n = 97 |
| No: 24 (24.7%) | ||
| Estudio no concluyente: 11 (11.3%) |
CPRE: colangiopancreatografía retrógrada endoscópica; DE: desviación estándar.
Según las características clínicas, bioquímicas e imagenológicas se estratificó a 48 pacientes (40.3%) como de riesgo intermedio y 14 (11.8%) como de riesgo bajo. La CPRE se realizó a 97 (81.5%) pacientes. Hubo una pérdida de 22 (9.2%) pacientes, en la mayoría de los casos se tiene evidencia de que se solicitó alta voluntaria, debido al tiempo de espera de la CPRE.
Finalmente, se confirmó coledocolitiasis por CPRE en 62 (63.9%) pacientes. En 24 (24.7%) pacientes en los que se realizó CPRE por sospecha de coledocolitiasis no se confirmó tal diagnóstico (se reporta ausencia de defectos de llenado, ausencia de extracción de cálculos posterior al barrido con balón y/o vía biliar normal, sin dilatación). En 11 (11.3%) de los pacientes no fue concluyente el estudio diagnóstico-terapéutico, por lo cual se descartan para el análisis (se reportan dificultades técnicas, sobre todo para obtener la canulación del ámpula).
Se obtuvo para el análisis un total de 86 pacientes en los que se pudo llevar a cabo la colangiografía y por lo tanto confirmar o descartar el diagnóstico de coledocolitiasis (Fig. 2).
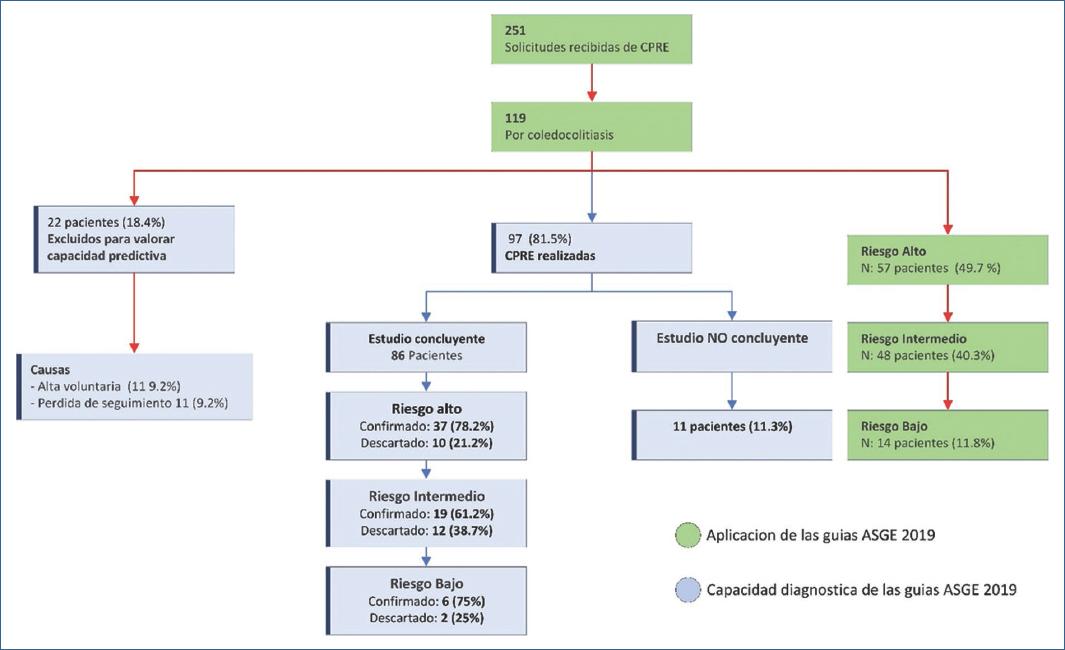
Figura 2 Pacientes incluidos y excluidos en el desarrollo del estudio. ASGE: American Society for Gastrointestinal Endoscopy; CPRE: colangiopancreatografía retrógrada endoscópica.
Se confirmó coledocolitiasis por CPRE en 37 pacientes (78.2%) y se descartó en 10 pacientes (21.2%) pertenecientes al grupo de alto riesgo. Se confirmó coledocolitiasis por CPRE en 19 pacientes (61.2%) y se descartó en 12 pacientes (38.7%) pertenecientes al grupo de riesgo intermedio. Se confirmó coledocolitiasis por CPRE en seis pacientes (75%) y se descartó en dos pacientes (25%) pertenecientes al grupo de riesgo bajo (Tabla 2).
Tabla 2 Confirmación de coledocolitiasis por CPRE de acuerdo con el grupo de riesgo según las guías ASGE 2019
| Riesgo/diagnóstico | Coledocolitiasis (+) | Coledocolitiasis () | Total |
|---|---|---|---|
| Alto | 37 (78.3%) | 10 (21.2%) | 47 (100%) |
| Intermedio | 19 (61.2%) | 12 (38.7%) | 31 (100%) |
| Bajo | 6 (75%) | 2 (25%) | 8 (100%) |
| Total | 62 (72%) | 24 (27.9%) | 86 (100%) |
ASGE: American Society for Gastrointestinal Endoscopy; CPRE: colangiopancreatografía retrógrada endoscópica.
Se hizo el análisis de 86 pacientes en los que se realizó CPRE y se pudo llevar a cabo la colangiografía (Tabla 3).
Tabla 3 Confirmación de coledocolitiasis por CPRE en pacientes con riesgo alto según las guías ASGE 2019
| Riesgo/diagnóstico | Coledocolitiasis (+) | Coledocolitiasis () | Total |
|---|---|---|---|
| Alto | 37 (38.1%) | 10 (11.6%) | 47 (54.7%) |
| Sin alto riesgo | 25 (29.1%) | 14 (16.3%) | 39 (45.3%) |
| Total | 62 (72%) | 24 (27.9%) | 86 (100%) |
ASGE: American Society for Gastrointestinal Endoscopy; CPRE: colangiopancreatografía retrógrada endoscópica.
Discusión
En el 2010, la ASGE emitió las guías clínicas para el manejo de los pacientes con sospecha de coledocolitiasis; sin embargo, la capacidad predictiva y el rendimiento diagnóstico de estas directrices fue limitado31. En el año 2019, se modifican los criterios individuales por el mismo organismo con el fin de aumentar la capacidad predictiva y tener un mayor rendimiento diagnóstico.
Se identificó en nuestro medio la aplicación del 47.9% de los casos y una falta de apego del 52.1%, similar a lo que reporta Rashtak et al.29 en su estudio. Se identificaron razones que pudieran desencadenar esta falta de apego, como la falta o demora de CPRM o USE, como pasa en la mayor parte de los hospitales de México.
Diversos estudios han evaluado la capacidad predictiva de las guías de la ASGE 2019 para coledocolitiasis en distintas partes del mundo (Tabla 4).
Tabla 4 Estudios que han evaluado el rendimiento diagnóstico de las guías de la ASGE 2019 para coledocolitiasis
| Referencia | Lugar | n | Prevalencia | Sensibilidad | Especificidad | VPP | VPN |
|---|---|---|---|---|---|---|---|
| Sadeghi et al.20 | Irán | 124 | 56% | 62% | 52% | 62% | 51% |
| Chandran et al.17 | EE.UU., multicéntrico | 744 | 73% | 41% | 76% | 83% | 32% |
| Silva-Santisteban et al.21 | EE.UU. | 359 | 63% | 72% | 71% | 81% | 60% |
| Tunruttanakul et al.22 | Tailandia | 521 | 61% | 84% | 53% | 74% | 68% |
| Wangchuket al.23 | Tailandia | 280 | 74% | 75% | 73% | 89% | 49% |
| Steinway et al.10 | EE.UU., multicéntrico | 1,378 | 60% | 61% | 63% | 71% | 53% |
| Woo et al.25 | Corea del sur | 1,223 | 23% | 43% | 99% | 92% | 84% |
| Reddy et al.26 | India | 173 | 37% | 62% | 83% | 68% | 79% |
| Hasak et al.24 | EE.UU. | 1,098 | 67% | 65% | 79% | 86% | 54% |
ASGE: American Society for Gastrointestinal Endoscopy; VPN: valor predictivo negativo; VPP: valor predictivo positivo.
Se reporta una sensibilidad del 41% en población estadounidense al 84% en población tailandesa, especificidad del 51% en población iraní al 83.4% en población de la India, VPP del 62% en población iraní al 89% reportado en Tailandia, VPN del 32% en EE.UU., hasta de un 79.3% en la India10,17,20-26.
En Corea del Sur se realizaron modificaciones para adaptarlas a su población, lo que mejoró su sensibilidad, especificidad, VPP, VPN y exactitud global25.
Por su parte en México se obtuvo una sensibilidad del 69%, especificidad del 52%, VPP del 79%, VPN del 38% y una exactitud global del 64%, LR+ de 1.43 y LR de 0.611.
En nuestro estudio se calculó una prevalencia del 72%. Se obtuvo una sensibilidad del 60% y una especificidad del 58%. Se calculó un VPP del 79% y un VPN del 36%. Para analizar el rendimiento diagnóstico se calculó una LR+ de 1. 43, LR de 0.69 y una exactitud global del 59.3% para los pacientes clasificados como de riesgo alto.
El 18.4% de los pacientes que fueron sometidos a CPRE presentaron complicaciones, una tasa de complicaciones más alta que la descrita en la literatura2,5,6, e incluso se registraron dos fallecimientos derivados del procedimiento. Un paciente por hemorragia y el segundo derivado de perforación intestinal, lo que remarca la importancia de implementar una herramienta con la mayor capacidad predictiva posible para disminuir la presencia de estos infortunios.
Múltiples estudios han evaluado la aplicación de las guías ASGE 2019 en distintas poblaciones. Sin embargo, en México la literatura al respecto es limitada. Este estudio busca aportar evidencia que respalde su uso o sugiera la necesidad de una adaptación, aplicación de otras directrices validadas como las emitidas por la ESGE o quizá utilizar la inteligencia artificial en nuestra población como directrices para los pacientes con sospecha de coledocolitiasis. Las herramientas predictivas diagnósticas son de suma importancia como guía terapéutica en los sitios donde se tiene alcance limitado a recursos diagnósticos como colangiorresonancia magnética y USE, como en nuestro caso, un hospital de segundo nivel.
El estudio presentado tiene ciertas limitaciones. La primera de ellas es la naturaleza retrospectiva del estudio. La segunda es la pérdida de pacientes en el transcurso del tiempo, la causa más constante fue la alta voluntaria por el prolongado tiempo de espera.
La principal fortaleza de este estudio radica en que establece una base fundamental para la evaluación continua del rendimiento diagnóstico de estas guías y otras herramientas no invasivas con el objetivo de identificar la más eficaz para nuestra población.
Conclusión
A más de cinco años de la emisión de las guías ASGE 2019 para coledocolitiasis, se ha demostrado que su aplicación contribuye en disminución de costos, la reducción de la estancia intrahospitalaria y una capacidad de predecir coledocolitiasis por arriba del 50% en los pacientes que se recomienda la realización de CPRE sin otro estudio complementario (alto riesgo). Es fundamental realizar más estudios en la población mexicana, para poder definir de una manera adecuada la utilidad clínica de estas guías en nuestra población, sobre todo en hospitales de segundo nivel donde se limitan las herramientas diagnósticas no invasivas.











 nueva página del texto (beta)
nueva página del texto (beta)


