Introducción
Las prácticas agropecuarias en busca de mayor producción han contribuido al incremento de las emisiones de CO2 hacia la atmósfera, ocasionando por una parte la degradación y pérdida de carbono en el suelo, el cual se libera, debido a la falta de cobertura vegetal principalmente, en los procesos de erosión, lixiviación y arrastre (FAO 2006). Por lo que se deben buscar estrategias de mitigación de CO2 en los sistemas ganaderos, mediante el establecimiento de arbustivas forrajeras, como alternativa en la conservación, recuperación y mejoramiento de suelos; así como en la captura de carbono atmosférico y su transformación en carbohidratos en la biomasa aérea. En este sentido, las especies arbustivas y cultivares forrajeras son una opción, como lo mencionan Alecrim et al. (2022) que al incorporar leguminosas con adecuado contenido en taninos puede ser una práctica importante para mejorar la cantidad de forraje y la calidad de la dieta animal, además de mitigar los impactos ambientales, como las emisiones de gases de efecto invernadero en sistemas ganaderos. Aspectos de mejora de rendimientos productivos y calidad de canal en ovinos por uso de taninos se han observado (Orzuna-Orzuna et al. 2021). Por lo que el uso de árboles y arbustos representa una alternativa, contribuyendo a mejorar la calidad de la alimentación del ganado a un costo bajo con cantidades bajas de concentrados elaborados a base de granos (Gallego et al. 2012, Castro et al. 2021). Al respecto Argüello et al. (2019) reportan en los países tropicales se puede incentivar el uso de sistemas silvopastoriles, en los que se combinan gramíneas y leguminosas que favorecen los indicadores productivos y reproductivos del ganado. Estos arreglos, con plantas leñosas perennes (árboles y arbustos leguminosas) y gramíneas, proporcionan una mayor oferta forrajeras en distintos estratos, lo que se traduce en una dieta más nutritiva en comparación con los sistemas tradicionales. Es fundamental disponer de alternativas forrajeras para la alimentación bovina, especialmente en el contexto global del cambio climático y sus efectos sobre el medio ambiente, que impactan de forma directa las explotaciones agropecuarias, en particular la ganadería. Contar con materiales vegetales adecuados como opciones forrajeras es una estrategia clave para suplir las necesidades nutricionales del ganado y garantizar la sostenibilidad de la producción. Los sistemas silvopastoriles son una alternativa productiva de gran valor para la alimentación animal, al ofrecer mayor diversidad botánica en comparación con los sistemas tradicionales. Además, contribuyen a la mitigación del cambio climático y pueden traducirse en una reducción de los costos de operación para la ganadería que adopte la diversificación de especies en los sistemas pastoriles (Osorio-Giraldo et al. 2024).
Por otro lado, hay diversas técnicas para determinar el valor nutrimental de los forrajes, entre las cuales destaca la técnica in vitro de producción de gas (TIVPG), que permite determinar la extensión y la cinética de degradación de los alimentos a través del volumen de gas liberado durante el proceso fermentativo (Theodorou et al. 1994). Conforme aumenta la población microbiana, se espera mejor la fermentación y mayor disponibilidad de los componentes solubles (Pell y Schofield 1993). Ante la necesidad de incrementar el conocimiento sobre la oferta y el aprovechamiento de nutrientes en los sistemas de producción, la TIVPG representa una herramienta útil para cuantificar el grado de degradación ruminal de especies vegetales arbustivas y arbóreas, mediante el análisis de la cinética de producción de gas (García-Montes-de-Oca et al. 2011).
En leguminosas herbáceas se han realizado estudios para evaluar la relación entre la calidad proteica y la fermentación in vitro. Por ejemplo, Rojas et al. (2018) observaron que Phaseolus lunatus L. var. Silvester (frijolillo), Centrocema plumiere Benth (centrocema) y frijolillo-tamarindo presentaron en hojas contenidos de proteína cruda (PC) de 22.1, 18.5 y 16.3%, respectivamente, con volúmenes de gas de 118.9, 160.4 y 115.5 mL g-1 MS; mientras que la vaina se registraron valores de PC de 9.47, 16.15 y 14.4%, y volúmenes máximos de gas de 161.4, 234.8 y 172.3 mL g-1 MS, respectivamente. Estos resultados reflejan diferencias entre especies y órganos, mostrando que los frutos o vainas generan mayor volumen de gas. En el caso de leguminosas arbóreas, la información es aún limitada respecto a su importancia de estas especies en la alimentación del ganado como complemento forrajero en el pastoreo de agostaderos. Al respecto, Guerrero-Rodríguez et al. (2021) reportan en la selva baja caducifolia diversas especies leguminosas con valores de PC entre 13.2 y 20.6%, y de fibra detergente ácida de 14.8 a 28.7%, la cual mostró correlacionado negativa con la digestibilidad (48.9 a 83.6%). También Torres-Salado et al. (2018) observaron que especies arbóreas como Guazuma ulmifolia Lam y Leucaena spp. tuvieron un volumen máximo de gas in vitro en hojas de 123.2 y 133.3 mL g-1 MS, y vainas de 112.6 y 126.0 mL g-1 MS, respectivamente. Con base en lo anterior, y dada la poca información actualizada sobre el potencial forrajero de las leguminosas arbóreas, el presente estudio planteó como objetivo evaluar la composición química, la fermentación ruminal y la producción de gas in vitro del follaje y fruto de Jacaranda mimosifolia D. Don, Moringa oleifera Lam y nueve especies de leguminosas, empleando la técnica in vitro de producción de gas.
Materiales y métodos
Recolección y preparación de material vegetal
En los meses de julio y agosto se cosecharon en agostaderos, campos, caminos y bordos de carretera follaje y fruto de Jacaranda mimosifolia D. Don, Bauhinia variegata L., Prosopis laevigata Willd., Leucaena leucocephala Lam y Pithecellobium dulce (Roxb.) Benth colectadas en Soledad de Graciano Sánchez, a 22°14' LN, 100°52' LO (GPS Garmin etrex 10). Clima seco templado con 353 mm de precipitación, temperatura media anual de 17 °C y altura de 1 840 msnm. La Moringa oleífera Lam. fue colectada en Jala, Nay, a 21°06' LN, 104°26' LO, clima cálido suhúmedo con 860 mm de precipitación, temperatura media anual de 23 °C y altura de 1 070 m. En tanto que Acacia farnesiana (L.) Willd. Fue colectada en Cerritos, S.L.P., a 22°36' LN, 99°58' LO, clima seco semicálido con 500 mm de precipitación, temperatura media anual de 19 °C y altura de 1 153 m. Mientras que Acacia polyacantha Willd., Cassia fistula L., y Delonix regia (Hook.) Raf. fueron colectadas en San Ciro de Acosta, S.L.P., a 21°38' LN, 99°49' LO, clima semicálido suhúmedo con 650 mm de precipitación, temperatura media anual de 22.4 °C y altura de 1 860 m. En lo referente a Erythrina coralloides DC. fue colectada en Texcoco, Edo. de México a 19°25' LN, 98°53' LO, clima templado semiseco con 686 mm de precipitación, temperatura media anual de 15.9 °C y altura de 2 267 m (García 2004), todas utilizadas como fuentes de forraje (Tabla 1). El material vegetal fue colectado en verde en estado reproductivo en fructificación directamente del árbol. De cada especie se eligieron entre 5 y 10 árboles visiblemente sanos y sin daño físico, de los cuales se obtuvieron muestras de 200 g, tanto de follaje, como de fruto maduro, y se depositaron por separado en bolsas de papel estraza y fueron rotuladas para su identificación. Todas las muestras se sometieron a un proceso de deshidratación a 55 °C en una estufa de secado de aire forzado durante tres y siete días para el follaje y los frutos, respectivamente. Para luego molerlas en un molino de martillos (Thomas Wiley® Laboratory Mill modelo 4, Swedesboro, EE.UU.) con criba de 1 mm y almacenaron en frascos de vidrio hasta los análisis químicos y la incubación in vitro. La identificación taxonómica se realizó por comparación con otros ejemplares colectados por los herbarios Herbarium of Arizona State University (Jacaranda), Herbario MEXU, UNAM (Moringa, Lluvia de oro, Pata de vaca, Mezquite, Guaje y Framboyán), Herbario Nacional, Instituto de Biología, México (Huizache), Herbario de Cheringoma, Mozambique (Espina blanca), Herbario Jerzy Rzendowski, Querétaro, México (Colorín) y Herbario Carlos Contreras Pages, UNAM (Guamúchil).
Tabla 1 Información taxonómica y lugar de recolección de las especies forrajeras evaluadas mediante la técnica in vitro de producción de gas para follaje y fruto.
| Nombre científico | Nombre común | Familia | Lugar de colecta | Follaje | Fruto |
|---|---|---|---|---|---|
| Acacia farnesiana (L) Willd. | Huizache | Fabaceae | Cerritos, SLP | Si | Si |
| Acacia polyacantha Willd. | Espina blanca | Fabaceae | San Ciro de Acosta, SLP | Si | No |
| Bauhinia variegata L. | Pata de vaca | Fabaceae | Soledad de G. S., SLP | Si | Si |
| Cassia fistula L. | Lluvia de oro | Fabaceae | San Ciro de Acosta, SLP | Si | Si |
| Delonix regia (Hook.) Raf. | Framboyán | Fabaceae | San Ciro de Acosta, SLP | Si | Si |
| Erythrina coralloides DC. | Colorín | Fabaceae | Texcoco, Edo. De Méx. | Si | Si |
| Jacaranda mimosifolia D. Don | Jacaranda | Bignoniaceae | Soledad de G. S., SLP | Si | Si |
| Leucaena leucocephala Lam. | Guaje | Fabaceae | Soledad de G. S., SLP | Si | Si |
| Moringa oleífera Lam. | Moringa | Moringaceae | Jala, Nayarit | Si | Si |
| Pithecellobium dulce (Roxb.) Benth | Guamuchil | Fabaceae | Soledad de G. S., SLP | Si | Si |
| Prosopis laevigata Willd. | Mezquite | Fabaceae | Soledad de G. S., SLP | Si | Si |
Análisis químicos
Los análisis se realizaron en el Laboratorio de Nutrición Animal del Instituto de Ciencias Agropecuarias de la Universidad Autónoma del Estado de Hidalgo, ubicado en el municipio de Tulancingo de Bravo, Hidalgo, México. El contenido de materia seca (MS), materia orgánica (MO = 1 000 − ceniza) y proteína cruda (PC = contenido de nitrógeno × 6.25) se estimó en el forraje y fruto de todas las especies siguiendo los métodos de la AOAC (1995).
Incubación in vitro
Se utilizó un ovino (Suffolk × Rambouillet) de tres años con condición corporal 3 (Russel et al. 1969), con cánula ruminal como donador de contenido ruminal, y la extracción se realizó con bomba de vacío y sonda orogástrica a las 08:00 horas, antes de la alimentación. El contenido ruminal extraído se filtró con cuatro capas de gasa para separar las macropartículas de alimento del líquido ruminal, y posteriormente se mezcló con medio nutritivo (agua destilada, solución buffer, macrominerales, microminerales y agente reductor) preparado conforme la metodología de Theodorou et al. (1994), en una proporción de 1:9. Esta mezcla se realizó sobre una placa calefactora de cerámica con agitador magnético (Thermo Scientific Cimarec, mod. SP131325, Waltham, Massachusetts, EUA) para mantener la temperatura a 39 °C y la agitación constante. Además, durante la preparación se mantuvo un flujo constante de CO2 y se añadió 1 mL de solución reductora a base de sulfato de sodio anhidro e hidróxido de sodio por cada 30 mL de mezcla. La incubación se realizó por triplicado en frascos de vidrio transparente con capacidad de 120 mL, a cada uno se le agregaron 500 mg de follaje o vaina de cada especie y 40 mL de la mezcla obtenida del líquido ruminal y el medio nutritivo. Los frascos se sellaron de forma hermética con tapón de silicón y casquillo de aluminio donde se utilizó una engarzadora manual, y posteriormente se colocaron en baño maría con recirculación (Thermo Scientific, mod. 2864, Marietta, Ohio, EE.UU.) a 39 °C durante 48 horas.
Se utilizaron frascos transparentes para la incubación in vitro con el fin de facilitar la observación visual del proceso fermentativo, sin necesidad de interrumpir el sistema ni exponerlo al oxígeno atmosférico. Es importante mencionar que los frascos permanecieron en todo momento en condiciones de oscuridad durante la incubación en baño María, excepto durante los breves momentos en que se realizaron las mediciones, lo cual evitó la exposición directa a la luz y, por lo tanto, no afectó la actividad microbiana ni los resultados de la fermentación. Además, el uso de frascos de vidrio transparente ha sido reportado en estudios previos de fermentación ruminal in vitro, incluidos aquellos que utilizan jeringas de vidrio, lo cual respalda la validez metodológica de esta elección.
Medición de la producción de gas y pH
La producción de gas total (PGT) se midió en mililitros a las 1, 2, 3, 4, 5, 6, 7, 9, 12, 24 y 48 h de incubación mediante el método de desplazamiento de volumen de agua, que consiste en insertar una aguja en el tapón del frasco y conectarla a una bureta de 100 mL con agua a través de una manguera de látex. Después de cada medición, se liberó el gas acumulado en cada frasco y al finalizar la incubación se registró el pH con un potenciómetro de mesa (Hanna Instruments®, mod. HI-2211, Cluj-Napoca, Transilvania, Rumanía). La medición de la producción de gas se limitó a las 48 h, ya que diversos estudios han demostrado que la mayor proporción de gas se genera durante las primeras 24 a 48 h de fermentación, siendo este el periodo más representativo para evaluar diferencias entre tratamientos.
Cálculos y análisis estadístico
Los valores de la producción de gas se utilizaron para estimar el volumen máximo y tasa de producción de gas total con el procedimiento NLIN de SAS® Ver. 9.3 (SAS 2011), mediante el modelo logístico propuesto por Schofield y Pell (1995) :
Donde: Vf = volumen fraccional de gas total (mL g−1 MS); Vm = volumen máximo de producción de gas total (mL g−1 MS); S = tasa de producción de gas total (h−1) y L = fase de retardo (h).
Los datos de MS, MO y PC fueron promediados y se calculó el coeficiente de variación para cada variable, mientras que la producción fraccional de gas total se analizó bajo un diseño completamente al azar, con medias repetidas en el tiempo y cada frasco se consideró como unidad experimental. En el análisis de Vf, Vm, S y pH se utilizó el procedimiento MIXED de SAS® Ver. 9.3 (SAS 2011) y los modelos estadísticos fueron los siguientes:
Donde: yijk = variable de respuesta; µ = media general; Ei = efecto fijo de la i-ésima especie (11 especies para follaje y 9 especies para fruto); Tj = efecto fijo del j-ésimo tiempo de incubación (11 tiempos de incubación); ETij = efecto fijo de la interacción especie × tiempo de incubación y 𝜀ijk = efecto aleatorio del error experimental. Las medias de cuadrados mínimos se obtuvieron con LSMEANS, la comparación de medias se realizó para variables con efecto significativo del tratamiento utilizando PDIFF y el nivel de significancia fue de p ≤ 0.05.
Resultados
Contenido de materia seca, materia orgánica y proteína cruda
El coeficiente de variación más alto se obtuvo para el contenido de PC, tanto en follaje como en fruto (Tabla 2). El contenido de MS y MO tuvo rangos de 88.3 a 91.9% y de 87.7 a 95.5% en el follaje, mientras que en el fruto fue de 87.6 a 91.6% y de 94.0 a 97.3%, respectivamente. La especie con menor contenido de PC fue Jacaranda mimosifolia (0.6% en follaje y 3.8% en fruto), mientras que la de mayor contenido en follaje fue Moringa oleifera (31.2%) y en fruto fue Leucaena leucocephala (24%).
Tabla 2 Promedio y coeficiente de variación (CV) del contenido de materia seca (MS), materia orgánica (MO) y proteína cruda (PC), en follaje y fruto de Jacaranda mimosifolia, Moringa oleifera y nueve especies de leguminosas forrajeras.
| Especie | Follaje | Fruto | ||||
|---|---|---|---|---|---|---|
| MS (%) | MO (%) | PC (%) | MS (%) | MO (%) | PC (%) | |
| Acacia farnesiana (L) Willd. | 90.4 | 91.8 | 15.7 | 88.1 | 95.7 | 20.1 |
| Acacia polyacantha Willd. | 90.4 | 92.7 | 20.6 | - | - | - |
| Bauhinia variegata L. | 89.8 | 92.1 | 14.5 | 91.6 | 96.9 | 13.4 |
| Cassia fistula L. | 88.3 | 94.2 | 16.8 | - | - | - |
| Delonix regia (Hook.) Raf. | 89.5 | 91.0 | 21.9 | 89.6 | 96.4 | 7.0 |
| Erythrina coralloides DC. | 91.3 | 91.0 | 17.3 | 89.2 | 94.0 | 16.7 |
| Jacaranda mimosifolia D. Don | 91.2 | 95.5 | 0.6 | 89.9 | 97.3 | 3.8 |
| Leucaena leucocephala Lam. | 90.8 | 91.9 | 14.1 | 91.2 | 94.7 | 24.0 |
| Moringa oleífera Lam. | 89.8 | 87.7 | 31.2 | 90.6 | 94.8 | 20.6 |
| Pithecellobium dulce (Roxb.) Benth | 90.6 | 92.8 | 20.0 | 87.6 | 94.7 | 13.6 |
| Prosopis laevigata Willd. | 91.9 | 90.7 | 16.7 | 91.5 | 95.2 | 10.1 |
| CV (%) | 1.05 | 2.09 | 40.3 | 1.52 | 1.11 | 43.7 |
Fermentación ruminal in vitro de follaje
La Tabla 3 presenta las medias del volumen máximo (Vm) y la tasa de producción de gas total (S), así como el pH final obtenido de la fermentación in vitro del follaje de las especies evaluadas. Con base en las similitudes entre medias de Vm (Tabla 3), se identificaron seis grupos de especies para la fermentación de follaje (Figuras 1A a 1F), y se ordenan de valores menores a mayores de Vm del follaje.
Tabla 3 Volumen máximo de producción de gas total (Vm), tasa de producción de gas total (S) y pH de la fermentación ruminal in vitro del follaje de Jacaranda mimosifolia, Moringa oleifera y nueve especies de leguminosas forrajeras.
| Especie | Vm (mL g−1 MS) | S (h−1) | pH |
|---|---|---|---|
| Acacia farnesiana (L) Willd. | 125.1 bc | 0.037 ab | 7.04 e |
| Acacia polyacantha Willd. | 74.1 a | 0.028 a | 7.02 de |
| Bauhinia variegata L. | 149.0 cd | 0.035 ab | 6.90 bc |
| Cassia fistula L. | 173.7 def | 0.034 ab | 6.86 b |
| Delonix regia (Hook.) Raf. | 123.0 bc | 0.041 bc | 6.99 d |
| Erythrina coralloides DC. | 162.8 de | 0.043 bcd | 6.94 c |
| Jacaranda mimosifolia D. Don | 186.7 ef | 0.035 ab | 6.80 a |
| Leucaena leucocephala Lam. | 120.5 b | 0.068 e | 6.98 d |
| Moringa oleífera Lam. | 188.8 f | 0.029 a | 7.00 d |
| Pithecellobium dulce (Roxb.) Benth | 161.2 d | 0.053 d | 6.89 b |
| Prosopis laevigata Willd. | 105.8 b | 0.050 cd | 7.01 de |
| EEM | 9.2 | 0.004 | 0.02 |
a,b,c,d,e,f Medias con diferente literal en superíndice dentro de columnas son diferentes (p ≤ 0.05); EEM = error estándar de la media. Vm = volumen máximo de producción de gas total (mL g−1 MS); S = tasa de producción de gas total (h−1).
Grupo 1. Acacia polyacantha. Es la especie que presentó menor Vm respecto al resto de las especies (p ≤ 0.05, Tabla 3) en la fermentación del follaje. La S en esta especie también menor (p ≤ 0.05), junto con Moringa oleifera, Acacia farnesiana, Jacaranda mimosifolia y Bauhinia variegata, y no presentaron diferencias entre sí (p > 0.05). El pH final de A. polyacantha fue de los más altos, junto con A. farnesiana y Prosopis laevigata. La Figura 1 A presenta el comportamiento de la curva de volumen fraccional de producción de gas total (Vf) de esta especie a través del tiempo, y se observa de las 2 a las 12 h, los valores están entre 2.7 y los 5.2 mL de gas g−1 MS. Posteriormente, hay un incremento que no rebasa los 25 mL a las 48 h.
Grupo 2. Acacia farnesiana, Delonix regia, Leucaena leucocephala y Prosopis laevigata. El valor de Vm para las especies de este grupo estuvo en el rango de 105.8 a 125.1 mL g−1 MS, sin diferencias entre medias (p > 0.05, Tabla 3). El valor de S fue diferente entre especies (p ≤ 0.05), mientras que el pH fue similar entre especies (p > 0.05), excepto para A. farnesiana que mostró el valor más alto (p ≤ 0.05). En la Figura 1B, se observa un comportamiento similar de Vf de las especies de este grupo en las primeras 12 h de incubación, excepto L. leucocephala, la cual mostró un incremento de las 7 a las 9 h, y las diferencias más notables entre especies se observan a las 12 y 48 h (p ≤ 0.05).
Grupo 3. Bauhinia variegata, Acacia farnesiana y Delonix regia. Los valores de Vm para este grupo estuvieron entre 123.0 y 149.0 mL g−1 MS, sin diferencias entre medias (p > 0.05, Tabla 3), y los valores de S tampoco fueron diferentes (p > 0.05), pero sí los valores de pH. Este grupo se caracterizó porque las curvas de Vf son similares entre especies en las primeras 12 h de incubación (Figura 1C), pero a las 24 h B. variegata mostró un incremento superior a las otras especies (p ≤ 0.05) y a las 48 h D. regia presentó menor Vf que las otras dos especies (p ≤ 0.05). Por su parte, los valores de S fueron similares entre las especies de este grupo (p > 0.05), y el pH final fue diferente (p ≤ 0.05) entre especies.
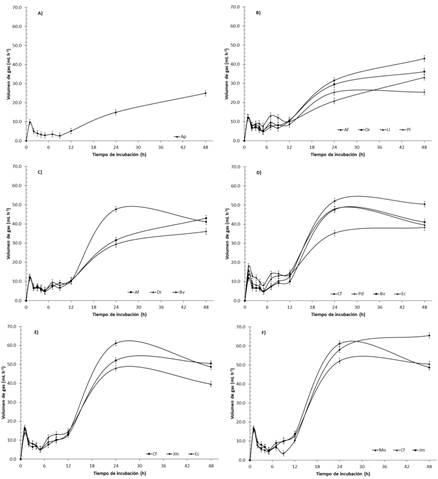
Figura 1 Volumen fraccional de gas total (Vf) registrado durante la fermentación in vitro del follaje de Acacia farnesiana (Af), Acacia polyacantha (Ap), Bauhinia variegata (Bv), Cassia fistula (Cf), Delonix regia (Dr), Erythrina coralloides (Ec), Jacaranda mimosifolia (Jm), Leucaena leucocephala (Ll), Moringa oleifera (Mo), Pithecellobium dulce (Pd) y Prosopis laevigata (Pl).
Grupo 4. Cassia fistula, Erythrina coralloides, Pithecellobium dulce y Bauhinia variegata. El valor de Vm para estas especies estuvo en el rango de 149.0 a 173.7 mL g−1 MS, sin diferencias entre medias (p > 0.05, Tabla 3). Sin embargo, el valor de S fue diferente entre especies (p ≤ 0.05) mostrando el valor más bajo para Cassia fistula, pero similar para Pithecellobium dulce y Erythrina coralloides (p > 0.05). El pH más bajo se observó con Cassia fistula y Pithecellobium dulce, sin diferencias entre ellas (p > 0.05). En este grupo se observó un comportamiento de Vf similar entre especies de las 2 a las 5 h de incubación (Figura 1D), excepto para P. dulce la cual mostró un incremento de la hora 2 a la 7 (p ≤ 0.05). Las diferencias más notables entre especies se observaron de las 24 a 48 h, y en el caso de Cassia fistula rebasó los 50 mL de gas g−1 MS (p ≤ 0.05).
Grupo 5. Cassia fistula, Jacaranda mimosifolia y Erythrina coralloides. Las especies de este grupo mostraron un valor de Vm entre 162.8 y 186.7 mL g−1 MS, sin diferencias entre medias (p > 0.05, Tabla 3), y de manera similar, no se observaron diferencias para el valor de S (p > 0.05), pero sí para pH (p ≤ 0.05), siendo menor para J. mimosifolia. En la Figura 1E se observa un comportamiento de Vf similar entre especies en las primeras 12 h de incubación (p > 0.05), y las diferencias significativas más notables entre especies se observaron a las 24 h (p ≤ 0.05), tiempo en el que J. mimosifolia rebasó los 60 mL g−1 MS.
Grupo 6. Moringa oleifera, Jacaranda mimosifolia y Cassia fistula. Este es el grupo de especies con los valores más altos de Vm, sin diferencias entre medias (p > 0.05; Tabla 3), las cuales estuvieron entre 173.7 y 188.8 mL g−1 MS. Sin embargo, estuvieron entre las especies con los valores más bajos de S, y no difirieron entre ellas (p > 0.05). Respecto a su pH, las medias fueron diferentes entre especies (p ≤ 0.05), siendo Jacaranda mimosifolia la de menor valor. En las especies de este grupo (Figura 1F), se observó un comportamiento similar de Vf (p > 0.05) en las primeras 7 h de incubación. Las diferencias significativas se observaron a las 24 h, destacando Jacaranda mimosifolia con un volumen mayor de gas (p ≤ 0.05). A las 48 h se observó que Moringa oleifera obtuvo el valor más alto de gas rebasando los 65 mL g−1 MS.
En la Tabla 4 se presentan las medias de Vm, S y pH final del medio obtenido de la fermentación in vitro del fruto de las especies evaluadas. Al igual que en el follaje, en el fruto se obtuvieron cinco grupos con base en las similitudes de las medias de Vm (Tabla 4), y se describen a continuación ordenados de menores a mayores valores de Vm del fruto:
Tabla 4 Volumen máximo de producción de gas total (Vm), tasa de producción de gas total (S) y pH de la fermentación ruminal in vitro del fruto de Jacaranda mimosifolia, Moringa oleifera y nueve especies de leguminosas forrajeras.
| Especie | Vm (mL g−1 MS) | S (h−1) | pH |
|---|---|---|---|
| Acacia farnesiana (L) Willd. | 196.02e | 0.041bc | 6.89a |
| Bauhinia variegata L. | 104.75b | 0.027a | 7.00cd |
| Delonix regia (Hook) Raf. | 149.35c | 0.032ab | 6.98bc |
| Erythrina coralloides D.C | 147.78c | 0.065d | 7.04de |
| Jacaranda mimosifolia D. Don | 60.88a | 0.038bc | 7.04de |
| Leucaena leucocephala Lam. | 134.66c | 0.039bc | 6.97bc |
| Moringa oleífera Lam | 73.72a | 0.029a | 7.09e |
| Pithecellobium dulce (Roxb.) Benth | 173.67d | 0.047c | 6.93ab |
| Prosopis laevigata Willd. | 190.80de | 0.078e | 6.93ab |
| EEM | 7.99 | 0.003 | 0.02 |
a,b,c,d,e,f,g Medias con diferente literal en superíndice dentro de columnas son diferentes (p ≤ 0.05); EEM = error estándar de la media. Vm = volumen máximo de producción de gas total (mL g−1 MS); S = tasa de producción de gas total (h−1).
Grupo A. Moringa oleifera y Jacaranda mimosifolia. Las especies de este grupo no presentaron diferencias (p > 0.05) entre medias para Vm y obtuvieron valores entre 60.88 y 73.72 mL g−1 MS (Tabla 4), y del mismo modo, el pH final no difirió (p > 0.05) entre especies y presentaron un promedio de 7.06. En el caso de S, las medias mostraron diferencias (p ≤ 0.05), siendo M. oleifera la de menor valor (0.029 h−1). La Figura 2A muestra el comportamiento de la curva de Vf de estas especies a través del tiempo, y se observó un comportamiento similar (p > 0.05) hasta las 24 h, pero a las 48 h Moringa oleifera superó (p ≤ 0.05) a J. mimosifolia.
Grupo B. Bauhinia variegata. Esta especie tuvo un valor de Vm superior a las especies del Grupo A y menor (p ≤ 0.05) al del resto de las especies (Tabla 4). Sin embargo, fue una de las especies con menor valor de S, junto con M. oleifera y D. regia sin diferencias entre medias (p > 0.05), mientras que el pH se mantuvo neutro junto con otras especies. La Figura 2B presenta la curva de Vf para B. variegata, y se observa un incremento notable de Vf a partir de las 24 h de incubación.
Grupo C. Delonix regia, Erythrina coralloides y Leucaena leucocephala. Las especies de este grupo tuvieron valores de Vm entre 134.66 y 149.35 mL g−1 MS, sin diferencias entre medias (p > 0.05; Tabla 4). Sin embargo, E. coralloides fue la que mostró mayores valores de S y pH respecto a las otras dos especies (p ≤ 0.05). En la Figura 2C, se presenta el comportamiento de Vf de estas especies, y se observó que difiere entre las especies de este grupo (p ≤ 0.05). Destaca E. coralloides, la cual obtuvo los valores más altos durante la primera 9 h de incubación, mientras que de las 24 a las 48, D. regia fue la de mayor valor de Vf (p ≤ 0.05) con más de 45 mL g−1 MS.
Grupo D. Prosopis laevigata y Pithecellobium dulce. Los valores de Vm para estas especies estuvieron entre 173.67 y 190.80 mL g−1 MS y no presentaron diferencias (p > 0.05) entre medias (Tabla 4), y del mismo modo, el pH final no difirió entre especies y en promedio fue de 6.93. Sin embargo, P. laevigata presentó mayor tasa de producción de gas que P. dulce (p ≤ 0.05). En este grupo se observó que el comportamiento de Vf entre especies fue diferente (p ≤ 0.05) durante las primeras 9 h, y P. laevigata obtuvo los valores más altos (Figura 2D). Las diferencias (p ≤ 0.05) se observaron también a las 24 y 48 h, tiempo en el que P. dulce registró el valor más alto.
Grupo E. Acacia farnesiana y Prosopis laevigata. Las especies de este grupo fueron las de mayor valor de Vm en comparación con el resto de las especies (Figura 2). Algo similar a lo ocurrido con las especies del Grupo D, ocurrió para las del Grupo 5 dado que A. farnesiana y P. laevigata mostraron valores de Vm y pH final similares (p > 0.05) entre sí (Tabla 4), con pH promedio de 6.91. Sin embargo, P. laevigata presentó mayor S con respecto a P. laevigata (p ≤ 0.05). Además, las especies de este grupo presentaron un comportamiento de Vf diferente en las primeras 9 h de incubación, donde P. laevigata registro los valores más alto (p ≤ 0.05), pero a las 24 a 48 h fue A. farnesiana quien registró los valores más alto en este grupo (p ≤ 0.05).
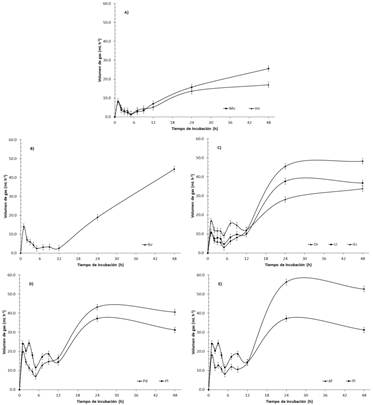
Figura 2 Volumen fraccional de gas total (Vf) registrado durante la fermentación in vitro del fruto de Acacia farnesiana (Af), Bauhinia variegata (Bv), Delonix regia (Dr), Erythrina coralloides (Ec), Jacaranda mimosifolia (Jm), Leucaena leucocephala (Ll), Moringa oleifera (Mo), Pithecellobium dulce (Pd) y Prosopis laevigata (Pl).
Discusión
Contenido de materia seca, materia orgánica y proteína cruda
Los resultados concuerdan con Pinto et al. (2002), quienes para especies como Acacia farnesiana (L) Willd, Pithecellobium dulce Lam y Leucaena leucocephala Lam obtuvieron valores de MS de 90 a 93%, de MO de 89 a 92%, y de PC de 18 a 21%. Mientras que Narváez y Lascano (2004) reportan para Delonix regia (Hook) Raf. valores de MS, MO y PC de 89.5, 90.3 y 21.2%, respectivamente; en tanto que Rodríguez et al. (2014) registraron para Moringa oleifera Lam un contenido de MS, MO y PC de 90, 91.8 y 22.2%, respectivamente. Para Prosopis laevigata Willd, Montañez-Valdez et al. (2021) reportaron valores de MS, MO y PC de 80.5, 89.6 y 13.4%, y Ndlovu y Nherena (1997) para Jacaranda mimosifolia D. Don reportan valores de MS, MO y PC de 90.4%, 92.4% y 95 g kg−1 MS, respectivamente. En tanto que Apráez (2014) reportan para Cassia fistula L. MS, MO y PC de 89.5, 92.6 y 16%, respectivamente. Estos autores mencionan que, hay variación en los valores de MS, MO y PC, probablemente por el efecto que tienen las estructuras botánicas de las plantas, su estado fenológico, época del año en que se colectan, frecuencia de corte y ambiente en que crecen. Para el contenido de MS, se encontró efecto del estado fenológico de la planta, ya que la mayoría del follaje y fruto fue cosechado en estado de fruto seco y solo para la Acacia polyacantha Willd fue cosechada cuando ya había terminado de fructificar. Al respecto, Ojeda et al. (2012) reportan diferencias en el contenido de MS en la época de sequía, lo que repercute en la humedad del tejido vegetal y justifica la variación entre especies de plantas evaluadas. También Guerrero-Rodríguez et al. (2021) observaron variación para la MS de hojas en arbustos leguminosos del trópico seco conforme la época de recolección.
Sobre el contenido de MS, Velázquez et al. (2011) en vainas de Acacia farnesiana (L) Willd reportan contenidos de MS, MO y PC de 89.6, 96.2 y 11.5%. Al respecto, para el huizache colectado en Cerritos, S. L. P. se tuvo un alto valor nutricional por su contenido de PC y concentración de aminoácidos esenciales no proteicos (ácido a-acetyldiaminobutirico), motivo por el que su vaina es valorada como recurso alimenticio de bajo costo para rumiantes. Al respecto, Rodríguez et al. (2014) reportan para Moringa oleifera Lam MS, MO y PC de 88.3, 92.6 y 18.4%, valores que son menores a los obtenidos en el presente estudio. Para Delonix regia (Hook) Raf. se reportan contenidos de MS, MO y PC de 90.7, 93.4 y 17.9%, respectivamente (Roa y Muñoz 2012), en tanto que para Pithecellobium dulce Lam se reportan contenidos de MS, MO y PC de 88.9, 94.2 y 18.6%, respectivamente (Pinto et al. 2002). En otro estudio, Espinoza et al. (1996) encontraron para Leucaena leucocephala Lam MS, MO y PC de 90.7, 91.8 y 20.37%, respectivamente. Para Prosopis laevigata Willd se reportan contenidos de MS de 90.6 y PC de 9.1% (García-López et al. 2019). Tanto los pastos como los forrajes son portadores de factores antinutricionales, pero aparecen en mayor concentración en las plantas con altos niveles de nitrógeno como las leguminosas. Los metabolitos como taninos totales, fenoles totales, taninos condensados totales, taninos condensados libres, alcaloides, saponinas, triterpenos, esteroides y flavonoides (Herrera et al. 2017), actúan principalmente en la digestión y la absorción de proteínas, pero también tienen influencia sobre la digestión de carbohidratos, utilización de minerales y la disponibilidad de vitaminas.
El uso de árboles y especies leguminosas representa una estrategia eficaz y sostenible para recuperar suelos, mejorar la biodiversidad y fortalecer la adaptación de los ecosistemas ante los restos de la agricultura sostenible y el cambio climático. Estas especies contribuyen al almacenamiento, la fijación de carbono (C), fijación biológica de nitrógeno y la restauración del suelo mediante relaciones simbióticas con microorganismos edáficos (Domínguez-Núñez 2022). Además, mejoran la calidad del forraje y ofrecen servicios ambientales, económicos y sociales que favorecen la protección y recuperación de los pastizales (Argüello et al. 2019).
Fermentación ruminal in vitro
La producción de gas total está asociada con la composición química del forraje, y es razonable considerar que, de acuerdo con la estequiometría de la fermentación ruminal, la fermentación de carbohidratos deriva en la producción de ácidos grasos de cadena corta (AGCC; acetato, propionato y butirato), CO2 y CH4, y el pH disminuyen a mayor concentración de AGCC. El gas producido durante la fermentación se genera por dos vías: la síntesis de AGCC y por la reacción de H+ con el bicarbonato, y la síntesis de acetato y butirato genera CO2 y H+; mientras que el CH4 se genera al reaccionar el CO2 con H+ (Williams 2000). Además, el volumen de gas producido durante la fermentación está asociado al grado de degradación del sustrato (Fondevila y Barrios 2001), por lo que el valor de Vm de la cinética de producción de gas es un indicador del grado en que se degrada el sustrato, mientras que el valor de S es indicador de la tasa de degradación del sustrato. En ese sentido se puede observar una variabilidad de perfiles de degradabilidad y fermentación de las especies evaluadas, y aunque en la literatura científica no se encontraron resultados sobre la cinética de producción de gas de todas las especies aquí evaluadas, se hacen comparaciones con la información disponible.
Para follaje, los resultados de Vm para Acacia polyacantha Willd fueron mayores a los reportados por Kaitho et al. (1998), quienes observaron 47.0 (mL g−1 MO). Mientras que Torres-Salado et al. (2018) reportaron valores mayores de Vm para Leucaena leucocephala Lam. donde se apreció 133.3 (mL g-1 MS), pero en valores de S fueron menores (0.03 h−1) en follaje de 35 días de edad de rebrote. Mientras que Hernández et al. (2010) reportan valores inferiores para Prosopis laevigata Willd. de 25.91 (mL g−1 MS) y datos de S menores a esta investigación (0.033 h−1). Para Moringa oleifera Lam. Alexander et al. (2008) determinaron valores menores de Vm a los aquí encontrados (88.3 mL g−1 MS).
En el caso del fruto, en general la variable V mostró diferencias significativas entre las especies estudiadas, para Acacia farnesiana (L) Willd y Prosopis laevigata Willd. Se tuvieron los mayores valores con 196.02 y 190.80 mL g−1 MS; los cuales superan a los obtenidos por Hernández et al. (2010) quienes reportan valores de 15.24 a 46.30 mL g−1 MS; pero menores a los de Rojas et al. (2018) con 234.8 mL g−1 MSen vainas de 30 plantas fisiológicamente maduras. Así mismo, los valores de S de estas especies fueron los más altos junto a Erythrina coralloides DC. con 0.065 (h−1); pero similares a los de Hernández et al. (2010) con valores de 0.066 (h−1) y menores a los encontrados por Rojas et al. (2018) con 0.0378 a 0.381 (h−1).
En general, la reducción del pH por debajo de 6.0, afecta de forma negativa la fermentación ruminal, lo que promueve disminución de la digestión de la MO y de la fibra, cambiando el tipo de AGV producidos (Sánchez-Santillán y Cobos-Peralta 2016). El pH ruminal refuerza el balance entre la capacidad amortiguadora y la acidez de la fermentación. Al disminuir el pH, se estrechan las relaciones acetato-propionato, por consecuencia al incrementarse el pH se amplían las relaciones (Hobson 1972). La composición de la dieta y las prácticas de alimentación influyen sobre el pH ruminal, ya que a medida que se incrementa la proporción de ingredientes de fermentación rápida disminuye el pH y viceversa (Kaufmann 1976). Aun cuando no puede definirse un pH óptimo en el medio ruminal, los microorganismos presentan cierto intervalo en el cual se reproducen mejor y su metabolismo es más eficiente. Los protozoarios manifiestan su principal desarrollo a pH cercano a 6.5 y son severamente afectados en pH superiores a 8 e inferiores a 5.5, donde este último es uno de los factores que más afecta su población (Hind et al. 1973). Al respecto, Cheng et al. (1984) concluyeron que, en condiciones ruminales de pH bajo, el ataque bacteriano a las paredes celulares es difícil y por lo tanto se reduce su digestión. Se considera que un pH ruminal superior a 6.2 es el óptimo para obtener una buena digestión de celulosa (Rodríguez y Llamas 1990). La importancia de amortiguar el pH a nivel ruminal tiene la finalidad de mantener el metabolismo de los microorganismos ruminales en un intervalo óptimo para su crecimiento.
Conclusiones
La composición química de las especies estudiadas fue variable, especialmente en la proteína, donde el grado de variabilidad fue mayor, tanto para el follaje como para el fruto. La especie Jacaranda mimosifolia de la familia Bignoniaceae fue la que presentó el menor porcentaje de proteína cruda y Moringa oleifera de la familia Moringaceae fue la que presentó el mayor valor. En cuanto al gas total, la producción fue variable entre todas las especies estudiadas, y dependió de pH, de tal forma que se observó una asociación negativa entre el pH final de la fermentación in vitrode fruto y hoja con la producción de gas total.











 nueva página del texto (beta)
nueva página del texto (beta)



