Introducción
En México, la producción de mezcal se concentra en los estados con denominación de origen, siendo Oaxaca el principal productor con 90.51%, seguido por Puebla (4.94%), Michoacán (1.33%), Durango (1.07%), San Luis Potosí (0.88%), Guerrero (0.68%), Zacatecas (0.30%), Tamaulipas (0.24%) y Guanajuato (0.05%) (COMERCAM 2024).
En Oaxaca, la producción de Agave representa una actividad de gran relevancia cultural, social y económica para la obtención de mezcal (Del-Valle et al. 2018, García et al. 2020, Sánchez et al. 2022). Este recurso no solo se considera un producto forestal y agrícola, sino que también se utiliza para elaborar artesanías, productos medicinales y agroalimentarios (Arrazola et al. 2020, Sánchez et al. 2022). Dado su amplio uso, el cultivo y la producción de Agave se realiza en altitudes que varían entre 1 389 hasta los 1 921 msnm (Martínez-Jiménez et al. 2019); lo que se ha reflejado en la expansión de su cultivo en laderas, el cambio de uso de suelo, la adopción de nuevas técnicas y tecnologías para mejorar la producción tradicional en viveros y campos (González et al. 2023). Las nuevas formas de producción acelerada han provocado el uso excesivo de agroquímicos para aumentar su producción y controlar daños causados por enfermedades y plagas, principalmente el picudo del agave (Scyphophorus acupunctatus) conocida como una de las plagas de mayor importancia por las repercusiones en la planta (Recéndiz-De la Mora et al. 2024). En tanto que, Palma et al. (2016) describen las etapas esenciales para la obtención de destilados en la cadena productiva del agave-mezcal: 1) método de reproducción, 2) producción de hijuelos o plántulas en vivero, 3) producción de agave en campo, 4) producción del destilado, 5) envasado y 6) comercialización. Villa Sola de Vega presenta todas las etapas, lo que ha inducido a la expansión en producción y superficie cultivada debido al aumento en la demanda de piñas como materia prima; esto promovió el aumento de costo por kilo, de $2.00 hasta $15.00 (González et al. 2023). Sola de Vega tiene la creciente demanda de plantas de Agave angustifolia producidas intensivamente en viveros con costos elevados de la materia prima y producción, reflejándose en precios de venta que oscilan desde $2.00 hasta $20.00 por planta, aunado a esto, las plantas no presentan uniformidad en altura, tamaño de piña y en su mayoría carecen de sanidad (Del-Valle et al. 2018).
La producción de plantas en viveros es una etapa crítica (Arrazola et al. 2020), donde se obtienen plantas de calidad, sanas e inocuas, con buen desarrollo radical, tamaño adecuado de roseta y altura apropiada. Estas características físicas les permiten tolerar el trasplante en campo, así como las condiciones edafoclimáticas y la exposición a otros factores bióticos (Crespo et al. 2013). Sin embargo, los recientes acontecimientos prolongados de sequía, escasez de lluvias, así como los efectos adversos de la producción extensiva en el suelo para aumentar rendimientos, hacen necesaria la búsqueda de soluciones sostenibles a fin de optimizar el método de fertilización convencional para la obtención de plantas de Agave angustifolia de calidad que toleren el trasplante en campo. Por tanto, el objetivo de esta investigación fue evaluar el efecto de aplicación de guano (abono orgánico de la región) en crecimiento de agave en vivero y en la calidad del suelo, como una alternativa para la producción sostenible de planta de Agave angustifolia.
Materiales y métodos
Área de estudio
Este trabajo se realizó en el periodo noviembre 2020 a junio 2023 en un vivero de A. angustifolia ubicado en el municipio de Villa Sola de Vega, Oaxaca, México (16° 51' 21" LN, 97° 12' 43" LO y 1 478 msnm) en un vivero de crecimiento de plantas de agave para campo. El suelo fue de tipo luvisol, clima templado subhúmedo con lluvias en verano, con precipitaciones de 900 mm y la temperatura promedio de 26 °C (INEGI 2010).
Instalación y desarrollo del experimento
Se construyeron cuatro camas de crecimiento de 1.5 m de ancho y 22 m de largo, en el que se aplicaron los tratamientos correspondientes en cada uno. El diseño experimental empleado fue completamente al azar, los tratamientos fueron: TEST (0 kg de guano m-2), TC (fertilización convencional con dos g L-1 de triple 20-20-20, Mezfer®), G6 (seis kg de guano m-2) y TCG6 (fertilización convencional combinada con seis kg de guano m-2). Posteriormente se realizó el trasplante de plántulas de Agave angustifolia de 35 días de germinación y altura promedio de 10 cm, previamente se desinfectaron las raíces con la solución de cupravit® al 30%. Las plántulas se trasplantaron a 15 cm entre cada planta en un arreglo topológico de tres bolillo. La humedad se mantuvo mediante sistema de riego localizado, el cual se aplicó con intervalo de diez días y con un gasto de 16 L h-1, por este medio se suministró la fertilización convencional a los tratamientos TC y TCG6 en la cama correspondiente.
Evaluación de tratamientos
En la evaluación se seleccionaron aleatoriamente 20 plantas por tratamiento, considerando cada planta como una unidad experimental. Las variables de crecimiento vegetal se evaluaron a los 208 días después del trasplante. La altura de planta se midió verticalmente con un flexómetro a nivel del suelo hasta la punta de la hoja más alta. El diámetro inferior del tallo se midió en dirección norte-sur utilizando un vernier digital, tomando la lectura en la parte media del tallo. El diámetro superior se obtuvo de igual manera en la zona media de la planta, a la altura de la roseta de hojas. El número de hojas desplegadas se contabilizó después de medir las rosetas y posteriormente se separaron del tallo. Las hojas fueron secadas en horno de aire forzado a 70 °C durante 10 días, hasta el registro de peso constante y con ello se calculó el porcentaje de humedad y biomasa seca. La determinación de sólidos solubles totales de savia se realizó con un refractómetro HANNA®, para cada tratamiento se tomaron cuatro plantas, se molieron los tallos en fresco para obtener la savia.
La cuantificación de bacterias fijadoras de nitrógeno y colonización micorrízica se realizó en muestras de rizosfera y raíz de agave. Para ello, se tomaron diez submuestras de suelo por tratamiento, a 10 cm de profundidad en la parte central de cada cama de crecimiento, también se extrajeron 10 plantas de agaves completas.
La cuantificación de bacterias fijadoras de nitrógeno se llevó a cabo en cada tratamiento mediante diluciones seriadas (de 10-2 a 10-6), sembradas por triplicado en placas con agar que contenían una fuente combinada de carbono (C), según el método descrito por Rennie et al. (1981) y detallado por Zúñiga (2012). Finalmente, se realizó el conteo de colonias a las 24 horas de la siembra y se calcularon en unidades formadoras de colonias (UFC) por gramo de suelo rizosférico.
El porcentaje de colonización micorrízica se determinó mediante el método de Biermann y Linderman (1981), el cual consistió en aclarado y la tinción de las raíces más finas y delgadas con azul de tripano. Las muestras se montaron en portaobjetos y se observaron al microscopio óptico a 10X; la colonización se calculó a partir de la presencia de al menos una de las estructuras fúngicas características: vesículas, micelio intra-radical o arbúsculos.
Se realizaron dos evaluaciones de fertilidad física y química del suelo, la primera antes del establecimiento y la segunda después de la evaluación experimental. Para la primera, se tomaron 15 submuestras en todo el lote y se formó una muestra compuesta. En la segunda evaluación, se tomaron 10 submuestras por cada tratamiento y se formó una muestra compuesta para cada uno. En ambos, se extrajeron a 25 cm de profundidad, mediante el método de zigzag, se rotularon y enviaron al laboratorio para su análisis. En el laboratorio se realizó el proceso de análisis con la metodología descrita en la NOM-021-SEMARNAT-2000.
Análisis estadístico
En el análisis de datos se utilizó el software R-Studio, versión 4.2.2. Se realizó la prueba de Shapiro-Wilk para verificar la normalidad de los datos y la prueba de Bartlett para evaluar la homogeneidad de varianzas. Posteriormente, se realizó el ANOVA (Alpha = 0.95) y posteriormente la comparación de medias mediante la prueba de Tukey (P ≤ 0.05).
Resultados
En las variables de crecimiento evaluadas, se obtuvieron diferencias estadísticas significativas entre tratamientos (Figuras 1 y 2). El mayor número de hojas desplegadas (Figura 1a) se obtuvo con la adición de guano (G6) como fuente de fertilización y el menor con el tratamiento sin fertilización (TEST). Resultados similares se registraron en la altura de las plantas, la mayor altura en el tratamiento G6 respecto al tratamiento testigo (Figura 1b).
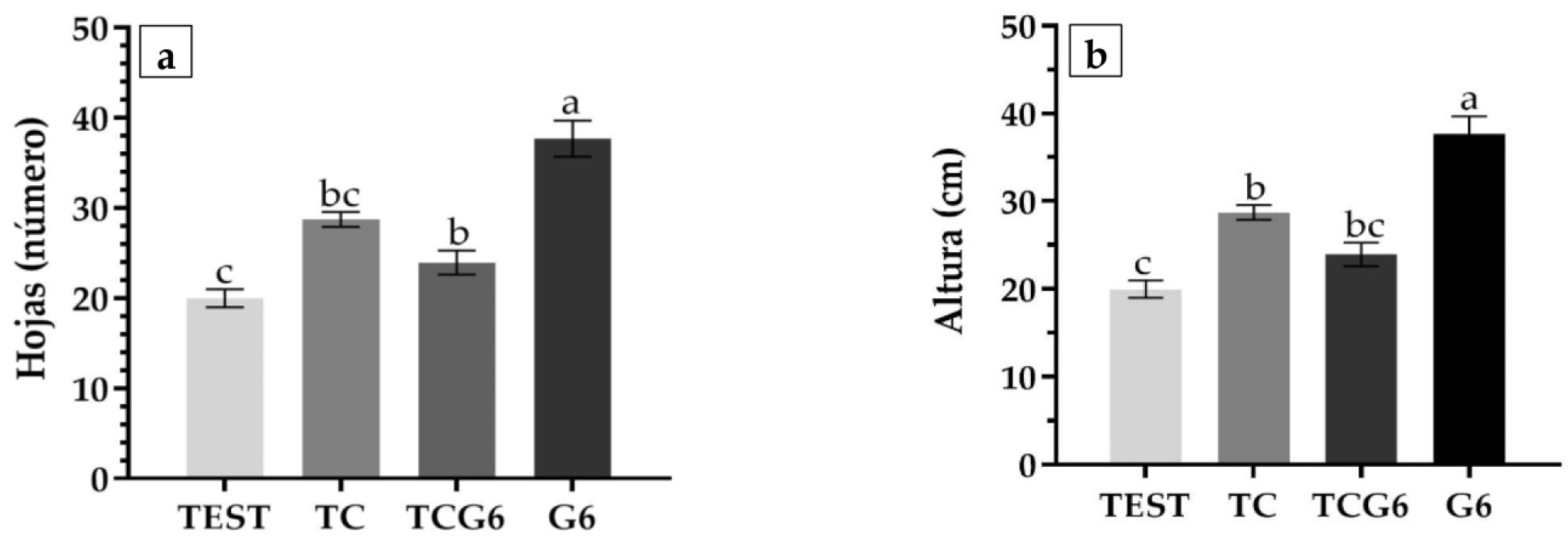
Figura 1 Variables de desarrollo en Agave angustifolia. a) Número de hojas desplegadas, b) Altura de la planta. Barras ± error estándar con letras distintas, indican diferencias estadísticas (Tukey ≤ 0.05).
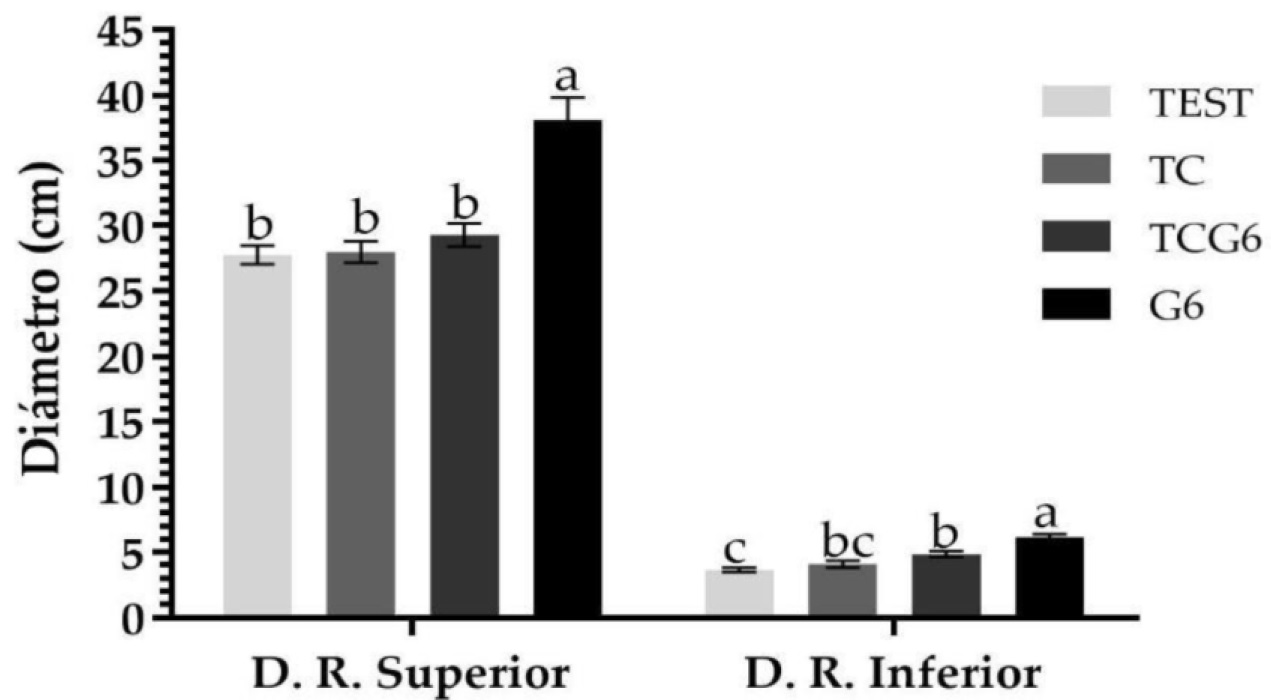
Figura 2 Diámetro de roseta (D.R.), superior e inferior de Agave angustifolia. Barras ± error estándar con letras distintas, indican diferencias estadísticas (Tukey ≤ 0.05).
Se encontraron diferencias estadísticas significativas entre tratamientos para las variables de diámetro superior e inferior de la roseta, destacando el tratamiento G6 en comparación con el tratamiento testigo (Figura 2).
En las variables de biomasa seca y humedad, los tratamientos presentaron diferencias estadísticas significativas (Figura 3); la combinación de guano con fertilizante inorgánico (TCG6) incrementó el porcentaje en peso, mientras que el tratamiento sin fertilización (TEST) registró menor biomasa. Resultados similares se obtuvieron en el contenido de humedad (Figura 3).
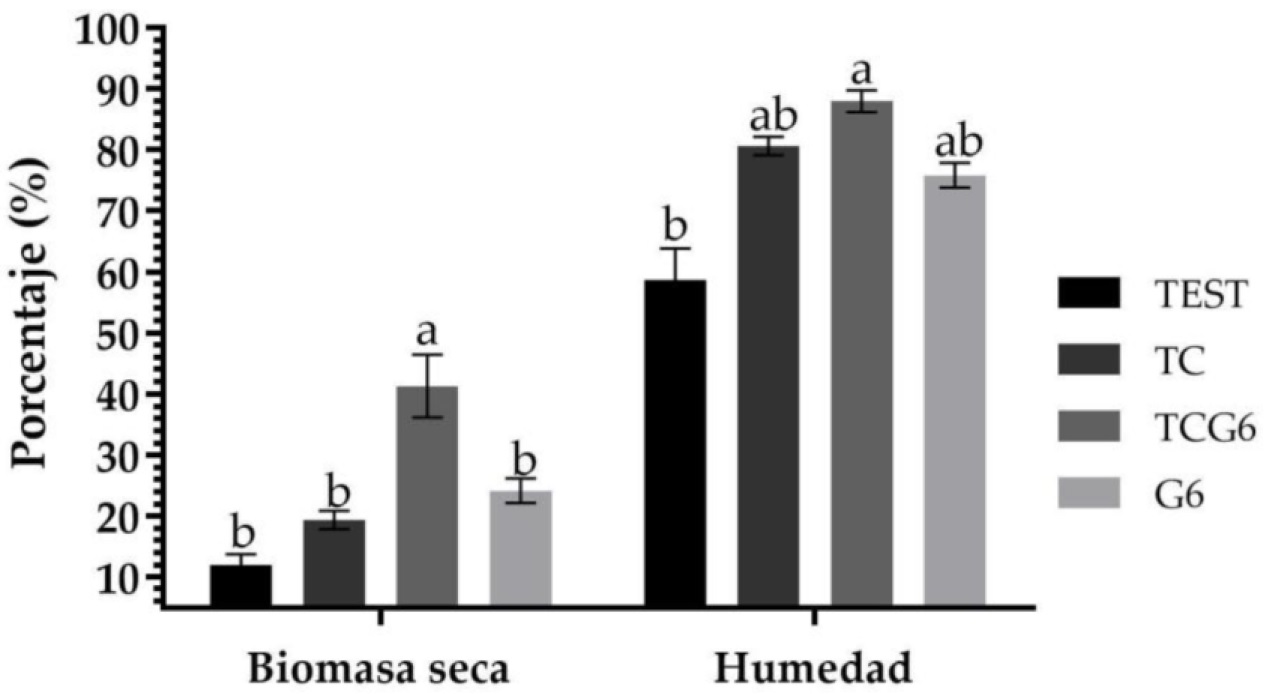
Figura 3 Biomasa seca vegetativa y porcentaje de humedad en parte vegetativa de Agave angustifolia. Barras ± error estándar con letras distintas, indican diferencias estadísticas (Tukey ≤ 0.05).
La cantidad de sólidos solubles totales, expresados en grados Brix, se presentó en mayor concentración en el tratamiento TCG6, seguido del tratamiento G6, mientras que el resto de los tratamientos no fueron estadísticamente diferentes (Figura 4).
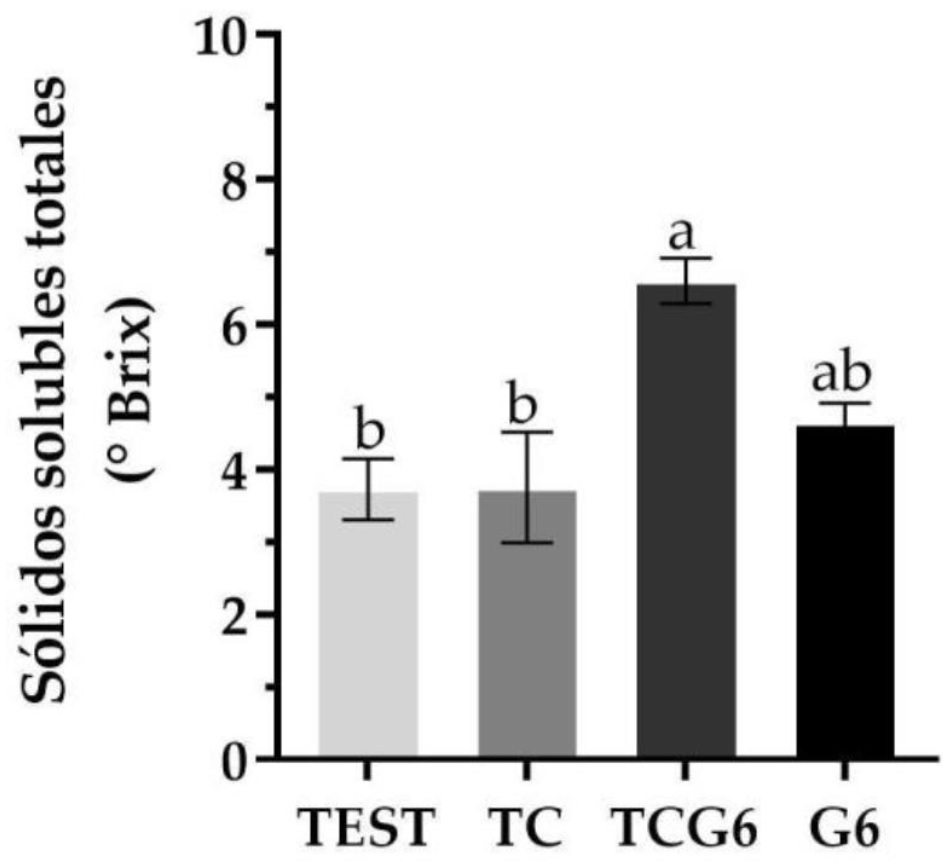
Figura 4 Concentración de sólidos solubles totales de la roseta inferior en Agave angustifolia. Barras ± error estándar con letras distintas, indican diferencias estadísticas (Tukey ≤ 0.05).
En la colonización micorrízica en raíces de agaves se presentaron diferencias estadísticas significativas entre tratamientos (Figura 5a) y los mejores resultados se registraron con el tratamiento TCG6 (fertilizante triple 20-20-20 y guano); mientras que los tratamientos TC, G6 y TEST presentaron colonizaciones menores.
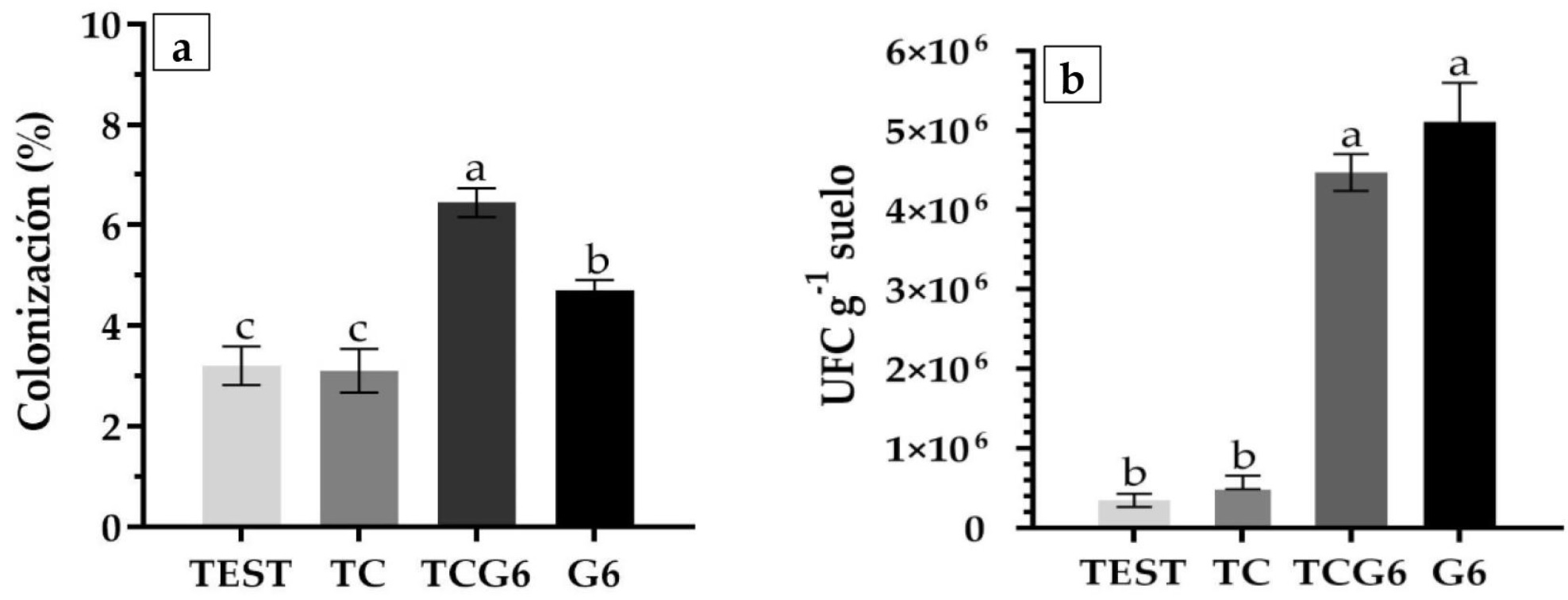
Figura 5 Rizosfera de Agave angustifolia. a) Colonización micorrízica en raíces, b) Unidades formadoras de colonias (UFC) con capacidad de fijación biológica de nitrógeno atmosférico. Barras ± error estándar con letras distintas, indican diferencias estadísticas (Tukey ≤ 0.05).
La adición de guano al suelo incrementó la diversidad microbiana benéfica y la disponibilidad de nutrimentos; esto se mostró en el incremento de microorganismos rizosféricos de vida libre con capacidad de fijación de nitrógeno atmosférico de los tratamientos G6 y TCG6, mientras que los tratamientos sin aplicación de guano presentaron menores valores de unidades formadoras de colonias como se muestra en la Figura 5b.
El análisis físico y químico del suelo mostró que la adición de guano mejoró aspectos importantes del suelo, como la densidad aparente y el porcentaje de materia orgánica, lo que derivó en mayor disponibilidad de nutrimentos en comparación con el tratamiento testigo. En este sentido, el aumento en la cantidad de guano por unidad de superficie elevó los niveles de fertilidad y mejoró la calidad del suelo (Tabla 1).
Tabla 1 Análisis de parámetros físicos y químicos del suelo en los tratamientos evaluados.
| Parámetros | Análisis inicial | Análisis Final /Tratamientos | |||
|---|---|---|---|---|---|
| TEST | TC | TCG6 | G6 | ||
| Densidad Aparente (g cm-3) | 1.41 | 1.39 | 1.35 | 1.31 | 1.19 |
| Textura | Franco arcillo arenoso | Franco arcillo arenoso | Franco arcillo arenoso | Franco arcillo arenoso | Franco arcillo arenoso |
| pH | 7.81 | 7.75 | 7.72 | 7.80 | 7.29 |
| Conductividad Eléctrica (dS m-1) | 0.35 | 0.32 | 0.29 | 0.28 | 0.88 |
| Materia orgánica (%) | 1.05 | 1.12 | 1.23 | 3.89 | 4.73 |
| Nitrógeno inorgánico (mg kg-1) | 12.80 | 11.50 | 15.10 | 9.84 | 106.92 |
| Fósforo (mg kg-1) | 1.12 | 1.08 | 2.38 | 1.94 | 17.78 |
| Potasio (mg kg-1) | 149.00 | 154.00 | 191.00 | 146.00 | 184.00 |
| Calcio (mg kg-1) | 13 827.00 | 13 471.7 | 12 568.10 | 13 860.4 | 12 770.40 |
| Magnesio (mg kg-1) | 509.00 | 421.68 | 348.76 | 387.96 | 341.50 |
| Azufre (mg kg-1) | 1.89 | 2.84 | 2.10 | 2.88 | 6.96 |
Discusión
Las respuestas obtenidas por la aplicación de fertilizante inorgánico y orgánico en las variables de crecimiento presentaron diferencia estadística significativa. Se observó al inicio del trasplante que los magueyes del tratamiento con seis kg m-2 de guano mostraron estrés y pérdida de hojas, mientras que, las plantas del tratamiento convencional crecieron de manera continua. La aplicación de guano al suelo incrementó el contenido de materia orgánica, mejoró sus características físicas, la retención de humedad y la disponibilidad de nutrimentos para su absorción por las plantas. Estos efectos se reflejaron en un mayor crecimiento en altura, mayor número de hojas desplegadas y un mayor diámetro de roseta, en comparación con el tratamiento testigo y la fertilización convencional. Esto coincide con otros autores que han documentado la producción de agave en vivero con diversas fuentes nutrimentales y han observado respuestas similares, como Del-Valle et al. (2018), quienes obtuvieron incrementos significativos de altura al aplicar abonos orgánicos y solución nutritiva en plantas micropropagadas de Agave angustifolia. Mientras que Canales et al. (2021) indicaron que la aplicación de abonos orgánicos en plántulas de Agave cupreata Trel y Berger en fase de vivero incrementó el crecimiento en altura, número, longitud y ancho de hojas, así como diámetro de roseta.
Los valores mayores de diámetro de roseta inferior se obtuvieron en plantas del tratamiento G6; esta es una variable de importancia al momento del trasplante en campo; se ha observado que mientras mayor diámetro del tallo, la respuesta de adaptación y generación de raíces adventicias es mayor, así como la tolerancia al estrés abiótico. Al respecto, Crespo et al. (2013) reportaron que en plántulas de A. tequilana Weber con aplicación de composta de gabazo de agave 50% mejoró el diámetro tallo, número de hojas y longitud de hoja en comparación con turba y polvo de coco.
La biomasa seca total de las plantas, así como la concentración de sólidos solubles totales en la piña, se incrementaron con la aplicación combinada de guano y fertilización inorgánica. Se ha reportado que las plantas bajo un manejo agronómico adecuado presentan un crecimiento más eficiente y mayores valores de °Brix (Canales et al. 2021, Sánchez-Mendoza et al. 2022). En este sentido, Arrazola et al. (2020), en un ensayo con plántulas de A. salmiana bajo fertirriego con solución Steiner al 25 % mejoró el número de hojas desplegadas, ancho de hoja, biomasa seca total y biomasa seca de raíz; no obstante, el diámetro de la roseta fue superior con la solución Steiner al 100% y ningún tratamiento mostró efecto sobre el contenido de azúcares totales en el tejido foliar. Mientras que Martínez et al. (2013) indicaron que la fertilización de plántulas de A. angustifolia y A. potatorum con 30-20-15 de N-P2O5-K2O mejoró el crecimiento (diámetro de roseta, hojas desplegadas y biomasa seca) de ambas especies. En A. potatorum la fertilización con N (47.5 mg kg1) y P (42.5 mg kg1) incrementa 77.4% los sólidos solubles totales en tallo, por el contrario, cuando se aplica N (47.5 mg k-1) y P (0 mg kg1) el número de hojas desplegadas incrementa de 7.7 a 14.6 hojas, respecto al testigo (Sánchez et al. 2022).
La adición de guano al suelo estimuló la presencia de bacterias fijadoras de nitrógeno en la rizosfera. Además, la combinación de guano con fertilizantes inorgánicos promovió una sinergia entre los hongos micorrízicos y su hospedante, favoreciendo su desarrollo y crecimiento a través de una asociación simbiótica. Esta asociación beneficia al hospedero al facilitarle nutrimentos, agua y tolerancia al estrés y a cambio el hospedero le confiere azúcares obtenidos de la fotosíntesis (García et al. 2020). Mientras que Bautista y Martínez (2020), mostraron que Flavobacterium sp. incrementa 164.8% la producción de biomasa seca total y Paenibacillus amylolyticus aumenta tres veces más la biomasa seca del tallo con respecto al control y presentan efectos positivos en diámetro de roseta, altura y área foliar. Por otro lado, el uso de consorcio micorrízico nativo (Acaulospora denticulata, Acaulospora scrobiculata, Acaulospora spinosa, Claroideoglomus etunicatum, Diversispora aurantia y Glomus desertícola) en bulbillos florales de A. tequilana Weber obtuvo 30.7% de colonización y la producción de biomasa fresca aumentó 60.8% (Quiñones et al. 2023).
Respecto a la calidad y fertilidad del suelo, el guano mejora la calidad física del suelo como la porosidad, consistencia, e incluso su interacción con los organismos del suelo y con ello el desarrollo de las plantas (Valladares et al. 2020); el guano tiene un alto contenido de fósforo, potasio, nitrógeno y hierro, y su liberación lenta o gradual de nutrimentos proporciona una mayor disponibilidad y acceso nutricional para el agave (Pinochet et al. 2017), por tanto, garantiza un abastecimiento constante y eficiente para la planta y promueve un equilibrio del microbioma rizosférico.
Conclusiones
La aplicación de abono orgánico al suelo incrementa el contenido de materia orgánica, fomenta la diversidad biológica en la rizosfera, mejora la retención de humedad, las propiedades físicas y químicas del suelo y con ello la disponibilidad de nutrientes. En Agave angustifolia, este tipo de fertilización favorece el crecimiento y el aumento de tamaño de piña. Por ende, el guano es una alternativa sostenible de fertilización para la producción de plantas de agave en vivero.











 nueva página del texto (beta)
nueva página del texto (beta)



