Introducción
El pez diablo (Hypostomus plecostomus) es una especie nativa de la cuenca del Amazonas en América del Sur. Sin embargo, se ha convertido en un problema ambiental para varios países, principalmente América del Norte y el Sudeste Asiático. Se considera una especie invasora exótica que altera el funcionamiento de los elementos que integran un ecosistema y deteriora los servicios ambientales del lugar donde se introduce (Peña et al. 2019). Recientemente, ha sido catalogado como "muy alta amenaza" de ser o convertirse en invasor (Vilizzi et al. 2019). Estos peces han invadido exitosamente aguas dulces en América, África, Asia y las islas del Pacífico.
La explotación para su control y erradicación aún es limitada. A veces se capturan con la única intención de evitar que causen un impacto en los ecosistemas acuáticos, sin darles ningún otro uso; otras veces su carne se utiliza para producir alimentos (Mendoza et al. 2007, Orfinger y Goodding 2018). Por lo tanto, se deben investigar nuevos usos para aprovechar su biomasa y controlar y erradicar su población, o valorar sus residuos (huesos), que pueden aprovecharse para el ensilaje y la diversificación de los alimentos para peces (Aguilera-Flores et al. 2021).
En México, especialmente, han sido introducidos accidental o intencionalmente fuera de su distribución natural. Su dispersión es una amenaza para la diversidad biológica, causando daños al ambiente, a la economía y a la salud humana (Zworykin et al. 2023). Esta especie se considera como la segunda causa a nivel global de la pérdida de biodiversidad (Rodríguez et al. 2001, Leung et al. 2002). Además, diversos ecosistemas se han visto modificados debido, entre otras causas, a la aparición de esta especie exótica invasora, que tiene un elevado potencial para afectar negativamente al ecosistema, ya que desplaza a las especies nativas por competencia directa, depredación, transmisión de enfermedades, modificación del hábitat y alteración en la estructura de los niveles tróficos (Cisneros et al. 2023). En ocasiones, las especies invasoras se hibridan con especies nativas, alterando así el banco genético original del ecosistema. La captura del pez diablo en estos ecosistemas ha crecido exponencialmente, generando problemas de índole ecológico, económico y social. Por lo tanto, el pez diablo puede desestabilizar la comunidad de peces endémica y alterar la estructura del ecosistema (Mooney et al. 2001).
El quitosano es un polisacárido que se obtiene a partir de la quitina, el segundo polisacárido más abundante en la naturaleza. Es un copolímero lineal formado por residuos de unidades de D-glucosamina en mayor medida y N-acetil D-glucosamina en menor medida, distribuidos aleatoriamente y unidos por enlaces β 1,4. Según la Unión Internacional de Química Pura y Aplicada (IUPAC), es 2-amino-2-desoxi-D-glucopiranosa (D-glucosamina GlcN) y 2-acetamida-2-desoxi-D-glucopiranosa (N-acetil glucosamina). Tiene la capacidad de ser biodegradable, es biocompatible y no tóxico, por lo que se considera un compuesto muy atractivo. Su importancia comercial radica en su aplicación en diversas áreas como la biotecnología, farmacéutica, biomédica, alimenticia y agricultura (Matica et al. 2019, Khrunyk et al. 2020 y Minh et al. 2020). Por lo tanto, existe interés en la purificación de este biopolímero debido a la necesidad de tener sustratos y procesos más económicos. Se sabe que el quitosano se encuentra en elevada concentración en exoesqueletos de crustáceos y escamas de peces, siendo la corteza o placas dérmicas del pez diablo una nueva fuente exótica de explotación, debido a la similitud en el contenido de quitosano (López et al. 2016, Sánchez et al. 2020). Últimamente, algunos autores como Muslim et al. (2013), García et al. (2016), Sebaaly et al. (2021), Selvakumar et al. (2021), Kumaran et al. (2021), Joseph et al. (2021), Alghurabi et al. (2022), Cutajar et al. (2022) y Dinculescu et al. (2024) han comenzado a explorar la extracción y caracterización de quitosano a partir de escamas residuales de tilapia roja (Oreochromis sp), tilapia del Nilo (Oreochromis niloticus), Labeo rohita, pez Carpa (Cyprinus carpio), trucha arcoíris (Oncorhynchus mykiss), entre otras. Por tal razón esta investigación propone un plan de prevención y control de la especie, para disminuir su dispersión e impacto a través de la obtención de quitosano a partir de una fuente exótica invasora. El procedimiento para obtenerlo consiste en aislarlo de proteínas, minerales; generalmente calcáreos y pigmentos. Las etapas de este procedimiento se denominan procesos de desproteinización, desmineralización y caracterización de la quitina en relación con su contenido de humedad, grado de desacetilación y contenido de nitrógeno, entre otros, permitiendo reconocer su calidad (Reyes-Pérez et al. 2020). En base a lo anterior, el objetivo de esta investigación fue extraer, caracterizar y evaluar la purificación química del quitosano a partir de corazas tegumentarias de peces diablo comparándolo con quitosano comercial a base de exoesqueletos de camarón.
Materiales y métodos
Obtención y tratamiento de la muestra
Para la realización de esta investigación se utilizaron dos muestras, la primera de pez diablo (Hypostomus plecostomus) adquiridas por pescadores establecidos en el mercado municipal de Loma Bonita, Oaxaca y la segunda fueron desechos de camarón, los cuales se obtuvieron en la ciudad y puerto de Alvarado, Veracruz. Éstas se lavaron previamente con agua potable y destilada, se despulparon quitando el exceso de carne y viseras para la obtención de las placas dérmicas, secándose a 50 °C por 12 h (Horno, marca: Scorpion scientific, modelo: A62060, USA). Una vez limpios, se ultracongelaron a -65 °C, posteriormente se liofilizaron a temperatura -40 °C y vacío de -133 mBar con una liofilizadora (Labconco 77540-00, MO, USA.). A la postre, se molieron (Molino ProctorSilex® 72500RY, Japón) y tamizaron (Tamiz No. 50 Test Sieve 090233332 Alemania) a un tamaño de partícula de 300 µm. Finalmente, la harina se almacenó en bolsas herméticas medianas de 18 × 20 cm (Ziploc, Johnson y Sons, Inc., Racine, WI, USA) protegiéndola de la humedad y la luz hasta su posterior uso.
Tratamiento químico
Hidrólisis alcalina (Desproteinización)
Se realizó en vasos de precipitado de 2.0 L con una solución acuosa de Hidróxido de Sodio (NaOH) a 0.4 M, a una relación (1/15) peso volumen (p/v) y agitación constante a 1 000 rpm durante 3 h a temperatura de 28 °C. Al término, la muestra sólida se lavó con agua corriente hasta la neutralidad.
Hidrólisis ácida (Desmineralización)
Esta se efectuó en vasos de precipitado de 2.0 L conteniendo una solución de ácido clorhídrico (HCl) a 0.6 N en una relación (1/15) (p/v) y agitación constante de 1 000 rpm durante 1 h a temperatura de 25 °C. Una vez concluida se lavó con agua corriente hasta la neutralidad.
Desacetilación
Se realizó en vasos de precipitado de 2.0 L con una solución acuosa de Hidróxido de Sodio (NaOH) al 40%, con una relación (1/15) peso volumen (p/v) y agitación constante a 1000 rpm durante 5.5 h a una temperatura de 110 °C. Al término, la muestra sólida se lavó con agua corriente hasta la neutralidad.
Despigmentación
Se realizó empleando un doble blanqueado, el cual consistió en resuspender los residuos desproteinizados, desmineralizados y desacetilados (utilizando matraces de 2.0 L) en una solución de Hipoclorito de Sodio (NaClO) al 38%, bajo agitación constante (1 000 rpm) a temperatura ambiente durante 20 min. Al término del primer blanqueado, las muestras fueron filtradas y resuspendidas por segunda vez en hipoclorito bajo las condiciones antes descritas. Las muestras resultantes se lavaron hasta llegar a neutralidad y se secaron a 35 °C durante 24 h (Horno, marca: Felisa, modelo: FE-132AD, México) conforme a las condiciones determinadas por Amador-Mendoza et al. (2022).
Análisis de las muestras quitinosas
Se tomaron muestras por triplicado (3 a 5 g por determinación) de exoesqueletos de camarón y placas dérmicas pez diablo (Hypostomus plecostomus), provenientes de las diferentes etapas de purificación: desproteinización, desmineralización, desacetilación y despigmentación, para sus respectivos análisis de humedad, proteínas (Kjeldahl), minerales (Cenizas), lípidos (Soxhlet), potencial de hidrógeno (pH) y determinación de color (Colorímetro ColorFlex EZ, marca: ColorFlex Hunter Lab, model: DIFUSE, USA).
Análisis de las muestras tratadas
Acordes a los métodos estándar (AOAC 2005), se cuantificó el % de proteínas y % de minerales (cenizas) en las muestras quitinosas resultantes de los diferentes tratamientos de purificación en los exoesqueletos de camarón y placas dérmicas del pez diablo (Hypostomus plecostomus). Por último, los porcentajes de desmineralización (% DM) y desproteinización (% DP) fueron calculados por la siguiente ecuación.
Donde, “Y” es el porcentaje de desmineralización o desproteinización, “x0” y “xf” son el porcentaje inicial y final del contenido de cenizas o proteínas respectivamente, “s0” y “sf” el peso inicial y final de las muestras tratadas (g) respectivamente.
Caracterización de las muestras quitinosas
Determinación de solubles
El contenido de solubles se determinó por diferencia de peso al disolver 0.5% (p/v) de muestra quitinosa en una solución de ácido acético 0.1 M y dejando en agitación a 200 rpm por 24 h, posteriormente fue filtrado y llevado a peso constante (Kasaai et al. 2000). La solubilidad del quitosano (Q) en medio acuoso fue evaluada mediante la determinación de la turbidez por espectrofotometría UV-visible a una longitud de onda de 450 nm, basado en el método descrito por Chen y Park 2003.
Determinación del peso molecular
El peso molecular se calculó determinando la viscosidad intrínseca η , empleando como solvente una solución de ácido acético glacial (2%) y acetato de sodio (0.2 M). Los parámetros se determinaron empleando la ecuación de Mark-Houwink-Sakurada (MHS) y las constantes determinadas a y k para el disolvente empleado (Shrinivas et al. 2005, Mao et al. 2007, Pacheco-Aguilar et al. 2009).
Dónde: k = 1.38 x 10-5 L/g; a = 0.85; PM = Peso Molecular.
Obtención de espectros infrarrojo (FTIR)
Se obtuvieron espectros infrarrojos de las muestras de quitosano a partir de camarón y pez diablo (Hypostomus plecostomus), se utilizó como blanco el quitosano comercial (Sigma-Aldrich México). Estas muestras fueron pulverizadas (<0.5 mm de diámetro) y mezcladas con Bromuro de potasio (KBr) a una relación 1:15, para obtener pastillas (160 mg). Estas fueron analizadas por espectroscopía de infrarrojo en un intervalo de 400-4 000 cm-1 utilizando un espectrofotómetro e interferómetro con reflectancia total atenuada (Perkin Elmer, DYNASCAN espectrum 100, USA), obtenidos con una resolución de 4 cm-1 en un rango de 4 000-515 cm-1 con un total de 16 barridos.
Análisis termogravimétrico (TGA)
El análisis termogravimétrico se llevó a cabo en un analizador térmico Discovery TA Instruments (EE.UU.), en un rango de temperatura de 30 a 700 °C, con una velocidad de calentamiento de 10 °C/min en atmósfera inerte de nitrógeno con una velocidad de flujo de 20 mL/min.
Microscopia Electrónica de Barrido (SEM)
La morfología superficial de las muestras se examinó mediante un microscopio de barrido con emisión de campo (FE-SEM) de la marca Tescan, modelo MIRA 3LMU, de alta resolución, con un detector de electrones secundarios. Las muestras se secaron y recubrieron de oro mediante un bombardeo iónico de capa fina, y se observaron con una aceleración de voltaje de 10 kV.
Análisis estadístico
Se llevó a cabo un diseño completamente al azar en los experimentos variando el tipo de tratamiento. El porcentaje de humedad, cenizas, proteínas, lípidos, pH y color, fueron considerados como las variables de respuesta utilizándose el programa MINITAB® versión 21.0 (2022). Así mismo, se realizó una comparación de medias agrupadas con un análisis de varianza (ANDEVA) y una comparación con la prueba de Tukey para verificar si las diferencias fueron estadísticamente significativas (P ≤ 0.05).
Resultados
Análisis proximal de fuentes quitinosas
En la Tabla 1 se presentan los resultados del análisis proximal, se encontró que el porcentaje de humedad de los exoesqueletos de camarón y placas dérmicas del pez diablo fue de 40.75 ± 0.01 y 22.01 ± 0.01%, cenizas 45.85 ± 0.02% y 42.31 ± 0.03%, proteínas de 50.78 ± 0.01% y 51.69 ± 0.01%, grasas 1.43 ± 0.01% y 10.64 ± 0.02%, y pH de 0.6.9 ± 0.02 y 5.14 ± 0.01. Así mismo, se observó que si existe diferencia significativa entre los porcentajes proximales de los exoesqueletos de camarón y placas dérmicas del pez diablo (p < 0.05).
Tabla 1 Composición proximal de fuentes quitinosas.
| Determinación | Fuentes quitinosas | |
|---|---|---|
| Camarón | Pez diablo | |
| Humedad (%) | 40.75 ± 0.01 | 22.01 ± 0.01 |
| Cenizas (%) | 45.85 ± 0.02 | 42.31 ± 0.03 |
| Proteínas (%) | 50.78 ± 0.01 | 51.69 ± 0.01 |
| Grasas (%) | 1.43 ± 0.01 | 10.64 ± 0.02 |
| pH | 6.9 ± 0.02 | 5.14 ± 0.01 |
Promedio de tres repeticiones ± error estándar de las pruebas realizadas por triplicado.
Hidrólisis química
La Tabla 2 presenta los resultados obtenidos mediante el método químico, mostrando el contenido de proteínas (0.54 y 1.19%) y de cenizas (0.79 y 0.62%) en el camarón y el pez diablo, respectivamente. Los porcentajes de desproteinización fueron de 98.91 y 97.67%, y para la desmineralización de 98.19 y 97.95% respectivamente. Por último, en los exoesqueletos de camarón se presentó una despigmentación con valores medios de L, A y B, es decir, de “Naranja suave” (#E3A87B) a “Naranja muy pálido (principalmente blanco)” (#FFF7F0), se presentaron diferencias estadísticamente significativas (p < 0.05) para ambos sustratos.
Tabla 2 Porcentajes de proteínas, cenizas y descripción del color obtenidos mediante el método químico en los exoesqueletos de camarón y placas dérmicas del pez diablo.
Promedio de tres repeticiones ± error estándar. Valores promedio que no comparten una letra son significativamente diferentes (P > 0.05).
Las placas dérmicas del pez diablo mostraron valores de L, A y B, de “Café desaturado muy oscuro” (#653D2A) a “Pálido grisáceo claro” (#EADEDF), con diferencias significativas (p < 0.05). Este estudio es pionero en evaluar la despigmentación mediante colorimetría CIE-LAB en muestras quitinosas purificadas de pez diablo.
Caracterización de muestras quitinosas
El estudio por espectroscopia infrarroja con transformada de Fourier (FT-IR) fue realizado en muestras quitinosas que provenían de las placas dérmicas del pez diablo (Hypostomus plecostomus) y desechos de camarón obtenidas por un tratamiento de hidrólisis química (Figura 1). En este estudio pueden distinguirse las señales típicas del infrarrojo del quitosano-UNPA (camarón), quitosano pez diablo comparados con un blanco comercial quitosano (Sigma-Aldrich México). Se observan bandas de absorción entre 3433 y 3255 cm-1 correspondientes al estiramiento O-H.
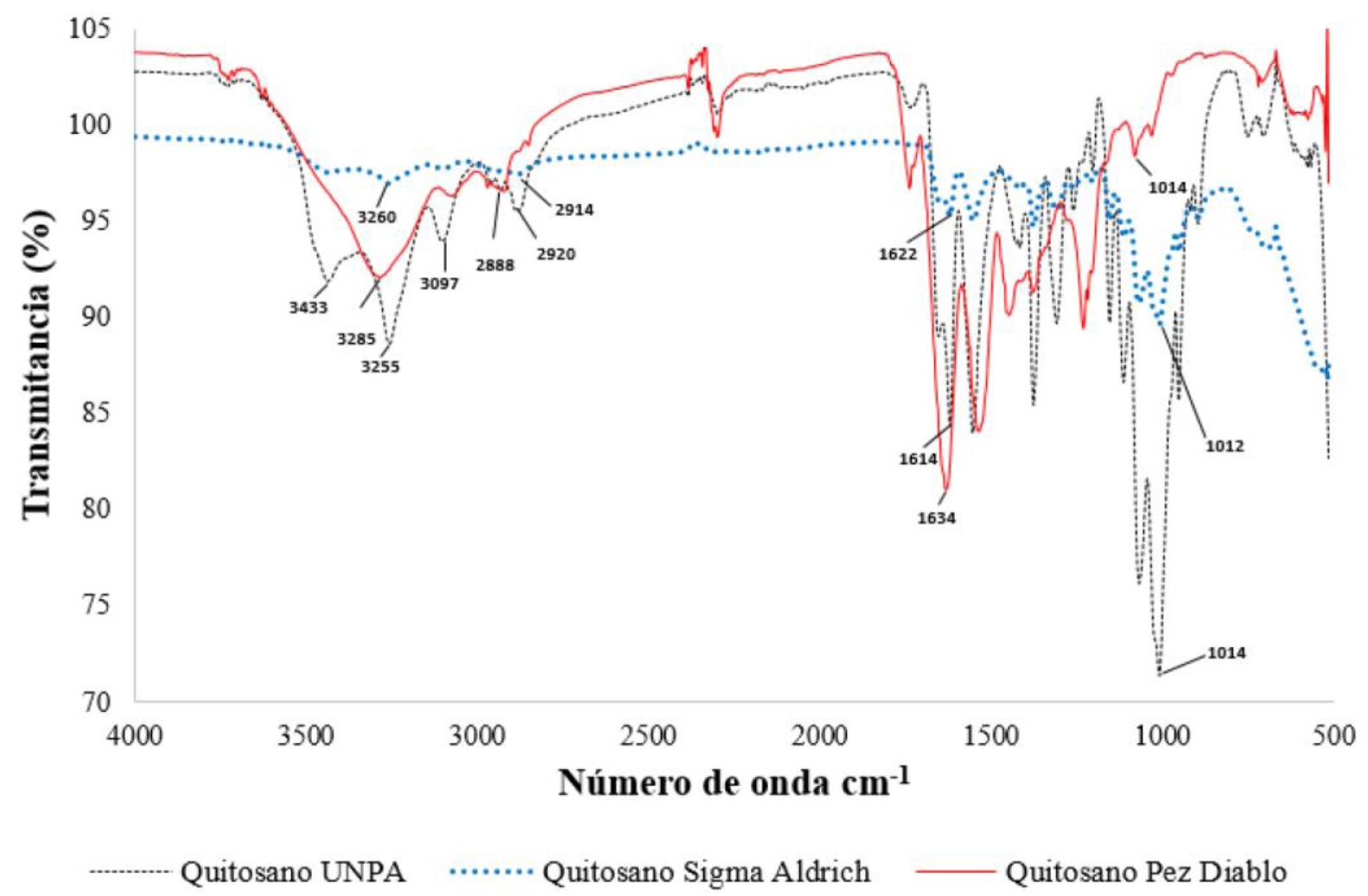
Figura 1 Espectros FTIR de quitosanos obtenidos por hidrólisis química, Quitosano UNPA ( ), Quitosano Sigma Aldrich (
), Quitosano Sigma Aldrich ( ), Quitosano pez diablo (
), Quitosano pez diablo ( ) a partir de exoesqueletos de camarón y placas dérmicas del pez diablo.
) a partir de exoesqueletos de camarón y placas dérmicas del pez diablo.
Por otro lado, estos mismos picos corresponden a un estiramiento N-H característico de una amina secundaria. En la región comprendida entre 3097 a 2914 cm-1 se aprecia dos bandas de absorción moderada correspondientes a las vibraciones de tensión (C-H) propias de grupos -CH. Así mismo, en los picos 1622 a 1634 cm-1 muestran bandas de absorción de intensidad moderada correspondiente al estiramiento del C=O propio de una amida primaria. Sin embargo, en la misma figura se muestra el espectro del quitosano comercial (Sigma-Aldrich México) espectro color rojo, donde se aprecian los grupos funcionales característicos del quitosano, se ven diferencias en los tres tratamientos combinados con respecto al estándar comercial. El peso molecular del quitosano obtenido del pez diablo (112.934 y 206.507 kDa) es considerablemente menor que el del quitosano comercial de camarón de bajo peso molecular (300 kDa). Esta diferencia influye en sus propiedades fisicoquímicas y aplicaciones potenciales. Un menor peso molecular generalmente mejora la solubilidad y facilita la manipulación en soluciones ácidas diluidas, como se observa con la alta solubilidad (93.22 y 93.545%). Además, puede incrementar la actividad biológica, incluyendo efectos antimicrobianos y antioxidantes, debido a la mayor facilidad de interacción con superficies celulares. Sin embargo, implica menor viscosidad y posiblemente menor resistencia mecánica en aplicaciones como recubrimientos o películas. Optimizar el proceso de extracción permitiría ajustar el peso molecular según las necesidades específicas.
Análisis termogravimétrico (TGA)
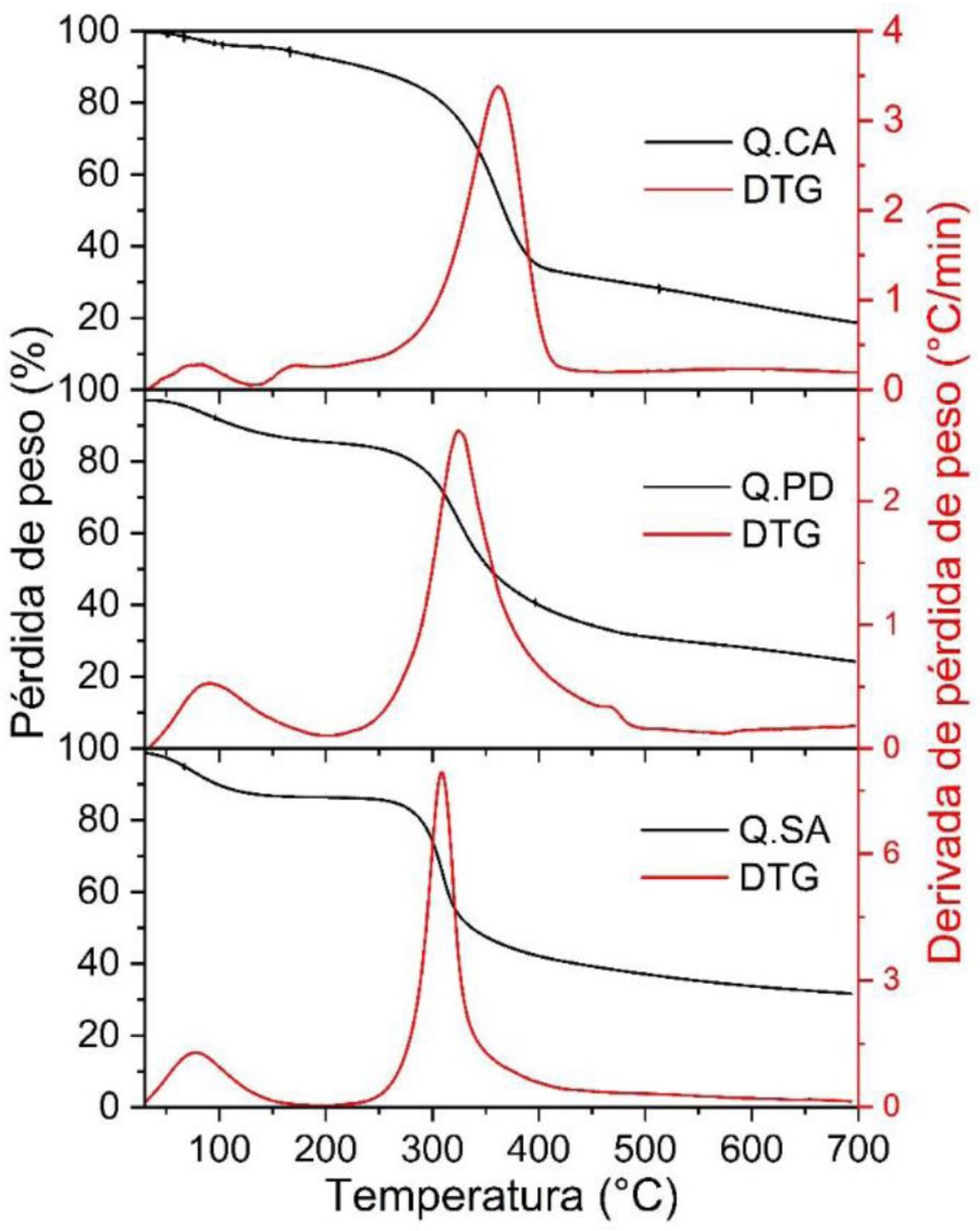
La Figura 2 muestra el análisis termogravimétrico (TGA) y térmico diferencial (DTG) del quitosano de camarón (Q.CA), pez diablo (Q.PD) y Sigma-Aldrich (Q.SA), revelando dos etapas de degradación térmica. La primera etapa, entre 50 y 100 °C, que corresponde a la eliminación de agua superficial con una pérdida de peso cercana al 10% en todas las muestras, característico de materiales higroscópicos como el quitosano. La segunda etapa, entre 220 y 410 °C, se atribuye a la degradación de las cadenas poliméricas mediante desacetilación y ruptura de enlaces glicosídicos, con una pérdida de peso aproximada del 60%. El quitosano de camarón mostró mayor estabilidad térmica, desplazando su segunda etapa de degradación a temperaturas más altas, lo que sugiere una mayor cristalinidad o grado de desacetilación. En contraste, el quitosano del pez diablo presentó una degradación a temperaturas más bajas, indicando menor estabilidad térmica posiblemente por impurezas o un menor grado de desacetilación. El quitosano Sigma-Aldrich mostró un perfil de degradación más definido, reflejando una estructura más homogénea y mayor pureza. El análisis DTG indicó picos más agudos en Q.SA en comparación con Q.CA y Q.PD, lo que reafirma su mayor pureza. Estos resultados destacan las diferencias estructurales y térmicas entre los quitosanos analizados.
Propiedades microestructurales
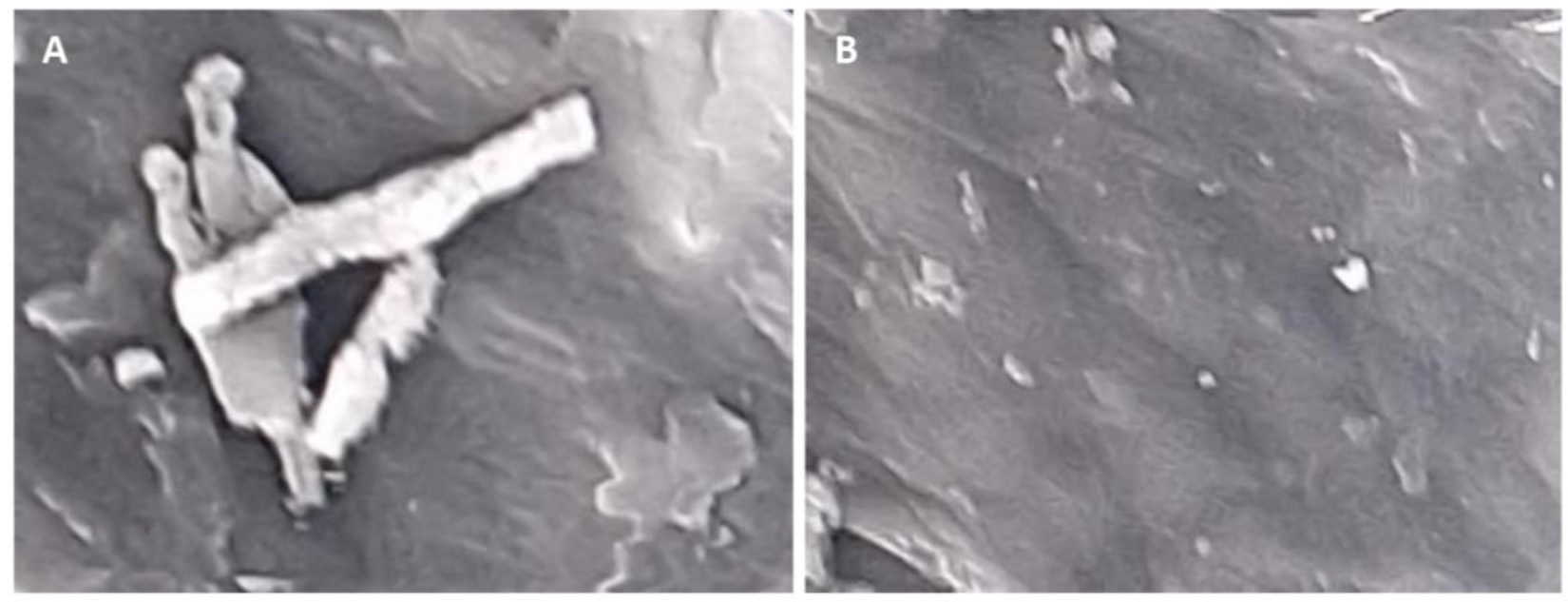
La Figura 3 muestra el análisis microestructural mediante microscopía electrónica de barrido del quitosano obtenido del pez diablo mostró una estructura fibrosa y bien definida en la superficie, con un aspecto laminar y la presencia de algunos espacios interlaminares visibles en la microfotografía. En contraste, la superficie del quitosano de referencia presentó una estructura laminar incompleta con espacios interlaminares, lo cual podría atribuirse a diferencias en el procesamiento y la fuente de extracción. En términos generales, los resultados revelaron un daño mínimo en la microestructura de ambos biopolímeros obtenidos. Considerando la morfología superficial de las quitinas y los quitosanos analizados, se observaron estructuras de microfibras con una conformación cristalina bien organizada, caracterizadas por un entramado de fibras antiparalelas, más notorias en los materiales obtenidos a partir del pez diablo. La conformación fibrilar de estos biopolímeros sugiere su potencial aplicación en la elaboración de textiles y películas biodegradables. Asimismo, los resultados obtenidos fueron consistentes con observaciones previas en quitinas y quitosanos extraídos de diversos insectos y crustáceos, donde se ha reportado una estructura fibrilar distintiva y bien conservada. En las muestras de quitosanos comerciales, en cambio, no se observaron microfibras tan definidas como en los biopolímeros obtenidos en esta investigación, lo que puede atribuirse a las diferencias en el origen y los métodos de procesamiento. Finalmente, se identificó que las propiedades morfológicas de las quitinas y quitosanos no solo dependen de la fuente de origen, sino también del método de secado utilizado. La preservación de la estructura fibrilar durante la desacetilación confirma la estabilidad de la morfología característica de estos materiales, incluso tras tratamientos químicos intensivos.
Discusión
Composición proximal de las fuentes quitinosas
La composición proximal de las fuentes quitinosas analizadas (Tabla 1) presentó valores por debajo de la media reportada por Kaya et al. (2016), Monter et al. (2016), Amador-Mendoza et al. (2022) y Martínez et al. (2022). Estas diferencias pueden deberse a factores como la variabilidad biológica entre especies, su estado fisiológico, la dieta recibida, la edad o etapa reproductiva, así como las condiciones ambientales en las que se desarrollaron. La proporción de proteínas, lípidos y minerales en los exoesqueletos es altamente dependiente de estos factores, lo que afecta directamente la eficiencia en la obtención de quitina y su posterior transformación en quitosano. Por otro lado, trabajos como los de Muslim et al. (2013), Borain y Graciano et al. (2016), García et al. (2016) y Jiménez et al. (2021) reportaron composiciones incluso más bajas, lo que evidencia la influencia del origen y tratamiento de la muestra. En nuestro estudio, los altos rendimientos (≥89 %) obtenidos en las etapas de despigmentación, desproteinización y desmineralización pueden atribuirse, en parte, al control del tamaño de partícula, un parámetro clave para optimizar el contacto entre reactivos y matriz biológica, tal como fue señalado por Colina et al. (2014).
Despigmentación y color del quitosano
La Tabla 2 presenta los resultados de despigmentación del quitosano extraído de exoesqueletos de camarón y placas dérmicas de pez diablo. Este efecto se debe al poder oxidante del hipoclorito de sodio, utilizado como agente decolorante. El quitosano más valorado comercialmente es el de color beige (producido por hongos), seguido del blanco a grisáceo, que proviene de calamar o camarón. Nuestros resultados mostraron que el quitosano derivado del pez diablo presenta una coloración blanco grisáceo (#EADEDF), correspondiente a un valor comercial intermedio, como lo establece Romero-Serrano y Pereira (2020). Sin embargo, una desventaja de esta metodología es el elevado consumo de agua, requiriendo entre 25 y 30 litros por cada 50 g de material procesado. Este aspecto debe considerarse al explorar alternativas de extracción más sustentables, como sugieren Khanafari et al. (2008) y Pacheco-Aguilar et al. (2009).
Caracterización por espectroscopía infrarroja (FTIR)
La Figura 1 muestra los espectros FTIR de las muestras de quitosano obtenidas por hidrólisis química a partir de tres fuentes: residuos de camarón procesados en la UNPA, quitosano comercial (Sigma-Aldrich) y exoesqueletos del pez diablo. En todos los casos, los espectros presentaron señales características del quitosano, lo que confirma la transformación exitosa de los residuos quitinosos en una materia prima funcional mediante procesos de desproteinización, desmineralización, despigmentación y desacetilación. Se observó una banda ancha entre 3 200-3 500 cm-1 atribuida a las vibraciones de estiramiento del grupo hidroxilo (-OH) y del grupo amino (-NH2), típicas de la estructura del quitosano. Las señales en la región de 2 870-2 920 cm-1 corresponden a los estiramientos C-H del esqueleto glucosídico. La banda en 1 655 cm-1 se asocia al estiramiento del grupo carbonilo (C=O) de la N-acetilglucosamina, indicando la fracción acetilada presente, mientras que la banda en 1 595 cm-1 corresponde al grupo amino libre (-NH2), evidenciando un grado de desacetilación significativo. Las bandas entre 1 020-1 080 cm-1, relacionadas con los enlaces C-O-C del esqueleto polisacárido, confirman la presencia de una red estructural típica del quitosano. La comparación entre los espectros permitió identificar variaciones sutiles en intensidad y posición de bandas, posiblemente debidas a diferencias en pureza, cristalinidad o fuente biológica. En particular, el quitosano derivado del pez diablo presentó un perfil espectral comparable al comercial, lo que valida su potencial como fuente alternativa. Los tratamientos aplicados fueron adecuados para obtener quitosano funcional, promoviendo así la valorización de residuos biológicos no convencionales en aplicaciones biotecnológicas y agroindustriales
Peso molecular del quitosano
El peso molecular del quitosano extraído en este estudio fue superior al reportado por García et al. (2016), quienes obtuvieron valores entre 5.2 y 6.8 kDa a partir de escamas de tilapia roja y negra (Oreochromis sp.). No obstante, los valores aquí obtenidos siguen siendo considerablemente menores que el de la quitina comercial sin desacetilar, cuyo peso molecular ronda los 300 kDa. Esta diferencia sugiere que el proceso de desacetilación e hidrólisis química aplicado no solo logró convertir la quitina en quitosano, sino que también fragmentó las cadenas poliméricas hasta alcanzar un peso molecular medio. Este rango intermedio de peso molecular es relevante, ya que influye directamente en propiedades clave del quitosano, como su solubilidad, viscosidad, actividad antimicrobiana y capacidad para formar películas. Quitosanos de bajo a medio peso molecular tienden a ser más solubles en medios ácidos, lo que los hace útiles para aplicaciones biomédicas, agrícolas y alimentarias, especialmente en formulaciones donde se requiere una rápida biodisponibilidad o interacción con superficies biológicas. Así, el quitosano obtenido a partir del pez diablo y otros residuos utilizados en este estudio no solo representa una alternativa sostenible, sino también versátil desde el punto de vista funcional, ampliando su potencial en diversas industrias.
Análisis térmico (TGA y DTG)
El análisis termo-gravimétrico (TGA) y su derivado (DTG) revelaron diferencias notables en la estabilidad térmica entre el quitosano comercial y el extraído del pez diablo. El quitosano derivado de esta especie tuvo una temperatura de degradación mayor (324 °C), evidenciando mayor estabilidad térmica. Esta característica puede relacionarse con una estructura molecular más ordenada y mayor grado de cristalinidad. Una estructura más organizada implica cadenas poliméricas más densamente empaquetadas, que requieren mayor energía para romper los enlaces intermoleculares durante el proceso de degradación térmica. En contraste, el quitosano comercial mostró una temperatura de degradación inferior (308 °C), posiblemente como resultado de un menor grado de desacetilación o una baja masa molar, factores que afectan negativamente la organización estructural del biopolímero. Estudios previos como los de Rodríguez et al. (2010) y Barbosa et al. (2019) han demostrado que estos parámetros tienen un impacto directo en la estabilidad térmica y en la calidad general del quitosano. Estos hallazgos sugieren que el quitosano extraído del pez diablo no solo es viable desde un punto de vista técnico, sino que incluso podría ofrecer propiedades superiores. Su aprovechamiento representa una alternativa sustentable para el manejo de esta especie invasora, además de su integración en aplicaciones industriales donde se requiere estabilidad térmica, como en envases activos o sistemas de liberación controlada.
Microestructura del quitosano
El análisis microestructural reveló una organización altamente ordenada, con la presencia de microfibras dispuestas en una conformación α-cristalina. Esta configuración estructural se caracteriza por fibras antiparalelas entrelazadas, lo que refleja un grado de organización molecular elevado. Esta disposición específica ha sido asociada con propiedades mecánicas superiores y una mayor capacidad para formar películas delgadas, como lo mencionan Kaya et al. (2016). La presencia de estas fibras sugiere que el quitosano de pez diablo posee un potencial significativo para su utilización en productos de valor agregado, como materiales biodegradables, empaques comestibles, textiles con funcionalidad específica y membranas de liberación controlada. A diferencia de estructuras amorfas o desordenadas, esta disposición mejora la resistencia mecánica y la barrera a gases y humedad, características esenciales en aplicaciones industriales. Además, este tipo de estructura podría facilitar la funcionalización química del quitosano, permitiendo la incorporación de compuestos bioactivos o propiedades antimicrobianas. En comparación, el quitosano comercial suele presentar una microestructura menos definida, lo cual podría limitar su desempeño en ciertas aplicaciones. En consecuencia, el aprovechamiento del quitosano proveniente del pez diablo no solo contribuye a la valorización de una especie problemática, sino que también abre oportunidades para su incorporación en cadenas productivas sostenibles y de alta tecnología, particularmente en bioplásticos y biomateriales.
Conclusiones
Se obtuvo quitosano a partir de las placas dérmicas del pez diablo por método químico (Hidrólisis alcalina-ácida), obteniéndose un rendimiento del 25%. La caracterización del quitosano obtenido a partir de esta nueva fuente evidenció una conformación estructural y molecular similar al quitosano comercial. Los resultados obtenidos sugieren que esta especie invasora dulceacuícola puede considerarse como una fuente importante para la preparación de quitosano y utilizarse para diversas aplicaciones de la región.











 nueva página del texto (beta)
nueva página del texto (beta)