Introducción
La especie Suaeda edulis Flores Olv. & Noguez, es una halófita conocida en México como “romerito”, no es una especie que se cultive en áreas muy extensas, pues su cultivo se limita a la región del Centro de México (San Andrés Mixquic, Ciudad de México; Texcoco, San Pedro Tláhuac, San Gregorio Atlapulco y Santiago Tulyehualco, Estado de México) siguiendo las tradiciones culturales de los antepasados de los pueblos (Noguez-Hernández et al. 2013). Los autores citados anteriormente, señalan que, la especie no está totalmente domesticada, las semillas se obtienen de las áreas de cultivos o donde crece de manera natural, en suelos inundados, con niveles altos de salinidad, suelos húmedos en pastizales halófilos como Distichlis spicata a intervalo altitudinal de 1,347 a 2,351 m. Los mismos autores afirman que la especie se distribuye en lagos salinos de Guanajuato, Jalisco, Michoacán, Estado de México, Ciudad de México, Tlaxcala y Puebla, desarrollando una variabilidad fenotípica alta como respuesta a tales condiciones (Negrão et al. 2017). La especie es tolerante a niveles altos de salinidad por lo que es un modelo potencial para su uso en sistemas hidropónicos utilizando agua con exceso de sales que no es posible usar en especies glicófitas tradicionales (Costa-Becheleni et al. 2021).
El problema de la degradación de las tierras de cultivo por el uso inadecuado de técnicas de cultivo y métodos de riego que utilizan agua con exceso de sales ha estimulado el interés en el uso de especies halófitas para su cultivo. Se ha demostrado que, las halófitas ayudan a la rehabilitación de suelos y aprovechamiento de aguas residuales procedentes de la acuicultura (Buhmann et al. 2015, Lutts y Lefevre 2015).
El uso eficiente del agua es una necesidad impetuosa para enfrentar la situación mundial de carencia y calidad de este recurso. En ese sentido, Kumari et al. (2015) afirma que, las halófitas son especies alternativas para cultivarse porque son eficientes en el uso del agua en comparación con las especies glicófitas. Por otro lado, se han utilizado métodos novedosos de cultivo de especies a través de técnicas como la acuaponía y la hidroponía (El-Kazzaz y El-Kazzaz 2017) lo cual ha generado problemas por las características del agua residual que en ellas se produce. Estas aguas, pueden contener niveles altos de elementos que, de ser vertidos al suelo o a las cuencas, provocan contaminación o degradación (Yep y Zheng 2019). Las propiedades de esas aguas pueden ser propicias para el cultivo en ciclos cerrados o abiertos de hidroponía con especies halófitas (Doncato y Costa 2021) como la Suaeda que minimizan el posible impacto negativo. Por lo anterior, el objetivo de este estudio fue evaluar las características morfométricas, fisiológicas, bioquímicas y acumulación de minerales de ecotipos de S. edulis Flores Olv. & Noguez sometidos a estrés con mezclas de agua de mar diluida con agua residual del cultivo de tilapia (Oreochromis niloticus).
Materiales y métodos
Área de estudio
El experimento se realizó en el Centro de Investigaciones Biológicas del Noroeste, S.C. (CIBNOR), ubicado en la ciudad de La Paz, Baja California Sur, México, localizado en los 24° 08 10.8 LN y los 110° 25 40.1 LO, a una altitud de 7 msnm, en una casa tipo invernadero, la cual es una estructura construida con tubos de acero galvanizado, cubierta con malla de 1610 PME CR. La temperatura promedio dentro de la casa sombra durante el periodo de estudio fue de 21.63 ± 5.27 °C, con 67.55 ± 16.80% de humedad relativa. La precipitación total registrada fue de 20.05 mm, con una máxima de 5.59 mm. Los datos de las variables climatológicas que se registraron durante el estudio se obtuvieron de una estación climatológica portátil Vantage Pro2® (Davis Instruments, Hayward, CA, USA) colocada al interior de la estructura tipo invernadero.
Material genético
Las semillas de S. edulis Flores Olv. & Noguez utilizadas, se colectaron en tres sitios, Colegio de Posgraduados, Montecillo, Texcoco, Estado de México identificado como ecotipo E1, Cráter La Alberca, Valle de Santiago, Guanajuato identificado como ecotipo E2 y Lago Cuitzeo, Cuitzeo del Porvenir, Michoacán identificado como ecotipo E3 (Tabla 1).
Tabla 1 Localización geográfica, pH y conductividad eléctrica del suelo de los sitios de colecta de ecotipos de Suaeda edulis Flores Olv. & Noguez en la región central de México.
| Ecotipos | Sitios de colecta | Localización geográfica | pH | CE (dS m-1) |
|---|---|---|---|---|
| E1 | Colegio de Postgraduados, Montecillo, Texcoco, Estado de México | 19° 2757.8 LN, 098° 5504.3 LO | 11.04 | 27.00 |
| E2 | Cráter La Alberca, Valle de Santiago, Guanajuato | 19° 1514.8 LN, 099° 0022.5 LO | 9.79 | 27.80 |
| E3 | Lago Cuitzeo, Cuitzeo del Porvenir, Michoacán | 19° 5757.3 LN, 101° 0910.8 LO | 9.83 | 0.03 |
CE = conductividad eléctrica.
Siembra
El proceso de siembra inició al colocar 500 semillas de cada ecotipo en charolas de poliestireno de 200 cavidades con un volumen de 10.87 cm3 y profundidad de 4.3 cm por cada cavidad mismas que contienen orificios inferiores para el drenaje del exceso de agua. El sustrato utilizado para la germinación fue una mezcla de 50:50 de turba (Sphagnum canadiense peat moss, 65-75% vol-1, premier Horticulture Ltd., Quebec, Canadá) y lombricomposta, manteniendo la humedad del sustrato al regarlo cada dos días.
Trasplante
El trasplante se realizó a los 20 días posteriores a la emergencia de las plántulas, cuando éstas alcanzaron una altura promedio de 8 cm. Las plántulas se colocaron en canastillas para hidroponía del número 5 con un volumen de 71.66 cm3 y una altura de 5 cm, utilizando como soporte piezas de esponja (espuma de poliuretano), colocando una plántula por canastilla.
Diseño experimental
El experimento se estableció en un diseño completamente al azar con arreglo factorial. El primer factor consistió en tres ecotipos de S. edulis colectados en tres diferentes regiones del Centro de México (Tabla 1), los cuales se sometieron a un segundo factor que consistió en preparar cuatro conductividades eléctricas (2.5, 10.0, 15.0, 30.0 dS m-1) utilizando agua de mar diluida con agua residual procedente del cultivo de tilapia. El total de tratamientos fue de 12 con tres repeticiones por tratamiento y 24 plantas por cada repetición.
Sistema hidropónico
El sistema hidropónico utilizado fue del tipo raíz flotante, compuesto por 12 tinas rectangulares de fibra de vidrio de 2.50 × 1.25 m de largo y ancho, respectivamente. En las tinas se vertieron 500 L de una mezcla de agua de mar con agua residual de cultivo de tilapia (Oreochromis niloticus), con los volúmenes y porcentajes que se muestran en la tabla 2. Para el caso de la conductividad eléctrica de 2.5 dS m-1, a los 470 L de agua residual de tilapia con 3.3 dS m-1 de conductividad eléctrica, se adicionaron 30 L de agua procedente de la planta desaladora del campo experimental del CIBNOR para obtener 2.5 dS m-1. El sistema de hidroponia posee un tanque por cada tina donde se almacena el agua que se mantiene circulando por medio de bombas sumergibles (Evans® 18 W, modelo Aqua18W, Monterrey, N.L., México) colocadas en cada tanque, las cuales tienen a la salida del agua, un tubo que provoca el efecto Venturi que proporciona el oxígeno constantemente al agua de todo el sistema. Las canastillas con las plántulas se colocaron en una cama flotante consistente en placa de poliestireno de 2 pulgadas de espesor (Foamular®, modelo CAN24P3/0E, Owens Corning, USA) con 72 cavidades cada una.
Tabla 2 Volumen y porcentaje de agua de mar y agua residual de tilapia para obtener los valores de conductividad eléctrica.
| Conductividad eléctrica (dS m-1) | Volumen agua de mar (L) | Porcentaje | Volumen agua residual (L) | Porcentaje | Volumen total (L) |
|---|---|---|---|---|---|
| 10 | 70 | 14 | 430 | 86 | 500 |
| 20 | 165 | 33 | 335 | 67 | 500 |
| 30 | 285 | 57 | 215 | 43 | 500 |
Características del agua de mar
El agua de mar utilizada presentó las características siguientes, pH de 8.58 ± 0.01, conductividad eléctrica de 55.71 ± 0.14 dS m-1, sólidos disueltos totales (ppm) 27.30 ± 0.07, salinidad (PSU -practical salinity units-) de 36.87 ± 0.11, sodio (ppm) 14 000 ± 346.41, potasio (ppm) 316.67 ± 30.55, calcio (ppm) 453.33 ± 20.82, nitratos (ppm) 470 ± 40. El agua de mar proviene de la toma de agua del CIBNOR que se utiliza como fuente que proporciona el agua a las áreas donde se realizan experimentos con especies marinas. El agua de cultivo de tilapia presentó las características siguientes, pH de 3.45, conductividad eléctrica de 3.3 dS m-1, 90.5 ppm de Na, 36.2 ppm de K, 182.7 ppm de Ca, 78.4 ppm de Mg, 0.3 ppm de Mn y 0.04 ppm de Fe.
Variables morfométricas
Las variables morfométricas evaluadas fueron, peso fresco y seco de tallos, hojas y raíces (g), longitud de tallos y de raíces (cm) y área foliar (cm2), mismas que se midieron al final del experimento, que se realizó a los 60 días después del transplante, seleccionando para ello, tres plantas por cada tratamiento y repetición. El peso fresco y seco se midió con una balanza analítica (Mettler Toledo®, modelo AG204, Mettler-Toledo GmbH, Suiza). El peso seco se obtuvo al colocar por separado los tejidos (hojas, tallos y raíces) en bolsas de papel que se colocaron en una estufa de secado (Terlab TE-H80dm, Terlab®, S.A. de C.V., El Arenal, Jalisco. México) a una temperatura de 70 °C hasta peso constante lo cual ocurrió a las 72 h. Las longitudes de tallo y raíces se determinaron con una regla metálica graduada en milímetros y centímetros. El área foliar se determinó con un equipo integrador de área foliar (Li-Cor® Bioscience, modelo LI-3000A, serie PAM 1701, Lincoln, NE, USA).
Variables fisiológicas
Las variables fisiológicas evaluadas fueron el contenido de clorofila a, b y total por los métodos directo e indirecto (valores de SPAD-502) y el potencial hídrico. El contenido de clorofila por el método directo se determinó al extraer la clorofila en muestras de 0.5 g de hojas sanas, las cuales se colocaron en tubos de ensayo con una solución de acetona al 80% y se mantuvieron en oscuridad por 72 h. Las lecturas se realizaron en un espectrofotómetro UV (Hach® DR-3900, Hach Chemical Company, USA). La concentración de clorofila se calculó con las ecuaciones propuestas por Strain y Svec (1966). La clorofila por el método indirecto no destructivo (valores de SPAD) se determinó con un medidor portátil (SPAD-502 Plus, Minolta®, Japón), el cual estima el contenido relativo de clorofila midiendo la absorbancia de la hoja en dos regiones de longitud de onda, la azul (400-500 nm) y la roja (600-700 nm). El SPAD utiliza las dos absorbancias y calcula un valor numérico llamado valor de SPAD que es proporcional al contenido de clorofila en la hoja. En cada hoja se realizaron tres lecturas y se obtuvo un valor promedio. El potencial hídrico se evaluó al final del experimento, al mediodía solar que, en La Paz, Baja California Sur se alcanza aproximadamente a las 12:00 h. Para medirlo, se utilizó un psicrómetro para muestras de suelo y plantas, hojas, tejidos, granos, semillas (WP4-T®, Decagon Devices Pullman WA, USA). De cada unidad experimental se seleccionaron tres plantas al azar y una hoja sana y completa de cada planta. Cada hoja se colocó en una cubeta cubierta de papel parafilm y se trasladó al laboratorio en bolsa de plástico. De cada hoja se cortó un disco de 1 cm × 1 cm, se colocó en la cubeta del equipo y se introdujo a la cámara sellada del equipo para realizar la lectura. Las mediciones se realizaron en condiciones de laboratorio en las que la temperatura se fijó en 25 °C. Los discos de las hojas se colocaron en la cámara del equipo en la misma posición con la cara abaxial. Las lecturas se registran aproximadamente a los 40 segundos después de colocar la muestra.
Análisis proximal
Las variables de la composición bioquímica de los tejidos (hojas+tallos) evaluadas fueron el contenido de proteína, extracto etéreo y fibra cruda. Para realizar estos análisis, las muestras de plantas se secaron en horno (HTP-80, Lumistell®, Biotécnica de Bajío S.A. de C.V., Celaya, Guanajuato, México) a 70 °C hasta peso constante. El contenido de proteína se determinó en un destilador (Foss Kjeltec 230®, Foss®, Dinamarca) durante 4 min y en digestor (Foss Kjeltec 2040®, Foss®, Dinamarca) durante 25 min, por el método microkjeldahl. La fibra cruda se cuantificó por hidrólisis sucesiva en una multi-unidad de extracción (Fiber Tec M6 Tecator®, Foss®, Dinamarca). El extracto etéreo se determinó mediante el Método Soxtec-Avanti, Tecator (Foss®, Dinamarca).
Composición mineral
Para el análisis de minerales, las muestras secas se molieron finamente utilizando un molino (Braun® tipo 4-041 Modelo KSM-2, Braun®, Alemania). Los minerales se determinaron en parte aérea (tallos+hojas) y en raíces y fueron los siguientes, Ca, Fe, K, Mg, Mn y Na (en g kg-1). La cuantificación fue mediante una digestión ácida previa y midiendo su concentración en un espectrofotómetro de absorción atómica (Shimadzu® AA-660, Shimadzu Corporation, Japón).
Análisis estadístico
Las bases de datos se elaboraron en Excel y los análisis estadísticos se realizaron con Statistica v. 13.5 (TIBCO® 2018). Los análisis de varianza se realizaron considerando el diseño experimental establecido, así como comparaciones múltiples de medias utilizando el método de Tukey HSD (p ≤ 0.05).
Resultados
Variables morfométricas
Los análisis de varianza mostraron que, la mayoría de las variables morfométricas presentaron diferencias significativas en la interacción de los factores, ecotipos × conductividad eléctrica, excepto las variables peso fresco y seco de hojas, área foliar y longitud de masa radicular (Tabla 3). La longitud de tallo, el peso fresco y seco de tallo mostraron valores mayores en las plantas del ecotipo E2 con 10 dS m-1. El ecotipo E3 con 30 dS m-1 mostró la longitud de tallo menor, mientras que, el ecotipo E1 en 2.5 dS m-1 mostró los valores inferiores de peso fresco y seco de tallo, peso fresco y seco de hojas. Si bien el peso fresco y seco de hojas no mostraron diferencias significativas, el ecotipo E3 en 20 dS m-1 mostró mayor peso fresco de hoja y el mayor peso seco de hoja lo presentaron las plantas del ecotipo E2 en 20 dS m-1. Los ecotipos E3 en 20 dS m-1 y E1 en 30 dS m-1 presentaron mayor y menor área foliar, respectivamente. Las plantas del ecotipo E3 en 20 dS m-1 mostraron los valores superiores de longitud de raíces y peso fresco de raíces; lo contrario lo presentó el ecotipo E1 en 30 dS m-1. Las plantas del ecotipo E3 en 2.5 dS m-1 presentaron los valores superiores de longitud de masa radicular; lo contrario lo mostró el ecotipo E1 en 30 dS m-1. Las plantas del ecotipo E2 mostraron mayor peso fresco de raíces, mientras que, el ecotipo E1 en 30 dS m-1, mostró los valores menores. Las variables morfométricas mostraron un desarrollo siguiendo una respuesta tipo polinomio, observándose que, en las concentraciones de 2.5 y en 30 dS m-1 de conductividad eléctrica, los valores de la mayoría de las variables disminuyeron y, en valores intermedios de conductividad eléctrica, las variables presentaron valores superiores (Figura 1). La Figura 1 muestra que, el peso fresco y seco de tallo, incrementaron conforme aumentó la conductividad eléctrica; sin embargo, en conductividades eléctricas a partir de 20 dS m-1, el peso fresco y seco de tallo disminuyeron. Esta respuesta la presentaron la mayoría de las variables morfométricas. Al incrementar los niveles de conductividad eléctrica, las variables morfométricas presentaron valores superiores en 10 y 20 dS m-1. El ecotipo E1 cuya semilla se colectó en el Colegio de Postgraduados, Montecillo, Texcoco, Estado de México, mostró los valores inferiores en la mayoría de las variables morfométricas, mientras que, el ecotipo E2 cuya semilla se colectó en el Cráter La Alberca, Valle de Santiago, Guanajuato, que es el sitio de mayor conductividad eléctrica en el suelo, presentó valores superiores en cinco variables morfométricas, al igual que el ecotipo E3, cuyo sitio de colecta de semilla corresponde al Lago Cuitzeo, Cuitzeo del Porvenir, Michoacán, con la conductividad eléctrica menor del suelo en dicho sitio de colecta. El ecotipo E3 también presentó valores superiores en cinco variables, solo que éste último, se caracterizó por exhibir valores superiores en longitud de raíces y longitud de masa radicular (Tabla 3).
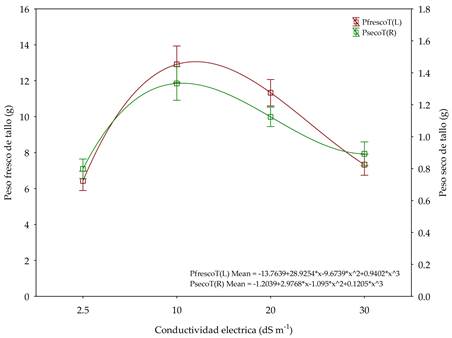
Figura 1 Respuesta óptima tipo cuadrática/cúbica de dos variables morfométricas de plantas de tres ecotipos de S. edulis sometidos a estrés con mezclas de agua de mar (2.5, 10, 20 y 30 dSm-1) y agua de tilapia.
Tabla 3 Valores promedio de variables morfométricas de tres ecotipos de S. edulis sometidos a estrés con mezclas de agua de mar (2.5, 10, 20 y 30 dSm-1) y agua de tilapia.
| Ecotipos | CE | LT | PFT | PST | PFH | PSH |
|---|---|---|---|---|---|---|
| E1 | 2.5 | 21.71 ± 1.73bc* | 2.46 ± 0.38f | 0.40 ± 0.06c | 4.42 ± 0.74a | 0.61 ± 0.08a |
| E1 | 10 | 29.85 ± 1.04abc | 5.78 ± 1.36cdef | 0.90 ± 0.19bc | 12.95 ± 2.34a | 1.44 ± 0.23a |
| E1 | 20 | 24.84 ± 1.42bcd | 4.42 ± 0.41def | 0.62 ± 0.06bc | 7.42 ± 0.51a | 0.86 ± 0.06a |
| E1 | 30 | 21.65 ± 1.30bc | 2.99 ± 0.58ef | 0.44 ± 0.08bc | 5.16 ± 1.07a | 0.65 ± 0.13a |
| E2 | 2.5 | 26.56 ± 1.63bcd | 5.76 ± 0.92cdef | 0.70 ± 0.10bc | 16.94 ± 1.21a | 1.43 ± 0.13a |
| E2 | 10 | 37.58 ± 2.09a | 20.66 ± 3.80a | 2.15 ± 0.42a | 31.93 ± 4.71a | 2.38 ± 0.46a |
| E2 | 20 | 30.86 ± 1.79ab | 13.41 ± 2.11abc | 1.41 ± 0.22ab | 40.83 ± 6.12a | 2.86 ± 0.44a |
| E2 | 30 | 27.63 ± 1.80bc | 11.13 ± 2.20bcd | 1.44 ± 0.31ab | 32.33 ± 3.82a | 2.75 ± 0.36a |
| E3 | 2.5 | 28.88 ± 2.09abc | 11.05 ± 1.81bcdef | 1.28 ± 0.24abc | 25.69 ± 3.43a | 2.14 ± 0.31a |
| E3 | 10 | 25.73 ± 2.83bcd | 12.28 ± 1.97abcd | 0.94 ± 0.19bc | 37.16 ± 4.73a | 2.34 ± 0.42a |
| E3 | 20 | 29.20 ± 1.60abc | 16.15 ± 1.59ab | 1.32 ± 0.14abc | 41.25 ± 3.52a | 2.43 ± 0.17a |
| E3 | 30 | 17.88 ± 1.71c | 7.85 ± 1.43bcdef | 0.78 ± 0.12bc | 30.08 ± 4.53a | 2.25 ± 0.30a |
| AF | LR | LMR | PFR | PSR | ||
| E1 | 2.5 | 42.52 ± 6.62a | 13.12 ± 1.98c | 7.82 ± 1.15a | 0.64 ± 0.15fg | 0.11 ± 0.04bc |
| E1 | 10 | 94.14 ± 19.58a | 17.30 ± 2.19c | 9.17 ± 1.34a | 1.23 ± 0.39defg | 0.26 ± 0.08abcd |
| E1 | 20 | 60.08 ± 4.77a | 14.47 ± 2.66c | 5.27 ± 0.54a | 0.70 ± 0.10efg | 0.12 ± 0.02cd |
| E1 | 30 | 41.65 ± 9.78a | 12.23 ± 1.08c | 4.72 ± 0.36a | 0.50 ± 0.08g | 0.08 ± 0.02c |
| E2 | 2.5 | 152.27 ± 11.04a | 30.87 ± 3.35bc | 22.67 ± 2.24a | 1.36 ± 0.10cdef | 0.18 ± 0.03bcd |
| E2 | 10 | 286.20 ± 45.72a | 43.67 ± 5.25b | 27.70 ± 4.38a | 3.11 ± 0.37bcd | 0.37 ± 0.05abc |
| E2 | 20 | 329.93 ± 49.08a | 38.33 ± 5.26b | 23.43 ± 3.72a | 4.43 ± 0.51ab | 0.50 ± 0.06a |
| E2 | 30 | 259.00 ± 34.25a | 15.92 ± 1.80c | 12.53 ± 1.46a | 2.84 ± 0.52bcde | 0.40 ± 0.08ab |
| E3 | 2.5 | 238.45 ± 34.40a | 45.95 ± 5.22ab | 31.85 ± 4.03a | 2.77 ± 0.47bcdef | 0.42 ± 0.06ab |
| E3 | 10 | 301.46 ± 39.23a | 41.92 ± 2.50b | 28.33 ± 2.64a | 3.50 ± 0.48abc | 0.42 ± 0.08ab |
| E3 | 20 | 349.49 ± 33.23a | 63.40 ± 6.17a | 31.13 ± 3.59a | 5.53 ± 0.98a | 0.26 ± 0.06abcd |
| E3 | 30 | 236.18 ± 38.33a | 37.28 ± 4.82b | 17.17 ± 2.60a | 2.90 ± 0.42bcd | 0.35 ± 0.05abc |
CE = Conductividad eléctrica (dS m-1); LT = Longitud de tallo (cm); PFT = Peso fresco de tallo (g); PST = Peso seco de tallo (g); PFH = Peso fresco de hoja (g); PSH = Peso seco de hoja (g); AF = Área foliar (cm2); LR = Longitud de raíces (cm); LMR = Longitud de masa radicular (cm); PFR = Peso fresco de raíces (g); PSR = Peso seco de raíces (g). *Valores promedio con misma literal en columna, no difieren estadísticamente (Tukey HSD p ≤ 0.05). Los valores representan el promedio ± el error estándar (n = 3).
Variables fisiológicas
El análisis de varianza mostró que, el potencial hídrico y el contenido relativo de clorofila (valores SPAD), presentaron diferencias significativas en la interacción de los factores ecotipos × conductividad eléctrica. El contenido de clorofila no mostró diferencias significativas (Tabla 4). En los tres ecotipos, el potencial hídrico fue menos negativo en 2.5 dS m-1 y los valores fueron más negativos conforme la conductividad eléctrica se incrementó en el medio de cultivo. Las plantas del ecotipo E3 en 2.5 dS m-1 mostraron el potencial hídrico menos negativo, mientras que las plantas del ecotipo E1 en 30 dS m-1 mostraron lo contrario.
Tabla 4 Valores promedio de variables fisiológicas de tres ecotipos de S. edulis sometidos a estrés con mezclas de agua de mar (2.5, 10, 20 y 30 dSm-1) y agua de tilapia.
| Ecotipos | CE | Clorofila a (μg cm-2) | Clorofila b (μg cm-2) | Clorofila total (μg cm-2) | Potencial hídrico (-MPa) | Valores SPAD |
|---|---|---|---|---|---|---|
| E1 | 2.5 | 30.12 ± 11.97a* | 25.62 ± 10.63a | 55.74 ± 22.53a | -3.46 ± 0.31bcd | 11.36 ± 2.31c |
| E1 | 10 | 25.82 ± 10.85a | 19.77 ± 9.96a | 45.60 ± 20.76a | -4.11 ± 0.27de | 20.73 ± 4.20abc |
| E1 | 20 | 27.37 ± 3.69a | 22.49 ± 5.55a | 49.86 ± 9.21a | -4.84 ± 0.42de | 17.68 ± 1.31abc |
| E1 | 30 | 28.12 ± 9.57a | 23.79 ± 9.95a | 51.92 ± 19.49a | -5.78 ± 0.54e | 15.30 ± 3.23bc |
| E2 | 2.5 | 17.19 ± 1.27a | 11.41 ± 1.34a | 28.60 ± 2.05a | -2.12 ± 0.54ab | 30.36 ± 1.21a |
| E2 | 10 | 19.31 ± 2.22a | 12.22 ± 0.93a | 31.53 ± 1.64a | -2.97 ± 0.27abc | 27.33 ± 3.55ab |
| E2 | 20 | 21.69 ± 4.03a | 13.49 ± 2.67a | 35.18 ± 6.37a | -5.33 ± 0.28e | 18.53 ± 3.75abc |
| E2 | 30 | 19.14 ± 1.56a | 16.43 ± 2.13a | 35.58 ± 3.02a | -5.32 ± 0.35e | 15.80 ± 1.79bc |
| E3 | 2.5 | 20.71 ± 4.45a | 14.74 ± 2.85a | 35.46 ± 7.09a | -1.49 ± 0.06a | 19.23 ± 2.75abc |
| E3 | 10 | 21.60 ± 3.74a | 11.60 ± 2.45a | 33.20 ± 4.19a | -2.37 ± 0.10abc | 20.56 ± 3.25abc |
| E3 | 20 | 32.84 ± 10.40a | 25.47 ± 8.76a | 58.31 ± 18.97a | -4.74 ± 0.30de | 18.26 ± 1.33abc |
| E3 | 30 | 28.83 ± 7.20a | 19.81 ± 5.16a | 48.65 ± 12.07a | -5.02 ± 0.17de | 14.26 ± 0.82bc |
CE= Conductividad eléctrica (dS m-1); *Valores promedio con misma literal en columna, no difieren estadísticamente (Tukey HSD p ≤ 0.05). Los valores representan el promedio ± el error estándar (n = 3).
El contenido relativo de clorofila (valores SPAD) fue mayor en las plantas del ecotipo E2 en 2.5 dS m-1, mientras que, los valores inferiores de SPAD los presentaron las plantas del ecotipo E1 en 2.5 dS m-1. Si bien el contenido de clorofila no mostró diferencias significativas en la interacción, el contenido mayor de clorofila a, b y total lo presentaron las plantas del ecotipo E3 en 20 dS m-1 y E1 en 2.5 dS m-1, mostrando lo contrario, las plantas del ecotipo E2 en 2.5 dS m-1. En el ecotipo E2 se observó que el contenido de clorofila total aumentó a medida que la conductividad eléctrica incrementó.
Análisis proximal
El análisis de varianza mostró que, el contenido de proteínas, extracto etéreo y fibra cruda, mostraron diferencias significativas en la interacción de los factores ecotipos × conductividad eléctrica. Las plantas del ecotipo E3 en 2.5 dS m-1 mostraron el mayor contenido de proteínas mientras que, el ecotipo E2 en 30 dS m-1 mostró lo contrario. El contenido de extracto etéreo fue mayor en las plantas del ecotipo E1 en 10 dS m-1, lo contrario lo mostró el ecotipo E3 en 30 dS m-1. Las plantas del ecotipo E1 en 10 dS m-1 mostraron el contenido mayor de fibra cruda, mostrando lo contrario el ecotipo E3 en 30 dS m-1 (Tabla 5).
Tabla 5 Valores promedio de la composición bioquímica (análisis proximal) de tres ecotipos de S. edulis sometidos a estrés con mezclas de agua de mar (2.5, 10, 20 y 30 dSm-1) y agua de tilapia.
| Ecotipos | CE (dS m-1) | Proteínas (%) | Extracto etéreo (%) | Fibra cruda (%) |
|---|---|---|---|---|
| E1 | 2.5 | 24.57 ± 0.05c* | 2.46 ± 0.01c | 8.44 ± 0.03e |
| E1 | 10 | 20.73 ± 0.01h | 3.79 ± 0.001a | 11.17 ± 0.05a |
| E1 | 20 | 16.86 ± 0.05i | 2.64 ± 0.02b | 7.78 ± 0.05fg |
| E1 | 30 | 22.66 ± 0.02f | 2.13 ± 0.01c | 9.91 ± 0.03d |
| E2 | 2.5 | 21.20 ± 0.03g | 1.66 ± 0.01f | 9.91 ± 0.03d |
| E2 | 10 | 25.09 ± 0.01b | 1.88 ± 0.01e | 10.77 ± 0.05b |
| E2 | 20 | 21.23 ± 0.006g | 1.43 ± 0.01h | 6.62 ± 0.03h |
| E2 | 30 | 15.87 ± 0.01j | 1.33 ± 0.01j | 7.68 ± 0.05g |
| E3 | 2.5 | 26.78 ± 0.07a | 1.53 ± 0.01g | 10.34 ± 0.03c |
| E3 | 10 | 23.38 ± 0.06e | 1.38 ± 0.01i | 7.95 ± 0.03f |
| E3 | 20 | 23.86 ± 0.003d | 1.66 ± 0.01f | 6.45 ± 0.03h |
| E3 | 30 | 17.91 ± 0.03h | 1.23 ± 0.01k | 6.12 ± 0.03i |
*Valores promedio con misma literal en columna, no difieren estadísticamente (Tukey HSD p ≤ 0.05). Los valores representan el promedio ± el error estándar (n = 3).
Contenido mineral en parte área
El análisis de varianza mostró que la composición mineral de parte aérea presentó diferencias significativas entre la interacción de los factores ecotipos × conductividad eléctrica para el contenido de Ca, K, Mg, Mn y Na. El contenido mayor de Ca lo presentaron las plantas del ecotipo E1 en 2.5 dS m-1, mostrando lo contrario las plantas de los ecotipos E1 y E2 en 30 dS m-1. El contenido mayor de K se presentó en las plantas del ecotipo E3 en 2.5 dS m-1 y disminuyó en el mismo ecotipo en 30 dS m-1, así como en los ecotipos E1y E2 en 20 y 30 dS m-1. Las plantas del ecotipo E1 en 2.5 dS m-1 mostraron el contenido mayor de Mg y lo contrario lo presentaron las plantas de este ecotipo en 30 dS m-1, así como los ecotipos E2 y E3 en 20 y 30 dS m-1. El Mn mostró los valores mayores en las plantas del ecotipo E2 en 2.5 dS m-1, expresando lo contrario las plantas del ecotipo E1 en 20 y 30 dS m-1. El contenido de Na fue mayor en las plantas del ecotipo E3 en 30 dS m-1 y disminuyó en los tres ecotipos en 2.5 dS m-1. El contenido de Fe, aunque no mostró diferencias significativas en la interacción de los factores, el contenido mayor de Fe fue en las plantas del ecotipo E1 en 20 dS m-1 y disminuyó en los tres ecotipos en 30 dS m-1 (Tabla 6).
Tabla 6 Valores promedio del contenido mineral en parte aérea y raíces de tres ecotipos de Suaeda edulis sometidos a estrés con mezclas de agua de mar (2.5, 10, 20 y 30 dSm-1) y agua de tilapia.
| Contenido mineral en parte área (tallos + hojas). Valores expresados en g kg-1 | |||||||
|---|---|---|---|---|---|---|---|
| Ecotipos | CE | Ca | Fe | K | Mg | Mn | Na |
| E1 | 2.5 | 39.64 ± 0.16a | 0.07 ± 0.009a | 31.38 ± 1.69c | 26.50 ± 1.11a | 0.09 ± 0.005d | 50.41 ± 3.06f |
| E1 | 10 | 23.05 ± 1.43c | 0.07 ± 0.005a | 18.96 ± 0.54de | 25.09 ± 0.81b | 0.07 ± 0.003d | 85.23 ± 2.26e |
| E1 | 20 | 12.44 ± 0.28de | 0.37 ± 0.34a | 11.11 ± 0.08f | 20.53 ± 0.29bc | 0.02 ± 0.004ef | 103.10 ± 2.62cd |
| E1 | 30 | 8.19 ± 0.22e | 0.05 ± 0.002a | 10.68 ± 0.21f | 17.29 ± 0.91c | 0.01 ± 0.0003f | 107.39 ± 4.28c |
| E2 | 2.5 | 37.19 ± 1.58b | 0.10 ± 0.005a | 46.44 ± 2.01b | 25.29 ± 1.22ab | 0.13 ± 0.003a | 57.16 ± 1.96f |
| E2 | 10 | 14.23 ± 0.30d | 0.09 ± 0.002a | 29.09 ± 1.27c | 21.58 ± 0.81bc | 0.09 ± 0.003cd | 86.60 ± 1.38de |
| E2 | 20 | 10.59 ± 0.45de | 0.08 ± 0.004a | 13.58 ± 0.10ef | 18.26 ± 0.48c | 0.10 ± 0.006b | 119.44 ± 3.52bc |
| E2 | 30 | 9.38 ± 0.07e | 0.05 ± 0.002a | 11.33 ± 0.32f | 17.41 ± 0.20c | 0.04 ± 0.001e | 114.48 ± 4.88bc |
| E3 | 2.5 | 29.51 ± 1.79b | 0.16 ± 0.01a | 54.46 ± 3.11a | 25.50 ± 0.42ab | 0.10 ± 0.003b | 45.74 ± 3.39f |
| E3 | 10 | 24.58 ± 0.91c | 0.09 ± 0.007a | 20.52 ± 0.29d | 28.19 ± 1.38a | 0.09 ± 0.006cd | 103.75 ± 4.80c |
| E3 | 20 | 10.99 ± 0.44de | 0.08 ± 0.002a | 13.38 ± 0.51ef | 18.76 ± 0.37c | 0.09 ± 0.003c | 125.10 ± 0.95ab |
| E3 | 30 | 9.81 ± 0.09de | 0.06 ± 0.003a | 10.05 ± 0.37f | 20.23 ± 1.34c | 0.06 ± 0.002d | 141.77 ± 3.98a |
| Contenido mineral en raíces. Valores expresados en g kg-1 | |||||||
| Ecotipos | CE | Ca | Fe | K | Mg | Mn | Na |
| E1 | 2.5 | 23.42 ± 0.01a | 7.34 ± 0.02a | 10.82 ± 0.008l | 11.01 ± 0.01i | 0.17 ± 0.007bc | 5.68 ± 0.007j |
| E1 | 10 | 17.23 ± 0.01c | 3.33 ± 0.01e | 33.50 ± 0.006e | 13.02 ± 0.01f | 0.14 ± 0.006d | 20.72 ± 0.01e |
| E1 | 20 | 15.74 ± 0.01d | 5.65 ± 0.03b | 19.33 ± 0.01k | 16.56 ± 0.03d | 0.11 ± 0.005de | 40.76 ± 0.03c |
| E1 | 30 | 19.24 ± 0.02b | 5.16 ± 0.03c | 21.25 ± 0.02j | 18.80 ± 0.01c | 0.13 ± 0.008de | 37.75 ± 0.02d |
| E2 | 2.5 | 9.41 ± 0.01i | 0.66 ± 0.03i | 26.64 ± 0.02g | 7.22 ± 0.01k | 0.31 ± 0.007b | 8.71 ± 0.005h |
| E2 | 10 | 10.30 ± 0.005g | 4.12 ± 0.01d | 22.14 ± 0.02i | 12.26 ± 0.03h | 0.15 ± 0.006cd | 16.74 ± 0.01g |
| E2 | 20 | 6.27 ± 0.01l | 0.76 ± 0.03hi | 48.76 ± 0.03c | 14.35 ± 0.03e | 0.16 ± 0.007bcd | 43.00 ± 0.01c |
| E2 | 30 | 9.16 ± 0.03j | 2.00 ± 0.01f | 46.34 ± 0.02d | 22.64 ± 0.02a | 0.09 ± 0.005ef | 48.12 ± 0.01b |
| E3 | 2.5 | 11.21 ± 0.01f | 1.61 ± 0.01f | 32.93 ± 0.01f | 6.03 ± 0.02l | 0.16 ± 0.005cd | 7.91 ± 0.007i |
| E3 | 10 | 14.66 ± 0.03e | 1.14 ± 0.02g | 25.65 ± 0.02h | 10.11 ± 0.01j | 0.38 ± 0.005a | 19.61 ± 0.007f |
| E3 | 20 | 6.73 ± 0.02k | 1.92 ± 0.01f | 58.65 ± 0.02b | 12.66 ± 0.03g | 0.06 ± 0.004g | 42.95 ± 0.02c |
| E3 | 30 | 10.17 ± 0.03h | 0.83 ± 0.02h | 63.31 ± 0.007a | 19.36 ± 0.03b | 0.08 ± 0.005fg | 51.15 ± 0.02a |
Contenido mineral en raíces
El análisis de varianza mostró que, la composición mineral de raíces exhibió diferencias significativas entre la interacción de los factores para el contenido de Ca, Fe, K, Mg, Mn y Na. El contenido mayor de Ca lo presentaron las plantas del ecotipo E1 en 2.5 dS m-1, mostrando lo contrario las plantas de los ecotipos E2 y E3 en 20 dS m-1. El contenido de Fe fue mayor en las plantas del ecotipo E1 en 2.5 dS m-1 y disminuyó en el ecotipo E2 en 2.5 y 20 dS m-1. El contenido mayor de K fue en las plantas del ecotipo E3 en 30 dS m-1 y disminuyó significativamente en el ecotipo E1 en 2.5 dS m-1. Las plantas del ecotipo E2 en 30 dS m-1 mostraron el contenido mayor de Mg y lo contrario lo presentaron las plantas del ecotipo E3 en 2.5 dS m-1. El Mn mostró el contenido mayor en las plantas del ecotipo E3 en 10 dS m-1, manifestando lo contrario las plantas de este ecotipo en 20 y 30 dS m-1. El contenido mayor de Na fue en las plantas del ecotipo E3 en 30 dS m-1 y disminuyó significativamente en los tres ecotipos en 2.5 dS m-1 (Tabla 6).
Discusión
Variables morfométricas
La respuesta del ecotipo E3 en la longitud de raíces sugiere que este ecotipo incrementó su sistema radicular con el propósito de evadir o escapar a la salinidad en el medio de cultivo. Este estudio demuestra que las diferencias en la respuesta al efecto de la salinidad, además de ser notorio entre especies, es también apreciable en una misma especie. Las expresiones de la variedad en el genotipo de las especies permiten diferenciar varios ecotipos de acuerdo con las variables ambientales que se presenten en el área donde crece o se desarrolle (Juraniec et al. 2024). Los estudios con especies glicófitas reportan que estas son afectadas en su morfometría en condiciones de salinidad, disminuyendo sus valores (Rasouli et al. 2021). Aunque no existen suficientes estudios con S. edulis, otras especies de este género han mostrado la plasticidad que en ellas se presenta como respuesta a variaciones ambientales y la expresión de su genotipo (Gianella et al. 2021). El desarrollo en las especies halófitas como S. edulis es distinto al de las plantas que no toleran niveles de salinidad elevados. En este estudio se observó que algunas variables morfométricas aumentaron al incrementar la conductividad eléctrica en el agua. La investigación de Noguez-Hernández et al. (2013) reportó que, S. edulis presentó variación entre localidades del Centro de México, entre las que existen variaciones de salinidad en el suelo. En estos sitios de características ambientales distintas, S. edulis desarrolla diferencias, dando como resultado una variedad de ecotipos, lo cual coincide con los resultados de este estudio. La S. edulis, como especie halófita es tolerante a la sal a la que se adapta y crece en hábitats salinos, como otras especies halófitas suculentas (Griffiths y Males 2017). Esta especie como otras halófitas se distingue porque utiliza más de un mecanismo para regular la salinidad y evitarla. Estos mecanismos dependen de sus características anatómicas, morfométricas y fisiológicas para tolerar y/o resistir dicho estrés. En ese sentido, algunas variables morfométricas en el presente estudio no mostraron diferencias significativas entre ecotipos en los niveles de conductividad eléctrica en los cuales se cultivaron y, en algunas otras variables, la diferencia numérica no fue evidente, lo cual coincide con Rahman et al. (2021).
Variables fisiológicas
El potencial hídrico tiene un efecto directo en la disminución del contenido relativo de agua en la planta, pues se asocia a la disminución de la intensidad de flujo de agua desde las raíces a la parte aérea, porque a una conductancia estomática menor le corresponderá un intercambio de vapor de agua menor y, por tanto, menor transpiración y como consecuencia un menor movimiento del agua en la planta, lo que conlleva a una menor hidratación de la parte aérea de la planta, provocando una depresión en los potenciales osmóticos, lo cual coincide con lo reportado por Goto et al. (2021). En relación con otras especies del género Suaeda, Levinsh (2023) clasifica a S. salsa como una especie halófita suculenta cuyo incremento en el contenido de agua se asoció con una mayor conductancia hidráulica de las raíces y la inducción de la expresión de un gen que codifica las acuaporinas. Sin embargo, en otro estudio, el incremento de la salinidad (hasta 400 mM de cloruro de sodio) no provocó cambios en el contenido de agua de los brotes o las raíces en S. salsa y S. glauca, pero el contenido de agua de los brotes disminuyó a una concentración alta de 28 mM de carbonato de sodio en ambas especies (Li et al. 2019).
Los ecotipos de S. edulis del presente estudio, mostraron una respuesta similar tanto a las especies halófitas como no halófitas, demostrando que, como especie halófita suculenta, tiene tejidos especializados para almacenar agua y su contenido de agua generalmente aumenta con el incremento de la salinidad. Este incremento solo se presenta hasta cierto nivel de salinidad, seguido de una disminución en el contenido de agua. La suculencia es una estrategia adaptativa de las plantas expuestas al estrés por salinidad, que provoca un aumento en el contenido de humedad de las plantas.
La S. edulis presenta hojas suculentas, lo cual le permite mantener un contenido de agua mayor para diluir la concentración alta de sal en los tejidos de la planta y disminuir la presión osmótica. Otras especies mantienen su crecimiento en condiciones salinas, al producir solutos como prolina y glicina betaína, para regular la turgencia, provocando un aumento en el volumen celular (Ghanem et al. 2021); sin embargo, las respuestas a la salinidad por lo general dependen de la especie, ecotipo o variedad.
El estrés salino no solo tiene un efecto negativo en los pigmentos fotosintéticos y en la estructura interna de la hoja sino también, conduce a cambios significativos en el estado hídrico de las plantas debido al estrés osmótico de la salinidad (EI-Hendawy et al. 2019). Si bien el contenido de clorofila no mostró diferencias significativas en la interacción de los factores, es evidente que la respuesta de S. edulis a la salinidad en el medio de cultivo es positiva en cuanto a acumular pigmentos como la clorofila, lo cual se presenta también en otras especies halófitas. Al parecer el incremento de la clorofila se atribuye al aumento en el espesor de la capa del mesófilo, lo que provoca un incremento en la clorofila, así como en la capacidad fotosintética de la planta, lo cual coincide con los estudios de Lombardi et al. (2022) y Bhattacharya (2022). En el presente estudio las plantas de los ecotipos E1 y E3 mostraron un verde más intenso, lo cual se asocia con el contenido más alto de clorofila, que las hace más atractivas para los consumidores. El color es una de las características que se valoran en las halófitas, por lo que estos ecotipos serán preferidos al momento de consumirlos, lo cual coincide con lo reportado por Castañeda-Loaiza et al. (2020). Estos autores afirman que el color es muy valorado en las halófitas y que las plantas silvestres de las especies que estudiaron podrían ser las preferidas por los consumidores por presentar una coloración verde más intensa. El contenido de clorofila “b” y “total” mostró una correlación significativa pero negativa con los valores de SPAD-502 (n = 36, r = -0.44, p = 0.007 y r = -0.37, p = 0.027, respectivamente). Esta correlación demuestra que el aumento de la conductividad eléctrica del medio de cultivo afectó las características de reflectancia espectral, al presentar un coeficiente de correlación significativo y negativo con la conductividad eléctrica (n = 36, r = -0.37, p = 0.02), mostrando que, conforme se incrementó la conductividad eléctrica, los valores de clorofila SPAD, disminuyeron.
Análisis proximal
Los estudios con especies halófitas como la Salicornia fruticosa reportan que esta especie cultivada en diferentes concentraciones de NaCl no varía de manera significativa su contenido de proteínas totales y de lípidos (Agudelo et al. 2021). Si bien las halófitas se consideran vegetales por sus propiedades organolépticas, sabor salado y plantas medicinales por la presencia de compuestos bioactivos, estudios recientes afirman que la composición nutricional/química de las halófitas no ha sido investigada en detalle (Maatallah et al. 2020). En el presente estudio, el contenido de proteínas de los tres ecotipos de S. edulis se mantuvo con valores similares en las diferentes conductividades eléctricas; sin embargo, en 30 dS m-1 se redujo significativamente. Esta respuesta se explica debido a que las halófitas adoptan una estrategia para reducir la tasa de crecimiento a través de varios mecanismos, incluido el aumento de la síntesis de proteínas, lo que conduce a una mayor fijación de nitrógeno (Akhtar 2019). En relación con las macromoléculas, se ha demostrado que las proteínas constituyen el porcentaje mayor en algunas especies como Halocnemum strobilaceum y Suaeda fruticosa, seguida de los carbohidratos y luego los lípidos (Gheraissa et al. 2023). Este hallazgo es consistente con el estudio de Qasim et al. (2017), donde la proporción de proteína fue mayor que la proporción de carbohidratos en las cinco especies halófitas estudiadas (Thespesia populneoides, Salvadora persica, Ipomoea pes-caprae, Suaeda fruticosa, and Pluchea lanceolata). Las características fisicoquímicas y fisiológicas mostradas por los ecotipos de S. edulis en este estudio evidencian que los tres ecotipos tienen un contenido nutricional importante para el ser humano incluso para animales domésticos. Este resultado sugiere su explotación como fuente de alimento o pastoreo en la región noroeste de México, donde el agua para la agricultura se está agotando y los suelos presentan un proceso progresivo de salinización con afectaciones futuras hasta del 40% de la superficie agrícola, siendo necesario introducir especies cultivables tolerantes a la salinidad y a las condiciones extremas de precipitaciones escasas y erráticas, así como temperaturas altas (Costa-Becheleni et al. 2021). Los romeritos (S. edulis) se consumen preparados en diversos platillos en la cocina mexicana y son productos alimenticios, aditivos con propiedades sensoriales para alimentos y alimentos funcionales que tienen un efecto fisiológico deseable más allá de la nutrición básica, suplementos dietéticos o nutracéuticos. Los romeritos al igual que todos los quelites, contienen sustancias bioactivas como ácidos fenólicos (ácido ferúlico y ácido gálico), flavonoides como quercetina y rutina, así como ácidos ferúlico y sináptico por lo que se consideran especies potenciales para nuevos alimentos funcionales por su alta concentración de compuestos fenólicos (Costa-Becheleni et al. 2024).
Contenido mineral
Las especies del género Suaeda se han utilizado con éxito para el tratamiento de suelos afectados por salinidad (Wang et al. 2022). Estas especies se reportan que acumulan niveles altos de minerales como el Na, K, Cl y Ca. Por lo anterior, su uso con fines bio-remediadores está avalado y recomendado. El contenido de Na de los ecotipos de S. edulis es superior a los reportados en Salicornia (Agudelo et al. 2021). En sentido general, los estudios con S. edulis son casi nulos, pero algunos realizados con especies del mismo género los reconocen como acumuladoras de minerales (Ibraheem et al. 2022, Naz et al. 2022). En este estudio, fue evidente que el uso de agua residual de tilapia proporcionó los minerales para el crecimiento y desarrollo de S. edulis, como se ha mostrado para otras especies (Chiquito-Contreras et al. 2022, Álvarez-García et al. 2019)). La acumulación mayor de Na tanto en parte aérea como en raíces se presentó en las plantas del ecotipo E3 sometidas a 30 dS m-1. Cabe señalar que, este ecotipo se colectó en el sitio Lago Cuitzeo, Cuitzeo del Porvenir, Michoacán en donde la conductividad eléctrica del suelo fue de 0.03 dS m-1 y fue el sitio de colecta con menor conductividad eléctrica en el suelo. Esta respuesta debe tomarse en consideración si se pretende elegir un ecotipo con capacidad de bio-remediación para absorber el Na del suelo o del agua. En general, los tres ecotipos mostraron tendencia de incrementar la acumulación de Na en sus tejidos, tanto en parte aérea como en raíces conforme la conductividad eléctrica incrementó (Tabla 5). En relación con la acumulación de minerales por tejido vegetal, el Ca, Mg y Na se acumularon mayormente en parte aérea (hojas + tallos), mientras que, Fe, K y Mn, se acumularon mayormente en raíces (Tabla 5). La diferencia de concentración de iones se atribuye a la sensibilidad diferencial entre ecotipos de una especie. Sin embargo, para algunas glicófitas la sensibilidad a ciertos iones como el de Na es mayor en parte aérea (Bueno y Cordovilla 2020), contrario a lo que generalmente se observa en especies halófitas. En este estudio, el Ca y Na mostraron valores mayores en parte aérea que en raíces, resultados que difieren de los reportados para halófitas (Zhao et al. 2022). Los estudios con otras especies reportan que los niveles de iones de Na se incrementan conforme aumentan los niveles salinos del medio de cultivo (Hniličková et al. 2019). Asimismo, se observan diferencias entre las concentraciones de iones en la parte aérea y las raíces de distintos genotipos de una especie en distintos niveles de salinidad (Zhang et al. 2022), lo que coincide con los resultados de este estudio. La acumulación de Na tanto en parte aérea como en raíces en los tres ecotipos en los niveles de conductividad eléctrica de 20 y 30 dS m-1, es una característica de S. edulis como planta halófita. Lo anterior se atribuye a la adaptación a la salinidad la cual realiza mediante el equilibrio osmótico al aumentar la acumulación de minerales, resultados que coinciden con los reportados por Jēkabsone et al. (2022). De esta manera, S. edulis, al ser una halófita, también adopta la estrategia de acumular sales dentro del tonoplasto, las cuales obtiene del sustrato en el que se cultiva, en este caso, sustrato acuoso (hidroponia) función que realiza como respuesta a condiciones de alta salinidad, asegurando con ellos sus requerimientos hídricos. Esta respuesta de S. edulis coincide con lo reportado por Hao et al. (2021).
Conclusiones
Los ecotipos mostraron una respuesta diferencial en las variables morfométricas, fisiológicas, bioquímicas y acumulación de minerales en parte aérea y raíces por efecto del estrés en el medio de cultivo hidropónico. El uso de agua de mar mezclada con agua procedente del cultivo de tilapia con diferentes conductividades eléctricas provocó una respuesta de tipo polinomial (cúbica/cuártica) en la mayoría de las variables evaluadas. Las variables mostraron valores bajos en bajas conductividades eléctricas y una respuesta máxima positiva a niveles intermedios de conductividad eléctrica. Esta respuesta sugiere condiciones óptimas para el crecimiento en esa conductividad, mientras que, en alta conductividad, se observó una disminución en la mayoría de las variables, lo que indica un efecto negativo, como estrés salino o limitación fisiológica.











 nueva página del texto (beta)
nueva página del texto (beta)



