Introducción
En la avicultura de traspatio que se desarrolla en México la cría de patos (Anas platyrhynchos domesticus y Cairina moschata domesticus) y guajolotes (Meleagris gallopavo gallopavo) proporcionan proteína de alta calidad y son una fuente de ingresos para las familias de escasos recursos de las zonas marginales de Tepatepec, Hidalgo, México. Hay poca información sobre las características físicas, el color de la yema y el contenido de ácidos grasos del huevo de pato y guajolote criollo. Los patos son aves que tiene la destreza de adaptarse a distintos tipos de climas, pueden subsistir con dietas sencillas realizadas con ingredientes disponibles locamente (Al-Obaidi y Al-Shadeedi 2016). La cría del guajolote criollo es de importancia cultural en los pequeños y medianos poblados de México. Al respecto, García-Flores y Guzmán-Gómez (2016), mencionan que los principales usos de esta ave es el auto consumo, la venta y como obsequios o regalos en las fiestas familiares y religiosas, sin embargo, el incremento de las zonas urbanas ha reducido la cría y producción de esta especie en los últimos años y por consecuencia esta actividad avícola ha tenido un descenso considerable, al punto de que en muchas zonas rurales tiende a desaparecer (Cruz-Lujan et al. 2023). Mientras que Camacho-Escobar et al. (2008)), mencionan que el estudio del guajolote criollo es una necesidad urgente, debido a que no se descarta la posibilidad de una extinción a corto plazo, lo que sería una pérdida de un valioso recurso genético.
Los huevos de pato son de mayor tamaño que el de las gallinas, su peso oscila entre los 60 y 90 g (Hong y Benjakul 2019), se observan tres partes importantes: la yema, la clara y el cascarón. El color de la yema es un aspecto importante para el consumidor, debido a que se tiende a asociar el color amarillo intenso a naranja con un estado de frescura y buena salud (Galobart et al. 2004). El color intenso en la yema refleja un consumo elevado de xantofilas presentes en las hojas verdes y semillas (Thomas y Johnson 2018). El color amarillo y anaranjado de la yema proviene de la luteína y zeaxantina, se ha evidenciado que el consumo de la yema aporta pequeñas cantidades de estas xantofilas, benéficas para la salud humana (Ortiz et al. 2021). La luteína y zeaxantina se acumulan en el cerebro y pueden desempeñar una función en la salud cognitiva, mientras que, las xantofilas reducen los radicales libres debido a su actividad antioxidante (Thomas y Johnson 2018). Es necesario impulsar la producción de estas aves en la avicultura de traspatio debido a que son una alternativa económica para reducir la desnutrición y evitar la extinción de estas especies, el objetivo de esta investigación fue describir las características físicas externas e internas, el color de la yema y el contenido de ácidos grasos del huevo de pato y guajolote criollo.
Materiales y métodos
El trabajo se desarrolló en la Unidad Avícola de la Universidad Politécnica de Francisco I. Madero, ubicada a 1 900 m de altitud (Rodríguez-Ortega et al. 2021) en Tepatepec, Hidalgo México. Se utilizaron 114 huevos de pato (Anatidae spp.) y 114 huevos de guajolote criollo (Meleagris gallopvo gallopavo), los cuales fueron colectados en las pequeñas unidades de producción que se desarrollan en las zonas rurales del Valle del Mezquital Hidalgo, México. El huevo colectado se almacenó en un refrigerador a 12°C hasta su análisis, se registró su peso, largo o diámetro polar, ancho o diámetro ecuatorial y el grosor del cascarón mediante un vernier digital (Modelo HER-411, STEREN, México) con rango de medición de 0 a 150 mm y resolución de 0.1 mm. Las aves que se desarrollan en las pequeñas unidades de producción basan su alimentación en pequeños insectos, plantas del lugar y desechos de cocina (Camacho-Escobar et al. 2023).
El peso de yema, clara y cascarón fueron registrados con báscula digital con capacidad de 200 g y resolución de 0.01 g (Modelo MH-200, Marca MKS Tools, China). La pigmentación de la yema se midió visualmente utilizando el abanico de colores de DSM, tres evaluadores calificaron el color que coincidió con el abanico, los colores del abanico van desde amarillo pálido (valor:1) a naranja obscuro (valor: 15), la cantaxantina es responsable del color naranja de la yema y su intensidad esta correlacionada con la cantidad presente (Umar et al. 2018), mientras que, la luteínas y zeaxantina son responsables del color amarillo en la yema (Zaheer 2017).
El perfil de ácidos grasos del huevo de pato y guajolote criollo se determinó con la metodología de Palmquist y Jenkins (2003) y Jenkins (2010), en un cromatógrafo de gases HP 6890 (Estados Unidos, New York) con inyector automático y detector de ionización de flama con columna capilar SUPELCO SP 2560 de 100 m, diámetro interno de 0.25 mm y 0.2 micras de película, con helio como gas acarreador. Para la identificación de los ácidos grasos se utilizó un estándar FAME Mix C4-C24 100 mg SUPELCO con número de catálogo 18919-1 en ampolleta (St. Louis, MO, USA).
Análisis estadístico. El peso de: huevo, yema, clara, cascarón, largo, ancho y grosor del cascarón del huevo de guajolote y pato fueron analizados con el procedimiento PROC GLM, y las medias fueron comparadas con la prueba de Tukey. El color de la yema fue analizado con el procedimiento GLM y PROC FREQ de SAS (2013), la determinación de ácidos grasos fue realizada en una sola repetición debido a los elevados costos del análisis, por tal motivo solo se describen. Se utilizó el procedimiento PROC CORR para determinar la relación entre el peso de huevo con el peso de la clara.
Resultados
Las características físicas externas: peso, largo y ancho fueron superiores (P < 0.05) en el huevo de guajolote criollo y pato (Tabla 1). El grosor del cascarón fue superior en el huevo de guajolote criollo con respecto al cascarón del huevo de pato (Tabla 1).
Tabla 1 Peso, largo y ancho de huevo de guajolote criollo y pato.
| Huevo | Peso (g) | Largo (mm) | Ancho (mm) | Grosor del cascarón (mm) |
|---|---|---|---|---|
| Guajolote criollo | 81.94a | 65.48a | 48.67a | 0.39a |
| Pato | 66.62b | 60.95b | 44.59b | 0.31b |
| Error estándar | 0.887 | 0.377 | 0.814 | 0.006 |
Letras diferentes por columna indican diferencias significativas, de acuerdo con la prueba de Tukey (P < 0.05).
La clara presentó mayor peso relativo que la yema, mientras que, el cascarón es el componente con menor peso relativo. El peso relativo de la clara fue mayor (P < 0.05) en el huevo de guajolote con respecto al de pato, mientras que, la yema de pato tuvo mayor peso relativo. El cascarón es considerado el empaque natural del huevo, no contamina y es biodegradable, el peso relativo del cascarón fue similar (P > 0.05) en el huevo de guajolote y de pato (Tabla 2).
Tabla 2 Peso de la clara, yema y cascarón en relación con el peso de huevo (peso relativo).
| Peso relativo | |||
|---|---|---|---|
| Huevo | Clara (%) | Yema (%) | Cascarón (%) |
| Guajolote criollo | 52a | 35b | 13a |
| Pato | 45b | 42a | 13a |
| Error estándar | 0.5341 | 0.4694 | 0.2827 |
Letras diferentes por columna indican diferencias significativas, de acuerdo con la prueba de Tukey (P < 0.05).
El color de la yema es una característica interna importante para el consumidor, en el huevo de guajolote criollo la yema fue más (P < 0.05) colorida que la de pato (Figura 1).
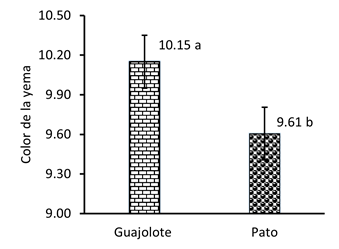
Figura 1 El color de la yema de huevo de guajolote criollo y pato, de acuerdo con el abanico de color de yema de DSM. Letras diferentes en columna indican diferencias significativas, al comparar las medias con la prueba de Tukey (P < 0.05).
El color de la yema es un reflejo de la alimentación de las aves, una alimentación rica en carotenoides incrementa el color de la yema. La yema en el huevo de guajolote criollo presentó la mayor intensidad de color. El 34.2% de las yemas tuvieron una intensidad de color en la escala 11, 29.8% presentaron el valor de 10 y el 21.9% el valor 9. La yema en huevo de pato fue menos intenso su color con respecto a la de guajolote, 9.7% mostraron valores de 5 y 7 y el 29.8% tuvieron valores de 11 (Tabla 3).
Tabla 3 Color de la yema (%) de huevo de guajolotas criollas y pato, las escalas de color de acuerdo con la escala de color del abanico de DSM.
| Escala de colores | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Especie | 4 | 5 | 7 | 8 | 9 | 10 | 11 | 12 | 15 |
| Guajolote | 0 | 0 | 1.8 | 3.5 | 21.9 | 29.8 | 34.2 | 8.8 | 0.0 |
| Pato | 4.4 | 9.7 | 9.7 | 0.0 | 8.8 | 23.7 | 29.8 | 10.5 | 3.5 |
La búsqueda de ingredientes con alto contenido de ácidos grasos esenciales omega 3 se ha incrementado por parte de los consumidores, por tal motivo es importante evaluar los ácidos grasos presentes en el huevo de guajolote criollo y pato, es una posibilidad para incrementar el consumo de este producto y a su vez evitar que estas especies se extingan. El huevo de guajolote criollo tuvo ligeramente mayor contenido de ácido mirístico, miristoléico, pentadecanoico, palmítico, palmitoleico, heptadecanoico, esteárico, linoleico y docosahexaenoico (DHA) con respecto al huevo de pato (Tabla 4). Sin embargo, el huevo de pato presentó mayor contenido de ácido linolénico (omega 3) y oleico (omega 9, Tabla 4).
Tabla 4 Contenido de ácidos grasos de huevo de pato y guajolotes criollos, colectados en la avicultura de traspatio.
| Composición | Nombre del ácido graso | % | |
|---|---|---|---|
| Pato | Guajolote | ||
| C14:0 | Mirístico | 0.416 | 0.449 |
| C15:0 | Pentadecanoico | No detectado | 0.0904 |
| C16:0 | Palmítico | 26.437 | 27.706 |
| C17:0 | Heptadecanoico | 0.072 | 0.217 |
| C18:0 | Esteárico | 7.716 | 10.134 |
| Total de ácidos grasos saturados | 34.641 | 38.596 | |
| C14:1 | Miristoléico | 0.046 | 0.069 |
| C16:1n9 | Palmitoleico | 2.201 | 4.351 |
| C18:1n9 | Oleico (omega 9) | 44.784 | 37.934 |
| C18:2n6 | Linoleico (omega 6) | 7.674 | 11.770 |
| C18:3n3 | Linolénico (omega 3) | 0.292 | 0.120 |
| C20:4n6 | Araquidónico | 4.590 | 1.566 |
| C22:6n3 | Docosahexaenoico (DHA) | 0.405 | 0.764 |
| Total de ácidos grasos insaturados | 59.992 | 56.574 | |
Discusión
La calidad externa del huevo incluye el peso y forma, así como el color e integridad del cascarón (WingChing-Jones et al. 2023). El peso es una característica importante para el consumidor, una pieza de huevo de mayor tamaño tiene mayor aceptabilidad que una pieza de huevo pequeña. El peso del huevo de pato fue menor (p < 0.05) que el de guajolote criollo (66.62 vs 81.94 g, Tabla 1), esto podría deberse que las hembras de pato son más pequeñas que las guajolotas. Mientras que Kuru y Kırmızıbayrak et al. (2023) reportaron que las hembras de pato Pekin tienen un peso vivo de 1 788 g, en tanto que, López et al. (2008) observaron que las guajolotas criollas tienen un promedio de peso vivo entre 2 920 a 4 350 g.
El huevo de pato y guajolota son un recurso económico para las familias de escasos recursos en México, estos se venden en los mercados tradicionales, por tal motivo es necesario impulsar la producción de estas aves, el peso de huevo observado coincide con los reportados por Sogunle et al. (2017), quienes reportan que el peso de huevo de pato fue de 63.49 ± 0.98 g. Mientras que Biesiada-Drzazga et al. (2014) mencionan que el tamaño del huevo de pato incrementa con la edad de las aves. En tanto, que el peso del huevo de guajolote criollo concuerda con Juárez-Caratachea et al. (2011) quienes reportaron un peso promedio de 79.7 ± 5.31 g. Mientras que WingChing-Jones et al. (2023) mencionan que el peso de huevo, el largo, ancho, color y grosor del cascarón son características morfológicas externas que pueden ser afectadas por factores como la edad de las aves, el tipo de alimentación y el peso corporal. Sobre el peso Camacho-Escobar et al. (2008) clasificaron el peso de huevo de guajolotes criollos de la siguiente manera: con 53.8 g son considerados chicos, con 59.6 g medianos, con 62.7 g grandes y de 72. 9 g extragrandes, de acuerdo con esta clasificación el huevo utilizado se consideran de talla extragrande (Tabla 1). En tanto que, Juárez-Caratachea et al. (2011) observaron en el huevo de guajolote criollo tiene valores similares a los encontrados en el presente trabajo (Tabla 1).
El color, peso y grosor del cascarón son características importantes para el consumidor y la industria avícola, una reducción del grosor del cascarón incrementa las perdidas por rupturas o grietas. El grosor fue menor (P < 0.05) en el huevo de pato en comparación con el huevo de guajolote criollo (Tabla 1). El grosor y peso del cascarón se encuentra determinado por la edad de la hembra. Al respecto, Valdés et al. (2011) reportaron que el grosor del cascarón disminuye a medida que las aves envejecen, dietas con un adecuado nivel de calcio puede revertir la disminución de este. En lo referente al cascarón en buen estado está formado por 95% de CaCO3, 3% de fósforo, de 2 a 3% de magnesio y pequeñas cantidades de Na, Zn, Mn, Fe y Cu, con respecto al CaCO3 de un huevo en buen estado se tiene en promedio 2.2 a 3 g de calcio (Ajayan et al. 2020). La principal función del cascarón por su dureza y grosor es proteger la clara y la yema que se encuentran en su interior. El peso relativo del cascarón del huevo de guajolote criollo fue similar (P > 0.05) al de pato (Tabla 2). Los valores del peso relativo del cascarón son similares a los observados por Montenegro et al. (2019), quienes reportaron que el peso relativo del cascarón del huevo de gallinas se encuentra entre 9 y 10% con correlación positiva entre el peso del huevo y el peso relativo del cascarón (r = 0.83), lo cual indica que mientras más pesado sea un huevo mayor peso relativo de cascarón debe tener.
El huevo es un alimento rico en proteína, ácidos grasos y pigmentos que son benéficos para la salud humana, por otra parte, en México es la fuente de proteína animal más barata, la clara es la principal fuente de proteína y la yema de lípidos (Abeyrathne et al. 2013). El huevo de guajolote tuvo mayor (P < 0.05) peso relativo de clara que el de pato (52 vs 45%, Tabla 2). El menor peso de la clara esta correlacionado (r = 0.904) con el peso de huevo, mientras más pequeño menor contenido de clara, el huevo de pato fue más pequeño que el huevo de guajolota. Al respecto Abeyrathne et al. (2013) observaron que la clara ocupa el 60%, 30-33% la yema y 12% el cascarón en el huevo de gallina, valores que son similares a los encontrados en esta investigación. Al respecto se sabe que la clara está compuesta de agua y proteínas como la ovoalbúmina, ovotransferrina, ovomucoide, ovomucina y la lisozima (Lomakina y Míková 2006).
La yema, contiene ácidos grasos, proteínas, carbohidratos, vitaminas, minerales, y xantofilas, el consumidor tiene preferencias por una yema grande y colorida (Patil et al. 2022), el peso relativo de la yema fue mayor (P < 0.05) en el huevo de pato (Tabla 2). Los valores observados en el peso relativo de la yema de este trabajo son similares a los observados por Van-der-Wagt et al. (2020) quienes reportan valores entre 28 y 32% en el huevo de pato y en el de guajolote entre 26 y 33%. El peso de la yema es responsabilidad del hígado. Al respecto, Liu et al. (2018) mencionaron que el eje hígado-sangre-ovario es el responsable de la formación y deposición de la yema. El color de la yema es una de las principales características por las cuales se juzga la calidad del huevo, la luteína y zeaxntina son las xantofilas responsables del color amarillo de la yema (Patil et al. 2022), el abanico colorimétrico de DSM es un instrumento práctico y confiable para medir el color de la yema (Beardsworth y Hernández 2007). El color de la yema del huevo de guajolote criollo fue mayor (P < 0.05) en comparación con el huevo de pato (Figura 1). El contenido de xantofilas presentes en la dieta de las gallinas son las responsables de la intensidad de color amarillo o naranja en la yema (Shevchenko et al. 2021). La yema de guajolote presentó los valores más altos de color en comparación con la yema de huevo de pato, el 34.2% de las yemas analizadas mostraron el valor 11, algunas yemas en el huevo de pato fueron muy coloridas y coincidieron con valores 12 y 15, sin embargo, el porcentaje de yemas con estas escalas fue menor (10.5 y 3.5%, Tabla 3). La yema de huevo de guajolote presentó mayor color debido a que los guajolotes tienen mayor preferencia al pastoreo y un elevado consumo de plantas y semillas ricas en carotenoides comparado con los patos, que pasan más tiempo en zonas húmedas. El consumo de yemas coloridas provenientes del huevo de aves en pastoreo es benéfico para la salud humana, debido a que la luteína y zeaxantina tienen efectos antioxidantes (Carranco et al. 2011, Yunitasari et al. 2023).
La preocupación del ser humano por su salud se ha centrado en el consumo de alimentos con ácidos grasos de buena calidad, que no se sintetizan en el organismo humano y que tienen que ser consumidos en los alimentos, la yema es un producto con alto contenido en ácidos grasos insaturados y poliinsaturados. El ácido mirístico (ácido graso saturado; C14:0) se encuentra en concentraciones bajas en el huevo de ambas especies (Tabla 4), lo que es benéfico para la salud humana, debido que este es un ácido graso que induce la concentración de liproteínas de baja densidad (LDL) en el plasma sanguíneo y eleva los niveles de perilipina-2 (Burdock y Carabin 2007), sin embargo, es fundamental en el recién nacido, el olor del ácido mirístico integra señales sensoriales que guían al recién nacido hacia el seno materno (Gutiérrez-García et al. 2017). El ácido miristoléico se encuentra en pequeñas cantidades en el huevo de pato y guajolote criollo, en un rango de 0.04 a 0.069% (Tabla 4), este ácido graso (C14:1) tiene propiedades antisépticas, lo cual es benéfico para el ser humano, se usa para reducir las lesiones en la piel ocasionadas por Cutibacterium acnés y Staphylococcus aureus (Kim et al. 2021).
El ácido pentadecanoico (ácido graso saturado; C15:00) es un ácido graso de cadena impar que no fue detectado en el huevo de pato, sin embargo, si se observó una pequeña concentración en el huevo de guajolote criollo (Tabla 4). Al respecto, Venn-Watson y Schork (2023) mencionan que este acido es esencial para el ser humano, se incorpora en la bicapa lipídica de las membranas celulares, para reducir el riesgo de la peroxidación lipídica y lisis prematura, concentraciones similares fueron encontradas por Hernández-Guzmán et al. (2021), reportan que el huevo azul de gallinas Araucanas y café de gallinas Marans contienen una pequeña concentración de ácido pentadecanoico (0.07%). El huevo de guajolote mostró ligeramente mayor contenido de ácido palmítico (ácido graso saturado; C16:0) con respecto al huevo de pato (Tabla 4). Este ácido graso participa en la pigmentación de la yema, mientras que Reszczynska et al. (2023) reportan que el ácido palmítico protege las moléculas de luteína de los efectos nocivos del pH y temperatura, y le confiere una mejor solubilidad. Por lo que la ingesta elevada de este ácido graso tiene efectos negativos para la salud humana, como observaron Nestel et al. (1994) quienes reportan que la ingesta elevada de ácido palmítico incrementó los niveles de colesterol (LDL). Mientras que Senyilmaz-Tiebe et al. (2018) mencionan que el consumo de este ácido graso eleva el colesterol (LDL) y el riesgo de aterosclerosis.
La concentración de ácido palmitoleico (ácido graso monoinsaturado; C16:1n9) es mucho menor que la concentración de ácido palmítico, la presencia de ácido palmitoleico fue mayor en el huevo de guajolote que en el huevo de pato (Tabla 4). Este ácido graso tiene acciones benéficas en la salud humana; como lo mencionan Bermudez et al. (2022) quien reportan que este ácido graso tiene acciones biológicas únicas, que actúa como una hormona lipídica o lipocina que coordina las respuestas metabólicas entre los tejidos. Mientras que Cao et al. (2008) observaron que la liberación de ácido palmitoleico en el tejido adiposo mejoró la señalización de la insulina en el músculo y ejerce efectos antiinflamatorios en el tejido adiposo de ratones. El ácido heptadecanoico (ácido graso saturado; C17:0) es un ácido graso de cadena impar, las concentraciones en el huevo son muy pequeñas entre 0.21-0.22% en el huevo de gallinas Araucanas y Marans, (Hernández-Guzmán et al. 2021). En este trabajo el huevo de pato tuvo menor contenido de ácido heptadecanoico en comparación con el huevo de guajolote (Tabla 4). Este ácido graso tiene efectos positivos para la salud (Pfeuffer y Jaudszus 2016), mientras que Xu et al. (2019) observaron que el ácido heptadecanoico promovió la apoptosis en células con cáncer de pulmón. El ácido esteárico (ácido graso saturado; C18:0) no tiene efectos negativos en la salud humana, al respecto, Senyilmaz-Tiebe et al. (2018) mencionan que el ácido esteárico no incrementa los niveles de aterosclerosis y no afecta la función cardiaca, observaron que el consumo induce rápidamente la fusión mitocondrial en los neutrófilos humanos. El contenido de ácido esteárico en el huevo de pato y guajolote no fue tan elevado como el contenido de ácido palmítico (C16: 0), el huevo de guajolote mostró mayor presencia de C18:0 que el de pato (Tabla 4).
El ácido oleico (ácido graso monoinsaturado; C18:1n9), se ha observado que tiene efectos benéficos para la salud (Karacor y Cam, 2015). Al respecto Carrillo et al. (2012) mencionaron que el ácido oleico puede inducir apoptosis en células tumorales, el huevo de pato mostró mayor concentración de ácido oleico con respecto al huevo de guajolote (Tabla 4), el porcentaje de este ácido graso en el huevo de pato y guajolote fue el más sobresaliente en comparación con los otros ácidos grasos (Tabla 4). El consumo de huevo de pato y guajolote de forma moderada puede ser benéfico para la salud humana, es importante concientizar a la población de los efectos saludables que tienen estos tipos de huevo, debido a que es mínima su producción en la región de estudio y pueden llegar a extinguirse ambas especies debido a la pérdida de su habitad por el incremento de zonas urbanas. El ácido linoleico es un ácido graso poliinsaturado (C18: 2n6), la ingesta excesiva de este ácido no es recomendable para la salud, debido que promueve la producción del ácido araquidónico tisular. El contenido de ácido linoleico que tiene el huevo de pato (7.674%) y guajolote (11.770%), fue similar a lo reportado por Sujiwo et al (2017) en el huevo comercial (12.37%). El huevo de guajolote mostró un contenido superior de ácido linoleico que el huevo de pato (Tabla 4). El ácido araquidónico (ácido graso saturado; C20:4n6) se sintetiza a partir del ácido linoleico y es el precursor de las prostaglandinas y otros eicosanoides que son inflamatorios (Jandacek 2017) por lo que su presencia en elevadas concentraciones no es benéfica para la salud.
El huevo de pato tuvo mayor contenido de ácido α-linolénico (C18:3n3), este ácido es esencial para el ser humano y el consumo de alimentos con elevado contenido de este ácido es benéfico para la salud, este ácido se puede transformar en ácido eicosapentaenoico y posteriormente en ácido docosahexaenoico (Castro-González 2002). El huevo de guajolote tuvo menor contenido de ácido áraquidonico (Tabla 4), el contenido de este ácido en ambos tipos de huevo fue muy pequeña, la cantidad de ácido araquidónico en el huevo de pato fue similar a lo que reporta Sujiwo et al (2017) en el huevo (4.32%). El ácido docosahexaenoico (DHA, C22:6n3) es esencial para el crecimiento y desarrollo funcional del cerebro, éste absorbe el DHA con preferencia a otros ácidos grasos (Horrocks y Yeo 1999). El DHA está presente en mayor concentración en el huevo de guajolote (Tabla 4), sin embargo, el huevo de ambas especies son una fuente de DHA que beneficia la salud del ser humano.
Conclusiones
En esta investigación se concluye que el huevo de guajolote criollo presentó las mejores características físicas como el tamaño, largo, ancho y grosor del cascarón, así como el mayor peso relativo de clara. El color de la yema fue más intenso en el huevo de guajolote criollo, lo que indica una mayor presencia de carotenoides benéficos para la salud humana. El huevo de guajolote tuvo mayor contenido de ácido docosahexaenoico (DHA), sin embargo, el huevo de pato tuvo mayor contenido de omega 3 (linolénico), estos dos ácidos grasos presentes en ambos tipos de huevo son benéficos para la salud humana.











 nueva página del texto (beta)
nueva página del texto (beta)



