Introducción
Las tortugas o quelonios (Testudines), son un grupo de vertebrados acuáticos y terrestres, ampliamente distribuidos en el mundo, desde los arroyos, charcas, ríos, lagunas, mares, hasta los desiertos, bosques y selvas tropicales. A pesar de la diversidad de ecosistemas, donde se encuentran las tortugas; los estudios biológicos y ecológicos en el orden Testudines, es reducido, y al parecer solo el grupo de las tortugas marinas ha sido el que más se ha estudiado en disciplinas como ecología, reproducción, genética; incluyendo estudios celulares e intracelulares en sangre periférica (Flower et al. 2018, Ramakrishnan et al. 2018, Sinaei et al. 2019). Lo anterior, debido al desarrollo creciente de proyectos de ecología y conservación, en zonas costeras donde se distribuyen y se reproducen tales especies (García-Grajales et al. 2017, Macíp-Ríos et al. 2018). En la mayoría de las tortugas dulceacuícolas registradas, la información científica oportuna es reducida, básicamente la concerniente a la historia natural y biología básica (Macíp-Ríos et al. 2015). Solo un caso excepcional, es el de la tortuga orejas rojas o Trachemys scripta, especie en la que se han realizado diversos estudios de biología, entre los que destacan por su importancia los de hematología (Martínez-Silvestre y Cuenca 2011, Allender y Mitchell 2013, Carrascal-Velásquez et al. 2014, Hernández et al. 2017, Hadžimusić et al. 2020).
En el mundo hay registros de aproximadamente 352 especies de tortugas, siendo 345 de origen dulceacuícola y terrestre, y siete especies marinas (Rhodin et al. 2021); del total de registros, 61 taxas (tortugas de agua dulce y terrestres) están presentes en México, distribuidos en 48 especies, 13 géneros y siete familias (Macíp-Ríos et al. 2015, Rhodin et al. 2021). En la región tropical del sureste mexicano, compartida con Guatemala, Belice, El Salvador y Honduras, existen 22 especies integradas en ocho géneros, Kinosternon, Staurotypus, Claudius, Trachemys, Dermatemys, Rhinoclemmys, Chelydra y Terrapene (Flores-Villela y García-Vázquez 2014, Rhodin et al. 2021); lamentablemente cada una de ellas está en diferentes estatus de conservación de acuerdo con la norma oficial mexicana NOM-059-SEMARNAT-2010 y Lista Roja de Especies Amenazadas de la Unión Internacional para la Conservación de la Naturaleza (Rhodin et al. 2021, Barragán-Vázquez et al. 2022). En tales especies, muy pocos estudios formales han sido abordados y documentados; limitándose al conocimiento de la alimentación, distribución geográfica, fisiología, citogenética, manejo, parasitología y reproducción (Arias-Rodriguez et al. 2019). Sin embargo, se ha evidenciado que los programas de conservación, requieren de amplio conocimiento de la biología básica de las especies sujetas a manejo; en dicho contexto los estudios hematológicos son importantes de considerar, dado que se emplean básicamente para el diagnóstico de enfermedades (Zhang et al. 2011, Corrales-Ramírez y Caycedo-Lozano 2020), así también para el análisis de otros atributos fisiológicos y genéticos, como el estrés, daño celular, nivel de ploidía, entre otros aspectos celulares de importancia biológica (Hadžimusić et al. 2020, Machado et al. 2020, Radisic et al. 2020).
En dicho contexto, tales metodologías han sido desarrolladas a partir de estándares para humanos y otros mamíferos como los ratones, vacas, caballos, entre otros (Perpiñán y Sánchez 2009, Campbell 2015). Algunas de estas técnicas, han sido adaptadas para su aplicación en el estudio hematológico en pequeños vertebrados; a través de diversos campos como la acuicultura en amplia variedad de especies acuáticas y en zootecnia para herpetofauna, aves y mamíferos (Stacy et al. 2011, Zhang et al. 2011). Dada la importancia de los estudios hematológicos para la comprensión de la estructura y dinámica de las células sanguíneas, las adaptaciones de dichas metodologías no siempre repercuten con el procedimiento más apropiado, lo que resulta en detrimento del tiempo, de recursos económicos y de falsas interpretaciones. Actualmente, no hay metodologías hematológicas específicas para las tortugas dulceacuícolas, puesto que los métodos estándar actuales, son aparentemente apropiados para observar y evaluar la morfología celular; aunque la calidad de las tinciones basado en las observaciones de las imágenes, no son las óptimas, debido a los artefactos originados por las propiedades químicas, físicas y bioquímicas de las células en cada especie (Dessauer 1970, Snyder y Sheafor 1999, Arikan y Çiçek 2010, 2014).
Lo anterior, eventualmente ha dilucidado con la escasez de estudios hematológicos en las tortugas, principalmente en las especies dulceacuícolas de origen tropical. El mencionado hecho, ha conducido mediante el presente estudio al diseño comparativo de los métodos de mayor uso para estudios hematológicos en vertebrados, con el fin de establecer un procedimiento específico; y económicamente viable para especies dulceacuícolas, empleando como modelo biológico a tres especies de tortugas nativas del sureste mexicano, la jicotea Trachemys venusta venusta, el tres lomos Staurotypus triporcatus y la mojina Rhinoclemmys areolata.
Materiales y métodos
Origen de los especímenes y taxonomía
Los especímenes adultos fueron recolectados del entorno silvestre en acuerdo con el siguiente esquema: tortuga jicotea T. v. venusta (12 hembras y 10 machos), tres lomos S. triporcatus (ocho hembras y cuatro machos) y mojina R. areolata (9 hembras y 5 machos), fueron capturados por observación y tomados manualmente de las lagunas del Pueblo y Huapacal de la Villa Luis Gil Pérez del municipio del Centro, de los márgenes de los pantanos de la Villa Sánchez Magallanes, municipio de Cárdenas y de los humedales del poblado Federico Álvarez, municipio de Jonuta, respectivamente, todas las localidades del estado de Tabasco, México. La recolecta de los ejemplares en vida silvestre se llevó a cabo con el permiso federal de la SEMARNAT (SGPA/DGVS/04315). Los ejemplares recolectados, se mantienen vivos y en condiciones óptimas de mantenimiento, calidad de agua y alimentación en las Instalaciones del Laboratorio en Genética y Ecofisiología de la DACBiol-UJAT. La identificación taxonómica específica, se basó en la nomenclatura de Legler y Vogt (2013), Ernst y Barbour (1989), Smith y Smith (1979); atendiendo la última actualización en taxonomía, sinonimia, distribución y estatus de conservación de todas las especies de tortugas en el mundo de Rhodin et al. (2021). El desarrollo del presente protocolo de Investigación, fue evaluado y autorizado por la Comisión Institucional de Ética en Investigación (CIEI) de la Universidad Juárez Autónoma de Tabasco (Folio: 0985-30/Enero/2022).
Extracción de sangre y extendido celular
La sangre periférica se extrajo de la vena coccígea, desinfectando la región terminal de la cola con algodón humedecido de alcohol etílico al 70%. En dependencia del peso de cada espécimen; se empleó jeringas estériles de 0.5 mL para organismos con pesos entre 300-900 g, jeringas de 1 mL para especímenes con peso de 1 a 2 kg y de 3 mL para organismos con pesos mayores a los 2 y hasta los 6 kg, extrayendo máximo 300 µL (0.3 mL) de sangre por cada tortuga. Inmediatamente, se colocó una gota (20 µL aproximadamente) de sangre sobre cada portaobjetos (45 portaobjetos por cada espécimen) limpios y estériles; luego fue extendida por capilaridad suave y homogéneamente, evitando dañar las células, secando cada extendido celular o frotis al aire a temperatura ambiente (28.0 ± 0.5 °C) por 60 min.
Fijado post-frotis (Fase experimental I)
Las muestras control consistieron de cinco frotis sanguíneos sin tratamiento o fijado, las cuales fueron analizadas inmediatamente después del secado de los extendidos sanguíneos. Para experimentar el efecto del tiempo de fijado, se prepararon dos fijadores, el metanol absoluto al 99.8% y el fijador elaborado con etanol al 70% que fue desnaturalizado con benzoato de denatonio (0.7 mg 100 mL), ambos mantenidos a 4 °C. Posteriormente, los cinco frotis sanguíneos por tratamiento, fueron sumergidos de modo individual a los tiempos (o tratamientos) de exposición de: 0.5, 1.0, 5.0 y 10.0 min. Luego, fueron secados a 26 ± 1.0 °C sobre una bandeja de polipropileno, extrayendo cuidadosamente el exceso del fijador (metanol absoluto y etanol desnaturalizado).
Tinción post-frotis (Fase experimental II)
Las muestras control fueron analizadas inmediatamente después del secado del frotis. Posteriormente, las muestras que fueron fijadas, se dejaron a temperatura ambiente (28.0 °C) durante 12 h previo a la aplicación del colorante. Subsiguientemente, se aplicó la tinción con Giemsa al 10% y con Giemsa en solución madre. La Giemsa al 10% o tinción de Romanosky a 4.0 °C, se empleó con modificaciones del protocolo de Campbell (2015), utilizando como diluyente el buffer de fosfatos a pH 7.0 y las preparaciones citológicas fueron teñidas por 1.0, 5.0, 10.0 y 20.0 min, respectivamente. Por otro lado, para la tinción con Giemsa en solución madre a 4.0 °C (sin diluyente), las muestras citológicas respectivas se expusieron a 5.0, 10.0, 20.0 y 30.0 s de tinción con el colorante. Transcurridos los tiempos de tinción, a cada una de las muestras, se les retiró el exceso de colorante, colocando las preparaciones citológicas en posición vertical sobre un recipiente cilíndrico de polipropileno y luego se aplicó agua destilada para lavar los restos de colorante y permitir el escurrido y secado rápido.
Microscopía óptica y criterios de la calidad celular
Los campos hematológicos fueron analizados, utilizando las herramientas de contraste de fases en campo claro/oscuro y seleccionados al azar en el microscopio AxioScope A1 (Carl Zeizz®) con el objetivo 10X+1.25X del optovar (Carl Zeizz® Microscopy GmbH, 2011). Después, se fotodigitalizaron con el módulo de adquisición de imágenes de la cámara AxioCam ERc5s y con el objetivo 40X + 1.25X del optovar. Las imágenes procedentes de la fase experimental I, se analizaron detalladamente con las herramientas digitales para el procesamiento posterior y filtrado mediante canales fluorescentes falsos (LUTS) del programa ZEN/2011 (Carl Zeizz® Microscopy GmbH, 2011). Las imágenes procedentes de la fase experimental II, se analizaron detalladamente con las herramientas digitales para el procesamiento a posteriori y filtrado de canales en campo claro, basado en los patrones de tinción de Giemsa con el programa ZEN/2011 (Carl Zeizz® Microscopy GmbH, 2011).
Los eritrocitos se evaluaron y contabilizaron, tomando dos criterios esenciales en la integridad de la membrana celular: a) Daño en la membrana y citoplasma celular (Dmc): Son aquellas células eritrocitarias que manifiestan alteraciones morfológicas o pérdida de simetría como son contracción, fractura del citoplasma, fractura de la membrana y pérdida parcial o total de la integridad de la membrana celular. En estas dispersiones, las células y el perímetro, muestran presencia de residuos e impurezas de origen orgánico y biológico. B) Sin daño en la membrana y citoplasma celular (Smc): Son aquellas células eritrocitarias que no presentan alteraciones morfológicas del citoplasma, de la membrana y mantienen simetría celular integra. Además, la coloración del área nuclear, es homogénea con tinción en tonalidad purpura o azul intenso. Por otro lado, las dispersiones celulares y perímetro, deben observarse (externamente) libres de impurezas (química o biológica) como estructuras refractarias, residuos de la tinción, bacterias y hongos.
Análisis de datos y estadísticos
Los valores obtenidos, se registraron en bases de datos individuales y les fueron calculados el promedio y la desviación estándar (D.E.), con el empleo del programa Excel para Windows (Microsoft® 2022). Los porcentajes, fueron calculados basados en la siguiente fórmula:
Los porcentajes, fueron analizados en acuerdo al cumplimiento de las pruebas de homogeneidad y homocedasticidad, luego se aplicó el análisis de Kruskal-Wallis y la prueba de Dunn´s a P ≤ 0.05 (Zar 2010), en todos los casos se empleó el programa SigmaPlot® (12.3 de Systat Software Inc®).
Resultados
Fijado post-frotis o fase experimental I
El fijado de los frotis sanguíneos con metanol absoluto y etanol desnaturalizado, permitió el análisis total de 57 626 células eritrocitarias; de las cuales 26 852 correspondieron a los eritrocitos de la jicotea T. v. venusta, 15 835 células a la tortuga tres lomos S. triporcatus y 14 939 eritrocitos a la tortuga mojina R. areolata (Tabla 1). Con el empleo del metanol absoluto, se observó que, en las muestras de sangre de las tres especies empleadas como modelo, hubo incremento significativamente progresivo del número y de los porcentajes de células con daño en la membrana celular (Dmc) en relación con los tiempos de exposición (0, 0.5, 1, 5 y 10 min) (Tabla 1).
Tabla 1 Número de células con daño y sin daño en la membrana celular, que fueron expuestas a diferentes tiempos de exposición con metanol absoluto y etanol desnaturalizado.
| Medio fijador: Metanol absoluto | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| T. v. venusta | S. triporcatus | R. areolata | |||||||
| T.e. | Dmc | Smc | Total | Dmc | Smc | Total | Dmc | Smc | Total |
| Control | 0 | 2504a | 2504 | 0 | 1508a | 1508 | 0 | 1394a | 1394 |
| 0.5 min | 12 | 2343a | 2355 | 19 | 1644a | 1663 | 0 | 1563a | 1563 |
| 1 min | 181 | 2927b | 3108 | 284 | 1672b | 1956 | 134 | 1386a | 1520 |
| 5 min | 1248 | 1804c | 3052 | 1270 | 270c | 1540 | 1078 | 303b | 1381 |
| 10 min | 3108 | 329d | 3347 | 1254 | 78d | 1332 | 1470 | 174c | 1644 |
| Total de células: | 14366 | 7999 | 7502 | ||||||
| Medio fijador: Etanol desnaturalizado | |||||||||
| T. v. venusta | S. triporcatus | R. areolata | |||||||
| Control | 0 | 2504a | 2504 | 0 | 1509a | 1509 | 0 | 1477a | 1477 |
| 0.5 min | 0 | 2502a | 2502 | 0 | 1598a | 1598 | 0 | 1492a | 1492 |
| 1 min | 2 | 2408a | 2410 | 0 | 1575a | 1575 | 0 | 1481a | 1481 |
| 5 min | 3 | 2619a | 2622 | 3 | 1460a | 1463 | 7 | 1474a | 1481 |
| 10 min | 2 | 2446a | 2448 | 5 | 1686a | 1691 | 12 | 1494a | 1506 |
| Total de células: | 12486 | 7836 | 7437 | ||||||
T.e. = Tratamiento experimental, Dmc = Daño en la membrana celular, Smc = Sin daño en la membrana celular, min = minutos. Literales iguales en cada columna, representa que no hay diferencias significativas con P ≤ 0.05 y en caso contrario las diferencias existen.
En dicho sentido, en la tortuga T. v. venusta, se registró nula presencia de células con daño en las muestras del tratamiento control y 12 células con daño en la membrana celular, por efecto del metanol absoluto con el tiempo de exposición más bajo de 0.5 min, hasta los 3 108 eritrocitos atrofiados por exposición al metanol absoluto por exposición de 10 min. Los conteos más bajos, de células que no tuvieron daño en la morfología de la membrana celular (Smc), se observaron a los 10 min de exposición, con presencia de 329 eritrocitos y los registros más altos de Smc, fueron significativamente notables en los tiempos de exposición menores de 0, 0.5, 1 y 5 min (Tabla 1). En S. triporcatus, no se identificaron eritrocitos dañados en las muestras control (sin presencia de alcohol), pero se logró observar aumento en el número de células con daño (Dmc,) con el incremento en los tiempos de exposición al metanol (Tabla 1). Fue así, que se logró observar 19 eritrocitos con daños en la membrana celular eritrocitaria, por exposición al metanol absoluto de 0.5 min y hasta 1 254 eritrocitos dañados por el tiempo de exposición de 10 min (Tabla 1). En la tortuga tres lomos, las células que manifestaron estructura celular normal o sanas (sin daño en la membrana celular, Smc), presentaron registros bajos de 78 eritrocitos a los 10 min de exposición al metanol absoluto y conteos altos con el decremento de los tiempos de exposición (Tabla 1).
Por otro lado, también en el caso particular de R. areolata, hubo muestras que carecieron (valores de cero) de daños en la membrana celular, en las observaciones microscópicas de las preparaciones hematológicas del control y de todas aquellas de los primeros 0.5 minutos de exposición al metanol absoluto. A partir de 1 min de exposición al metanol absoluto, se inició el registro de 134 células con Dmc y hasta 1 470 eritrocitos afectados por 10 min de exposición al metanol. Las muestras que presentaron el número más bajo de eritrocitos sanos, fueron aquellas tratadas con 10 min de exposición, pues se observaron 174 células sin daños. Mientras que valores más altos de eritrocitos Smc, fueron también observados con el decremento significativo de los tiempos de exposición al metanol como fijador.
El metanol absoluto, como fijador de tejidos, causa mayor impacto en la estructura de los eritrocitos, debido a que registró una respuesta inmediata a los 0.5 min de exposición de las muestras hematopoyéticas de las tres especies de tortugas; en dicho sentido se lograron observar porcentajes bajos de 9.37 ± 7.79% (a 10 min) de células sin daños en la estructura de la membrana celular en T. v. venusta; en la tortuga tres lomos con 5.78 ± 3.91% (a 10 min) y en R. areolata con 10.52 ± 2.97% (a 10 min) (Tabla 1). Lo anterior indica, que al incrementar el tiempo de exposición de las muestras o dispersiones de las células sanguíneas (frotis sanguíneo) al metanol absoluto, mayor será el daño en la estructura, morfología y composición celular eritrocitaria; en acuerdo con las diferencias significativas (Dunn´s ≤ 0.001) encontradas entre los valores reportados para las muestras control y todos los tratamientos con el metanol absoluto (Figura 1).
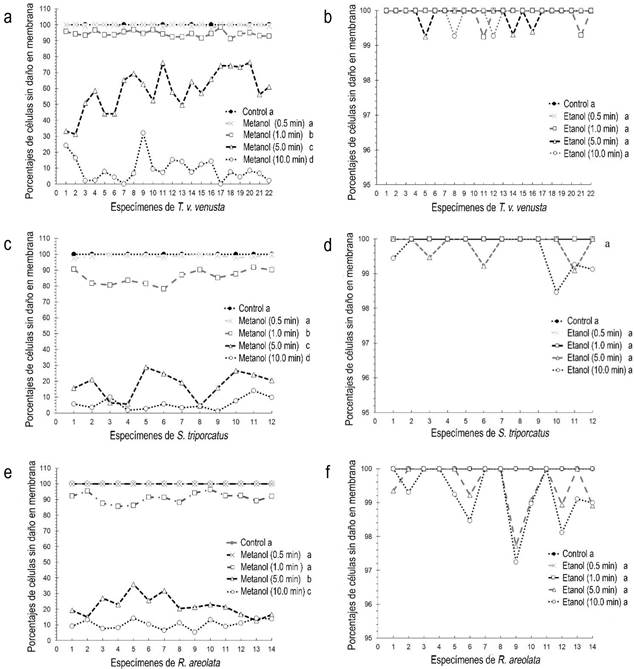
Figura 1 Comportamiento de la membrana celular (eritrocitos sin daños en porcentajes) expuestos a metanol y etanol en las tortugas T. v. venusta (a, b), S. triporcatus (c, d) y R. areolata (e, f). Literales iguales en cada gráfico, representa que no hay diferencias significativas con P ≤ 0.05 y en caso contrario las diferencias existen.
En la observación de las muestras fijadas con el etanol desnaturalizado, se registró baja frecuencia de daños en los eritrocitos, desde cero y hasta tres células en T. v. venusta, de 0 a 5 células en S. triporcatus y de 0 a 12 células en R. areolata; incluso en los tiempos de exposición más prolongadas (5 a 10 min). Asimismo, el número de células sanas o sin daño en la membrana celular, fueron elevados desde 2 619 eritrocitos, con exposición de 5 min en etanol desnaturalizado para los frotis sanguíneos expuestos de T. v. venusta. En S. triporcatus o tortuga tres lomos, se identificaron 1 686 eritrocitos sanos con el tiempo máximo de exposición de 10 min y en R. areolata o mojina, fueron identificados 1 494 eritrocitos sin daños en la membrana y estructura intracelular; después de la exposición de 10 min o tiempo máximo de exposición al etanol (Figura 1).
Altos porcentajes de células sin daño en la estructura de la membrana y del citoplasma celular, fueron observados en el tratamiento con etanol desnaturalizado, con registros desde 100% (a 0.5 min de exposición) y hasta 99.93 ± 0.22% (a 10 min de exposición) en la hicotea T. v. venusta; en la tortuga tres lomos S. triporcatus con 100% (a 0.5 min de exposición) y hasta 99.69 ± 0.51% (a 10 min de exposición). Mientras que en la tortuga mojina R. areolata se observó 100% (a 0.5 min de exposición) y hasta 99.25 ± 0.85% (a los 10 min de exposición). Lo anterior, fue también respaldado al observarse que no existen diferencias significativas (Dunn´s ≤ 0.001) entre las muestras control y los tratamientos con etanol en las tres especies estudiadas (Figura 1).
Fase experimental II o tinción de muestras con Giemsa Madre y Giemsa al 10%
La segunda fase experimental, se basó en el análisis total de 54 191 células eritrocitarias; en T. v. venusta fueron observados 24 239 eritrocitos, en S. triporcatus 15 161 eritrocitos y en R. areolata 14 791 eritrocitos (Figura 2). En la tortuga T. v. venusta, se identificó número elevado de eritrocitos con daño o atrofia en la membrana celular (2 045 células); a partir de la tinción por 1 min de exposición con Giemsa al 10%.
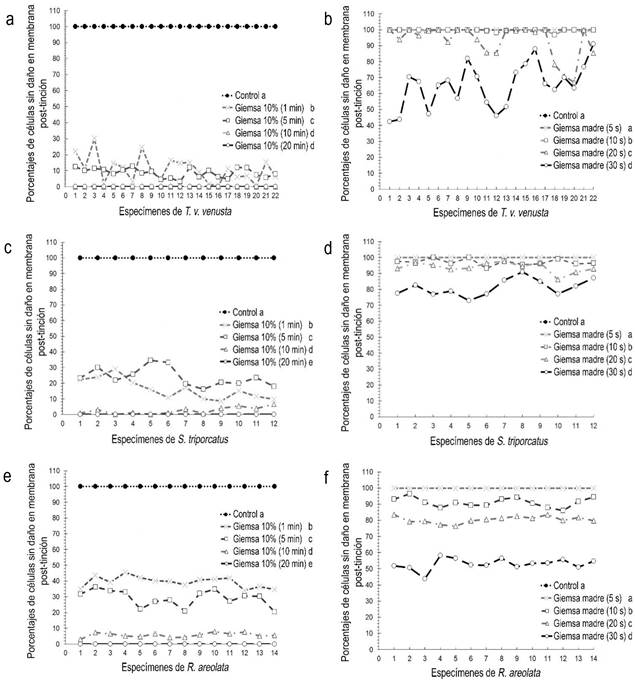
Figura 2 Comportamiento de la estructura celular eritrocitaria post-tinción (Giemsa 10% vs Giemsa madre) en T. v. venusta (a, b), S. triporcatus (c, d) y R. areolata (e, f). Literales iguales en cada gráfico, representa que no hay diferencias significativas con P ≤ 0.05 y en caso contrario las diferencias existen.
Cuando las preparaciones fueron sometidas a 20 min de tinción con Giemsa al 10%, se registraron 2 336 células dañadas. En la tortuga S. triporcatus, se identificaron 1 262 eritrocitos atrofiados a partir de la tinción con 1 min de tratamiento y hasta 1 362 eritrocitos atrofiados, cuando las muestras fueron teñidas por 10 min (Figura 3). En la tortuga R. areolata, con 1 min de exposición de Giemsa al 10%, se obtuvieron registros de 972 eritrocitos con daños en la membrana y hasta 1 451 eritrocitos atrofiados con 10 min de exposición al colorante. Por otro lado, el número de células sanas (sin daño en la membrana celular) no llegaron a registrarse (cero células) con exposición de 10 y de 20 min para muestras de T. v. venusta; y con 20 min de tinción de las muestras de las tortugas S. triporcatus y R. areolata (Tabla 2).
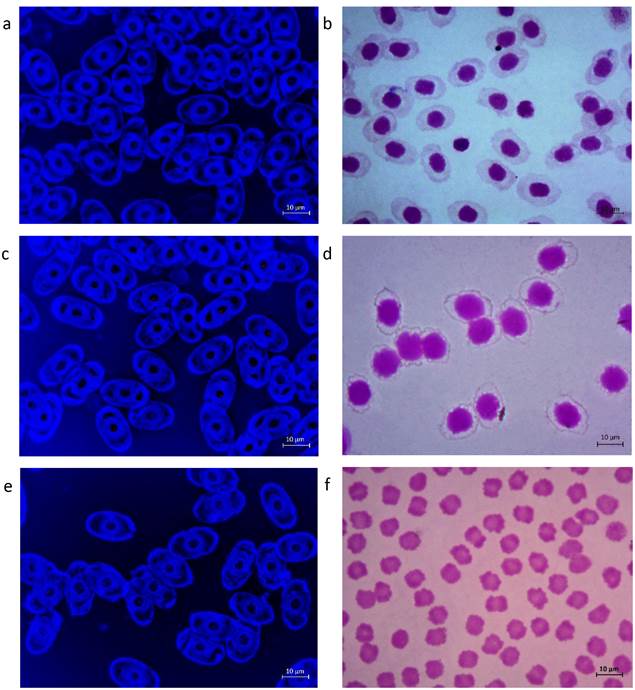
Figura 3 Células hematopoyéticas con pérdida severa de simetría en la estructura extracelular, intracelular y del citoplasma por efecto del metanol (a, c, e) y tinción con Giemsa al 10% (b, d, f) en las tortugas tropicales T. v. venusta (a, b), S. triporcatus (c, d) y R. areolata (e, f). La barra en cada microfotografía equivale a 10 μm.
Tabla 2 Resultados de la fase experimental II y respuesta de la estructura celular expuesta a dos métodos de tinción.
| Tinción: Giemsa 10% | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| T. v. venusta | S. triporcatus | R. areolata | |||||||
| T.e. | Dmc | Smc | Total | Dmc | Smc | Total | Dmc | Smc | Total |
| Control | 0 | 2504a | 2504 | 0 | 1450a | 1450 | 0 | 1441a | 1441 |
| 1 min | 2045 | 234b | 2279 | 1262 | 246b | 1508 | 972 | 641b | 1613 |
| 5 min | 2299 | 225c | 3108 | 1174 | 376c | 1550 | 914 | 385c | 1299 |
| 10 min | 2275 | 0d | 2275 | 1362 | 39d | 1401 | 1332 | 81d | 1413 |
| 20 min | 2336 | 0d | 2336 | 1339 | 0e | 1339 | 1451 | 0e | 1451 |
| Total de células: | 11918 | 7248 | 7217 | ||||||
| Tinción: Giemsa madre | |||||||||
| T. v. venusta | S. triporcatus | R. areolata | |||||||
| Control | 0 | 2504a | 2504 | 0 | 1402a | 1402 | 0 | 1373a | 1373 |
| 5 s | 0 | 2237a | 2237 | 0 | 1411a | 1411 | 0 | 1490a | 1490 |
| 10 s | 11 | 2577b | 2588 | 41 | 1396b | 1437 | 135 | 1419b | 1554 |
| 20 s | 184 | 2251c | 2435 | 101 | 1586c | 1687 | 317 | 1294c | 1611 |
| 30 s | 881 | 1676d | 2557 | 370 | 1606d | 1976 | 729 | 817d | 1546 |
| Total de células: | 12321 | 7913 | 7574 | ||||||
T.e. = Tratamiento experimental, Dmc = Daño en membrana celular, Smc = Sin daño en membrana celular, min = minutos, s = segundos. Literales iguales en cada columna, representa que no hay diferencias significativas con P ≤ 0.05 y en caso contrario las diferencias existen.
El análisis estadístico aplicado a los tratamientos de la tinción con Giemsa al 10%, reveló diferencias significativas (Dunn´s ≤ 0.001) respecto a las observaciones registradas con las muestras del tratamiento control, lo que indica baja eficacia de aplicación de dicha técnica en la tinción de las células sanguíneas (principalmente eritrocitos) de las tres especies de tortugas dulceacuícolas. En las muestras o frotis sanguíneos de las tres especies de tortugas dulceacuícolas T. v. venusta, S. triporcatus y R. areolata, que fueron teñidas con Giemsa en solución madre, se logró registrar ausencia de células sanguíneas atrofiadas durante los primeros segundos de exposición (5 s) al colorante (Figura 4). El mayor número de células atrofiadas, se presentó a los 30 s de tinción en las muestras de las tres especies de tortugas, registrándose 881 eritrocitos dañados en T. v. venusta, 370 eritrocitos en S. triporcatus y 729 eritrocitos en R. areolata.
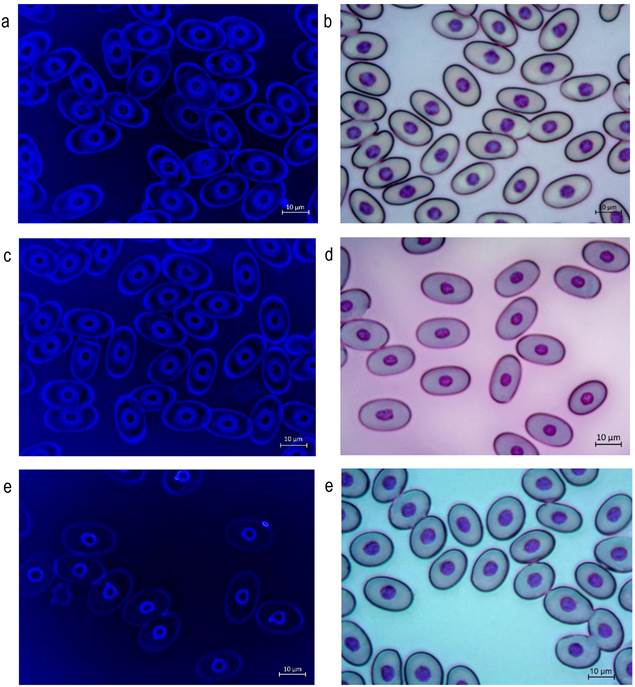
Figura 4 Células hematopoyéticas con la estructura celular integra y normal de muestras sanguíneas de tres especies de tortugas dulceacuícolas T. v. venusta (a, b), S. triporcatus (c, d) y R. areolata (e, f), que fueron tratadas con el mejor procedimiento de fijado (etanol desnaturalizado, 5 min) y tinción (Giemsa madre, 10 s). La barra en cada microfotografía equivale a 10 μm.
En el caso de las células normales (sin daño en la membrana y estructura celular), se registró el mayor número de eritrocitos con esta característica a los 10 s de exposición al colorante, con registro de 2 577 células normales en T. v. venusta. Dicha particularidad, también se observó en las muestras de S. triporcatus y R. areolata (Tabla 2). En términos de porcentajes, hubo registros de 100% de eritrocitos sin daños en la membrana y estructura celular a los 5 s en las tres especies de tortugas (T. v. venusta, S. triporcatus y R. areolata), lo cual fue comprobado al no existir diferencias significativas (Dunn´s ≤ 0.001) en los porcentajes registrados para dicho tratamiento (Figura 2). El análisis estadístico, aplicado a los tratamientos de la tinción con Giemsa madre, reveló que no existen diferencias significativas entre las muestras control y los tratamientos de 5 y 10 s de exposición después de la comparación múltiple de Dunn´s ≤ 0.001. Sin embargo, las muestras expuestas desde 20 hasta 30 s de tinción, manifestaron diferencias significativas respecto a los demás tratamientos comparados (Figura 2).
Discusión
En las tortugas marinas, dulceacuícolas y terrestres, los estudios hematológicos siguen siendo pocos en relación con los estudios enfocados a comprender aspectos de carácter ecológico, genético, fisiológico, de alimentación, distribución y comportamiento (Hernández-Guzmán y Arias-Rodriguez 2019, Price et al. 2019, Phillips et al. 2022). La carencia de estudios hematológicos en las tortugas, ha sido limitado por aspectos de tipo metodológico, debido a que son poco accesibles (se debe pagar por acceder a la publicación), no económicos (la serie de reactivos/equipos son variados y costosos) y especie específicos, lo que no ha permitido el desarrollo de investigaciones con resultados de buena calidad interpretativa y comparativa. En contraste, con la gran variedad de métodos desarrollados para su empleo en citología humana y en animales de importancia económica en el sector pecuario, como las vacas, caballos y gallinas (Stephens et al. 2019, Chen et al. 2022, Yang et al. 2022).
En dicho sentido, en esta investigación en tres especies de tortugas tropicales nativas de Centroamérica, se desarrolló un método que se aplica en dos fases (Fijado y tinción), siendo su aplicación fácil y económicamente accesible para su empleo en especies de tortugas tropicales. En la fase I, que involucró el fijado con metanol absoluto o etanol desnaturalizado post-frotis, permitió la observación microscópica y el análisis detallado de miles de células eritrocitarias (en total 57 626) de ejemplares adultos de la jicotea T. v. venusta, la tortuga tres lomos S. triporcatus y de la tortuga mojina R. areolata. Durante las observaciones de las preparaciones hematológicas, fue evidente la presencia de diversos daños en la integridad celular eritrocitaria en dependencia del tipo de fijador (metanol absoluto y/o etanol desnaturalizado) y los tiempos de exposición de las muestras de tejido (Tabla 1).
Con el empleo del metanol absoluto y del etanol como fijadores, se observó incremento significativamente (P ≤ 0.001) progresivo del número y de los porcentajes de células eritrocitarias con daños en la membrana (Dmc) y citoplasma celular; en las preparaciones citológicas de las especies empleadas como modelo experimental. Todo lo anterior, fue experimentado en relación con los tiempos de exposición desde 0.5, 1, 5 y hasta los 10 min de tratamiento (Tabla 1). Mientras que las células observadas en las muestras del tratamiento control (o cero minutos de exposición), no mostraron daño o alteración en la estructura de la membrana y citoplasma celular.
El análisis estadístico comparativo de los tratamientos, sobre el efecto de los fijadores empleados, mostró que el metanol versus etanol, resulta significativamente (Dunn´s ≤ 0.001) con mayores lesiones (del metanol) sobre la estructura e integridad de las células mitóticas eritrocitarias. En el caso específico de las muestras fijadas con etanol desnaturalizado, presentaron conteos muy bajos de eritrocitos dañados, con registros desde cero y hasta tres células en T. v. venusta, de cero hasta cinco células en S. triporcatus y desde cero a 12 células en R. areolata; incluso en los tiempos de exposición más prolongados desde 5 y hasta 10 min. Fue así, que el número de células sanas o sin daño en la membrana celular fueron elevados, desde 2 619 eritrocitos en la exposición de 5 min al etanol desnaturalizado en T. v. venusta, en S. triporcatus se identificaron 1 686 eritrocitos sanos con el tiempo máximo de exposición (de 10 min) y en R. areolata, fueron identificados 1 494 eritrocitos sin daño en la membrana celular con 10 min de exposición (Figura 1).
El metanol absoluto como fijador de células sanguíneas, causa mayor impacto en la estructura extracelular e intracelular de los eritrocitos, llegando a dar respuesta inmediata a partir de los 0.5 min de exposición de las muestras de células sanguíneas. Dicho resultado fue contrastado, con los porcentajes extremadamente bajos de células sin daño estructural, con observaciones a los 10 min de exposición con porcentajes de 9.37 ± 7.79% en T. v. venusta; en la tortuga tres lomos con 5.78 ± 3.91% y en R. areolata con 10.52 ± 2.97% (Tabla 1). Lo anterior, indica que al incrementar el tiempo de exposición de las muestras o células sanguíneas (frotis sanguíneo) en el metanol absoluto, mayor será el daño estructural y morfológico que recibirá la membrana de las células eritrocitarias, siendo corroborado por los resultados de los análisis estadísticos, al existir diferencias significativas (Dunn´s ≤ 0.001) entre los porcentajes registrados entre las muestras control y todas aquellas correspondientes a los diferentes tratamientos con el empleo del metanol absoluto (Figura 1). De acuerdo con los pocos estudios reportados respecto a las metodologías empleadas para la fijación y tratamiento de las dispersiones sanguíneas (o frotis sanguíneo) en las tortugas, la revisión bibliográfica indica que no existe un método idóneo, aunque hay la tendencia hacia el empleo del método rápido de tinción general que está basado en las tinciones tipo Romanowsky (Work et al. 1998) con diferentes grados de calidad celular en términos de morfología, presencia de residuos y diferenciación de los diferentes grupos celulares del tejido hematopoyético. Autores como López-Olvera et al. (2003), Barrows et al. (2004), Montilla et al. (2006) y Casal y Orós (2009), señalan que las tinciones tipo Romanowsky, son típicamente patentes de tipo comercial, las cuales otorgan “buena calidad” en las dispersiones celulares sanguíneas para la identificación y descripción apropiada de las células en tortugas, dicho procedimiento se basa primero en el fijado por 5 segundos de las dispersiones celulares en una solución metílica de triarilmetano y la posterior tinción. Pero algunos resultados ponen en duda la calidad de las células cuando son observadas bajo el microscopio, como los estudios realizados en Chelonia mydas (Work et al. 1998, Montilla et al. 2006). Lo anterior, hace pensar en la estandarización sistemática del método de fijación como es el caso de lo que se reporta en la presente investigación. Al respecto, se sabe que pequeños cambios en la composición del ambiente de las membranas celulares, pueden modificar su composición, principalmente de todos aquellos componentes que están integrados por proteínas, lípidos y canales de comunicación iónica e hídrica (Patra et al. 2006). Tales efectos, ocasiona deformación de la membrana celular, como se ha demostrado en células eritrocitarias humanas expuestas a bajas concentraciones alcohólicas, que van de 0.5 a 5.0% de metanol, de 0.5 a 7.0% de etanol, de 0.5 a 7.0% de propanol y de 0.5 a 2.0% de butanol (Sonmez et al. 2013). En el caso particular del presente estudio, se observó daño severo o deformación de la membrana celular eritrocitaria de las tres especies de tortugas tropicales por exposición al metanol absoluto (99.8%), desde 0.5, 1, 5 y hasta los 10 min de tratamiento, como lo reporta Sonmez et al. (2013). Los estudios in vitro, reportan que los alcoholes como el metanol, impactan de forma negativa la bicapa lipídica de la membrana celular (Patra et al. 2006, Collin et al. 2014), con ello destruyen proporcionalmente a la concentración y el tiempo de exposición, la estructura/estabilidad típica del citoesqueleto celular, generando morfología irregular de la célula, como fue observado en la jicotea T. v. venusta, la tortuga tres lomos S. triporcatus y la tortuga mojina R. areolata cuando se empleó el metanol como fijador de las células sanguíneas. En dicho sentido, en estudios in vitro, en los que se ha simulado en membranas artificiales la dinámica molecular de alcoholes, como el etanol y metanol; las observaciones indican que el etanol tiene mayor efecto sobre las propiedades estructurales de las membranas celulares de humanos, incluso en tiempos de exposición extremadamente rápidos (nanosegundos) (Patra et al. 2006, Collin et al. 2014). Sin embargo, en este estudio, cuando fueron fijadas con el etanol desnaturalizado las células sanguíneas de la jicotea T. v. venusta, la tortuga tres lomos S. triporcatus y la tortuga mojina R. areolata, se tuvieron los mejores resultados en términos de ausencia de pérdida de simetría celular y estabilidad morfológica (sin daño en la estructura celular), requisitos necesarios para estudios de citología, sobre todo de aquellos donde el diagnóstico es obligatorio para generar reportes de estudios hematológicos comparativos y de sanidad acuícola. También, se difiere con lo reportado por Sonmez et al. (2013), pues ellos señalan que la membrana celular tiene efectos perjudiciales derivados de la exposición al etanol, en contraste, no se observaron efectos en la membrana celular por exposiciones al metanol. En dicho sentido Mesquita et al. (1999), afirman que el etanol en diferentes concentraciones, ocasiona empaquetamiento de lípidos/proteínas y con ello cambios estructurales en la membrana y citoesqueleto de los eritrocitos, lo que origina cambios drásticos en la morfología y citometría celular como fue observado en el presente estudio cuando se utilizó etanol al 70%. Se reporta que en células sanguíneas humanas individuales sometidas desde 0.1-0.3% de etanol, la anatomía o esfericidad de las células eritrocitarias incrementa y mejora sustancialmente en acuerdo con los resultados de los tomogramas (índices refractivos tridimensionales) y en comparación con las células control y todas aquellas muestras que fueron sometidas al 0.5% de tratamiento (Lee et al. 2015).
Las observaciones registradas en las células eritrocitarias de T. v. venusta, S. triporcatus y R. areolata, muestran que presentaron comportamiento bifásico progresivo en la dinámica estructural de las membranas (Figura 1 y 2), aumentando el volumen o daño celular y después reduciéndolo conforme aumentaba el tiempo de exposición al etanol desnaturalizado o al metanol absoluto, comportamiento que ha sido reportado en estudios mediante curvas de elongación y de capacidad de turgencia en eritrocitos humanos (Sonmez et al. 2013, Lee et al. 2015).
En el caso particular de los procedimientos de tinción empleados y comparados en el presente estudio con Giemsa diluida al 10%, al requerirse más tiempo de exposición al colorante, la aplicación del procedimiento tiene mayor impacto en la integridad de las membranas celulares, llegando a registrar hasta 100% de células con alguna alteración morfológica a los 20 min de exposición en las tres especies de tortugas, y en el caso particular de las células de T. v. venusta, tales efectos se presentaron a partir de los 10 min de exposición (Tabla 2). En contraste, fue evidente el resultado cuando se empleó la solución madre de Giemsa, con tiempos de exposición cortos que mejoraron la calidad de las preparaciones hematológicas, en las muestras de las tres especies de tortugas; pues la estructura celular observada en los eritrocitos presentó integridad celular y homogeneidad de la tinción (coloración electrodensa). No cabe duda, que la relación entre los beneficios proporcionados por la capacidad de fijación del etanol (al 70%) desnaturalizado y la calidad de la tinción rápida proporcionada por la solución madre de Giemsa, fue crucial para que las preparaciones hematológicas de las tres especies de tortugas tropicales muestren buenos atributos para que se recomiende su empleo en estudios de biología celular.
Actualmente, los estudios hematológicos realizado en las especies nativas de tortugas, son complejos de comparar, principalmente por la carencia de técnicas hematológicas en especies específicas. Un ejemplo de ello, es que los resultados de estudios hematológicos en varias especies de organismos acuáticos, muestran fotografías de eritrocitos con anormalidades morfológicas y evidente pérdida de simetría celular, presumiblemente por un inadecuado método de fijación y tinción; dichas evidencias han sido publicadas en diferentes especies de organismos acuáticos como los peces Clarias batrachus, Heteropneustes fossilis, Anabas testudineus, Channa punctatus, C. striatus, Oreochromis niloticus, Labeo rohita, Catla catla, Cirrhinus mrigala, C. reba y Notopterus notopterus (Osman et al. 2018, Acharya y Mohanty 2019). Mientras que, en otros estudios, se observa que los eritrocitos han sido teñidos incorrectamente, ya que es evidente la poca diferenciación de la tinción entre el núcleo y la membrana celular; así como alteraciones en la morfología de la membrana celular, principalmente en estudios citológicos realizados en la tortuga Lepidochelys olivacea (Ramakrishnan et al. 2018). Tales particularidades morfológicas y de tinción celular inapropiadas, pueden conducir a interpretaciones incorrectas y resultados artificiales cuando se trate de un diagnóstico, sobre todo de tipo clínico. Por ello, es recomendable desarrollar o adaptar protocolos hematológicos apropiados o especie específicos, como ha sido demostrado con el presente estudio mediante la eficacia de los resultados obtenidos.
Conclusiones
Se determinó que el etanol desnaturalizado, es el mejor medio fijador, ya que causa menor impacto en la membrana celular de los eritrocitos con tiempos de exposición de 0.5 a 10 minutos en T. v. venusta, S. triporcatus y R. areolata. En la segunda fase experimental, se demostró que el método de tinción más eficiente, rápido y económico, es empleando como colorante la Giemsa en solución madre a 5 segundos de exposición. Con el empleo del protocolo hematológico desarrollado en el presente estudio, se abre una ventana de oportunidades para ampliar las fronteras de estudios hematológicos en todas las especies de tortugas dulceacuícolas tropicales, desde el punto de vista biológico, evolutivo, clínico, de ciencia básica y aplicada.











 nueva página del texto (beta)
nueva página del texto (beta)



