La semilla ocupa una posición crítica en la historia de vida de las plantas, ya que es el medio por el cual se genera un nuevo individuo, y el éxito de su establecimiento está determinado por las características fisiológicas y bioquímicas de la semilla (Bewley et al. 2013). Cuando las semillas alcanzan su madurez y son liberadas, algunas quedan en estado quiescente y otras entran en estado de latencia, estas últimas mantienen su viabilidad hasta que existen condiciones favorables para germinar; sin embargo, cuando la latencia se prolonga en exceso, la capacidad de germinación eventualmente puede verse afectada de manera negativa (Bewley et al. 2013, Graeber et al. 2014, Lopez del Egido et al. 2019).
En coníferas, la latencia física es común y es generada por la cubierta de la semilla que actúa como barrera protectora del embrión, pero también limita el acceso del agua, de modo que la imbibición y el inicio de los procesos fisiológicos de la germinación no se activan (Barnett 1998, Bewley et al. 2013, Iralu et al. 2019). En Pinus pinceana Gordon, la cubierta de la semilla prolonga considerablemente la latencia, de tal manera que para mejorar la germinación es necesario removerla (Ramírez-Herrera et al. 2008). En algunas especies, la remoción mecánica de la testa es necesaria para no extender la latencia y evitar que los procesos celulares sufran daños que afectan negativamente la viabilidad y capacidad de germinación (Demir et al. 2022).
Dependiendo del tipo de latencia, se pueden utilizar diferentes tratamientos pre-germinativos, los cuales pueden incrementar el porcentaje de semillas germinadas, disminuir el tiempo de germinación y mejorar la uniformidad de ésta, lo que ayuda a reducir tiempo y costos de producción e incrementar la probabilidad de éxito de las plantas producidas (Maciel et al. 2022). Entre los métodos más utilizados para estos fines se encuentra la escarificación y la aplicación exógena de promotores de germinación.
La finalidad de la escarificación es romper la latencia física, aumentar la permeabilidad de la testa y mejorar la uniformidad de la germinación. Los métodos de escarificación son de tipo mecánico, térmico y químico (Ardiarini et al. 2021). Las semillas escarificadas por el método de lijado de testa se embeben más rápidamente porque la cubierta se vuelve permeable al permitir con facilidad el paso del agua (Rostami & Shasavar 2009, Han et al. 2022), especialmente cuando la semilla permanece más tiempo en el agua.
Otro método para estimular la germinación es la aplicación de especies reactivas de oxígeno (ROS, por sus siglas en inglés), que influyen en los procesos bioquímicos de la semilla y embrión (Wojtyla et al. 2016). En Pinus roxburghii Sarg. la imbibición de las semillas en peróxido de hidrógeno (H 2 O 2 ) al 1 % v/v durante 24 horas en tres temperaturas diferentes, incrementó la capacidad de germinación respecto a los testigos (Ghildiyal et al. 2007). Varios autores señalan que el H 2 O 2 actúa directamente como un mensajero dentro de la red fito-hormonal, regulando el catabolismo del ácido abscísico (ABA) y promoviendo la biosíntesis de giberelinas (GA) durante la imbibición de la semilla (Liu et al. 2010, Arc et al. 2013). Además, se considera una molécula de señalización involucrada en la germinación de semillas ortodoxas (Wojtyla et al. 2016). En este sentido, la aplicación exógena de H 2 O 2 en bajas concentraciones (1-3 %) ha demostrado tener efecto positivo en la germinación de semillas de diversas especies (Ghildiyal et al. 2007, Ghildiyal et al. 2009, Gniazdowska et al. 2010, Ishibashi et al. 2013, Chaudhuri et al. 2013, Zhang et al. 2014, El-Maarouf-Bouteau & Bailly 2016).
En el estudio de la regeneración de especies forestales, especialmente en aquellas en peligro de extinción, es fundamental comprender los factores que influyen en la germinación y el establecimiento exitoso de plántulas. Tradicionalmente, la germinación se evalúa bajo condiciones controladas de laboratorio, lo cual permite estimar el potencial fisiológico de las semillas en un ambiente libre de estrés (Bewley et al. 2013). Sin embargo, estas condiciones no representan completamente los escenarios reales en los que ocurre el establecimiento natural, por lo que es importante considerar la dinámica de emergencia en ambientes más cercanos al natural, como el invernadero.
Un aspecto relevante es conocer si la condición experimental (laboratorio o invernadero) influye en la respuesta de las semillas a diferentes tratamientos pre-germinativos y con ello fortalecer el diseño de protocolos de propagación de planta para fines de restauración o de conservación (El-Kassaby et al. 2008, Iralu et al. 2019, Kavanova et al. 2023).
Pinus coulteri D.Don es una especie que se distribuye de manera natural desde las montañas costeras del centro y sur de California en Estados Unidos hasta el norte de Baja California en México (Minnich 1987, Minnich et al. 2015, Farjon 2010, Chardon et al. 2015). De manera general, crece en rodales aislados en elevaciones variadas y tolera suelos pobres (Krugman & Jenkinson 1974). En Baja California está representada por seis poblaciones y de acuerdo con los criterios de la NOM-059 (SEMARNAT 2010) está considerada en peligro de extinción. Su semilla es grande, de tamaño similar a la semilla de Pinus lambertiana Douglas y Pinus sabiniana Douglas ex D. Don.; mide entre 10 a 18 mm de largo y entre 7 a 10 mm de ancho (Farjon 2010) y con la cubierta gruesa y dura, a la que se ha considerado como una característica adaptativa de las especies de pino en ecosistemas con frecuencia regular de fuego (He et al. 2016). La dispersión de semilla se da principalmente por roedores como Dipodomys agilis Gambel, Chaetodipus californicus Merriam y Peromyscus maniculatus Wagner, que mueven la semilla lejos del árbol madre y se estima que son responsables de una parte importante del establecimiento de plántulas (Borchert et al. 2003). Esta barrera física de la cubierta puede prolongar o retardar considerablemente la germinación (Bewley et al. 2013). Poco se sabe sobre la latencia física que podría imponer la testa en las semillas de P. coulteri y la implicación en su capacidad de germinación (Krugman & Jenkinson 1974). En este trabajo las semillas de esta especie fueron sometidas a varios tratamientos pre-germinativos con el objetivo de evaluar el efecto individual y combinado de la escarificación mecánica, la aplicación de H 2 O 2 y la inmersión prolongada en agua sobre la capacidad y dinámica de la germinación. Con el incremento de la permeabilidad de la testa causada por la escarificación, la hidratación y la señalización promotora del H 2 O 2 en los procesos de germinación, se espera que al menos uno de estos tratamientos mejore la capacidad y velocidad de germinación en semillas de esta especie, en condiciones de laboratorio e invernadero, esta comparación permitirá conocer la dinámica de germinación y de emergencia para obtener una visión integral del comportamiento de las semillas y de las condiciones que favorecen su establecimiento, proporcionando información para el manejo y conservación de la especie.
Materiales y métodos
Material biológico. Se utilizó semilla recolectada de árboles localizados en la población de Santa Catarina, municipio de Ensenada, Baja California, entre las coordenadas 31° 41’ 59.25” de latitud Norte y 115° 45’ 48.01” longitud Oeste, con elevación de 1,070 m snm. De acuerdo con la clasificación bioclimática de Macías-Rodríguez et al. (2014), esta población se encuentra en el bioclima Mediterráneo Xérico oceánico (MEXO) en el piso Termomediterráneo con formaciones vegetales de tipo chaparral y Mesomediterráneo donde se presenta la formación Pinar del Mediterráneo (PIME). La precipitación media anual de esta población para la década 2011-2020 se estimó en 176 mm y la temperatura media anual de 16.3 °C (ClimateNA v. 7.50; Wang et al. 2016).
Desde la recolección de la semilla hasta la realización del experimento pasaron al menos 12 años, durante este tiempo, la semilla estuvo almacenada en bolsas plásticas y en refrigeración a 4 °C en las instalaciones del Departamento Forestal de la Universidad Autónoma Agraria Antonio Narro (UAAAN), en Saltillo, Coahuila, y posteriormente fueron trasladadas, al Colegio de Postgraduados Campus Montecillo, en las bolsas plásticas colocadas dentro de una caja de cartón, en un tiempo de 24 h. Los experimentos se establecieron en las instalaciones del laboratorio de biotecnología del Posgrado en Ciencias Forestales del Colegio de Postgraduados, Campus Montecillo, Estado de México.
Previo a la aplicación de tratamientos, se realizó la limpieza y selección de semillas llenas por el método de inmersión, para separar las semillas llenas (precipitadas) de las semillas vacías (flotantes), después de mantener las semillas en un vaso de precipitado con agua destilada estéril durante 18 horas. El porcentaje de semillas llenas se obtuvo con la siguiente fórmula:
Tratamientos y diseño experimental. Los tratamientos pre-germinativos se aplicaron a las semillas llenas 24 h después de su separación.
Se utilizó el diseño experimental completamente al azar con arreglo factorial; incluyó tres factores que generaron 12 tratamientos: 1) hidratación de las semillas, en dos periodos de tiempo, 24 y 48 h, se llevó a cabo con la inmersión de semillas en bolsas de gasa dentro de vasos de precipitado de 1 L con la solución correspondiente al tratamiento; 2) inmersión de semillas en solución de H 2 O 2 al 0, 2 y 3 %, la dilución de H 2 O 2 se hizo a partir de H 2 O 2 grado reactivo (30 %); y 3) escarificación, semilla lijada y semilla sin lijar, el lijado se hizo a baja presión (hasta visualizar la división de apertura de la testa) en dirección al micrópilo, con lija de grano medio para madera marca Fandeli® (Tabla 1).
Tabla 1 Formulación de tratamientos pre-germinativos para semillas de Pinus coulteri D.Don establecidos en laboratorio e invernadero.
| Factores | Tratamiento | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | |
| Hidratación (horas) | 24 | 24 | 24 | 24 | 24 | 24 | 48 | 48 | 48 | 48 | 48 | 48 |
| Concentración de H2 O2 | 0 | 0 | 2 | 2 | 3 | 3 | 0 | 0 | 2 | 2 | 3 | 3 |
| Escarificación | sí | no | sí | no | sí | no | sí | no | sí | no | sí | no |
El experimento se estableció en dos condiciones: 1) en laboratorio, bajo condiciones controladas en una cámara de germinación, donde se registró la germinación perse definida como la protrusión visible de la radícula, y 2) en invernadero, se realizó la siembra directa de la semilla en sustrato a una profundidad de 0.5 cm, donde se consideró como germinación exitosa la emergencia completa de la plántula sobre la superficie del sustrato. Si bien las definiciones de germinación y emergencia difieren operacionalmente, el enfoque estadístico uniforme permite comparar tendencias en porcentaje, velocidad y uniformidad entre las condiciones, entendiendo la emergencia como una extensión fenológica posterior a la germinación.
Para cada tratamiento se usaron 18 semillas, que se separaron en tres repeticiones de seis semillas cada una. En total se utilizaron 432 semillas ya que el experimento se estableció en dos condiciones diferentes: laboratorio e invernadero. Para el lijado, las semillas se separaron en dos grupos: 1) 216 semillas lijadas y 2) semillas sin lijar. Enseguida, se aplicaron los tratamientos de hidratación y H 2 O 2 y cada uno de los grupos se dividió en seis subgrupos de 36 semillas, los cuales se envolvieron en bolsitas de gasa. Por un lado, tres de estos grupos se llevaron a hidratación durante 24 h en: 1) agua destilada estéril, 2) H 2 O 2 a 2 %, y 3) H 2 0 2 a 3 %; mientras que los otros tres grupos se sometieron a hidratación durante 48 h con los mismos tres tratamientos de H 2 O 2 . El 50 % de las semillas sometidas a los tratamientos se establecieron en la condición de laboratorio y el otro 50 % en la condición de invernadero.
Establecimiento en laboratorio. En una campana de flujo laminar, las semillas sometidas a los 12 tratamientos se colocaron en cajas tipo Magenta®, seis semillas por caja (unidad experimental) y tres repeticiones por cada uno de los 12 tratamientos; por lo que en total se utilizaron 36 cajas. Previamente, al interior de cada caja se colocaron toallas de papel absorbente Servitoalla® para mantener la humedad, y se etiquetaron con el código del tratamiento y número de repetición. Una vez que las semillas tratadas se establecieron en la Magenta correspondiente, se colocaron aleatoriamente en una cámara de germinación, en la que se controlaron las horas luz (12 horas) y temperatura (16 y 24 °C). Para mantener húmedas las toallas, cada dos días se aplicó agua destilada estéril y cada 10 días se aplicó una solución de Captán® en una concentración de 1 gL-1 de agua, como preventivo de ataques fúngicos. En esta condición se consideró como germinación exitosa cuando la radícula alcanzó al menos el tamaño del largo de la semilla.
Establecimiento en invernadero. Las semillas destinadas para sembrar en invernadero se colocaron en el almácigo (140 × 60 cm), con la mezcla de sustrato a base de peat moss®, perlita y vermiculita en proporción 3:1:1. En el almácigo se delimitaron 36 cuadrantes (11 × 16 cm), simulando el espacio de una caja magenta. De igual manera se distribuyeron los tratamientos al orden de la cámara de germinación. Para llevar un control adecuado se colocaron etiquetas en cada cuadrante, correspondientes al dato de tratamiento y repetición. El riego fue ligero y se realizó cada tercer día y se hicieron aplicaciones de Captan® a 1 gL-1 de agua cada 10 días como preventivo de enfermedades fúngicas. La temperatura varió de 18 hasta 41 °C, con humedad relativa (HR) superior a 80 % que se midieron con un termohigrómetro Extech®. En esta condición se consideró como germinación exitosa al momento en que la plántula emergió del sustrato.
Obtención de datos y análisis estadísticos. La evaluación de la germinación se llevó a cabo durante 48 días, r egistrando las semillas germinadas (laboratorio) o plántulas emergidas (invernadero), cada dos días.
La capacidad germinativa se analizó a través de un análisis de varianza, para lo cual los datos originales de semillas germinadas se ajustaron a un modelo lineal generalizado (GLM), asumiendo una distribución binomial, con la función de enlace logit en Rstudio, con la finalidad de detectar si existe significancia estadística en el efecto de la condición, tratamiento y la interacción condición x tratamiento:
donde Y ijk es la capacidad germinativa, μ es la media general, C i es el efecto de la condición 1, …, i - ésima, τ j es el efecto del tratamiento 1, 2, 3… j - ésimo, C i τ j , es la interacción entre la condición y el tratamiento.
Con base en los resultados obtenidos del análisis de varianza, se hizo un segundo anova, para cada condición por separado, para identificar el factor o factores que tuvieron efecto significativo en la capacidad germinativa, ajustando los datos al siguiente modelo:
Donde Y ijkl es la capacidad germinativa, μ es la media general, H i es el nivel i - ésimo del tiempo de hidratación, P j es nivel j - ésimo de concentración de peróxido, E k es el nivel k - ésimo de lijado, H i P j es la interacción entre los niveles del factor hidratación y los niveles del factor concentración de peróxido de hidrógeno, H i E k es la interacción entre los diferentes niveles del factor hidratación y los niveles de escarificación, P j E k es la interacción entre los diferentes niveles de peróxido de hidrógeno y los niveles del factor escarificación, y ϵ ijkl es el error experimental para cada condición del ensayo.
Para el análisis de la dinámica de la germinación los datos obtenidos de la condición de laboratorio y la condición de invernadero se ajustaron mediante la Función de Hill de cuatro parámetros (FH4P) con el paquete germinationmetrics (Aravind et al. 2023) del software Rstudio. Esta función permite la caracterización del proceso en diferentes momentos durante la prueba y es adecuada para describir procesos biológicos como la germinación (El-Kassaby et al. 2008). Germinationmetrics permite ajustar la curva acumulativa a la función de Hill y estimar así los parámetros asociados a dicha función: Y=y0+axbcb+xb. Donde Y es el porcentaje de germinación acumulada en el tiempo x (cada dos días en el presente estudio), y 0 es el intercepto en el eje y (≤ 0), a es la asíntota o porcentaje máximo de germinación acumulada, que es equivalente a la capacidad de germinación, b es un parámetro matemático que controla la forma y la pendiente de la curva de germinación, cuanto mayor sea el valor de b, más pronunciado será el aumento hacia la asíntota a o G max y menor será el tiempo entre el inicio de la germinación y la germinación máxima, y c es la “mitad del nivel de activación máximo” medido en días y representa el tiempo requerido para que germine el 50 % de las semillas viables o T 50 (El-Kassaby et al. 2008).
La FH4P se ajustó para cada unidad experimental con base en los valores acumulados de germinación. Se realizó un ANOVA con los parámetros estimados para las tres repeticiones de cada tratamiento, incluyendo a) el tiempo en germinar 5 % de las semillas viables (Lag 5%), b) el tiempo en germinar 50 % de las semillas viables (T 50), y c) el valor de la uniformidad de germinación (U 7525) , que es el intervalo de tiempo de germinación entre 25 y 75 % de las semillas (El-Kassaby et al. 2008). Cuanto más bajo es el valor de Lag 5%, U 7525, y T 50 , más vigoroso es el lote de semillas.
Para probar la hipótesis de que los tratamientos pre-germinativos aplicados mejoran la dinámica de germinación de P. coulteri, los valores acumulados obtenidos para cada repetición de los tres parámetros derivados de las curvas de germinación (Lag 5%, T 50 y U 7525) se ajustaron al modelo 1 para conocer el efecto de la condición, el tratamiento y la interacción de estos en los parámetros de la dinámica de germinación. Por otro lado, con el modelo 2 de anova se evaluó el efecto de cada factor y de sus interacciones para cada condición por separado. Para la comparación de medias de cada parámetro se realizó una prueba de Tukey con un α = 0.05.
Resultados
El 100 % de las semillas estuvieron llenas, de las cuales 44 % no germinaron o tuvieron germinación anormal (falta de desarrollo radicular, emergencia de cotiledones antes que de raíz) que impidió el desarrollo de las plántulas (ISTA, 2018). Sin embargo, la semilla mantiene el porcentaje de germinación por arriba del 50 %, lo cual es aceptable para semillas de pino de acuerdo con los resultados registrados por Housková et al. 2021.
Efecto de la condición del ensayo en la capacidad y dinámica de germinación. La condición en que se realizó la germinación no tuvo un efecto significativo en la capacidad germinativa de las semillas (Tabla 2), con valores promedio de 69 % en laboratorio y 64 % en invernadero (Figura 1A), por lo que para fines prácticos de producción de planta es indistinto usar cualquiera de las dos condiciones.
Tabla 2 Valores de p de los factores condición, tratamiento e interacción condición × tratamiento en el modelo 1, para la capacidad germinativa (G max ), retraso (Lag 5%), T 50 y U 7525 en semillas de Pinus coulteri D.Don.
| Efecto | Pr > F | |||
|---|---|---|---|---|
| Gmax | Lag5% | T50 | U7525 | |
| Condición (Laboratorio-Invernadero) | 0.3437 | 5.534e-07 | 3.5e-07 | 0.00365 |
| Tratamiento (1-12) | 0.0272 | 0.15158 | 0.17401 | 0.2672 |
| Interacción (Condición x tratamiento) | 0.0008 | 0.01413 | 0.00175 | 0.1851 |
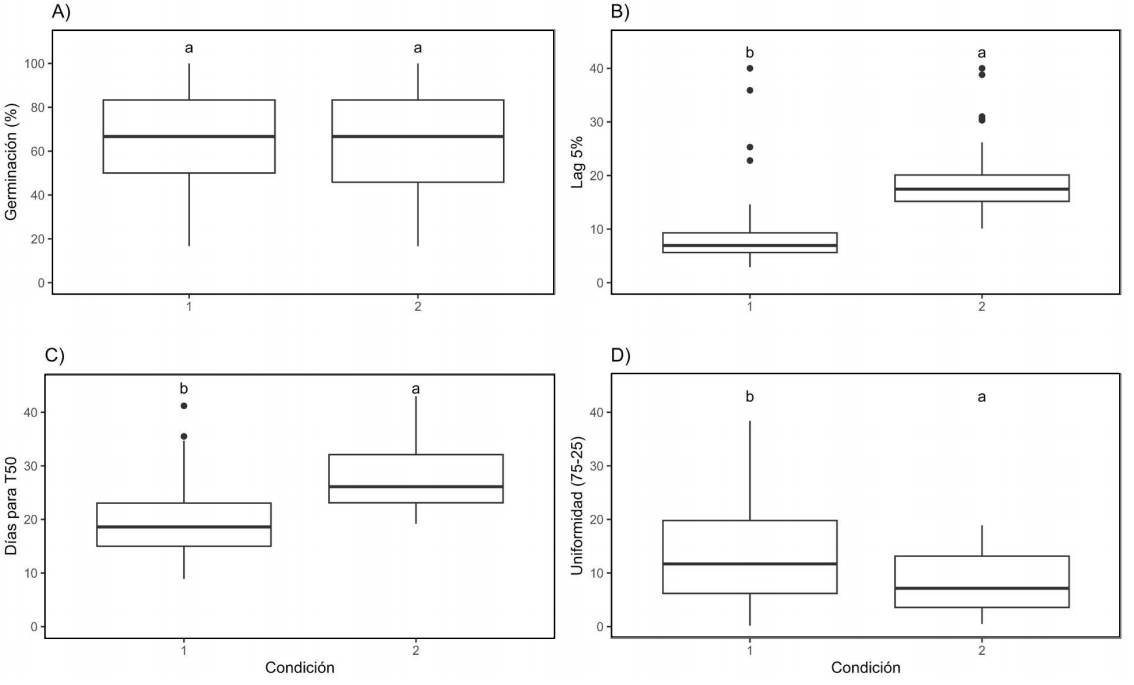
Figura 1 Diferencia de medias para: A) capacidad de germinación en laboratorio (1) e invernadero (2), B) días para germinar el 5 % de las semillas (Lag 5%), C) tiempo para llegar al 50 % de germinación de semillas viables en ambas condiciones (T 50), y D) el tiempo en germinar entre en 25 y el 75 % de semillas viables (U 7525) de Pinus coulteri en condiciones de laboratorio (1) e invernadero (2).
A diferencia de los resultados obtenidos en la capacidad germinativa, la condición de germinación, si afectó de manera significativa los tres parámetros estimados de la dinámica de la germinación (Lag 5%, T 50 y U 7525) (Tabla 2). En laboratorio, la germinación al 5 y 50 % de las semillas viables fue 10 y 8 días, respectivamente, más rápido que en el invernadero (Figura 1B, C); pero la germinación fue más uniforme en invernadero que en laboratorio (Figura 1D). Se debe considerar que la germinación en el laboratorio se evalúa con mayor precisión, ya que se registra directamente la emisión de la radícula, mientras que en el invernadero es la emergencia de la plántula sobre el sustrato (días después de la emisión de la radícula). Esto permite observar mayor uniformidad del proceso en invernadero, sin embargo, la capacidad de distinguir el momento en que aparece la radícula hace que los resultados obtenidos para las variables (Lag 5%, T 50 y U 7525) en laboratorio sean más precisos.
Los tratamientos pre-germinativos también tuvieron un efecto significativo en la capacidad germinativa, pero no en los parámetros estimados de la dinámica de germinación (Tabla 2). Sin embargo, dado que se encontró una interacción significativa de los tratamientos pre-germinativos con la condición de germinación en la capacidad germinativa y en dos de los parámetros de la curva de germinación (Tabla 2), se analizó el efecto de los factores involucrados en los tratamientos pre-germinativos en cada condición por separado.
Efecto de los factores de los tratamientos y su interacción en la capacidad y la dinámica de germinación en cada condición. El factor Hidratación (H) no tuvo efecto significativo para ninguna de las variables en ninguna condición.
El factor Peróxido de Hidrógeno (P) solo tuvo efecto significativo en las variables G max , Lag 5%, T 50 y en la condición de invernadero; mientras que, el factor Escarificación (E) tuvo efecto significativo para las variables G max , Lag 5%, T 50 en la condición de laboratorio. En cuanto a las interacciones, H × P fue significativa para T 50 y U 7525 en laboratorio, y para G max en invernadero; H × E no fue significativa para ninguna variable y P × E resultó significativa para Lag 5% en invernadero (Tabla 3).
Tabla 3 Valores de p de los factores hidratación, peróxido, escarificación e interacciones en el modelo 2, para la capacidad germinativa (G max), retraso (Lag 5%), T 50 y U 7525 en semillas de Pinus coulteri D. Don., en condición de laboratorio e invernadero.
| Efecto | Laboratorio | Invernadero | ||||||
|---|---|---|---|---|---|---|---|---|
| Pr >F | Pr >F | |||||||
| Gmax | Lag5% | T50 | U7525 | Gmax | Lag5% | T50 | U7525 | |
| Hidratación (H) | 0.6483 | 0.9549 | 0.6851 | 0.9779 | 0.6255 | 0.1088 | 0.5713 | 0.1908 |
| Peróxido (P) | 0.1191 | 0.1697 | 0.0627 | 0.2043 | <0.0001 | 0.0002 | 0.0024 | 0.5752 |
| Escarificación (E) | <0.0001 | 0.0289 | 0.0068 | 0.9558 | 0.7912 | 0.1010 | 0.7649 | 0.1012 |
| H × P | 0.6526 | 0.7496 | 0.0224 | 0.0105 | 0.0205 | 0.0658 | 0.0699 | 0.6132 |
| H × E | 0.2479 | 0.9984 | 0.3244 | 0.2668 | 0.8269 | 0.6118 | 0.8252 | 0.8026 |
| P × E | 0.5945 | 0.3715 | 0.2434 | 0.8587 | 0.5163 | 0.0188 | 0.0773 | 0.4156 |
Efecto del factor peróxido de hidrógeno.- A diferencia de la condición de laboratorio, en invernadero, la aplicación de H 2 O 2 en una concentración del 2 o 3 % mejoró la germinación en un 35 % (Figura 2A), permitió acelerar el inicio de la germinación, reduciendo el valor de Lag 5% en 6 días (Figura 2B) y redujo el tiempo a T 50 en 8 días, respecto al testigo (Figura 2C).
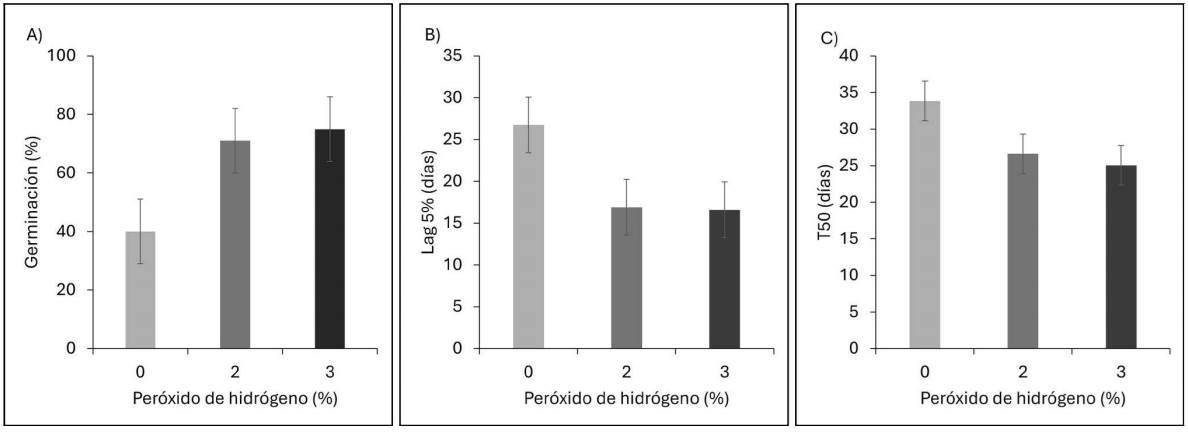
Figura 2 Efecto de la concentración de peróxido de hidrógeno (%) en A) capacidad germinativa, B) retraso de la germinación (Lag 5%) y C) tiempo a germinar el 50 % de semillas viables (T 50 ) de Pinus coulteri, en condición de invernadero.
Efecto del factor escarificación.- En condiciones de laboratorio, la escarificación con el lijado de semillas alcanzó una germinación del 80 %, donde las semillas lijadas superaron en 30 % a las no lijadas (Figura 3Aa). El tiempo para alcanzar 5 % de semillas germinadas (Lag 5%) se redujo en 12 días en las semillas lijadas (Figura 3B); mientras que para alcanzar el 50 % de germinación de las semillas viables (T 50 ) disminuyó siete días en promedio, con respecto a las semillas no escarificadas (Figura 3C). Este resultado sugiere que romper la barrera física que forma la testa permite un inicio más rápido de la germinación de la semilla de P. coulteri.
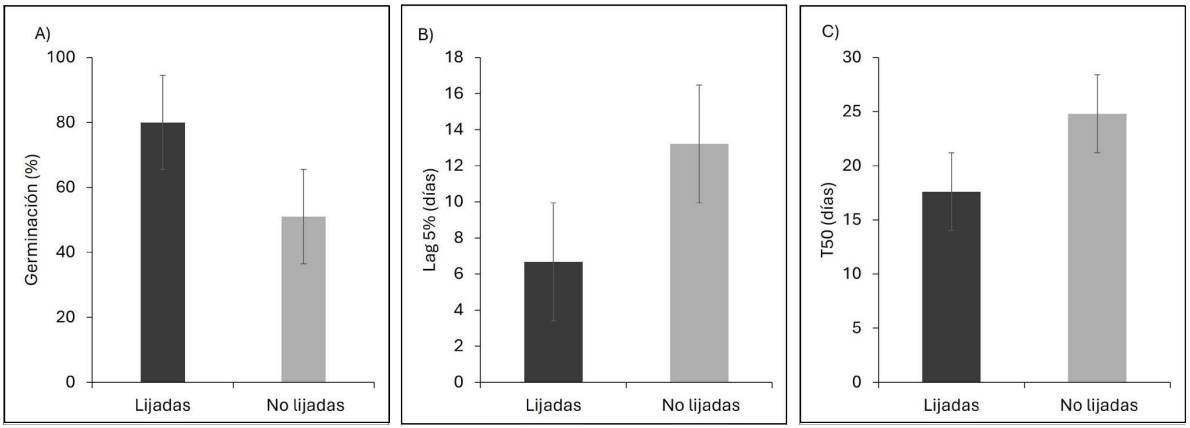
Figura 3 Efecto de la escarificación (semillas lijadas y no lijadas) en A) germinación, B) retraso al inicio de la germinación (Lag 5%), C) tiempo en germinar el 50 % de semillas viables (T 50 ) de Pinus coulteri, en condición de laboratorio.
Efecto de la Interacción de los factores Hidratación × Peróxido de hidrógeno.- En invernadero, el efecto del H 2 O 2 sobre la capacidad germinativa de la semilla resultó más efectivo cuando aumentó el periodo de hidratación de 24 a 48 h; mientras que en ausencia de H 2 O 2 disminuyó en más de 30 % (Figura 4A), particularmente cuando la semilla permaneció más tiempo en agua. Este efecto se debe posiblemente a un agotamiento del oxígeno disponible cuando la hidratación es prolongada (Yasin 2016). La aplicación de 2 o 3 % de H 2 O 2 proporciona oxígeno adicional, lo que permite que la capacidad germinativa se mantenga a pesar del periodo de hidratación. La combinación de una concentración de 2 % de H 2 O 2 con 48 h de hidratación proporcionó la mayor capacidad germinativa (83 %) de la semilla en este ensayo.
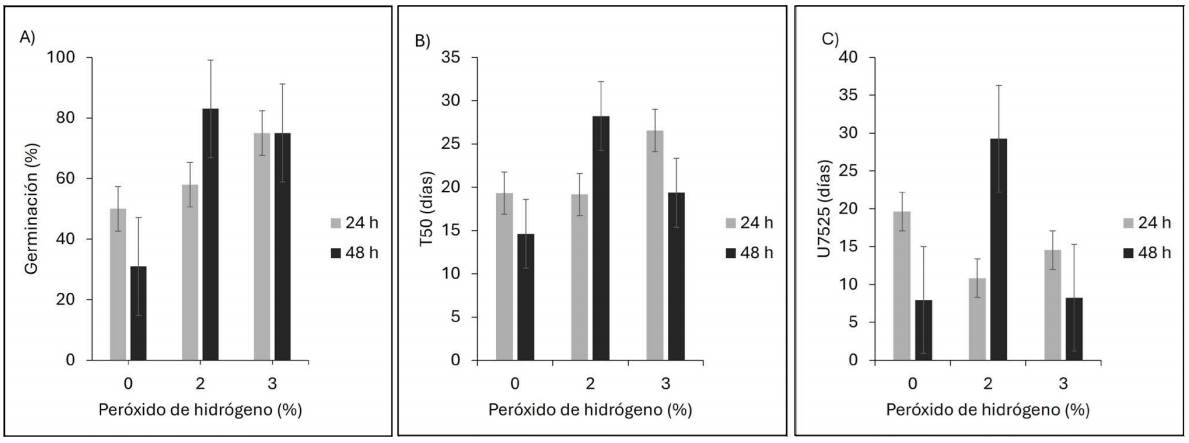
Figura 4 Efecto de la interacción de los factores hidratación y concentración de peróxido de hidrógeno (%) (H × P) en: A) capacidad germinativa en condición de invernadero, B) tiempo en germinar el 50 % de semillas viables T 50 , y C) uniformidad de la germinación en condición de laboratorio en semillas de Pinus coulteri.
En laboratorio, la interacción H × P modificó el valor de T 50 , el efecto 24 h de hidratación al 0 y 2 % de H 2 O 2 no fue diferente de hidratar 48 h con una concentración del 3 %, sin embargo, se obtuvo un valor menor de T 50 (tiempo más corto) con hidratación durante 48 h sin H 2 O 2 (Figura 4B). En relación con la uniformidad, al aumentar el periodo de hidratación de 24 h a 48 h, sin la aplicación de H 2 O 2 , aumentó la homogeneidad de la germinación (i.e., se redujo el valor de U 7525), mientras que al aplicar 2 % de H 2 O 2 se redujo de manera significativa con la hidratación a 24 h; en cambio, cuando se agregó 3 % de H 2 O 2 , el aumento en el periodo de hidratación no afectó la uniformidad de germinación (Figura 4C).
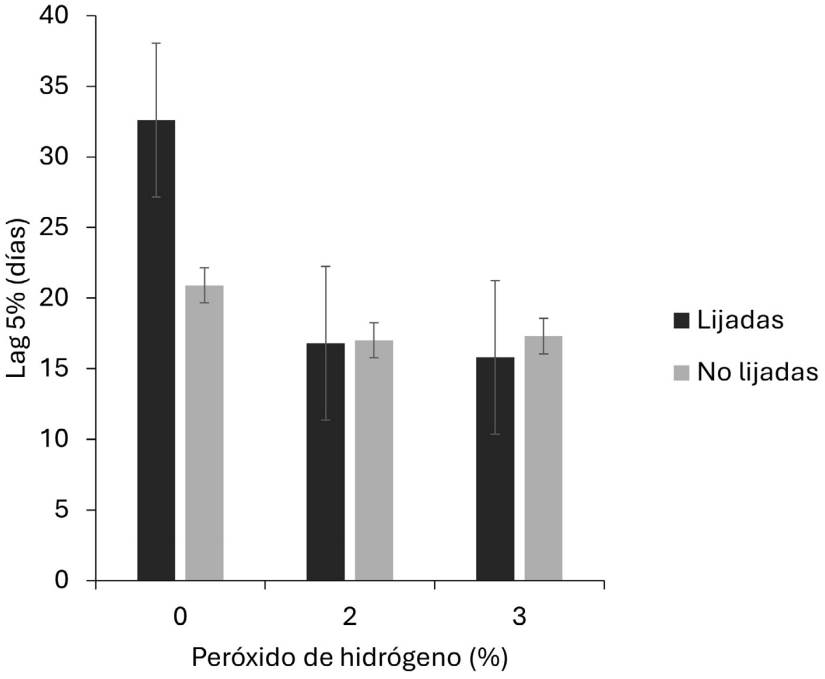
Efecto de la Interacción de los factores Peróxido de hidrógeno × Escarificación.-La interacción peróxido de hidrógeno × escarificación fue significativa para la variable Lag 5% en la condición de invernadero, disminuyendo entre 22 y 16 días el tiempo al inicio de la germinación en semillas sometidas a concentraciones de 2 y 3 % de H 2 O 2 indistintamente del nivel de escarificación de las semillas (Figura 5). En esta condición la escarificación de la semilla no es relevante si no se combina con la aplicación de H 2 O 2 . Sin embargo, un retraso a la germinación de 16 días es mucho tiempo comparado con otros tiempos como el obtenido al escarificar la semilla en condiciones de laboratorio, ya que el valor de Lag 5% fue de 6.5 días.
Discusión
Se conoce que el deterioro de las semillas ocurre aún bajo condiciones de almacenamiento controlado, ya que el tiempo es uno de los principales agentes en el proceso de envejecimiento natural de las semillas (Thirusendura & Saraswathy 2017). En estudios con semillas de pino se ha encontrado que después de dos años de a lmacenamiento, las semillas gradualmente empiezan a perder su capacidad de germinación, debido a procesos de oxidación y degradación de elementos nutritivos, como los ácidos grasos (Manjarrez-Juárez et al. 2017, Mendoza-Hernández et al. 2024). Sin embargo, esto puede variar según la condición de almacenamiento, calidad de semilla y la especie en cuestión (Barnett & Varela 2004, Özel et al. 2022).
Efecto de la condición del ensayo en la capacidad y dinámica de germinación. La aplicación de algunos tratamientos pre-germinativos mejora significativamente la capacidad de germinación de semillas de pino (Ghildiyal et al. 2009, Javanmaer & Kouchaksaraei 2017, Nawrot-Chorabik et al. 2021, Song et al. 2023, Qu et al. 2023).
Al efecto de los tratamientos también se le suma el efecto de la condición donde se establece la prueba de germinación, ya que los entornos controlados como un laboratorio o un invernadero permiten una manipulación precisa de la temperatura y la luz. Por un lado, en laboratorio se observa el proceso de germinación per se, lo cual permite la detección de problemas como malformaciones, poliembrionismo y albinismo; además de llevar un mejor control de enfermedades. Diversos experimentos indican que las pruebas de germinación en laboratorio con control de temperatura, luz y humedad pueden dar lugar a mejores resultados en la germinación de diversas especies de coníferas (Castro et al. 2005, Kueppers et al. 2017, Javanmaer & Kouchaksaraei 2017, Nawrot-Chorabik et al. 2021, Qu et al. 2023). Por otro lado, en invernadero no es necesario hacer el traslado de las semillas germinadas de un lugar a otro, evitando el daño mecánico de la raíz y en consecuencia evitar el riesgo de muerte de la plántula; pero cuando la semilla no germina quedan espacios vacíos en los contenedores, lo que representa un costo en el proceso de producción de planta (Maciel et al. 2022), sin embargo, comparado con el éxito de germinación en un ambiente natural, en invernadero se tienen mejores resultados (Nawrot-Chorabik et al. 2021, Kavanova et al. 2023, Qu et al. 2023).
Efecto de los factores de los tratamientos y su interacción en la capacidad y la dinámica de germinación en cada condición. El efecto del factor hidratación durante 24 o 48 h por sí solo, no tuvo un efecto significativo en la mejora de la capacidad y velocidad de germinación de semillas de P. coulteri, así como se ha reportado para otras especies como Pinus sylvestris L. (Housková et al. 2021). Por otro lado, el factor peróxido de hidrógeno (P) al 3 % en P. coulteri, al igual que en otras especies de pino como P. roxburgii (Ghildiyal et al. 2007, 2009) y P. taeda L., además de mejorar el porcentaje de germinación, también funcionó como desinfectante (Barnett & Varela, 2004). Un efecto similar se reportó en semillas de P. elliottii Engelm, P. echinata P. Mill. y P. palustris P.Mill. para las que la aplicación de H 2 O 2 al 30 % durante una hora resultó en porcentajes de germinación y desinfección mayores (Barnett & Varela 2004). Se ha reconocido que el H 2 O 2 , como molécula exógena, rompe la latencia de la semilla ya que promueve la expresión génica y regula los niveles oxidativos en el proceso; por lo que su uso es útil para mejorar el tiempo y capacidad de germinación (Chu et al. 2022). Mientras que el factor escarificación, en semillas de P. pinceana, P. Lambertiana Douglas ex R. Taylor & R.Phillips, y P. sylvestris, para las que se reportan resultados similares a los encontrados en el presente estudio, es indispensable para romper la latencia de la semilla, permitir la entrada del agua y activar el proceso de germinación (Ramírez-Herrera et al. 2008, Shen & Cho 2021, Nawrot-Chorabik et al. 2021). Otro efecto con resultados favorables en la capacidad y dinámica de emergencia de plántulas de nuestra especie de estudio fue la interacción de los factores Hidratación × Peróxido de hidrógeno (H × P) que es consistente con los resultados reportados para semillas de P. taeda, en las que también en condición de invernadero, la hidratación por 24 y 48 horas con 3 % de H 2 O 2 mejoró significativamente la emergencia de plántulas (Barnett & Varela 2004). Finalmente, la interacción de los factores Peróxido de hidrógeno × Escarificación (P × E), refuerza los resultados obtenidos con cada factor por separado, acentuando la efectividad de su aplicación en semillas de P. coulteri.
Estos resultados, revelan que la viabilidad de la semilla es buena, a pesar del tiempo que ha estado en almacenamiento (más de 10 años), lo que coloca a P. coulteri entre las especies de pino cuya semilla tiene la capacidad de conservar su viabilidad durante periodos largos de tiempo, por ejemplo 10 años, como P. banksiana Lamb., P. halepensis Mill., P. nigra J.F.Arnold y P. strobus L. o incluso mayor como P. lambertiana o P. contorta Douglas ex Loudon (Krugman & Jenkinson 1974). Por otro lado, la dinámica de germinación se modificó con el ambiente utilizado para realizar el ensayo; el tiempo y velocidad de germinación son más precisos en la prueba de laboratorio; ya que la germinación de las semillas es un proceso dinámico, por lo que su resultado debe estar determinado por el tiempo, la velocidad y la homogeneidad (Hernández-Anguiano et al. 2018, Kumar et al. 2023). Los resultados del Lag 5%, T 50 y U 7525, nos dan información muy importante para la toma de decisiones en la elección del tratamiento adecuado para mejorar la germinación de semillas de P. coulteri.
Los tratamientos pre-germinativos probados modificaron la capacidad germinativa de semillas de P. coulteri. Es necesario usar diferentes tratamientos para estimular la germinación de acuerdo con la condición donde se establezca la prueba; ya que depende de esta la efectividad del tratamiento. La escarificación de la semilla de P. coulteri se recomienda bajo condiciones de laboratorio; mientras que, la aplicación de H 2 O 2 solo o en combinación con hidratación por 48 h para invernadero. El tiempo para el inicio de la germinación es más corto en condición de laboratorio, así como el tiempo en alcanzar el 50 % de germinación de las semillas, aunque con menor uniformidad que al evaluar la emergencia de plántulas en invernadero. Para especies en peligro de extinción como P. coulteri es preferible realizar la germinación en laboratorio y posteriormente establecer la semilla germinada en contenedores para garantizar la producción de planta de calidad y con mayor probabilidad de éxito al establecer en campo, esta práctica permite un uso eficiente de semillas. Además, las semillas de P. coulteri mostraron alta viabilidad tras largos periodos de almacenamiento, lo que representa una ventaja para la conservación in situ o ex situ de la especie.











 nueva página del texto (beta)
nueva página del texto (beta)