Introducción
El parvovirus porcino (PPV, por sus siglas en inglés) de importancia dentro del hato reproductor, pertenece al grupo SMEDI, (por sus siglas en inglés)1,2 debido a los signos que presentan: lechones nacidos muertos, momificados e infertilidad en las cerdas3,4. El PPV es estable en el ambiente y es ubicuo en cerdos5,6, por lo que es importante el desarrollo de un correcto programa de inmunización contra éste7,8,9.
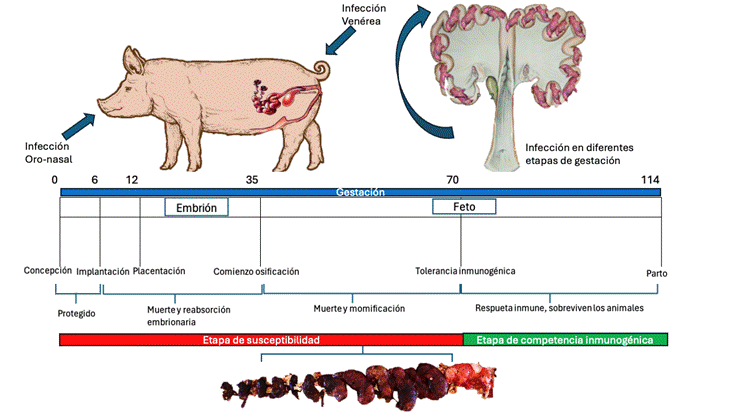
El desarrollo de la enfermedad clínica en animales se limita a las cerdas que están en etapa reproductiva, si la infección se lleva a cabo durante la primera mitad de la gestación puede ocurrir la muerte del embrión o del feto seguido de reabsorción embrionaria, o momificación fetal. Si la transmisión ocurre después de la primera mitad de la gestación, los fetos pueden sobrevivir en el útero sin efectos clínicos (Figura 1)10.
Los programas de inmunización que se emplean en las granjas porcinas se basan en dos principales métodos, el primero consiste en el uso de vacunas comerciales (en México, únicamente se emplean vacunas inactivadas), que pueden ir solas o acompañadas con agentes bacterianos como Erysipelothrix rhusopathiae y Leptospira spp. El segundo método es la administración oral de materia fecal, momias y placenta, trituradas (feedback), a las cerdas de reemplazo 4,7,11,12 , este último presenta el riesgo de diseminar otros patógenos existentes en la granja4,11, además debido a que no se determina la concentración o carga viral del inóculo, es posible que no haya inducción de una respuesta inmune adecuada13.
El parvovirus porcino, presenta varios genotipos estos pueden afectar la epidemiología de la enfermedad y su control en las explotaciones porcinas. La vigilancia y el manejo adecuado son cruciales para prevenir brotes y minimizar el impacto en la producción porcina. En los continentes, europeo y asiático se reporta la circulación de los genotipos 1 al 7 del PPV8,14,15,16, en América del norte se han reportado los genotipos 1, 2, 5 y 6 del PPV17,18. También se ha demostrado que puede haber coinfecciones con diferentes genotipos del PPV19,20. Estudios referentes a la vacunación contra PPV, muestran que hay seroconversión, pero no es homogénea, ya que puede haber sub-poblaciones susceptibles2. En México, los estudios epidemiológicos se limitan a la detección de anticuerpos específicos contra el PPV. Recientemente, García-Camacho, et al21, reportaron la presencia de diferentes genotipos de PPV, en diferentes estados de la república mexicana, pero no hay reportes que asocian la presencia de estos con signología reproductiva.
El objetivo de este trabajo fue determinar la seroconversión inducida por dos tratamientos (feedback y una vacuna comercial) contra parvovirus e identificar el genotipo circulante en cerdas primerizas en el área de adaptación y en cerdas multíparas.
Material y métodos
Historia de la granja
La granja porcina evaluada se encuentra en el noroeste de México (Ciudad Obregón, Sonora), la cual cuenta con un inventario 3,000 cerdas de pie de cría de genética Pig Improvement Company (PIC), con estatus sanitario, negativo a PRRSV (por sus siglas en inglés) Síndrome Reproductivo y Respiratorio Virus) y Mycoplasma hyopneumoniae y positivo a influenza porcina. El programa sanitario de la granja incluye la aplicación de una bacterina frente a Salmonella spp a las dos semanas de edad (Enterisol SC Boehringer Ingelheim®), dos aplicaciones frente a circovirus porcino tipo 2 (PCV-2) (Circumvent PCV2- MSD®) a las tres y seis semanas de edad; dos administraciones de una vacuna contra ileitis (Lawsonia intracellularis (Porcilis Ileitis MSD®) a las 8 y 20 semanas de edad. Para parvovirus porcino, el programa sanitario se realiza mediante dos tratamientos (una exposición controlada feedback y la administración de una vacuna comercial) a cerdas de reemplazo y multíparas. En el año de 2020, el comportamiento reproductivo fue afectado principalmente por el incremento de lechones nacidos momificados 11.12 % y nacidos muertos (4.46 %), la disminución en la tasa de concepción en un 13 % de 93 a 80 % y en la fertilidad al parto de 88 % hasta 65 % en la etapa más crítica. El protocolo de manejo y tratamientos realizados en este trabajo fue aprobado por el Subcomité del Cuidado y su uso de animales experimentales (SICUE) de la Facultad de Medicina Veterinaria y Zootecnia de la UNAM (MC-2019/3-10).
Tratamientos
El presente estudio se realizó en dos escenarios diferentes: en el primero, se evaluó a las cerdas de reemplazo y el segundo a las multíparas. No se evaluaron en conjunto, ya que las cerdas de reemplazo están en la unidad de desarrollo genético (GDU, por sus siglas en inglés) hasta antes de su incorporación a la línea de producción.
Se utilizaron dos protocolos de inmunización contra parvovirus porcino, feedback y vacuna (Farrowsure B â Zoetis) la cual contiene parvovirus porcino-1 cepa apatógena tipo NADL-7 (PPV). En la elaboración de feedback se utilizaron momias licuadas no mayores a 16 cm de longitud (provenientes de cerdas jóvenes 1-2 partos), las cuales se maceraron con agua purificada, en presencia de antibióticos (estreptomicina 1.25 mg) y se congeló en tubos de 50 ml hasta su uso, el macerado se analizó para descartar la presencia de PRRSV por PCR.
Los tratamientos realizados fueron: El tratamiento 1 (T1), consistió en una sola administración de 20 ml de feedback a las 24 semanas de edad a 30 cerdas de reemplazo. El tratamiento 2 (T2), consistió en la administración de 2 ml de la vacuna (Farrowsure B â Zoetis) a las 24 semanas de edad a 30 cerdas de reemplazo, con una segunda aplicación a la semana 27 de edad. El tratamiento 3 (T3), consistió en la administración de 20 ml de feedback a 80 cerdas multíparas, al momento del destete. El tratamiento 4 (T4), consistió en la administración de 2 ml de la vacuna (Farrowsure B ® Zoetis), a 80 cerdas multíparas, dos semanas antes del parto.
Determinación de anticuerpos
Se recolectaron muestras de suero para la determinación de anticuerpos por la prueba de inhibición de la hemoaglutinación (IH) mediante el método Beta, utilizando eritrocitos de cobayo al 0.5 % y Parvovirus vacunal (Synparv, cepa NADL-8 Syva ®) ajustado a 4 unidades hemoaglutinates (UHA), para los T1, T2, T3 y T4. El criterio de positividad se estableció de un valor 1:480 (2.68 log10), de acuerdo con lo reportado por Cobos et al22. Para los tratamientos T1 y T2 se tomaron muestras de suero en intervalos de 3 semanas cada uno (24, 27 y 30 semanas de edad). En el caso de /los tratamientos T3 y T4, se tomaron muestras al destete.
Análisis estadístico
La seroconversión en las cerdas de reemplazo se analizó mediante estadística descriptiva. El efecto de los tratamientos T1 y T2 se comparó utilizando la prueba de supervivencia de Kaplan-Meier y con la prueba de log-rank de Mantel-Cox con una significancia de P<0.0523,24. El análisis de los tratamientos T3 y T4, de las cerdas multíparas, se realizó mediante un modelo de efectos mixtos, los resultados se expresaron en Log10. El efecto fijo fue el tratamiento, el parto se evaluó como un efecto aleatorio ya que este fue una condición propia del animal que no fue considerada para la selección de las unidades experimentales25,26.
Modelo de efectos mixtos utilizado para la evaluación de los tratamientos:
Donde:
Yijk es la respuesta en log10 en el i-ésimo individuo en el j-ésimo parto en el k-ésimo trat;
µ es la media general;
δi(j) es el efecto aleatorio asociado al i-ésimo individuo en el j-ésimo parto;
τi es el efecto del k-ésimo tratamiento;
(δτ) jk es la interacción del j-ésimo parto en el k-ésimo tratamiento.
Todos los análisis se realizaron con el programa SAS OnDemand for Academics (SAS Institute, Cary, North Carolina, USA) con el procedimiento (PROC) MIXED.
Prueba de PCR
Los sueros positivos por IH fueron agrupados en pooles de cinco sueros (se analizaron 31 pools), se realizó la extracción del ADN por medio del sistema de extracción automatizado para ADN/ARN Taco TM (GeneReach Biotechnology, Taiwan), la metodología de extracción se llevó a cabo siguiendo las indicaciones del fabricante. Para detectar la presencia de los genotipos 1-6 de PPV, se usaron primers para cada genotipo previamente reportados (Cuadro 1)21.
Cuadro 1 Primers empleados para la amplificación de parvovirus porcino
| Primers | Secuencia 5´3´ | T° de alineamiento |
Tamaño (pb) |
Posición Genbank/número de acceso |
|---|---|---|---|---|
| PPV1-F PPV1-R |
CACACCAGCAGCACCTAGAA
TCCTACCTGAGCTGGCCTAA |
60°C | 454 | 3364‐3817/U44978a |
| PPV2-F PPV2-R |
AACCACGCCAAATCAAAGTC
TAACAGACCCGTCCATTTCC |
60°C | 413 | 4015‐ 4427/EU200677a |
| PPV3-F PPV3-R |
ATTGTGCGCATTAATATACCA
TGGTCCCAAGCAATAGGAT |
57°C | 578 | 3590‐ 4167/GU938300a |
| PPV4-F PPV4-R |
TAGCACTATGGCGAGCAAA
AAGCAAGCAGTGTAGCAGAGTT |
59°C | 675 | 3800‐ 4474/NC014665a |
| PPV5-F PPV5-R |
TTTGGGCGCCATATATTGAT
ATGCGGAAAAGAGCTAAGCA |
58°C | 521 | 3363‐ 3883/JX896318 |
| PPV6-F PPV6-R |
ATTCCCAACAGACAGACAGAA
TTAGGTCGGAAGGCATCAT |
58°C | 550 | 3791‐ 4340/KR709268 |
PPVs= parvoviruses. aICTV secuencia de referencia.
Para la amplificación se realizó la prueba de PCR con una reacción ajustada a 25 µl utilizando los primers a una concentración de 25 µM, en la reacción se utilizó una mezcla maestra Taq PCR Master mix Qiagen( (conteniendo 5 U Taq DNA polimerasa, el buffer 1X cloruro de magnesio 25µM, 10 µM de cada dinucleótidos trifosfato (dNTP), 0.5µM de cada primer y 25 ng de DNA de templado ) y fueron amplificados en un termociclador C1000 Touch Thermal Cycler,BIO-RADTM bajo las siguientes condiciones de reacción: 94 °C por 3 min, 35 ciclos a 94 °C durante 1 min, como temperatura de alineamiento, se emplearon 60 °C para PPV1 y PPV2, 57 °C para PPV3, 59 °C para PPV4 y 58 °C para PPV 5 y PPV6 y 72 °C de elongación durante 1 min, así como una extensión final de 72 °C durante 10 min. El producto amplificado de PCR fue separado por electroforesis capilar horizontal con gel de agarosa al 1.5 % para la visualización de los fragmentos.
Secuenciación metagenómica
Las muestras positivas a parvovirus por PCR punto final se analizaron mediante secuenciación de siguiente generación (Shot gun), la cual se realizó en la Unidad de Secuenciación del Instituto de Biotecnología, UNAM. Para la construcción de las bibliotecas genómicas, se cuantificó la concentración del material genético extraído de las muestras, mediante el espectrofotómetro de microvolumen Genova Nano 737,501, Jenway, Staffordshire, Reino Unido. Posteriormente se utilizó el Kit de Preparación de Biblioteca de ADN (Nextera XT.) utilizando 5 µl de ADN. La secuenciación se realizó en la plataforma Illumina NextSeq 2 x 75, con una profundidad de 1 millón de lecturas. La calidad de las secuencias crudas fue evaluada con el programa FASTQC (Babraham Bioinformatics, Reino Unido), la eliminación de adaptadores se realizó con Cutadapt v1.11. Así mismo, las lecturas limpias se filtraron inicialmente utilizando el software de alineación Bowtie2 contra el genoma de referencia de Sus scrofa (GCF_000003025.6) para retirar el genoma del hospedero.
Las secuencias filtradas se ensamblaron mediante el programa SPADES, así mismo el análisis de los ensambles se realizó con Kraken2. Además, se realizaron alineamientos para la búsqueda específica de lecturas compatibles con parvovirus porcino (Porcine parvovirus 4 isolate PPV4/COL/Valle575/2021, complete genoma), utilizando el programa Bowtie2 (bowtie2 --no-unal --sensitive-local).
Resultados
Los resultados de seroconversión para el T1 (feedback) en las semanas de edad 24, 27 y 30, seroconvirtieron el 23.2, 63.3 y 90 % respectivamente, mientras que el grupo T2 (vacuna), la seroconversión fue de 33.3, 53.3 y 83.3%, respectivamente (Cuadro 2). El análisis comparativo realizado entre los dos tratamientos, T1 y T2, mediante la prueba de supervivencia de Kaplan-Meier no mostró diferencia significativa (P>0.05).
Los resultados de seroconversión obtenidos para los tratamientos realizados en las hembras multíparas, T3 y T4, mostraron una seroconversión del 78.7 % de las cerdas (P<0.05) con el T3, mientras que para el T4 sólo el 50 % de las cerdas mostraron seroconversión (P<0.05).
Cuadro 2 Porcentaje de cerdas de seroconversión de T1, T2, T3, T4 por la prueba de inhibición de la hemoaglutinación
| Tratamiento | T1
(Feedback) n=30/edad |
T2
(vacuna) n=30/edad |
T3
n=80 |
T4
n=80 |
||||
|---|---|---|---|---|---|---|---|---|
| Edad en semanas | 24 | 27 | 30 | 24 | 27 | 30 | Multíparas | Multíparas |
| Positivos | 7 | 19 | 27 | 10 | 16 | 25 | 63 | 40 |
| Negativos | 23 | 11 | 3 | 20 | 14 | 5 | 17 | 40 |
| %
seroconversión |
23.3 | 63.3 | 90 | 33.3 | 53.3 | 83.3 | 78.7 | 50 |
Los resultados obtenidos mostraron efecto significativo en T3 por número de parto (P<0.0292). El análisis de la seroconversión por número de parto y no por tratamiento no fue estadísticamente significativo (P>0.05) (Cuadro 3).
Cuadro 3 Cerdas seropositivas por prueba de inhibición de la hemoaglutinación, por tratamiento (T3 y T4) y número de parto en cerdas multíparas
| Feedback T3 | Vacuna T4 | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Título IH | Número de parto | Número de parto | |||||||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 1 | 2 | 3 | 4 | 5 | 6 | ||
| 1:60 | 1 | - | - | - | - | - | 6 | 3 | 3 | 1 | - | - | |
| 1:120 | 1 | - | 2 | 1 | - | - | 4 | 3 | 2 | 4 | 1 | 2 | |
| 1:240 | 3 | 5 | 3 | 1 | - | - | 2 | 3 | - | 2 | 4 | - | |
| 1:480 | 4 | 5 | 2 | 2 | 3 | 2 | - | 1 | - | 1 | 1 | - | |
| 1:960 | 3 | 5 | 2 | 2 | 2 | 2 | - | 2 | 3 | 1 | 2 | - | |
| 1:3840 | 4 | 2 | - | 3 | 3 | 1 | 3 | 6 | 2 | - | 1 | - | |
| 1:7680 | 4 | 3 | 3 | 2 | 2 | 2 | 5 | 1 | 3 | 2 | 4 | 2 | |
Título positivo a partir de 1:480; - = sin muestra.
En la Figura 2, se muestra el resultado de PCR de los sueros analizados que fueron positivos a parvovirus porcino por medio de IH, de los cuatro tratamientos. De las cuales se corroboran por PCR cuatro muestras positivas de parvovirus porcino tipo 4, en los tratamientos T1, T2, T4 (dos positivas) lo que representa 9.67 %.

Carril 1 M= 1000kb. carril 2 muestra positiva (fragmento de 675 pb) obtenida del tratamiento 1, carril tres muestras positivas del tratamiento dos y carriles cuatro y cinco muestras positivas del tratamiento 4.
Figura 2 Productos de amplificación de parvovirus 4
Resultados de metagenómica
De las muestras secuenciadas se obtuvo un total de 2,199 millones de lecturas para la muestra analizada del tratamiento T1, de las cuales el 0.04 % correspondieron a genomas virales, y 0.04 % a genomas bacterianos; 2,145 millones para el tratamiento T2, de las cuales el 0.4 % correspondieron a genomas virales, y 0.5 % a genomas bacterianos, 21,938 millones para el tratamiento T3, de las cuales el 0.03 % correspondieron a genomas virales, y 0.01 % a genomas bacterianos y 12,379 millones para el tratamiento T4, de las cuales el 0.1 % correspondieron a genomas virales, y 0.008 % a genomas bacterianos. La presencia de bacterias reportadas incluye microorganismos ambientales que pueden estar asociados con las diferentes etapas de producción en los cerdos, así como revelar el desarrollo inicial del microbioma; esta etapa es crucial, ya que le microbioma temprano está relacionado con el desarrollo del sistema inmunológico, la maduración de órganos y la salud general de los animales, y la presencia de patógenos asociados a problemas reproductivos en las cerdas.
En el Cuadro 4 se resume las especies de virus y bacterias identificados mediante secuenciación y su importancia en las granjas, algunas de ellas como se ha mencionado están relacionadas con bacterias ambientales, como Diaphorobacter sp.
Cuadro 4 Microorganismos encontrados por metagenómica
| Microrganismo | Importancia | Referencias |
|---|---|---|
| Clostridium botulinum | Es raro en cerdos, la infección provoca
incoordinación, parálisis motora, anorexia y muerte. Se asocia a alimento contaminado o alimentación con dietas no convencionales (desechos), es de importancia en salud pública. |
27 |
| Staphylococcus aureus | Está involucrado en lesiones en piel, así como,
causante de septicemia, mastitis, vaginitis, metritis, osteomielitis y endocarditis, es de importancia en salud pública. |
28 |
| Cupriavidus neocaledonicus | Microorganismo capaz de crecer en suelos ricos
en metales pesados, no se reportan asociaciones con enfermedades en humanos o animales. |
29 |
| Comamonas testosteroni | Se considera una bacteria comensal, sin
embargo, se ha reportado en humanos con procesos septicémicos. |
30 |
| Haloterrigena sp. | Bacterias que se encuentran en ambientes
desérticos, no hay reportes o asociaciones con enfermedades en animales y humanos. |
31 |
| Diaphorobacter sp. | Bacterias que se pueden ser aisladas en lodo,
forma parte de la microbiota intestinal, se ha encontrado frecuentemente en humanos con cáncer, no se tienen reportes en animales domésticos. |
32,33 |
| Malassezia restricta | Asociado a enfermedades cutáneas, otitis en
animales y humanos, no se tiene documentado en cerdos. |
30,34 |
| Leishmania mexicana | Provoca enfermedad cutánea, es de importancia
en salud pública. La leishmaniasis puede ser catalogada como enfermedad ocupacional donde veterinarios y trabajadores en el sector agrícola y animal son mayormente afectados. |
35 |
| Gamaretrovirus porcino C | El oncovirus porcino tipo c es un virus
endógeno, tiene gran relevancia sobre todo en animales que son destinados para xenotrasplantes, ya que puede infectar células humanas y representa un riesgo de infección a humanos con retrovirus. |
36,37 |
| Parvovirus porcino 4 | Virus que afecta a cerdos, no se ha reportado
en investigaciones asociación con enfermedad, sin embargo, se menciona que puede estar implicado en coinfecciones con otros agentes virales. |
38,39 |
Identificación de parvovirus porcino 4
Con base en los resultados de los análisis de las muestras por PCR, las secuencias obtenidas también se analizaron para identificar el genoma del parvovirus porcino tipo 4. Se utilizó el genoma de referencia de PVP4 OR359295.1 Porcine parvovirus 4 isolate PPV4/COL/Valle575/2021 y se alinearon las secuencias para mapear el genoma de referencia bajo. Los contigs recuperados que se alinearon con la referencia fueron analizados mediante la herramienta Blastn del NCBI para comprobar su identidad con secuencias de PVP4.
De las cuatro muestras analizadas en dos de ellas se identificaron secuencias correspondientes al PVP4. En la muestra T1 (tratamiento feedback a las 24 semanas de edad en cerdas de reemplazo), se obtuvieron 9 contigs que se alinearon a lo largo del genoma de referencia, de las cuales seis fueron concordantes. Estas secuencias identificadas tienen un 96 % de cobertura y un 100 % de identidad con muestras reportadas en China en 2017 (Cuadro 5). Así mismo, la muestra T4 (Cuadro 6) se obtuvieron 8 lecturas que se alinearon a lo largo del genoma de referencia, todas concordantes. Estas secuencias identificadas tienen entre un 40 y 80 % de cobertura y un 100% de identidad con muestras reportadas en China entre 2017 y 2022 y la cepa KY586146 reportada en Brasil en 2008.
Cuadro 5 Contigs recuperados correspondientes con PVP 4, de la muestra del tratamiento T1
| Lectura | Posición genoma | Secuencia |
|---|---|---|
| R1 | 480 | GTGTATAAGAGACAGGAGCAGAACTCCGTCGTTTTCG GCCTGTATTTGAAGATGGA |
| R2 | 460 | CGGCCTGTATTTGAAGATGGAAACCTACTGGACAGGT ATTTCTGTCTCTTATACAC |
| R2 | 2456 | CGTCGGCAGCGTCAGATGTGTATAAGAGACAGGTATT ATACCGATACTAACATGGG |
| R1 | 2940 | GATTCTGATGACACCAGTAAAGAAAAATTCTATGCAT TTATGGAAAAAATTCAGC |
| R2 | 2838 | GAAGCTCCTGTTACAGCAGTTCCGGTTGAGACATCACC AACTGAAAAACAGGTAC |
| R1 | 4636 | AAGATTTAAAGACGGTGATTATTCAATAACAGGTCCA GGAGATAGAGATAAAACA |
| R2 | 4726 | CACCAGAGATACCTATCTCTTCTCCAGCGATTTAGCT AAAACTGAAAGAGAACAGC |
| R1 | 5280 | GCGCCTGCAGCGGATCCATTCCAAGTAATACATATTTG AACCAATATTGCCAATTT |
| R2 | 5259 | CAAGTAATACATATTTGAACCAATATTGCCAATTTTTG CTTACATATGAAATGGAA |
Cuadro 6 Contigs recuperados correspondientes con PVP 4, de la muestra del tratamiento T4
| Lectura | Posición genoma |
Secuencia |
|---|---|---|
| R1 | 339 | GCATGATTTATGCAAAGAGGAAGTTAACCTGATTGGTCAGTT TTTTTGGCGGGA |
| R2 | 279 | TTGATTGGACGGGAACTCAAGTCCTAATTTGAATTGACGTGG ACCAATCAGAATC |
| R2 | 1062 | TAAGCTTCTTTGTGCCCCATAAGAATAAACACGGGGCCTGGA AGAGCACGGACG |
| R1 | 946 | CACCATCGGTGGAGCCATCGGTGATGCTTGCCTAAATACTGA TAAGAGAAAGGAGT |
| R2 | 1245 | AGGAGTTGCTGGATAATAGACAGGACCCAGCGGTGATCGAA GAGCTCTCAGCTCCC |
| R1 | 1112 | CAGATGGGAAAATAAGATTGCTCTAAGTCTATACTCGTTTCT GGCCACCCAGGCAG |
| R2 | 4189 | TTTAATACACCATGGTACTATTATGATCTAAACATTATGTCCT GCCATTTCTCTCC |
| R1 | 3911 | ACCGGGACAACCATATCAACTACCAAAATACTCATACAGAA CTGTTGGAAAA |
Los resultados del análisis de Blastn de los contigs obtenidos de las muestras T1 y T4 se muestran en el Cuadro 7, se incluye el porcentaje de identidad y la cobertura.
Cuadro 7 Alineación de las secuencias obtenidas con las secuencias de referencia de PPV4
| No. de acceso |
País/año | Descripción | Nombre científico |
Max score |
Total score |
Query cover |
E value | % Ident |
Acc. Len |
|---|---|---|---|---|---|---|---|---|---|
| MK092421.1 | China, 2015 | Porcine parvovirus 4 isolate
PPV4-DJH18, partial genome |
Porcine parvovirus 4 |
104 | 104 | 96% | 2.00E-18 | 100.00 | 5036 |
| MK378290.1 | China, 2017 | Porcine parvovirus 4 isolate
PPV4_VIRES_TJ01_C2 capsid protein gene, partial cds |
Porcine parvovirus 4 |
104 | 104 | 96% | 2.00E-18 | 100.00 | 1482 |
| MK378288.1 | China, 2017 | Porcine parvovirus 4 isolate
PPV4_VIRES_SX02_C2 capsid protein gene, partial cds |
Porcine parvovirus 4 |
104 | 104 | 96% | 2.00E-18 | 100.00 | 1355 |
| MK378286.1 | China, 2017 | Porcine parvovirus 4 isolate
PPV4_VIRES_SX01_C1 replicase gene, partial cds; and ORF3 and capsid protein genes, complete cds |
Porcine parvovirus 4 |
104 | 104 | 96% | 2.00E-18 | 100.00 | 4835 |
| MK378278.1 | China, 2017 | Porcine parvovirus 4 isolate
PPV4_VIRES_NX02_C1 replicase, ORF3, and capsid protein genes, complete cds |
Porcine parvovirusv 4 |
104 | 104 | 96% | 2.00E-18 | 100.00 | 5174 |
| MK378276.1 | China, 2017 | Porcine parvovirus 4 isolate
PPV4_VIRES_NM02_C1 replicase gene, partial cds; and ORF3 and capsid protein genes, complete cds |
Porcine parvovirus 4 |
104 | 104 | 96% | 2.00E-18 | 100.00 | 4835 |
| MK378270.1 | China, 2017 | Porcine parvovirus 4 isolate
PPV4_VIRES_JL01_C1 replicase gene, partial cds; ORF3 gene, complete cds; and capsid protein gene, partial cds |
Porcine parvovirus 4 |
104 | 104 | 96% | 2.00E-18 | 100.00 | 4786 |
| MK378269.1 | China, 2017 | Porcine parvovirus 4 isolate PPV4_VIRES_HuN02_C1 replicase gene, partial cds; ORF3 gene, complete cds; and capsid protein gene, partial cds | Porcine parvovirus 4 |
104 | 104 | 96% | 2.00E-18 | 100.00 | 4721 |
| MK378268.1 | China, 2017 | Porcine parvovirus 4 isolate
PPV4_VIRES_HuN01_C1 replicase, ORF3, and capsid protein genes, complete cds |
Porcine parvovirus 4 |
104 | 104 | 96% | 2.00E-18 | 100.00 | 5500 |
| MK378264.1 | China, 2017 | Porcine parvovirus 4 isolate
PPV4_VIRES_HeN01_C1 replicase gene, partial cds; ORF3 gene, complete cds; and capsid protein gene, partial cds |
Porcine parvovirus 4 |
104 | 104 | 96% | 2.00E-18 | 100.00 | 4778 |
Acc. Len= Accession length.
Discusión
El parvovirus porcino (PPV) es un patógeno crucial en la producción porcina, su ubicuidad en cerdos subraya la necesidad de estrategias preventivas efectivas, como la vacunación y el uso de métodos de exposición como el feedback4,13. Recientemente, se han identificado siete genotipos de PPV en diferentes regiones, con signología reproductiva21,40-43.
Diversos estudios proporcionan una visión integral sobre la seroconversión y la respuesta inmune frente al parvovirus porcino tipo 1 (PPV1) en cerdas de reemplazo y sus implicaciones reproductivas6,44, sin embargo, poco se ha descrito sobre los otros genotipos de parvovirus porcino. Luevano et al45 observaron que los anticuerpos contra el PPV1 en cerdas jóvenes pueden persistir hasta las 20 semanas de edad; este hallazgo sugiere que los anticuerpos detectados en el presente trabajo en el primer muestreo a las 24 semanas, podrían ser de origen materno y un factor crítico a considerar cuando se interpreta la respuesta inmune en cerdas primerizas. La presencia prolongada de anticuerpos maternos puede interferir con la eficacia de la vacunación, y debe tenerse en cuenta al planificar los calendarios de vacunación y muestreo45,46, también puede explicar la respuesta heterogénea en las cerdas vacunadas, tanto en la positividad reportada como en los títulos de anticuerpos.
Como se ha mencionado existen vacunas comerciales contra el parvovirus porcino 1, éstas han sido evaluadas por diversos grupos, Noguera et al47, evaluaron tres vacunas comerciales contra PPV1, los porcentajes de seroconversión variaron entre 50 y 70 %, similar a lo obtenido en el presente estudio. En el presente trabajo los resultados obtenidos con el tratamiento convencional de feedback (T1), y con una vacuna comercial (T2), mostraron en las cerdas primerizas seropositividad del 90 y 83.3, respectivamente; este resultado concuerda con lo reportado por otros investigadores48, quienes reportaron seroconversión del 70 % tras la vacunación con una vacuna comercial contra PPV1. Los resultados del presente trabajo indican una buena respuesta inmune inicial, pero también reflejan que el porcentaje de seroconversión puede no ser absoluto, similar a lo observado en otros estudios46,47, además, en esos estudios se observó que pese a la vacunación se presentaron de lechones momificados, lo que subraya la importancia de la elección adecuada de la vacuna y su potencial impacto en la salud reproductiva de las cerdas. En el presente estudio se encontró que en los grupos con vacunación (T2 y T4), se continuaron presentando lechones momificados, lo cual puede ser asociado a que el componente de la vacuna es el parvovirus genotipo 1, y no protege contra otros genotipos del parvovirus porcino.
El efecto del número de parto en las cerdas frente a la vacunación es un tema importante en la producción porcina, ya que influye en la eficacia de la inmunización y en la salud reproductiva del hato. Generalmente, las cerdas primerizas pueden tener una respuesta inmune más robusta debido a su falta de exposición previa a patógenos. Sin embargo, las cerdas multíparas, que han sido expuestas a múltiples ciclos reproductivos y potencialmente a más patógenos, éstas pueden tener una respuesta inmune menos predecible debido a la variabilidad en su historial de exposición y en su estado de salud general. Los resultados del presente estudio para los grupos T3 y T4, con seroconversiones del 78.7 % y 50 %, respectivamente, revelan que, a pesar de la vacunación, la seropositividad puede variar significativamente. Es particularmente notable que el grupo T3, con una alta seroconversión sin vacunación previa, sugiere una exposición previa al virus, mientras que en el grupo T4, a pesar de la vacunación continua, la mitad de los animales no mostró anticuerpos contra PPV1; cabe señalar que en los casos en que sí se encontraron anticuerpos por la técnica de inhibición de la hemaglutinación algunos de los títulos estos fueron altos (1:7680); esto podría indicar variabilidad en la respuesta inmune individual, el número de parto o problemas en la cobertura y administración de la vacuna. Los resultados de feedback concuerdan con lo reportado por Streck et al48 quienes reportan una seropositividad del 84.7 % en cerdas de 4 partos o más, mientras que en paridades mayores disminuye.
No utilizar la vacuna adecuada para el genotipo específico del parvovirus porcino puede causar varios problemas en la producción porcina; si la vacuna utilizada no cubre el genotipo del virus prevalente en la granja, la respuesta inmune inducida puede ser insuficiente para proteger a las cerdas contra el virus. Esto puede resultar en una protección parcial o nula frente a la infección, comprometiendo la eficacia de la vacunación. Los estudios moleculares han identificado varios genotipos de PPV, clasificados como PPV1, PPV2, PPV3, hasta PPV7, estos genotipos pueden tener variaciones en su capacidad para causar enfermedad y en su distribución geográfica. Con la finalidad de determinar el genotipo del parvovirus presente en la granja analizada en este estudio, se realizaron análisis mediante PCR en punto final para los genotipos 1-6, y los resultados mostraron muestras positivas para el genotipo 4. En México, se reportó la presencia de parvovirus 8 en coinfecciones con circovirus porcino 221. Brown menciona que no ha sido posible asociarlo directamente con alguna enfermedad reproductiva en las granjas porcinas25. Sin embargo, se ha mencionado que PPV4 puede tener implicaciones reproductivas49.
En este trabajo se reporta por primera vez la presencia de parvovirus porcino 4, en granjas con problemas reproductivos. Además, las muestras positivas por PCR para el genotipo 4 de parvovirus porcino se analizaron mediante secuenciación de siguiente generación, que permite la secuenciación simultánea de millones de fragmentos de ADN en una sola ejecución, generando grandes volúmenes de datos y confirmando la presencia de parvovirus porcino 4 y de bacterias, hongos y parásitos. La secuenciación de siguiente generación se ha utilizado para caracterizar las comunidades microbianas en animales y humanos, así como entornos ambientales. Esta es una herramienta valiosa para detectar de manera no específica diversos microorganismos en muestras, ofreciendo ventajas únicas para la detección de patógenos emergentes, patógenos exigentes o no cultivables, e infecciones mixtas. En comparación con el cultivo bacteriano y las pruebas de PCR, la secuenciación metagenómica demuestra ventajas en la detección de bacterias difíciles de cultivar y virus menos comunes o que se encuentran en baja cantidad en las muestras. La composición de la comunidad microbiana es dinámica y puede desarrollarse a partir de complejas interacciones entre el hospedador y los factores ambientales externos, en donde las infecciones virales pueden modificar estas interacciones. Los resultados mostraron la presencia de Clostridium botulinum Cupriavidus neocaledonicus Staphylococcus aureus, Diaphorobacter sp, Comamonas testosteroni, Haloterrigena sp, Malassezia restricta, Leishmania mexicana, asi como especies de origen vegetal como Beta vulgaris, Solanum pennellii, Vitis vinifera, Telopea speciosissima, Solanum tenotomums, Zingiber officinale, Manihot esculenta, Vigna angularis, Physcomitrium patens y Gossypium raimondii. También se reporta la presencia de virus de la familia gamaretrovirus porcino tipo C; los retrovirus endógenos porcinos (PERV) no están muy estudiados; son liberados por células porcinas normales y son infecciosos. Se han reportado los virus PERV-A, PERV-B y PERV-C, los virus A y B son virus politrópicos que infectan células de varias especies, incluidos los humanos, lo que los convierte en un riesgo para la xenotransplantación. PERV-C es un virus ecotrópico que solo infecta células porcinas. Se ha demostrado la infectividad de estos virus en experimentos de co-cultivo in vitro. En los últimos años, ha aumentado la evidencia de que los PERV, a diferencia de los retrovirus endógenos humanos (HERV), siguen activos in vivo en los cerdos. Mientras que los HERV se expresan como ARN mensajero, proteínas y partículas no infecciosas, los PERV siguen siendo activos en los cerdos. El número de copias de PRV en diferentes razas de cerdos es variable. El significado biológico de la presencia de estos agentes en las muestras analizadas debe estudiarse en el entorno de las interacciones entre la microbiota y los patógenos (virus o bacterias).
El parvovirus porcino tipo 4 es un agente patógeno emergente; su presencia en cerdos podría tener como consecuencia la presencia de otras infecciones virales o bacterianas, lo que puede complicar los diagnósticos y el manejo de enfermedades, haciendo aún más importante la vigilancia y el estudio de este virus. Las consecuencias económicas debido a la reducción en la producción y los costos adicionales para el control y tratamiento de las infecciones, puede generar un problema serio a la producción porcina en México.
Conclusiones e implicaciones
Los métodos utilizados para la prevención de PPV como lo son el uso de vacunas comerciales o feedback son ampliamente utilizados en las unidades de producción porcina y depende de muchos factores como el estatus sanitario de la granja, los programas de inmunización y por lo tanto los anticuerpos maternales, lo anterior hace que su efectividad sea más difícil de evaluar, en cambio el uso de las vacunas con el esquema e inmunógeno adecuado ayudan a prevenir o controlar al virus; es importante mencionar que al momento ninguna vacuna contra el parvovirus porcino tiene como componente vacunal al PPV4. La variabilidad en la seroconversión y la incidencia de problemas reproductivos subraya la necesidad de una evaluación cuidadosa de los programas de vacunación y la adaptación de estrategias para asegurar una protección óptima y minimizar las pérdidas reproductivas. La identificación del PPV4, en granjas con signos reproductivos, subraya la necesidad de mejorar las estrategias de vigilancia, diagnóstico y control de enfermedades virales en cerdos. El PPV4 es relativamente nuevo en comparación con otros patógenos porcinos más conocidos, por lo que su estudio puede proporcionar información valiosa sobre la virología de los parvovirus porcinos, sus mecanismos de transmisión, cómo afecta a los cerdos y cómo se puede controlar, así como su posible interacción con otros virus o bacterias presentes en las granjas porcinas.











 texto en
texto en