Introducción
La demanda global por productos de origen animal se ha incrementado en los últimos años1. Debido al constante aumento de la población se han buscado alternativas en las que se produzca mayor cantidad de alimento de mejor calidad proteica y con mayor eficiencia. En la ganadería extensiva se usan los pastos nativos como principal fuente de alimento y durante el periodo de sequía es necesario usar suplementos alimenticios debido a que la calidad de estos pastos disminuye, lo que incrementa los costos de alimentación. Por ello, los ganaderos buscan fuentes alimenticias que sean accesibles tanto por su disponibilidad como por su bajo costo y que no impliquen competencia con el humano2.
Por otro lado, los rumiantes producen gases de efecto invernadero como el metano (CH4) que es emitido a la atmósfera1,3. El uso de arbustivas y arbóreas en la alimentación animal puede ser una alternativa para incrementar la digestibilidad, mejorar el valor nutritivo de la dieta y buscar reducir la producción de metano4. Existen investigaciones enfocadas en probar que el uso de hojas de diversas plantas, así como el follaje de algunos árboles pueden servir como alimento, con nutrientes adecuados para lograr una producción económica y ecológicamente viable, que reduzca la producción de gases de efecto invernadero1. El forraje de moringa (Moringa oleifera) es una de estas plantas2, ya que se caracteriza por tener facilidad de propagación y por la baja demanda de nutrientes y agua en su crecimiento5. Se ha demostrado que puede ser una buena fuente de proteína, lo que puede representar una alternativa para sustituir insumos proteicos convencionales en rumiantes6.
Moringa oleifera es un árbol delgado, perene, caducifolio, originario de la India, que se ha extendido a otras partes del mundo. A nivel mundial, es uno de los árboles de más rápido crecimiento que presenta alto rendimiento de biomasa, alto contenido de proteína bruta (˃25%) y un balance de otros nutrientes en sus hojas7. También se considera uno de los árboles más útiles en el mundo, ya que todas sus partes pueden ser usadas como alimento, como medicamento o para propósitos industriales8,9,10. Las diferentes partes de M. oleifera contienen minerales importantes, además de ser una buena fuente de proteína, vitaminas y aminoácidos. También se ha reportado que tiene propiedades agronómicas benéficas como lo es la tolerancia a la sequía, la alta producción de biomasa y el alto contenido de proteína cruda, lo que la vuelve competitiva con forrajes de alta calidad8,11 además de que en sus hojas contiene muchos compuestos activos como flavonoides, saponinas, taninos, alcaloides8. Se ha usado M. oleifera para alimentación de ganado, ya que las hojas son ricas en minerales esenciales para la ganancia de peso y para la producción de leche, además de ser una excelente fuente de proteína que puede mejorar la síntesis de proteína microbiana en el rumen12. También se analizó su efecto nutricional en ovejas, donde tuvieron una mejora en la producción y calidad de la leche12. Sin embargo, no se han reportado estudios sobre el uso de moringa cultivada en el estado de Chihuahua y la repercusión de su uso como alimento sobre la producción animal. Por lo que el objetivo del presente estudio fue evaluar el efecto de hojas de Moringa oleifera cultivada en la región centro del estado de Chihuahua sobre diferentes parámetros de fermentación ruminal in vitro, para tener un primer acercamiento de la viabilidad del uso de esta arbustiva como alimento para ganado en esta región.
Material y métodos
Este estudio se realizó en el Laboratorio de Nutrición Animal de la Facultad de Zootecnia y Ecología de la Universidad Autónoma de Chihuahua (UACh), ubicado en el Km 1 del Periférico Francisco R. Almada de la ciudad de Chihuahua, Chihuahua, México (28°35′10.9″ N; 106°6′26.6″ O; altitud 1,440 msnm).
Suplemento de moringa
Se obtuvo a partir de una plantación de árboles de M. oleifera ubicada en la región centro del estado de Chihuahua, México. Se colectaron las hojas de la planta, se secaron a la sombra y posteriormente se maceraron para obtener alimento en polvo13.
Caracterización del perfil bromatológico
Se realizó la caracterización bromatológica de las hojas de M. oleifera y de la alfalfa (tratamiento testigo) por medio de un análisis proximal. Se midió fibra detergente neutro (FDN) y fibra detergente ácido (FDA) con el método descrito por Van Soest et al14 adaptado para el equipo “Ankom 200 Fiber Analyzer” (Ankom Technology, Fairport NY). La proteína cruda (PC), materia seca (MS), ceniza y EE se determinaron de acuerdo a los métodos estándares de la “Association of Official Analytical Chemistry”15. Los minerales se analizaron por absorción atómica y el perfil de aminoácidos por cromatografía.
Animales y alimentación
El líquido ruminal se obtuvo de tres ovinos fistulados en rumen, de raza Pelibuey (45 ± 3 kg). Previo al proceso de fistulación, los animales se vacunaron (Lapibac; Lapisa®) y desparasitaron (Levax ADE; BioZoo®). Posteriormente se adaptaron a la dieta (forraje de alfalfa) por 15 días. Se ofreció el alimento dos veces al día (0800 y 1700 h). Una vez terminado el periodo de adaptación los animales se dietaron durante 24 h y posteriormente se tomaron las muestras de líquido ruminal de los tres animales directamente de la cánula para realizar las pruebas de fermentación in vitro.
Tratamientos y diseño experimental
Una vez caracterizado el perfil bromatológico de M. oleifera (Cuadro 1), se establecieron tres tratamientos, buscando que tuvieran valores isoprotéicos; TT (Testigo: 100% alfalfa), MB (Moringa bajo: 15% moringa y 85% alfalfa) y MA (Moringa alto: 30% moringa y 70% alfalfa). En la prueba de fermentación in vitro, se utilizó un diseño completamente al azar con medidas repetidas en el tiempo. Se tuvieron tres repeticiones para cada tiempo de fermentación (6, 12, 24 y 48 h). El análisis de producción de gas se realizó de acuerdo a la técnica de Theodorou16, para ello se pesaron directamente 2 g del sustrato en tubos de vidrio de 100 ml con tapón de butilo y agrafe. Para el análisis del resto de las variables estudiadas se pesaron 0.5 g del sustrato en bolsas FN57 (Ankom™) con un tamaño de poro de 25 µm y posteriormente cada bolsa se selló y se colocó en frascos de 250 ml. El inóculo microbiano ruminal se preparó utilizando dos partes de una solución buffer17 y una parte de líquido ruminal. El líquido ruminal se recolectó de los tres ovinos Pelibuey fistulados previamente, directamente de la cánula antes de la alimentación. El inóculo se filtró con muselina y se dispensó en condiciones de anaereobiosis con CO2 (15 ml para producción de gas y 40 ml para el resto de parámetros); se selló inmediatamente y se colocó en una incubadora con agitación a 120 rpm y temperatura controlada a 39 °C. Se prepararon tres repeticiones sin sustrato como control para la producción de gas.
Cuadro 1 Análisis bromatológico del suplemento de Moringa oleifera
| Variable | % |
|---|---|
| Materia seca | 93.87 |
| Ceniza | 15.68 |
| Extracto etéreo | 5.99 |
| FDA | 14.85 |
| FDN | 26.42 |
| Proteína cruda | 16.97 |
| Ca | 3.23 |
| P | 0.27 |
| Mg | 0.8 |
| K | 1.35 |
| Mn, ppm | 120.4 |
| Cu, ppm | 18.64 |
| Zn, ppm | 20.63 |
La producción total de gas se midió con un transductor de presión FESTO® (SIEMENS). El pH se midió con un potenciómetro electrónico inmediatamente después de la toma de muestras. La digestibilidad de la FDN y FDA se evaluó utilizando el método IVTD - Daisy (in vitro True Digestibility Method)18. La determinación de FDN y FDA se llevó a cabo al final de cada tiempo de incubación, el procesamiento se realizó en el analizador de fibra Ankom® 2000 de acuerdo con los métodos descritos por Van Soest et al14. El cálculo de N-NH3 se determinó por espectrofotometría19. La determinación de ácidos grasos volátiles (AGV) se realizó por cromatografía de gases con detección de ionización de flama. Se usó un cromatógrafo de gases Claurus 400® (Perkin Elmer) adaptado con una columna Varian capilar CP-wax58 (FFAP) CB (15 m × 0.53 mm, 0.5 µm)20. La determinación de CH4 y CO2 se calculó a partir de las concentraciones de AGV mediante el uso del método de ecuaciones propuesto por Wolin21.
Análisis estadísticos
Los datos se analizaron con un diseño completamente aleatorizado mediante el procedimiento GLM (SAS ver. 9.4), para las variables pH y PG se consideraron medidas repetidas en el tiempo y el análisis se realizó mediante el Proc MIXED de SAS versión 9.422.
Resultados y discusión
Análisis bromatológico del suplemento de Moringa
Los resultados del análisis bromatológico que se realizó al suplemento de moringa se describen en el Cuadro 1.
Los valores obtenidos varían respecto a lo reportado, ya que la PC fue menor y el contenido de EE fue mayor (Cuadro 1), con respecto a lo reportado en otros estudios23-27. El contenido de PC tuvo un valor aceptable (16.97 %) para su inclusión en la dieta de rumiantes en diferentes etapas de alimentación (NRC), pero es menor con respecto a la alfalfa28, que es uno de los principales forrajes henificados utilizados en dietas de ganado lechero. Sin embargo, en el norte de México es común el uso de heno de avena en la alimentación de ganado de carne, lo cual sugiere que la moringa puede representar una alternativa al uso del heno de avena, que presenta un valor de PC inferior28. El contenido de ceniza fue mayor (15.68 %) a lo reportado en otros estudios8,11,23. Esto sugiere que en las hojas secas de moringa se almacenan una cantidad considerable de ellos. El calcio, magnesio, cobre y potasio tuvieron valores mayores comparados con lo reportado en la literatura25,27,29. El valor del calcio, fue mayor incluso a lo reportado para el heno de avena y alfalfa30; esto le da un valor importante a M. oleifera ya que este mineral es de gran importancia para la regulación de diferentes procesos31, aspectos productivos y para el mantenimiento de la estructura ósea y dental29.
A continuación, se presenta el perfil de aminoácidos encontrado en el suplemento de moringa (Cuadro 2).
Cuadro 2 Perfil del contenido de aminoácidos del suplemento de Moringa oleifera
| Aminoácido | g/100 g |
|---|---|
| Alanina | 0.87 |
| Glicina | 0.63 |
| Valina | 0.53 |
| Leucina | 0.56 |
| Isoleucina | 0.52 |
| Treonina | 0.54 |
| Serina | 0.76 |
| Prolina | 0.69 |
| Aspartato | 1.93 |
| Metionina | 0.11 |
| Glutamato | 6.05 |
| Fenilalanina | 0.75 |
| Lisina | 0.43 |
| Histidina | 0.53 |
| Triptofano | 0.27 |
| Cisteína | 0.04 |
El glutamato, aspartato, alanina, leucina y serina, tuvieron una concentración mayor a lo reportado32. Por su parte, el contenido de alanina fue similar y de leucina fue menor con respecto a lo encontrado en la literatura32. Sin embargo, los datos reportados otros estudios1,5,8,25 son inconsistentes. Todos los valores de los aminoácidos están por debajo de lo reportado por estos autores a excepción del glutamato y el aspartato; esto pudo deberse a que la moringa analizada por ellos se cultivó en condiciones de humedad, altura y temperatura muy diferentes a las que se presentan en la zona de cultivo de M. oleifera utilizada en este estudio, de tal manera que el comportamiento bioquímico de la planta pudo haber generado concentraciones distintas de estos metabolitos. Si bien estos aminoácidos, a excepción de la leucina, son no esenciales, sí representan una buena fuente de nitrógeno para el metabolismo microbiano y, por lo tanto, para la síntesis de proteína microbial33.
Composición nutricional de tratamientos
La composición nutricional de los tres tratamientos usados en la fermentación in vitro se presenta en el Cuadro 3.
Cuadro 3 Composición de las dietas usadas en las pruebas de fermentación in vitro
| Variable (%) | TT | MB | MA |
|---|---|---|---|
| Materia seca | 89.4 | 90.1 | 90.7 |
| Ceniza | 11 | 11.7 | 12.4 |
| Extracto etéreo | 2.08 | 2.7 | 3.3 |
| FDA | 29 | 26.9 | 24.8 |
| FDN | 36.1 | 34.6 | 33.2 |
| Proteína cruda | 21.2 | 20.6 | 19.9 |
| Ca | 1.4 | 1.7 | 1.9 |
| P | 0.26 | 0.3 | 0.3 |
| Mg | 0.32 | 0.4 | 0.5 |
| K | 3.03 | 2.8 | 2.5 |
TT= tratamiento testigo (100% alfalfa) MB= tratamiento moringa bajo (15% moringa 85% alfalfa) MA= tratamiento moringa alto (30% moringa 70% alfalfa).
Fermentación ruminal in vitro
Se realizó con los tres tratamientos antes descritos. Los resultados de las variables evaluadas a partir de la fermentación ruminal in vitro se muestran en el Cuadro 4.
Cuadro 4 Variables evaluadas en las pruebas de fermentación in vitro
| Variable | TT | MB | MA | Valor de P |
|---|---|---|---|---|
| pH | 6.74 a | 6.86 a | 6.76 a | ≥ 0.05 |
| Digestibilidad de la MS, % | 63.88 a | 66.65 ab | 67.87 b | <0.05 |
| FDN, % | 24.64 a | 30.96 ab | 32.09 b | <0.01 |
| FDA, % | 17.80 a | 22.53 ab | 23.54 b | <0.01 |
| PG | 49.06 a | 51.18 ab | 55.93 b | <0.05 |
| Ácido acético, mmol/L | 63.9 a | 42.3 b | 31.2 c | <0.05 |
| Ácido propiónico, mmol/L | 30.6 a | 21.0 b | 11.1 c | <0.05 |
| Ácido butírico, mmol/L | 9.3 a | 4.6 b | 4.2 b | <0.05 |
| TAGV, mmol/L | 103.9 a | 67.9 b | 46.5 c | <0.05 |
| Producción de CO2, % molar | 51.7 a | 48.5 b | 51.9 a | <0.05 |
| Producción de CH4, % molar | 28.6 a | 26.0 b | 32.3 c | <0.05 |
| NH3, mmol/ml | 14.6 a | 14.9 a | 15.1a | >0.05 |
TT= tratamiento testigo (100% alfalfa) MB= tratamiento moringa bajo (15% moringa 85% alfalfa) MA= tratamiento moringa alto (30% moringa 70% alfalfa).
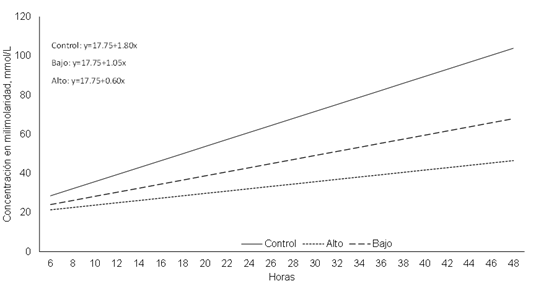
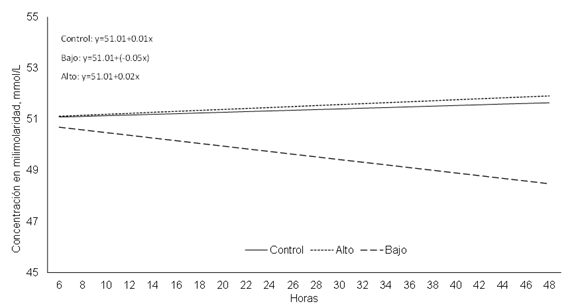
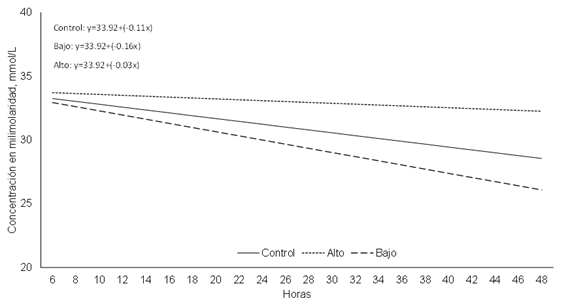
Para pH no se observaron diferencias entre tratamientos, tiempo o su interacción (P≥0.05; Cuadro 4). Esto coincide con lo previamente reportado34,35,36 donde evaluaron el efecto de extractos de hojas de moringa en diferentes cinéticas de fermentación y no observaron diferencias entre tratamientos. Estos resultados garantizan la viabilidad de la microbiota ruminal37. Por otro lado, para digestibilidad de la materia seca (MS) se observaron diferencias entre tratamientos (P<0.05), la cual fue mayor para el tratamiento MA (30 % moringa). Esto difiere a lo reportado por otros investigadores38 quienes encontraron una disminución en la digestibilidad conforme se aumenta la concentración de moringa en las raciones de alimentos, sin embargo, coincide con Morsy et al6 quienes observaron que, al aumentar la proporción del extracto de moringa, la digestibilidad aumenta. Este incremento en digestibilidad está relacionado a los cambios en la cantidad de FDN y FDA, los cuales disminuyeron a medida que incrementó el nivel de moringa en la dieta (Cuadro 3), permitiendo observar el impacto que tiene la adición de este ingrediente sobre una dieta integral. Esta diferencia en la digestibilidad de la materia seca puede estar relacionado con diferencias en la composición de las comunidades bacterianas6 que pudieran haber sido impactadas por la presencia e incremento de moringa en la dieta. La producción de gas (PG) mostró diferencias entre tratamientos y fue mayor para el tratamiento MA (P<0.05; Cuadro 4); sin embargo, este incremento no tuvo el impacto deseado sobre los productos terminales de la fermentación, en donde el total de ácidos grasos volátiles (TAGV) fue menor para el tratamiento MA (Figura 1). Esto se relaciona directamente a la producción de CO2 (Figura 2) que mostró el mismo comportamiento que el TAGV, disminuyendo a medida que se incrementó el nivel de moringa en la dieta (P<0.05). Por su parte, la producción de metano (CH4) no mostró el mismo comportamiento; se puede observar que el tratamiento MB fue menor que los otros tratamientos (P<0.05, Figura 3). Finalmente, para NH3 no se observaron diferencias entre tratamientos, tiempo o su interacción (P>0.05; Cuadro 4).
Las emisiones de CO2 y CH4 durante la fermentación ruminal causan una pérdida de energía de entre 2 y 12 %36. La reducción de metano por presencia de Moringa oleifera también se ha reportado en otros estudios24,35,39. Resulta interesante notar también que, a niveles más altos de moringa, las concentraciones de metano aumentan. Está bien documentado que los metabolitos secundarios de algunas especies de plantas pueden mitigar la producción de CH4 en la fermentación ruminal y Moringa oleifera es rica en metabolitos secundarios como taninos, saponinas y otros compuestos fenólicos que tiene propiedades antimicrobianas y antiprotozooarias que, en consecuencia, podrían estar modificando la composición de la microbiota y con ello la producción de CH46.
También se calculó el porcentaje molar de las concentraciones milimolares de los AGV para los tres tratamientos (Cuadro 5). El patrón de fermentación de las tres dietas fue principalmente acético, ya que este ácido fue el que se encontró en mayor proporción. Esto coincide con lo reportado en la literatura donde se menciona que, en dietas a base de forrajes, la concentración de ácido acético suele estar entre el 60 y el 75 %40. En cuanto al ácido propiónico, la literatura indica que su proporción en este tipo de dietas varía entre el 15 % y el 19 %40. Sin embargo, en este experimento se obtuvo una proporción mayor, siendo la más baja de 23.82 % en el tratamiento MA y la más alta de 30.93 % en MB. La proporción de ácido butírico también coincide con lo reportado en la literatura40, aunque se encuentra en los niveles más bajos del rango esperado, que varía entre el 8 y el 16 %.
Cuadro 5 Comparativo de la concentración de ácidos grasos volátiles (AGV) en mmol/L y su conversión a porcentaje molar
| TT | MB | MA | ||||
|---|---|---|---|---|---|---|
| mmol/L | % | mmol/L | % | mmol/L | % | |
| Total AGV | 103.9 | 100 | 67.9 | 100 | 46.6 | 100 |
| Ácido acético | 63.9 | 61.5 | 42.3 | 62.3 | 31.2 | 66.95 |
| Ácido propiónico | 30.6 | 29.45 | 21 | 30.93 | 11.1 | 23.82 |
| Ácido butírico | 9.3 | 8.95 | 4.6 | 6.77 | 4.2 | 9.01 |
TT= tratamiento testigo (100% alfalfa) MB= tratamiento moringa bajo (15% moringa 85% alfalfa) MA= tratamiento moringa alto (30% moringa 70% alfalfa).
Conclusiones e implicaciones
Casi todos los parámetros de fermentación se vieron afectados por la presencia de Moringa oleifera, a excepción de pH y N-NH3. Si bien, las concentraciones obtenidas de FDN, FDA y TAGV, no fueron las esperadas, se encuentran en proporciones aceptables para alimento de rumiantes. Sin embargo, algunas de las variables tuvieron comportamientos deseables, como lo es digestibilidad de la materia seca, producción de gas, dióxido de carbono y metano. Cabe recalcar que tanto el CO2 como el CH4 tuvieron una disminución en el tratamiento de moringa al 15 % (MB) que pudo deberse a la presencia de los metabolitos secundarios propios de esta planta que, a su vez, afectan a la población de protozoarios y de microorganismos metanogénicos. De forma similar, al aumentar la cantidad de moringa al 30 % también se pueden estar aumentando los factores antinutricionales propios de M. oleifera, mismos que pueden afectar la microbiota ruminal. Debido a lo anterior, se propone realizar análisis de la población ruminal, para identificar a los microorganismos presentes, así como las rutas metabólicas activas para buscar su relación con estos resultados.











 texto en
texto en