INTRODUCCIÓN
Actualmente, los tratamientos de ortodoncia son comúnmente solicitados en el consultorio dental, por razones tanto estéticas como funcionales. Pese a que estos tratamientos pueden llevar a efectos adversos, incluyendo la resorción radicular, dolor, cambios pulpares, enfermedad periodontal, descalcificaciones, y disfunción temporomandibular; tales efectos secundarios no se comprenden en su totalidad, pero se asocian a tratamientos prolongados1. Por lo anterior, se considera que el reducir el tiempo de tratamiento podría también disminuir los efectos secundarios1,2.
A lo largo del tiempo se han desarrollado métodos para acelerar el movimiento dental y acortar la duración de los tratamientos ortodónticos, incluyendo la estimulación quirúrgica, farmacológica, física, y las pulsaciones ultrasónicas piezoeléctricas de baja intensidad (lipus)1,3-6. En odontología se han desarrollados dispositivos como AcceleDent® (OrthoAccel® Technologies, Inc., Bellaire, Estados Unidos), que buscan facilitar el movimiento dental mediante la estimulación vibratoria, aunque su eficacia es objeto de debate. En este contexto, los pacientes tratados con AcceleDent® no presentan diferencias significativas en la nivelación de la dentición mandibular, la reducción del dolor o la aceleración del cierre de espacios interproximales durante el tratamiento con aparatos fijos, en comparación con el grupo de control4,7.
Por otro lado, la teoría detrás de dispositivos como AcceleDent® sugieren que las fuerzas vibratorias estimulan la diferenciación y maduración celular, lo que podría acelerar la remodelación ósea y el movimiento dental a través de un efecto anabólico en el hueso. Asimismo, estudios realizados en modelos animales muestran que la terapia vibratoria mejora el tiempo de consolidación de fracturas y aumenta la expresión de genes relacionados con la osteogénesis8,9.
Investigaciones in vitro han estudiado el efecto de la estimulación vibratoria en osteoblastos, osteocitos, y osteoclastos, así como en las células troncales mesenquimales (MSCS). Las MSCS son células multipotentes que juegan un papel crucial en la regeneración y reparación tisular10. Entender cómo las vibraciones mecánicas afectan el comportamiento y la diferenciación de las células troncales mesenquimales es esencial en medicina regenerativa y ortodoncia.
Este estudio tuvo como objetivo evaluar el efecto de las vibraciones en tres líneas celulares: osteoblastos, MSCS derivadas de la pulpa dental (DPSCS) y MSCS derivadas de tejido gingival (GMSCS), para establecer protocolos para la aplicación de vibraciones mecánicas en tratamientos ortodónticos. Se espera que los resultados contribuyan al desarrollo de terapias para acelerar la regeneración de tejidos o tratar condiciones médicas específicas, incluyendo el tratamiento de ortodoncia.
MATERIAL Y MÉTODOS
El presente estudio es de tipo experimental in vitro, observacional y prospectivo. Para ello, se ensambló una plataforma de vibración sostenida basada en metodologías previas11-13. Utilizando un generador de funciones marca Feeltech (FY-2300) y un amplificador de audio (XH-M542) se emitieron señales sinuosidades que producían vibraciones mediante una bocina de 300 watts (Cerwin Vega, XED650C). Para evaluar el estímulo vibratorio, las placas de cultivo se fijaron a una pantalla de acrílico de 3 mm adherida al cono de la bocina con seguros de resorte. Se aplicaron frecuencias de 20 y 60 Hz, calibradas a una amplitud de + 0.3 mm usando un acelerómetro (AX3, Axivity) de tres ejes, y un osciloscopio MD03032 (Tektronix). La amplitud se seleccionó con base en investigaciones previas en el campo utilizando equipos similares12. El acelerómetro capaz de medir vibraciones en tres dimensiones: eje X, eje Y, y eje Z, se fijó en la base de la placa de acrílico, registrando las vibraciones en una tasa de muestreo de 3200 Hz.
El desplazamiento producido se calculó utilizando el valor de la raíz del error cuadrado medio (RECM) y las equivalencias marcadas del calibrador y del acelerómetro. La ecuación utilizada para determinar el volumen óptimo en el amplificador de potencia para alcanzar la amplitud designada fue:
Donde D = desplazamiento (m), G = gravedad (constante a 9,81 m/s²), A = aceleración (g) y F = frecuencia (Hz).
Se utilizaron tres líneas celulares: osteoblastos (hFoB 1.19), células troncales mesenquimales derivadas de la pulpa dental (DPSCS) y de tejido gingival (GMSCS). Las MSCS fueron de un banco de células preexistente y han sido caracterizadas según los criterios de la Sociedad Internacional de Terapia Celular (ISCT)14. Las DPSCS y las GMSCS expresan altos niveles de los marcadores de superficie CD105, CD90 y CD73. También una alta expresión de CD13, y expresan niveles moderados de hla-abc, son negativas para la expresión de hla-dr y no expresan marcadores hematopoyéticos (CD34, CD45 y CD14) ni endoteliales (CD31). Las células presentan una morfología fibroblastoide y capacidad de diferenciarse hacia linajes adipogénicos, osteogénicos y condrogénicos14. La línea hFoB 1.19 fue adquirida de la atcc.
Las DPSCS y GMSCS se cultivaron en Medio Modificado Eagle de Dulbecco (DMEM), suplementado con 10% de suero fetal bovino (FBS), solución antibiótica-antimicótica al 1% y 2 mM de glutamina, e incubadas en condiciones estándar (37° C, 5% CO₂). Las células hFoB 1.19 se cultivaron en medio DMEM/F12, suplementado con 10% de suero fetal bovino y solución antibiótica-antimicótica al 1%, e incubadas en las condiciones antes mencionadas.
La estimulación vibratoria a 20 Hz o 60 Hz se realizó durante 20 minutos antes de sembrar las células en las placas de 12 pozos y se repitió a las 24, 48 y 72 horas, dentro de una campana de flujo laminar. Para el grupo control no vibrado (0 Hz), las placas de cultivo se dejaron 20 minutos en la campana de flujo laminar sobre la plataforma sin activarla.
Se evaluó la viabilidad celular mediante el ensayo de resazurina (10% de 44µm v/v) en medio base no suplementado, incubando las placas de cultivo por 4 h, con una densidad de 1,500 células/cm² para las MSCS y de 1,000 células/cm² para los osteoblastos (n = 9 muestras por condición). Los tiempos de medición fueron a las 24, 48 y 72 h. Se utilizó un pozo sin células, con medio de cultivo y resazurina, como blanco. Finalmente, la densidad óptica (d.o.) se midió a 570 nm.
Para evaluar la integridad de la membrana celular posterior a la estimulación vibratoria (a las 72 h de cultivo), se empleó la tinción de Calceína am (1µM) (InvitrogenTM Calcein am, Thermo Fisher Scientific Inc., Carlsbad, Estados Unidos) durante 10 min a 37º C. Las células se visualizaron utilizando un microscopio de Epi-fluorescencia (AmScope, Irvine, Estados Unidos). La cantidad de células por campo se contabilizó con ayuda del software ImageJ (NIH, Bethesda, Estados Unidos), cada fotografía del campo de interés se ajustó al umbral tipo Otsu, y se convirtió a 8 bits, y después a imagen binaria, seguido del plugin Watershed y se aplicó la función de Analizar partículas.
Finalmente, utilizamos una anova de una vía, seguida de la prueba de rango de Tukey con el fin de evaluar diferencias estadísticamente significativas entre los grupos examinados. Para lo anterior se utilizó el software Graph Pad Prism versión 10.3.1 (GraphPad Software, Inc., San Diego, Estados Unidos), y se consideró el valor de p≥0.05 como estadísticamente significativa.
RESULTADOS
Las vibraciones fueron exitosamente generadas por un dispositivo acústico diseñado para producir ondas sinusoidales con frecuencia y amplitud determinadas. La placa de cultivo recibía la vibración de manera vertical, con desplazamiento lineal respecto a la base estacionaria. Los registros de frecuencia y desplazamientos se muestran en la Tabla 1.
Tabla 1 Registro de frecuencia y cantidad de desplazamiento
| Frecuencia
Programada |
Promedio
registrado |
Máximo | Mínimo | Desplazamiento
rms |
Aceleración pico a pico | |
| Valor | Media | |||||
| 20 Hz | 19.95 Hz | 20.05 Hz | 19.83 Hz | 7.4 µm | 232 mV | 237 m |
| 60 Hz | 60.04 Hz | 60.41 Hz | 58.88 Hz | 6 µm | 202 mV | 196 m |
La generación de ondas sinusoidales con frecuencias de 20 Hz y 60 Hz afectó a todas las líneas celulares estudiadas. A las do del blanco se restaron a las do del ensayo de viabilidad celular de resazurina de todas las líneas celulares, incluyendo el grupo control. La estimulación vibratoria tuvo un efecto negativo en la viabilidad de los osteoblastos a las 24 horas, con una D.O. promedio de 0.5177 (DE ± 0.003) a 20 Hz y 0.4906 (DE ± 0.025) a 60 Hz, en comparación con el control, que presentó una D.O. de 0.5519 (DE ± 0.001). A las 48 horas, la viabilidad disminuyó aún más, con una D.O. de 0.3206 (DE ± 0.0659) a 20 Hz y 0.2270 (DE ± 0.0659) a 60 Hz, en comparación con el control, que tuvo una D.O. promedio de 0.6257 (DE ± 0.0072). A las 72 horas, la viabilidad se recuperó, mostrando una D.O. de 0.6508 (DE ± 0.0416) a 20 Hz, y 0.9066 (DE ± 0.0737) a 60 Hz, mientras el control fue de 0.7514 (DE ± 0.0351). Las diferencias y el análisis estadístico se presentan en la Figura 1. A.
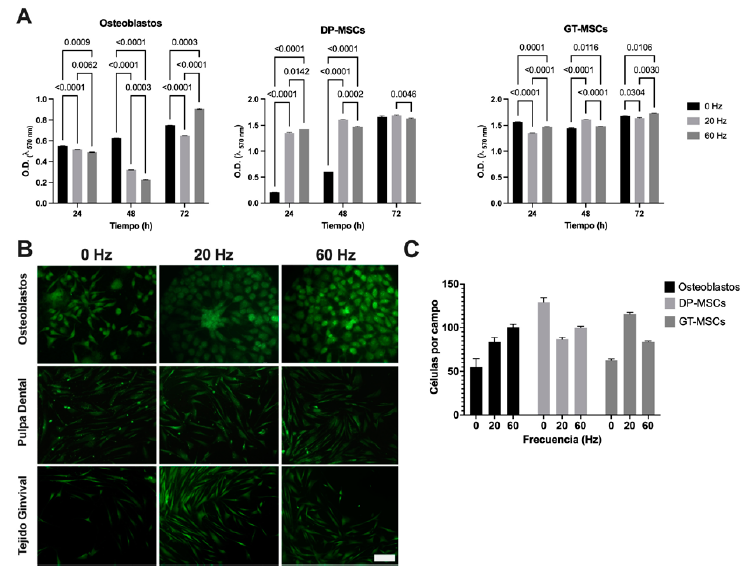
Figura 1 Efectos de las vibraciones in vitro. A. Se presentan los efectos en la viabilidad de los osteoblastos, las células mesenquimales de pulpa dental (DPSCS) y las células mesenquimales de tejido gingival (GMSCS) mediante el ensayo de resazurina. Los corchetes indican los resultados del análisis estadístico de ANOVA y Tukey post hoc. B. Imágenes representativas de la tinción fluorescente de Calceína am. La fluorescencia verde brillante indica resultado positivo, sin cambios en la viabilidad y la morfología celular a las 72 horas de cultivo tras el estímulo vibratorio. Los osteoblastos muestran agregados complejos y largas prolongaciones citoplasmáticas. Magnificación de 20X, barra de escala 50 µm. C. El recuento de células por campo se realizó mediante el software Image J en fotografías a una magnificación de 20X sin encontrar diferencias estadísticamente significativas. Por otro lado, a la examinación visual simple se observó un mayor número de células por campo en los grupos vibrados comparados con los no vibrados, se analizaron 9 campos (n=9) por condición experimental o control, después de 72 horas de cultivo. do Densidad Óptica.
Para las DPSCS, la estimulación vibratoria mejoró la viabilidad celular. A las 24 horas, se observó una d.o. promedio de 1.354 (DE ± 0.0115) a 20 Hz y 1.468 (DE ± 0.001) a 60 Hz, en comparación con el control que presentó una D.O. de 0.2116 (DE ± 0.00125). A las 48 horas, la viabilidad celular aumentó aún más, alcanzando una D.O. de 1.604 (DE ± 0.0072) a 20 Hz, 1.468 (DE ± 0.0156) a 60 Hz, comparado a la D.O. de 0.6117 (DE ± 0.0605) del control. Después de 72 horas, la viabilidad fue similar entre los grupos, observándose diferencias significativas solo entre los grupos de 20 Hz (D.O. 1.689) y 60 Hz (D.O. 1.631), mientras que el control mostró una D.O. de 1.660 (DE ± 0.0173).
Las GMSCS mantuvieron una viabilidad similar a lo largo de todos los tiempos de cultivo, presentando solo ligeras variaciones. A las 24 horas, la viabilidad presentó una D.O. de 1.354 (DE ± 0.0036) a 20 Hz y de 1.467 (DE ± 0.052) a 60 Hz, en comparación con el control, que mostró una D.O. de 1.571 (DE ± 0.410). A las 48 horas, la viabilidad aumentó mostrando una D.O. de 1.6083 (DE ± 0.0055) a 20 Hz y a 1.4826 (DE ± 0.0032) a 60 Hz, mientras que el control presentó una D.O. de 1.447 (DE ± 0.072). Finalmente, a las 72 horas, la D.O. de la viabilidad fue de 1.675 (DE ± 0.0141) en el control, de 1.641 (DE ± 0.0146) a 20 Hz y de 1.7283 (DE ± 0.040) a 60 Hz.
Los ensayos de viabilidad indicaron que las DPSCS tenían mayor actividad metabólica, mientras que las de GMSCS mostraron mayor estabilidad sin cambios bruscos. La observación microscópica mostró que las células permanecieron intactas y bien distribuidas. A las 72 horas, la tinción de Calceína-am demostró que la integridad de las membranas celulares en los grupos vibrados y no vibrados era similar (Figura 1. B y C), indicando que el estímulo vibratorio no contribuye sustancialmente ni afecta la adhesión de las células utilizadas en este estudio. Sin embargo, no se encontraron diferencias estadísticamente significativas entre grupos (Figura 1. C).
Los osteoblastos formaron estructuras intracelulares alargadas con la vibración a 20 Hz y en menor medida a 60 Hz (Figura 1. B). Las DPSCS y las GMSCS mantuvieron su forma fibroblástica, desarrollando extensas prolongaciones citoplasmáticas con la estimulación a 20 y 60 Hz. Estas extensiones facilitaron un mayor contacto célula-célula en los grupos experimentales, comparadas con el control.
DISCUSIÓN
Actualmente, pocos estudios abordan los efectos de la vibración en cultivo de células troncales mesenquimales (MSCS) derivadas de tejidos dentales15. A pesar de que la terapia vibratoria ya se está aplicando en el ámbito clínico odontológico, lo que hace crucial entender sus efectos para mejorar las terapias y planes de tratamiento4.
Los estudios realizados hasta la fecha se han centrado en la diferenciación osteogénica mediante osteoblastos o MSC de médula ósea, y en marcadores de estrés/inflamación celular en células epiteliales16,17. Los ensayos clínicos se enfocan en los efectos de la vibración sobre músculo y tejido óseo, encontrando que la terapia vibratoria tiene un efecto anabólico sobre el hueso, mejorando la consolidación de fracturas y aumentando la expresión de fosfatasa alcalina, osteocalcina, Col-1, Runx2 y Osterix18-20.
Dispositivos como el AcceleDent® han sido desarrollados para promover el movimiento dental ortodóntico mediante la estimulación vibratoria a 30 Hz, aun cuando los resultados son contradictorios4,7,21. Durante la resorción ósea, la matriz extracelular libera factores de crecimiento que reclutan MSCS para la remodelación ósea, un proceso regulado por las vías de señalización que implican la hormona paratiroidea y el factor de crecimiento tumoral beta (TGF-β)22. Las MSCS contribuyen a la regeneración ósea mediante su diferenciación hacia osteoblastos y secreción de factores paracrinos que promueven la angiogénesis, además de encargarse de reclutar células hematopoyéticas e inmunitarias al sitio de remodelación (Figura 2)16,23.
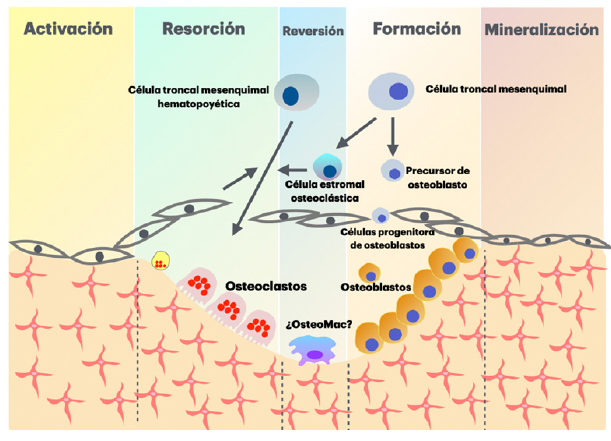
Figura 2 Proceso de remodelación ósea. Durante el proceso de resorción ósea, la mátriz extracelular del hueso libera factores de crecimiento que se encargan de reclutar MSCS de sitios residentes, y desde la médula ósea a los sitios de resorción, dando lugar a proceso de remodelación ósea, el cual ocurre entre etapas de formación y resorción. Osteomac es un término que se refiere a un subgrupo especializado de macrófagos que desempeñan un papel crucial en la homeostasis y remodelación ósea. Se piensa que los osteomac se encuentran relacionados con los osteoblastos y las células troncales mesenquimales en el microambiente óseo y colaboran en la formación y mantenimiento del hueso, así como en la cicatrización de fracturas.
Para estudiar los efectos de las vibraciones mecánicas en MSCS derivadas de tejidos dentales y osteoblastos, se desarrolló un sistema de vibración vertical caracterizado mediante un acelerómetro de tres ejes, confirmando que la vibración era perpendicular a la superficie de cultivo. Se observaron armónicos impares y frecuencias ligeramente superiores a las esperadas, posiblemente debido a resonancias mecánicas de la placa de acrílico, aunque estos no afectaron el desplazamiento de los pozos de cultivo. Esta caracterización permitió evaluar directamente los efectos vibratorios in vitro.
En un entorno inflamatorio, los estímulos mecánicos influyen significativamente en la actividad de las MSCS y osteoblastos durante la remodelación ósea10. Comprender la interrelación entre las MSCS, las moléculas de señalización y el microambiente óseo es esencial para desarrollar terapias efectivas para la reparación ósea. Nuestro estudio presenta un modelo in vitro capaz de replicar estímulos mecánicos contribuyendo a un mejor entendimiento de los procesos relacionados con la terapia vibratoria.
La estimulación vibratoria sinusoidal a 20 y 60 Hz tuvo efectos en todas las líneas celulares estudiadas. Inicialmente, hubo efectos negativos en la viabilidad de los osteoblastos, los cuales se regularizaron después de 72 horas, subrayando la importancia de la mecanosensitividad en la arquitectura ósea. Estudios similares reportan que las frecuencias entre 30 y 90 Hz no causan efectos tóxicos sobre osteoblastos in vitro y activan la vía del receptor de estrógeno α24. También estimulan la osteogénesis en MSCS derivadas de médula ósea y tejido adiposo, con mayores efectos observados entre 40 y 50 Hz11,24.
En las MSCS derivadas de la pulpa dental (DPSCS) y MSCS derivadas de tejido gingival (GMSCS), la estimulación vibratoria tuvo efectos positivos sobre la viabilidad, siendo más notable en DPSCS a 60 Hz. En tanto, las GMSCS mostraron respuestas similares entre el grupo no vibrado y los vibrados, debido quizás a que el tejido gingival tiene una mayor exposición a estímulos físicos y químicos por lo que podría ser más resistente a la estimulación mecánica. Los efectos observados en las DPSCS sugieren que la terapia vibratoria podría prevenir cambios en la pulpa dental durante el tratamiento ortodóntico. Por consiguiente, se propone la modificación de las frecuencias utilizadas para evitar posibles efectos secundarios25,26.
Se ha observado que las vibraciones entre 30 y 90 Hz estimulan la diferenciación osteogénica de las MSCS y las frecuencias de 30 Hz inducen la expresión de rankl a través de la vía de la ciclooxigenasas y prostaglandina 2 (COX/PGE2), moléculas relacionadas con el dolor27. Lo anterior podría justificar el uso de dispositivos vibratorios para controlar el dolor durante los tratamientos de ortodoncia.
El proceso de diferenciación osteoblástica incluye proliferación, depósito, y maduración y mineralización de la matriz extracelular (Figura 2), lo cual requiere de procesos de proliferación y migración celular. Estudios en MSCS de ligamento periodontal muestran que la vibración de baja magnitud y alta frecuencia promueve proliferación, migración y diferenciación osteogénica15. En el presente estudio, pese a que no se encontraron diferencias estadísticas entre el número de células por campo entre grupos vibrados y no vibrados, sí se observó que tanto los osteoblastos como las MSCS se distribuyen abordando áreas más extensas en el plato de los grupos vibrados, por lo que la estimulación podría tener efectos sobre la migración celular, lo que requiere un estudio más a profundidad. Igualmente, tanto las MSCS como los osteoblastos formaron estructuras intercelulares extensas, reflejando una característica fenotípica de arquitecturas complejas, similar a lo que ocurre en el tejido óseo28,29.
Los estudios in vitro muestran variabilidad en los parámetros utilizados, dificultando conclusiones definitivas10,30. No obstante, magnitudes por debajo de 1 gravedad y frecuencias entre 20 y 100 Hz estimulan la diferenciación osteogénica en MSCS10,16,31. Una de las limitantes de nuestro estudio fue que no se estudiaron tanto los cultivos en condiciones de diferenciación, o por un periodo más largo de tiempo, por lo que sería importante explorar los efectos de la vibración bajo diferentes condiciones de diferenciación en las células estudiadas.
CONCLUSIÓN
Los resultados de este estudio, junto con investigaciones previas, sugieren que las vibraciones de baja magnitud y alta frecuencia pueden ser un tratamiento no invasivo y económico en ortodoncia. En particular la frecuencia de 20 y 30 Hz, que es la sugerida para la utilización de dispositivos como AcceleDent® parece ser la adecuada para el tejido óseo. Se necesitan estudios más extensos que aborden los efectos de la terapia en MSCS derivadas de tejidos dentales, para conocer los mecanismos por los cuales esta terapia influye en la biología celular de la remodelación ósea, así como un mayor número de ensayos clínicos para optimizar los protocolos de su aplicación.











 texto en
texto en 


