Introducción
El plomo (Pb) es un metal clasificado como tóxico aún a bajas concentraciones y de extensa distribución en el ambiente debido a su amplio uso industrial (WHO, 2010). Su eliminación en la gasolina y los convertidores catalíticos disminuyeron su dispersión atmosférica (Soto-Jiménez et al., 2006); pero aún existen procesos de contaminación con Pb como el reciclaje de baterías para autos, curtido de cuero, alfarería y la minería, que pueden incidir en los riesgos de intoxicación (Caravanos et al., 2016). Diversos estudios han demostrado que la principal causa de intoxicación por Pb en algunas partes de México, es el uso de cerámica vidriada con óxido de Pb o “greta” (Chaudhary et al., 2003; Estrada-Sánchez et al., 2017; Olympo et al., 2017); esto a pesar de que está prohibido en la elaboración de utensilios de barro de acuerdo a la la NOM-231-SSA1-2016 (Secretaría de Salud, 2016). El uso frecuente de utensilios de barro vidriado con Pb (UBPb) en la preparación de alimentos se ha asociado con la concentración de Pb en la sangre (PbS) de los niños mexicanos, predominando sobre otros hábitos como consumir dulces potencialmente contaminados, chupar objetos o comer pintura (Farías et al., 2014).
La mayoría de los estudios sobre intoxicación alimentaria con Pb en México se han realizado en regiones alfareras, pero no hay estudios sobre el riesgo de intoxicación con Pb en otras regiones, como las turísticas que utilizan mucho estos utensilios por ser parte del folklor mexicano como símbolo de complemento a la cocina regional. Tal es el caso de los poblados del río Sonora, que es un corredor turístico, actividad que fue afectada por un derrame de lixiviados en 2014 causando la dispersión de metales en las aguas superficiales y subterráneas, sedimentos y organismos que forman parte del ecosistema (Luque-Agraz et al., 2019). Después del derrame, se reportaron enriquecimientos de varios metales en agua y organismos a lo largo de la cuenca del río, que fueron asociados al derrame (Romo-Morales et al., 2020; SEMARNAT, 2023). Esto puede implicar que elementos como el Pb pueden estar siendo dispersados en esa región.
La exposición al Pb es asociada con un amplio espectro de enfermedades como anemia, daño neurológico, enfermedades cardiovasculares, insuficiencia renal, hipertensión, infertilidad y abortos (WHO, 2010). Los niveles de PbS indican exposición reciente y es un biomarcador usado para estimar posibles riesgos a la salud (Hsieh et al., 2017). En niños, los niveles de PbS se asocian con disminución del coeficiente intelectual (CI) (Estrada-Sánchez et al., 2017) y en bajas concentraciones se asocia a deficiencias neurológicas irreversibles, por lo que se considera que no existe una cantidad de PbS que sea segura (CDC, 2012). El consumo de hierro (Fe) y calcio (Ca) ha demostrado tener un efecto antagonista a los efectos del Pb, ya que limitan su absorción, transporte y almacenamiento o en el organismo, por lo que una baja ingesta de estos nutrientes puede aumentar el riesgo de intoxicación con Pb en personas expuestas (Ahamed et al., 2007; Liu et al., 2015). Se estima una deficiencia en el consumo de Fe y Ca en la población mundial de 66 y 65 %, respectivamente (Passarelli et al., 2024). En México, la ingesta promedio de Ca se estima en 805 mg d-1 en adultos, por debajo de la ingesta diaria recomendada (IDR = 1000 mg día-1) (Balk et al., 2017), mientras la deficiencia de Fe en mujeres de 12-49 años tiene una prevalencia de 35.5 % y en niños preescolares y escolares es de 19.6 % y 21.1 %, respectivamente. Además, el bajo consumo de Fe y Ca trae consigo el riesgo de padecer enfermedades asociadas a su deficiencia como osteoporosis y anemia (Shamah-Levy et al., 2023). Por lo anterior, el problema de la exposición al Pb es de gran relevancia en poblaciones que manifiestan tener efectos por la exposición a metales asociados a actividades mineras, exposición que puede incrementarse por el uso de UBPb para elaborar alimentos, que junto con la deficiencia del consumo de Fe y Ca, puede incidir en la posibilidad de intoxicación y los efectos derivados. El objetivo de este estudio fue detectar la presencia de UBPb y como éstos influyen en la cantidad de Pb en alimentos y sangre de las personas que los consumen para identificar fuentes, incluyendo hábitos de alimentación y de exposición al Pb, que representan un riesgo de intoxicación con este elemento en poblaciones no alfareras, pero que pertenecen a una zona que es un corredor turístico en la que se emplean utensilios de barro.
Materiales y métodos
Tipo de estudio y población
Es un estudio de tipo transversal y descriptivo ya que se midió la exposición al Pb en una muestra poblacional en un momento determinado, se identificaron UBPb y se cuantificó Pb en alimentos preparados en esos utensilios, agua y sangre en habitantes de algunos poblados ubicados en la cuenca del río Sonora. Se realizó un muestreo poblacional estratificado seleccionando 49 hogares distribuidos en las poblaciones de Aconchi, Baviácora, Huépac, San Felipe de Jesús, San José de Baviácora y Hermosillo.
Criterios de inclusión y consentimiento informado
Para este estudio se incluyeron pobladores que emplean utensilios de barro vidriado para preparar (cocinar, servir o almacenar) alimentos y aceptaron participar voluntariamente. Se excluyeron aquellos que solo emplean los utensilios de barro como ornato. Después de confirmar la utilización de utensilios de barro, se solicitó el consentimiento para realizar la prueba cualitativa del rodizonato in situ y posteriormente una muestra de algún alimento elaborado en ese utensilio, agua con la que preparan los alimentos, ya sea del grifo o purificada, y una muestra de sangre a cada voluntario. Previo al muestreo, se proveyó un consentimiento informado sobre el análisis clínico, el manejo de las muestras y de la información obtenida de los estudios el cual fue avalado por el comité de ética del Centro de Investigación en Alimentación y Desarrollo A.C. (Registro: CONBIOÉTICA-26-CEI-001-20200122 CEI/004-2/2024)
Encuestas sobre información nutricional y fuentes de contaminación con Pb
Mediante una entrevista estructurada se recabó información sobre la ingesta de alimentos, frecuencia de consumo y hábitos de exposición al Pb. Se realizó un recordatorio de 24 h (R-24h) para evaluar el consumo de alimentos y cuantificar el consumo de Fe y Ca. Esta evaluación consiste en interrogar a la persona sobre todo lo que ingirió el día anterior, sólidos y líquidos, para conocer las cantidades de alimentos, horario de las comidas, nombre del platillo, los ingredientes, la cantidad consumida y quien lo preparó (Suverza-Fernández y Haua-Navarro, 2010). Posteriormente se obtiene la cuantificación energético-nutrimental de esos alimentos tomando como modelo el sistema mexicano de alimentos equivalentes (SMAE) (Pérez-Lizaur et al., 2022). La entrevista incluye un cuestionario de frecuencia de consumo de alimentos, para conocer la frecuencia del consumo de estos dos minerales. Al entrevistado se le mencionan los diferentes alimentos y bebidas, naturales o procesados cuyo consumo se categorizan en diario, semanal, a veces o nunca; para catalogar los hábitos de alimentación como buenos, regulares y malos (Suverza-Fernández y Haua-Navarro, 2010). Adicionalmente, se recabó información sobre las posibles fuentes de contaminación con Pb en el hogar (uso de utensilios de barro, uso de juguetes, consumo de dulces, tipo de tuberías y la antigüedad de la casa), hábitos de alimentación y enfermedades asociadas al Pb (anemia, enfermedades, renales, cardiovasculares, etc.).
Prueba cualitativa rápida para detección de UBPb (método de rodizonato)
La detección rápida de Pb en utensilios de barro vidriado se realizó por el método sugerido por la SEDESOL y la FONART (Covarrubias-Pérez y Estrada-Sánchez, 2010). Se analizaron todos los utensilios de cocina que se emplean para cocinar, almacenar o servir alimentos de cada hogar participante. Se emplearon materiales y reactivos de laboratorio adaptados para realizar la prueba de detección de Pb in situ. En un tubo de ensayo con 5 mL de vinagre blanco comercial (pH≈3), se agregó una cantidad pequeña de rodizonato de sodio (Sigma-Aldrich, Austria) (aproximadamente 0.25 g) y se mezcló para obtener una solución indicadora de color amarillo; luego, se humedeció un hisopo con la solución indicadora y se frotó sobre la superficie de la pieza de barro esmaltado que tiene contacto con el alimento. La presencia de un viraje de color de amarillo a rojo en el hisopo es indicadora de la presencia de Pb.
Muestreo
Se recolectaron 55 muestras de alimentos sólidos y líquidos de las cuales 49 fueron cocinados, servidos o almacenados en utensilios de barro y 6 en utensilios que no son de barro, para cuantificar el contenido de Pb. Las muestras fueron transportadas al laboratorio en hieleras, se les midió el pH con potenciómetro de mesa y se almacenaron en congelación a -20 ºC hasta su posterior procesamiento y análisis. Las muestras de alimentos se procesaron de acuerdo con la Norma Oficial Mexicana NOM-117-SSA1-1994 (Secretaría de Salud, 1994). Para recolectar las muestras de sangre, se hizo una punción venosa del antebrazo utilizando el kit Vacutainer® para recolectar de 2 a 4 mL de sangre en un tubo con anticoagulante EDTA y las muestras fueron refrigeradas para su posterior análisis.
Preparación y análisis de las muestras
Las muestras de alimento sólidas fueron homogenizadas y se pesaron 1.25 ± 0.003 g en un vaso de digestión, se agregó 6 mL de ácido nítrico (HNO3) (Sigma-Aldrich, Austria) concentrado y se reposó a temperatura ambiente por 24 h; luego se agregó 1 mL de peróxido de hidrógeno (H2O2) al 30 % (Sigma-Aldrich, Austria) y se calentó a 100 °C por 1 h; se enfrió y se filtró en papel filtro libre de cenizas (Whatman #41). Finalmente se aforó a 10 mL con agua grado HPLC. Las muestras de alimentos líquidos se procesaron similarmente excepto que se usaron 5 mL de muestra, no se filtró y se aforó a 15 mL. La digestión de las muestras de sangre consistió en agregar 2 mL de HNO3 concentrado a 0.5 mL de muestra de sangre en un vaso de digestión, se calentó a 120 °C por 1 hora, se enfrió y se aforó a 10 mL con agua grado HPLC. En el caso de las muestras de agua, 50 mL de agua se acidificaron (pH≈2) con 50 µL de ácido nítrico (HNO3) concentrado para posteriormente refrigerarse previo a su análisis. Las muestras digeridas fueron cuantificadas para Pb usando un espectrofotómetro de absorción atómica (EAA; Varian SpectrAA 240 FS, Victoria, Australia) con una flama de aire-acetileno (muestras de alimentos) y acoplada a horno de grafito (muestras de agua y sangre).
Control de calidad
Como control de calidad, se evaluó la exactitud del método de determinación de Pb en las muestras de alimento y sangre comparando el porcentaje de recuperación el cual deriva de la relación entre el valor promedio experimental obtenido y el valor de referencia o teórico. Para su estimación, se prepararon muestras fortificadas con estándar de Pb (Sigma-Aldrich, Austria) y un estándar certificado (NIST-1577b, hígado bovino del Instituto Nacional de Estándares y Tecnología de EU). Las muestras fortificadas se prepararon al agregar 200 µL de una solución estándar de 100 µg mL-1 de Pb a la muestra seleccionada (sólida o líquida), para ser digerida como se describió anteriormente; luego se aforó para una concentración final de 2 µg g-1. El estándar certificado se preparó de acuerdo con las especificaciones del proveedor.
Análisis de prevalencias
Debido a que este estudio es de tipo transversal, se comparó la razón de prevalencia de los niveles de PbS por encima de los valores de referencia establecidos por la Norma Oficial Mexicana NOM-199-SSA1-2000 (Secretaría de Salud, 2002) (5 g dL-1 para menores de 15 años y 25 µg dL-1 para adultos no expuestos) entre los pobladores que usan UBPb y los que no. Las prevalencias se calcularon de acuerdo a la razón de proporciones (RP) sugerido por Sánchez et al. (2011) y con un intervalo de confianza del 95 % como se indica en la Tabla 1. También se comparó la presencia de enfermedades asociadas a la intoxicación con Pb entre las personas con cantidad de PbS por encima de los valores de referencia y las que no. Dichas enfermedades se clasificaron como padecimientos crónicos (enfermedades cardiovasculares y renales, anemia, hipertensión, abortos e infertilidad) (ATSDR, 2020) y agudos (dolor o inflamación abdominal, diarrea, náusea o vómito, convulsiones, pérdida de memoria y/o problemas para concentrarse), estos últimos asociados a síntomas clínicos en una intoxicación con Pb (WHO 2010). Las personas con cantidades de PbS mayores a los valores de referencia se consideraron como “expuestos” y aquellas con cantidades menores como “no expuestos”. Como “enfermos” se consideró a los encuestados que refirieron padecer o haber padecido, ellos o algún miembro de la familia, alguna enfermedad asociada con la intoxicación con Pb y como “sanos” a los que no. De igual forma se comparó la razón de prevalencia de las mismas enfermedades entre las personas que están expuestas otras posibles fuentes de contaminación con Pb como el uso de UBPb, el uso de juguetes de economía informal, consumo de dulces potencialmente contaminados, que tengan casas con más de 40 años de antigüedad y/o tengan tuberías metálicas, de lo contrario, se consideraron como “no expuestos”.
Table 1: 2 X 2 table for calculating odds ratio.
| Enfermos | Sanos | Total | |
| Expuestos | a | b | a+b |
| No expuestos | c | d | c+d |
| Total | a+c | b+d | a+b+c+d |
| ecuación | |||
| 95% IC* | |||
1 La razón de proporciones determinada en un estudio transversal, se denomina razón de prevalencias (Sánchez et al., 2011). *Intervalo de confianza: IC 95 % = Ln RP ± 1.96 * Error Estándar, donde 1.96 = constante fija para 95 % cuando n > 30.
Análisis estadístico
El contenido de Pb en las muestras de alimento y sangre en los diferentes grupos, así como la ingesta de Fe y Ca se sometieron a pruebas de normalidad usando pruebas de Shapiro-Wilks. La comparación entre el contenido de Pb en las muestras de alimento y sangre entre los diferentes poblados, así como entre personas expuestas y no expuestos al Pb en utensilios de barro se realizó por un análisis de varianza (ANOVA) usando la prueba no paramétrica de Kruskal-Wallis. La comparación de la ingesta de Fe y Ca entre poblados, expuestos y no expuestos a Pb en utensilios de barro se realizaron con un ANOVA paramétrico y la correlación entre las concentraciones de PbS con alimentos e ingesta de Fe y Ca se realizó mediante la prueba de Pearson. Todos estos análisis fueron realizados con el paquete estadístico del software Minitab®.
Resultados y discusión
Datos poblacionales
Las personas que participaron en este estudio (n = 49) fueron de las poblaciones de Aconchi (n = 11), Baviácora (n = 16), Hermosillo (n = 8), Huépac (n = 7), San Felipe de Jesús (n = 5) y San José de Baviácora (n = 2). La edad promedio de los participantes fue de 52.0 ± 13.6 años, con el mayor porcentaje de participación (38.8 %) en el intervalo de 50 - 59 años. Los encuestados son principalmente mujeres, generalmente amas de casa (92.0 %), mientras que solo el 8.2 % fueron hombres. Ocho participantes no utilizan barro vidriado para elaborar alimentos y dos participantes se reusaron a entregar muestra de alimentos.
Método de rodizonato (prueba cualitativa rápida)
La prueba in situ con rodizonato de sodio permite detectar cualitativamente la presencia de Pb en utensilios de barro y fue utilizada como herramienta de clasificación de los participantes como expuestos y no expuestos al Pb. Se analizaron un total de 61 utensilios de barro vidriado que son utilizados para preparar alimentos y pertenecen a 36 de los hogares participantes, ya que en algunos hogares emplean más de un utensilio. Se excluyeron todos aquellos utensilios que no sean usados para elaborar, servir o almacenar alimentos. Del total de los utensilios de barro analizados, 49 (80.3 %) fueron positivos y 12 (19.7 %) fueron negativos a la presencia de Pb (Tabla 2). La mayoría de los utensilios fueron adquiridos hace más de tres años por lo que, a pesar de que el esmalte vidriado se va desgastando con el tiempo, fue posible la detección de Pb mediante esta prueba.
Tabla 2 Proporción de utensilios de barro con y sin Pb en las poblaciones y niveles de Pb en alimentos y sangre de los participantes 1.
Table 2: Proportion of lead and lead-free clay utensils and Pb levels in food and participants blood in the different towns.
| Poblado / participantes | Utensilios | Pb en | Pb en |
| de barro | alimentos | sangre | |
| con / sin Pb | (µg g-1) | (µg dL-1) | |
| Aconchi (n=11) | 17/3 | 3.08a ± 3.05 | 18.6a ± 5.73 |
| Baviácora (n=16) | 16/2 | 3.19a ± 3.77 | 13.2b ± 4.40 |
| Hermosillo (n=8) | 1/2 | 1.69a ± 0.18 | 48.8c ± 24.38 |
| Huépac (n=7) | 4/1 | 2.17a ± 1.83 | 12.5ab ± 9.05 |
| San Felipe de Jesús (n=5) | 10/4 | 2.95a ± 1.32 | 16.5ab ± 6.69 |
| San José de Baviácora (n=2) | 1/0 | 3.36a ± 2.92 | 10.8ab ± 9.44 |
| Total | 49/12 | - | - |
1. Diferente letra en el superíndice indica diferencia significativa a p < 0.05.
Los UBPb empleados para elaborar alimentos pertenecen a 30 (83.3 %) de los hogares participantes, mientras que en los otros 6 hogares (16.6 %) usan utensilios negativos a la presencia de Pb. Por lo tanto, se encontró que prácticamente 8 de cada 10 hogares que emplean utensilios de barro vidriado están expuestos a la presencia de Pb en sus alimentos. Este resultado supera el porcentaje de UBPb reportado en un estudio realizado en Hermosillo, Sonora, donde se detectó Pb en 67 de 217 (30.9 %) utensilios de distintos hogares por el mismo método (Ortiz, 2023). Sin embargo, es necesario un muestreo más grande y representativo de cada poblado para obtener datos más precisos que permitan estimar el grado de exposición en esta región que pertenece al norte del país donde la prevalencia de intoxicación con Pb por el uso de utensilios de barro es la mitad de la prevalencia a nivel nacional (Téllez-Rojo et al., 2019). La prueba in situ con rodizonato de sodio y vinagre blanco para detectar UBPb es un método confiable, sencillo y económico que puede ser utilizada para descartar utensilios de barro sin Pb en estudios de asociación para obtener prevalencias más precisas.
Contenido de Pb en alimentos
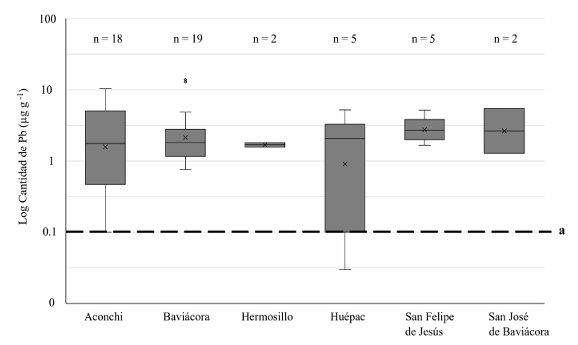
Se recolectaron un total de 55 muestras de todos los participantes, ya que algunos de ellos otorgaron más de una muestra por utilizar más de un utensilio de barro en la preparación de alimentos. También se recolectaron seis muestras de alimento de participantes que no emplean utensilios de barro para preparar alimentos y se consideraron como control negativo. En la validación del método de digestión y cuantificación de Pb mediante la fortificación de muestras se obtuvo un intervalo de 77 - 105 % de recuperación y en la validación mediante el estándar certificado de hígado bovino 1577b se obtuvo una recuperación de 106 ± 4.38 % (Tabla 3), estos valores se consideran aceptables en este tipo de métodos (Martínez-Durazo et al., 2023). El valor promedio de la concentración de Pb en los alimentos fue de 2.95 ± 2.97 µg g-1 (0.03-13.9 µg g-1) y no hubo diferencia significativa en las cantidades de Pb en alimentos entre los diferentes poblados (Tabla 2). La mayoría de las muestras (51 de 55) presentaron valores superiores a los 0.1 µg g-1 (Figura 1), valor límite para regulaciones internacionales para diferentes tipos de alimentos (USDA, 2012; Unión Europea, 2017). Cantidades similares de Pb (promedio 0.10 mg kg-1) fueron reportadas en otro estudio donde analizaron 48 muestras de alimento preparados con salsa ragú que contiene carne de jabalí obtenida de la caza deportiva (Lenti et al., 2021), lo cual indica valores aproximados de Pb en alimentos preparados expuestos a contaminación ambiental. Aunque no existen datos precisos sobre las cantidades de Pb permisibles en alimentos preparados, se han reportado niveles de PbS de 2.5 µg dL-1 en ratas que fueron expuestas a cantidades de hasta 100 µg Pb L-1 en limonada preparada en utensilios de barro (Díaz et al., 2016). La acidez facilita la lixiviación de Pb, aumentando su concentración en alimentos ácidos, pero en este estudio, el pH promedio de los alimentos analizados fue de 6.08, lo cual sugiere que las concentraciones de Pb pudieran ser mayores a medida que aumente la acidez de los alimentos que son preparados, almacenados y/o posteriormente calentados en estos mismos utensilios (Villalobos et al., 2009).
Figura 1: Cantidad de Pb en alimentos de diferentes poblaciones (ajustada Log y + 10). a) La línea gruesa punteada indica el valor máximo permitido por la Unión Europea (2017) y la Administración de Drogas de Estados Unidos (USDA, 2012).
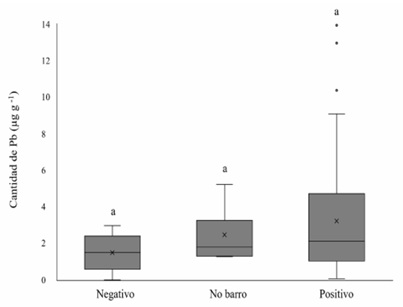
Este estudio se enfocó en determinar el contenido de Pb en alimentos preparados y servidos en UBPb; sin embargo, se detectaron niveles de Pb por encima de los valores de referencia en 5 alimentos preparados en utensilios de barro sin Pb y en 6 alimentos preparados en otro tipo de utensilios. Esto indica que la fuente de Pb en los alimentos es variada y no exclusiva del barro vidriado. Aunado a esto, y aunque la concentración promedio de Pb en alimentos preparados en UBPb (2.36 µg g-1) fue mayor al promedio determinado en alimentos preparados en utensilios negativos a Pb (1.8 µg g-1), no se encontraron diferencias significativas entre ambos grupos (p = 0.380). Asimismo, tampoco se determinaron diferencias significativas entre las concentraciones de Pb en alimentos preparados en barro y las concentraciones de Pb en alimentos preparados en otro tipo de utensilios diferentes a los de barro (p = 0.448) (Figura 2). Esta heterogeneidad en la distribución de Pb en los alimentos puede deberse a varias fuentes de Pb que han sido documentadas como la movilización de polvos que contaminan los alimentos o a la presencia de niveles altos de Pb en sedimentos y alimentos como los berros en algunas regiones del río Sonora (Del Rio et al., 2012; Romo et al., 2020).
Contenido de Pb en agua
Con el propósito de descartar el agua utilizada para la elaboración de alimentos como fuente de Pb, se recolectaron un total de 53 muestras de agua con la que los participantes dijeron preparar sus alimentos, algunos de ellos proveyeron una sola muestra de agua, ya sea purificada o de grifo, y algunos proveyeron ambos tipos de agua. Los niveles de Pb fueron no detectables en todas las muestras de agua, indicando que esta no es una fuente del elemento. Esto concuerda con el Dictamen Diagnóstico Ambiental 2023 realizado por la Secretaría de Medio Ambiente y Recursos Naturales (SEMARNAT, 2023) en el que no se reportaron niveles detectables de Pb y otros metales tóxicos en el agua de diferentes fuentes de diversos poblados del río Sonora. En un estudio en el que se analizó la calidad del agua del río Sonora en el periodo 2014 - 2019, se reportaron solamente 6 de 3040 muestras de agua subterránea con Pb por encima del límite permitido 0.01 mg L-1 y ninguna muestra pertenecía a alguno de los poblados evaluados en este estudio (Díaz-Caravantes et al., 2024). Adicionalmente, el consumo de agua purificada aumentó de 14 a 84 % después del derrame de lixiviados en el 2014 (Luque-Agraz, 2019), lo cual se confirma en este estudio donde la mayoría (62.26 %) utiliza agua purificada para elaborar los alimentos, mientras que el resto utiliza agua del grifo o de manantial. Por lo tanto, considerando que la mayoría del agua potable concesionada para riego y suministro urbano es agua subterránea limpia, la eliminación de metales se salvaguarda mediante los procesos de potabilización y el uso preferente de agua purificada para preparar alimentos.
Detección de PbS
Se recolectaron muestras de sangre de 50 participantes (38 mujeres, 12 hombres y 2 menores de edad). La concentración media de PbS entre los pobladores analizados fue de 21.5 ± 18.5 µg dL-1, pero en 13 participantes, los niveles de PbS estuvieron por encima de los valores límites recomendados (5 µg dL-1 para menores y 25 µg dL-1 para adultos) (Secretaría de Salud, 2002). Este valor de PbS obtenido es similar al valor promedio reportado (19.63 µg dL-1) en la recolección de datos de 56 muestras de sangre de 62 sitios diferentes de México hasta el 2012 (Caravanos et al., 2016). Aunque se necesita más evidencia sobre los niveles de PbS en la población adulta y su asociación con el estado de salud (Pfadenhauer et al., 2016), es importante señalar que en niveles de PbS inferiores al límite máximo existen riesgos en la salud, ya que por cada 5 µg dL-1 de PbS, aumenta 1.25 mmHg la presión sanguínea y el riesgo relativo (RR) es mayor de 1 para enfermedades cardiovasculares (Fewtrell et al., 2004).
Hubo diferencias significativas (p = 0.008) al comparar la cantidad de PbS entre la población de Hermosillo (promedio 48.8 ± 24.38 µg dL-1) y la de los poblados rurales (Aconchi: 18.6 ± 5.73 µg dL-1; Baviácora (13.2 ± 4.4 µg dL-1; Huépac: 12.5 ± 9.05µg dL-1; San Felipe de Jesús 16.5 ± 6.69 µg dL-1; y San José de Baviácora: 10.8 ± 9.44 µg dL-1). La concentración promedio de PbS entre los diferentes poblados rurales no tuvo diferencia significativa (p > 0.05) excepto entre Aconchi y Baviácora (p = 0.04) (Tabla 2). Este resultado contrasta con lo observado en un metaanálisis que recolectó datos en pobladores mexicanos hasta el año 2010, en el que reportaron promedios de PbS menores en áreas urbanas (8.8 µg dL-1) que en poblaciones rurales (22.2 µg dL-1). Esto se debe a que en el metaanálisis se consideraron estudios realizados en poblaciones rurales en las que se practica la alfarería, mientras que esta actividad no se realiza en los poblados del río Sonora. A pesar de esto, los niveles de PbS de los poblados rurales en nuestro estudio (intervalo de 13.2-18.6 µg dL-1; Tabla 2) son similares a los niveles de PbS de adultos (10.9 µg dL-1) obtenidos en dicho metaanálisis (Caravanos et al., 2014). Por otro lado, los altos niveles de PbS en pobladores de Hermosillo, indica que se debe considerar la exposición a otras fuentes del elemento, posiblemente relacionadas con la industrialización (Del Río et al., 2012).
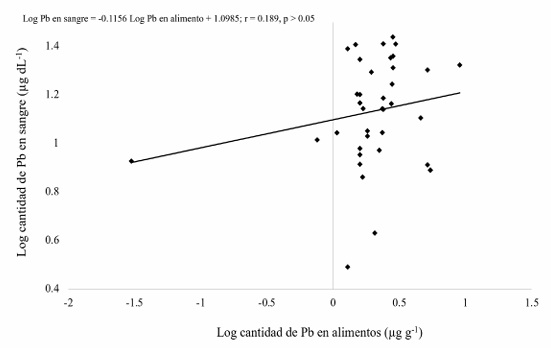
Los niveles de PbS de participantes expuestos por el uso de barro vidriado con y sin Pb no mostraron diferencias significativas (p = 0.11), lo que refuerza la afirmación de que el barro vidriado no es la fuente única del elemento. Como se mencionó anteriormente, los niveles de Pb en los alimentos estuvieron por encima de dos regulaciones internacionales, pero solamente presentaron una débil correlación positiva con los niveles de PbS (Figura 3; r = 0.19) la cual no fue significativa (p = 0.25). Por lo tanto, es imperativo un mayor muestreo para obtener una correlación significativa entre el Pb en alimentos y PbS, como lo reportado en otro estudio donde se observó un cambio moderado del 3 % en la cantidad de PbS en 353 niños por el consumo de dulces contaminados con Pb (Tamayo y Ortiz et al., 2016).
Evaluación dietética de Fe y Ca
Respecto a la evaluación de la frecuencia de consumo de alimentos, los participantes tienen una baja ingesta de alimentos ricos en Fe, ya que solo el 12 % los consumen diariamente, 24 % semanalmente, 33 % en ocasionalmente y 31 % no los consumen nunca. Respecto a la ingesta de alimentos ricos en Ca, solo el 11% de los entrevistados los consumen diariamente, 29 % semanalmente, 35 % ocasionalmente y 25 % no los consumen nunca. Los buenos hábitos de alimentación son aquellos donde los alimentos son variados con respecto a los diferentes grupos alimenticios, mientras que en los malos hábitos la variedad de grupos de alimentos es poca, el 55 % de los hábitos de alimentación entre los participantes son malos mientras que el 45 % restante demostró hábitos regulares.
Para determinar si los participantes cumplen con la IDR de Fe y Ca, se estimaron las cantidades de estos minerales en los alimentos reportados en el R-24h y se compararon con la IDR de referencia. La cuantificación energético-nutrimental de los alimentos con base en el SMAE indicó que el 82 % (n = 40) de los encuestados no logran cubrir la IDR de Fe (18 %, n = 9, sí lo cubre). La determinación de la IDR de Fe de cada participante se basó tanto en la edad como en el sexo (18 mg día-1 para las mujeres adultas y 8 mg día-1 para hombres adultos maduros y adultos mayores de ambos sexos). Respecto al Ca, el 87.7 % (n = 43) de los encuestados no logran cubrir la IDR (12.2 %, n = 6, sí lo cubre). La determinación de la IDR de Ca de cada participante también se basó en la edad y sexo (1200 mg día-1 para las mujeres adultas y 1000 mg día-1 para hombres adultos maduros y los adultos mayores de ambos sexos). Se ha estimado que el 65 % de la población mundial no consume suficiente cantidad de Fe y el 66% no consume la cantidad suficiente de Ca (Passarelli et al., 2024), lo que es superado por lo encontrado en este estudio. Esto sugiere que puede aumentar el riesgo de intoxicación con Pb, debido a que el 80% de los hogares están expuestos por consumir alimentos preparados en UBPb, y están desprovistos de una cantidad suficiente de estos dos minerales que ejercen un efecto antagónico y protector a dicho elemento (Ahamed et al., 2007).
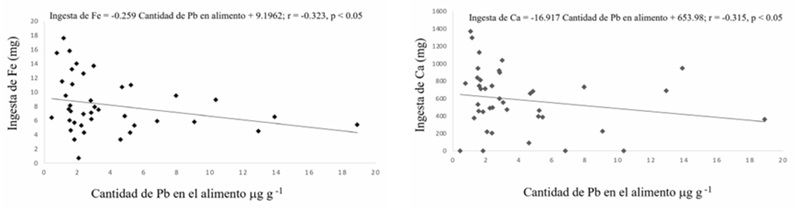
Aunque la ingesta de Fe y Ca entre quienes usan utensilios de barro vidriado negativos al Pb y los que usan UBPb no fue diferente significativamente (p > 0.05), se determinaron correlaciones negativas significativas entre la cantidad de Pb en alimentos y la ingesta de Fe (r = - 0.32; p < 0.05), y también con la ingesta de Ca (r = -0.31, p < 0.05) (Figura 4). Esto también soporta que el riesgo de intoxicación con Pb puede aumentar por la baja ingesta de estos nutrientes, que tiene un factor de protección contra la absorción del Pb desde los alimentos (Ahamed et al., 2007). Asimismo, se determinaron correlaciones negativas no significativas (p > 0.05) entre la concentración de PbS y la ingesta de Fe y Ca (r = - 0.11 y r = - 0.30 respectivamente). Sin embargo, es necesario un estudio más profundo que permita elucidar el posible efecto protector del consumo de estos nutrientes en la prevención de la intoxicación con Pb.
Hábitos de exposición al Pb
Se realizaron 49 entrevistas del mismo número de hogares en las que se incluyó información sobre algunas prácticas habituales o características de la casa que pudieran representar una fuente de exposición al Pb. Se encontró que 25 de los encuestados (51.0 %) mencionó consumir alimentos en la calle, principalmente en establecimientos que emplean utensilios de barro en la preparación de alimentos; 19 entrevistados (38.8 %) mencionaron consumir dulces como paleta Tutsi pop, Rockaleta diablo, Ricaleta chamoy, Tiramindo, Chaca-chaca, entre otros, de los cuales se ha reportado la presencia de Pb en cantidades por encima de los valores recomendados (Tamayo y Ortiz et al., 2016); 10 personas (20.4 %) reportaron tener juguetes que provienen de la economía informal o artesanal, los cuales (dependiendo de su origen y de su calidad), pueden contener pinturas con Pb (Njati y Maguta, 2019); 22 de los participantes (44.9 %) mencionaron tener viviendas construidas en la década de los setenta o antes; o bien, poseer tuberías metálicas de cobre o acero galvanizado lo cual es importante ya que la pintura y algunos componentes de tuberías de casas antiguas están relacionados con la presencia de Pb (Isley et al., 2022). Finalmente, y como se mencionó anteriormente, el consumo de alimentos elaborados en utensilios de barro fue considerado como otro hábito de exposición al este elemento, resultando que en 30 de los hogares entrevistados (61.2 %) usan UBPb (Tabla 4).
Tabla 4: Riesgo a enfermedades asociadas a la intoxicación con Pb por diferentes hábitos de exposición.
Table 4: Risk of Pb poisoning associated diseases due to different exposure habits.
| Hábito de exposición | % de hogares con exposición | Prevalencia de enfermedades crónicas asociadas a la intoxicación con Pb1 | Prevalencia de enfermedades agudas asociadas a la intoxicación con Pb1 |
| Niveles de PbS mayores a los valores de referencia | 20.9 | 1.40 (I.C. 95 %: 1.01-1.96)a | 0.97 (I.C, 95 %: 0.57-1.66) |
| Uso de UBPb para elaborar alimentos. | 61.2 | 1.99 (I.C. 95 %: 1.06-3.70)a | 0.88 (I.C. 95 %: 0.49-1.57) |
| Comer en la calle donde utilizan barro vidriado. | 48.8 | 1.02 (I.C. 95 %: 0.64-1.63) | 1.34 (I.C. 95 %: 0.74-2.41) |
| Comer dulces relacionados con la presencia de Pb | 39.1 | 0.96 (I.C. 95 %: 0.59-1.56) | 0.79 (I.C. 95 %: 0.42-1.86) |
| Usar juguetes provenientes de la economía informal o artesanal. | 20.9 | 0.81 (I.C. 95 %: 0.41-1.95) | 1.15 (I.C. 95 %: 0.61-2.17) |
| Vivienda con más de 40 años o con tubería metálica. | 44.9 | 0.86 (I.C. 95 %: 0.53-1.39) | 1.03 (I.C. 95 %: 0.58-1.84) |
Razón de Prevalencias
No se observó una mayor prevalencia en la cantidad de PbS al comparar los dos grupos de personas que usan UBPb y los que no (RP = 0.41, 95 % IC 0.16 - 1.07) y esto concuerda con el hecho de que no hubo diferencia significativa en los niveles de PbS entre ambos grupos. Además, solo cinco usuarios de UBPb presentaron valores de PbS por encima de los valores de referencia, mientras que 8 de los usuarios que no utilizan barro tienen valores altos de PbS. Indicando así, la baja repercusión del uso de UBPb en los niveles de PbS.
Debido a que los niveles altos de PbS se asocian a varias enfermedades crónicas, comparamos directamente la razón de prevalencia de las enfermedades crónicas y agudas asociadas a la intoxicación con Pb entre los grupos con niveles de PbS (altos y bajos) y los grupos que se usan o no UBPb. Las personas con concentración de PbS mayor a los valores de referencia, tienen 40 % más de prevalencia de enfermedades crónicas (RP = 1.40, 95% IC 1.01-1.96) que aquellas con cantidades de PbS menores. No hubo diferencia en la prevalencia de enfermedades agudas relacionadas a la cantidad de PbS (Tabla 4). Los valores de referencia se basan en los valores criterio mencionados en la normatividad para tomar acciones básicas de protección a la población, sin embargo, es importante destacar que padecimientos como daño neurológico, renal, cardiovascular, al sistema inmune, a órganos reproductivos, bajo peso al nacer y anemia, están asociadas a concentraciones de PbS de ≤ 5 - 10 µg dL-1 (ATSDR, 2020; Téllez-Rojo et al., 2019; Ahamed et al., 2007). Adicionalmente, existe riesgo de padecer algunos tipos de cáncer (esófago, estómago, colo-rectal, vejiga y tracto urinario) asociado a niveles de PbS que van de 2.81-23 µg dL-1 (Vagnoni et al., 2024). Por lo tanto, a pesar de que el 80 % de las personas tuvieron valores por debajo del valor de referencia, los niveles de PbS reportados en este estudio representan por sí mismos un riesgo de padecer enfermedades asociadas a la intoxicación con Pb considerando que no se puede establecer un umbral de seguridad para PbS.
Por otro lado, se observó un aumento del 99 % en la razón de prevalencia de enfermedades crónicas relacionadas con la intoxicación con Pb (RP = 1.99, 95 % IC: 1.06-3.72) en personas que usan UBPb, con respecto a las personas que usan utensilios de barro sin Pb u otro tipo de utensilios. No se observó una mayor prevalencia de enfermedades agudas por el uso de UBPb (Tabla 4). En otro estudio de tipo transversal, Farías y colaboradores encontraron una asociación similar entre el uso de UBPb con niveles de PbS en niños ≥ 5 µg dL-1 obteniendo una razón de probabilidades de 2.68 (Farías et al., 2014). Si bien, en nuestro estudio no encontramos relación de los niveles de PbS con el uso de UBPb, al hacer una comparación directa con las enfermedades, se puede obtener información que guíe a un acercamiento al diagnóstico de estos padecimientos multifactoriales.
Respecto a los otros tipos de exposición evaluados, los hábitos que presentaron una razón de prevalencia mayor fueron comer en la calle en establecimientos que utilizan barro vidriado (2 % para enfermedades crónicas y 34% para enfermedades agudas), el uso de juguetes de economía informal (15 % para enfermedades agudas) y las viviendas de más de 40 años de antigüedad (3 % para enfermedades agudas), pero ninguna fue estadísticamente significativa (p > 0.05). Esto coincide con que el uso de barro vidriado es el mayor predisponente al Pb en la población sobre otros factores de exposición (Farías et al., 2014).
Conclusiones
En ocho de cada diez hogares que participaron en este estudio se emplean UBPb y la presencia de este elemento en los alimentos es variable, pero en la mayoría de los casos los valores superan los límites establecidos en dos normatividades internacionales. El agua utilizada para elaborar los alimentos no es fuente de Pb por no tener cantidades detectables. Los niveles de PbS detectados promediaron 21.5 µg dL-1 y 13 de los pobladores estuvieron por encima de los valores de referencia, aunque la sola presencia de Pb representa un riesgo a la salud, ya que la organización mundial de la salud (OMS) declara que no hay cantidad segura de PbS. La mayoría de los participantes tienen deficiencia en la ingesta de Fe y Ca, que aunado a los malos hábitos de alimentación, representan un riesgo mayor de intoxicación con Pb en los pobladores encuestados. La razón de prevalencia de enfermedades crónicas relacionadas a la intoxicación con Pb aumenta un 40 % con los niveles altos de PbS, mientras que el uso de UBPb aumentan la razón prevalencia de enfermedades crónicas en un 99 %. Se detectaron fuentes de exposición y deficiencias nutricionales que representan un riesgo para la intoxicación con Pb en los pobladores participantes, aunque las posibles fuentes del elemento en los alimentos no está completamente relacionado con el uso de uso de UBPb.











 nueva página del texto (beta)
nueva página del texto (beta)