Introducción
En la agricultura se utilizan diversos agroquímicos para proteger los cultivos asegurando una mayor producción al reducir las pérdidas de cultivos (Sharma et al., 2019). En México, durante el año 2021, se emplearon un total de 43,578.14 toneladas de agroquímicos, donde los insecticidas representaron aproximadamente el 22.9 % (FAOSTAT, 2021). Los insecticidas pueden tener impactos negativos en el ambiente, incluyendo efectos perjudiciales en organismos no objetivo como las abejas (Zhang et al., 2018; Devi et al., 2022). En las últimas dos décadas, se ha observado un creciente interés en las evaluaciones toxicológicas de insecticidas en abejas polinizadoras, debido a la preocupante disminución de sus poblaciones (Silviter et al., 2021; Bernardes et al., 2022). Las abejas sin aguijón (Hymenoptera: Meliponini) han sido incluidas en las evaluaciones toxicológicas, pero con menor frecuencia, con sólo 7.84 % de los estudios comparado con el 79.7 % de estudios en abejas melíferas (Bernardes et al., 2022). Las abejas sin aguijón cuentan con más de 500 especies distribuidas en los trópicos del planeta y desempeñan un papel crucial en la polinización. Se estima que son responsables de polinizar entre el 40 % y el 90 % de las plantas nativas (Cham et al., 2018; Quezada-Euán, 2018). Estas abejas incluyen diversas especies de importancia económica. Por ejemplo, Melipona beecheii y Nannotrigona perilampoides, cuya distribución abarca desde el centro de México hasta el sur de Costa Rica (Quezada-Euán, 2018). Se asocian con cultivos como el achiote (Bixa orellana L.), chile habanero (Capsicum chinense Jack.) y aguacate (Persea americana Mill.) (Caro et al., 2017; Real-Luna et al., 2022). Además, M. beecheii es especialmente destacada en la práctica de la meliponicultura (González-Acereto et al., 2006).
Los insecticidas sistémicos plantean una preocupación ya que son absorbidos por las plantas y transportados al néctar o al polen mediante la conducción de la savia, lo que expone a las abejas a la contaminación por ingestión (Goulson, 2013). Esta contaminación también puede ocurrir cuando las abejas entran en contacto con residuos de insecticidas, resultado de la aplicación foliar a los cultivos (Fairbrother et al., 2014). La pimetrozina y el flonicamid, dos insecticidas sistémicos comunes, afectan los receptores sensoriales llamados órganos cordotonales en las articulaciones de los insectos (Yack, 2004; Kavlie y Albert, 2013; Maienfisch, 2019). Estos receptores controlan la locomoción y detectan estímulos externos como gravedad, sonido y vibraciones del sustrato (Field y Matheson, 1998; Yack, 2004; Kavlie y Albert, 2013). La pimetrozina interrumpe la coordinación locomotora de los insectos e inhibe la alimentación a través de la sobreestimulación de los receptores de los órganos cordotonales (Nesterov et al., 2015; Salgado, 2017; Huang et al., 2023). Por otro lado, el flonicamid también actúa selectivamente sobre los órganos cordotonales del insecto, pero inhibe la actividad de la nicotinamidasa, una enzima implicada en una variedad de procesos metabólicos, incluyendo la respiración celular, la producción de energía y la reparación del ADN (Spalthoff et al., 2022; Qiao et al., 2022).
La falta de estudios sobre el impacto de la pimetrozina y el flonicamid en las abejas sin aguijón resalta la necesidad de investigar los efectos de estos plaguicidas en estos insectos clave. Por lo tanto, el objetivo de este estudio fue evaluar la supervivencia y los efectos subletales en la locomoción, específicamente, en la actividad de caminata y vuelo, de las abejas sin aguijón M. beecheii y N. perilampoides mediante ingestión oral o exposición residual a los insecticidas sistémicos flonicamid y pimetrozina en condiciones de laboratorio.
Materiales y métodos
Colecta de abejas e insecticidas probados
Se emplearon obreras adultas de M. beecheii y N. perilampoides, obtenidas del meliponario ubicado en el Tecnológico Nacional de México, campus Conkal, en Conkal, Yucatán, México (21° 04′2 4″ N 89° 31′ 15″ O y 8 m.a.s.n.m.). La recolección se realizó en días soleados con temperaturas superiores a 25 °C. Se capturaron exclusivamente obreras que regresaban a la colonia con polen en sus corbículas, utilizando un aspirador manual, y se agruparon en frascos de plástico de 500 mL. Los frascos utilizados estaban equipados con papel filtro en la base (Whatman grado 1) y una sección de tela de malla de tul de 20 cm² en un lateral del frasco para facilitar la ventilación en cuya parte central se insertó un microtubo de centrifuga de 1.5 mL que contenía una solución de sacarosa (sacarosa/agua destilada 1:1) como alimento, disponible ad libitum. Después de la recolección, las obreras se mantuvieron en un cuarto oscuro (temperatura: 30 ± 1 °C; HR: 70 ± 2 %) durante 24 h antes del inicio de las pruebas, con el fin de reducir el estrés del confinamiento.
En este estudio se evaluaron dos insecticidas: flonicamid (Beleaf, 500 g/kg; FMC Agroquímica de México) y pimetrozina (Plenum® 50 GS, 500 g/kg; Syngenta Agro), ambos utilizados para el control de insectos succionadores de savia de las familias Aleyrodidae y Aphididae en cultivos hortícolas. Las concentraciones de los insecticidas se seleccionaron siguiendo las recomendaciones de aplicación en campo proporcionadas por los fabricantes para el control de la mosca blanca (Bemisia tabaci Genn.). La concentración de flonicamid fue de 250 mg de ingrediente activo (i.a./L) mientras que la de pimetrozina fue de 500 mg i.a./L. Las dosis de los insecticidas se calcularon considerando el volumen de aspersión por hectárea de 500 L utilizado para el control de la mosca blanca en cultivos hortícolas. Todos los experimentos se llevaron a cabo mediante dos vías de exposición: oral y residual.
Efecto en la supervivencia de los insecticidas sobre M. beecheii y N. perilampoides
Para la exposición oral, las abejas fueron alimentadas con una solución de azúcar contaminada con la dosis respectiva. En frascos de plástico de 500 mL, se colocaron diez abejas con un período de ayuno de dos h para asegurar la ingestión durante el experimento. Posteriormente, se añadió 1 mL de la dieta contaminada en un microtubo de 1.5 mL insertado en los frascos. El grupo control fue alimentado con 1 mL solución azucarada (sacarosa/agua destilada 1:1) sin insecticida.
Para la exposición residual, se emplearon cajas Petri de plástico de 9 cm de diámetro por 2 cm de altura con perforaciones en la tapa para permitir la respiración de las abejas. En el fondo de cada caja se colocó papel filtro de 9 cm de diámetro (Whatman grado 1), al cual se aplicó 1 mL de solución insecticida acuosa a la concentración evaluada o agua destilada para el control. Tras un período de secado de dos h a temperatura ambiente, se añadieron microtubos de 1 mL de alimento sin insecticida (sacarosa/agua destilada 1:1). Luego, se introdujeron diez abejas adultas en cada caja Petri. En ambos tipos de exposición, se registró el número de abejas vivas y muertas en cada unidad experimental (frascos de plástico o cajas Petri) en intervalos de cuatro, ocho y 12 h, después de la exposición a los insecticidas. Se consideró que los individuos estaban muertos si no podían moverse o ponerse de pie. Cada tratamiento se replicó cinco veces, y cada réplica contuvo diez obreras adultas. Todas las unidades experimentales se mantuvieron en un cuarto obscuro a una temperatura de 30 ± 1 °C y una humedad relativa de 70 ± 2 %.
Efectos subletales de los insecticidas en la actividad de caminata y vuelo vertical de M. beecheii y N. perilampoides
La actividad de caminata se evaluó en una placa de madera con dimensiones de 75 x 30 x 15 cm, la cual estaba equipada con tubos de silicona de 60 cm de longitud acoplados. Las abejas fueron expuestas a las dosis de aplicación recomendada en campo de los insecticidas, tanto por vía oral (dieta contaminada) o exposición residual (residuos secos), como se describió anteriormente. Después de dos h de exposición, los insectos fueron liberados individualmente en un extremo de los tubos de silicona. En el extremo opuesto de los tubos se colocó una lámpara fluorescente de 60 watts y 800 lúmenes, como un estímulo de atracción para las abejas. Treinta segundos antes de comenzar la prueba, se encendió la lámpara, y luego de ese intervalo, se liberaron diez abejas en cada ronda del experimento, por triplicado. Se registró el tiempo que cada abeja tardó en recorrer una distancia de 50 cm hacia la fuente de luz, y se calculó la velocidad promedio de cada abeja. En los tratamientos control, las abejas recibieron dieta sin insecticida (exposición oral), o fueron expuestas a una superficie tratada con agua destilada (exposición residual).
La actividad de vuelo vertical se realizó en una torre con una altura de 105 cm, la cual estaba abierta en su interior para permitir el libre vuelo de los insectos a través de ella. A una distancia de 10 cm por encima de la torre, se colocó una lámpara fluorescente de 60 watts y 800 lúmenes. Las abejas fueron expuestas a las dosis de aplicación recomendada en campo insecticidas por vía oral (dieta contaminada) o residual (residuos secos). Después de dos h de exposición, se liberaron diez abejas en cada ronda del experimento, realizadas por triplicado. Los insectos se liberaron individualmente en la base de la torre, a una altura de 0 cm, y se les permitió un período de dos minutos para completar el vuelo. Se clasificó el despegue del vuelo de la siguiente manera: (a) ningún vuelo (es decir, la abeja permaneció en la base de la torre), (b) vuelo de hasta 35 cm de altura, (c) vuelo entre 35 y 70 cm de altura, (d) vuelo entre 70 y 105 cm de altura y (e) vuelo alcanzando la fuente de luz a una altura de 120 cm. En los tratamientos control, las abejas recibieron dieta sin insecticida (exposición oral), o fueron expuestas a una superficie tratada con agua destilada (exposición residual).
Análisis estadístico
Todos los experimentos siguieron un diseño completamente al azar. Las curvas de supervivencia se generaron utilizando estimadores de Kaplan-Meier basados en datos de mortalidad observados en intervalos de evaluación de cuatro, ocho y 12 h, después de la exposición a los insecticidas. Las funciones de supervivencia estimadas se compararon con una prueba no paramétrica de Log-Rank (método de Holm-Sidak). Los datos de velocidad de caminata se sometieron a un análisis de varianza. Las medias se compararon mediante la prueba de Tukey, con un nivel de significancia del 5 %. Para evaluar la asociación entre el vuelo de las abejas y las altitudes en relación con los tratamientos, se construyeron tablas de contingencia y se realizó un análisis estadístico utilizando la prueba χ2 de Pearson (p<0.05). Todos los análisis se llevaron a cabo utilizando el programa estadístico InfoStat versión 2018 (Di Rienzo et al., 2018).
Resultados
Tasa de supervivencia de M. beecheii y N. perilampoides
La exposición oral y residual de M. beecheii y N. perilampoides al flonicamid y pimetrozina tuvo impacto significativo en la supervivencia (Figura 1). En M. beecheii, la exposición oral a los insecticidas resultó en una disminución en la tasa de supervivencia, que osciló entre el 79 % y 89 % a las 12 h (Figura 1a). Sin embargo, no se detectó ningún efecto adverso cuando las abejas fueron expuestas a los insecticidas residualmente (Figura 1b). En N. perilampoides, la exposición oral a los insecticidas no tuvo efectos en la tasa de supervivencia (Figura 1c), pero la exposición residual resultó en una disminución de 79 % y 82 % de supervivencia (Figura 1d).
Figura 1 Curvas de supervivencia de Kaplan-Meier de M. beecheii expuestas por vía oral (a) o residual (b) y de N. perilampoides expuestas por vía oral (c) o residual (d) a las dosis recomendadas en campo de flonicamid (250 mg i.a/L) y pimetrozina (500 mg i.a/L) después de 4, 8 y 12 h de exposición. Las funciones de supervivencia estimadas se compararon con una prueba no paramétrica de Log-Rank (método de Holm-Sidak). Las diferencias significativas (p < 0.05) entre los tratamientos insecticidas se indican con letras diferentes.
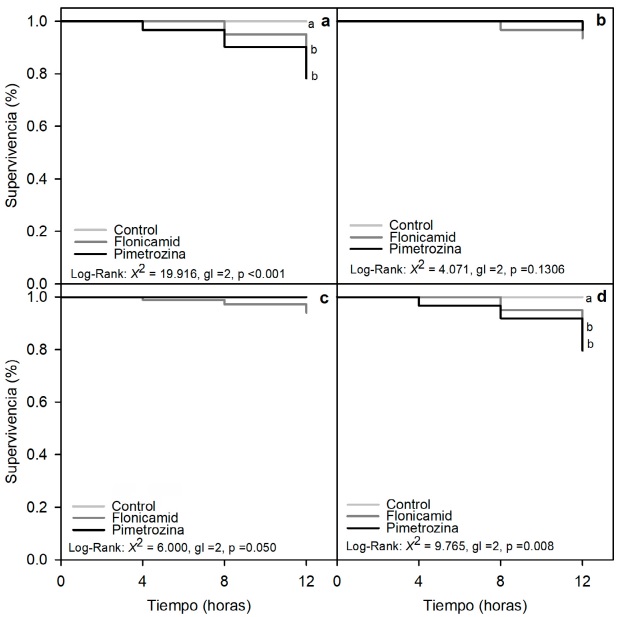
Figure 1: Kaplan-Meier survival curves of M. beecheii exposed orally (a) or residually (b) and of N. perilampoides exposed orally (c) or residually (d) to the recommended field doses of flonicamid (250 mg a.i./L) and pymetrozine (500 mg a.i./L) after 4, 8 and 12 hours of exposure. The estimated survival functions were compared with a nonparametric Log-Rank test (Holm-Sidak method). Significant differences (p < 0.05) among insecticide treatments are indicated by different letters.
Evaluación de la actividad de caminata de los insecticidas sobre M. beecheii y N. perilampoides
La exposición oral y residual por dos h de M. beecheii y N. perilampoides a flonicamid y pimetrozina afectó significativamente la velocidad de caminata (Figura 2). En M. beecheii, la exposición oral resultó en una reducción de la velocidad de caminata, con valores de 1.66 ± 0.30 cm/s para flonicamid y 0.96 ± 0.21 cm/s para pimetrozina, en comparación al grupo control (3.79 ± 0.35 cm/s). En exposición residual, la velocidad de caminata fue similar en los tres tratamientos (Figura 2a). En N. perilampoides, durante la exposición oral, las abejas expuestas al flonicamid exhibieron una velocidad de caminata más lenta (0.50 ± 0.09 cm/s), mientras que las abejas tratadas con pimetrozina (0.93 ± 0.11 cm/s) mantuvieron una velocidad similar a las abejas del grupo control (1.26 ± 0.13 cm/s). En exposición residual, tanto el flonicamid como la pimetrozina causaron reducción de la velocidad de caminata, con valores de (0.64 ± 0.08 cm/s) y (0.44 ± 0.07 cm/s) respectivamente, comparado con el grupo control (0.97 ± 0.06 cm/s) (Figura 2b).
Figura 2 Efecto de flonicamid (250 mg i.a/L) y pimetrozina (500 mg i.a/L) sobre la velocidad de caminata de M. beecheii (a) y N. perilampoides (b) después de dos h de exposición oral y residual. Medias ± error estándar con letra distinta dentro de las barras indican diferencia estadística (Tukey, p < 0.05).
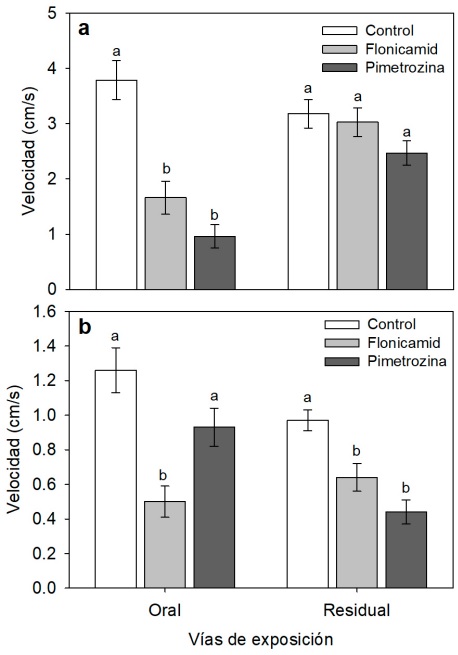
Figure 2: Effect of flonicamid (250 mg a.i./L) and pymetrozine (500 mg a.i./L) on the walking speed of M. beecheii (a) and N. perilampoides (b) after two hours of oral and residual exposure. Means ± standard error with different letters within the bars indicate statistical significance (Tukey, p < 0.05).
Evaluación de la actividad de vuelo de los insecticidas sobre M. beecheii y N. perilampoides
La exposición oral y residual por dos h de M. beecheii y N. perilampoides a flonicamid y pimetrozina afectó significativamente la capacidad de vuelo (Figura 3). En M. beecheii, el 70 % de los individuos no tratados (grupo control) volaron hacia la fuente de luz a una altura de 120 cm durante la exposición oral. En contraste, sólo el 10 % y 0 % de las abejas tratadas con flonicamid y pimetrozina, respectivamente, alcanzaron esa altura (Figura 3a). En exposición residual, ninguno de los insecticidas tuvo efecto sobre la actividad de vuelo (Figura 3b). En N. perilampoides, el 70 % de los individuos no tratados (grupo control) volaron hacia la fuente de luz a una altura de 120 cm durante la exposición oral. En contraste, sólo el 6.67 % y 0 % de las abejas tratadas con flonicamid y pimetrozina, respectivamente, alcanzaron esa altura (Figura 3c). En exposición residual, todas las abejas control volaron hacia la fuente de luz a 120 cm, mientras que el 63.33 % de las abejas tratadas con flonicamid mostraron el mismo comportamiento. Sólo el 26.67 % de las abejas tratadas con pimetrozina alcanzaron los 120 cm (Figura 3d).
Figura 3 Efecto de flonicamid (250 mg i.a/L) y pimetrozina (500 mg i.a/L) sobre el porcentaje de adultos de M. beecheii expuestas por vía oral (a) o residual (b) y N. perilampoides expuestas por vía oral (c) o residual (d) que aterrizaron en diferentes niveles de alturas después de dos h. La prueba de chi-cuadrado de Pearson indica significación estadística indicada como (***= p < 0.0001; **= p < 0.005; *= < 0.05; ns = diferencia no significativa).
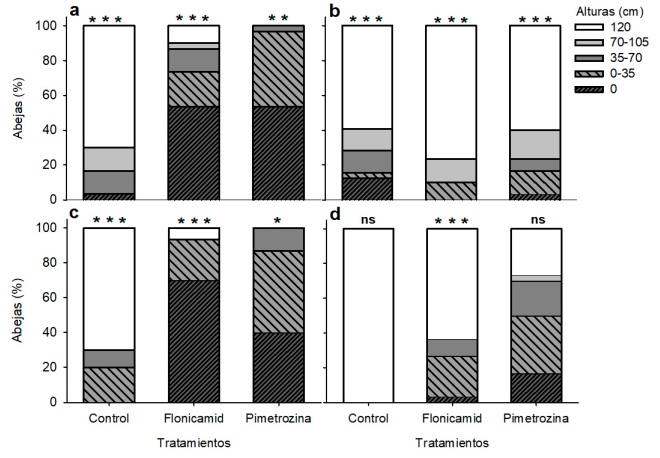
Figure 3: Effect of flonicamid (250 mg a.i./L) and pymetrozine (500 mg a.i./L) on the flight activity of M. beecheii exposed orally (a) or residually (b), and N. perilampoides exposed orally (c) or residually (d) that landed at different height levels after two hours. Pearson’s χ2 test indicates a significant difference (*** p < 0.0001; * p < 0.05; n.s., statistically not significant).
Discusión
La aplicación de insecticidas químicos en los agroecosistemas ha traído consecuencias negativas para especies clave en la polinización, como las abejas sin aguijón (Lima et al., 2016; Toledo-Hernández et al., 2022). En particular los insecticidas que actúan en el sistema nervioso central representan una seria amenaza para la supervivencia de las abejas sin aguijón (Tomé et al., 2015a; Lima et al., 2016; Góngora-Gamboa et al., 2022). Estos productos suministrados en dosis subletales causan efectos negativos en la locomoción de las abejas a corto plazo (Tomé et al., 2015a; Tomé et al., 2015b; Piovesan et al., 2020). Existen insecticidas químicos que actúan en sitios de acción, como los órganos cordotonales de los insectos, y ese efecto de estos productos no se conoce, pues la mayor parte de los estudios se han hecho usando insecticidas que actúan en el sistema nervioso central. En el presente trabajo se evaluaron los efectos de dos insecticidas (flonicamid y pimetrozina) que actúan en los órganos cordotonales, en la supervivencia y locomoción de las abejas sin aguijón M. beecheii y N. perilampoides.
Mediante exposición oral y residual, se observó que la tasa de supervivencia disminuyó ligeramente a las 12 h después de la exposición a dosis de campo. Otros insecticidas como el organofosforado clorpirifós, el neonicotinoide imidacloprid y la spinosina spinosad tienen un impacto mucho mayor en la supervivencia de abejas sin aguijón, incluso en un lapso muy corto de tiempo (Tomé et al., 2015b; Leite et al., 2021). Al igual que en el presente estudio, se ha observado que el flonicamid y la pimetrozina causan efectos ligeros a moderados en la abeja europea Apis mellifera (L.), utilizando concentraciones de 0.25 a 80 mg/L para el flonicamid y de 250 a 300 mg/L para la pimetrozina (Abramson et al., 2012; Badawy et al., 2014; Meikle y Weiss 2022; Anwar et al., 2022).
Aunque algunos insecticidas no presentan efectos letales en las abejas sin aguijón, sí pueden causar efectos subletales, como inhibición de la alimentación y disminución en la capacidad de vuelo (Tomé et al., 2015b; Bernardes et al., 2017; Pereira et al., 2023). En el presente estudio, aunque el flonicamid y pimetrozina no causaron alta mortalidad, se detectaron efectos en la velocidad de caminata y vuelo vertical. En general, se encontró que N. perilampoides tuvo efectos más pronunciados que M. beecheii. La velocidad de caminata se redujo significativamente, además de disminuir la capacidad de vuelo vertical. Estos efectos en la locomoción de M. beecheii y N. perilampoides pueden ser debido al mecanismo de acción de estos insecticidas, sobre los órganos cordotonales de los insectos, ya que los órganos cordotonales son receptores sensoriales que controlan la locomoción (Field y Matheson, 1998; Yack, 2004; Kavlie y Albert, 2013). El flonicamid es una piridina carboxamida e interrumpe la actividad de la enzima nicotinamidasa, provocando la sobreactivación de los receptores del canal de potencial transitorio tipo vaniloide (TRPV) en los órganos cordotonales (Qiao et al., 2022). En contraste, pimetrozina, una piridina azometina, actúa directamente sobre los canales TRPV, causando parálisis (Spalthoff et al., 2022).
La exposición de M. beecheii y N. perilampoides a flonicamid y pimetrozina resultó en una disminución significativa de la velocidad de caminata y la actividad de vuelo. Estos efectos sugieren que estas abejas podrían enfrentar serias dificultades para pecorear de manera eficaz y podría resultar en una menor polinización de los cultivos, afectando negativamente la producción agrícola. Melipona beecheii y N. perilampoides son dos especies de abejas sin aguijón que pertenecen a diferentes géneros dentro de la tribu Meliponini, lo que implica variaciones en su biología, por ejemplo, M. beecheii es más grande y forma colonias de 800 a 1500 individuos, anidando principalmente en cavidades de árboles en áreas preservadas (Quezada-Euán, 2018). En contraste, N. perilampoides es más pequeña y tiene colonias de 700 a 1200 individuos. Esta abeja anida en árboles vivos, pero también se adapta a ambientes urbanos, utilizando grietas y hendiduras de edificios para establecer sus colonias (May-Itzá et al., 2021). Estas caracteristicas podrían influir en sus capacidades de adaptación y resistencia a estresores como los insecticidas.
Como los efectos fueron más pronunciados en N. perilampoides, esta especie podría ser especialmente vulnerable en entornos donde se usan estos insecticidas. Sin embargo, es crucial realizar estudios sobre los efectos de pimetrozina y flonicamid en condiciones de campo e invernadero. Esto permitirá investigar los impactos de estos productos en escenarios más realistas.
Conclusiones
Los insecticidas flonicamid y pimetrozina causaron disminución ligera en la tasa de supervivencia de M. beecheii y N. perilampoides a las 12 h de exposición por ambas rutas, oral y residual. Después de dos h de exposición, ambos insecticidas provocaron reducción significativa en la velocidad de caminata y la actividad de vuelo vertical en ambas especies de abejas, particularmente en exposición oral. Estos efectos fueron más pronunciados en N. perilampoidesque en M. beecheii.











 nueva página del texto (beta)
nueva página del texto (beta)



