Introducción
Los compuestos fenólicos, son metabolitos secundarios presentes en las plantas, frutas, hortalizas, raíces y cereales (Klepacka et al., 2011). Los compuestos fenólicos perteneces a los compuestos de alto valor biológico (CAVB) que incluyen enzimas, microorganismos y metabolitos secundarios con actividad biológica benéfica para los seres vivos (Ramos-Hernández et al., 2018). Se ha reportado que las hojas de mango son una fuente importante de compuestos fenólicos tales como benzofenonas, flavonoides, terpenoides y xantonas (Guamán-Balcázar et al., 2017; Kumar et al., 2021). Además, se han atribuido a estos compuestos diversas actividades biológicas, tales como, antioxidante, antimicrobiana y antifúngica (Albuquerque et al., 2021). Sin embargo, estas propiedades pueden perderse debido a factores medioambientales, como exposición a la luz, la humedad y oxígeno (Ballesteros et al., 2017). Por lo que se buscan alternativas de protección, en este sentido, la encapsulación provee una barrera física entre el medio circundante y los compuestos encapsulados brindándoles estabilidad (Ribeiro et al., 2019). Una de las técnicas de encapsulación más utilizadas en la industria es el secado por aspersión debido a que es un proceso continuo, económico y de fácil escalabilidad (Yazdi et al., 2021).
El secado por aspersión requiere materiales de pared para encapsular el compuesto de interés y obtener un producto en polvo (Ziaee et al., 2019). Por lo que debe haber compatibilidad del material de pared con el compuesto de interés, para asegurar una encapsulación eficiente (Nedović et al., 2013). Los materiales de pared deben ser económicos, no reaccionan con el núcleo y se identifican como GRAS, entre los más utilizados debido a su alta solubilidad, baja viscosidad, gelificación y formación de películas son las proteínas y polisacáridos (Safeer-Abbas et al., 2023); más específicamente la maltodextrina, alginato, almidones y gomas (Macías-Cortés et al., 2020; Díaz-Montes, 2023). Se ha reportado que la mezcla de dos o más materiales de pared incrementa la eficiencia de encapsulación, así como la estabilidad térmica conservando sus propiedades biológicas (Tao et al., 2019; Dierings de Souza et al., 2021). Por estas razones el objetivo de la investigación fue obtener y caracterizar las cápsulas de extracto de hojas de mango, obtenidas por secado por aspersión con alginato de sodio y goma arábiga para su aplicación en frutos de interés comercial.
Materiales y métodos
Encapsulación del extracto mediante secado por aspersión
Se preparó una solución utilizando la metodología propuesta por Calderón‐Santoyo et al. (2022) con algunas modificaciones. Una solución de 250 mL (p/v) conformada por alginato de sodio 0.03 % el cual se disolvió en agua destilada por agitación magnética con una placa Fisher Scientific a 350 rpm durante 24 h a 25 ± 1 °C. Pasadas las 24 h, a la solución de alginato de sodio se le añadió goma arábiga (7.5 % m/v) y 3 % (m/v) del extracto óptimo de las hojas de mango, la cual se homogenizó y después se encapsuló usando un equipo de escala laboratorio de secado por aspersión mini Spray Dryer (Modelo B-290, Büchi, Flawil, Suiza), con una boquilla de alimentación de 7 mm de diámetro bajo caudal constante y presión de aire (35 m3/h y 0.7 MPa, respectivamente), se mantuvo bajo una agitación constante a temperatura ambiente y 350 rpm, se alimentó por una bomba peristáltica a un caudal de 5 mL/min, la temperatura del aire de entrada y de salida fue de 105 y 63 °C, respectivamente.
Determinación de la higroscopicidad
Se llevó a cabo de acuerdo a la metodología descrita por Arepally et al. (2020). Se colocó 1 g de muestra en cajas Petri de 9 cm de diámetro (previamente a peso constante obtenido una vez que la caja de Petri perdió por completo su humedad a 105 ºC y la diferencia de peso entre dos mediciones sucesivas no excedió los 0.0003 g), se colocaron en un desecador a 21 °C y 76 % de humedad relativa (HR) (solución de 36 g NaCl en 100 g de agua). Se registró el incremento del peso después de 7 días, la higroscopicidad fue calculada de acuerdo a la ecuación 1.
Donde Mf es el peso de las cajas con muestra después de 7 días y Mi el peso de las cajas al inicio de la prueba.
Distribución del tamaño de partícula
La distribución del tamaño de partícula se determinó de acuerdo a la metodología propuesta por Calderón‐Santoyo et al. (2022). Se utilizó un difractómetro láser Mastersizer (Modelo 3000, Malvern instruments, Malvern, Reino Unido). Las mediciones se realizaron a 25 °C y se colocaron 3 g de polvo manualmente en la tolva. Las condiciones de operación fueron: suministro de aire y el sistema de extracción de vacío conectados al 30 % de vibración, abertura de salida de 1 mm y aire comprimido a 2 bar de presión. Luego, la muestra pasó al Mastersizer con un valor oscurecimiento del 15 % y un índice de refracción de 1.432.
Determinación de la solubilidad
Se utilizó la metodología propuesta por Jiménez-Sánchez et al. (2017), brevemente, se colocó 1 g de polvo en 100 mL de agua destilada, se agitó manualmente hasta que se solubilizó toda la muestra, y se centrifugaron 15 mL (Modelo X4R PRO-MD, Thermo Fisher Scientific Inc., Osterode am, Harz, Alemania) a 5260 rpm durante 5 min. Se tomó una muestra de 2 mL del sobrenadante y se colocó en cajas Petri (previamente a peso constante obtenido una vez que la caja de Petri perdió por completo su humedad a 105 ºC y la diferencia de peso entre dos mediciones sucesivas no excedió los 0.0003 g). Finalmente, se secó en una estufa a 105 °C por 5 h. La solubilidad (%) fue calculada por diferencia de peso mediante la ecuación 2.
Donde: Mf: masa final y Mo= masa inicial.
Determinación de la densidad aparente
La densidad aparente se realizó mediante la metodología propuesta por Jiménez-Sánchez et al. (2020), 5 g de cápsulas se transfirieron a una probeta graduada de 50 mL, después se movió verticalmente 10 veces. La densidad aparente se calculó dividiendo la masa entre el volumen, y se expresó como g/mL.
Determinación de humedad
La humedad se determinó de acuerdo a la metodología propuesta por Ruiz-Montañez et al. (2019). Se utilizó un método termogravimétrico con equipo (TGA 550, TA instrumentos, New Castle, USA). Se colocaron 5 mg de muestra en una charola de platino HT, la velocidad de calentamiento fue de 10 °C/min en un rango de 25 a 800 °C bajo una atmósfera de nitrógeno.
Eficiencia de encapsulación
La eficiencia de encapsulación fue calculada mediante la metodología propuesta por Navarro-Flores et al. (2020), con algunas modificaciones. La eficiencia de encapsulación se determinó para la actividad antioxidante total. Para ello, a 200 mg de cápsulas se les añadió 2 mL de una solución compuesta por metanol y agua (1/1). La muestra se agitó en un vórtex por 1 min y se sonicó en un baño de ultrasonido (Modelo CD4820, Kendal, Eaton Sacon, Reino Unido) a 42 kHz, por 20 min a 25 °C. Finalmente, la muestra se centrifugó a 4000 rpm por 5 min. La actividad antioxidante se calculó utilizando una curva de calibración con ABTS+, como estándar se utilizó Trolox y la absorbancia se midió a 734 nm en un espectrofotómetro (Modelo Varían Cary 50 UV-VIS, Sídney, Australia). Para determinar los compuestos en la superficie de las cápsulas, 200 mg de las cápsulas se combinó con 2 mL de la solución de metanol/ agua y se agitó en un vórtex por 1 min. La muestra fue centrifugada a 4000 rpm por 5 min. La eficiencia se calculó con la ecuación 3.
Donde: Aa total es la actividad antioxidante total y Aa superficie es la actividad antioxidante en la superficie.
Evaluación de la termoestabilidad del extracto crudo y encapsulado
Se realizó el análisis termogravimétrico (TGA) con un analizador termogravimétrico (Modelo TGA 550, TA instrumentos, New Castle, USA). Se colocaron 5 mg de muestra en una charola de platino HT, la velocidad de calentamiento fue de 10 °C/min en un rango de 25 a 800 °C bajo una atmósfera de nitrógeno. La pérdida de peso con respecto a la temperatura se expresó de acuerdo con la curva termogravimétrica (TG) y la curva termogravimétrica derivada de primer orden (TGD) mediante el software TRIOS. Las transiciones térmicas fueron analizadas por calorimetría diferencial de barrido en un equipo de calorimetría diferencial de barrido (DSC) (Modelo DSC 250, TA Instruments, New Castle, USA). Para ello, 5 mg de muestra se sellaron herméticamente en una charola de aluminio, como referencia se usó una charola sin muestra. Las muestras se calentaron de 25 a 400 °C con una velocidad de 10 °C/min bajo una atmósfera de nitrógeno con flujo de 50 mL/min, la calibración se realizó con un estándar de indio. Los datos temperatura de transición vítrea (Tg) y la temperatura de fusión (Tm) se analizaron en el software TRIOS (Calderón‐Santoyo et al., 2022).
Evaluación de la fotoestabilidad del extracto crudo y encapsulado
Se utilizó una lámpara Osram Ultra-Vitalux 300 W que simuló la radiación UV-A. El procedimiento se realizó en una cámara oscura, la distancia entre la lámpara y la muestra fue de 41 cm. La muestra se mantuvo expuesta a la luz en tiempos de 0, 24, 48, 96, 120 y 148 h, esta metodología se utilizó para evaluar el extracto encapsulado (Ramos-Hernández et al., 2018). Al finalizar cada tiempo de exposición se evaluó la actividad antioxidante, para ello, a 200 mg de cápsulas se les añadió 2 mL de una disolución compuesta por metanol y agua (1/1). La muestra se agitó en un vórtex por 1 min y se sonicó en un baño de ultrasonido a 42 kHz, por 20 min a 25 °C. La muestra se centrifugó a 4000 rpm por 5 min. La actividad antioxidante se calculó utilizando una curva de calibración con ABTS+, como estándar se utilizó trolox y la absorbancia se midió a 734 nm en un espectrofotómetro.
Evaluación de la actividad antifúngica in vivo de los encapsulados
Las frutas de interés comercial (naranja y arándanos), fueron lavadas y desinfectadas con 2 % (v/v) de hipoclorito de sodio por 2 min. Se realizaron soluciones de cápsulas y extracto a las concentraciones mínimas inhibitorias y fueron asperjadas con estas soluciones. Las frutas se perforaron (3 mm de diámetro y 3 mm de profundidad) con una aguja estéril. Los frutos se inocularon con 20 µL de suspensión de esporas de Penicillium digitatum (1 × 105 esporas/mL) y Botrytis cinerea (1 × 103 esporas/mL). Los frutos se almacenaron en una cámara de incubación por 7 días a 28 ± 3 °C y 80 % HR. Se utilizaron 15 frutos para cada tratamiento y se obtuvieron los datos de incidencia (Ecuación 4) y severidad (Ecuación 5) de los frutos (Ayón-Macías et al., 2023).
Donde: dC es el diámetro de la lesión producida en los frutos control y dT diámetro de la lesión producida en los frutos tratados.
Análisis estadístico
Los resultados se expresaron como media ± desviación estándar. Cada experimento se repitió tres veces con tres réplicas por tratamiento. Las variables de respuesta se evaluaron con un análisis de varianza de una vía. Para determinar las diferencias significativas entre tratamientos se aplicó una prueba de Tukey con un nivel de confianza del 95 % (P < 0.05). Los datos se procesaron con el programa MINITAB.
Resultados y discusión
Evaluación de la disolución polimérica por DSC
Con el fin de determinar la temperatura de entrada para el secado por aspersión de la disolución polimérica conformada por goma arábiga y alginato de sodio, con y sin extracto, se realizó un análisis por DSC. Es importante comentar que la miscibilidad de los componentes es un factor importante en la determinación de la Tg, ya que, si los polímeros no están integrados completamente en la disolución, el análisis de DSC mostraría el valor de Tg del compuesto mayoritario. La Tg de la disolución con y sin extracto fue de 112.5 ± 0.5 °C. Este comportamiento indica que no existen interacciones fuertes entre el extracto y los polímeros (Iñiguez-Moreno et al., 2021). En este estudio, en base a la Tg obtenida de la disolución polimérica, se decidió utilizar 105 °C como temperatura de entrada de aire al secado por aspersión. Lo anterior de acuerdo a Islam et al. (2010), quienes comentan que la temperatura de secado por aspersión se define con una diferencia menor a 10 °C respecto de la Tg para evitar el cambio amorfo de los polímeros.
Actividad de agua
La actividad de agua (aw) de las cápsulas con extracto fue de 0.275 ± 0.01. Este resultado es un indicativo de la estabilidad de las cápsulas, ya que existe una menor cantidad de agua disponible que pueda ser usada para la proliferación de microorganismos (Ferrari et al., 2013). Este resultado fue comparable al obtenido por Ferrari et al. (2013) quienes utilizaron individualmente goma arábiga y alginato de sodio para encapsular ácido ascórbico, obteniendo aw de 0.34 y 0.26, respectivamente. Los valores de aw bajos son atribuidos a la alta tasa de transferencia de energía del aire caliente del secado por aspersión, en función de la viscosidad de la solución polimérica, lo que determina la velocidad de evaporación del agua contenida en la disolución alimentada para convertirla en polvo (Islam et al., 2010). Al tener las cápsulas una aw mayor a 0.4, el agua libre puede crear reacciones negativas en los compuestos encapsulados, en general son de tres tipos oxidación, hidrólisis y polimerización de las moléculas (Chiou y Langrish, 2007; Kuck et al., 2017).
Distribución de tamaño de partícula
El tamaño promedio de las partículas obtenidas por secado por aspersión fue de D [4,3] = 6.53 µm. Este diámetro indicó la estabilidad de las cápsulas, ya que, a medida que se reduce su tamaño se tiene una mayor superficie de contacto, lo que facilita la liberación del compuesto activo de la cápsula (Shimanovich et al., 2014). Este resultado es mejor a los obtenidos por Chew et al. (2018), quienes al emplear goma arábiga y caseína de sodio en una proporción de 4:1 a una temperatura de aire de entrada de 160 °C, obtuvieron partículas con diámetro promedio de D [4,3]= 25 µm. Esto puede deberse a que el uso de una mayor temperatura de aire de entrada facilitó la formación de partículas más grandes, causadas por la rápida evaporación del agua, ya que el vapor de agua puede quedar atrapado en la coraza de la cápsula, incrementado su tamaño (Chegini y Ghobadian, 2005; Tonon et al., 2011). De igual manera, el aumento de temperatura acelera la migración de los materiales que forman dicha coraza (Aghbashlo et al., 2013).
Eficiencia de encapsulación
La eficiencia de encapsulación es un parámetro importante, ya que además de evaluar la rentabilidad del proceso, evalúa la calidad de las cápsulas, debido a que refleja la cantidad de extracto en el núcleo (Karagozlu et al., 2021). Se obtuvo una eficiencia de encapsulación del 80 % para las cápsulas compuestas de goma arábiga, alginato de sodio y extracto de hoja de mango. Este valor clasifica al proceso como de alta eficiencia de encapsulación, la cual se asocia con la combinación de los materiales de pared utilizados. La respuesta obtenida es comparable y superior a lo reportado por González et al. (2019), quienes encapsularon extracto de hojas de olivo con alginato de sodio y obtuvieron 60 % de eficiencia de encapsulación. De acuerdo con Al-Maqtari et al. (2021) la combinación de los materiales encapsulantes tiene un papel importante en la eficiencia de encapsulación, ya que, un sólo material de pared no presenta todas las propiedades necesarias para una encapsulación eficiente. La diferencia en la eficiencia de encapsulación se asocia fuertemente con la compatibilidad de los materiales encapsulantes utilizados, condiciones y el tipo de proceso, entre otras (Nedović et al., 2013).
Hidrosolubilidad de las cápsulas
La solubilidad en agua es uno de los factores más importantes en las propiedades de los encapsulados, puesto que, de esta propiedad dependen sus aplicaciones e incorporación en diversos sistemas (Tomsone et al., 2020). La solubilidad de las cápsulas con extracto de hoja de mango presentó un valor de 95 ± 2 %. La solubilidad presentada fue comparable con lo reportado por Navarro et al. (2020) quienes utilizaron diferentes proporciones de maltodextrina con otros polímeros (goma arábiga, proteína de soya, goma de semillas de cajanus, y pectina de cáscara de cacao). Estos autores reportan solubilidades entre 82.15 y 86.54 %. La solubilidad es un factor que afecta la liberación del material del núcleo en el medio líquido (Bhattachar et al., 2006). Además, los polisacáridos como la goma arábiga tienen fuerte afinidad a las moléculas de agua debido al exceso de grupos hidroxilo (Savjani et al., 2012). Las diferencias existentes para esta propiedad se pueden atribuir a la característica individual de cada material encapsulante. Stanisavljevi´c et al. (2018) mencionan que la goma arábiga se caracteriza por una alta solubilidad y una baja viscosidad la cual es apropiada para el proceso de secado por aspersión. Adicionalmente, Al-Maqtari et al. (2021) describe que la goma arábiga consiste en cadenas proteicas hidrofóbicas y polisacáridos hidrofílicos, lo que le confiere una alta solubilidad. Por su parte, el alginato de sodio es un copolímero binario lineal de residuos de ácido manurónico y gulurónico que es menos anfifílico que la goma arábiga (Li et al., 2021). Por lo anterior, la alta solubilidad de las cápsulas se puede atribuir a la alta concentración de goma arábiga en la formulación.
Densidad aparente
La densidad aparente es un factor importante para el manejo, transporte y envasado de polvos, es por esto que, una mayor densidad aparente, indica que el polvo es más deseable debido a la menor ocupación de volumen (Zhang et al., 2020). Las cápsulas con extracto de hoja de mango mostraron una densidad aparente de 0.32 ± 0.02 g/mL. Al aumentar el valor de la densidad aparente, Rodríguez‐Ramírez et al. (2012), mencionan que las partículas no forman aglomerados, tienen un tamaño de partícula uniforme y las partículas son de menor tamaño, lo cual favorece el manejo y envasado del polvo. Este dato es superior a lo obtenido por George et al. (2021), quienes elaboraron cápsulas de goma arábiga con una densidad aparente de 0.177 g/mL. La diferencia puede atribuirse a la viscosidad de la solución polimérica, ya que el incremento de viscosidad incrementa el tamaño de las partículas. Como consecuencia hay una mayor ocupación del volumen en las capsulas con extracto y la densidad aparente disminuye (Sarabandi et al., 2019).
Higroscopicidad
La higroscopicidad de las cápsulas fue de 1.15 g H2O/100 g de muestra. La baja higroscopicidad confirma la alta solubilidad obtenida. Adicionalmente, mejora la estabilidad física, el transporte y almacenaje de los polvos (Fujimori et al., 2016). Los resultados obtenidos fueron mejores a los reportados por Karrar et al. (2021), quienes al utilizar aislado de proteína de suero y la combinación de goma arábiga con maltodextrina para encapsular el aceite de semilla de gurum, obtuvieron 6.95 y 8.76 g H2O/100 g de muestra, respectivamente. Las diferencias en las higroscopicidades de los materiales se deben a la estructura química, su composición y la existencia de grupos funcionales (Juárez-Enríquez et al., 2017). De igual manera, los grupos hidroxilo de los polisacáridos pueden formar enlaces con el hidrógeno de las moléculas de agua, lo que incrementa esta propiedad (Chew et al., 2018; Tao et al., 2019).
Evaluación de la termoestabilidad del extracto encapsulado
Las cápsulas con y sin extracto mostraron una primer pérdida de masa de 8 y 8.91 %, respectivamente a temperaturas de 52-54 °C (Tabla 1). La segunda pérdida de masa se registró a la temperatura de descomposición de las cápsulas de 290.82 °C (con extracto) y 295.9 °C (vacías), con pérdidas de masa de 71.11 y 67.53 %, respectivamente. Estos porcentajes másicos, indican la presencia del extracto en las cápsulas correspondientes. En lo que respecta al extracto, la temperatura de descomposición fue de 233.59 °C. Al comparar con la temperatura de descomposición de las cápsulas con extracto (290.82 °C) se evidenció que existió una termo protección en la encapsulación sobre el extracto. Además, en base a la bibliografía se encontró la temperatura de máxima descomposición de los compuestos identificados: mangiferina de 275.3 °C (Taiwo et al., 2024), ácido clorogénico de 283 °C (Owusu-Ware et al., 2013), ácido hidroxobenzoico de 215.03 °C (Rzokee y Ahmad, 2014), ácido cafeico de 230.3 °C (Liudvinaviciute et al., 2019) y el ácido cumárico de 275 °C (Lonashiro et al., 2012). Lo que permitió asumir que la temperatura de descomposición del extracto (233.59 °C) ha sido correctamente determinada. Adicionalmente, al comparar la temperatura de descomposición de las cápsulas con extracto y la de los componentes presentes en el extracto, se puede confirmar el incremento de la temperatura de descomposición, lo que evidencia la termoprotección para los componentes encapsulados.
Tabla 1 Análisis térmico de cápsulas de goma arábiga, alginato de sodio y extracto de hojas de mango.
Table 1: Thermal analysis of arabic gum, sodium alginate, and mango leaf extract capsules.
| Muestra | Eventos térmicos por TGA | ||||||
| Rango (°C) | Inicio (°C) | Punto medio (°C) | Final (°C) | Td(°C) | Pérdida de peso (%) | Atribución de la pérdida de peso | |
| Extracto | 25-110 | 52.05 | 76.38 | 101.07 | 4.18 | Pérdida de agua libre y ligada | |
| 110-410 | 175.5 | 233.59 | 285.30 | 233.59 | 47.57 | Descomposición del extracto | |
| 410-800 | 450.08 | 518.08 | 583.64 | 25.4 | Minerales | ||
| 22.84 | Masa residual | ||||||
| Cápsulas vacías | 25-190 | 29.03 | 52.60 | 69.18 | 8.91 | Pérdida de agua libre y ligada | |
| 190-372 | 273.98 | 295.90 | 319.20 | 295.90 | 67.35 | Descomposición de goma arábiga y alginato de sodio | |
| 373-800 | 384.80 | 321.07 | 792.69 | 12.66 | Minerales | ||
| 11.07 | Masa residual | ||||||
| Cápsulas + extracto | 25-130 | 29.76 | 54.26 | 72.09 | 8.02 | Pérdida de agua libre y ligada | |
| 130-563 | 255.92 | 290.82 | 326.33 | 290.82 | 71.10 | Descomposición de goma arábiga, alginato de sodio y extracto de hoja de mango | |
| 563-800 | 647.54 | 713.59 | 785.83 | 6.47 | Minerales | ||
| 14.39 | Masa residual | ||||||
Td: temperatura de descomposición.
El análisis DSC mostró que las cápsulas con y sin extracto, presentaron temperaturas de transición vítrea de 129 ± 0.5 y 130 ± 0.3 °C, respectivamente (Tabla 2). Los valores de Tg fueron estadísticamente iguales, lo que indica que no existen interacciones entre el extracto y los polímeros (Iñiguez-Moreno et al., 2021). La temperatura de transición vítrea es aquella donde los materiales amorfos pasan a un estado gomoso, este se ve afectado por la estructura química y el peso molecular del material de pared utilizado (Karrar et al., 2021).
Tabla 2 Temperatura de transición vítrea de biopolímeros, cápsulas sin extracto y extracto encapsulado.
Table 2: Glass transition temperature of biopolymers, capsules without extract, and encapsulated extract.
| Biopolímero/cápsula | Tg (°C) |
| Goma arábiga | 135.22 ± 0.3a |
| Alginato de sodio | 120.65 ± 0.4c |
| Cápsulas sin extracto | 130.87 ± 0.3a |
| Cápsulas con extracto | 129.45 ± 0.5a |
Los resultados expresan la media ± desviación estándar. Las letras diferentes significan diferencia significativa (P < 0.05).
Evaluación de los enlaces producidos en las cápsulas por FTIR
El análisis FTIR de las cápsulas reveló los enlaces característicos de la goma arábiga y el alginato de sodio (Tabla 3). Estos enlaces estuvieron presentes en ambas cápsulas. El primero de los enlaces encontrados en las cápsulas sin extracto fue un grupo hidroxilo, siendo el primero de estos a 3300-3280 cm-1. Además, se observó un enlace C-O, correspondiente a un anillo de piranosa a 1075 - 1000 cm-1 (Tabla 3). En cuanto al alginato de sodio Nair et al. (2020) reportaron un grupo hidroxilo a longitud de onda de 3281 cm-1 y el anillo de piranosa característico del alginato de sodio a 1023 cm-1. Así mismo, los enlaces que no están presentes en las cápsulas sin extracto, son característicos del extracto de las hojas de mango, siendo el enlace C=O reportado por Bello et al. (2014), el grupo característico en el extracto de hoja de mango. Este enlace está presente en una gran proporción de los compuestos ya anteriormente identificado en las hojas de mango, entre los más representativos son las xantonas, los ácidos fenólicos y flavonol (Kumar et al., 2021). Por otra parte, el enlace N-O reportado por Adelaja et al. (2019) representa el grupo de los nitroderivados en el extracto (Tabla 3). Este grupo puede ser utilizado para su conversión a grupos carbonilos utilizando la reacción de Nef (Ballini y Petrini, 2004).
Tabla 3 Tipos de enlaces producidos en las cápsulas de goma arábiga y alginato de sodio con y sin extracto.
Table 3: Types of bonds produced in arabic gum and sodium alginate capsules with and without extract.
| Enlaces obtenidos por FTIR | Número de onda (cm-1) | Modo del enlace | Tipo de enlace reportado |
| OH | 3300-3280 | Estiramiento | Hidroxilo |
| C-O | 1075-1000 | Estiramiento | Anillo de piranosa |
| C=O | 1700-1600 | Estiramiento | Carbonilo |
| N-O | 950-920 | Estiramiento | Nitroderivado |
Fotoestabilidad de las cápsulas
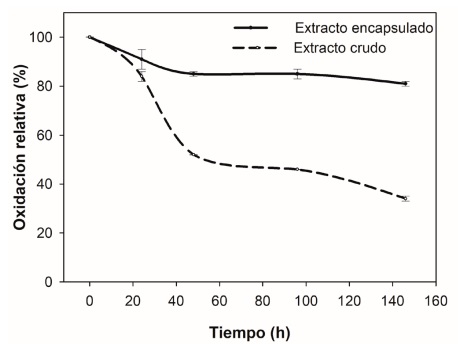
La elección de un material de pared es un punto crítico para la encapsulación. Según Tang et al. (2020), la goma arábiga posee excelentes capacidades para proveer protección efectiva. Esta propiedad se demuestra en la Figura 1, en la que se observa como la combinación de los materiales de pared utilizados proveen foto protección efectiva del 80 % al extracto, respecto al extracto expuesto a radiación UV sin encapsular (32 % de oxidación relativa) después de 148 h de exposición. Los datos obtenidos son similares a los reportados por Ramos-Hernández et al. (2018) quienes obtuvieron una fotoprotección del 88 % en la encapsulación de β-caroteno utilizando fructanos de agave. La fotoprotección se debió a que los polisacáridos por su estructura tienen la capacidad de absorber y reflejar la radiación UV a través de los grupos carbonilo que funcionan como cromóforos, evitando que las radiaciones penetren al interior de las cápsulas (Wondraczek et al., 2011).
Inhibición in vivo de los hongos de interés comercial
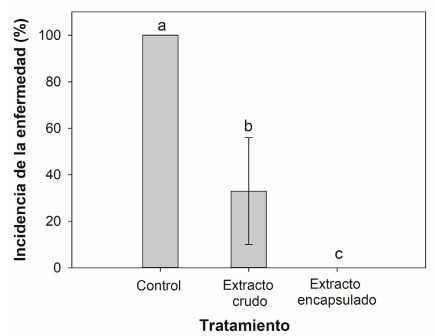
La efectividad de las cápsulas obtenidas se evaluó mediante pruebas de inhibición in vivo en diferentes frutas de interés comercial, tales como naranja y arándano. La prueba de severidad de P. digitatum en naranjas mostró diferencia significativa (P > 0.05) entre los controles y el tratamiento con las cápsulas. Se observó que las cápsulas con extracto de hoja de mango redujeron en un 70 % la lesión causada por P. digitatum (Figura 2A). Sin embargo, no existieron diferencias significativas respecto a la incidencia (80 %) (Figura 2B). Los resultados obtenidos superan a los presentados por Pérez-Alfonso et al. (2012), quienes utilizaron por separado carvacrol y timol, logrando reducir la severidad de P. digitatum en un 40 % después de 72 h en naranjas utilizando concentraciones de 50 a 250 µL/L.
Figura 2 Actividad antifúngica del extracto de hoja de mango crudo y encapsulado contra P. digitatum en naranjas. En cada gráfica los valores con la misma letra no son estadísticamente diferentes (P < 0.05). Las barras representan la media y las líneas verticales la desviación estándar. A) diámetro de la lesión y B) incidencia de la enfermedad.

Figure 2: Antifungal activity of crude and encapsulated mango leaf extract against P. digitatum in oranges. In each graph, the values with the same letter are not statistically different (P < 0.05). The bars represent the mean and the vertical lines the standard deviation. A) lesion diameter and B) incidence of the disease.
De acuerdo a la composición fitoquímica del extracto, según Martínez et al. (2017) el ácido clorogénico puede aumentar la permeabilidad de la membrana celular de los fitopatógenos. Por otra parte, el ácido cafeico induce a la desorganización de la membrana celular (Santiago et al., 2010). Los efectos que puede producir el ácido cafeico son malformaciones de las hifas, desorganización de la membrana celular y fuga de líquido citoplasmático (Gatto et al., 2011). Además, el ácido cumárico produce una alteración de la membrana debido a los grupos hidroxilos (Hernández et al., 2021). Por otra parte, la alta reducción de la severidad se puede atribuir a que los materiales utilizados para la encapsulación pueden formar películas en el epicarpio del fruto, facilitando la adherencia y liberación de los compuestos encapsulados (Felton, 2013; Chaumun et al., 202).
Adicionalmente, los arándanos empleados como control mostraron un 100 % de incidencia de B. cinerea, mientras que los arándanos tratados con las cápsulas mostraron un 0 % de incidencia (Figura 3). Este resultado indicó que las cápsulas con extracto de hoja de mango pueden emplearse como método preventivo en estos frutos. Los resultados obtenidos son similares a los reportados por Romeo et al. (2015) quienes al utilizar una concentración de 10 mg/mL de extracto fenólico de hojas de zumaque redujeron la incidencia en un 92 %.
En lo que respecta a B. cinerea, el efecto del ácido clorogénico podría causar lisis celular y cambios en la permeabilidad de la membrana (Ma et al., 2018). Los compuestos fenólicos como el ácido cafeico pueden causar cambios en la morfología celular y en la membrana (Rao et al., 2010). Asimismo, el ácido cumárico puede desestabilizar la membrana celular afectando con ello su polaridad (Morales et al., 2017).
Conclusiones
El secado por aspersión, con el uso de materiales de pared adecuados, es una tecnología eficiente para la encapsulación, con la que se obtienen partículas con características fisicoquímicas deseables que permiten la estabilización de los CAVB. Las cápsulas permitieron una liberación adecuada del extracto para el control de los hongos fitopatógenos, reduciendo la incidencia de P. digitatum en naranjas y severidad de B. cinerea en arándanos. Se demostraron las excelentes capacidades de la goma arábiga y alginato de sodio para crear una coraza alrededor de los compuestos de alto valor biológico con efecto termo y fotoprotector. Las microcápsulas de extracto polifenólico de hoja de mango se presentan como una alternativa viable y efectiva para el control de frutos de interés comercial como naranjas y arándanos.











 nueva página del texto (beta)
nueva página del texto (beta)