Introducción
La hipoglucemia hiperinsulinémica persistente de la infancia (HHPI), antes conocida como nesidioblastosis1, fue descrita por primera vez por George Laidlaw en 19382. Es una enfermedad poco frecuente que provoca hipoglucemia hiperinsulinémica (HH) de origen pancreático en un 0.5 a 5% de los pacientes pediátricos3, generalmente causando hipoglucemia posprandial e hiperinsulinismo endógeno4.
Los síntomas resultan de una respuesta neurogénica con activación simpática o parasimpática. En lactantes incluyen hipotonía, palidez, apneas, llanto débil, temblores e irritabilidad5. En niños mayores, mareos, sudoración fría, pérdida de consciencia, memoria y capacidad de reacción6.
El diagnóstico se establece con niveles de glucosa persistentes por debajo de 50 mg/dl. Tras el nacimiento, la glucosa desciende a 56 mg/dl a las 2 horas, aumenta a 63 mg/dl entre las 2 y 24 horas, y alcanza 68 mg/dl a las 24 horas, para luego disminuir a 67 mg/dl a las 48 horas7. Los pacientes muestran niveles elevados de insulina, que normalmente se suprime con hipoglucemia8, y se vuelve indetectable cuando la glucosa cae por debajo de 54 mg/dl9. También presentan niveles altos de péptido C (VN 0.5-2 ng/ml)6.
La HHPI se caracteriza por hallazgos histológicos típicos, como hipertrofia e hiperplasia de los islotes pancreáticos y la formación de nuevos islotes a partir del epitelio ductal3.
Es crucial identificar las diversas causas de HH para un diagnóstico diferencial preciso. Entre las más comunes se encuentran la restricción del crecimiento intrauterino, eritroblastosis fetal, asfixia perinatal, diabetes materna y ciertos medicamentos, como las sulfonilureas, que provocan hipoglucemia transitoria. Las formas congénitas de HH, de origen genético, incluyen mutaciones que alteran los canales de potasio en las células β pancreáticas o la sobreexpresión de la enzima glutamato deshidrogenasa, afectando la secreción de insulina. Es esencial descartar estas causas para un diagnóstico y tratamiento adecuado10.
En estos pacientes, los tratamientos incluyen diazóxido, análogos inhibidores del crecimiento, antagonistas de canales de calcio e inhibidores de la α-glucosidasa6.
La nesidioblastosis se diagnostica erróneamente como insulinoma nodular6. Un diagnóstico temprano y un tratamiento oportuno son esenciales para prevenir retrasos en el desarrollo y daños neurológicos11.
Los rarámuri, también conocidos como tarahumaras, son un pueblo indígena que habita principalmente en la Sierra Tarahumara, Chihuahua, México. Esta región remota y montañosa, caracterizada por profundos cañones y mesetas, ha permitido la preservación de su cultura y tradiciones a lo largo del tiempo. Su lengua principal, el rarámuri, pertenece a la familia lingüística uto-azteca. Son ampliamente reconocidos por su fuerte identidad cultural y su notable resistencia frente a la colonización, lo que les ha permitido mantener sus costumbres y estilo de vida por generaciones.
Casos clínicos
Caso 1
Paciente de sexo masculino de 4 días, perteneciente a la etnia rarámuri, sin antecedentes familiares relevantes. Es el tercer embarazo de la madre, sin control prenatal, y nació por cesárea debido a compromiso fetal, con un peso de 3,850 g y una puntuación de la escala de APGAR (apariencia, pulso, gestos, actividad y respiración) de 8/8. Fue ingresado en la unidad de cuidados neonatales (UCIN) por dificultad respiratoria e hipoglucemias graves (< 20 mg/dl), y posteriormente trasladado al Hospital Infantil de Especialidades (HIE) con diagnóstico de neumonía y para el manejo de hipoglucemias refractarias, presentando una glucemia de 20 mg/dl.
Exploración física: peso 4,290 g, talla 54 cm, frecuencia cardiaca 147 lpm, frecuencia respiratoria 62 rpm y temperatura de 36.8 °C, sin otras alteraciones.
Resultados de laboratorio: hemoglobina 12.9 g/dl, hematocrito 36.3%, leucocitos 21.7 ×103/μl, plaquetas 200 ×103, ácido úrico 2.7 mg/dl, nitrógeno ureico 1.8 mg/dl, creatinina 0.4 mg/dl, glucosa 27 mg/dl. Tamiz metabólico ampliado normal, cortisol 9.9 μg/ml, hormona del crecimiento 4.9 ng/ml, insulina 79.6 μU/ml y péptido C 5.2 ng/ml.
Se inició tratamiento con solución glucosada a 12 g/kg/min, además de alimentación con fórmula y maicena (4 g/kg/dosis). Se realizó una pancreatectomía subtotal del 90%, con biopsia intraoperatoria, que confirmó el diagnóstico de HHPI (Fig. 1).
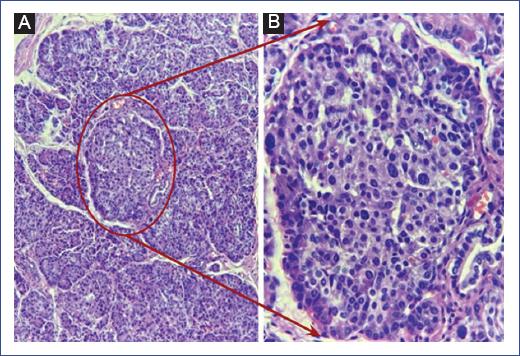
Figura 1 Biopsia de pancreatectomía y reporte histopatológico. A: corte histológico del páncreas teñido con hematoxilina y eosina 10x; se observan islotes de Langerhans aumentados de tamaño (círculo rojo) y unidades ductoinsulares ocasionales. B: corte histológico del páncreas 40x (aumento de imagen A); islotes de Langerhans aumentados de tamaño con células insulares afectadas de manera difusa.
El paciente fue dado de alta con octreótida (12.5 μg cada 6 horas) por episodios leves de hipoglucemia (40-48 mg/dl). Actualmente, se encuentra estable.
Caso 2
Paciente de sexo masculino de 3 días, también de la etnia rarámuri, sin antecedentes familiares relevantes. Nació por cesárea debido a preeclampsia materna, con una puntuación de la escala de APGAR de 7/9 y necesidad de un ciclo de ventilación por presión positiva. El Capurro indicó 41 semanas de gestación. Ingresó al HIE por hipoglucemias recurrentes desde el nacimiento, con valores tan bajos como 18 mg/dl.
Exploración física: peso 4,100 g, talla 52 cm, glucosa 207 mg/dl, tensión arterial 88/65 mmHg, frecuencia cardiaca 153 lpm, sin otras alteraciones.
Resultados de laboratorio: hemoglobina 20 g/dl, hematocrito 67.1%, plaquetas 39 ×103, leucocitos 9.04 ×103/μl, ácido úrico 3.4 mg/dl, nitrógeno ureico 4.67 mg/dl, creatinina 0.60 mg/dl, glucosa < 20 mg/dl, insulina 20.4 μU/ml, cortisol 0.80 μg/ml, péptido C 5.1 ng/ml, hormona del crecimiento 4.4 ng/ml, prolactina 21.45 ng/ml. Los niveles elevados de insulina y la glucosa baja, junto con un cortisol bajo, indicaron la necesidad de hidrocortisona. La gammagrafía reveló una lesión compatible con insulinoma (Fig. 2).
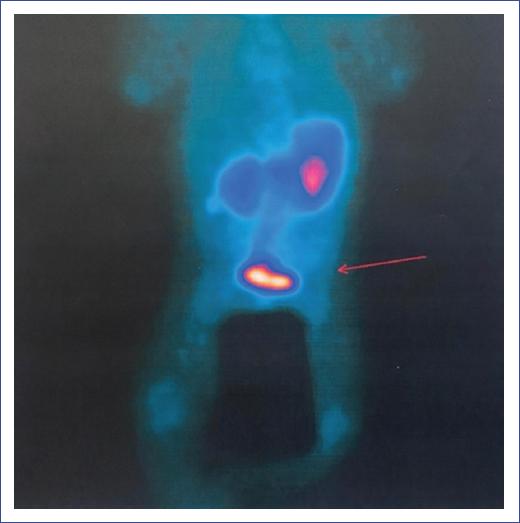
Figura 2 Gammagrafía pancreática. Se identificó un patrón anómalo en la región mesogástrica, donde se observó un aumento en la captación y metabolismo del marcador.
Se inició tratamiento con solución glucosada a 14 g/kg/min y octreótida. Se realizó una pancreatectomía subtotal del 95%, con biopsia confirmando el diagnóstico de HHPI difusa. El paciente actualmente se encuentra estable, bajo tratamiento con octreótida y alimentación complementada con maicena, mostrando una respuesta parcial al tratamiento. Se capacitó a la madre para el cuidado del paciente.
Caso 3
Paciente de sexo femenino de 3 días, segunda gestación, nacida por cesárea, con un peso de 3,240 g. Fue trasladada a la UCIN por hipoactividad y rechazo de la vía oral. Al ingresar a urgencias del HIE, presentaba una glucemia capilar de 15 mg/dl, sin otras alteraciones.
Exploración física: peso 3,240 g, talla 51 cm.
Resultados de laboratorio: hemoglobina 16.80 g/dl, hematocrito 55.60%, plaquetas 263 ×103, leucocitos 10.71 ×103/μl, ácido úrico 6.7 mg/dl, nitrógeno ureico 23.83 mg/dl, creatinina 1 mg/dl, glucosa 15 mg/dl. Perfil tiroideo normal, cortisol 8.1 μg/ml, ACTH 58 pg/ml, insulina 34 μU/ml, péptido C 5.4 ng/ml.
Se inició tratamiento con solución glucosada a 10 g/kg/min, además de alimentación con fórmula, tolerando hasta 168.16 ml/kg/día. Se realizó una pancreatectomía del 65%, confirmando el diagnóstico de HHPI mediante biopsia. Fue dada de alta por mejoría clínica con tratamiento de diazóxido a 5 mg/kg/día. Actualmente, se encuentra estable sin episodios de hipoglucemia.
Discusión
El término HHPI describe todas las formas de hiperinsulinismo congénito persistente en niños, asociadas a anomalías congénitas y enfermedad pancreática. En neonatos y lactantes, los síntomas comunes son hipotonía, palidez, apneas, llanto débil, temblores e irritabilidad5. En niños mayores, los síntomas incluyen ansiedad, temblor, palpitaciones, debilidad, fatiga, visión borrosa, confusión, convulsiones, déficit neurológico y coma12. En nuestros pacientes se presentaron hipoglucemia, debilidad y convulsiones.
Los pacientes con HHPI suelen presentar un tamaño superior al promedio debido al efecto promotor del crecimiento de la insulina13. En dos de nuestros casos, los pacientes tenían un peso al nacer que superaba el percentil 75.
El diagnóstico de HHPI es principalmente histológico, con criterios que incluyen aumento en el tamaño y número de células β en los islotes de Langerhans, incremento en islotes periductales, núcleos hipercromáticos, citoplasma claro y exclusión de insulinoma por microscopia e inmunohistoquímica14. En nuestros casos, los reportes histopatológicos describen islotes de Langerhans hipertróficos y unidades ductoinsulares afectadas. Sin embargo, las pruebas de imagen no detectaron la lesión; solo en un paciente se identificó una lesión por gammagrafía, mientras que en los demás no hubo anomalías.
Las pruebas de laboratorio muestran niveles de glucosa en sangre < 50 mg/dl, acompañados de síntomas de hipoglucemia, con insulina plasmática > 6 μU/ml14 y péptido C elevado (> 2 ng/ml)15. Normalmente, los niveles de insulina disminuyen cuando la glucosa plasmática cae < 80-85 mg/dl y se detienen entre 45 y 54 mg/dl7. En nuestros pacientes, todos presentaron glucosa < 20 mg/dl, insulina > 20 μU/ml y péptido C alrededor de 5.1 ng/ml.
El tratamiento de la HHPI comienza con manejo médico, que incluye glucosa y medicamentos como diazóxido, análogos del crecimiento, antagonistas de canales de calcio e inhibidores de la α-glucosidasa. La mayoría requiere cirugía, con pancreatectomía casi total recomendada por su bajo riesgo de recidiva16. En nuestros pacientes se utilizó glucosa intravenosa, alimentación oral y medicamentos como octreótida y diazóxido. Como las hipoglucemias no se controlaron completamente, se realizó una pancreatectomía subtotal en los tres casos, y los pacientes continúan con medicamentos a dosis bajas.
El diazóxido es el tratamiento de primera línea en neonatos y lactantes, con una dosis inicial de 5 mg/kg/día, y los valores objetivo no deben exceder los 20 mg/kg/día17.
Hasta ahora no se han reportado casos de HHPI en pacientes de la etnia rarámuri en la literatura médica, lo que resalta la importancia de divulgar estos casos clínicos en poblaciones vulnerables. La difusión de estos casos clínicos es fundamental para facilitar diagnósticos tempranos y oportunos en pacientes con hipoglucemias refractarias.











 nueva página del texto (beta)
nueva página del texto (beta)


