Introducción
El mundo identifica el cáncer infantil como una de las principales causas de mortalidad en niños y adolescentes. Para países desarrollados se reporta que más del 80% de los niños afectados por la patología se recuperan; sin embargo, para aquellos países en vía de desarrollo la tasa de curación se acerca al 20%1. Los países en vía de desarrollo registran bajas tasas de supervivencia, que se asocian con las limitaciones para obtener un diagnóstico preciso y la baja accesibilidad a los tratamientos. De hecho, estar en dicho contexto aumenta la probabilidad de abandono al tratamiento, muerte por toxicidad y recidivas, relacionándose con las restricciones para acceder a los medicamentos y tecnologías1.
En Colombia, la Cuenta de Alto Costo (CAC) del año 2021 reportó a 7,801 menores de 18 años con algún tipo de cáncer, con mayor incidencia de leucemia linfoide aguda, tumores del sistema nervioso central y los linfomas no Hodgkin. Las regiones de Colombia con mayor mortalidad fueron Bogotá 50.4, Amazonía 34.1, Central 28.22, Pacífico 24.85, Oriental 22.92 y Caribe 20.7 (cifras del 2021) por cada millón de habitantes menores de 18 años; encontrándose un aumento de 1,583 casos nuevos de cáncer comparado con las cifras del año 20182, donde se reportó una incidencia de 6,218 menores diagnosticados con cáncer, representando un incremento del 20.3% de diagnósticos con esta enfermedad.
Un diagnóstico correcto es vital para tratar a los niños, porque cada cáncer requiere un régimen terapéutico concreto que puede incluir cirugía, radioterapia o quimioterapia3. Cuando el cáncer es detectado en la fase inicial y de forma temprana, la probabilidad de responder favorablemente al tratamiento es más alta, y secundario a esto, también se aumenta la tasa de supervivencia que si se identifica en fases tardías. Al ser instaurada la terapia de manera temprana, los esquemas pueden ser de baja intensidad y por ello se logra mitigar algunos efectos y manifestaciones clínicas.
El diagnóstico de cáncer en un niño es una situación que impacta y modifica la estructura y dinámica familiar, debido a las implicaciones que reviste la gravedad de la patología, los efectos del tratamiento y la probabilidad latente de morir4. Los cambios físicos y las molestias en niños con cáncer son ampliamente descritas, entre las que se encuentra el dolor, el miedo, la angustia y la desesperanza, entre otras muchas.
Los niños que se enfrentan a un tratamiento contra el cáncer deben experimentar síntomas y molestias que alteran sus actividades diarias y la vida misma, situación que impacta a los padres y hermanos. Es necesario que el equipo de salud tenga la capacidad de evaluar la presencia de síntomas y molestias, para poderlas controlar y de esa manera desplegar intervenciones que favorezcan la resiliencia, calidad de vida y el afrontamiento de la enfermedad5.
La calidad de vida relacionada con la salud (CVRS) y la fatiga se aceptan como mediciones desde la perspectiva del sujeto que experimenta la enfermedad, como indicadores esenciales en la evaluación de resultados que supera medidas tradicionales como la morbimortalidad y la expectativa de vida. Es muy importante tener datos del desenlace de la enfermedad en cada fase de esta que contemplen la percepción del paciente y permitan develar los deseos y motivaciones en el proceso de la toma de decisiones y la percepción del sujeto en la calidad de la asistencia sanitaria.
Teniendo presentes las implicaciones del cáncer tanto para el niño como para la familia es necesario hablar de la CVRS, medida que permite a los cuidadores valorar el impacto que genera la enfermedad y los tratamientos derivados de esta sobre el ámbito físico, psicológico y social6. La medición del impacto de las intervenciones sobre la salud de los sujetos ya no requiere únicamente la elaboración de indicadores tradicionales, por lo que se hace necesario medir variables asociadas que permitan establecer de forma integral el impacto de la enfermedad y el tratamiento, así como la orientación de los esfuerzos terapéuticos.
Desde esta perspectiva, para los programas hospitalarios que ofrecen tratamiento y seguimiento a los niños con cáncer es primordial comprender cómo la CVRS se comporta en cada fase de la enfermedad y en cada circunstancia que se desprende de esta. Por esta razón, la implementación de escalas validadas para el seguimiento de indicadores complejos como la calidad de vida y de evaluaciones funcionales de enfermedades crónicas es esencial en los escenarios de cuidado directo y programas de seguimiento. En la región se cuenta con resultados de investigación en los que se ha empleado la escala PedsQL Cancer Module (Inventario Pediátrico de Calidad de Vida Módulo Cáncer)7 y FACIT-F Peds (Functional Assessment of Chronic Illness Therapy, Evaluación funcional de la terapia de enfermedades crónicas o agotamiento)8, que han orientado la toma de decisiones en entornos clínicos y de seguimiento de pacientes en el campo de la consulta externa. Por ello, este trabajo se enfocó en describir cómo se comporta la calidad de vida en los niños con cáncer y cómo la perciben los padres de estos, de igual manera se exploró el nivel de fatiga percibido por los niños, lo que permitió un análisis respecto al cansancio y niveles de energía percibidos.
Método
Se desarrolló un estudio observacional analítico de una cohorte de niños y adolescentes con edades de 2 a 18 años durante el periodo de estudio con un muestreo por conveniencia, que tuvieran diagnóstico de algún tipo de cáncer y que se encontraran en alguna fase del tratamiento de dicha patología. Se definió desde el protocolo que serían excluidos aquellos pacientes con diagnóstico de cáncer que no tuvieran instaurado tratamiento o que se encontrarán en estado crítico, o que los padres no contarán con habilidades de lectoescritura.
La recolección de datos se realizó mediante el registro de variables sociodemográficas y variables clínicas individuales. Además, se aplicaron los instrumentos PedsQL Cancer Module7 y FACIT-F Peds tanto en los pacientes incluidos como en sus padres o cuidadores.
El primer instrumento es un producto derivado del PedsQL Versión 3.0 - español (Colombia), diseñado para la evaluación genérica de la calidad de vida autorreportada por niños que enfrentan la enfermedad, así como la calidad de vida informada por los padres en el contexto colombiano7. Esta escala abarca 27 ítems distribuidos en ocho dominios que evalúan diversas dimensiones vinculadas con la calidad de vida, presentando adaptaciones en su diseño según la edad de los pacientes. Para este estudio se contó con la firma de un acuerdo de utilización y se recibieron instrucciones de uso y gestión de los datos según el manual de los autores. Los dominios que contempla PedsQL Cancer Module son los siguientes:
– Dolor y molestia (2 ítems).
– Náuseas (5 ítems).
– Ansiedad frente a los procedimientos (3 ítems).
– Ansiedad frente a los tratamientos (3 ítems).
– Preocupaciones (3 ítems).
– Problemas cognitivos (5 ítems).
– Apariencia física percibida (3 ítems).
– Comunicación (3 ítems).
Cada uno de los ocho dominios, integra diferentes preguntas que pretenden indagar por la presencia de dichas manifestaciones en los últimos 30 días y en la última semana. El rango de posibles respuestas varía desde 0 «nunca ha sido un problema» hasta 4 «casi siempre ha sido un problema». Se emplea una escala Likert de 5 puntos, que varía desde 0 (nunca) hasta 4 (casi siempre), a excepción de los informes de niños de 5 a 7 años, quienes utilizan una escala Likert de 3 puntos (0 = nunca, 2 = a veces, 4 = casi siempre), la cual se combina con un apoyo visual representado por expresiones faciales (0 = cara feliz, 2 = cara neutral, 4 = cara triste). Cada puntuación individual en los ítems se invierte y luego se transforma de manera lineal en una escala de 0 a 100 (0 = 100, 1 = 75, 2 = 50, 3 = 25, 4 = 0). Las puntuaciones superiores reflejan una mayor calidad de vida en relación con la salud7.
Adicionalmente, se aplicó el cuestionario FACIT-F Peds, el cual evalúa otras enfermedades y afecciones crónicas. Este es un instrumento diseñado para evaluar la sensación de fatiga en niños y adolescentes de 8 a 18 años durante los últimos siete días. Incluye 13 ítems de tipo Likert que evalúan dos dimensiones. La puntuación para la dimensión de cansancio varía de 0 a 44, mientras que la dimensión de energía se evalúa en una escala de 0 a 8. También esta escala permite generar un score global, donde unas puntuaciones más elevadas señalan una menor sensación de fatiga diaria8,9. La aplicación de los cuestionarios se realizó en las habitaciones de los pacientes, en las casas de los pacientes o en la consulta externa de los pacientes, siempre garantizando un ambiente libre de ruidos y de factores distractores.
El estudio contó con aval ético del comité de Colsubsidio con acta y aval 300-1 que verificó la idoneidad del consentimiento y asentimiento informado.
Análisis estadístico
Se realizó un análisis estadístico descriptivo y se calcularon medidas de tendencia central y de dispersión, como la media, la mediana, la moda, la desviación estándar y el rango intercuartílico (RIC), para obtener información sobre el comportamiento de las variables.
Se realizó el cálculo de los puntajes acorde a la guía de PedsQL módulo de cáncer para niños y padres y posteriormente se realizó pruebas de hipótesis con un alfa de 0.05 para determinar si existieron diferencias en las medianas de las diferentes dimensiones del PedsQL entre los niños y los padres con el test de U de Mann-Whitney.
Para estimar la confiabilidad se aplicaron las pruebas de reproducibilidad test-retest evaluada mediante el coeficiente de correlación intraclase (CCI) y el coeficiente alfa de Cronbach. Un CCI menor de 0.40 indica una concordancia pobre, valores entre 0.41 y 0.60 una concordancia moderada, valores entre 0.61 y 0.80 una buena concordancia y > 0.80 una concordancia excelente10. Por su parte, el coeficiente alfa de Cronbach varía de 0 a 1, considerándose aceptables valores superiores a 0.711.
Por último, se realizó un análisis multivariante con un modelo de regresión de Poisson con variable dependiente el puntaje total de FACIT-F y con variables independientes la sintomatología reportada por la población de estudio y variables relacionadas con la patología. Se seleccionó el modelo más parsimonioso con el menor valor del criterio de Akaike (AIC), la bondad de ajuste del modelo se examinó por medio el pseudo R cuadrado de Nagelkerke y la prueba de la devianza y la sobredispersión del modelo Poisson fue valorada para la confirmación del modelo. La información fue procesada y analizada con el software estadístico R versión 4.3.
Resultados
Se incluyeron 46 pacientes pediátricos con diagnóstico hematooncológico. Se obtuvieron diferentes variables sociodemográficas, antropométricas, clínicas y de calidad de vida en cada uno de los pacientes y sus familias. En la tabla 1 se resumen las características de los pacientes incluyendo edad, sexo, diagnóstico y otras variables relevantes de su entorno.
Tabla 1 Características sociodemográficas de los niños con cáncer que se encontraban en tratamiento en una institución de alta complejidad
| Información demográfica | n (%) |
|---|---|
| Edad (años) | |
| Mediana (RIC) | 11 (8-14) |
| Sexo | |
| Masculino | 30 (65.2) |
| Estrato socioeconómico | |
| Bajo (1-2) | 34 (73.9) |
| Medio (3) | 11 (23.9) |
| Alto (4) | 1 (2.2) |
| Tipo de afiliación | |
| Contributivo | 34 (73.9) |
| Subsidiado | 12 (26.1) |
| Procedencia | |
| Bogotá D.C. | 33 (71.7) |
| Otras ciudades | 13 (28.3) |
| Estructura parental | |
| Nuclear | 27 (58.7) |
| Monoparental | 12 (26.1) |
| Extensiva | 4 (8.7) |
| Reconstruida | 3 (6.5) |
| Asistencia escolar | |
| Sí | 34 (73.9) |
| Virtual | 17 (50) |
| Presencial | 17 (50) |
| Inasistencias regulares desde el diagnóstico (n = 35) | |
| Sí | 19 (54.3) |
| Reducción de rendimiento escolar (n = 35) | |
| Sí | 13 (37.1) |
| Reducción de actividades de entretenimiento (n = 45) | |
| Sí | 25 (55.6) |
| Apoyo familiar | |
| Excelente | 16 (34.8) |
| Bueno | 12 (26.1) |
| Regular | 8 (17.4) |
| Deficiente | 10 (21.7) |
| Calidad de relaciones sociales (n = 32) | |
| Buena | 22 (68.8) |
| Regular | 7 (21.9) |
| Mala | 3 (9.4) |
RIC: intervalo intercuartílico.
Entre los pacientes incluidos, la edad mediana entre ambos sexos fue de 11 años (8-14). Treinta (65.2%) pacientes fueron de sexo femenino, encontrándose una razón femenino: masculino de 1:1,8. El 71.7% (n = 33) de los pacientes y sus familias provenían de la capital del país, el resto procedían de ciudades secundarias o zonas rurales. En 41 pacientes se tenía información disponible relacionada con el diagnóstico principal. El cáncer más frecuente fue la leucemia (n = 23/41, 56.1%), seguido de los tumores óseos (n = 6/41, 14.6%) y los linfomas (n = 4/41, 9.7%). En relación con los estadios de la enfermedad, el 22.6% (n = 7/31) se encontraba en estadio 1 y el 12.9% (n = 4/31) en estadio 4. En relación con el tratamiento, el 69.2% (n = 27/39) recibió quimioterapia, el 12.8% (n = 5/39) fue llevado a cirugía y 3 pacientes (7.7%) recibieron quimioterapia y radioterapia concomitante. El tiempo mediano de tratamiento fue de 4 meses (3-10) (Tabla 2).
Tabla 2 Características clínicas de diagnóstico y tratamiento de pacientes que se encontraban en tratamiento en una institución de alta complejidad
| Información clínica | n (%) |
|---|---|
| Diagnóstico (n = 41) | |
| Neoplasias hemato-linfoides | |
| Leucemia | 23 (56.1) |
| Linfoma de Hodgkin | 3 (7.3) |
| Otros linfomas | 1 (2.4) |
| Neoplasias sólidas | |
| Osteosarcoma | 6 (14.6) |
| Otros sarcomas | 3 (7.3) |
| Cáncer de SNC | 1 (2.4) |
| Tumor de Willms | 1 (2.4) |
| Otros | 3 (7.3) |
| Edad de diagnóstico (años) | |
| Mediana (RIC) | 6 (4-12) |
| Tratamiento (n = 39) | |
| Cirugía | 5 (12.8) |
| Quimioterapia | 27 (69.2) |
| Radioterapia | 2 (5.1) |
| Quimio-radioterapia | 3 (7.7) |
| Trasplante de células progenitoras | 2 (5.1) |
| Tiempo de tratamiento (meses) | |
| Mediana (RIC) | 4 (3-10) |
| Ingresos a UCI (n = 21) | |
| > 1 ingreso | 7 (33.3) |
RIC: intervalo intercuartílico; SNC: sistema nervioso central; UCI: unidad de cuidados intensivos.
Dentro de los síntomas físicos más frecuentes reportados por los pacientes se encuentran las náuseas (n = 15/46, 32.6%), la fatiga/adinamia (n = 15/46, 32.6%), la hiporexia (n = 12/46, 26.1%) y la pérdida de pelo (n = 11/46, 23.9%), entre otros. Los síntomas psicológicos más frecuentes fueron la irritabilidad (n = 14/46, 30.4%), la tristeza (n = 12/46, 26.1%) y el miedo (n = 11/46, 23.9%), entre otras cosas.
En relación con los resultados del PedsQL se observó que el puntaje total global para los niños fue de Q2 (cuartil 2 o mediana) de 69.4 y un rango intercuartílico (RIC) 53.5-83.1 y en los padres un puntaje similar, Q2 de 68.5 (RIC: 55.6-83.5). Al analizar cada una de las dimensiones se evidenció que los puntajes más altos en Q2 fue de 80 para náuseas tanto para los padres como para los niños (RIC: 72.5-92.5) y (RIC: 70-91.3), seguido de apariencia física percibida en niños (Q2: 79.2; RIC: 52.1-91.7) y en padres (Q2: 83.3; RIC: 66.7-100) (Fig. 1). Se exploró si existían diferencias en el puntaje global y por dimensión entre los padres y los niños. La única diferencia estadísticamente significativa fue la dimensión de ansiedad en los procedimientos (p = 0.036) siendo el puntaje de la mediana más alta en el grupo de niños (Q2: 75; RIC: 52.1-100) y en padres menor (Q2: 50; RIC: 20.8-83.3) (Fig. 1). En las dimensiones restantes se observan puntajes similares para ambos grupos.
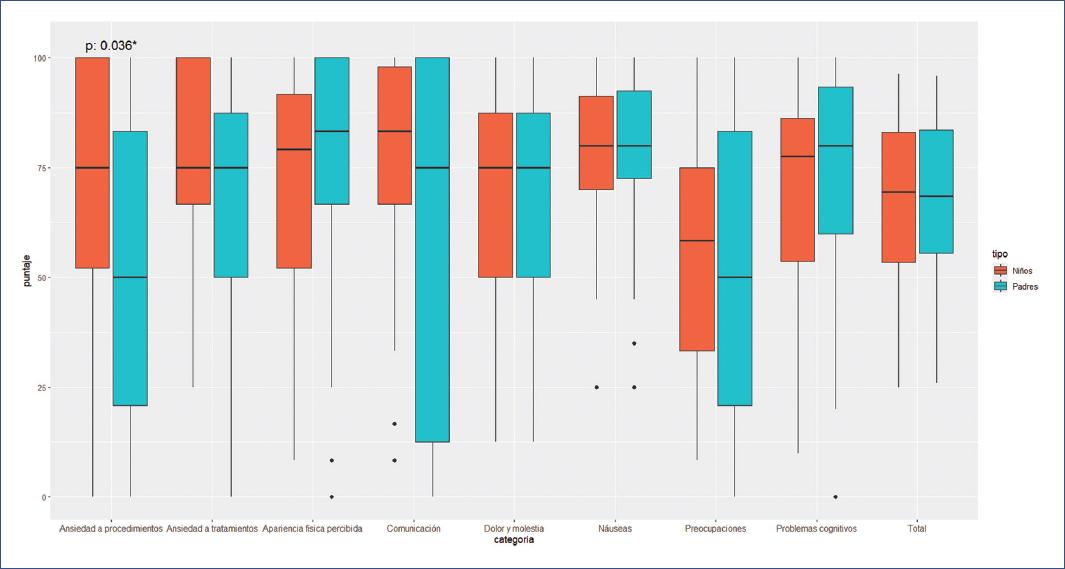
Figura 1 Puntaje total y por dimensiones del intrumento PedsQL Cancer Module (Inventario Pediátrico de Calidad de Vida Módulo Cáncer) niños y padres.
En relación con la confiabilidad entre las mediciones de los pacientes y sus padres, se realizó un CCI para cada uno de los dominios y para el total. Se encontró una concordancia excelente en los dominios de dolor y molestia (CCI: 0.85; intervalo de confianza del 95% [IC95%]: 0.69-0.93), ansiedad hacia los procedimientos (CCI: 0.95; IC95%: 0.88-0.98), problemas cognitivos (CCI: 0.83; IC95%: 0.65-0.92) y apariencia física (CCI: 0.94; IC95%: 0.86-0.97). La concordancia para el dominio de náuseas fue perfecta, y la concordancia de la valoración total de los dominios fue también excelente (CCI: 0.96; IC95%: 0.90-0.98). En la tabla 3 se detallan los CCI de todos los dominios.
Tabla 3 Coeficiente de correlación intraclase (CCI)
| Dominio PedsQL Cancer Module | CCI | IC95% |
|---|---|---|
| Dolor y molestia | 0.85 | 0.69-0.93 |
| Náuseas | 1.00 | |
| Ansiedad frente a los procedimientos | 0.95 | 0.88-0.98 |
| Ansiedad frente a los tratamientos | 0.68 | 0.39-0.84 |
| Preocupaciones | 0.78 | 0.54-0.89 |
| Problemas cognitivos | 0.83 | 0.65-0.92 |
| Apariencia física percibida | 0.94 | 0.86-0.97 |
| Comunicación | 0.37 | –0.02 a 0.66 |
| Total | 0.96 | 0.90-0.98 |
IC95%: intervalo de confianza del 95%.
Para la valoración de la sensación de fatiga se usó la escala FACIT-F aplicada en la población de estudio, donde se obtuvo una mediana de energía de 5 (RIC: 4- 5), cansancio (Q2: 11; RIC: 9-13) y un puntaje global de 15 (RIC: 13-18).
Por último, se realizó un modelo de regresión Poisson para determinar las variables de síntomas reportados por niños, así como las de características de su tratamiento. El modelo evidenció significancia estadística en la relación entre tener dispositivos médicos, náuseas y ansiedad con un menor puntaje en la escala FACIT-F. A su vez, se encontró una relación inversa entre meses de diagnóstico y el puntaje de FACIT-F (Tabla 4).
Tabla 4 Modelo de regresión de Poisson para puntaje FACIT-F en la población de estudio
| Variable | Error estándar | p valor | Exp (B) | IC 95% |
|---|---|---|---|---|
| Número previo de cirugías | 0.02194 | 0.4004 | 1.01 | 0.97-1.06 |
| Tener dispositivos médicos | 0.10681 | < 0.001 | 0.74 | 0.60-0.92 |
| Náuseas | 0.11393 | < 0.001 | 0.69 | 0.55-0.87 |
| Ansiedad | 0.12620 | < 0.001 | 0.67 | 0.52-0.86 |
| Horas de sueño | 0.04434 | 0.8755 | 1.00 | 0.92-1.1 |
| Meses de diagnóstico | 0.00532 | 0.0258 | 0.98 | 0.97-0.99 |
| Pseudo R cuadrado de Nagelkerke 0.70 | ||||
| Criterio de Akaike (AIC) 201.67 | ||||
| Test de sobredispersión p valor 0.07 | ||||
| Prueba de deviance < 0.001 | ||||
FACIT: Functional Assessment of Chronic Illness Therapy; IC95%: intervalo de confianza del 95%.
Discusión
Adentrarse en la complejidad del cáncer infantil brinda información relevante para optimizar la atención en salud de esta población. Al comprender mejor este fenómeno, se puede fortalecer el seguimiento clínico, tomar decisiones interdisciplinarias que sean precisas y enfocarse en las soluciones de los problemas específicos que enfrentan los niños y adolescentes con cáncer12, lo cual se alinea con el enfoque de esta investigación, en la que se logró recopilar información sobre diversos aspectos de la vida de los niños con cáncer y sus familias.
La muestra refleja las condiciones sociodemográficas y clínicas. La edad mediana de 11 años y la predominancia del sexo femenino (65.2%) son consistentes con reportes previamente realizados en estudios pediátricos de oncología13.
La conformación de los datos sociodemográficos, clínicos y relacionados con la calidad de vida permiten tener una aproximación a las necesidades, y conceptos que subyacen del hecho de experimentar una enfermedad y tratamiento complejo. Detallar el espectro de impacto de la enfermedad y del tratamiento en aquellos menores que experimentan cáncer es esencial para enfocar intervenciones y estrategias de seguimiento y control de necesidades de cuidado. En este sentido, en Colombia se han realizado pocos estudios sobre niños y adolescentes con enfermedades crónicas en cuanto a lo que sienten antes, durante y después del diagnóstico y del tratamiento. La mayoría de los estudios realizados en Colombia se centran en evaluar la calidad de vida de los adultos, pero no hay muchos estudios sobre los niños y adolescentes con cáncer14-16, lo que impulsa el fortalecimiento de estas áreas de conocimiento y la adopción de nuevas maneras de cuidar según emerge la nueva evidencia.
El predominio de leucemia está en línea con las tendencias globales de incidencia de cáncer en niños, donde la leucemia representa la mayoría de los casos17, sin embargo para nuestro estudio este tipo de cáncer está seguido por tumores óseos y linfomas lo cual es diferente a las cifras globales reportadas.
En cuanto al tratamiento, el tiempo promedio de tratamiento fue de cuatro meses y la mayoría de los niños recibieron quimioterapia; a algunos también se les realizó cirugía y en algunos casos se combinó la quimioterapia con radioterapia. Desde este punto de vista se contrasta con los resultados de un estudio realizado en Pakistán, donde se reportó que los pacientes en su mayoría estaban bajo quimioterapia durante la recolección de la información18, lo que refuerza la necesidad de que los proveedores de cuidado promuevan un enfoque multidisciplinario que aborde tanto los aspectos clínicos como los psicológicos, físicos y sociales que se pueden ver afectados por presencia de la enfermedad y el tratamiento mismo.
Los resultados del estudio muestran que los síntomas más comunes experimentados por niños en tratamiento oncológico incluyen náuseas, fatiga, pérdida del pelo e hiporexia. Estos síntomas son característicos de los efectos secundarios asociados con los tratamientos de cáncer, como la quimioterapia, que tiene impacto significativo en la calidad de vida. La presencia de náuseas y hiporexia sugiere desafíos en términos del control de síntomas molestos e indeseables, que adicionalmente se configuran como factores de riesgo para impactar el estado nutricional del paciente, ya que comprometen la ingesta adecuada y suficiente de alimentos y por ello marcan pautas sobre la necesidad de planear cuidados enfocados en estrategias nutricionales y de uso de fármacos para controlar dichos síntomas19. La fatiga, reportada en un tercio de los pacientes, compromete el rendimiento escolar y disminuye la interacción con pares, aspectos todos fundamentales para el desarrollo emocional y social del niño20. Por lo tanto, se debe entender y abordar la fatiga por medio de intervenciones multidisciplinarias que pueden incluir ajustes en el régimen de tratamiento, terapia física y apoyo psicosocial21.
Además, los síntomas psicológicos como irritabilidad, tristeza y miedo destacan la carga emocional que el tratamiento del cáncer impone a los niños. Estos efectos no solo afectan al paciente sino también a su familia, lo que subraya la necesidad de apoyo psicológico integral, como se ha reportado en otros estudios20,22. El manejo de estos síntomas debe ser una prioridad dentro de los programas de tratamiento, incorporando el asesoramiento y las terapias de apoyo para ayudar a los niños y sus familias a manejar mejor el estrés emocional asociado con la enfermedad y su tratamiento. Los datos del presente estudio confirman que existe una conexión significativa entre el agotamiento y todas las dimensiones de la CVRS en niños y adolescentes con un diagnóstico hematooncológico durante su tratamiento.
El análisis del PedsQL mostró que tanto niños como padres reportan impactos similares en términos de calidad de vida, aunque los niños reportaron mayor ansiedad relacionada con los procedimientos médicos. Este hallazgo sugiere que mientras los padres pueden estar al tanto de la disminución de la CVRS física, podrían no percibir completamente la ansiedad que sus hijos experimentan durante los tratamientos, como se refuerza en otros estudios23 y que hacen resaltar la importancia de comunicar efectivamente las experiencias y preocupaciones de los niños a sus cuidadores y proveedores de salud. Sin embargo, hay estudios que muestran que las mediciones reportadas por los padres pueden ser una herramienta útil para evaluar el estado de salud de los pacientes pediátricos con cáncer, especialmente en aquellos casos donde la comunicación directa con el paciente puede ser limitada16.
Por otra parte, cuando se realizó el análisis multivariante, este estudio evidenció cómo el cansancio en los pacientes pediátricos se asocia de manera estadística con el uso de dispositivos médicos, las náuseas y ansiedad. Sin embargo, es importante considerar que este análisis no abarca todos los posibles factores que podrían influir en el cansancio, como el apoyo psicológico y factores familiares, entre otros, que pueda haber recibido el grupo de pacientes durante este periodo o el impacto de su entorno social. Por lo tanto, estos resultados deben interpretarse dentro del contexto de las limitaciones de este estudio, se reconoce la importancia de generar más estudios que tengan en cuenta la experiencia de cansancio en los pacientes como factor multifactorial y que cuenten con un tamaño de muestra suficiente para mayor precisión de los estimadores, control de error tipo I y validez de los resultados16.











 nueva página del texto (beta)
nueva página del texto (beta)


