Introducción
La insuficiencia coronaria es un trastorno fisiopatológico caracterizado por un desbalance crítico entre la oferta de oxígeno al miocardio y su demanda metabólica. Este fenómeno tiene una representación electrocardiográfica distintiva, lo que ha consolidado al electrocardiograma (ECG) como una herramienta de diagnóstico esencial en el ámbito cardiológico, con una sensibilidad de hasta el 66% y una especificidad del 33.7%1,2.
Entre los conceptos fundamentales que emergen del estudio de las manifestaciones electrocardiográficas de la insuficiencia coronaria se encuentra la «corriente de lesión», fenómeno derivado de diferencias en los potenciales eléctricos entre el tejido lesionado y el sano. En este artículo se analizarán los procesos fisiopatológicos y las implicaciones clínicas de las corrientes de lesión.
Isquemia, lesión y necrosis
Desde el punto de vista electrofisiológico, el tejido miocárdico puede categorizarse en tres zonas principales durante un evento hipóxico: isquemia, lesión y necrosis; cada una con características específicas que afectan su comportamiento eléctrico.
La zona isquémica es una región que conserva una repolarización diastólica normal, pero presenta un retardo en la repolarización durante el ciclo cardiaco, lo que prolonga la duración de los potenciales monofásicos de activación, en particular a nivel de la meseta intermedia1 (Fig. 1).
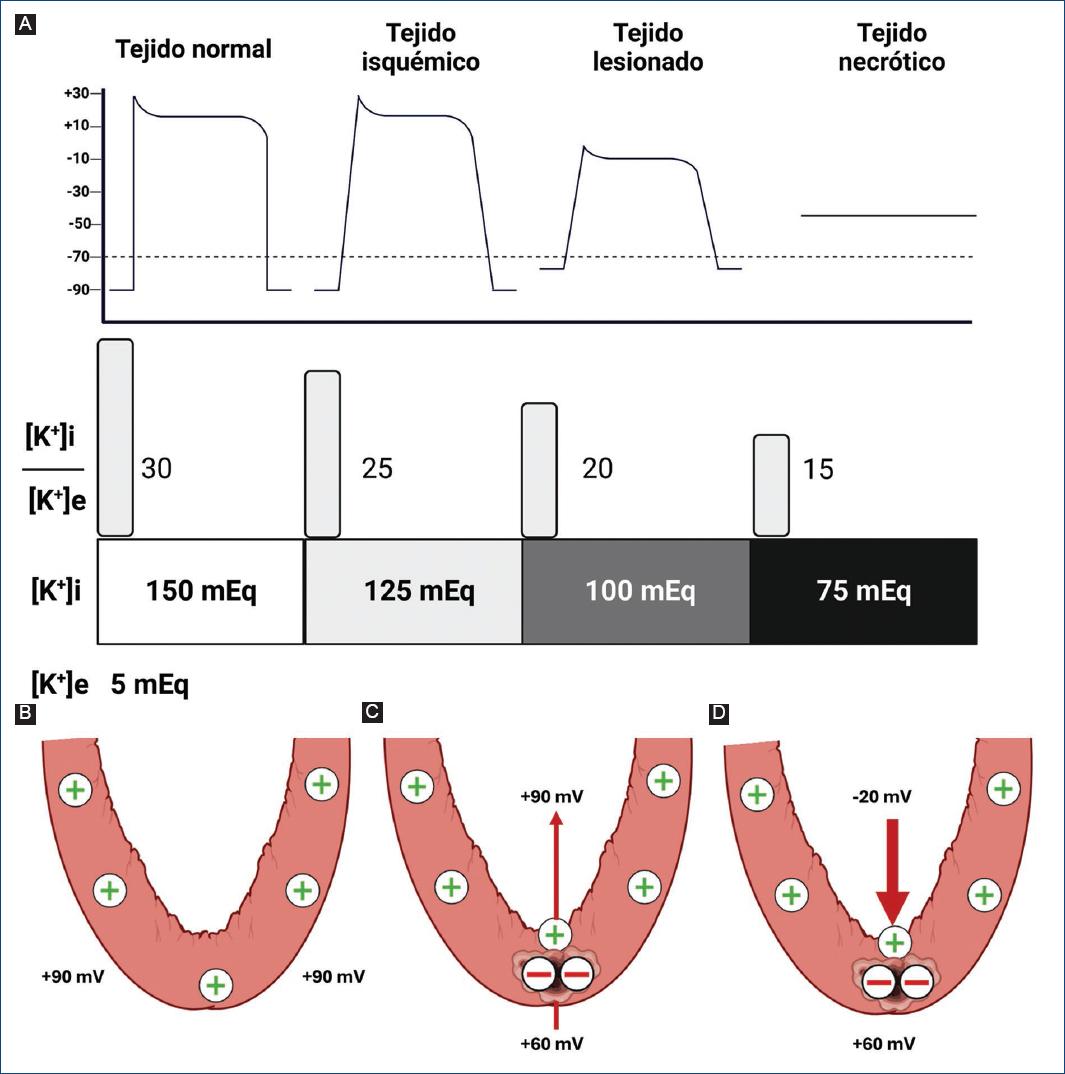
Figura 1 A: diferentes grados de despolarización diastólica en tejido normal, isquémico, lesionado y necrótico, comparado con la relación de potasio intra- y extracelular. Nótese que cuanto más se reduce la relación [K+i]/[K+e], más despolarización diastólica presenta el tejido, acercándose primero al potencial umbral (aumento del automatismo) hasta superarlo (pérdida de la excitabilidad). En la parte inferior, la imagen muestra los potenciales de membrana poniendo el 0 en el espacio intracelular y como positivo el extracelular. En el sano (B), el potencial de membrana es de 90mV. En diástole (C), la célula lesionada no puede repolarizarse por completo y es menos positiva que el tejido sano (corriente de lesión diastólica de 30 mV). Cuando se produce la despolarización (D), la zona sana se vuelve intensamente negativa respecto a la lesionada y se produce una corriente sistólica de lesión hacia la zona lesionada (80 mV). Al llegar a la diástole eléctrica, las polaridades vuelven a cambiar en la zona sana y se vuelve a la posición B (reinicio de la corriente diastólica de lesión).
La zona de lesión, en cambio, se caracteriza por una despolarización diastólica parcial, resultando en un gradiente de voltaje intramiocárdico. Las zonas más lesionadas muestran una menor polarización, lo que puede inducir automatismo anómalo y, en casos graves, extrasístoles o taquicardias ventriculares paroxísticas. Esta disfunción eléctrica tiene como base molecular la disfunción de la ATPasa de Na+/K+, lo que lleva a acumulación de K+ extracelular y Na+ y agua intracelular1,3 (Figs. 1 y 2).
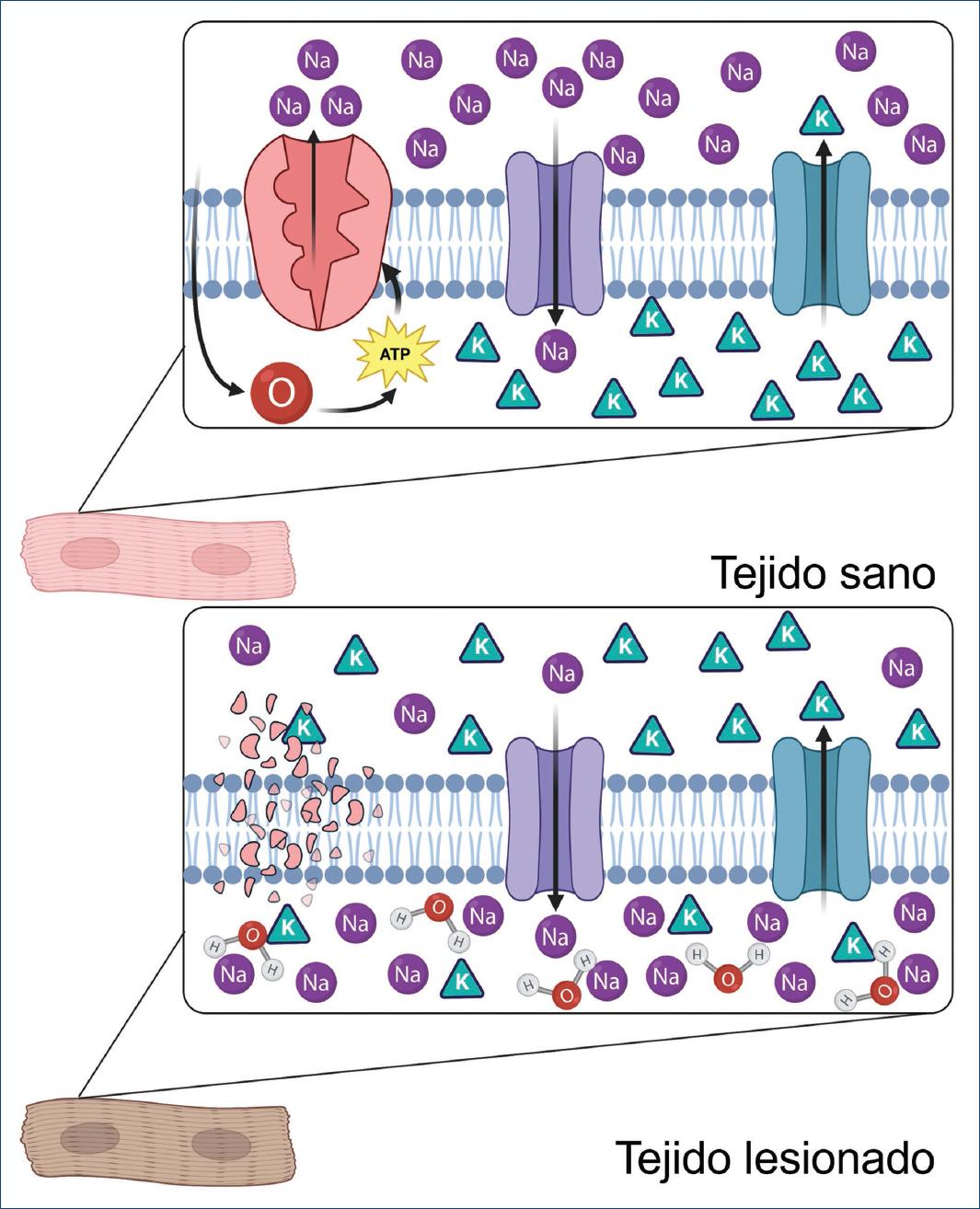
Figura 2 Actividad de la ATPasa de Na+/K+ y los canales iónicos de Na+ y K+ en tejido sano y lesionado.
La zona de necrosis es aquella que ha perdido por completo su capacidad de generar potenciales de acción. Actúa como un segmento inerte en términos eléctricos, sin contribuir al campo eléctrico global del corazón1,3.
Teoría de la corriente de lesión diastólica
En 1922, Pardee4 describió por primera vez la elevación del segmento ST como un signo de enfermedad coronaria, desencadenando un prolongado debate sobre su origen. Inicialmente, los electrocardiógrafos de la época introducían ajustes de base cero para facilitar la interpretación de los trazos, lo que desplazaba artificialmente el segmento ST hacia arriba. Con el tiempo, investigaciones como las de Nahum et al.5 revelaron que el intervalo TQ (diástole eléctrica) no era realmente isoeléctrico en caso de lesión, existiendo una corriente eléctrica durante la diástole, denominada «corriente de lesión diastólica». Para confirmar esta corriente se utilizaron dispositivos de medición directa con amplificadores de acoplamiento directo sin corrección de base cero, lo que permitió observar una desviación negativa en el intervalo TQ. A partir de estos datos, se planteó que la elevación del segmento ST no era un fenómeno real del tejido miocárdico, sino un artefacto generado por los ajustes de los equipos.
Esta corriente surge debido a que, en condiciones normales, todas las zonas del miocardio tienen el mismo potencial durante la diástole. Sin embargo, en presencia de lesión miocárdica, las diferencias de voltaje entre regiones lesionadas y sanas generan un vector eléctrico diastólico dirigido desde la zona lesionada hacia la zona sana1,3 (Fig. 3).
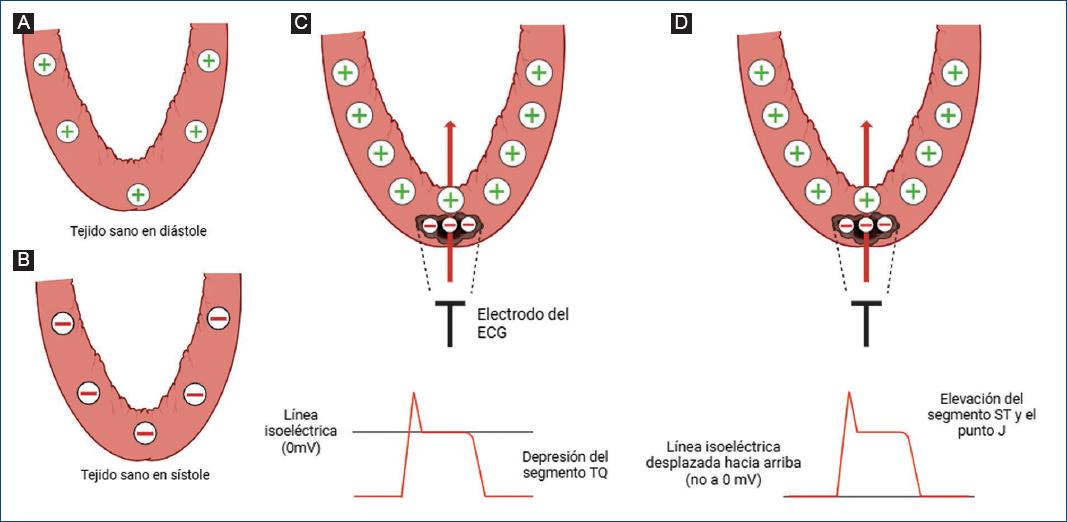
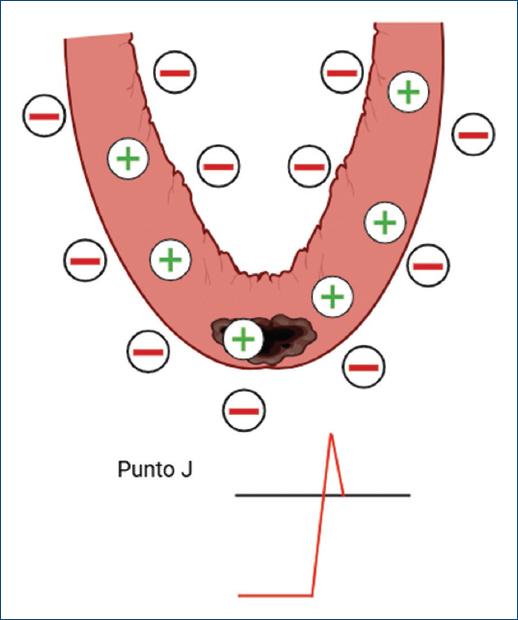
Figura 3 A: tejido sano durante la diástole, con cargas positivas en el medio extracelular. B: tejido sano en sístole, con cargas negativas en el medio extracelular. C: las zonas de lesión presentan una despolarización diastólica parcial (no puede repolarizarse adecuadamente), lo que hace que se genere un dipolo respecto al tejido sano. En este caso, sin corrección, la derivación electrocardiográfica mostrará una depresión del segmento TQ donde el electrodo explorador «verá» cómo el vector eléctrico se aleja de sí, mientras que el punto J permanece en su línea isoeléctrica original (0 mV). D: la corrección de la depresión TQ por los nuevos electrocardiógrafos produce una elevación del punto J y el segmento ST, sugiriendo erróneamente que es una alteración que ocurre solo en la sístole eléctrica.
Según el concepto de que el tejido lesionado presenta una despolarización diastólica parcial, se asume que al final de la fase 0 del potencial de acción, es decir, al término de la despolarización, tanto el tejido isquémico como el sano se encontrarían con el mismo voltaje (+20 mV, por ejemplo), lo cual coincide con el punto J del ECG (Fig. 4)1,3,5,6. Es importante recordar que los autores que se adhieren a esta hipótesis no conceden importancia a la corriente de lesión sistólica porque la consideran un artefacto producido por la corrección a cero del infradesnivel TQ.
Corriente de lesión sistólica
Además de la corriente de lesión diastólica, se ha propuesto la existencia de una corriente de lesión sistólica que se manifiesta durante la sístole eléctrica (intervalo QT). Esta corriente sería la causa de un desvío «verdadero» del segmento ST y el punto J en el ECG, debido a los gradientes eléctricos generados entre la zona lesionada y la sana. Estos gradientes resultan de una despolarización más lenta y limitada en las células lesionadas, junto con una meseta del potencial de acción deprimida y de menor duración6.
La corriente de lesión sistólica presenta polaridad opuesta a la diastólica: el vector de despolarización se orienta hacia la región lesionada (Fig. 4). En el ECG, al «corregirse» la corriente diastólica negativa llevándola a cero, la corriente sistólica se magnifica, generando un supradesnivel del ST, que en casos graves puede incluso alterar el complejo QRS. Este fenómeno ocurre porque el espacio extracelular de las células sanas es más negativo en comparación con el de las células lesionadas, lo que crea un vector dirigido desde el tejido sano hacia la zona isquémica6.
En 1938, Eyster y sus colaboradores hicieron un experimento en corazones de animales que clarificaron las bases de la electrocardiografía y las corrientes de lesión7. Pusieron una derivación unipolar en la base del corazón y otra en la región apical (la unipolar consiste en que el polo positivo es el único que cuenta porque el otro está anulado, como en la central de Wilson, o está muy lejos del corazón y mide muy poca actividad eléctrica). También, usando estos dos electrodos crearon una derivación bipolar ápex-base del corazón (es decir, comparando los voltajes que registraban simultáneamente los unipolares de ambas regiones)7,8. Una vez obtenidos los trazados basales, se produjo una lesión en el ápex cardiaco y se comprobó que el trazado unipolar de la región basal (no lesionada) no presentaba cambios apreciables; además, la derivación unipolar en la región lesionada presentaba corriente de lesión diastólica negativa y corriente de lesión sistólica positiva. Ambas corrientes tenían una amplitud muy superior a la basal de la región, y esto se comprobaba porque la derivación bipolar ápex-basal, que comparaba ambas regiones, después de la lesión presentaba un trazado igual al que registraba el electrodo unipolar en la región lesionada (Fig. 5)7.
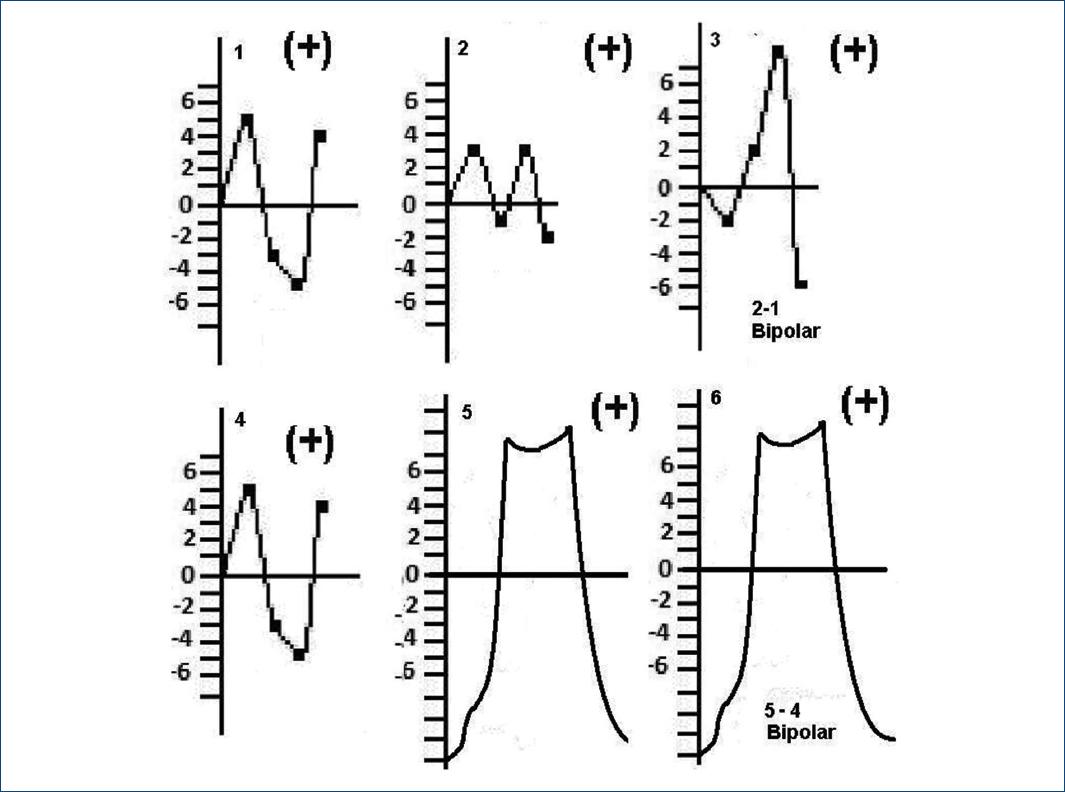
Figura 5 1, 2 y 3: antes de la lesión miocárdica. 4, 5 y 6: después de la lesión. 1 y 4: electrodo unipolar en la base. 2 y 5: electrodo unipolar en el ápex. 3 y 6: bipolar creada restando el trazado de la zona sana del de la zona lesionada (hay que recordar que, en la resta, lo que es positivo se hace negativo). Se observa que el electrodo que explora la zona no lesionada (basal) no registra mayores cambios con la lesión, mientras que el del ápex muestra una corriente negativa diastólica y una positiva, sostenida, sistólica. La amplitud eléctrica de las señales de la zona apexiana es mayor que las de la zona sana, lo que se refleja en la bipolar.
Alteraciones electrocardiográficas de las corrientes de lesión
En 1959, Conrad y su equipo estudiaron la isquemia aguda en perros usando electrodos intramurales unipolares9. Detectaron que, tras los primeros 2 minutos de oclusión de la arteria coronaria descendente anterior, además de las corrientes de lesión, en todos los casos (29/29) se producía un bloqueo intramural en la zona de máxima isquemia. Este bloqueo, con retrasos de hasta 25 ms, se debía a un deterioro de la activación radial del miocardio (endocardio a epicardio). En casos graves, el bloqueo permitió la activación tangencial desde zonas menos isquémicas hacia las más afectadas. Un hallazgo relevante fue la desaparición de la onda S en la región subendocárdica y el aumento de la amplitud de la onda R en la subepicárdica, que se duplicaba a los 5 minutos de oclusión. Las áreas con máxima amplitud de la onda R coincidían con las de mayor bloqueo intramural, aunque eran de tamaño reducido, requiriendo una evaluación cuidadosa9.
Los estudios en pacientes con oclusión temporal de la arteria coronaria descendente anterior han confirmado alteraciones en el QRS que explican el supradesnivel del ST. Al inflar un balón en la porción proximal de la arteria, se registraron cambios en el bucle de despolarización: en el 93% de los casos, la rotación del bucle pasó de antihoraria a horaria, generando desplazamientos significativos del punto J hacia delante y a la izquierda (Figs. 6 y 7). En el 66% de los casos, los cambios ocurrieron entre 32 y 49 ms desde el inicio del QRS, alterando el resto del bucle y provocando un inicio anormal de la repolarización6,8,10-12.
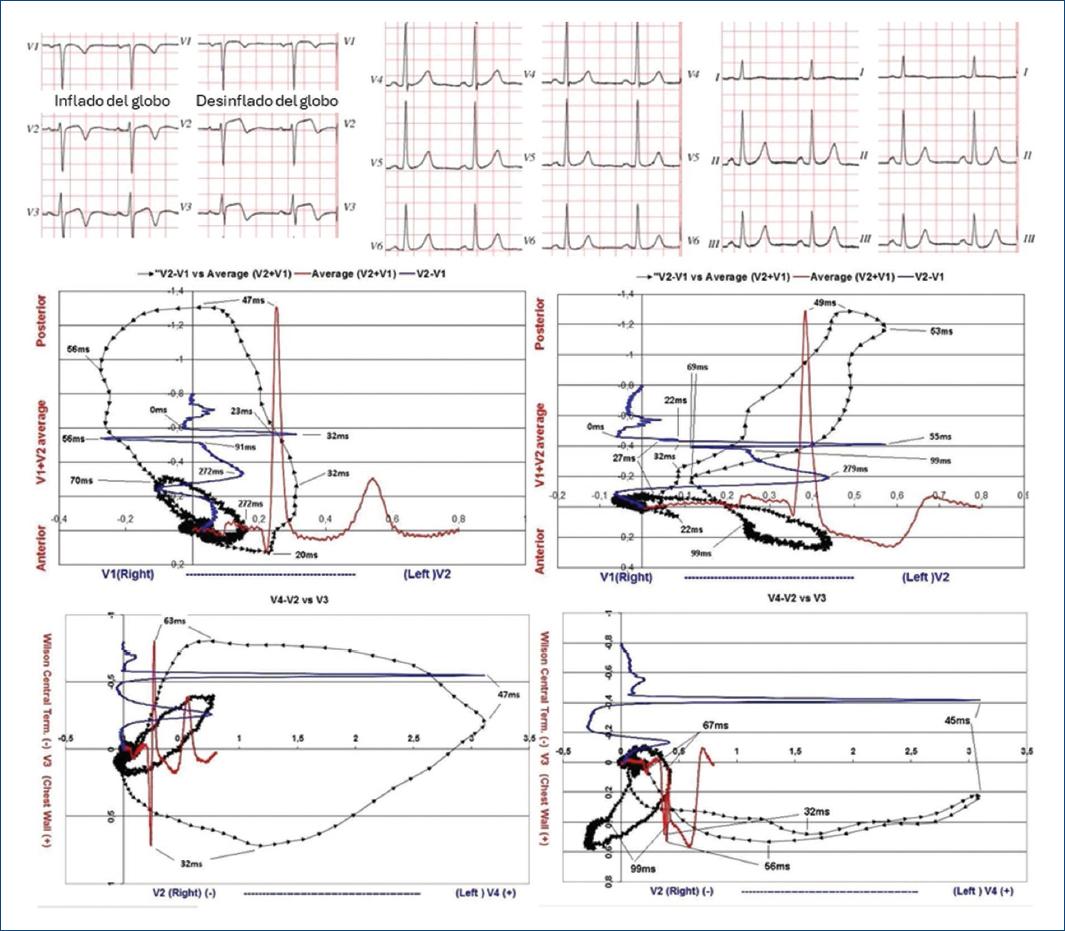
Figura 6 Mujer de 46 años, antes y después del inflado de un balón en la arteria descendente anterior proximal. Se muestran los registros basales del electrocardiograma estándar y los bucles transversos de la derivación bipolar precordial V2-V1 (en azul) frente a la derivación promedio ponderada V1+V2 (en rojo) y V4-V2 frente a la unipolar V3. Además, se representan los registros durante la isquemia inducida por el inflado del balón en la arteria descendente anterior proximal. Se observa un cambio especular del bucle a los 32 ms con rotación de antihoraria a horaria, lo que desplaza las fuerzas eléctricas hacia la izquierda y adelante. La reducción del voltaje en la onda S (de −0.7 mV a −0.4 mV) genera un desplazamiento del punto J hacia estas posiciones, con un inicio anómalo de la repolarización.
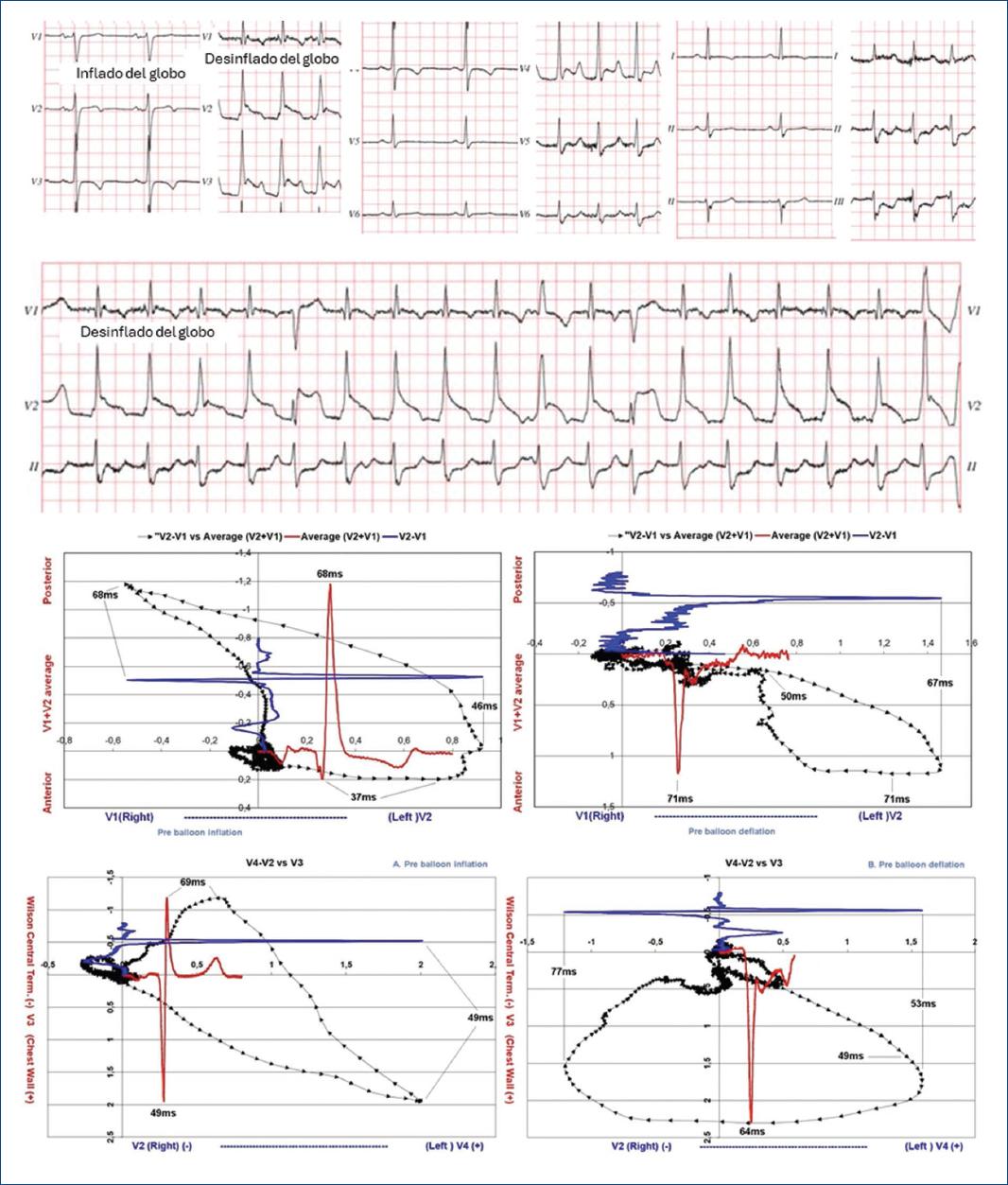
Figura 7 Varón de 51 años, antes y después del inflado de un balón en la arteria descendente anterior proximal. Se presentan los registros basales del electrocardiograma estándar y los bucles transversos de la derivación bipolar precordial V2-V1 (en azul) frente a la derivación promedio ponderada V1+V2 (en rojo) y V4-V2 frente a la unipolar V3. El bucle muestra un plegamiento hacia delante y a la izquierda, con un cambio en las fuerzas eléctricas finales que desplaza el punto J hacia estas posiciones. Es de notar que el pico de la onda R de la bipolar V2-V1 basal, que se daba a los 46 ms, se produce en la isquemia a los 67 ms (21 ms más tarde). Si bien esto podría sugerir un bloqueo de conducción intramiocárdico, la desaparición isquémica de la onda S de esta bipolar (que en el basal se daba a los 68 ms) puede indicar que solo se trata de una inversión del vector, sin que necesariamente se deba a un bloqueo de conducción intramiocárdico. Lo mismo ocurre con la onda S de la unipolar estándar V3. Estos cambios reflejan la influencia de las corrientes de lesión en el segmento ST y en la dinámica del bucle de despolarización.
Además, un reciente trabajo demuestra la inversión isquémica de las ondas del QRS (p. ej., una onda S convertida en un R’), explicando los cambios de los bucles vectorcardiográficos y poniendo en discusión si el bloqueo intramural se debe a un bloqueo real o a diferencias de potencial eléctrico que cambian la dirección del vector del QRS13. Esto se debería a que en la zona isquémica hay células que no logran repolarizarse en diástole o despolarizarse en sístole, teniendo un potencial de membrana menor. En otras palabras, mientras que en diástole el tejido normal extracelular recupera su condición positiva, la inhabilidad de repolarización de las células isquémicas genera un espacio extracelular relativamente negativo y produce un vector cuya cabeza positiva apunta al tejido sano. En sístole, el tejido normal negativiza su espacio extracelular, mientras que las células isquémicas no lo hacen y, por ende, son positivas respecto al tejido sano. Esto resulta en un vector eléctrico cuya cabeza (positiva) se dirige hacia la zona isquémica (Fig. 1).
Conclusión
Las corrientes de lesión, tanto sistólica como diastólica, representan un fenómeno clave en la interpretación del ECG en la isquemia miocárdica aguda. Son el resultado de los gradientes eléctricos generados por las diferencias en la despolarización y la repolarización entre regiones isquémicas y sanas. La corriente de lesión diastólica, con su vector dirigido hacia el tejido sano, y la corriente sistólica, que apunta hacia la zona lesionada, son las que producen las alteraciones características en el segmento ST y el complejo QRS observadas en la isquemia.
Estudios experimentales y clínicos han demostrado que estas corrientes están estrechamente vinculadas a cambios intrínsecos en la electrofisiología miocárdica, tales como el bloqueo intramural, la inversión del bucle de despolarización y la redistribución de las fuerzas eléctricas dentro del miocardio. Estas alteraciones subyacen al desvío del ST y otros cambios en el ECG que permiten diagnosticar y localizar la lesión de manera precisa. Debido a que tanto el supradesnivel como el infradesnivel isquémico del segmento ST representan el mismo fenómeno, diferenciándose solo por su dirección respecto al electrodo explorador, resultaría más correcto definir la corriente de lesión por su dirección, más que por su representación electrocardiográfica.
El análisis exhaustivo de los vectores eléctricos y su correlación con los hallazgos clínicos y experimentales reafirma la importancia del ECG como herramienta diagnóstica en la isquemia miocárdica aguda. Además, proporciona una base fisiopatológica sólida para interpretar los cambios en el ECG asociados a la lesión isquémica, y resalta la relevancia del tiempo en la detección y el tratamiento oportuno de estos eventos.











 nueva página del texto (beta)
nueva página del texto (beta)