Prólogo
Esta guía mexicana de insuficiencia cardiaca reúne el consenso de los más destacados médicos especialistas en falla cardiaca, miembros de diversas sociedades médicas de nuestro país y los indicados en darnos pautas para el adecuado diagnóstico y tratamiento de esta enfermedad, que es la epidemia cardiovascular emergente más importante de nuestros días.
La enfermedad cardiovascular mata a más de 18 millones de personas en el mundo, y la insuficiencia cardiaca es un evento extremo y en muchos casos final de la patología cardiovascular.
En la actualidad, los nuevos conceptos en el abordaje clínico, las novedosas moléculas terapéuticas y los innovadores dispositivos de tratamiento intervencionista y quirúrgico para tratar este síndrome han cambiado su evolución natural de manera ostensible. La insuficiencia cardiaca puede prevenirse, pero también diagnosticarse y tratarse en etapas más tempranas o, en otros casos, graves. Sin embargo, esto requiere un correcto conocimiento de la enfermedad y de procesos que todo médico cardiólogo y de especialidades afines a la cardiología debe conocer con precisión.
Esta guía es muy esperada por la comunidad médica mexicana porque pone en nuestro contexto, en la realidad de los países latinoamericanos como México, los adelantos que seguro incidirán en beneficio de los pacientes con insuficiencia cardiaca.
Es un gran honor, en nombre de la Sociedad Mexicana de Cardiología y de todas las sociedades que avalan esta guía, escribir este prólogo que estaría incompleto si no se reconociera todo el esfuerzo de cada médico que ha participado activamente en su elaboración.
Dr. Jorge Eduardo Cossío Aranda
Presidente de la Sociedad Mexicana de Cardiología
Introducción
La insuficiencia cardiaca es un síndrome multifacético que pone en riesgo la vida debido a su morbimortalidad elevada y su afectación en la capacidad funcional y en la calidad de vida relacionada con la salud (CVRS). Se considera que afecta a unos 64 millones de personas en todo el mundo, con una prevalencia del 1-3% en la población general adulta, y se espera que esta cifra pueda aumentar debido a la gran cantidad de pacientes subdiagnosticados y que serían clasificados de una manera más temprana con el uso de las herramientas diagnósticas más precisas desarrolladas en los últimos años1. La insuficiencia cardiaca crónica es una de las principales causas de hospitalización en adultos mayores de 65 años, con mal pronóstico y una supervivencia del 50% a 5 años de haber sido diagnosticados2. México sigue ocupando uno de los primeros lugares en el mundial en cuanto a prevalencia de factores de riesgo, como hipertensión arterial sistémica, diabetes y obesidad. Los padecimientos cardiovasculares, además, son la primer causa de mortalidad y de discapacidad en nuestro país2. Se calcula que una de cada cuatro personas desarrollarán insuficiencia cardiaca a lo largo de su vida3. Aunque en los últimos años el pronóstico de la insuficiencia cardiaca ha mejorado discretamente con la incorporación de nuevos tratamientos y de métodos diagnósticos más sensibles, la mortalidad permanece alta, con un riesgo de muerte del 15-30% a 1 año y del 75% a 5 años de haber sido hecho el diagnóstico. Aunque la muerte por causa cardiovascular sigue representando el motivo principal de mortalidad en pacientes con insuficiencia cardiaca, ha ido disminuyendo con el tiempo. La presencia de comorbilidad cardiovascular y no cardiovascular es frecuente en estos pacientes, y normalmente se asocia a un peor pronóstico. La incidencia de hospitalizaciones se relaciona de igual manera con un riesgo aumentado de muerte, por lo que sigue siendo de los desenlaces más importantes en cuando a evaluación de alternativas terapéuticas se refiere4,5.
La carga de la insuficiencia cardiaca también se ve reflejada en los aspectos económicos. Se calcula que cada paciente genera unos costos de alrededor de 25,000 euros anuales en los países de ingresos altos, la mayoría de ellos asociados a gastos directos de hospitalización y de manejo de la comorbilidad. Se espera que con los cambios demográficos y el envejecimiento de la población se observe un aumento en la incidencia de la enfermedad, y por lo tanto también de los costos para las instituciones y los pacientes1.
El tratamiento de la insuficiencia cardiaca ha evolucionado de manera vertiginosa en los últimos años. Tradicionalmente se había enfocado en aliviar los síntomas, reducir la retención de fluidos y mejorar la contractilidad cardiaca6. Con el advenimiento de la combinación de distintas terapias modificadoras de la enfermedad y la medicina de precisión se ha ganado terreno a la enfermedad, lo que nos ha dado la oportunidad de hacer un «traje a la medida» para el fenotipo individual de cada paciente, considerando aspectos clínicos, fisiológicos, biomarcadores e imagenológicos6.
Este documento sintetiza la mejor evidencia actual en el diagnóstico y el tratamiento de los pacientes con insuficiencia cardiaca. Esperamos que esta iniciativa de la Sociedad Mexicana de Cardiología, en colaboración con otras sociedades y colegios de reconocido prestigio, brinde recomendaciones que aporten a una mejor calidad en la atención clínica de los pacientes en todas las etapas de la enfermedad, y se logre una disminución significativa de las hospitalizaciones, de la morbilidad, de la afectación funcional y de la mortalidad asociadas a la insuficiencia cardiaca.
Método
La toma de decisiones en salud es un proceso sumamente complejo en el que el profesional sanitario debe considerar una gran cantidad de información obtenida durante su proceso de información y actualizada por distintos medios. La medicina basada en la evidencia es la toma de decisiones cuidadosa considerando la mejor evidencia científica y la experiencia clínica, considerando también los valores y las preferencias de los pacientes7. Las revisiones sistemáticas (RS) de la literatura se conducen a través de protocolos explícitos, rigurosos y exhaustivos que identifican, evalúan de forma crítica y sintetizan la evidencia científica relevante, convirtiéndose en la piedra angular de la medicina basada en la evidencia7,8. Este trabajo intenta adherirse a los estándares de calidad internacionales descritos en el reporte del Institute of Medicine (IOM) de los Estados Unidos de América. Los objetivos primordiales de las GPC son cerrar la brecha entre el conocimiento científico y la toma de decisiones por parte de los profesionales de la salud y los pacientes, apoyar los procesos de educación médica, auxiliar a los desarrolladores de políticas públicas y administradores para hacer más eficiente el uso de recursos, y decidir sobre las tecnologías en salud más costo-efectivas.
Las GPC requieren un protocolo que de manera sistematizada identifique la evidencia, su extracción, su síntesis y la incorporación de la experiencia clínica9-13 (Fig. 1). Se clasificó la evidencia científica tomando en cuenta la clasificación desarrollada por la Scottish Intercollegiate Guidelines Network (SIGN) de Escocia, en la cual se otorga el nivel más alto de evidencia a las RS de estudios clínicos aleatorizados (ECA) con muy bajo riesgo de sesgo, y va disminuyendo la calidad de la evidencia pasando por ECA con alto riesgo de sesgo, estudios de cohortes y estudios de casos y controles, hasta llegar a los estudios no analíticos, como las series de casos y los reportes de casos, y en el nivel inferior de la evidencia la opinión de los expertos14 (Tabla 1).
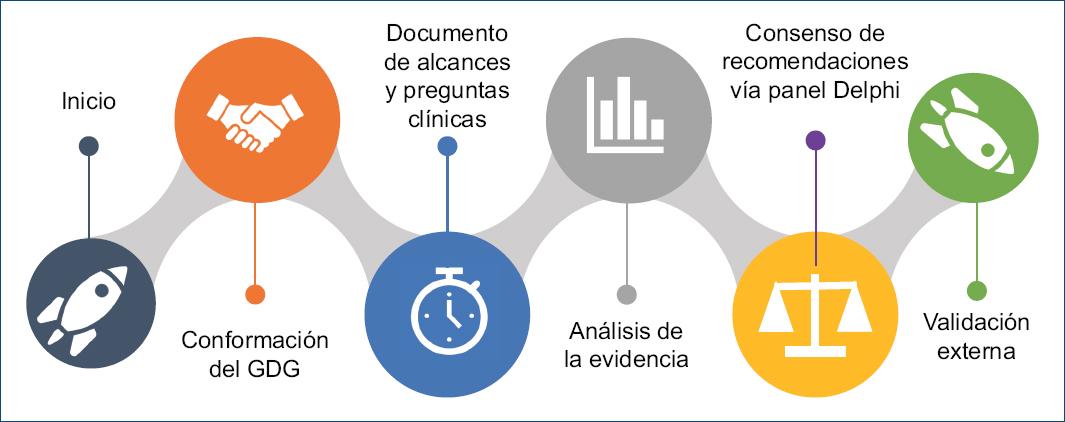
Figura 1 Desarrollo global de la guía de práctica clínica (modificada de: Mayorga J, Velasco L, Ochoa F. Guías de práctica clínica basadas en evidencia, cerrando la brecha entre el conocimiento científico y la toma de decisiones clínicas. Documento de la serie MBE, 3 de 3. Gac Mex Oncol. 2015;6:329-34).
Tabla 1 Evaluación de la calidad de la evidencia, SIGN 50
| Nivel de evidencia | |
|---|---|
| 1++ | Revisiones sistemáticas con o sin metaanálisis de ECA, o ECA con muy bajo riesgo de sesgo |
| 1+ | Revisiones sistemáticas con o sin metaanálisis bien desarrolladas o ECA con bajo riesgo de sesgo |
| 1− | Revisiones sistemáticas con o sin metaanálisis de ECA con alto riesgo de sesgo |
| 2++ | Revisiones sistemáticas de alta calidad de estudios de cohortes o de casos y controles Estudios de alta calidad de cohortes o de casos y controles con un riesgo muy bajo de sesgo y una alta probabilidad de que la asociación sea causal |
| 2+ | Estudios de cohortes y de casos y controles bien desarrollados con un riesgo bajo de sesgo y una alta probabilidad de que la asociación sea causal |
| 3 | Estudios observacionales no analíticos, como series de casos y reportes de casos |
| 4 | Opinión de expertos |
| Grados de recomendación | |
| A | Por lo menos una revisión sistemática con o sin metaanálisis o ECA calificado como 1++, y directamente aplicable a la población en estudio, o un cuerpo de evidencia que consiste principalmente en estudios calificados como 1+, directamente aplicable a la población en estudio y que ha demostrado resultados consistentes |
| B | Un cuerpo de evidencia que incluye estudios clasificados como 2++, directamente aplicable a la población en estudio y que ha demostrado resultados consistentes; o evidencia extrapolada de estudios clasificados como 1++ o 1+ |
| C | Un cuerpo de evidencia que incluye estudios clasificados como 2+, directamente aplicable a la población en estudio y que ha demostrado resultados consistentes; o evidencia extrapolada de estudios clasificados como 1++ |
| D | Un cuerpo de evidencia clasificada como 3 o 4; o evidencia extrapolada de estudios clasificados como 2+ |
Es importante resaltar que el grado de recomendación se relaciona con la fuerza de la evidencia en la cual se ha basado la recomendación clínica; no refleja la importancia clínica de la recomendación. ECA: estudio clínico aleatorizado. Modificada de: Scottish Intercollegiate Guidelines Network (SIGN). A guideline developers handbook. Edinburgh: SIGN; 2019. (SIGN publication no. 50). [November 2019]. Disponible en: http://www.sign.ac.uk.
Grupo de desarrollo de la guía
La SMC convino un grupo de trabajo multicolaborativo e interdisciplinario con la inclusión de distintas sociedades médicas e integrado por expertos clínicos en diversas áreas terapéuticas, entre las que se encuentran cardiología, cardiología intervencionista, cardiología con especialidad en insuficiencia cardiaca, cardiología-electrofisiología, cardiología especialista en oxigenación por membrana extracorpórea (ECMO) y cardiología especialista en medicina crítica; además, se invitaron expertos metodológicos con experiencia en la conducción de RS y GPC. Las organizaciones invitadas a colaborar en esta iniciativa de la SMC fueron la Asociación Nacional de Cardiólogos de México (ANCAM), la Asociación Nacional de Insuficiencia Cardiaca (ANIC), la Sociedad de Cardiología Intervencionista de México (SOCIME), la Sociedad Mexicana de Electrofisiología y Electroestimulación Cardiaca (SOMEEC), la Sociedad Nacional de Ecocardiografía de México (SONECOM), la Asociación Mexicana para la Prevención de Aterosclerosis y sus Complicaciones (AMPAC), el Colegio de Medicina Interna de México (CMIM) y el Colegio Nacional de Médicos Generales (CONAMEGE).
El grupo nuclear se reunió en varias ocasiones a distancia, a través de plataformas on line, para definir el modo de trabajo, los tiempos y la distribución de las responsabilidades, así como los aspectos importantes en la definición de alcances generales de la GPC y la lista de preguntas clínicas estructuradas. El 1 de febrero de 2023 se llevó a cabo una reunión, de manera virtual, para consensuar los primeros documentos intermedios del proyecto. Después de ello, se mantuvieron diversas reuniones asistidas por vídeo a través de plataformas electrónicas, con la finalidad de discutir los resultados de las búsquedas sistematizadas y la redacción de las recomendaciones iniciales.
Definición de alcances
Se integró de manera consensuada el documento de alcances de la GPC, en donde se establecieron las características de la población incluida a tratar y de la población que no sería considerada en el documento. Esta sección delimita el marco general del proyecto y se describieron los aspectos generales de la enfermedad y los aspectos clínicos que se cubrieron. Además, se estableció la audiencia a la que se dirigen las recomendaciones contenidas en este documento.
Preguntas clínicas estructuradas
Se identificaron las brechas en la práctica clínica del manejo de los pacientes con insuficiencia cardiaca y las brechas en el conocimiento para elaborar la base de datos de preguntas clínicas que posteriormente desarrollan el tema que afronta la GPC. De igual forma se consideraron nuevos tratamientos y pruebas diagnósticas que actualmente están mejorando la calidad de la atención de estos pacientes. Se intentó que las preguntas clínicas fueran claras, precisas y específicas para facilitar la búsqueda y la identificación de la evidencia científica, y así evitar recomendaciones poco ajustadas a los problemas clínicos que plantea la GPC. Se siguió el esquema PICO, el cual considera incluir la población, la intervención, el comparador y el desenlace (outcome) clínico, lo que facilita la identificación de la evidencia científica.
Búsqueda exhaustiva de la evidencia científica
Se identificaron y emplearon términos MeSH (Medical Subject Headings) para ensamblar una estrategia de búsqueda sensible y específica, además de explícita, para que sea reproducible en un futuro8. La revisión bibliográfica preliminar incluyó la localización de GPC relevantes ya existentes sobre el mismo tema. Esto permitió facilitar el ensamblaje del documento de alcances y la identificación de preguntas clínicas relevantes. A partir de aquí se llevaron a cabo la identificación, la evaluación y la síntesis de la evidencia científica.
Las bases de datos que recopilan GPC fueron consultadas usando los términos MeSH en caso de que existieran, o en su defecto, términos médicos avalados en RS ya publicadas. Para la identificación de GPC se consultaron, en el Reino Unido, Guidelines Finder National Electronic Library for Health; en España, Guiasalud. Trip Database. También se consultaron las bases de datos de las principales sociedades y academias del área de la especialidad en búsqueda de GPC publicadas: National Institute for Clinical Excellence (NICE) del Reino Unido, Scottish Intercollegiate Guidelines Network (SIGN) de Escocia, National Health and Medical Research Council de Australia (NHMRC) y New Zealand Guidelines Group (NZGG) de Nueva Zelanda). Finalmente, se consultaron las bases de datos de sociedades médicas reconocidas por su labor en la investigación y el desarrollo de documentos sobre el tema.
En la búsqueda exhaustiva de RS se ensamblaron distintas estrategias de búsqueda y se utilizaron diversas bases de datos generales y especializadas en RS. Se emplearon estrategias de búsqueda publicadas y validadas que hayan demostrado ser sensibles y específicas, así como términos MeSH. Se consultaron Cochrane Library, The Campbell Collaboration Library of Systematic Reviews, Centre for Reviews and Dissemination Databases (includes DARE), Centre for Reviews and Dissemination, National Institute for Health Research (NIHR), Trip Database, MEDLINE, PubMed (National Library of Medicine in the United States) y EMBASE, a través de ELSEVIER y NICE, para identificar HTA de alta calidad.
Solo en los casos en que las preguntas clínicas no encontraron una RS para ser respondidas o las GPC no hubieran identificado evidencia científica de alta calidad se llevaron a cabo búsquedas exhaustivas de la literatura para identificar estudios clínicos que respondieran a esa pregunta.
Las bases de datos que se consultaron para identificar estudios clínicos publicados fueron The Cochrane Library, Cochrane Central Register of Controlled Trials, Cochrane Database of Systematic Reviews, Database of Abstracts of Reviews of Effects (DARE) (Issue 1, 2019), MEDLINE (1950-2023) (OVID), Embase (1980-2023) (OVID), CINAHL (1982-2023) (NLH Search 2.0), LILACS (1998-2023), ARTEMISA (1999-2023) y SciELO (1999-2023).
Evaluación de la calidad y jerarquización de la evidencia
Se han publicado una gran cantidad de clasificaciones para evaluar la calidad de la evidencia; nosotros decidimos, por consenso, utilizar la escala desarrollada por SIGN, la cual considera dos atributos para evaluar la calidad (nivel) de la evidencia científica: el diseño del estudio y el riesgo de sesgo. Para la clasificación del diseño del estudio se utilizan los números del 1 al 4. El número 1 corresponde a ECA y RS, y el 4 a la opinión de expertos. Para evaluar el riesgo de sesgo se utilizan signos que informan sobre el grado de cumplimiento de los criterios clave relacionados con ese potencial riesgo (++, + y −). De esta forma, con la ayuda de la plantilla de lectura crítica se evalúa cada estudio, ya sean estudios individuales (ECA, cohortes, etc.) o RS9 (Tabla 2).
Tabla 2 Tipos de recomendación
| Evidencia y consenso clínico | Recomendación |
|---|---|
| Las consecuencias indeseables claramente superan los beneficios | Recomendación fuerte en contra |
| Las consecuencias indeseables probablemente superen a los beneficios | Recomendación condicionada en contra |
| El balance entre consecuencias indeseables y beneficios clínicos está equilibrado o es incierto | Recomendación para realizar investigación y posiblemente recomendación condicionada para uso en estudios clínicos |
| Los beneficios clínicos probablemente superen a las consecuencias indeseables | Recomendación condicionada |
| Los beneficios clínicos claramente superan a las consecuencias indeseables | Recomendación fuerte |
| Redacción de las recomendaciones | |
| «Recomendación fuerte» se puede hacer cuando hay confianza en que, para la mayoría de nuestros pacientes, la intervención o acción ofrece más beneficio que riesgo (o más riesgo que beneficio). La recomendación debe claramente dirigir y contener «debe/no debe» en su redacción | |
| «Recomendaciones condicionadas» pueden hacerse cuando la intervención o acción va a brindar más beneficio que riesgo en la mayoría de los pacientes. Las recomendaciones condicionadas pueden incluir «se puede considerar» en su redacción | |
Modificada de: Scottish Intercollegiate Guidelines Network (SIGN). A guideline developers handbook. Edinburgh: SIGN; 2019. (SIGN publication no. 50). [November 2019]. Disponible en: http://www.sign.ac.uk.
Extracción de la evidencia y análisis
Se llevaron a cabo reuniones a distancia con el grupo de desarrollo de la guía (GDG) para revisar el texto completo de cada una de las RS y así poder extraer los resultados. Se consideraron las medidas de asociación resultantes de los metaanálisis reportados en las GPC para determinar el tamaño del efecto global, ya fuera el riesgo relativo (RR), la razón de momios (RM), el cociente de riesgos (CR) o la diferencia de los promedios ponderados de los efectos (DPPE), de acuerdo con los distintos desenlaces definidos por el GDG. Para estudios de prueba diagnóstica se consideraron otras medidas de asociación, tales como la sensibilidad, la especificidad y los valores predictivos positivo y negativo. En las preguntas clínicas, cuando no se encontraron RS publicadas de buena calidad se llevó a cabo una RS para identificar los estudios clínicos pertinentes.
Consenso formal de los expertos
Se condujo un panel Delphi modificado como proceso para recoger la opinión de los expertos, de acuerdo con las recomendaciones internacionales15. Los miembros del GDG recibieron una invitación por correo electrónico para revisar todas las recomendaciones clínicas sugeridas, las cuales se colocaron en una plataforma digital diseñada para tal fin (Survey Monkey: https://es.surveymonkey.com). Cada experto clínico asignó una calificación utilizando una escala Likert según el grado de acuerdo que tuviera con el contenido, la aplicabilidad, la redacción y la actualidad de cada una de las recomendaciones clínicas. La escala Likert empleada va de 1 a 9, siendo 1 que el experto está «totalmente en desacuerdo» con el planteamiento de la recomendación y 9 que el experto está «totalmente de acuerdo» con ella. Los números intermedios manifiestan que el experto no tiene una postura bien definida con respecto al planteamiento o la redacción de la recomendación. Se calcularon la media con su intervalo de confianza, la mediana, la moda, el recorrido de los rangos intercuartiles y el porcentaje de consenso para cada una de las recomendaciones. Se consideró como un nivel mínimo de consenso una media de 7.0 y un porcentaje de al menos el 70% de respuestas en el rango de 7-9 en la escala Likert. Los miembros del GDG llevaron el control de la interacción de los participantes, procesando la información y filtrando el contenido relevante, y además modificaron las recomendaciones de acuerdo con los argumentos clínicos de todos los panelistas para poder enviar el nuevo texto a la siguiente ronda del panel Delphi y volver a ser evaluado por los mismos participantes de la ronda previa (Fig. 2).
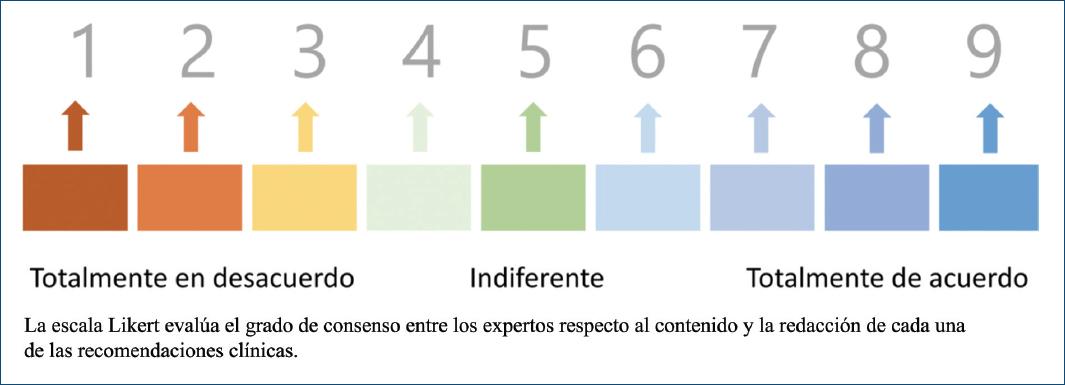
Figura 2 Escala Likert empleada en el panel Delphi modificado (modificada de: Mayorga J, Velasco L, Ochoa F. Guías de práctica clínica basadas en evidencia, cerrando la brecha entre el conocimiento científico y la toma de decisiones clínicas. Documento de la serie MBE, 3 de 3. Gac Mex Oncol. 2015;6:329-34).
Redacción de las recomendaciones
Los miembros del GDG se reunieron en diversas ocasiones para revisar el cúmulo de evidencia y los grados de recomendación. Tanto la evidencia científica analizada como la experiencia clínica del GDG y la relación riesgo/beneficio fueron consideradas para la redacción de las recomendaciones, en la que se puso especial cuidado para evitar ambigüedades (Tabla 2).
Recomendaciones clínicas y evidencia científica
La siguiente sección presenta las recomendaciones con respecto a los tópicos mencionados previamente.
Cuerpo de la evidencia
Se llevaron a cabo búsquedas para identificar GPC en las bases de datos antes mencionadas. Además, se implementaron estrategias de búsqueda exhaustiva de la literatura en PubMed y en Embase para identificar RS, con o sin metaanálisis, y ECA de acuerdo con estrategias validadas internacionalmente.
Los términos MESH empleados para identificar la evidencia científica fueron los siguientes: (((((((exp Heart Failure/) OR (((heart or cardiac or myocard*) adj2 (fail* or insufficien* or decomp*)).tw.)) OR (congestive heart failure[MeSH Terms])) OR (heart failure[MeSH Terms])) OR (heart failure, congestive[MeSH Terms])) OR (chronic heart failure[Text Word])) OR (chronic heart failure) AND (review[Filter])) AND (((("cochrane database syst rev"[Journal]) OR meta-analysis[MeSH Terms]) OR meta-analysis[Publication Type]) OR systematic review[Title/Abstract] AND (review[Filter]))Filters: Review Sort by: Most Recent.
Los términos empleados en Embase fueron: (congestive heart failure/exp OR congestive heart failure OR heart failure with preserved ejection fraction/exp OR heart failure with preserved ejection fraction OR heart failure with reduced ejection fraction/exp OR heart failure with reduced ejection fraction OR systolic heart failure/exp OR systolic heart failure OR diastolic heart failure/exp OR diastolic heart failure) AND ([cochrane review]/lim OR [systematic review]/lim OR [meta-analysis]/lim).
Con las estrategias de búsqueda empleadas se encontraron 1714 RS en PubMed y 3477 RS en Embase. Se llevaron a cabo estrategias de búsqueda específicas para algunas de las intervenciones terapéuticas para complementar la información y se encontraron RS adicionales.
Evidencia cientifica y recomendaciones
Pregunta 1: ¿Cuál es la definición de insuficiencia cardiaca crónica?
Recomendación: Para efectos de esta guía de práctica clínica se adoptará la definición universal propuesta en 2021 por Bozkurt et al.16, que especifica que se considera un síndrome clínico con síntomas y/o signos de insuficiencia cardiaca causados por alteraciones estructurales o funcionales del corazón, que debe ser corroborado por al menos uno de los siguientes criterios:
– Elevación de péptidos natriuréticos.
– Evidencia objetiva de congestión pulmonar o sistémica.
Nivel de evidencia 2+, grado de recomendación C (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
Históricamente, la falla cardiaca ha ocupado un lugar central en la práctica médica y sobre todo de los especialistas cardiovasculares. Lewis en 1933 escribió que "la esencia de la práctica clínica cardiovascular es la detección temprana de la falla cardiaca"17. La descripción de Harvey de la ciruclación en 1628 constituyó la piedra angular en el entendimiento de estas condiciones. Posteriormente el desarrollo de las placas radiográficas por Röntgen y del electrocardiograma por Einthoven a finales del siglo XIX aceleraron la investigación de las funciones del corazón y sus enfermedades17. Lewis en 1933 definió la insuficiencia cardiaca como aquella "condición en la cual el corazón falla en descargar su contenido de sangre adecuadamente" y unos años después, en 1980, Braunwald describe la insuficiencia cardiaca como "el estado fisiopatológico en el cual existe una función cardiaca anormal y es responsable de la falla del corazón para bombear la cantidad de sangre que la economía del organismo necesita"17.
Un grupo de trabajo convocado por la Sociedad Europea de Cardiología (ESC, por sus siglas en inglés) en el año de 1995 publicó las GPC sobre diagnóstico de insuficiencia cardiaca y posteriormente sobre manejo en 199718. Este documento define la insuficiencia cardiaca crónica como aquella "condición en la que están presentes: 1) síntomas de falla cardiaca, disnea o fatiga, en reposo o durante esfuerzos, o edema de tobillo y 2) evidencia de disfunción cardiaca en reposo o 3) respuesta a tratamiento". Los criterios 1) y 2) deben de estar presentes en todos los casos. El grupo de trabajo hace énfasis en que la respuesta al tratamiento de la insuficiencia no es suficiente para hacer el diagnóstico, aunque habitualmente el paciente debería demostrar cierta mejoría clínica con el mismo18.
Las GPC actualizada en 2021 de la ESC definen a la insuficiencia cardiaca como un "síndrome clínico caracterizado en la presencia de síntomas cardinales (disnea, edema de tobillo y fatiga) y acompañados de signos (elevación de la presión yugular, edema periférico y crepitaciones pulmonares); y es ocasionado por una anormalidad funcional o estructural del corazón que resulta en una elevación de las presiones intracardiacas y/o un expulsión cardiaca inadecuada en reposo o durante el ejercicio"5.
Por su parte, la Asociación Americana del Corazón (AHA, por sus singlas en inglés) en colaboración con el Colegio Americano de Cardiología (ACC, por sus siglas en inglés) definen a la insuficiencia cardiaca como un "síndrome clínico complejo con síntomas y signos que resulta de la afectación, estructural o funcional, del llenado ventricular o de la expulsión del volumen sanguíneo"4. Estas guías establecen que las etapas asintomáticas con enfermedades cardiacas estructurales o cardiomiopatías no son considerados en esta definición de pacientes con insuficiencia cardiaca4.
El consenso mexicano sobre insuficiencia cardiaca publicado en 2022 por Magaña et al.2 define a la insuficiencia cardiaca como el "síndrome clínico resultado de una alteración funcional o estructural que afecta la habilidad del corazón de contraerse o llenarse". Sin embargo, los autores hacen hincapie en el hecho de que al tratarse de un síndrome, no existe una solo entidad etiológica, sino por el contrario, un amplio espectro de alteraciones que afectan el sistema cardiovascular. Segundo, no es requisito que las alteraciones, ya sean estructurales o funcionales, sean graves para considerar a un paciente como con insuficiencia cardiaca. Por último, resaltan la importancia de la función diastólica como componente esencial en los pacientes con insuficiencia cardiaca con fracción de expulsión conservada19. Los autores señalan dentro de las principales causas de insuficiencia cardiaca, la hipertensión arterial sistémica (HAS), enfermedad valvular cardiaca o cardiopatías valvulares, cardiomiopatías, malformaciones cardiacas congénitas, enfermedad cardiaca reumática, diabetes, cardiotóxicos y enfermedad tiroidea, entre otras19.
Recientemente se publicó por Bozkurt et al. una definición universal de insuficiencia cardiaca. Esta iniciativa avalada por la sociedad americana de insuficiencia cardiaca (HFSA, por sus siglas en inglés), la Asociación de Insuficiencia Cardiaca de la ESC, la Sociedad Canadiense de Insuficiencia Cardiaca (CHFS, por sus siglas en inglés); entre otras sociedades de Japón, Australia, China e India16. Este grupo de expertos definen la insuficiencia cardiaca como el síndrome clínico con síntomas y signos causados por una anormalidad funcional y/o estructural y corroborada por niveles elevados de péptidos natriuréticos y por mediciones objetivas donde se demuestre congestión sistémica o pulmonar16.
Algunas definiciones relevantes en el tema de la insuficiencia cardiaca radican en los fenotipos clínicos basados en la fracción de expulsión ventricular izquierda (FEVI) medida mediate ecocardiografía. Las GPC de la ESC definen la falla cardiaca con fracción de eyección preservada (ICFEp) cuando la FEVI es ≥ 50%, reducida (ICFEr) ≤ 40% y en rango medio (ICFEm) entre 40-50%. Aquellos pacientes que tienen síntomas de insuficiencia cardiaca, con evidencia de anormalidades funcionales o estructurales y/o elevación de péptidos natriuréticos (PNs) pero con FEVI es ≥ 50% se consideran como con fracción de eyección preservada (ICFEp)5.
Pregunta 2: ¿Cuáles son los estadios clínicos de la insuficiencia cardiaca crónica?
Recomendación: La insuficiencia cardiaca debe considerarse como parte de un continuo cardiovascular, y para su estudio y comprensión se deben contemplar cuatro estadios o etapas clínicas que se reconocen por las letras A, B, C y D.
Nivel de evidencia 2++, grado de recomendación C (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
La evidencia científica actual indica que la insuficiencia cardiaca es usualmente progresiva que inicia con la presencia de factores de riesgo para la disfunción cardiaca, que dan como resultado cambios en la estructura y función del corazón y que inicialmente cursan asintomáticos; y que progresan a una falla en la función del mismo que repercute en la economía, causando afecciones funcionales importantes y ulteriormente la muerte20. Los grupos de expertos internacionales tienen como objetivo resaltar la importancia de este proceso fisiopatológico para apuntalar esfuerzos en la dismininución de la progresión de la enfermedad, el diagnóstico temprano y el tratamiento oportuno20; por ello, la GPC de AHA/ACC 2022 proponen 4 estadios de la enfermedad, en donde el estadio A considera a los pacientes "en riesgo de padecer insuficiencia cardiaca", el estadio B contempla a los pacientes que se encuentran en una etapa "previa a la insuficiencia cardiaca", el estadio C considera a aquellos pacientes con "insuficiencia cardiaca sintomática" y por último, el estadio D con "insuficiencia cardiaca avanzada"4. El consenso mexicano sobre insuficiencia cardiaca también propone esos 4 estadios de la enfermedad2. Bozkurt et al. en su consenso multinaciomal recientemente publicado también reconocen los 4 estadios clínicos propuestos por AHA16.
Estudios longitudinales han mostrado que el daño progresivo al corazón ocasiona progresivamente una remodelación estrucutral de las distintas cavidades cardiacas, incrementando su tamaño y afectando la función del mismo, lo que progresivamente causa síntomas de insuficiencia cardiaca.
Una revisión sistemática (RS) de la literatura publicada por Bergamasco et al.21 en 2022 tuvo como objetivo determinar la prevalencia de las distintos estadios de la insuficiencia cardiaca, porpuestos por AHA/ACC, progresión de la enfermedad y tasas de mortalidad21. Los autores incluyeron 12 estudios, de los cuales 10 reportaron la prevalencia y 1 reportó la progresión de la enfermedad y la mortalidad. La mayoría de los estudios se consideraron (70%) como con buena calidad metodológica. El 80% de los estudios emplearon evaluaciones ecocardiográficas para determinar la existencia de cambios pre-insuficiencia cardiaca. Los resultados de los metaanálisis mostraron una prevalencia de pre-insuficiencia cardiaca en la población general en un rango de 11 (estudio de Bélgica) a 59.1% (estudio de Italia). Se observó un incremento de la prevalencia conforme avanza el promedio de edad de los participantes (59.1% de prevalencia en pacientes entre 56 a 84 años de edad) y en estudios de medicina general (42.7% en pacientes de 59.6 años de edad promedio) en comparación a un estudio de población general en EE.UU. (12.5% de prevalencia en pacientes de 47 años de edad promedio)21. Hay poca información sobre la progresión de la enfermedad, de acuerdo a un estudio retrospectivo conducido en EE.UU. se reportó una incidencia de 1.14 por 100 personas al año en hombres y de 0.63 por 100 personas al año en mujeres de insuficiencia cardiaca sintomática en personas previamente diagnosticadas como con pre-insuficiencia cardiaca21. Otro estudio Italiano reportó un 9.8% de pacientes que requirieron hospitalizaciòn por síntomas de insuficiencia cardiaca y que previamente estaban diagnopsticados como con pre-insuficiencia cardiaca a un seguimiento de 22 meses21. La mortalidad se reportó en 0.881 por 100 personas al año (EE.UU.), 1.6% en Japón y de 0.6% en Italia, de pacientes diagnosticados como con pre-insuficiencia cardiaca21.
Pregunta 3: ¿Cuál es la clasificación de la insuficiencia cardiaca crónica de acuerdo a la clase funcional y a la fracción de de expulsión del ventrículo izquierdo?
Recomendación: De acuerdo con la FEVI, los pacientes con diagnóstico establecido de insuficiencia cardiada pertenecen a alguna de las siguientes cuatro categorías:
– Insuficiencia cardiaca con FEVI reducida (≤ 40%).
– Insuficiencia cardiaca con FEVI moderadamente reducida (41-49%).
– Insuficiencia cardiaca con FEVI preservada (≥ 50%).
– Insuficiencia cardiaca con FEVI mejorada (pacientes con FEVI reducida que incrementan al menos un 10% su valor basal o que superan el 40%).
Con relación a la clase funcional, la clasificación propuesta por la New York Heart Association (NYHA) permanece vigente.
Nivel de evidencia 1++, grado de recomendación A (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
Se ha demostrado que la fracción de expulsión del ventrículo izquierdo (FEVI) refleja con mayor precisión la función del ventrículo izquierdo (VI) que el volumen sistólico, debido a que toma en consideración la relación Frank-Starling. Sin embargo, la FEVI puede verse modifcada por la precarga, la postcarga, la contractibilidad. Los colúmenes absolutos del ventrículo izquierdo pueden reflejar esos factores de manera distinta: el volumen telesistólico se altera por la postcarga y la contractibilidad y el voluemn telediastólico por la precarga y la contractilidad22. En el escenario de la falla cardiaca con FEVI reducida (ICFEr, por sus siglas en inglés) y cardiopatía isquémica, tanto el volumen diastólico como el sistólico puden estar aumentados, y aunque el volumen sistólico se preserva, la FEVI puede estar reducida. Por ello, la FEVI también es un marcador preciso de remodelamiento cardiaco22.
Algunas limitantes de la FEVI como marcador de la función ventricular izquierda incluyen la falla cardiaca preclínica, la cual podría ser identificada por marcadores de deformación cuando la FEVI es normal. La afectación de la función cardiaca en la ausencia de una reducción de la FEVI es una situación que se presenta frecuentemente en la actualidad que se debería considerar como disfunción izquierda subclínica22. Cuando la fracción de expulsión es empleada como marcador de disfunción miocárdica, es importante recordar que es una medicion endocárdica, y que en el caso de existir hipertrofia del mismo, hay otros parámetros más precisos para evaluar la función ventiruclar iozquierda. La FEVI por lo tanto, se modifica con la geometría22.
La clasificación de los pacientes sintomáticos de acuerdo a los valores de FEVI ha sido parte de la piedra angular del manejo de estos pacientes, tradicionalmente, se consideran4,5,16:
– FEVI REDUCIDA (ICFEr): pacientes con FEVI < 40%.
– FEVI INTERMEDIA (HFmEF): pacientes con una FEVI entre 41% y 49%, concepto recientemente introducido en las guía clínicas.
– FEVI PRESERVADA (HPpEF): los pacientes con una FEVI > 50%, y son aquellos pacientes con datos clínicos de insuficiencia cardiaca, elevación de péptidos natriuréticos y datos de función cardiaca anormal.
Esta clasificación, aceptada por la mayoría de documentos de posicionamiento, consensos y guías clínicas alrededor del mundo, proviene de estudios clínicos controlados en donde se ha demostrado un beneficio en la supervivencia de pacientes con insuficiencia cardiaca que han incluido pacientes con una FEVI menor de 35-40%, catalogados como ICFEr. Aunque los signos y síntomas clásicos de insuficiencia cardiaca junto con la medición de la FEVI, son necesarios para el diagnóstico de HFmEF o ICFEp; la realización de estudios más extensos de disfunción cardiaca pueden incrementar la especificidad del diagnóstico. La elevación de los péptidos natriuréticos soportan el dioagnóstico de insuficiencia cardiaca, sin embargo, cifras normales no descartan el diagnóstico de HFmEF o ICFEp4,5,18,19.
Un concepto a tomar en cuenta, es el de aquellos pacientes que presentan una mejoría de su FEVI desde cifras de > 40%, y cuando se alcanza una mejoría del > 10% desde la línea basal y una segunda medición > 40%; se consideran como HFimpEF. Cabe destacar, que en la mayoría de los pacientes esto no significa que se ha normalizado la función cardiaca, y se pueden seguir encontrando datos de disfunción del ventrículo izquierdo en una alta proporción de ellos. Otro punto a considerar, es el empeoramiento que muestran algunos pacientes cuando suspenden su tratamiento farmacológico, regresando a las mediciones basales de FEVI4.
Otra clasificación muy importante en los pacientes con insuficiencia cardiaca es la propuesta por la NYHA (Asociación de Cardiología de Nueva York), que se basa principalmente en síntomas y actualmente hay indicadores objetivos que tienen una mejor correlación pronóstica y se ha usado por casi un siglo4. La clasificación de NYHA es un método sencillo de calificar la capacidad funcional de los pacientes basado en la historia clínica solamente y tiene un valor pronóstico claro, sin embargo, su reproducibilidad y su fiabilidad han sido ampliamente cuestionadas23.
Es importante señalar que pacientes con síntomas leves, pueden ser susceptibles a hospitalizaciones y muerte. Ha servido como una de las herramientas diagnósticas primordiales para estratificación de riesgo y se usa ampliamente como criterio de inclusión en estudios clínicos controlados. Recientemente los estudios en dispositivos invasivos como la terapia de resincronización cardiaca (TSC), entre otros, utilizan la clasificación de NYHA como parte de sus estrictos criterios de inclusión y desenlaces24. Algunos estudios han demostrado que la clasificación NYHA no tiene una adecuada capacidad de discriminar en los pacientes con insuficiencia cardiaca entre los pacientes en todo el espectro de alteraciones funcionales24.
La clasificación NYHA categoriza a los pacientes de acuerdo a una escala de I a IV: la clase I, sin limitaciones en la actividad física; clase II, limitación discreta en la actividad física; clase III, limitación marcada en la actividad física y clase IV, síntomas incluso en reposo y con cualquier actividad física16.
Una RS publicada por Bkork en 2016 et al.25 tuvo como objetivo revisar todos los estudios clínicos que evaluaron intervenciones en pacientes con insuficiencia cardiaca avanzada. Los autores incluyeron 134 estudios clínicos y encontraron que la clasificación de la NYHA fue el criterio más empleado (119 estudios clínicos, 88.8%), seguido de FEVI (84 estudios clínicos, 62.7%). Otros desenlaces empleados en estos estudios fueron el status de dependiencia a inotrópicos (12.7%), la VO2 pico (10.4%), admisiones hospitalarias (10.4%) índice cardiaco (10.4%), entre otras. Los autores concluyeron que la clasificación de NYHA junto con la FEVI fueron los critestios clínicos más ampliamente empleados para definir la insuficiencia cardiaca avanzada25.
En una gran cantidad de estudios clínicos, la clasificación de NYHA se utiliza como criterio de inclusión basal y como parte de la evolución de los participantes para decidir la terapéutica a evaluar. Con frecuencia, las nuevas terapias se prueban en pacientes con NYHA III-IV ya que se asocia a mayor ocurrencia de eventos a evaluar. Sin embargo, muchos estudios han demostrado que su eficacia no tiene una buena correlación con la clasificación de NYHA basal en los pacientes. Por ello, se ha propuesto que la clasificación de NYHA no tiene una buena correlación con la disminución de los riesgos relativos de ocurrencia de eventos cardiovasculares, sin embargo, se mantiene como una herramienta válida en el riesgo absoluto de la ocurrencia de esos eventos, y también para informa efectividad terapéutica23.
Una RS publicada por Miller et al. en 201523 tuvo como objetivo evaluar la correlación de la clasificación de NYHA respecto a la efectividad terapéutica. Los autores incluyeron 26 estudios clínicos controlados (ECAs) que incluyeron 36,406 pacientes de acuerdo la clase NYHA basal y reportaron mortalidad por cualquier causa. Los resultados mostraron que la reducción de mortalidad relativa con las intervenciones terapéuticas fue independiente de la clase NYHA basal23.
Pregunta 4: ¿Cuál es la precisión diagnóstica de la evaluación clínica en el consultorio para los pacientes con insuficiencia cardiaca crónica?
Recomendación: La sospecha diagnóstica se debe basar en una anamnesis minuciosa que considere los antecedentes familiares y personales de condiciones que favorezcan el desarrollo de insuficiencia cardiaca, así como en el cuadro clínico tomando en consideración los síntomas y signos más relevantes, por su sensibilidad y especificidad (ver anexo). Sin embargo, el cuadro clínico puede resultar insuficiente para confirmar el diagnóstico, por lo que es INDISPENSABLE considerar el uso de auxiliares paraclínicos en pacientes con sospecha de insuficiencia cardiaca.
Nivel de evidencia 2++, grado de recomendación C (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
La insuficiencia cardiaca ha sido definida en las guías de práctica clínica más recientes como aquella "condición en la que están presentes: 1) síntomas de falla cardiaca, disnea o fatiga, en reposo o durante esfuerzos, o edema de tobillo y 2) evidencia de disfunción cardiaca en reposo o 3) respuesta a tratamiento". Los criterios 1) y 2) deben de estar presentes en todos los casos5.
Por lo tanto, la evaluación clínica del paciente en el consultorio, tanto de medicina general y familiar como del especialista es invaluable. Para considerarse el diagnóstico de insuficiencia cardiaca crónica, el paciente debe de presentar síntomas y signos, los cuales incluyen disnea, fatiga, edema de tobillo. Sin embargo, los síntomas únicamente tienen una baja especificidad para poder establecer un diagnóstico confiable4. La historia clínica es importante, y la coexistencia con algunos padecimientos como infarto al miocardio (IM), hipertensión arterial sistémica (HAS), diabetes tipo 1 o 2 (DT1 o DT2), antecedente de quimioterapia asociada a cardiotoxicidad, enfermedad renal crónica (ERC), hace más probable la presentación de una insuficiencia cardiaca crónica. Antecedentes familiares de cardiomiopatía, son importantes en la anamnesis del paciente4,5,19. Un aspecto muy importante en la exploración física de estos pacientes en la consulta, es la de evaluar la presencia de signos compatibles con congestión clínica, entre los métodos recomendados por los lineamientos internacionales para la evaluación de la congestión clínica se encuentran ingurgitación de la vena yugular, ortopnea, edema de piernas y la maniobra de Valsalva. Incluso, la presencia de esos signos de congestión clínica, pueden servirle al clínico para "titular" la dosificación de algunos medicamentos4,5,19 (Fig. 3).
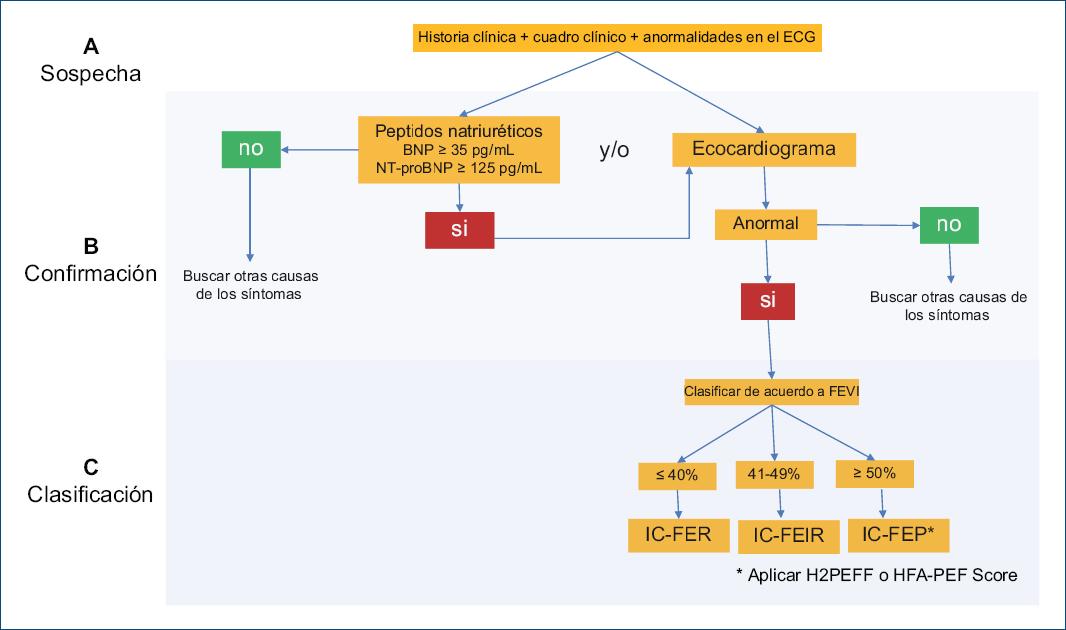
Figura 3 Algoritmo diagnóstico para la insuficiencia cardiaca. ECG: electrocardiograma; BNP: péptido natriurético B; IC-FElR: insuficiencia cardiaca con fracción de expulsión ligeramente reducida; IC-FEP: insuficiencia cardiaca con fracción de expulsión preservada; IC-FER: insuficiencia cardiaca con fracción de expulsión reducida; NT-proBNP: fracción amino-terminal del propéptido natriurético B.
Una RS publicada por Madhok et al.26 tuvo como objetivo el de evaluar la precisión diagnóstica de síntomas y signos en el diagnóstico de disfunción del ventrículo izquierdo en centros de atención primaria. La disfunción del ventrículo izquierdo es una de las principales causas de insuficiencia cardiaca. Los autores incluyeron 24 estudios de prueba diagnóstica (estudios de corte-transversal) con 10,710 pacientes con prevalencia de 29.9% de disfunción del ventrículo izquierdo. Todos los estudios consideraron la ecocardiografía como el "estándar de referencia" y la medición qué más se empleó como medida objetiva de la función ventricular izquierda fue la fracción de expulsión. Los resultados de los estudios muestran que ningún signo o síntoma tiene la suficiente precisión diagnóstica para confirmar o descartar la presencia de disfunción del ventrículo izquierdo26. La presencia del desplazamiento del latido del ápex mostró una adecuada precisión (LRT [Likelihood Ratio Test] de 16.0, IC95% 8.2; 30.9), pero solo se evaluó en dos estudios. En contraste, la presencia de un tercer ruido cardiaco mostró un rango muy amplio de LRT (1.6; 32.4), igual que la ingurgitación de la vena yugular (2.7; 7.4). El edema de miembros inferiores no tuvo valor diagnóstico (LRT 0.96; 1.48). La radiografía de tórax tampoco tuvo una buena precisión diagnóstica (LRT 1.2; 1.7). La conclusión de los autores es que estos signos clínicos tienen cierto valor en el diagnóstico de disfunción ventricular izquierda, sobre todo para la confirmación de esta. Por ello cabe resaltar, que ni la presencia de síntomas ni la ausencia de estos pueden confirmar o descartar la disfunción ventricular izquierda. No hay información suficiente para evaluar la precisión diagnóstica de la combinación de signos y síntomas26.
Otra RS publicada por Mant et al.27 tuvo como objetivo evaluar la precisión diagnóstica de los síntomas y signos de la insuficiencia cardiaca. Los autores llevaron a cabo un análisis a nivel de paciente individual en nueve estudios y una regresión logística para insuficiencia cardiaca. Los resultados de los análisis fueron que la disnea fue el único síntoma que mostró una alta sensibilidad (89%), pero baja especificidad (51%). Los datos clínicos que mostraron una alta especificidad incluyeron el antecedente de IM (89%), ortopnea (89%), edema (72%), ingurgitación de la vena yugular (70%), cardiomegalia (85%), ruidos cardiacos agregados (99%, crepitaciones pulmonares (81%) y hepatomegalia (97%). Sin embargo, todos estos datos clínicos mostraron baja sensibilidad. En contraste, el electrocardiograma (EKG) (89%), péptido natriurético cerebral (BNP, por sus siglas en inglés) (93%) y la porción N-terminal del pro-péptido natriurético tipo B (NT-proBNP, por sus siglas en inglés) (93%) tienen altas sensibilidades27. Los autores concluyeron en base a estos resultados que considerando un paciente que presenta síntomas y en el cual se sospeche de insuficiencia cardiaca, la recomendación es la referencia a la realización de ecocardiografía. Si el paciente tiene antecedente de IM o crepitaciones basales o es masculino con edema de tobillo, se recomienda levar a cabo la medición de BNP y de ecocardiografía27.
Pregunta 5: ¿Cuál es la precisión de los marcadores bioquímicos (BNP, NT-proBNP) para el diagnóstico de los pacientes con insuficiencia cardiaca crónica?
Recomendación: La cuantificación sanguínea de péptidos natriuréticos debe considerarse como parte esencial en el abordaje diagnóstico de la insuficiencia cardiaca debido a sus elevadas sensibilidad, especificidad y valores predictivos. Sin embargo, la elevación de los péptidos natriuréticos sin correlación clínica no es suficiente para definir el diagnóstico de insuficiencia cardiaca. Siempre que sea posible se debe preferir el uso de NT-proBNP sobre BNP debido a su mayor precisión.
Nivel de evidencia 2++, grado de recomendación C (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
El consenso mexicano de insuficiencia cardiaca 20222 hace énfasis en la importancia de apoyar el diagnóstico, seguimiento y pronóstico de los pacientes con insuficiencia cardiaca.
Los cardiomiocitos que se encuentran en el corazón de los seres humanos comprenden diversos fenotipos de células con funciones especializadas, como son la generación de impulsos eléctricos y su conducción, la contracción muscular y también le secreción de diversas hormonas polipéptidas28.
Los péptidos natriuréticos son particularmente abundantes en los cardiomiocitos del atrio en algunos mamíferos. El péptido atrial natriurético (ANP, por sus siglas en inglés) y el BNP, son referidos como péptidos natriuréticos28. En situaciones en donde se incrementa el estrés hemodinámico, los péptidos natriuréticos se sintetizan para promover la diuresis y la vasodilatación con la finalidad de disminuir la sobrecarga en un corazón en insuficiencia. Adicionalmente tienen un efecto antifibrótico, antiproliferativo y anti apoptósico19.
Los péptidos natriuréticos que tienen utilidad clínica son el ANP, BNP y NT-proBNP, sin embargo, se prefiere el uso de BNP y NT-proBNP por su vida media breve. BNP tiene una vida media más corta que NT-proBNP y es estable en la toma de sangre a temperatura ambiente con la adición de ácido etilendiaminotetraacético (EDTA, por sus siglas en inglés) al menos durante 24 horas, en comparación con el NT-proBNP que es estable al menos 72 horas con EDTA28.
La elevación de los niveles de BNP o de NT-proBNP tienen como significado clínico un incremento de la sobrecarga, por ello tienen un valor diagnóstico para la exclusión de insuficiencia cardiaca cuando los niveles son normales (90%), sobre todo en salas de urgencia en donde se requiere tomar decisiones terapéuticas inmediatas19. Desde su disponibilidad, la primera generación de estudios de péptidos natriuréticos empleaba radioinmunoensayos que requerían de la extracción de plasma, la segunda generación empleaba anticuerpos monoclonales y radioisótopos y mejoró su precisión diagnóstica. Por último, la tercera generación de análisis clínicos, utilizan métodos de inmunofluorescencia y permiten realizarlos en los puntos de atención (POC, por sus siglas en inglés) tan solo en algunos minutos28.
Una revisión de tecnologías en salud (HTA, por sus siglas en inglés) publicada por Ontario Health29 en 2021 tuvo como objetivo evaluar la precisión y utilidad diagnóstica. Los autores incluyeron 8 revisiones sistemáticas en la revisión de la evidencia científica. Los resultados de los metaanálisis mostraron que BNP o de NT-proBNP tuvieron una sensibilidad alta (80 a 94% y 86 a 96%, respectivamente) con una calidad de la evidencia alta y resultado de la prueba de razón de verosimilitud negativa bajo (0.08 a 0.30 y 0.09 a 0.23, respectivamente. Cuando BNP o de NT-proBNP fueron empleados para el diagnóstico de la insuficiencia cardiaca en el área de urgencias, hubo una disminución en el tiempo de estancia hospitalaria (–1.22 días, IC95% –2.31; –0.14). BNP no disminuyó la tasa de admisión hospitalaria (RM 0.82, IC95%: 0.67; 1.01), o la mortalidad hospitalaria (RM 0.96; IC95%: 0.65; 1.41). Las conclusiones de los autores son que tanto BNP o de NT-proBNP tienen alta sensibilidad y baja razón de verosimilitud negativa, por lo que con los puntos de corte establecidos pueden descartar la presencia de insuficiencia cardiaca con un alto nivel de confianza29.
Otra HTA publicada por la Agencia de Investigación y Calidad del Cuidado de la Salud de EE. UU. (AHRQ, por sus siglas en inglés) en 201530 tuvo como objetivo evaluar la precisión y utilidad diagnóstica de BNP o de NT-proBNP para diagnosticar la insuficiencia cardiaca. Los resultados reportados muestran que, en la sala de urgencias, BNP (51 estudios) y NT-proBNP (39 estudios) mostraron alta sensibilidad y baja especificidad, por lo que fueron útiles para descartar insuficiencia cardiaca, aunque no son útiles para confirmar la condición clínica30. Cuando BNP (12 estudios) y NT-proBNP (20 estudios) fueron evaluados en escenarios de atención primaria, se observaron resultados similares. Los estudios que evaluaron la precisión diagnóstica asociada a pronóstico (183 estudios) mostraron que cifras altas tuvieron una buena asociación para mortalidad cardiovascular, morbilidad, entre otros desenlaces; en pacientes con insuficiencia cardiaca crónica estable o descompensada30. En general, se ha demostrado que la terapéutica guiada por resultados de BNP y NT-proBNP reducen el riesgo de muerte de cualquier causa, aunque el nivel de evidencia se ha calificado como baja. La conclusión de la agencia es que tanto BNP como NT-proBNP tiene un buen desempeño como prueba diagnóstica para descartar insuficiencia cardiaca pero mal desempeño para confirmar la condición. Ambas tienen buen valor pronóstico en estos pacientes30.
Un estudio publicado en 2023 por Taylor et al.31 tuvo como objetivo evaluar la precisión diagnóstica de la medición de BNP como NT-proBNP de acuerdo con los puntos de corte de la ESC o de NICE reportados en bases de datos electrónicas en UK. Los autores encontraron en un total de 229,580 pacientes que se realizaron las pruebas y en los cuales en 21,102 (9.2%) se diagnosticaron como con insuficiencia cardiaca en un periodo de 6 meses. Los puntos de corte de NT-proBNP > 125 pg/mL de la ESC mostró una sensibilidad de 94.6% (IC95%: 94.2; 95.0%) y una especificidad de 50.0% (IC95%; 49.7; 50.3%), en comparación a una sensibilidad de 81.7% (IC95% 81.0; 82.3%) y una especificidad de 80.3% (IC95%: 80; 80.5%) cuando se tomaron en cuenta los puntos de corte > 400 pg/mL propuestos por NICE. Los valores predictivos positivos para NT-proBNP fueron de 16.4% (IC95%: 16.1; 16.6%) (ESC) y 30.0% (IC95% 29.6; 30.5%) (NICE). Las conclusiones de los autores fueron que el punto de corte más alto propuesto por NICE falla en detectar 1 de cada 5 pacientes, sin embargo, el punto de corte más bajo propuesto por ESC requiere de más estudios confirmatorios. Ambos puntos de corte mostraron buena sensibilidad para descartar la condición clínica31.
Las troponinas son marcadores de daño miocárdico y su uso más extendido se ubica en padecimientos coronarios agudos y también se ha visto una utilidad en la insuficiencia cardiaca descompensada aguda y en pacientes que reciben quimioterapia potencialmente cardiotóxica4,5,19.
Los lineamientos internacionales y nacionales concuerdan que dentro de los exámenes de laboratorio se soliciten las troponinas como parte de la evaluación del paciente con insuficiencia cardiaca en donde es importante descartar otras causas de daño al miocardio, como miocarditis o infarto. No hay la evidencia suficiente en este momento que establezca una adecuada precisión diagnóstica en pacientes con insuficiencia cardiaca crónica, a diferencia de BNP o NT-proBNP4,5,19.
QUÍMICA SANGUÍNEA
Los lineamientos internacionales recomiendan la toma de productos que nos den información sobre el estado general del paciente en donde sospechemos una insuficiencia cardiaca. Los pacientes con insuficiencia cardiaca, tanto crónica como aguda, pueden cursar con un síndrome de falla orgánica múltiple, por lo que tener un panorama general de las condiciones del paciente es importante. Se ha observado con frecuencia la elevación de indicadores de falla renal y hepática entre otros. La elevación de creatinina puede ser indicador de mal pronóstico sobre mortalidad a 1 año de seguimiento y a 180 días de hospitalización19. Por otro lado, es importante conocer el estado de la función renal y hepática para considerar ajuste de dosis de algunos medicamentos que así lo requieren. Los electrolitos séricos como el sodio y el potasio también han demostrado tener relevancia en el pronóstico de estos pacientes.
BIOMETRÍA HEMÁTICA
Es importante descartar la presencia de alteraciones de la línea roja, como anemia, que se ha reportado se presenta con frecuencia en pacientes con insuficiencia cardiaca (10 a 55%). Una RS publicada por Xia et al. en 2021 tuvo como objetivo evaluar el significado de la anemia como factor pronóstico en pacientes con insuficiencia cardiaca. Los resultados de los metaanálisis mostraron en 11 estudios con 53,502 participantes que la anemia se asocia a mortalidad por todas las causas (RM 1.43; IC95%: 1.29; 1.84) y discretamente para hospitalizaciones (RM 1.22, IC95%: 1.0; 1.58)32.
PRUEBAS DE FUNCIÓN HEPÁTICA
La afectación de diversos órganos en pacientes con insuficiencia cardiaca ha sido estudiada extensamente, no así, la relación con el hígado y algunos "síndromes cardio-hepáticos" que se han descrito en la literatura. Se considera que la congestión hepática por el incremento de la presión venosa central explica la afectación hepática. Un estudio de cohortes que incluyó 2,679 pacientes con insuficiencia cardiaca, estudio CHARM, reportó que los pacientes presentaban afectación en las pruebas de función hepática de manera frecuente (alteraciones de ALT 3.1%, albúmina 18.3%, bilirrubina total 13.0%). Los análisis multivariados demostraron que las alteraciones en la bilirrubina fueron los predictores más robustos asociados a muerte cardiovascular y a hospitalización por insuficiencia cardiaca (cociente de riesgos [CR] 1.21 por 1 DE, p < 0.0001)33.
Pregunta 6: ¿Cuáles son los exámenes de laboratorio complementarios que deben ser considerados en la evaluación diagnóstica de los pacientes con insuficiencia cardiaca crónica?
Recomendación: Una vez realizado el diagnóstico, es importante que todo paciente cuente con química sanguínea, biometría hemática, pruebas de función hepática y cinética de hierro, con el propósito de evaluar el involucro extracardiaco de la insuficiencia cardiaca y la presencia de comorbilidad. La elevación de las troponinas de alta sensibilidad expresa daño miocárdico y tiene valor pronóstico, por lo que siempre que sea posible se pueden considerar dentro de la evaluación diagnóstica de los pacientes con insuficiencia cardiaca.
Nivel de evidencia 2++, grado de recomendación C (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
Las GPC de AHA/ACC 2022 y ESC/ECC 2021 recomiendan en todos los pacientes realizar una evaluación de laboratorio inicial que considere la biometría hemática, análisis de orina, química sanguínea que incluya: electrolitos séricos (incluidos sodio, potasio, calcio y magnesio), nitrógeno ureico en sangre, creatinina sérica, glucosa, perfil de lípidos en ayunas, pruebas de función hepática, estudios de hierro, ferritina, saturación de transferrina), pruebas de función tiroidea. Hay que considerar que además de la evaluación de rutina, a menudo se necesitan pruebas diagnósticas y evaluaciones específicas para identificar la causa específica y otras comorbilidades en pacientes con insuficiencia cardíaca4,5 (Tabla 3).
Tabla 3 Exámenes complementarios para la evaluación inicial integral de la insuficiencia cardiaca
| Estudio | Utilidad | Comentarios | |
|---|---|---|---|
| Diagnóstico | Evaluación integral y pronóstico | ||
| Troponinas de alta sensibilidad | X | Elevaciones leves de las troponinas de alta sensibilidad pueden predecir el pronóstico de los pacientes con insuficiencia cardiaca | |
| Electrolitos séricos | X | La determinación de sodio, potasio y cloro es indispensable como parte de la evaluación integral y la guía terapéutica, particularmente la hiperpotasemia y la hiponatremia | |
| Pruebas de función renal | X | Se debe contar con una evaluación completa de la función renal para reconocimiento y estratificación de posible enfermedad renal crónica mediante la clasificación KDIGO | |
| Pruebas de función hepática | X | La evaluación de la función hepática permite conocer el estado nutricional de los pacientes y guiar las dosis de fármacos que pueden afectar la función del hígado | |
| Biometría hemática, cinética de hierro | X | El 30-50% de los pacientes con insuficiencia cardiaca crónica cursan con déficit de hierro, por lo que es indispensable conocer los valores de ferritina, transferrina y saturación de transferrina | |
| Glucemia en ayuno, hemoglobina glucosilada | X | El 30-40% de los pacientes con insuficiencia cardiaca cursan con disglucemia o diabetes, y la coexistencia de ambas enfermedades repercute en el pronóstico y requiere tratamientos específicos | |
| Modalidades especiales de ecocardiografía | X | Los ecocardiogramas transesofágico y de estrés son útiles para la evaluación de pacientes con sospecha de enfermedad isquémica del corazón, presencia de alteraciones estructurales complejas, trombos o masas intracavitarias, y en la evaluación funcional de pacientes con sospecha de IC con FEVI preservada | |
| Resonancia magnética cardiaca | X | X | Evaluación de la función del ventrículo derecho, reconocimiento de la etiología de las cardiomiopatías, evaluación de la isquemia miocárdica |
| Tomografía computarizada | X | Puede ser útil para el reconocimiento de alteraciones estructurales y vasculares complejas, así como para la evaluación de la anatomía coronaria | |
| Medicina nuclear | X | Debe ser considerada en pacientes con sospecha de enfermedad isquémica del corazón, amiloidosis o procesos inflamatorios | |
| Holter, estudio electrofisiológico | X | En pacientes con síncope o sospecha de arritmias cardiacas es necesaria la evaluación completa mediante monitoreo electrocardiográfico e incluso estudios electroficiológicos invasivos | |
| Cateterismo cardiaco | X | Los estudios de hemodinámica invasiva son útiles para el estudio de la función ventricular, las cardiopatías congénitas y le enfermedad isquémica del corazón, por lo que deben considerarse en casos especiales de pacientes con insuficiencia cardiaca como parte de la evaluación integral | |
| Estudios especiales (genética, microbiología, biología molecular) | X | X | Es necesario que todos los programas estructurados para el manejo de la insuficiencia cardiaca tengan acceso a la realización de pruebas especiales para el diagnóstico completo de pacientes seleccionados |
TROPONINAS
Las troponinas son marcadores de daño miocárdico y su uso más extendido se ubica en padecimientos coronarios agudos y también se ha visto una utilidad en la insuficiencia cardiaca descompensada aguda y en pacientes que reciben quimioterapia potencialmente cardiotóxica4,5,19.
Los lineamientos internacionales y nacionales concuerdan que dentro de los exámenes de laboratorio se soliciten las troponinas como parte de la evaluación del paciente con insuficiencia cardiaca en donde es importante descartar otras causas de daño al miocardio, como miocarditis o infarto. No hay la evidencia suficiente en este momento que establezca una adecuada precisión diagnóstica en pacientes con insuficiencia cardiaca crónica, a diferencia de BNP o NT-proBNP4,5,19.
QUÍMICA SANGUÍNEA
Los lineamientos internacionales recomiendan la toma de productos que nos den información sobre el estado general del paciente en donde sospechemos una insuficiencia cardiaca. Los pacientes con insuficiencia cardiaca, tanto crónica como aguda, pueden cursar con un síndrome de falla orgánica múltiple, por lo que tener un panorama general de las condiciones del paciente es importante. Se ha observado con frecuencia la elevación de indicadores de falla renal y hepática entre otros. La elevación de creatinina puede ser indicador de mal pronóstico sobre mortalidad a 1 año de seguimiento y a 180 días de hospitalización19. Por otro lado, es importante conocer el estado de la función renal y hepática para considerar ajuste de dosis de algunos medicamentos que así lo requieren. Los electrolitos séricos como el sodio y el potasio también han demostrado tener relevancia en el pronóstico de estos pacientes.
BIOMETRÍA HEMÁTICA
Es importante descartar la presencia de alteraciones de la línea roja, como anemia, que se ha reportado se presenta con frecuencia en pacientes con insuficiencia cardiaca (10 a 55%). Una RS publicada por Xia et al. en 2021 tuvo como objetivo evaluar el significado de la anemia como factor pronóstico en pacientes con insuficiencia cardiaca. Los resultados de los metaanálisis mostraron en 11 estudios con 53,502 participantes que la anemia se asocia a mortalidad por todas las causas (RM 1.43; IC95%: 1.29; 1.84) y discretamente para hospitalizaciones (RM 1.22, IC95%: 1.0; 1.58)32.
PRUEBAS DE FUNCIÓN HEPÁTICA
La afectación de diversos órganos en pacientes con insuficiencia cardiaca ha sido estudiada extensamente, no así, la relación con el hígado y algunos "síndromes cardio-hepáticos" que se han descrito en la literatura. Se considera que la congestión hepática por el incremento de la presión venosa central explica la afectación hepática. Un estudio de cohortes que incluyó 2,679 pacientes con insuficiencia cardiaca, estudio CHARM, reportó que los pacientes presentaban afectación en las pruebas de función hepática de manera frecuente (alteraciones de ALT 3.1%, albúmina 18.3%, bilirrubina total 13.0%). Los análisis multivariados demostraron que las alteraciones en la bilirrubina fueron los predictores más robustos asociados a muerte cardiovascular y a hospitalización por insuficiencia cardiaca (cociente de riesgos [CR] 1.21 por 1 DE, p < 0.0001)33.
Pregunta 7: ¿Cuál es la precisión diagnóstica del ecocardiograma en la evaluación de los pacientes con insuficiencia cardiaca crónica?
Recomendación:
– El ecocardiograma es el primordial estudio de imagen cardiovascular no invasiva debido a su disponibilidad, accesibilidad y costo.
– Es importante realizar un ecocardiograma transtorácico en todo paciente con sospecha clínica de insuficiencia cardiaca para confirmar o descartar el diagnóstico.
– El ecocardiograma es fundamental para clasificar la insuficiencia cardiaca de acuerdo con la FEVI.
– Más allá del cálculo de la FEVI, el ecocardiograma es útil para conocer la estructura del corazón, la función diastólica y la presencia de masas intracavitarias, y para realizar estimaciones hemodinámicas.
– Cuando existan dudas de los datos obtenidos mediante ecocardiografía transtorácica en reposo, se debe recurrir a modalidades como la ecocardiografía transesofágica o la ecocardiografía de esfuerzo.
– El ecocardiograma es útil para evaluar la evolución de la enfermedad y la respuesta al tratamiento, por lo que debe realizarse de forma periódica e individualizada para cada paciente.
– El ecocardiograma tiene limitantes para el estudio de la función ventricular derecha.
– En los pacientes en quienes la evaluación ecocardiográfica es insuficiente, se deben considerar otras técnicas de imagen como la resonancia magnética cardiaca (RMC).
Nivel de evidencia 2++, grado de recomendación C (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
Las GPC de la AHA/ACC/HFSA 2022, ESC 2021, NICE 2018, SIGN 2015 y el Consenso Mexicano2 de Insuficiencia Cardiaca4,5,34,35 establecen a la ecocardiografía como con un papel clave para la evaluación de los pacientes a los que se sospecha insuficiencia cardiaca debido a la gran cantidad de información útil para el diagnóstico y también para el pronóstico. El estudio de ecocardiografía provee información sobre la estructura y función del corazón que incluyen dimensiones de los ventrículos y su volumen, la geometría de las cámaras y la contractibilidad de las paredes ventriculares, esta información puede ser valiosa incluso para la modificación de esquemas de tratamiento. La función de la válvula tricúspide, así como el diámetro de la vena cava y sus cambios durante los ciclos respiratorios ofrecen datos confiables sobre la presión arterial pulmonar (PAP) y la presión venosa central (PVC).
Estas guías también recomiendan la realización de ecocardiogramas seriados con la finalidad de evaluar cambios en la fracción de expulsión, remodelación estructural y función valvular, aunque no es necesario hacerlo en pacientes estables. Los pacientes que muestran deterioro clínico o aquellos que responden a la terapéutica médica, revascularización o terapia con dispositivos; son pacientes que se pueden ver beneficiados de realizarles estudios de ecocardiografía seriados. La reevaluación de la FEVI en pacientes después de un infarto al miocardio (> 40 días), después de un procedimiento de revascularización (> 90 días) y después de la Terapia Médica Dirigida por Guías (GDMT, por sus siglas en inglés) (> 90 días) es útil para considerar a los pacientes candidatos a la colocación de un desfibrilador cardioversor implantable (ICD, por sus siglas en inglés) o terapia de resincronización cardiaca (CRT, por sus siglas en inglés); y finalmente en aquello pacientes que han sido expuestos a tratamientos cardiotóxicos4.
Los lineamientos publicados en 2016 por la Sociedad Americana de Ecocardiografía (ASE, por sus siglas en inglés) y la Asociación Europea de Imagen Cardiovascular (EACI, por sus siglas en inglés)36 consideran la evaluación de la función ventricular izquierda y de la función diastólica como una parte integral de la evaluación rutinaria de pacientes con un cuadro clínico sugestivo de insuficiencia cardiaca36. La disfunción diastólica del ventrículo izquierdo se asocia normalmente a una fase de relajamiento alterada con o sin succión diastólica y/o incremento de rigidez de las cámaras, lo que incrementa la presión de llenado. Por ello, estos lineamientos recomiendan buscar los signos de afectación en la relajación de las paredes del ventrículo izquierdo, reducción de las fuerzas de recuperación e incremento de la rigidez de las cámaras. Estos lineamientos hacen énfasis en que el equipo debe de ser de alta calidad y la señal del transductor Doppler adecuada. Se deben de considerar todos los factores hemodinámicos que afectan cada parámetro evaluado, algunas veces los valores medidos pueden caer dentro de rango de normalidad a pesar de que exista una disfunción diastólica, por lo que es importante considerar un grupo de mediciones y no tomar en cuenta valores aislados en las conclusiones. Es importante que el especialista en ecocardiografía conozca a detalle el mecanismo fisiológico detrás de cada de las variaciones, de las situaciones que las modifican y de los aspectos técnicos del análisis de las señales Doppler y 2D36.
Estos lineamientos establecen que para la evaluación de la disfunción diastólica en la presencia de una FEVI normal se deben de evaluar cuatro variables. La presencia de distintos resultados fuera de rango, así como el uso de diversos puntos de corte con alta especificidad para enfermedad del miocardio son recomendables para evitar los resultados falsos positivos de disfunción diastólica. Las cuatro variables recomendadas y sus puntos corte para considerar la medición como fuera de rango incluyen 1) velocidades del flujo mitral, 2) velocidad é del anillo mitral, relación E/é, 3) velocidad máxima de la regurgitación tricuspídea y 4) volumen máximo indexado de la aurícula izquierda. El diagnóstico ecocardiográfico de la disfunción diastólica requiere que al menos tres de los cuatro parámetros considerados sean positivos. Cuando se obtiene uno o ninguno de los valores considerados, se puede afirmar que no hay disfunción diastólica. Como muestra el algoritmo, el hallazgo de dos parámetros positivos no permite descartar la presencia o ausencia de disfunción diastólica36.
En los casos en donde se encuentra una FEVI reducida, existirá en todos los casos cierto grado de disfunción diastólica, y el algoritmo propone realizar el diagnóstico de acuerdo con el grado de disfunción diastólica y evaluar la presencia de aumento de presiones de llenado. Se inicia por la valoración de la velocidad de las ondas del flujo mitral, que permite la diferenciación del grado I de disfunción diastólica, patrón conocido como de relajación anormal donde la presión auricular izquierda (PAI) es siempre normal o baja, y en el otro extremo el patrón restrictivo que se acompaña siempre de incremento de la PAI. Es importante cuantificar el cociente E/e, el volumen de AI y la velocidad del gradiente sistólico aurícula derecha-ventrículo derecho. En estos casos la presencia de dos parámetros que superen el punto de corte establecido permite establecer la existencia de grado II de disfunción diastólica y aumento de las presiones de llenado. En este algoritmo también se considera la posibilidad de que sólo se disponga de dos de los tres parámetros36.
Pregunta 8: ¿Cuál es la precisión diagnóstica de los estudios de imagen no invasivos para los pacientes con insuficiencia cardiaca crónica?
Recomendación:
– Debido a su disponibilidad y bajo costo, el estudio radiográfico de tórax sigue siendo útil en la evaluación inicial de la insuficiencia cardiaca.
– La radiografía de tórax permite identificar alteraciones de la silueta cardiaca, los grandes vasos y la presencia de congestión pulmonar.
– La radiografía de tórax tiene limitantes importantes, por lo que no debe ser considerada como el único estudio de imagen en la evaluación diagnóstica de la insuficiencia cardiaca.
– La RMC es el estudio de imagen cardiovascular no invasivo con mayor precisión para evaluar la estructura y la función del ventrículo derecho.
– La RMC es fundamental en la evaluación de la etiología de las cardiomiopatías como causa de insuficiencia cardiaca.
– La RMC es auxiliar en la evaluación diagnóstica integral de la insuficiencia cardiaca cuando los datos del ecocardiograma se consideren insuficientes.
– Los estudios de medicina nuclear (tomografía por emisión de fotón único, tomografía por emisión de positrones) son útiles para la evaluación de isquemia y viabilidad miocárdica en pacientes con insuficiencia cardiaca.
– La gammagrafía cardiaca es útil para la evaluación diagnóstica de miocarditis o amiloidosis cardiaca como causas de insuficiencia cardiaca.
– La angiografía por tomografía computarizada es útil para evaluar la presencia de enfermedad arterial coronaria en pacientes con insuficiencia cardiaca y sospecha de enfermedad isquémica del corazón.
Nivel de evidencia 2++, grado de recomendación C (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
Históricamente la realización de estudios radiológicos simples en la enfermedad cardiaca, han servido de preámbulo para la realización de estudios de imagen más complejos. Tanto las proyecciones posteroanterior como lateral de tórax proveen imágenes útiles para ir definiendo la estructura cardiaca y pulmonar, sobre todo procesos congestivos pulmonares. Por ello el consenso mexicano en insuficiencia cardiaca2 recomiendan la realización en todos los pacientes en quienes se sospecha una insuficiencia cardiaca un estudio radiológico inicial. Las GPC ADA/ACC 2022 recomiendan la realización de estudios radiológicos simples ya que son útiles para la identificación de cardiomegalia, congestión de las venas pulmonares, edema alveolar o intersticial y puede descubrir datos de diagnósticos diferenciales de insuficiencia cardiaca. Sin embargo, resaltan su baja sensibilidad y especificidad para poder emplearlas como únicas pruebas diagnósticas4.
La realización de estudios como la tomografía computarizada cardiaca (TCC), la resonancia magnética cardiaca (RMC) o estudios de medicina nuclear también se encuentran dentro de las alternativas de pruebas diagnósticas no invasivas. La RMC provee una evaluación precisa y altamente reproducible del volumen cardiaco, de su masa y de la fracción de expulsión del ventrículo izquierdo y derecho. La RMC brinda detalles anatómicos precisos de la estructura cardiaca y de órganos vecinos, además que no emplea radiación ionizante. El uso de gadolinio como medio de contraste puede mostrar zonas de fibrosis u otro daño al miocardio y puede identificar zonas de infarto, agudas o crónicas. También puede detectar procesos infiltrativos o inflamatorios como la amiloidosis, miocarditis, sarcoidosis, entre otras. La presencia de reforzamiento retardado se ha asociado a peor pronóstico y puede ayudar a la estratificación del riesgo. La RMC también tiene un papel en la identificación de los pacientes candidatos al implante de Terapia de Resincronización Cardiaca (TRC).
Una RS publicada por Assadi et al. en 202137 evaluó la precisión diagnóstica de la RMC en el diagnóstico de insuficiencia cardiaca con fracción de expulsión conservada. Los autores incluyeron 9 estudios de prueba diagnóstica (cohortes observacionales prospectivas) con cegamiento a los resultados de la RMC. Se incluyeron 2,350 pacientes. Las técnicas de RMC que se evaluaron fueron el realce tardío de gadolinio (RTG), determinación de los tiempos de relajación T1 mediante el mapeo de T1 y evaluación de la isquemia. Se encontró una medida de asociación, coeficiente de riesgo (CR) de 1.52 (DE 0.24, IC95% 1.05; 1.99). El segundo grupo fue el de los estudios que caracterizaron el tejido cardiaco, donde 4 estudios resultaron en un coeficiente de riesgo (CR) de 1.25 (DE 0.18, IC95% 0.89; 1.60). El tercer grupo fueron 2 estudios que evaluaron isquemia miocárdica o función ventricular derecha. Las medidas de asociación fueron las más altas de todas con un coeficiente de riesgo (CR) de 3.19 (DE 1.47, IC95% 0.30; 6.08). La prueba de RGT ha demostrado un alto valor pronóstico en pacientes con insuficiencia cardiaca (ICFEp) en los cuales se presentaron más eventos cardiovasculares y muerte en razón proporcional al tejido cicatrizal. En cambio, la determinación de los tiempos de relajación T1 mediante el mapeo de T1 evalúa la extensión de la fibrosis difusa en el miocardio y es muy útil en diversas cardiomiopatías. El estudio de estrés cardiaco es útil en detectar patología subclínica, como enfermedad coronaria, disfunción microvascular, cardiomiopatía hipertrófica y pericarditis constrictiva. La disfunción sistólica ventricular derecha tiene buena precisión para predecir eventos cardiovasculares37.
Los avances en la tecnología de TCC incluyen equipos con detectores más amplios para poder recrear cortes de un solo latido (320 cortes), una resolución incrementada al aumentar la velocidad de rotación helicoidal (< 500 a 250 milisegundos) y el desarrollo de CT de doble fuente de poder. La resolución se ha incrementado dado que ahora podemos tener imágenes de 0.3 mm38. La enfermedad arterial coronaria ha sido reconocida como una de las principales causas de insuficiencia cardiaca crónica y aguda y la angiografía coronaria invasiva es el estándar de referencia en estos pacientes. La TCC está indicada para la exclusión de enfermedad arterial coronaria en pacientes de riesgo bajo a moderado debido a su excelente valor predictivo negativo y alta especificidad en esta población de pacientes. Además, ofrece información adicional del estado de las estructuras cardiacas y de estructuras vecinas38.
Una RS publicada por Paech et al.39 tuvo como objetivo evaluar la precisión de la TCC. Los autores incluyeron 28 estudios de prueba diagnóstica con 3,674 pacientes. Los resultados de los metaanálisis mostraron una sensibilidad de 98.2% y una especificidad de 81.6%, Los valores predictivos positivos (VPP) fueron de 90.5% (76-100%) y los valores predictivos negativos (VPN) de 99% (83-100%). Cuando se estratificaron los resultados se observó una menor precisión diagnóstica en la arterial anterior descendente izquierda y circunfleja y mayor en la arteria coronaria izquierda principal. La conclusión de los autores es que la TCC tiene una adecuada utilidad diagnóstica para evaluar enfermedad arterial coronaria39. Una RS publicada por Westwood et al.40 tuvo como objetivo el de valorar la precisión diagnóstica de la TCC para detectar la enfermedad arterial coronaria en pacientes difíciles de evaluar (pacientes con taquicardia, obesos, pacientes con concentraciones altas de calcio que producen artefactos o pacientes con "stents" coronarios). Los autores incluyeron 25 estudios que reportaron la precisión diagnóstica de la TCC. Los metaanálisis muestran una sensibilidad del 97.7% (IC95%: 88.0%, 99.9%) y del 97.7% (IC95%: 93.2%, 99.3%) en pacientes que presentaban arritmias y taquicardia. La especificidad calculada fue de 81.7% (IC95%: 71.6%, 89.4%) y de 86.3% (IC95%: 80.2%, 90.7%), respectivamente40.
La medición de la reserva fraccional de flujo (RFF) por TCC es posible con los equipos más modernos. Una RS publicada por Nørgaard et al.41 en 2022 tuvo como objetivo el de valorar la precisión diagnóstica de la medición de la reserva fraccional de flujo (RFF) por TCC. Los autores incluyeron 5 estudios con 5,460 pacientes. Los desenlaces ocurrieron en 60 pacientes (1.1%), de los cuales 0.6% (13/2126) con FFRCT > 0.80% y en 1.4% (47/3334) FFRCT < 0.80% con un RR (riesgo relativo) 2.31 (IC95%: 1.29; 4.13). De igual manera los eventos cardiovasculares mayores (MACE, por sus siglas en inglés) ocurrieron con más frecuencia en pacientes con FFRCT < 0.80%. Cada reducción de 0.10 unidades de FFRCT se asoció a un mayor riesgo cardiovascular (RR 1.67, IC96%: 1.47; 1.87)41.
La mayoría de los lineamientos concuerdan que la ecocardiografía seguirá siendo la investigación de primera línea para la insuficiencia cardíaca debido a su accesibilidad, versatilidad y portabilidad. Cuando se requiere información más detallada sobre el rendimiento ventricular o la caracterización del miocardio, las imágenes de RMC ya se han establecido como una prueba estándar de oro. En un corto período de tiempo, la TC cardíaca ha cambiado sus límites de ser una prueba para la enfermedad coronaria únicamente a una que tiene relevancia para una variedad de otras afecciones cardíacas. Las ventajas de la TCC para proporcionar alta resolución de imagen a un costo accesible, en un marco de tiempo rápido y con una radiación ionizante cada vez menor, le han permitido ganar relevancia en pacientes con insuficiencia cardíaca38.
Pregunta 9: ¿Cuál es la precisión diagnóstica de los estudios invasivos para los pacientes con insuficiencia cardiaca crónica?
Recomendación:
– La angiografía es el método de referencia para la evaluación anatómica y funcional de la circulación coronaria, por lo que se debe considerar como parte de la evaluación integral de los pacientes con insuficiencia cardiaca de origen isquémico con miras a procedimientos de revascularización miocárdica.
– El cateterismo derecho e izquierdo con toma de presiones es parte fundamental de la evaluación hemodinámica en los pacientes con insuficiencia cardiaca avanzada con miras a trasplante o asistencia mecánica de la circulación.
– El cateterismo cardiaco no es un estudio sistemático en la evaluación diagnóstica de los pacientes con insuficiencia cardiaca.
– La biopsia endomiocárdica debe considerarse como fundamental dentro del protocolo de seguimiento de los pacientes con trasplante cardiaco.
– La biopsia endomiocárdica puede considerarse como adyuvante en la evaluación de la etiología de la insuficiencia cardiaca cuando los métodos de imagen no invasivos no son concluyentes.
– La biopsia endomiocárdica no es un estudio sistemático en la evaluación diagnóstica de los pacientes con insuficiencia cardiaca.
Nivel de evidencia 2++, grado de recomendación C (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
Los estudios invasivos cardiacos, como el cateterismo y la angiografía coronaria, pueden ofrecer información importante para guiar el tratamiento de los pacientes con insuficiencia cardiaca. Las GPC ADA/ACC 2022 recomiendan la realización de biopsia endomiocárdica en los pacientes en los que es primordial tener un diagnóstico confirmado de las distintas entidades nosológicas que pueden conducir a un paciente a la insuficiencia cardiaca, sobre todo, cuando esta es rápidamente progresiva. La biopsia también debe ser considerada en los pacientes postransplantados que están manifestando síntomas de rechazo o en aquellos pacientes con enfermedades infiltrativas. El papel del cateterismo cardiaco del ventrículo derecho está bien establecido en la insuficiencia aguda, sin embargo, no está muy claro el mayor beneficio sobre el riesgo como método diagnóstico de rutina o periódico en el manejo de la insuficiencia cardiaca en general4.
Las GPC ESC 2021 recomiendan la realización de angiografía coronaria invasiva en pacientes con insuficiencia cardiaca y un riesgo intermedio alto de enfermedad coronaria aguda y la presencia de isquemia en la prueba de estrés no invasiva con la finalidad de establecer el diagnóstico y su gravedad5. Adicionalmente, el consenso mexicano 2022, propone un papel importante en la evaluación de las presiones intracardiacas, el cálculo de algunos parámetros hemodinámicos como le presión capilar pulmonar, las resistencias pulmonares, entre otros, los cuales son de gran importancia en la evaluación integral de pacientes con hipertensión arterial pulmonar (HAP) o en pacientes en protocolo de trasplante cardiaco y pulmonar19.
Las mediciones que han demostrado tener un valor pronóstico dependen principalmente de parámetros de prellenado como la presión de enclavamiento capilar pulmonar. Una RS publicada por Aalders et al.42 en 2019 tuvo como objetivo evaluar las variables hemodinámicas que tienen un valor pronóstico en la insuficiencia cardiaca. Los autores incluyeron 18 estudios que hicieron análisis multivariado y 2 estudios con análisis univariado de los distintos parámetros hemodinámicos que pudieran tener valor pronóstico en pacientes con insuficiencia cardiaca. Los autores se enfocaron en la medición del gasto o índice cardiacos, de la precarga la presión de enclavamiento capilar pulmonar y la postcarga, definida como la presión en las paredes del ventrículo izquierdo en sístole, dividida por el grosor de las paredes ventriculares. Los resultados de los análisis univariados de asociación fueron que el gasto cardiaco fue un factor significativo en los desenlaces en los pacientes y la presión de enclavamiento capilar pulmonar lo fue en prácticamente todos los estudios. Cuando se realizaron estudios multivariados, se encontró que el gasto cardiaco dejó de tener un valor predictivo, sin embargo, la presión de enclavamiento capilar pulmonar conservó su valor predictivo en los modelos multivariados en todos menos un estudio. Esto último tanto en pacientes con insuficiencias cardiaca crónica como en pacientes con insuficiencia cardiaca aguda. La presión sistólica fue el segundo mejor factor predictivo42.
Una revisión publicada por Hsu et al.43 sobre el papel de los estudios de hemodinamia en pacientes con insuficiencia cardiaca establecen que la Sociedad Americana de Insuficiencia Cardiaca (HFSA) recomienda en contra de la realización de rutina de estudios hemodinámicos en pacientes con insuficiencia cardiaca (ICFEr) debido a que el estudio ESCAPE falló en demostrar un beneficio en la reducción de la mortalidad en pacientes con insuficiencia cardiaca descompensada, sin embargo, la información que los estudios invasivos proveen son de gran utilidad en pacientes con insuficiencia cardiaca avanzada o shock cardiogénico43. En los pacientes candidatos a trasplante cardiaco es importante descartar un incremento de la resistencia vascular pulmonar, ya que es una contraindicación relativa debido al incremento del riesgo de muerte. La prueba con nitroprusiato de sodio puede identificar aquellos pacientes con resistencia incrementada reversible. En algunos casos el estudio hemodinámico con ejercicio puede ayudar a evaluar si el paciente es candidato a trasplante, midiendo al mismo tiempo el gasto cardiaco y la saturación de oxígeno venosa se puede calcular si el corazón todavía puede suplir la demanda metabólica corporal durante el ejercicio43.
Otra población de pacientes que se benefician de la evaluación hemodinámica, son aquellos a los que se les ha colocado un dispositivo de asistencia del ventrículo izquierdo (LVAD) debido a que la falla del ventrículo derecho sigue siendo una causa importante de morbi-mortalidad en estos pacientes. En los pacientes que acaban de recibir la colocación de LVAD se les recomienda evaluar el gasto cardiaco, las presiones de llenado, la postcarga, y la precisión diagnóstica aumenta cuando se incluye una valoración ecocardiográfica43.
Alrededor de la mitad de los pacientes con insuficiencia cardiaca tienen FEVI preservada (ICFEp). Es muy común que estos pacientes muestren resultados de estudios no invasivos dentro de parámetros normales en reposo, por lo que es importante llevar a cabo las evaluaciones hemodinámicas en reposo y durante el ejercicio para tener un estudio óptimo de estos pacientes43.
Una RS publicada por Bingel et al. publicada en 202244 tuvo como objetivo evaluar los cambios hemodinámicos durante estrés fisiológico y farmacológico en pacientes con insuficiencia cardiaca. Se analizaron 140 brazos de estudios y 7,248 pruebas durante el ejercicio y los resultados mostraron que no hubo diferencias en los parámetros entre pacientes ICFEr y ICFEp pero sí cuando se comparan con controles sanos44.
Pregunta 10.1: ¿En qué pacientes es recomendable realizar una prueba de la caminata de 6 minutos (6MWD, 6-minute walking distance) como parte de la evaluación diagnóstica de la insuficiencia cardiaca crónica?
Recomendación:
– Se recomienda realizar una 6MWD en los pacientes con insuficiencia cardiaca crónica en quienes la evaluación de la clase funcional por interrogatorio sea no concluyente.
– Se recomienda realizar una 6MWD en pacientes con insuficiencia cardiaca como parte de la evaluación de la respuesta al tratamiento.
Nivel de evidencia 2++, grado de recomendación C (recomendación fuerte).
Pregunta 10.2: ¿En qué pacientes con insuficiencia cardiaca crónica se recomienda realizar una prueba de ejercicio cardiopulmonar?
Recomendación: Se debe realizar una prueba de ejercicio cardiopulmonar con determinación del consumo de oxígeno en todo paciente con insuficiencia cardiaca crónica que se encuentre en protocolo de estudio para definir su ingreso a un programa de trasplante cardiaco o de asistencia mecánica de la circulación de largo plazo.
Nivel de evidencia 2++, grado de recomendación C (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
El consenso mexicano sobre insuficiencia cardiaca establece la importancia de realizar una evaluación de la clase funcional de manera acuciosa, sin embargo, también puede ser difícil llevarla a cabo de manera precisa, sobre todo en pacientes estables que reportan síntomas leves. Se ha reportado la tendencia de los pacientes por minimizar la gravedad de sus síntomas. De ahí la importancia de hacer lo más objetivo posible la evaluación de estos2.
Las pruebas para evaluar la capacidad funcional y la tolerancia al ejercicio se dividen en tres categorías. En primer lugar, el reporte autoadministrado o evaluado por el médico del estado físico de los pacientes percibido por ellos mismos. En segundo lugar, las pruebas cardiovasculares durante el ejercicio (CPET, por sus siglas en inglés) o ergoespirometría, que se consideran el estándar de referencia que mide la capacidad durante el ejercicio y el consumo de oxígeno pico. Sin embargo, se requiere de equipo especial y de profesionales capacitados para poderla llevar a cabo y en muchas ocasiones no está fácilmente disponible. En tercer lugar, la evaluación de la capacidad para realizar actividades diarias a través de ejercicio submáximo como la prueba de caminata de seis minutos (C6M), que fue concebida como una prueba que, aunque no conlleva un esfuerzo grande para el paciente, puede cuantificar de manera bastante precisa la capacidad de tolerancia a la actividad física y sus variaciones en relación con las intervenciones terapéuticas realizadas y respecto a la propia evolución de la enfermedad y ha sido validada ampliamente como una prueba fiable y fácilmente reproducible en pacientes con insuficiencia cardiaca. Es poco costosa y sencilla de realizar y se considera como una prueba con buena respuesta terapéutica en los pacientes que logran caminar al menos 30 metros, sin embargo, una caída de 4% o más en la saturación de oxígeno se considera de mal pronóstico45.
Una RS publicada por Giannitsi et al. en 202145 tuvo como objetivo la utilidad diagnóstica de la C6M en pacientes con insuficiencia cardiaca. La prueba de C6M no brinda información sobre el grado de funcionamiento de cada sistema de manera individual, a diferencia de la CPET. La prueba de C6M tiene una buena correlación con otras pruebas diagnósticas, se ha demostrado en estudios clínicos una correlación inversa entre las clases II a la IV de la NYHA y la prueba C6M (400 m, 320 m y 225 m), sin embargo, se observó pobre discriminación entre los pacientes con clase I y II y la C6M (400 m)45. Se ha reportado una correlación moderada a fuerte entre la prueba C6M y la CPET, que se considera que provee los mejores indicadores de la capacidad funcional de los pacientes (VO2 pico, VO2 máximo y punto de corte anaeróbico). La prueba C6M con resultado de < 350 m tiene una sensibilidad de 71% y una especificidad de 60% para predecir una VO2 máxima de < 14 ml/kg/min. La C6M ha mostrado tener una capacidad pronóstica similar a la CMET en algunos parámetros. La capacidad pronóstica de la C6M mejora aún más cuando se combina con los resultados de la ecocardiografía45. Una gran cantidad de condiciones clínicas han mostrado afectar el rendimiento en la prueba de C6M como la diabetes, las nefropatías, la depresión, síndrome de fragilidad, la anemia, entre otros. La prueba de C6M también tiene una buena correlación con la FEVI disminuida, así como otras variable ecocardiográfricas. Se ha reportado que en los pacientes ICFEr, una prueba C6M con bajo desempeño predice un incremento en el riesgo de mortalidad, eventos cardiovasculares no fatales y hospitalizaciones por insuficiencia cardiaca. La C6M se ha utilizado ampliamente para evaluar la respuesta a tratamiento de diversas clases terapéuticas45.
Una RS publicada por Pollentier et al.46 tuvo como objetivo evaluar la precisión diagnóstica de la prueba de C6M para evaluar la capacidad funcional en pacientes con insuficiencia cardiaca. Los autores incluyeron 14 estudios y reportaron una buena reproducibilidad y una moderada a alta correlación de la CM6 con los niveles de VO2 pico y la habilidad de predecir la capacidad funcional dependiendo de la distancia caminada. Los puntos de corte variaron de 300 a 490 metros46.
La prueba CPET típicamente involucra el empleo de grupos musculares grandes, miembros inferiores, hacia el límite de la tolerancia en una bicicleta estática o una caminadora, con un incremento rápido que impone un estrés progresivo hacia el límite de la tolerancia del individuo. Las variables clínicamente relevantes con la VO2 pico que es independiente del índice de incremento de trabajo. Una intolerancia al ejercicio puede explicarse por afectación a nivel ventilatorio, a nivel cardio circulatorio o a nivel metabólico muscular47.
Un documento de posicionamiento de la ESC en 2017 sobre el papel de la CPET48 establece que la CPET tiene un papel muy importante en los pacientes ICFEr. Actualmente, el uso de la CPET es más amplio e incluye mujeres, personas mayores, pacientes con comorbilidades, aquellos con ICFEp o con dispositivos de asistencia al ventrículo izquierdo. Por ello, la utilidad clínica y pronóstica de una CPET subóptima realizada en una prueba inframáxima se está considerando hoy en día, debido a que muchos pacientes no pueden concluir la prueba con los parámetros tradicionales. La realización de pruebas seriadas es útil en la estratificación del riesgo y en evaluación de la respuesta terapéutica a múltiples intervenciones48.
Pregunta 11.1: ¿Cuál es la precisión diagnóstica de los cuestionarios clinimétricos de riesgo y calidad de vida para los pacientes con insuficiencia cardiaca crónica?
Recomendación:
– Es recomendable realizar una evaluación de la calidad de vida con cuestionarios validados como parte del estudio inicial de los pacientes con insuficiencia cardiaca crónica.
– Es necesario realizar una evaluación de la calidad de vida con cuestionarios validados en todo paciente con sospecha de insuficiencia cardiaca avanzada.
– Es recomendable realizar una evaluación de la calidad de vida mediante cuestionarios validados como parte del seguimiento de los pacientes con insuficiencia cardiaca crónica.
Nivel de evidencia 2++, grado de recomendación C (recomendación fuerte).
Pregunta 11.2: ¿En qué pacientes es recomendable realizar una estratificación del riesgo durante la evaluación de la insuficiencia cardiaca crónica?
Recomendación: Es recomendable realizar una estratificación del riesgo de eventos mayores mediante escalas validadas durante la evaluación inicial de todo paciente con insuficiencia cardiaca crónica.
Nivel de evidencia 2++, grado de recomendación C (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
El impacto que la insuficiencia cardiaca tiene en los pacientes que viven con esta condición en su calidad de vida relacionada a su salud (HRQoL, por sus siglas en inglés) no es un tema de poca importancia. Reportes recientes calculan al menos 6.2 millones de personas con insuficiencia cardiaca tan solo en EE. UU. y se espera que rebase los 8 millones en los siguientes años. La carga de la enfermedad no se limita a la parte económica de pacientes y sistemas de salud, sino que las distintas alteraciones físicas y emocionales, como la fatiga, disnea, edema, depresión, ansiedad, entre otros. También se ha reportado que una disminución en la HRQoL de los pacientes con insuficiencia cardiaca se asocia a un riesgo incrementado de hospitalizaciones y de la mortalidad49.
Dado que uno de los objetivos principales en el tratamiento de pacientes con insuficiencia cardíaca es la de evaluar y mejorar la salud de los pacientes, incluidos los síntomas, la función y la calidad de vida, es intuitivo crear herramientas para medir de manera efectiva el estado de salud como resultado. La importancia del estado de salud ha sido reconocida por las autoridades reguladoras que los han respaldado como un posible resultado aprobable. Como tal, la recopilación de datos sobre el estado de salud en los ensayos clínicos se ha convertido en una rutina. Si bien medir el estado de salud ahora puede ser una rutina, la metodología para hacerlo está evolucionando. Este proceso inició con cuestionarios genéricas de calidad de vida y ahora se ha perfeccionado y reducido a cuestionarios clinimétricos validados internacionalmente y empleados en una gran cantidad de estudios clínicos. Uno de los cuestionarios clinimétricos más empleados es The Minnesota Living With Heart Failure Questionnaire (MLHFQ), validado y desarrollado por Rector, Kubo, y Cohn50 como instrumento específico para evaluar la HRQoL en pacientes con insuficiencia cardiaca. La escala de Minnesota tiene fiabilidad, reproducibilidad y validez que ha sido evaluada en múltiples estudios clínicos, incluso con el objetivo de medir la respuesta a distintas intervenciones clínicas49,50. El cuestionario consiste en que los pacientes responden 21 "ítems", con una escala cuantitativa de 6 puntos (0-5) y el total numérico puede ir en un rango de 0 a 105 puntos. Dos subescalas reflejan una dimensión física (8 "ítems") y un dominio emocional (5 "ítems"). Se ha demostrado que el cuestionario es sensible a la mejoría clínica como resultado del tratamiento, con un cambio de 5 puntos en la puntuación total para interpretarse como clínicamente significativo. Este cuestionario autoadministrado se ha empleado ampliamente debido a que es accesible, corto, sencillo de entender por individuos enfermos y ancianos49,50.
El Kansas City Cardiomyopathy Questionnaire (KCCQ) es un cuestionario autoadministrado que contiene 23 ítems desarrollado para medir de forma independiente la percepción del paciente sobre sus síntomas de insuficiencia cardíaca, impacto en la función física y social, y cómo su insuficiencia cardíaca afecta su calidad de vida (QOL) dentro de un período de 2 semanas. La herramienta KCCQ cuantifica los siguientes seis (6) dominios distintos y dos (2) puntuaciones de resumen. El KCCQ califica diversos dominios: síntomas, función física, HRQoL, limitación social, estabilidad de los síntomas, autosuficiencia, calificación global de síntomas y la evaluación global. Las respuestas se califican a través de una escala cuantitativa de peor a mejor, y el cuestionario de 23 "ítems" tarda de 4 a 6 minutos en ser respondido50-52.
Una RS publicada por Morgan et al.52 tuvo como objetivo identificar estudios clínicos que hubieran evaluado la HRQoL en pacientes con insuficiencia cardiaca. Los autores incluyeron 120 estudios, de los cuales 44 evaluaron alternativas terapéuticas, 19 procedimientos invasivos y 57 intervenciones de cuidados generales. Los autores encontraron que la escala de HRQoL más empleada fue la MLHFQ (87%) y los estudios en donde se observó una mejor respuesta con mejoría en la HRQoL de los pacientes con insuficiencia cardiaca fueron aquellos en los que se probaron procedimientos invasivos, a diferencia de los estudios en donde se evaluaron medicamentos que en la mayoría no pudieron demostrar un cambio significativo en las escalas de HRQoL52.
Una RS publicada por Garin et al.51 tuvo como objetivo evaluar los instrumentos de HRQoL para pacientes con insuficiencia cardiaca. Los autores identificaron siete distintos instrumentos de medición de HRQoL específicos para la enfermedad, entre ellos el Chronic Heart Failure Assessment Tool, el Cardiac Health Profile Congestive Heart Failure, el Chronic Heart Failure Questionnaire (CHFQ), el KCCQ, el Left Ventricular Disease Questionnaire (LVDQ), el MLHFQ y el Quality of Life in Severe Heart Failure Questionnaire. Los resultados de la evaluación por parte de los autores mostraron que los cuestionarios LVDQ, CHFQ, KCCQ y el MLHFQ tuvieron buenas calificaciones de validez (de 54.4 a 76.4 con la escala EMPRO [evaluating measures of patient-reported outcomes], que va del 0 al 100). El KCCQ tuvo la mayor sensibilidad al cambio (media: 94.4) y también tuvo calificación alta respecto a interpretabilidad (72.2) al igual que el CHFQ. Los instrumentos que recibieron las evaluaciones más altas en general de acuerdo con el instrumento EMPRO fueron el KCCQ (64.4) y el MLHFG (60.7), seguidos del CHFQ (59.2), por lo que fueron los sugeridos para su uso por este grupo de expertos.
Una RS más reciente, publicada por Moradi et al. en 2019 tuvo como objetivo evaluar el impacto en la HRQoL de los pacientes con insuficiencia cardiaca a nivel global, y los autores incluyeron 70 estudios clínicos (25,180 pacientes) publicados en un total de 23 países y los cuestionarios más empleados fueron el Short Form Health Survey (SF-36) (15 estudios), el MLHFQ (41 estudios)49 el Kansas City Cardiomyopathy Questionnaire (KCCQ) (9 estudios), y algunos otros en contados estudios. Los resultados de los metaanálisis mostraron en los estudios que emplearon el MLHFQ (12,520 pacientes) una media ponderada de 44.1 (IC95%, 40.6; 47.5) y cuando se estratificaron en los diversos continentes se obtuvieron en América (48.0), Europa (45.5) y Asia (35.1), este último con una diferencia estadísticamente significativa. Los análisis subgrupo mostraron que el grupo de adultos mayores tuvieron una mayor afectación en su HRQoL (media ponderada 46.6, IC95%: 43.0; 50.2) en comparación a los pacientes adultos (media ponderada 41.2, IC95%: 33.5; 48.9). Tanto las subescalas físicas y emocionales se vieron más afectadas en los grupos de adultos mayores. Estos hallazgos se reprodujeron en los estudios que emplearon escalas de HRQoL generales, como la SF-36, donde se reportó una afectación importante en estos pacientes. Cuando se empleó la escala de KCCQ, siete estudios con 4,272 participantes, se obtuvo una media ponderada de 60.9 (IC95% 56.2; 65.5). El MHLFQ indica una mayor afectación en la HRQoL cuanto mayor es la calificación, los puntos de corte son < 24 (buena HRQoL), 24 a 45 (moderada HRQoL) y > 45 (mala HRQoL), por lo que los resultados de esta RS muestran una afectación de moderada a grave en la HRQoL, tanto en la dimensión física como en la dimensión mental, en los pacientes con insuficiencia cardiaca crónica49.
Algunos de estos cuestionarios han sido validados en distintos idiomas incluido el español, y están disponibles para su uso en el consultorio y con fines de investigación53,54.
Pregunta 12: ¿Cuáles son los objetivos del tratamiento de los pacientes con insuficiencia cardiaca crónica?
Recomendación: Los objetivos del tratamiento deben considerar controlar los síntomas, mejorar la calidad de vida, reducir los episodios de empeoramiento y mejorar el pronóstico de vida.
Nivel de evidencia 1++, grado de recomendación A (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
Los lineamientos internacionales establecen que hay diversos objetivos terapéuticos en los pacientes con insuficiencia cardiaca4,5. Considerando que la farmacoterapia en la piedra angular del tratamiento de los pacientes HRrEF, esta debe de ser implementada antes de considerar el manejo con dispositivos invasivos. Dentro de los objetivos terapéuticos se consideran la reducción de la mortalidad, la prevención de las hospitalizaciones asociadas a un empeoramiento de la función cardiaca y la mejoría del estado clínico del paciente, de su HRQoL y de su capacidad funcional4,5. Las GPC de la Red Intercolegiada de Guías Clínicas de Escocia (SIGN, por sus siglas en inglés)35 establecen que los objetivos de la terapéutica en pacientes con insuficiencia cardiaca son el de prevenir la progresión de la enfermedad, mejorar los síntomas, la admisión hospitalaria y la mortalidad. Es importante además llevar a cabo un monitoreo de los posibles eventos adversos asociados a la terapéutica farmacológica y del uso de dispositivos con la meta de maximizar los beneficios, disminuyendo los riesgos35. Tanto las GPC de la Sociedad Cardiovascular de Canadá (CCS/CHFS)55 como las GPC del Ministerio de Sanidad Español coinciden en que los principales desenlaces en estos pacientes son los mencionados anteriormente56.
El consenso mexicano sobre insuficiencia cardiaca2 establece claramente que dentro de los objetivos y metas de un programa de insuficiencia cardiaca se debe considerar mejorar la HRQoL de los pacientes, disminuir las hospitalizaciones y el tiempo de estancia en los mismos, disminuir la mortalidad temprana (dentro de los primeros 5 años del diagnóstico de insuficiencia cardiaca), disminuir la carga de la enfermedad (social y económica). También es importante considerar dentro de los objetivos el de crear clínicas altamente especializadas con la formación de recursos adiestrados para el manejo interdisciplinario de estos pacientes y también en la generación de información científica que contribuya al mejor conocimiento de la enfermedad y de su terapéutica19 (Fig. 4 y 5).
Pregunta 13.1: ¿Qué recomendación se debe seguir respecto a la ingesta oral de sodio?
Recomendación: Se recomienda que todo paciente con insuficiencia cardiaca crónica debe moderar el consumo de sodio en la dieta con el propósito de disminuir el desarrollo de congestión pulmonar o sistémica. La restricción absoluta de la ingesta de sodio no se recomienda debido a que puede ser deletérea para la salud de los pacientes. No son recomendables los suplementos ni los sustitutos de sodio en la dieta de los pacientes con insuficiencia cardiaca.
Nivel de evidencia 1, grado de recomendación B (recomendación condicionada a realizar estudios de investigación robustos).
Pregunta 13.2: ¿Qué recomendación se debe seguir respecto a la dieta de los pacientes con insuficiencia cardiaca?
Recomendación: Se recomienda realizar una evaluación nutricional individual para los pacientes con insuficiencia cardiaca. En general, se recomienda adoptar dietas tipo DASH (Dietary Approaches to Stop Hypertension) o mediterránea para mantener un adecuado estado nutricional.
Nivel de evidencia 1, grado de recomendación B (recomendación condicionada a realizar estudios de investigación robustos).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
Tradicionalmente, la restricción de sodio en la dieta en los pacientes con insuficiencia cardiaca ha sido una de las medidas terapéuticas más empleadas en todo el mundo. Esto basado en la teoría que dice que una disminución en el gasto cardiaco lleva a la activación de la renina, lo que da como resultado la retención de sodio. Esta activación del sistema renina-angiotensina-aldosterona promueve la retención hídrica en pacientes con insuficiencia cardiaca. Sin embargo, recientemente se ha señalado que estas recomendaciones no han sido basadas en evidencia científica sólida57. Las GPC de la ADA 20225 actualmente recomienda la reducción del consumo de sodio a < 2300 mg/d como recomendación general de salud cardiovascular. La introducción de una dieta por un profesional de la salud con una restricción de 2 a 3 g/d mejora la clase funcional NYHA y el edema de miembros pélvicos en pacientes ICFEr. En general, estos lineamientos hacen énfasis en el hecho de que no hay evidencia robusta que demuestre beneficios de una restricción de sodio por debajo de esas cifras5, incluso, la restricción de ingesta de sodio se ha asociado a readmisión hospitalaria y aumento en la mortalidad. A esto se agrega que la adherencia a la restricción de sodio es pobre entre los pacientes con insuficiencia cardiaca57.
Una RS publicada por García et al.58 en 2022 tuvo como objetivo evaluar la evidencia sobre eficacia y seguridad de los cambios dietéticos en pacientes con insuficiencia cardiaca. Los autores incluyeron 9 estudios clínicos controlados (ECAs) y 6 estudios observacionales. Los resultados muestran que los autores encontraron una falta de evidencia científica sólida del beneficio de la restricción de sodio y líquidos en la dieta en pacientes con insuficiencia cardiaca crónica. La evidencia se limita a estudios con pocos pacientes con resultados contradictorios entre ellos. Los autores hacen énfasis en la importancia de contar con estudios controlados grandes en esta población de pacientes58. Contrario a lo que se pensaba, algunos estudios han demostrado que una restricción drástica del consumo de sodio puede ser perjudicial (< 2.3 g/d) debido a la posibilidad de hiponatremia e hipocloremia que son causas frecuentes de hospitalización en pacientes con insuficiencia cardiaca58.
Forsyth et al. publicaron una RS en 2022 que tuvo como objetivo evaluar la eficacia de distintas intervenciones dietéticas en pacientes con ICFEp. Los autores incluyeron 25 estudios clínicos, de los cuales 17 fueron incluidos en el metaanálisis. La mayoría de los estudios fueron calificados como con alto riesgo de sesgo. Los resultados de los metaanálisis mostraron que la dieta DASH (Dietary Approaches to Stop Hypertension) evaluada en 2 estudios mejoró discretamente la HRQoL (DME [diferencia de medias estandarizada] 0.59, IC95% –0.07; 1.24) lo que equivale a 11.8 puntos en el score KCCQ, siendo la calidad de la evidencia calificada como muy baja. La restricción de sodio mostró un cambio modesto en la HRQoL en 5 estudios que la evaluaron (DME 0.02, IC95% –0.22; 0.26) equivalente a 0.36 puntos en el score KCCQ y con muy baja calidad de la evidencia. Respecto a la disminución de las cifras de presión arterial, tampoco se encontró una diferencia estadísticamente significativa (DME –1.38, IC95% –11.04; 8.28) con la evidencia evaluada como con muy alto riesgo de sesgo, inconsistencia y heterogeneidad importante59.
Una RS publicada por Burgermaster et al. en 202057 tuvo como objetivo evaluar la adherencia a las dietas con restricción de sodio. Los autores incluyeron 10 ECAs que evaluaron reducción de sodio, adherencia a la dieta pobre en sodio, síntomas y estatus clínico. En esta RS cualitativa, los resultados muestran que en 7 de los 10 ECAs se pudo obtener una reducción de la ingesta de sodio, aunque ninguno pudo lograr una reducción de esta por debajo de 1,500 mg/d (rango de 1,938-4,564 mg/d). En la revisión de la evidencia, los autores consideran que son importantes la educación, las expectativas en los resultados, las normas culturales, el apoyo social, el acceso a la dieta, el hábito y la salud mental de los pacientes57.
Aunque la calidad de la evidencia respecto a la restricción de sodio y líquidos es de muy baja calidad, hay una mayor calidad en la evidencia respecto a que la restricción calórica y de carbohidratos con la suplementación proteica se asocian a una mejoría en la clase funcional, hemodinámica y antropométrica de los pacientes con insuficiencia cardiaca. Una RS publicada por Reis et al. en 201860 evaluó distintas estrategias dietéticas en la prevención secundaria de la insuficiencia cardiaca. Los autores incluyeron 12 estudios que cumplieron con sus criterios de inclusión, los cuales evaluaron dieta DASH, mediterránea, hiperproteica y baja en carbohidratos. Cuatro de los estudios fueron ECAs, cinco cohortes prospectivas y tres estudios transversales. La mayoría de los estudios clasificados como con moderado a alto riesgo de sesgo por falta de descripción de los métodos en los cuidados de la asignación y algunos del cegamiento. La dieta DASH fue evaluada en 2 ECAs y 5 estudios de cohortes. La dieta DASH se asoció a una mejoría en la función cardiaca, capacidad funcional, presión arterial y mortalidad. La dieta mediterránea fue evaluada en 3 estudios transversales y un estudio de cohorte y se asoció a una mejoría en la calidad de vida y de la función cardiaca. Las dietas hiperproteicas y bajas en carbohidratos también se asociaron efectos positivos en la capacidad funcional de estos pacientes, sin embargo, la cantidad y calidad de la evidencia todavía fue aún menor. Los autores concluyeron que se requieren estudios bien diseñados para conocer el impacto real de estas estrategias dietéticas en pacientes con insuficiencia cardiaca60.
De igual forma, Sanches et al.61 publicaron una RS que evaluó la evidencia en la eficacia y seguridad de la dieta DASH y mediterránea, pero en este caso para la prevención primaria de la insuficiencia cardiaca. La calidad de la evidencia nuevamente fue muy baja, los autores incluyeron 14 estudios, de los cuales 5 fueron ECAs, 7 estudios de cohorte y 2 estudios transversales. Los resultados mostraron que la adherencia a una dieta tipo mediterránea o DASH se puede asociar a beneficios para la prevención primaria de la insuficiencia cardiaca. Los resultados de los ECAs mostraron un efecto protector de la dieta mediterránea en la incidencia de insuficiencia cardiaca o en la disminución de la progresión de los parámetros de función cardiaca61. No se encontraron estudios que hayan evaluado la dieta baja en carbohidratos o hiperproteica. Se ha estipulado que el efecto benéfico de estas estrategias dietéticas se puede atribuir al alto contenido en ácido oleico, un ácido graso monoinsaturado (MUFA, por sus siglas en inglés) que puede proporcionar un efecto protector contra el estrés oxidativo. Algunos compuestos fenólicos también han mostrado efectos antioxidantes y antiinflamatorios. En general, el consumo de vegetales y frutas, y proteínas provenientes de pescado ha demostrado tener efectos benéficos en la salud cardiovascular61.
Pregunta 14: ¿Cuál es el papel de la actividad física y de los programas de rehabilitación para los pacientes con insuficiencia cardiaca crónica?
Recomendación: En los pacientes con insuficiencia cardiaca crónica estable se recomienda implementar actividad física individualizada para mejorar los síntomas, aumentar la capacidad funcional y lograr una mayor calidad de vida. La rehabilitación cardiaca debe formar parte del manejo multidisciplinario de todos los programas de insuficiencia cardiaca para mejorar la capacidad funcional y la calidad de vida.
Nivel de evidencia 1+, grado de recomendación A (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
Las GPC de AHA/ACC 2022 recomiendan en los pacientes que puede participar en actividades físicas, que se les organice un programa de ejercicio o actividad física regular para mejorar el estado funcional, la capacidad física y la HRQoL. De la misma manera, es recomendable incluir a los pacientes en un programa de rehabilitación cardiaca con los mismos objetivos. Diversos estudios han demostrado que el ejercicio físico ofrece numerosos beneficios como la reducción del riesgo de hospitalización y de mortalidad cardiovascular. Los programas de rehabilitación cardiaca pueden incluir evaluación médica, recomendaciones nutricionales, soporte psicosocial y entrenamiento físico.
Se han hecho grandes esfuerzos por promover la actividad física debido a la gran cantidad de evidencia que la asocia con una mejoría en la salud cardiovascular. Aune et al. revisaron 29 estudios prospectivo que evaluaron distintas intervenciones y su asociación al desarrollo de insuficiencia cardiaca. Los resultados de los metaanálisis mostraron un menor riesgo de desarrollo de insuficiencia cardiaca para actividad física (RR [riesgo relativo] 0.77, IC95% 0.70; 0.85), para actividad física en tiempo libre (RR 0.74, IC95% 0.68; 0.81), actividad rigurosa (RR 0.66, IC95% 0.59; 0.74), ciclismo y caminata (RR 0.81, IC95% 0.69; 0.94) y entrenamiento aeróbico (RR 0.31, IC95% 0.19; 0.49). Estos resultados confirman el efecto benéfico que la actividad física ha demostrado tener en la prevención de la insuficiencia cardiaca, como ya se ha demostrado que la tiene en otros padecimientos cardiovasculares como la enfermedad coronaria y la enfermedad vascular cerebral62.
Una RS publicada por Palevičiūtė et al.63 en 2023 tuvo como objetivo evaluar el impacto del entrenamiento físico y la fisioterapia en la función cardiaca y pulmonar en pacientes con insuficiencia cardiaca ICFEp. Los autores incluyeron 18 estudios clínicos con 418 participantes evaluando 4 a 52 semanas de entrenamiento. De estos estudios 14 fueron ECAs y 4 estudios observacionales. En general, la calidad de los estudios fue calificada como moderada, buena y muy buena. Los resultados mostraron que 9 de 14 ECAs reportaron cambios significativos en los distintos parámetros ecocardiográficos, tanto los que evalúan la función del ventrículo izquierdo como del ventrículo derecho, evaluados en los grupos en entrenamiento físico. Solo un estudio pequeño evaluó la función cardiaca por hemodinamia y ninguno por RMN cardiaca. En general, los resultados mostraron heterogeneidad, siendo que la mayoría de ellos mostraron resultados benéficos en los pacientes63.
Otra RS publicada por do Nascimiento et al. en 202264 evaluó el impacto de la actividad física en las mediciones de NT-proBNP, PCR, factor de necrosis tumoral alfa y algunas interleucinas (IL); en pacientes con insuficiencia cardiaca. Los autores incluyeron 38 estudios clínicos (2,652 participantes). Los resultados del metaanálisis mostraron que la actividad física se asoció a una disminución del NT-proBNP (p = 0.01), PCR (p = 0.00001), factor de necrosis tumoral alfa (p = 0.03) y de IL-6 (p = 0.01). Los autores concluyen que la actividad física se asocia a una disminución de los valores de importantes biomarcadores en insuficiencia cardiaca e inflamatorios64.
Otra RS reciente publicada por Amirova et al. en 2021 tuvo como objetivo evaluar la eficacia de la actividad física en pacientes con insuficiencia cardiaca y de algunas intervenciones para mejorar al apego a las distintas rutinas de terapia física. Los resultados mostraron que la combinación de una estrategia de modificación conductual y ejercicio físico cuando son integrados por un fisioterapeuta, en un formato grupal, lograron los mejores resultados65.
Al igual que la actividad física, los programas de rehabilitación cardiaca también han demostrado mejorar síntomas y HRQoL de los pacientes con insuficiencia cardiaca. Harwood et al. en 202166 publicaron una RS que evaluó la calidad del reporte de los programas estructurados de rehabilitación física, incluyeron 143 estudios y los resultados mostraron que en general, la mayoría de los estudios sobre rehabilitación física no llevan a cabo un adecuado reporte de las características de los distintos programas de rehabilitación para poder ser evaluados de una manera sistematizada66.
Una RS publicada por Taylor et al.67 evaluó la rehabilitación cardiaca basada en terapia física en pacientes con insuficiencia cardiaca. Los autores incluyeron 44 estudios con 5,783 participantes y los resultados del metaanálisis mostraron que, aunque los programas de rehabilitación no disminuyeron el riesgo de mortalidad (RR 0.89, IC95%: 0.66; 1.21), si reduce el riesgo de hospitalización (RR 0.70, IC95%: 0.60; 0.83) y mejora las calificaciones de cuestionarios específicos (MLHF) (DM [diferencia de medias] –7.1, IC95%: –10.5; –3.7)67.
Pregunta 15: ¿Cuál es el papel de las estrategias educativas y del apoyo psicológico para los pacientes con insuficiencia cardiaca crónica?
Recomendación: Se recomienda que los pacientes con insuficiencia cardiaca crónica, sus familiares y cuidadores sean capacitados sobre aspectos básicos de la insuficiencia cardiaca, el manejo de medicamentos y el automonitoreo, con el propósito de mejorar el apego y la persistencia al tratamiento, y reconocer tempranamente datos de alarma que requieran atención urgente. Se recomienda que los pacientes con insuficiencia cardiaca crónica sean evaluados por psicología con el propósito de brindar apoyo y detectar oportunamente enfermedades que requieran tratamiento específico.
Nivel de evidencia 1+, grado de recomendación A (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
La insuficiencia cardiaca es un síndrome muy complejo que impone una carga importante a los pacientes y sus familias. Síntomas y signos como la disnea, fatiga, edema y la disminución de la capacidad funcional y cognitiva afectan de manera importante a los pacientes. La pobre adherencia al tratamiento farmacológico a los cambios en el estilo de vida, dieta y actividad física, son una parte del problema por lo que los pacientes con insuficiencia cardiaca se descompensan y acuden a los servicios médicos para hospitalización68. Una de las principales causas por las que el paciente y sus cuidadores no pueden cumplir con un buen apego a toda la terapéutica es por una capacidad baja para ejercer su auto cuidado; entendido como el proceso de decisión natural en la cual el paciente y cuidadores están comprometidos en seguir su tratamiento. Un pobre nivel de conocimiento en salud, un déficit cognitivo, depresión, las comorbilidades y una baja funcionalidad afectan directamente esta capacidad de auto cuidado68. Un buen cúmulo de evidencia han demostrado que el involucro del paciente en su enfermedad a través de educación y apoyo, contribuyen a mejorar los resultados en salud de distintos padecimientos crónicos. Una RS publicada por Pereira et al.68 tuvo como objetivo evaluar la eficiencia de distintos programas educativos en pacientes con insuficiencia cardiaca. Los estudios incluyeron el grado de apego al tratamiento y de auto cuidado en los pacientes que recibieron estrategias educacionales. Los autores incluyeron 19 ECAs con un total de 1,841 participantes. Los resultados de los metaanálisis mostraron que el grupo que recibió la estrategia educativa mostró un mejor nivel de autocuidado (p = 0.0091), sin embargo, no se pudo demostrar una diferencia respecto al nivel de adherencia al tratamiento (p = 0.7604) aunque los resultados mostraron una alta heterogeneidad68.
Otra RS publicada por Cañon-Montañez et al. en 202169 tuvo como objetivo estimar el efecto de las intervenciones educativas en la disminución de readmisiones y tiempo de estancia hospitalaria en pacientes con insuficiencia cardiaca. Los autores incluyeron 45 ECAs y el metaanálisis demostró una disminución en las admisiones hospitalarias del 30% (RR 0.70, IC95%: 0.58; 0.84) y a 12 meses de 33% (RR 0.67; IC95%: 0.58; 0.76) a favor del grupo que recibió estrategia educativa. También se observó una disminución en promedio de 2 días en este grupo (DM –1.98; –3.27; –0.69). Estos resultados son consistentes con otros análisis publicados previamente. En general, las estrategias educativas desarrolladas y conducidas por personal de enfermería han mostrado ser las más efectivas, lo que resalta la importancia de este grupo de profesionales de la salud en su papel de educadoras para los pacientes y sus cuidadores69. Una RS publicada por Zhao et al. en 2020 evaluó la eficacia de las intervenciones de auto cuidado en pacientes con insuficiencia cardiaca para mejorar la HRQoL y disminuir las hospitalizaciones. Los autores incluyeron 15 ECAs con 2,630 participantes que fueron calificados en general como con moderado y bajo riesgo de sesgo, y los resultados de los metaanálisis demostraron que las intervenciones de auto cuidado mejoraron de manera significativa el conocimiento en la enfermedad (DM 0.61; IC95%: 0.27; 0.95), HRQoL (DM 0.20; IC95%: 0.02; 0.38) y hospitalizaciones (OR 0.40; IC95%: 0.29; 0.55)70.
Pregunta 16: ¿Cuál es la recomendación para el empleo de los inhibidores de la enzima convertidora de la angiotensina (IECA) en los pacientes con insuficiencia cardiaca crónica?
Recomendación:
– En los pacientes con ICFEr está recomendado el uso de IECA para disminuir el riesgo de muerte de causa cardiovascular y las hospitalizaciones por insuficiencia cardiaca.
– En los pacientes con ICFEr con alto riesgo de muerte súbita cardiaca no deben considerarse los IECA como la primera opción farmacológica para el control de la sobreactividad neurohumoral.
– En los pacientes con ICFEp no se recomienda el empleo de IECA debido a la falta de eficacia demostrada en los ensayos clínicos contemporáneos.
– En los pacientes con insuficiencia cardiaca crónica con fracción de expulsión ligeramente reducida, el empleo de IECA queda a criterio del médico tratante debido a la escasa evidencia científica en este grupo de pacientes.
– En los pacientes con insuficiencia cardiaca crónica con fracción de expulsión mejorada que se encuentren bajo tratamiento con IECA es recomendable continuar con este tratamiento en forma indefinida a pesar de la mejoría de la FEVI.
Nivel de evidencia 1+, grado de recomendación A (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
Las GPC de la AHA/ACC 20224 recomienda como primera línea de tratamiento la inhibición del sistema renina-angiotensina (SRA). La disfunción en el SRA es uno de los procesos fisiopatológicos más estudiados en enfermedad cardiovascular. Es además un sistema vital del cuerpo humano que se encarga de mantener la concentración plasmática de sodio, la presión arterial y el volumen extracelular71. El SRA resulta de la modificación estructural de diferentes proteínas. Iniciando por la acción de la renina, enzima que actúa sobre el angiotensinógeno, transformándolo en angiotensina I (Ang I). La que a su vez es transformada por la llamada enzima convertidora de angiotensina (ECA) en angiotensina II (Ang II). La ECA es una kininasa que modifica a la bradiquinina (BQ), activadora en el endotelio de la producción de óxido nítrico (NO) y de prostaciclina (PGI2). La angiotensina II, a su vez, tiene 2 receptores, AT1 y AT2, que tienen funciones antagónicas. La ECA es expresada en la membrana de las células endoteliales parenquimatosas e inflamatorias, presentando 3 isoformas: 1) ECA somática, expresada especialmente en el endotelio de arterias pulmonares, células endoteliales, células musculares lisas vasculares (CMLV), linfocitos T y adipocitos; 2) ECA plasmática o soluble; 3) ECA germinal o testicular71,72. La primera produce Ang II y está presente en las válvulas cardíacas, arterias coronarias, aorta, endotelio pulmonar, endocardio y epicardio. La activación de la ECA tiene fuerte dependencia de la función endotelial, cuyas acciones principales se vinculan con la regulación del tono de los vasos, y con efectos antiinflamatorios, antitrombóticos y anti proliferativos, etc., lo que contribuye a la regulación de la homeostasis circulatoria. La Ang II y la ECA desempeñan un papel fundamental en el remodelamiento vascular en respuesta a un daño en la insuficiencia cardíaca y en otras enfermedades cardiovasculares71,72. El SRA también tiene una importante actuación local, ya que la ECA se expresa tanto en los miocitos cardíacos como en los fibroblastos, al igual que la renina que facilita la síntesis local de angiotensina (ANG) II. La síntesis de ANG II tiene lugar en el espacio intersticial y en el intracelular. La síntesis extracelular de ANG II depende generalmente de la pro-renina y de la ECA. En miocitos cardíacos, la síntesis intracelular de ANG II puede ocurrir en el citoplasma, mediada por renina y quimasa, o en vesículas secretoras. La ANG II sintetizada en las vesículas secretoras puede producirse o relocalizarse intracelularmente. Los miocitos cardíacos y los fibroblastos aumentan en respuesta a hiperglucemia mediante la activación del SRA local. La respuesta de los miocitos cardíacos resulta en un fuerte aumento de la ANG II intracelular, los fibroblastos también actúan en la ANG II intracelular como extracelular. La síntesis de ANG II intracelular en los miocitos cardíacos es dependiente tanto de la renina como de la quimasa, mientras que en los fibroblastos es catalizada por la renina y por la ECA. La ANG II intracelular causa hipertrofia celular e incremento de la expresión génica en miocitos cardíacos y provoca en los fibroblastos: síntesis de colágeno y expresión del factor de crecimiento transformante-beta (TGF-beta, por sus siglas en inglés)71,72. El SRA es influenciado por una gran cantidad de hormonas, enzimas, vías complejas de señalización celular y mecanismos de contraregulación, dentro de los cuales se encuentran el estrógeno, tiroides, cortisol, principalmente71.
Los inhibidores de la enzima convertidora de angiotensina (iECA) son una clase terapéutica que inhibe la actividad de la ECA que se encarga de convertir la angiotensina-I (que carece de función fisiológica) en angiotensina-II, y aumenta los niveles de bradicinina, que tiene efectos vasodilatadores. Estos efectos farmacodinámicos se traducen en una reducción de la presión arterial y venosa, y en el riñón, aumenta la natriuresis y la diuresis, lo que disminuye el volumen circulante y el gasto cardiaco; pero con un efecto limitado en la frecuencia cardiaca y en los reflejos baroreceptores73.
La evidencia científica sobre la eficacia y seguridad de los iECA en pacientes con insuficiencia cardiaca es muy extensa, sin embargo, es importante recalcar que no es el caso de los pacientes con ICFEp. Las GPC ESC 2021 hace hincapié en que ninguna clase terapéutica ha mostrado de manera consistente la reducción del riesgo de mortalidad y morbilidad en este grupo de pacientes, aunque evidencia reciente ha mostrado resultados promisorios en algunos fenotipos de pacientes específicos5. Baral et al. en 202274 publicaron una RS que tuvo como objetivo evaluar la eficacia y seguridad de todas las clases terapéuticas en pacientes con ICFEp. Los autores incluyeron 14 ECAs con 6,370 participantes de 10 clases terapéuticas distintas. La evidencia fue escasa y los autores destacan que ninguna clase terapéutica evaluado demostró mejorar el VO2 máximo con excepción de ivabradina y pocos mostraron disminución del riesgo de mortalidad por cualquier causa y hospitalizaciones por insuficiencia cardiaca74.
Una RS publicada por Fu et al. en 201275 tuvo como objetivo evaluar la eficacia de los iECA en pacientes con ICFEp. Los autores incluyeron 7 ECAs que evaluaron distintos iECA como primera línea de tratamiento. Un total de 2,554 pacientes fueron incluidos (edad promedio 75 años, 58% mujeres) y seguidos en promedio 20 meses. Los resultados del metaanálisis mostraron que los iECA se asociaron a una reducción significativa del riesgo de muerte por cualquier causa en un 48% (razón de momios [RM] 0.52; IC95%: 0.41; 0.64), y las rehospitalizaciones en un subgrupo mayor a 75 años. Sin embargo, no hubo diferencias en la mortalidad por progresión de la enfermedad (RM 0.88, IC95% 0.66; 1.17), rehospitalizaciones por insuficiencia cardiaca (RM 0.81, IC95% 0.63; 1.05) o readmisiones por cualquier causa (RM 0.88, IC95% 0.68; 1.14)75.
Respecto a los pacientes con ICFEr, los iECA son parte de la primera línea de tratamiento. Las GPC de la AHA/ACC 2022 recomiendan el uso de iECA en pacientes con ICFEr, clase NYHA II-III, con síntomas crónicos ya que se ha demostrado un beneficio para reducir la morbi mortalidad cuando el uso de inhibidor de la neprilisina y del receptor de angiotensina (iNRA) no es factible. Es importante evitar el uso de iECA cuando hay antecedentes de angioedema. Es aconsejable iniciar a dosis bajas e ir subiendo la dosis conforme la respuesta del paciente al tratamiento, es importante evitar la interrupción abrupta del manejo con iECA en estos pacientes4,5 (Tabla 4).
Tabla 4 Dosis basadas en la evidencia de fármacos modificadores de la enfermedad en ensayos aleatorizados de registro en pacientes con insuficiencia cardiaca con fracción de eyección reducida
| Fármaco | Dosis inicial | Dosis objetivo |
|---|---|---|
| Captopril | 6.25 mg tres veces al día | 50 mg tres veces al día |
| Enalapril | 2.5 mg dos veces al día | 10-20 mg dos veces al día |
| Lisinopril | 2.5-5 mg al día | 20-35 mg al día |
| Ramipril | 2.5 mg dos veces al día | 5 mg dos veces al día |
| Trandolapril | 0.5 mg al día | 4 mg al dia |
Modificada de: McDonagh TA, Metra M, Adamo M, Gardner RS, Baumbach A, Böhm M, et al. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2021;42:3599-726.
Una RS publicada por Bœuf-Gibot et al. en 202076 tuvo como objetivo evaluar la eficacia y seguridad de esta clase terapéutica en pacientes ICFEr. Los autores incluyeron 11 ECAs con 13,882 participantes y calificaron la evidencia como de moderada calidad. Los resultados de los metaanálisis mostraron que los iECA se asociaron a una disminución en la mortalidad a los 6 meses del 24% (cociente de riesgos [CR] 0.76, IC95%: 0.66; 0.87), a los 12 meses en 9% (CR 0.91, IC95%: 0.84; 0.98) y en la mortalidad total de 15% (CR 0.85; IC95% 0.80; 0.90). Respecto a la seguridad, hubo una mayor frecuencia de mareo, hipotensión, incremento de la creatinina, hiperkalemia en el grupo con iECA y no hubo diferencias en rash cutáneo, angioedema o cáncer76.
Una RS publicada por Migliavaca et al.77 tuvo como objetivo evaluar los iECA a dosis baja y alta en pacientes con insuficiencia cardiaca (ICFEr). Los autores incluyeron 8 ECAs (5,829 participantes) y los metaanálisis no mostraron diferencias estadísticas respecto a la mortalidad de cualquier causa (RR 0.95; IC95% 0.88; 1.02), mortalidad cardiovascular (RR 0.93, IC95%: 0.85; 1.01), hospitalizaciones de cualquier causa (RR 0.95; IC95%: 0.82; 1.10) y hospitalizaciones por causa cardiovascular (RR 0.98; IC95% 0.83; 1.17). Las dosis altas de iECA se asociaron a una capacidad funcional mayor que en el otro grupo (DME 0.38; IC95% 0.20; 0.55)77.
Pregunta 17.1: ¿Cuál es la recomendación para el empleo de sacubitrilo/valsartán en los pacientes con ICFEr?
Recomendación:
– Siempre que sea posible, se debe recomendar el uso de sacubitrilo/valsartán como fármaco de primera línea para la reducción de las hospitalizaciones por insuficiencia cardiaca y la mortalidad por causa cardiovascular.
– En pacientes después de un internamiento por empeoramiento de la insuficiencia cardiaca, el uso de sacubitrilo/valsartán debe ser considerado como la opción preferente de modulación del SRA debido a su superioridad frente a los IECA.
– En pacientes con alto riesgo de muerte súbita cardiaca, el sacubitrilo/valsartán debe ser considerado como la opción preferente para la modulación del SRA.
– El sacubitrilo/valsartán no debe recomendarse en pacientes con una tasa de filtración glomerular estimada (TFGe) < 15 ml/min/m2.
– El sacubitrilo/valsartán no debe recomendarse en pacientes con potasio sérico > 6 mEq/l.
– El sacubitrilo/valsartán no debe recomendarse durante el embarazo y la lactancia.
– El sacubitrilo/valsartán no debe utilizarse en conjunto con IECA.
– El sacubitrilo/valsartán no debe emplearse en pacientes con antecedente de angioedema.
Nivel de evidencia 1+, grado de recomendación A (recomendación fuerte).
Pregunta 17.2: ¿Cuál es la recomendación para el empleo de sacubitrilo/valsartán en pacientes con insuficiencia cardiaca con FEVI ligeramente reducida o con FEVI preservada?
Recomendación: En pacientes con FEVI por debajo de lo normal resulta razonable emplear sacubitrilo/valsartán para disminuir el riesgo de eventos de empeoramiento, muerte de causa cardiovascular o progresión de daño renal.
Nivel de evidencia 2+, grado de recomendación A (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
El sacubitrilo/valsartán fue el primer medicamento aprobado de la clase de los iNRA, y consiste en una combinación de fármacos en la cual se inhibe la neprilisina y el receptor de la angiotensina mediante la inhibición simultánea de la neprilisina (endopeptidasa neutra; NEP) a través de LBQ657, metabolito activo de sacubitrilo y mediante el antagonismo del receptor de la angiotensina II a través del valsartán. El resultado de esto es el aumento de los péptidos, normalmente metabolizados por la neprilisina, como los péptidos natriuréticos, lo que provoca vasodilatación, natriuresis y diuresis, aumento de la tasa de filtración glomerular, inhibición de la liberación de renina y de aldosterona y disminución de la actividad simpática en el organismo4.
Las GPC de la AHA/ACC recomiendan el uso de los iNRA como tratamiento de primera línea, recomienda que en pacientes con ICFEr con clase funcional NYHA II – III que toleran adecuadamente un iECA o bloqueador del receptor de angiotensina (BRA), se deberían de cambiar al uso de iNRA debido al beneficio en morbi-mortalidad en estos pacientes. Se puede considerar también el uso de iNRA en pacientes "vírgenes" a tratamiento farmacológico para simplificar el tratamiento4. El consenso mexicano sobre insuficiencia cardiaca19 recomienda el uso de sacubitrilo-valsartán como la primera opción como fármaco que modifica la función del SRA en pacientes con ICFEr por su novedoso mecanismo de acción y los beneficios demostrados en este grupo de pacientes2.
Una RS publicada por Nie et al.78 tuvo como objetivo evaluar la eficacia y seguridad del sacubitrilo-valsartán en pacientes con ICFEp y HFmEF. Los autores incluyeron 6 estudios con un total de 5,503 participantes, que compararon sacubitrilo-valsartán contra iECA y BRA y los resultados de los metaanálisis mostraron que el sacubitrilo-valsartán se asocia con una disminución de la tasa de hospitalización (CR 0.84; IC95%: 0.77; 0.91) y una mejoría de la clase funcional NYHA (CR 1.25; IC95% 1.10; 1.43) en pacientes ICFEp y HFmEF. Ni la mortalidad por cualquier causa ni la mortalidad cardiovascular mostró diferencias significativas entre las distintas clases terapéuticas78. Otra RS más reciente publicada por Yu et al. en 202279 con el mismo objetivo, los autores incluyeron 3 ECAs con la participación de 7,663 participantes. Los resultados del metaanálisis mostraron que sacubitrilo-valsartán se asoció a una reducción del riesgo de hospitalización por exacerbación de la insuficiencia cardiaca del 22% (RM 0.78; 0.70; 0.88) y de la progresión del daño renal (RM 0.79), sin embargo, no hubo diferencias en la reducción de la mortalidad por cualquier causa (RM 0.99, IC95% 0.84; 1.15) y de mortalidad cardiovascular (RM 0.95; IC95%: 0.78; 1.15). Acerca de la incidencia de eventos adversos, sacubitrilo-valsartán se asoció a un riesgo incrementado de hipotensión sintomática (RR 1.44, IC95%: 1.25; 1.66) y angioedema (RR 2.66, IC95%: 1.04; 6.79)79.
Respecto a los pacientes ICFEr, sacubitrilo-valsartán ha demostrado brindar diferentes beneficios clínicos. Una RS publicada por Nielsen et al.80 en 2020 tuvo como objetivo evaluar la eficacia y seguridad de sacubitrilo-valsartán en pacientes ICFEr. Los autores incluyeron 4 ECAs con 10.794 participantes en un seguimiento en promedio de 22.8 meses. Los resultados de los metaanálisis mostraron una disminución del riesgo de mortalidad por cualquier causa (RR 0.86; IC95%: 0.79; 0.94) en comparación a los grupos con terapia estándar. Respecto a las hospitalizaciones, sacubitrilo-valsartán mostró un menor riesgo durante el seguimiento (RR 0.79; IC95%: 0.72; 0.87). No hubo diferencias en la incidencia de eventos adversos no serios entre ambos grupos (RR 0.91; IC95%: 0.74; 1.11) ni en eventos adversos serios (RR 0.99; IC95%: 0.94; 1.04). Una RS publicada por Kim et al. en 202181 tuvo el objetivo de evaluar la seguridad de sacubitrilo-valsartán. Los autores incluyeron 4 ECAs en pacientes con ICFEr, los metaanálisis mostraron que no hubo diferencias en la incidencia de eventos adversos entre el grupo de sacubitrilo-valsartán y los comparadores (RM 1.23; IC95% 0.98; 1.56). Sin embargo, si se encontraron diferencias para hipotensión (RM 1.57; IC95% 1.42; 1.73), disfunción renal (RM 0.78; IC95%: 0.69; 0.88). Rahhal et al.82 publicaron una RS evaluaron la efectividad de sacubitrilo-valsartán con datos provenientes de estudios de "vida real". Los autores incluyeron 9 estudios observacionales comparando sacubitrilo-valsartán vs. iECA y BRA en pacientes ICFEr en donde se incorporaron más de 3,200 pacientes. Los resultados del metaanálisis mostraron una disminución de la mortalidad por cualquier causa (CR 0.70; IC95%: 0.53; 0.93) y de hospitalización (CR 0.62; IC95%: 0.48; 0.80)83.
Una RS publicada por Park et al.84 en 2023 tuvo como objetivo evaluar la eficacia y seguridad, a través de un "metaanálisis en red" de distintas alternativas farmacológicas modificadoras del SRA en pacientes ICFEr. Los autores incluyeron 28 ECAs que incluyeron 47,407 pacientes. Los resultados muestran que los iRNA (inhibidores de los receptores de angiotensina/neprilisina) se asociaron con una disminución del riesgo de muerte por cualquier causa del 19% (RR 0.81; IC95%: 0.68; 0.96), muerte cardiaca (RR 0.79; IC95%: 0.64; 0.99) y de eventos adversos cardiacos mayores (MACE, por sus siglas en inglés), pero también con un mayor riesgo de hipotensión (RR 1.46; IC95%: 1.02; 2.10) en comparación a los BRA. En comparación a los iECA, los iRNA se asociaron a una disminución de eventos adversos cardiacos mayores (RR 0.85%; IC95%: 0.74; 0.97) pero también con un mayor riesgo de hipotensión (RR 1.69; IC95%: 1.27; 2.24). Los resultados del "metaanálisis en red" mostraron que los iRNA en comparación a placebo se asociaron a una disminución de la mortalidad del 25% (RR 0.63; IC95%: 0.63; 0.89), de muerte cardiaca del 29% (RR 0.71; IC95%: 0.57; 0.89), de MACE de 29% (RR 0.63; IC95%: 0.60; 0.84); y de hospitalización por insuficiencia cardiaca del 40% (RR 0.60; IC95%: 0.48; 0.75)84.
Song et al.85 reportaron que la combinación de sacubitrilo-valsartán mejoró la HRQoL, mediante escalas validadas internacionalmente como KCCQ y MLHFQ, en comparación a los iECA y BRA de manera significativa (DME 1.26; IC95% 0.14; 2.37) en pacientes con ICFEr, sin embargo, esta diferencia no se observó en pacientes con ICFEp (DME 0.37; IC95%: –0.35; 1.09)85.
Pregunta 18.1: ¿Cuál es la recomendación para el uso de BRA en pacientes con insuficiencia cardiaca con FEVI reducida?
Recomendación:
– El uso de BRA para disminuir las hospitalizaciones y las muertes por causa cardiovascular se debe restringir a aquellos pacientes intolerantes a los IECA o que por alguna razón no pueden recibir sacubitrilo/valsartán.
– Los BRA no deben recomendarse en pacientes con TFGe < 15 ml/min/m2.
– Los BRA no deben recomendarse en pacientes con K+ sérico > 6 mEq/l.
– Los BRA no deben recomendarse durante el embarazo ni la lactancia.
– Los BRA no deben utilizarse en conjunto con IECA.
Nivel de evidencia 1+, grado de recomendación A (recomendación fuerte).
Pregunta 18.2: ¿Cuál es la recomendación para el uso de BRA en pacientes con insuficiencia cardiaca con FEVI ligeramente reducida o preservada?
Recomendación: Los BRA pueden considerarse como parte del tratamiento antihipertensivo en pacientes con insuficiencia cardiaca con FEVI > 40%.
Nivel de evidencia 2+, grado de recomendación A (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
Las GPC de la AHA/ACC 2022 recomiendan en pacientes con ICFEr y clase funcional NYHA II a III el uso de un modificador del SRA. En pacientes con síntomas previos o actuales de HGrEF que son intolerantes a un iECA por tos o angioedema y cuando el uso de un iNRA no es factible, estos lineamientos sugieren el uso de un BRA es recomendable para disminuir la morbi mortalidad. Los BRA han demostrado, de acuerdo con las GPC ADA/ACC que disminuyen la mortalidad y las hospitalizaciones por insuficiencia cardiaca en pacientes ICFEr y producen cambios a largo plazo que se traducen en beneficios clínicos. Debido a que no inhiben la enzima kinasa tienen un menor riesgo de producir tos y angioedema, sin embargo, no se ve la vasodilatación observada con los iECA. Es recomendable que los BRA se inicien a dosis bajas y se vaya incrementando la posología de manera progresiva hasta llegar a la dosis que ha demostrado beneficios cardiovasculares. Es importante vigilar de cerca a los pacientes en los que se usan BRA y que tienen hipotensión, insuficiencia renal, hiperkalemia (> 5.0 mEq/L). Los pacientes que tienen ICFEr estable y que toleran adecuadamente un iECA o BRA, deberían ser cambiados a iNRA debido a los beneficios adicionales en hospitalizaciones y mortalidad que estos últimos ofrecen.
Una RS publicada por Meune et al.86 evaluó la eficacia y la seguridad de los BRA en pacientes ICFEp e identificaron 4 ECAs y los resultados de los metaanálisis mostraron que el tratamiento con un iECA o un BRA se asoció a una disminución a una menor tasas de hospitalización por insuficiencia cardiaca (RR 0.90; IC95%: 0.81; 0.99) aunque falló en demostrar una disminución en la mortalidad cardiovascular (RR 1.01; IC95%: 0.90; 1.13)86.
Una RS publicada por Park et al.84 en 2023 tuvo como objetivo evaluar la eficacia y seguridad, a través de un "metaanálisis en red" de distintas alternativas farmacológicas modificadoras del SRA en pacientes ICFEr. Los autores incluyeron 28 ECAs que incluyeron 47,407 pacientes. Los resultados muestran que los iRNA se asociaron con una disminución del riesgo de muerte por cualquier causa del 19% (RR 0.81; IC95%: 0.68; 0.96), muerte cardiaca (RR 0.79; IC95%: 0.64; 0.99) y de eventos adversos cardiacos mayores (MACE, por sus siglas en inglés), pero también con un mayor riesgo de hipotensión (RR 1.46; IC95%: 1.02; 2.10) en comparación a los BRA. En comparación a los iECA, los iRNA se asociaron a una disminución de eventos adversos cardiacos mayores (RR 0.85%; IC95%: 0.74; 0.97) pero también con un mayor riesgo de hipotensión (RR 1.69; IC95%: 1.27; 2.24). Los resultados mostraron que los BRA no se asociaron con una disminución de la mortalidad por cualquier causa en comparación a placebo (RR 0.92; IC95%: 0.84; 1.01), ni en muerte cardiaca (RR 0.90; IC95%: 0.79; 1.01), infarto agudo al miocardio (IAM) (RR 0.99; IC95%: 0.74; 1.31), pero si hubo una disminución del riesgo de MACE (RR 0.85; IC95%: 0.77; 0.94) y de hospitalización por insuficiencia cardiaca (RR 0.71; IC95%: 0.61; 0.81). Respecto a los desenlaces de seguridad, los BRA se asociaron a hipotensión (RR 2.04; IC95%: 1.43; 2.92), hiperkalemia (RR 2.13; IC95%: 2.12; 4.03) y angioedema (RR 1.18; IC95%: 0.36; 3.89)84.
Una RS publicada por Burnett et al. en 201787 tuvo como objetivo evaluar toda la evidencia científica disponible sobre diversas alternativas modificadoras del SRA a través de un "metaanálisis en red". Los autores incluyeron 57 ECAs en donde se evaluaron diversas combinaciones farmacológicas y también fármacos como monoterapia. Los resultados del "metaanálisis en red" fallaron en demostrar un beneficio de los BRA en la reducción de la mortalidad de cualquier causa (RR 0.88, IC95%: 0.61; 1.26), incluso cuando se combinaron con un iACE (RR 0.83; IC95%: 0.51; 1.24). Cuando el BRA se asocia a un fármaco beta bloqueador (BB), si se observó una disminución en la mortalidad (RR 0.47; IC95%: 0.23; 0.86). Con la triple terapia de un iECA + BRA + BB se observó una disminución de la mortalidad en 48% (RR 0.52; IC95%: 0.31; 0.80). Sin embargo, cuando se evaluó la combinación de un iRNA + BB + antagonista del receptor mineralocorticoide (ARM) se observó una disminución de la mortalidad de 63% (RR 0.37; IC95%: 0.19; 0.65). Este estudio tiene la limitante de que los resultados no provienen de estudios "cara a cara" en donde se haya hecho una comparación directa87.
Pregunta 19.1: ¿Cuál es la recomendación para el uso de BB en la insuficiencia cardiaca con FEVI reducida?
Recomendación:
– Se debe utilizar un BB (bisoprolol, carvedilol, succinato de metoprolol o nebivolol) en todo paciente para disminuir el riesgo de internamientos por insuficiencia cardiaca, muerte de causa cardiovascular y muerte súbita cardiaca.
Nivel de evidencia 1+, grado de recomendación A (recomendación fuerte).
Pregunta 19.2: ¿Cuál es la recomendación para el uso de BB en la insuficiencia cardiaca con FEVI ligeramente disminuida?
Recomendación: Es razonable utilizar BB (bisoprolol, carvedilol, succinato de metoprolol o nebivolol) para disminuir el riesgo de internamientos o de muerte de causa cardiovascular.
Nivel de evidencia 2+, grado de recomendación B (recomendación fuerte).
Pregunta 19.3: ¿Cuál es la recomendación para el uso de BB en la insuficiencia cardiaca con FEVI > 50%?
Recomendación:
– No está recomendado el uso de BB para disminuir el riesgo de eventos cardiovasculares mayores, como hospitalización por insuficiencia cardiaca o muerte de causa cardiovascular.
– Se pueden emplear BB para el control de la frecuencia cardiaca en pacientes con fibrilación auricular.
Nivel de evidencia 1+, grado de recomendación A (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
Ha sido ampliamente demostrado que, en el escenario de la insuficiencia cardiaca crónica, el SRA y el sistema simpático del sistema nervioso neurovegetativo se encuentran sobre activados. Hay un incremento de los niveles de epinefrina y norepinefrina y un incremento de la liberación sináptica de los mismos y de ahí a la circulación sistémica. Este aumento en la liberación de catecolaminas conduce a una estimulación persistente y sostenida de Beta receptores miocárdicos, con la repercusión que esto genera en un corazón que está progresando a la disfunción88. En pacientes ICFEr la disfunción en los beta receptores cardiacos se caracterizan por una reducción de la densidad de los receptores ß1 y un desacoplamiento de los receptores ß1 y ß2 de las proteínas G de membrana. Esto da como resultado una disminución de la reserva inotrópica cardiaca88. Las consecuencias clínicas de estos procesos fisiopatológicos consisten en la reducción de la función sistólica y la FEVI, así como el proceso de remodelamiento de las paredes ventriculares y trastornos del ritmo cardiaco88.
El tratamiento con medicamentos beta bloqueadores en insuficiencia cardiaca equivalen a un antagonismo directo de los efectos deletéreos cardiacos de las catecolaminas, modifican la regulación en la función de los receptores ß cardiacos, suprimen los niveles de otros sistemas neuro hormonales y mejoran el flujo coronario88.
Desde la década de los 90s, los beta bloqueadores se empezaron a probar en estudios aleatorios multicéntricos lo que detonó una gran cantidad de estudios de investigación al respecto. Las GPC ADA/ACC 2022 recomiendan el uso de cualquiera de los 3 beta bloqueadores que han demostrado reducir la mortalidad y las hospitalizaciones en pacientes ICFEr (bisoprolol, carvediol y metropolol de liberación prolongada) además de ser una terapia costoefectiva. Adicionalmente, los beta bloqueadores mejoran los síntomas y el estado funcional de los pacientes ICFEr. Estos lineamientos recomiendan que incluso en pacientes que no mejoran claramente sus síntomas, no es recomendable suspender el uso de beta bloqueadores por el riesgo de ocurrencia de eventos cardiovasculares4. Las GPC ESC 20215 sugieren iniciar el tratamiento con beta bloqueadores de manera simultánea a los iECA, en pacientes estables, a una dosis baja y progresivamente subir a la dosis máxima tolerada. Estos pueden iniciarse en pacientes hospitalizados una vez que se encuentren estabilizados.
Una SR publicada por Martin et al.89 tuvo como objetivo evaluar la eficacia y seguridad de los beta bloqueadores en pacientes ICFEp. Los autores incluyeron 10 estudios, con 3,087 participantes de entre 30 a 81 años, de los cuales 5 se compararon con placebo. Se observó una discreta reducción del riesgo de mortalidad cardiovascular (CR 0.78, IC95%: 0.62; 0.99), con un Número Necesario a Tratar (NNT) de 25. Sin embargo, la calidad de la evidencia fue calificada como baja. Respecto a la mortalidad por cualquier causa, no se pudo demostrar una disminución del riesgo significativa (CR 0.82, IC95%: 0.67; 1.00)89.
Respecto a los pacientes con ICFEr, una RS publicada por Komajda et al.90 publicada en 2018 realizó una "metaanálisis en red" para evaluar distintas alternativas farmacológicas para el tratamiento de estos pacientes. Los autores incluyeron en total 58 ECAs que evaluaron distintas alternativas farmacológicas, 9 estudios incluyeron menos de 100 participantes y 11 estudios incluyeron más de 2,000. El seguimiento tuvo un rango de 3 meses a 4 años, con 18 estudios que dieron seguimiento por más de 1 año90. Los resultados de los metaanálisis mostraron que la terapéutica con beta bloqueadores (9,969 pacientes/año) se asociaron a una disminución del riesgo de mortalidad por cualquier causa del 42% (CR 0.58; IC95%: 0.34; 0.95) en comparación a placebo, sin embargo, no se pudo demostrar una diferencia significativa en la disminución del riesgo de mortalidad cardiovascular (CR 0.62; IC95%: 0.27; 1.32) en comparación a placebo, ni de hospitalización por cualquier causa (CR 0.86; IC95%: 0.59; 1.18) o de hospitalización por insuficiencia cardiaca (CR 0.45; IC95%: 0.13; 1.39) en comparación a placebo. El "metaanálisis en red" mostró que las combinaciones que se asociaron a una mayor disminución de la mortalidad por cualquier causa fue BB + iRNA + ARM (antagonista al receptor mineralocorticoide) (CR 0.38; IC95%: 0.20; 0.65) y la combinación de iECA + BB + ARM + IVA (ivabradina) (CR 0.41; IC95%: 0.21; 0.70). Las combinaciones de BB + iECA + ARM (CR 0.44; IC95%: 0.27; 0.67), ARM + BB (CR 0.48; IC95%: 0.24; 0.86) y de iECA + BB + BRA (CR 0.52; IC95%: 0.32; 0.80) también se asociación con una disminución del riesgo de mortalidad por cualquier causa en comparación a placebo90 (Tabla 5).
Tabla 5 Tamaño del global del tratamiento frente a placebo para cada tratamiento como monoterapia o en combinación por cada desenlace importante
| Fármacos | Mortalidad por cualquier causa | Mortalidad por causa cardiovascular | Hospitalización por cualquier causa | Hospitalización por insuficiencia cardiaca |
|---|---|---|---|---|
| iRNA+BB+ARM | 0.38 (0.20-0.67)* | 0.36 (0.16-0.71)* | 0.58 (0.36-0.92)* | 0.27 (0.07-1.07)† |
| iECA+BB+ARM+IVA | 0.41 (0.21-0.70)* | 0.41 (0.19-0.82)* | 0.58 (0.36-0.92)* | 0.25 (0.07-0.99)* |
| iECA+BB+ARM | 0.44 (0.27-0.67)* | 0.45 (0.25-0.75)* | 0.65 (0.45-0.93)* | 0.34 (0.13-0.91)* |
| BRA+BB | 0.48 (0.24-0.86)* | 0.50 (0.19-1.12)† | 0.79 (0.47-1.21)† | 0.31 (0.07-1.29)† |
| iECA+BRA+BB | 0.52 (0.32-0.80)* | 0.47 (0.24-0.82)* | 0.74 (0.46-1.04)† | 0.42 (0.16-1.23)† |
| iECA+BB | 0.58 (0.42-0.73)* | 0.56 (0.37-0.65)* | 0.75 (0.54-0.92)* | 0.34 (0.17-0.56)* |
| iECA+ARM | 0.58 (0.36-0.90)* | 0.56 (0.31-0.95)* | 0.69 (0.45-0.96)* | 0.36 (0.12-0.96)* |
| BB | 0.58 (0.34-0.95)† | 0.62 (0.27-1.32)† | 0.86 (0.59-1.18)† | 0.45 (0.13-1.39)† |
| iECA+BRA | 0.83 (0.52-1.23)† | 0.80 (0.43-1.33)† | ND | 0.26 (0.08-0.57)† |
| iECA | 0.84 (0.67-1.01)† | 0.81 (0.60-1.04)† | 0.89 (0.71-1.05)† | 0.52 (0.32-0.76)* |
| BRA | 0.89 (0.61-1.27)† | 0.85 (0.51-1.28)† | 0.81 (0.56-1.01)† | 0.53 (0.26-1.03)† |
Resultados de los metaanálisis en red: razón de riesgo y sus intervalos de confianza del 95% en comparación con placebo.
*Estadísticamente significativo.
†Estadísticamente no significativo. BB: betabloqueadores; BRA: bloqueador del receptor de la angiotensina; iECA: inhibidores de la enzima convertidora de angiotensina; iRNA: inhibidores de los receptores de la angiotensina/neprilisina; IVA: ivabradina; ND: no disponible. Modificada de: Komajda M, Böhm M, Borer JS, Ford I, Tavazzi L, Pannaux M, et al. Incremental benefit of drug therapies for chronic heart failure with reduced ejection fraction: a network metaanalysis. Eur J Heart Fail. 2018;20:1315-22.
Los autores concluyen que se puede observar una evolución en el tratamiento de la insuficiencia cardiaca empleando medicamentos modificadores de la enfermedad, la evidencia apoya el hecho de que la combinación de distintas clases terapéuticas ha contribuido sustancialmente a la disminución en la mortalidad por cualquier causa (62% para la combinación de BB + ARM + iRNA Y 59% para iECA + BB + ARM + IVA), las hospitalizaciones por insuficiencia cardiaca (73% para la combinación de BB + ARM + iRNA Y 75% para iECA + BB + ARM + IVA) y la mortalidad cardiovascular (64% para la combinación de BB + ARM + iRNA Y 59% para iECA + BB + ARM + IVA). Sin embargo, es importante que los médicos evalúen cuidadosamente a los pacientes de manera individual para elegir la mejor combinación de agentes terapéuticos.
De Marzo et al. en 202291 publican una RS con "metaanálisis en red" donde analizaron todas las alternativas farmacológicas en más de 90,000 pacientes con ICFEr. Los autores incluyeron 69 ECAs con 91,741 participantes y los resultados de los metaanálisis coinciden con el trabajo de Komajda et al.90 respecto a que las terapias nuevas y las combinaciones han mejorado de manera considerable los desenlaces en pacientes ICFEr, logrando una disminución del riesgo de mortalidad por cualquier causa hasta de 57% con la combinación de BB + iECA + ARM en comparación a placebo (CR 0.43, IC95%: 0.27; 0.63). La disminución del riesgo de mortalidad con BB fue de 38% (CR 0.62; IC95%: 0.41; 0.89), pero no se pudo demostrar una diferencia significativa respecto a la disminución del riesgo de muerte cardiovascular (CR 0.46; IC95%: 0.46; 1.20) ni en la hospitalización por insuficiencia cardiaca (CR 0.84; IC95%: 0.54; 1.30)91.
Pregunta 20: ¿Cuáles son la eficacia y la seguridad de los ARM para los pacientes con insuficiencia cardiaca crónica?
Recomendación:
– Se debe recomendar el uso de ARM (espironolactona o eplerenona) en todo paciente con ICFEr para disminuir el riesgo de hospitalizaciones por insuficiencia cardiaca y de muerte por causa cardiovascular.
– En ciertos pacientes con insuficiencia cardiaca con FEVI > 40% resulta razonable considerar el uso de ARM.
– Es necesario conocer la TFG y los niveles séricos de potasio en todo paciente antes de iniciar un ARM.
– Es recomendable monitorear periódicamente la función renal y los niveles séricos de potasio en todo paciente bajo tratamiento con ARM.
– No se recomienda iniciar un ARM en pacientes con TFGe < 30 ml/min.
– En el momento actual no existe evidencia suficiente para sustituir la espironolactona o la eplerenona por finerenona en pacientes con insuficiencia cardiaca crónica.
Nivel de evidencia 1++, grado de recomendación A (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
Los diuréticos han sido piedra angular del manejo de distintos padecimientos cardiovasculares como la HAS, insuficiencia cardiaca, enfermedad renal crónica, entre otros92. Como su nombre lo indica, los antagonistas del receptor mineralocorticoide (ARM) son una clase terapéutica que inhibe el efecto de la aldosterona en el receptor mineralocorticoide (RM), provocando que la aldosterona no pueda activarlo. De acuerdo con su estructura química, pueden ser específicos (no-esteroideos) o no específicos (esteroideos), estos últimos siendo los primeros en ser empleados terapéuticamente. Los ARM no específicos tienen efecto anti androgénico por lo que muestran eventos adversos consistente con esa actividad. La espironolactona y la drospirenona son representantes de este grupo. La espironolactona ha mostrado un efecto anti proteinúrico lo que la hace valiosa en enfermedad renal crónica92. Los ARM específicos fueron diseñados para carecer de esos efectos esteroideos y contemplan eplerenona, canrenona, mexrenona y finerenona, siendo la primera la más estudiada92.
Las GPC AHA/ACC 2022 sugieren en pacientes ICFEp el uso de ARMs ya que han demostrado disminuir el riesgo de hospitalización, particularmente en pacientes con FEVI disminuido de manera importante. En cambio, en pacientes con ICFEr y clase funcional NYHA II a IV, se recomienda el uso de MRAs (espironolactona o eplerenona) para reducir la morbilidad y la mortalidad, si la tasa de filtrado glomerular (TFG) es > 30 mL/min/1.73m2 y el potasio sérico es < 5.0 mEq/L. Es importante llevar a cabo un monitoreo estrecho de los electrolitos séricos (particularmente potasio) y función renal. En el caso de los pacientes en los cuales no se puede mantener una cifra de potasio sérico por debajo de < 5.5 mEq/L es importante suspender el tratamiento con ARM4. El consenso mexicano en insuficiencia cardiaca 2022 publicado por Magaña et al.2 recomiendan el uso de inhibidores del SRA combinados con BB como parte del manejo inicial en pacientes con ICFEr por el efecto benéfico de un triple bloqueo neuroendocrino.
Una RS publicada por Xiang et al.93 en 2022 tuvo como objetivo evaluar a través de un "metaanálisis en red" distintas alternativas farmacológicas en pacientes con ICFEp. Los autores incluyeron estudios que eligieron pacientes con FEVI > 40% (20,633 participantes). Los resultados de los metaanálisis mostraron que ningún tratamiento, de 19 ECAs, se asoció a una disminución de la mortalidad por cualquier causa. Sin embargo, los ARM (CR 0.83; IC95%: 0.69; 0.99), iSGLT-2 (CR 0.71; IC95%: 0.60; 0.83), iRNA (CR 0.76; IC95%: 0.61; 0.95) se asociaron a una disminución de las hospitalizaciones por insuficiencia cardiaca93.
Una RS publicada por Martin et al. en 2021 con la Colaboración Cochrane89 evaluó distintas alternativas farmacológicas en pacientes ICFEp. Incluyó 13 ECAs con 4,459 participantes, de los cuales 8 se compararon con placebo y 5 con otras alternativas farmacológicas. Los resultados del metaanálisis muestran que la terapia con ARM se asoció a una disminución del riesgo de hospitalizaciones por insuficiencia cardiaca (RR 0.82; IC95: 0.69; 0.98) con una moderada calidad de la evidencia. Sin embargo, también en esta RS no se pudo demostrar una disminución del riesgo de moralidad por cualquier causa (RR 0.91; IC95%: 0.78; 1.06) ni del riesgo de mortalidad cardiovascular (RR 0.90; IC95%: 0.74; 1.11). Tampoco hubo una mejoría en la calidad de vida. (DM 0.84; IC95%: –2.30; 3.98). Respecto a la seguridad, el tratamiento con ARM se asoció a un riesgo incrementado de hiperkalemia (RR 2.11; IC95%: 1.77; 2.51)89.
Una RS publicada por Burnett et al. en 201787 evaluó distintas alternativas farmacológicas en pacientes ICFEr y a través de un "metaanálisis en red" reportó que la combinación de ARM + iECA logró una disminución de la mortalidad por cualquier causa del 43% (CR 0.57; IC95%: 0.35; 0.91); y cuando se combina un ARM + BB + iACE se observó una disminución de la mortalidad por cualquier causa del 56% (CR 0.57; IC95%: 0.26; 0.66) y con ARM + BB + iRNA se asocia a una reducción de la mortalidad por cualquier causa del 63% (CR 0.37; IC95%: 0.19; 0.65)87.
Komajda et al.90 publican una RS con "metaanálisis en red" en donde se evaluaron distintas alternativas farmacológicas con distintos desenlaces en pacientes con ICFEr. Los autores incluyeron estudios con un total de 3,326 pacientes/año para la combinación de ARM + iECA, 18,898 pacientes/año para la combinación de ARM + iRNA + BB y 12,515 pacientes/año con ARM + iACE + BB + IVA. Los resultados del "metaanálisis en red" mostraron que la combinación de ARM + iECA se asoció a una disminución de la mortalidad de cualquier causa de 42% (CR 0.58; IC95%: 0.36; 0.90), de la mortalidad cardiovascular en 44% (CR 0.56; IC95%: 0.31; 0.95); de las hospitalizaciones por cualquier causa en 31% (CR 0.69; IC95%: 0.45; 0.96) y de las hospitalizaciones por insuficiencia cardiaca en 64% (CR 0.58; IC95%: 0.12; 0.96). La combinación de ARM + BB + iECA se asoció a una disminución de la mortalidad de cualquier causa de 56% (CR 0.44; IC95%: 0.27; 0.67), de la mortalidad cardiovascular en 55% (CR 0.45; IC95%: 0.25; 0.75); de las hospitalizaciones por cualquier causa en 35% (CR 0.65; IC95%: 0.45; 0.93) y de las hospitalizaciones por insuficiencia cardiaca en 66% (CR 0.58; IC95%: 0.13 0.91). La combinación de ARM + iECA + BB + IVA mejoró aún más los desenlaces y se asoció a una disminución de la mortalidad de cualquier causa de 59% (CR 0.41; IC95%: 0.21; 0.70), de la mortalidad cardiovascular en 59% (CR 0.41; IC95%: 0.19; 0.82); de las hospitalizaciones por cualquier causa en 42% (CR 0.58; IC95%: 0.36; 0.92) y de las hospitalizaciones por insuficiencia cardiaca en 75% (CR 0.25; IC95%: 0.07; 0.99) y finalmente la combinación que mejores resultados mostró, la combinación de MRA + BB + iRNA que se asoció a una disminución de la mortalidad de cualquier causa de 62% (CR 0.38; IC95%: 0.20; 0.65), de la mortalidad cardiovascular en 64% (CR 0.36; IC95%: 0.16; 0.71); de las hospitalizaciones por cualquier causa en 42% (CR 0.58; IC95%: 0.36; 0.92), aunque no hubo diferencias estadísticamente significativas en las hospitalizaciones por insuficiencia cardiaca (CR 0.27; IC95%: 0.07; 1.07)90. Los autores del estudio hacen énfasis en que no todas las combinaciones funcionan igual para todos los pacientes y hay que individualizar cada caso para elegir las opciones terapéuticas que mejoren los desenlaces y disminuyan el riesgo de eventos adversos90.
Una RS publicada en 2022 por Tromp et al.94 llevó a cabo un "metaanálisis en red" en donde identificaron 75 ECAs con 95,444 participantes con ICFEr. Los resultados del metaanálisis mostraron que el uso de ARM se asoció a una disminución del riesgo de muerte por cualquier causa en 24% (CR 0.76; IC95% 0.67; 0.85), y la combinación de ARM + BB + iRNA + iSGLT-2 mostró la mayor disminución del riesgo de mortalidad por cualquier causa (61%) (CR 0.39; IC95%: 0.31; 0.49) seguido de la combinación de ARM + BB + iRNA + VERI (59%) (CR 0.41; IC95%: 0.32; 0.53) y la combinación de ARM + BB + iRNA (56%) (CR 0.44; IC95%: 0.36; 0.54). Los resultados fueron muy similares para la mortalidad cardiovascular. Se estimó en los análisis secundarios que el total de años vida ganados para un paciente de 70 años con la combinación de ARM + iRNA + BB + iSGLT-2 fue de 5.0 años (2.5 a 7.5 años) comparado con placebo94.
Pregunta 21: ¿Cuáles son las recomendaciones para el uso de iSGLT2 en pacientes con insuficiencia cardiaca?
Recomendación:
– Se debe iniciar un iSGLT2 en todo paciente con diagnóstico de insuficiencia cardiaca independientemente de su FEVI, para reducir el riesgo de muerte por causa cardiovascular y los episodios de empeoramiento que requieran o no hospitalización.
– El inicio de un iSGLT2 se debe considerar lo más tempranamente posible una vez realizado el diagnóstico de insuficiencia cardiaca.
– No es necesario un monitoreo de la glucemia ni de la hemoglobina glucosilada en pacientes con insuficiencia cardiaca sin diabetes que utilicen un iSGLT2.
– En pacientes con infección micótica genitourinaria activa se recomienda diferir el inicio de un iSGLT2 hasta resolver el proceso infeccioso.
– No se recomienda iniciar un iSGLT2 en pacientes con insuficiencia cardiaca con TFGe < 15 ml/min.
Nivel de evidencia 1++, grado de recomendación A (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
Los inhibidores del cotransportador sodio-glucosa 2 (iSGLT-2) bloquean las proteínas transportadoras de sodio y glucosa en la nefrona. La SGLT2 es la principal proteína de transporte y promueve la reabsorción de glucosa desde el filtrado glomerular y es responsable de aproximadamente el 90% de este mecanismo tubular. SGLT2 se encuentra principalmente en los riñones en las células epiteliales que recubren el primer segmento del túbulo contorneado proximal. El principal efecto metabólico de esto es inhibir la reabsorción de glucosa en el riñón y, por lo tanto, disminuir la concentración de glucosa sérica. Además de estos efectos fisiológicos, los iSGLT-2 aumentan la natriuresis, causan contracción del volumen intravascular y alteran la hemodinamia intra-renal, lo que contribuye a sus efectos benéficos en la presión arterial, disminución del peso corporal y disminución en la progresión de albuminuria95.
Las GPC ADA/ACC 2022 y las GPC ESC 2021 establecen que mantener cifras de presión arterial en rangos normales disminuye el riesgo de desarrollo de insuficiencia cardiaca. Se ha establecido una meta de < 130/80 mm HG en pacientes con un factor de riesgo cardiovascular mayor de 10%. En pacientes con DT2 con alto riesgo o enfermedad cardiovasculares aterosclerótica (ECVA) establecida, se recomienda el uso de iSGLT-2 para disminuir el riesgo de hospitalizaciones4. Estos lineamientos recomiendan en pacientes con ICFEr sintomática, el uso de iSGLT-2 es recomendado para reducir el riesgo de hospitalizaciones y mortalidad cardiovascular, independientemente si el paciente tiene DT2 o no la presenta4. Las GPC ESC recomiendan considerar el manejo combinado de un iSGLT-2 + iECA/IRNA + BB + ARM en pacientes con ICFEr independientemente si presentan DT2 o no la presentan5.
Una RS publicada Theofilis et al. en 2022 tuvo como objetivo evaluar el impacto del tratamiento con iSGLT-2 en parámetros ecocardiográficos. Los autores en el metaanálisis de 32 ECAS Y 2,351 pacientes mostraron una mejoría significativa en el FEVI (DM 1.97; IC95% 0.92; 3.02), un incremento de la deformación longitudinal global (GLS, por sus siglas en inglés) (DM 1.17; IC95% 0.25; 2.10), una reducción del volumen telediastólico del ventrículo izquierdo (LVESV, por sus siglas en inglés) (DM –3.10; IC95% –6.76; 0.56), aunque sin alcanzar la significancia estadística. Los valores que no mostraron cambios fueron el volumen telesistólico del ventrículo izquierdo (LVESV, por sus siglas en inglés), el índice de masa del ventrículo izquierdo ni del índice de volumen del ventrículo izquierdo96.
Wang et al.97 en 2022 publicaron una RS que evaluó el impacto de los iSGLT-2 en pacientes con ICFEp y ICFEm. Los autores incluyeron 6 ECAs con 15,989 participantes. Los resultados del metaanálisis mostraron que los iSGLT-2 reducen el riesgo de hospitalización por insuficiencia cardiaca (CR 0.74; IC95% 0.67; 0.82) y el riesgo combinado de muerte cardiovascular y hospitalización (CR 0.79; IC95% 0.72; 0.85). Los resultados se observaron cuando se estratificaron los grupos en ICFEp y ICFEm.
Con respecto a los pacientes ICFEr, Pandey et al.98 publicaron una RS en 2022 que evaluó la eficacia y seguridad de los i-SGLT2 en pacientes con ICFEr y EFpEF. Los autores incluyeron 4 ECAs con 15,684 pacientes, 2 ECAs con ICFEr, uno con ICFEp y otro más con pacientes combinados. Los inhibidores de iSGLT-2 disminuyeron el riesgo de muerte cardiovascular y hospitalización por insuficiencia cardiaca en un 24% (CR 0.76; IC95%: 0.70; 0.82). Esto se mostró también en pacientes ICFEr (CR 0.74; IC95%: 0.68; 0.81) y ICFEp (CR 0.78; IC95%: 0.68; 0.89). Zannad et al. en 202099 publican otra RS que evaluó el efecto de los iSGLT-2 basados en los estudios DAPA-HF y EMPEROR-Reduced. Ambos estudios reclutaron 8,474 pacientes y el metaanálisis demostró una reducción del 13% en mortalidad de cualquier causa (CR 0.87; IC95% 0.77; 0.98) y 14% de reducción en mortalidad cardiovascular (CR 0.86; IC95%: 0.76; 0.98). Mostró además una disminución una disminución del 26% en el riesgo relativo en el tiempo para la primer hospitalización y muerte cardiovascular y del 25% en el riesgo relativo en el tiempo para hospitalización recurrente y muerte cardiovascular99.
Yun et al.100 en 2023 evaluaron la combinación de ARNI + iSGLT-2 en comparación a las monoterapias separadas en pacientes ICFEr. Los estudios incluidos tuvieron bajo riesgo de sesgo. Los resultados de los metaanálisis en el desenlace compuesto por mortalidad de cualquier causa y primera hospitalización por insuficiencia cardiaca mostraron una disminución del riesgo con la combinación de iSGLT-2 + ARNI en un 32% (CR 0.68; IC95%: 0.53; 0.85) en comparación a ARNI como monoterapia, pero no mostraron diferencia en comparación al iSGLT-2 como monoterapia (CR 0.86; IC95%: 0.63; 1.17). La disminución en el riesgo de mortalidad cardiovascular fue menor con la combinación del iSGLT-2 + ARNI en comparación al iSGLT-2 (CR 0.64; IC95%: 0.46; 0.87) y en comparación a ARNI (CR 0.65; IC95%: 0.46; 0.93). El riesgo de muerte por cualquier causa también disminuyó con la combinación del iSGLT-2 + ARNI en comparación al iSGLT-2 (CR 0.72; IC95%: 0.56; 0.93) y en comparación a ARNI (CR 0.70; IC95%: 0.54; 0.92)100.
La RS de Tromp et al.94 que evaluó distintas alternativas farmacológicas, como monoterapia y combinaciones, a través de un "metaanálisis en red". Los resultados mostraron que la combinación de un iSGLT2 + IRNA + BB + ARM mostraron una disminución del riesgo de mortalidad por cualquier causa en 61%, más eficaz respecto al resto de combinaciones y monoterapias (CR 0.39, IC95%: 0.31; 0.49), de mortalidad cardiovascular u hospitalizaciones por insuficiencia cardiaca combinados en 64% (CR 0.36; IC95%: 0.29; 0.46) y de mortalidad cardiovascular en 67% (CR 0.33; IC95%: 0.26; 0.43)94.
Pregunta 22: ¿Cuáles son las recomendaciones para el uso de diuréticos en los pacientes con insuficiencia cardiaca crónica?
Recomendación:
– Se deben utilizar diuréticos de asa para el alivio sintomático de pacientes con insuficiencia cardiaca con evidencia de congestión pulmonar o sistémica independientemente de la FEVI.
– Se debe evitar el uso de dosis altas de diuréticos de asa en pacientes con insuficiencia cardiaca que no muestren evidencia de congestión pulmonar o sistémica, para evitar la depleción de volumen, la hipotensión arterial y el desequilibrio electrolítico.
– En pacientes con resistencia a los diuréticos es recomendable el bloqueo secuencial de la nefrona con manejo combinado (diurético de asa, tiazida, acetazolamida).
– En pacientes con persistencia de la congestión pulmonar o sistémica a pesar del uso de diuréticos por vía oral a las dosis adecuadas (monoterapia o terapia combinada), es recomendable valorar inmediatamente el uso de diuréticos por vía parenteral en servicios de urgencias, hospitalización o programas de hospital de día.
– Es recomendable monitorear periódicamente los niveles séricos de sodio y potasio en todo paciente con insuficiencia cardiaca que utilice diuréticos.
Nivel de evidencia 1++, grado de recomendación A (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
Las GPC AHA/ACC 2022 recomiendan en pacientes ICFEr que presentan retención de fluidos, usar diuréticos para mejorar la congestión, los síntomas, y prevenir el empeoramiento de la insuficiencia. Los diuréticos de ASA son la clase terapéutica, los diuréticos como la clortalidona o la hidroclorotiazida pueden ser considerados en pacientes con hipertensión arterial e insuficiencia cardiaca con retención de fluidos leve. La metalozona o la clorotiazida pueden ser adicionados a los diuréticos de ASA en pacientes con edema refractario a los diuréticos de ASA en monoterapia. Es deseable manejar los diuréticos a la dosis más baja posible hasta lograr respuesta clínica con ausencia de síntomas congestivos. La resistencia a los diuréticos puede manejarse escalando la dosis de estos, administrándolos por vía endovenosa de forma continua o en bolos o combinando distintas clases de diuréticos. Los diuréticos han fallado en demostrar una disminución de la mortalidad en insuficiencia cardiaca4 (Tabla 6).
Tabla 6 Diuréticos orales comúnmente empleados en el tratamiento de la congestión por insuficiencia cardiaca crónica
| Fármacos | Dosis inicial diaria | Dosis máxima diaria | Duración de acción |
|---|---|---|---|
| Diuréticos de asa | |||
| Bumetanida | 0.5-1.0 mg una o dos veces | 10 mg | 4-6 h |
| Furosemida | 20-40 mg una o dos veces | 600 mg | 6-8 h |
| Torasemida | 10-20 mg una vez | 200 mg | 12-16 h |
| Diuréticos tiazídicos | |||
| Clorotiazida | 250-500 mg una o dos veces | 1000 mg | 6-12 h |
| Clortalidona | 12.5-25 mg una vez | 1000 mg | 24-72 h |
| Hidroclorotiazida | 25 mg una o dos veces | 200 mg | 6-12 h |
| Indapamida | 2.5 mg una vez | 5 mg | 36 h |
| Metolazona | 2.5 mg una vez | 20 mg | 12-24 h |
Modificada de: Heidenreich PA, Bozkurt B, Aguilar D, Allen LA, Byun JJ, Colvin MM, et al. 2022 AHA/ACC/HFSA Guideline for the management of heart failure: a report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. 2022;145:e895-e1032.
Los diuréticos de ASA han mostrado que tienen el potencial de causar, hipernatremia e hipocalemia importantes, lo que puede llevar al desarrollo de arritmias cardiacas e hipotensión. Por otro lado, los diuréticos conservadores de potasio son menos efectivos, pero tienen menos riesgo de hipocalemia101.
Una RS publicada por Eid et al.101 en 2020 tuvo como objetivo evaluar la eficacia y seguridad de los distintos diuréticos en el manejo de la insuficiencia cardiaca. Los autores incluyeron 54 ECAs (10,740 participantes), 34 ECAs fueron elegibles para analizar la información en un "metaanálisis en red". Los autores calificaron la calidad de los estudios como moderada o alta calidad. Los resultados de los distintos metaanálisis mostraron que azosemide y torasemide se asociaron a una reducción significativa de los valores de BNP (DM –33.87; IC95%: –46.33; –21.40 y DM –64.00; IC95%: –122.57; –5.43, respectivamente). Espironolactona no mostró diferencias en comparación a furosemide (DM –7.00; IC95%: –73.75; 59.75). Respecto a la TFG, azosemide no mostró diferencia vs. furosemide (DM 0.113; IC95%: –0.081; 0.307) después de 6 meses y hasta 2 años de seguimiento. Respecto al edema, torasemide logró mejores resultados en comparación a furosemide (RR 1.54; IC95%: 1.01; 2.35), pero espironolactona y bendroflumetazida no fueron superiores a furosemide. Respecto a la natriuresis, no se observaron diferencias estadísticamente significativas entre los distintos fármacos. Diapamide causó más efectos adversos gastrointestinales que furosemide, espironolactona mostró cifras más altas de potasio en suero que furosemide y bumetamide cifras más altas de sodio que furosemide. Los autores no encontraron diferencias en peso corporal, presión arterial, urea sérica, síntomas neurológicos, desequilibrio hidroelectrolítico y deshidratación entre los distintos diuréticos. Las conclusiones de los autores fueron que torasemide fue superior a furosemide respecto a la disminución de BNP y edema101.
Una RS publicada por Wierda et al.102 en 2020 evaluó el tratamiento con diuréticos endovenosos o subcutáneos en pacientes de forma ambulatoria donde mostraron progresión de la insuficiencia cardiaca. Los autores incluyeron 11 estudios observacionales, no aleatorios. Los resultados mostraron que, en 984 pacientes analizados, se informaron pocos eventos adversos. Las tasas de rehospitalización a los 30 y 180 días fueron 28 a 46%. Las tasas más altas de rehospitalización fueron de 52 en 30 días en los grupos con diurético subcutáneo y de 42% en el grupo con diurético intravenoso. Los autores concluyeron que la calidad de la evidencia no es suficiente para realizar recomendaciones específicas y que se requiere más evidencia científica de alta calidad102.
Pregunta 23: ¿Cuáles son las indicaciones para el empleo de ivabradina en los pacientes con insuficiencia cardiaca crónica?
Recomendación:
– Se recomienda el empleo de ivabradina para disminuir el riesgo de hospitalizaciones y de muerte por insuficiencia cardiaca en todo paciente con insuficiencia cardiaca con FEVI reducida, en ritmo sinusal y que no logre el control de la frecuencia cardiaca a menos de 75 l.p.m. con el uso de BB.
– El uso combinado de ivabradina y BB para el control de la frecuencia cardiaca deberá recomendarse en forma temprana, particularmente en aquellos pacientes con ICFEr durante el periodo vulnerable de la enfermedad.
– Se recomienda el uso de ivabradina como monoterapia para el control de la frecuencia cardiaca en todo paciente con ICFEr, en ritmo sinusal, que tenga una contraindicación formal para el uso de BB.
– En el momento actual no existe evidencia suficiente para sustentar el uso de ivabradina en pacientes con insuficiencia cardiaca con FEVI > 40%.
– En el momento actual no existe evidencia suficiente para recomendar el uso de ivabradina en pacientes con insuficiencia cardiaca y fibrilación auricular.
Nivel de evidencia 1++, grado de recomendación A (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
La ivabradina (IVA) es un fármaco que provoca una reducción de la frecuencia cardiaca dosis dependiente. En el nódulo sinoauricular se encuentra un canal transmembranario no selectivo, operado por nucleótidos cíclicos y activado por la hiperpolarización en el nódulo sinoauricular, el cual tiene unas características únicas por el hecho de sus células poseen la capacidad innata de generar un cambio cíclico de su potencial de membrana en reposo103. La despolarización tiene su inicio con la apertura de canales iónicos específicos que conducen una corriente de entrada despolarizante, lenta, mixta de sodio-potasio, llamada corriente de marcapasos o corriente funny (If) y da como resultado, potenciales de acción espontáneos repetitivos que son la causa de su automatismo103. La IVA bloquea la cara intracelular de este canal transmembranario al inhibir el paso de los cationes con un alto grado de selectividad, y ello da lugar a una reducción de la pendiente de despolarización diastólica del potencial de acción del marcapasos, con lo que reduce la frecuencia cardiaca. La IVA bloquea el canal en su estado abierto, creando una característica especialmente favorable, consistente en una dependencia en función del uso (es decir, es más potente a frecuencias cardiacas más rápidas)103,104.
Las GPC AHA/ACC 2022 recomiendan el uso de IVA en pacientes sintomáticos clase funcional NYHA II – III que están recibiendo otras terapias de primera línea, incluyendo BB a dosis altas y que continúan con ritmo sinusal con una frecuencia cardiaca > 70 latidos/minuto debido a que la frecuencia cardiaca ha demostrado ser un fuerte predictor de eventos cardiovasculares, incluida la insuficiencia cardiaca. Es importante recalcar que los estudios con IVA, solamente el 25% de los pacientes se encontraban en dosis óptimas de BB, por lo que sugieren considerar agregar IVA solamente en los casos en los que el paciente está recibiendo BB a dosis terapéuticas adecuadas y persiste con una frecuencia cardiaca > 70 latidos/minuto4. Las GPC de la ESC 2021 recomiendan el uso de IVA como terapia alternativa en pacientes con una frecuencia cardiaca > 70 latidos/minuto a pesar del manejo a dosis adecuadas de un BB, iECA o iRNA y un ARM para reducir el riesgo de hospitalización por insuficiencia cardiaca; también en pacientes que son intolerantes al tratamiento con BB5.
Una RS publicada en 2021 por Conceição et al.105 evaluó el impacto de IVA en pacientes ICFEp en el ejercicio físico. Los autores incluyeron 4 ECAs y los resultados del metaanálisis demostraron que IVA no tiene ningún efecto en la capacidad para el ejercicio expresado por VO2 y 6MWT (DM 0.8; IC95%: –2.5; 4.3). Los análisis secundarios mostraron una disminución de la frecuencia cardiaca en reposo105.
Una RS publicada por Xiang et al.93 para evaluar todos los medicamentos que han demostrado tener cierto beneficio en pacientes con ICFEp y ICFEm. Los autores, aunque no incluyeron IVA, reportaron un total de 20,633 participantes y 19 ECAs. Ningún medicamento se asoció a una disminución en la mortalidad de cualquier causa y los iSGLT-2, iRNA y ARM se asociaron a una disminución del riesgo de hospitalización por insuficiencia cardiaca93.
Una RS publicada por Richard et al. en 2021 tuvo como objetivo evaluar el impacto de IVA en pacientes con insuficiencia cardiaca ICFEr. Los autores incluyeron 6 ECAs y los análisis de subgrupos mostraron que IVA mejoró la frecuencia cardiaca en reposo (DM –9.57, IC95%: –11.15; –8.00), mejoró la FEVI (DM 3.89; IC95%: 2.61; 5.17), mejoró la remodelación del ventrículo izquierdo (DM –3.73; IC95%: –4.25; –3.21), mejoró la capacidad durante el ejercicio (duración) (DM 8.52; IC95%: 0.09, 16.94) y también mostró una disminución significativa en las rehospitalizaciones debido a insuficiencia cardiaca (RR 0.76; IC95%: 0.69; 0.84). Sin embargo, no pudo demostrar una mejoría respecto a la HRQoL (DM 0.65; IC95%: –10.52; 11.82) y en mortalidad cardiovascular (RR 0.92; IC95%: 0.82; 1.03)104.
Una RS publicada por Tóth et al. en 2021 evalúan los efectos de IVA en reducción de la mortalidad, función de ventrículo izquierdo y reducción de la frecuencia cardiaca, tanto en pacientes ICFEr como ICFEp. Los resultados de los metaanálisis que no hubo diferencia en la mortalidad en ninguna de las dos poblaciones, pero si hubo una disminución de la frecuencia cardiaca, tanto en ICFEr (–17.64 latidos/minuto) y ICFEp (–11.43 latidos/minuto) y mejoría en la FEVI en ICFEr (5.93, IC95%: 4.19; 7.67) pero no en ICFEp106.
Una RS publicada por Tromp et al.94 en 2022 evaluó las distintas combinaciones de fármacos para insuficiencia cardiaca ICFEr y los "metaanálisis en red" mostraron que la combinación de iECA + BB + ARM + IVA lograron una disminución de la mortalidad por cualquier causa del 52% (CR 0.48; IC95% 0.39; 0.58) y una disminución de la mortalidad cardiovascular o de las hospitalizaciones por insuficiencia cardiaca de 51% (CR 0.49; IC95% 0.39; 0.61)94. Komajda et al. en 2018 encontró resultados similares en pacientes ICFEr con una disminución de la combinación de iECA + BB + ARM + IVA en el riesgo de mortalidad de cualquier causa de 59% (CR 0.41; IC95% 0.21; 0.70), disminución de la mortalidad cardiovascular de 59% (CR 0.41; IC95% 0.19; 0.82), disminución de la hospitalización de cualquier causa de 42% (CR 0.58; IC95% 0.36; 0.92) y una disminución de la hospitalización por insuficiencia cardiaca de 75% (CR 0.25; IC95% 0.07; 0.99)90.
Pregunta 24.1: ¿Cuáles son las recomendaciones para el empleo del vericiguat en los pacientes con insuficiencia cardiaca?
Recomendación:
– El vericiguat puede ser recomendado como adyuvante de la terapia farmacológica fundamental para disminuir el riesgo de muerte por causa cardiovascular y los internamientos por falla cardiaca en pacientes con ICFEr, en particular si tienen antecedente de un evento de empeoramiento reciente (menos de 12 meses).
– El vericiguat no debe ser recomendado como primera línea de manejo farmacológico en pacientes con insuficiencia cardiaca.
Nivel de evidencia 1++, grado de recomendación A (recomendación fuerte).
Pregunta 24.2: ¿Qué precauciones se deben tener para el empleo seguro del vericiguat en pacientes con insuficiencia cardiaca?
Recomendación: Se debe vigilar el comportamiento de la presión arterial cuando se administre vericiguat en pacientes con ICFEr.
Nivel de evidencia 1++, grado de recomendación A (recomendación fuerte).
Pregunta 24.3: ¿Cuáles son las recomendaciones para el uso de vericiguat en pacientes con insuficiencia cardiaca con fracción de eyección preservada o ligeramente reducida?
Recomendación: En el momento actual no existe evidencia para recomendar el uso de vericiguat en pacientes con insuficiencia cardiaca con fracción de eyección preservada o ligeramente reducida.
Nivel de evidencia 1++, grado de recomendación A (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
La vía de señalización óxido nítrico-guanilato ciclasa soluble es clave en la regulación del sistema cardiovascular en los pacientes con insuficiencia cardiaca. El guanilato ciclasa soluble (GCs) funciona como receptor para el óxido nítrico producido por el endotelio y, una vez acoplado, la GCs conduce la formación de la molécula de señalización GMPc, muy importante para regular ciertas funciones celulares como el tono vascular, la proliferación, la fibrosis o la inflamación107. En la insuficiencia cardiaca se produce una disfunción de las células endoteliales que genera una disminución en la producción de óxido nítrico y una insuficiente estimulación de la GCs, lo que da como resultado una reducción de la formación del GMPc. Esta reducción del GMPc provoca alteración multiorgánica. En el corazón, el déficit de GMPc hamostrado producir un aumento de la hipertrofia ventricular, remodelación de las paredes, fibrosis y rigidez miocárdica; en el lecho vascular, con más vasoconstricción y rigidez de los vasos, y en el riñón, con una disminución del flujo sanguíneo renal y una mayor retención de sodio y agua107. Los fármacos moduladores de la GCs, pueden ser activadores y estimuladores. Los primeros aumentan el GMPc mediante la activación directa e independiente del óxido nítrico de GCs y son efectivos principalmente cuando hay condiciones de aumento del estrés oxidativo y disfunción endotelial, aunque con un mayor riesgo de hipotensión. Sin embargo, los moduladores de la GCs (riociguat, vericiguat [VERI]) mejoran la sensibilidad de la GCs al óxido nítrico endógeno y luego ejercen una acción más fisiológica, lo que se traduce en efectos neutrales en la presión arterial107. Las GPC AHA/ACC 2022 proponen que el papel de estos moduladores de GCs se puede considerar al uso de vericiguat en pacientes con progresión de la ICFEr (hospitalizados en los últimos 6 meses y/o que hayan recibido furosemide endovenosa) y que están con medicamentos de primera línea, adicionado a estos. Esto debido a sus efectos benéficos como la vasodilatación, mejoría de la función endotelial, así como la disminución de la fibrosos y la remodelación cardiaca. Sin embargo, no se pudo demostrar una disminución en la mortalidad por cualquier causa4. Las GPC ESC 2021 por su parte, sugieren considerar el uso de vericiguat en pacientes clase funcional II – IV que han empeorado a pesar el tratamiento con iECA o iRNA, BB y un ARM para disminuir el riesgo de mortalidad cardiovascular y hospitalizaciones por insuficiencia cardiaca5.
Una RS publicada por Ullah et al.108 en 2020 tuvo como objetivo evaluar el tratamiento con moduladores de GCs en pacientes ICFEr y ICFEp. Los autores incluyeron 6 ECAs y 5,604 pacientes y los resultados del metaanálisis mostraron que el desenlace compuesto por disminución de la mortalidad cardiovascular y las hospitalizaciones por insuficiencia cardiaca mostró asociarse al uso de moduladores de GCs en un 8% (RR 0.92; IC95%: 0.85; 0.99), sin embargo, el riesgo de hospitalizaciones asociadas a insuficiencia no mostró diferencia significativa (RR 0.96; IC95%: 0.86; 1.07)108. Los resultados no se modificaron cuando se sub estratificaron los grupos entre ICFEr y ICFEp en comparación a placebo.
Una RS publicada Shaikh et al.109 en 2023 tuvo como objetivo evaluar el impacto de vericiguat en pacientes con ICFEr. Los autores incluyeron 7 ECAs y los resultados de los metaanálisis indican que el uso de vericiguat se asoció a una disminución en el riesgo de mortalidad de cualquier causa, muerte cardiovascular, y hospitalizaciones por insuficiencia cardiaca109. Una RS publicada por Zheng et al. en 2018 evaluó el impacto de los modificadores de GCs en pacientes con ICFEr. Los autores incluyeron 5 ECAs con 1,200 pacientes. Los resultados de los metaanálisis mostraron que los moduladores de GCs no se asocian a una disminución de la mortalidad (CR 1.25; IC95%: 0.50; 3.11) y solamente riociguat mostró disminuir los NT-proBNP (DM 0.78; IC95%: –1.01; –0.47) pero no en el grupo con vericiguat (DM 0.04; IC95%: –0.18; 0-25). No hubo diferencias importantes en la incidencia de eventos adversos entre los distintos grupos de tratamiento (CR 0.90; IC95%: 0.72; –1.12)110.
De Marzo et al. en 202291 publicaron una RS con "metaanálisis en red" que evaluó las distintas alternativas farmacológicas en pacientes ICFEr. Los resultados del "metaanálisis en red" mostraron que la combinación de vericiguat + iECA + BB + ARM disminuyó el riesgo de muerte por cualquier causa en 60% (CR 0.40; IC95%: 0.22; 0.65), muerte cardiovascular en 60% (CR 0.40; IC95%: 0.20; 0.67) y hospitalizaciones por insuficiencia cardiaca en 75% (CR 0.25; IC95%: 0.12; 0.43)91. Las combinaciones con IVA + iECA + BB + ARM, iSGLT-2 + iECA + BB + ARM y iRNA + BB + ARM fueron superiores en cuanto a disminución de mortalidad de cualquier causa91. Tromp et al94. por su parte, también publican una RS con "metaanálisis en red" y muestran que la combinación de vericiguat + iRNA + BB + ARM logró una disminución de la mortalidad de cualquier causa en 59% (CR 0.41; IC95%: 0.32; 0.53) y la combinación de vericiguat + iECA +BB + ARM logró una disminución de la mortalidad de cualquier causa en 51% (CR 0.49; IC95%: 0.39; 0.62). Respecto a la mortalidad cardiovascular ó la hospitalización por insuficiencia cardiaca la combinación de vericiguat + iRNA + BB + ARM se asoció a una disminución en 57% (CR 0.43; IC95%: 0.34; 0.55) y la combinación de vericiguat + iECA + BB + ARM logró una disminución de la mortalidad de cualquier causa en 46% (CR 0.54; IC95%: 0.43; 0.67)94.
Pregunta 25.1: ¿Cuáles son las recomendaciones actuales para el uso de digoxina en los pacientes con insuficiencia cardiaca?
Recomendación:
– La digoxina puede emplearse como adyuvante de la terapia fundamental para disminuir el riesgo de hospitalizaciones en pacientes con ICFEr que se encuentren en ritmo sinusal.
– La digoxina puede emplearse como parte de los medicamentos para el control de la frecuencia cardiaca en pacientes con ICFEr que presenten fibrilación auricular.
– La digoxina no debe considerarse como terapia de primera línea para el manejo de la insuficiencia cardiaca.
Nivel de evidencia 1, grado de recomendación B (recomendación condicionada a realizar estudios de investigación robustos).
Pregunta 25.2: ¿Cuáles son las precauciones que se deben tener en cuenta para el empleo seguro de la digoxina en el manejo de la insuficiencia cardiaca?
Recomendación:
– En todo paciente en quien se decida iniciar digoxina se deben considerar la función renal, las concentraciones de electrolitos séricos y el intervalo QTc en el electrocardiograma.
– Es importante mantener un monitoreo de la función renal, los electrolitos séricos y el electrocardiograma en todo paciente que reciba digoxina como parte del tratamiento de la insuficiencia cardiaca.
– Resulta deseable que se monitoricen los niveles séricos de digoxina, en particular en pacientes con alto riesgo de toxicidad por este fármaco.
Nivel de evidencia 1, grado de recomendación B (recomendación condicionada a realizar estudios de investigación robustos).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
La digoxina ha sido parte del armamento terapéutico en medicina desde hace más de 200 años, este fármaco tiene su mecanismo de acción basado en 3 mecanismos distintos: hemodinámico, neurohormonal y cronodepresor111. La digoxina inhibe la bomba Na+/K+-ATPasa, proteína de membrana que regula el flujo de sodio y potasio al interior de las células cardíacas. La inhibición de esta enzima provoca una mayor concentración intracelular de sodio, lo que se traducen en una mayor entrada de calcio en la célula e incremento de la contractilidad miocárdica. La digoxina endovenosa ha mostrado una mejoría a corto plazo en el gasto cardíaco, la fracción de eyección del ventrículo izquierdo (FEVI), la tolerancia al ejercicio y el consumo pico de oxígeno, en pacientes con insuficiencia cardiaca. Es importante recalcar, que todas esas funciones fisiológicas se presentan sin un incremento de la frecuencia cardíaca ni hipotensión arterial111.
Una RS publicada por Ziff et al.112 en 2015 tuvo el objetivo de evaluar la eficacia y seguridad de la digoxina en pacientes con enfermedades cardiovasculares. Los autores incluyeron 52 estudios clínicos, con 621,845 pacientes, con menor FEVI (33% vs. 42% controles), mayor incidencia de diabetes y con uso de medicamentos (diuréticos y antiarrítmicos). En comparación a los grupos control, el uso de digoxina mostró un mayor riesgo de muerte (CR 1.76, IC95%: 1.57; 1.97), sin embargo, en los análisis provenientes de ECAs se observó que no hay diferencias entre los grupos (CR 0.99; IC95% 0.93; 1.05). Los análisis de meta regresión demostraron que las diferencias en cuanto a la gravedad de la progresión de la enfermedad entre los grupos, fue determinante en la mortalidad mostrada. La conclusión de los autores fue que el uso de digoxina tuvo un efecto neutral en la mortalidad y una disminución en la admisión hospitalaria en estudios clínicos controlados112.
Una RS publicada por Vamos et al.113 en 2015 tuvo como objetivo revisar la evidencia disponible sobre el impacto de digoxina en la mortalidad en pacientes con insuficiencia cardiaca o con fibrilación auricular. Los autores incluyeron 19 estudios con 326,426 participantes. Los resultados del metaanálisis mostraron que la digoxina se asoció a un aumento del riesgo relativo de mortalidad por cualquier causa (CR 1.21; IC95%: 1.07; 1.38). En comparación a pacientes que recibieron glucósidos, la digoxina se asoció a un incremento del riesgo de mortalidad del 29% (CR 1.29; IC95% 1.21; 1.39) en pacientes con fibrilación auricular y en un 14% (CR 1.14; IC95%: 1.06; 1.22) en pacientes con insuficiencia cardiaca, por lo que los autores concluyen que el uso de doigoxina se asoció a un incremento de la mortalidad. Cabe recalcar, que solamente hay un estudio controlado (DIG trial) que evaluó la digoxina en pacientes con insuficiencia cardiaca y FEVI < 45% y ritmo sinusal. Los resultados de ese estudio no mostraron diferencia en la mortalidad (34.8% vs. 35.1%), aunque disminuyó discretamente el riesgo de hospitalización en el grupo con digoxina. Esto demuestra una falta de estudios clínicos controlados de alta calidad en pacientes con insuficiencia cardiaca113.
Las GPC AHA/ACC 2022 y las GPC ESC 2021 sugieren considerar el uso de digoxina en pacientes ICFEr sintomáticos en pacientes bajo terapéutica de primera línea recomendada por las guías o que no toleran esa terapéutica con el objetivo de disminuir hospitalizaciones en esos pacientes. Usualmente se recomienda iniciarse a dosis bajas ya que algunos reportes han asociado concentraciones séricas altas de digoxina con un aumento del riesgo de muerte y de EVC (enfermedad vascular cerebral) (> 1.2 ng/mL y > 1.6 ng/mL) y también se ha visto un detrimento clínico de los pacientes después de suspender el manejo con digoxina4. En especial, se debe de tener precaución el uso de digoxina en pacientes mayores de edad, síndrome de fragilidad, mujeres, hipocalemia y desnutrición5.
Pregunta 26: ¿Cuáles son la eficacia y la seguridad de otros agentes, como la trimetazidina, la coenzima Q10, la vitamina D y la carnitina, en los pacientes con insuficiencia cardiaca crónica?
Recomendación:
– En el momento actual no existe evidencia científica suficiente para recomendar el empleo de trimetazidina, coenzima Q10, vitamina D ni carnitina para disminuir el riesgo de muerte por causa cardiovascular ni los internamientos por causa cardiovascular o por insuficiencia cardiaca.
– Con el propósito de evitar la polifarmacia fútil no se puede recomendar el empleo de ninguno de estos agentes como parte del manejo de la insuficiencia cardiaca.
– En pacientes con insuficiencia cardiaca de origen isquémico que presenten angina, el uso de trimetazidina puede ser considerado como agente antianginoso.
L-Carnitina (nivel de evidencia 1, grado de recomendación B) (recomendación condicionada a realizar estudios de investigación robustos).
Coenzima Q10 (nivel de evidencia 1, grado de recomendación B) (recomendación condicionada a realizar estudios de investigación robustos).
Trimetazidina (nivel de evidencia 1++, grado de recomendación A) (recomendación fuerte).
Vitamina D (nivel de evidencia 1–, grado de recomendación B) (recomendación condicionada a realizar estudios de investigación robustos).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
Se han propuesto una gran cantidad de distintos fármacos y suplementos alimenticios para adicionar al tratamiento de la insuficiencia cardiaca, sin embargo, en general la evidencia es escasa y basada en estudios con pocos pacientes, diseños no controlados y desenlaces indirectos. Además, la falta de estandarización y la posibilidad de eventos adversos de muchos de los productos nutracéuticos sigue siendo motivo de preocupación4. Las GPC AHA/ACC 2022 establecen que existe una falta de evidencia respecto a la eficacia y seguridad de la vitamina D, tiamina, carnitina y la taurina; y una relación riesgo/beneficio posiblemente dañino en el caso de la vitamina E. Un estudio que evaluó la coenzima 10 (Q10) falló en demostrar difefrencias en sus desenlaces primarios (péptidos natriuréticos, mortalidad, cambio en la clase funcional NYHA), aunque se presentaron menos eventos cardiovasculres a los 2 años en el grupo con Q10. Sin embargo, el estudio mostró riesgos de sesgo importantes4.
Una RS publicada por Song et al.114 en 2017 evaluó el beneficio adicional de agregar L-Carnitina a la terapia en pacientes con insuficiencia cardiaca. Los autores incluyeron 17 ECAs con 1,625 pacientes, de los cuales, un número alto de estudios no reportaron adecuadamente la generación de la secuencia de aleatorización ni los métodos de cegamiento, además de sesgo de publicación. Por lo que la calidad de la evidencia fue calificada como moderada a baja. Los resultados mostraron que solamente 4 ECAs reportaron mortalidad de todas las causas y no encontraron diferencias entre grupos (RM 0.48; IC95%: 0.21; 1.06), 12 estudios mostraron diferencias a favor de L-Carnitina respecto a la mejoría de la clase funcional NYHA (al menos el cambio en 1 clase funcional) (RM 3.47; IC95%: 2.49; 4.82). Los estudios fallaron en demostrar una mejoría respecto a la tolerancia al ejercicio (6MW) (DMP [diferencia de medias ponderada] 45.41 minutos; IC95%: 14.46; 105.29 minutos). Aunque hubo una heterogeneidad alta, los metaanálisis mostraron una disminución de los péptidos natriuréticos (BNP y NT-proBNP) a favor del grupo con L-Carnitina en la disminución de BNP (DMP –124.60 pg/ml IC95%: –220.49; –28.71) y de NT-proBNP (DMP –510.36 pg/ml IC95%: –785.42; –235.30). Los análisis de subgrupos continuaron mostrando esas diferencias114. 12 ECAs evaluaron parámetros ecocardiográficos y se mostró en los metaanálisis una mejoría de la FEVI a favor del grupo con L-Carnitina (DMP 4.14%; IC95% 2.34; 5.93), así como otros parámetros114. No se reportaron diferencias significativas en cuanto a la incidencia de eventos adversos entre los grupos114.
Una RS publicada por Madmani et al.115 con la Colaboración Cochrane en 2021 para evaluar el beneficio de la Coenzima Q10 en pacientes con insuficiencia cardiaca. Los autores incluyeron 11 ECAs con 1,573 participantes, la mayoría con tamaños muestrales pequeños con heterogeneidad importante respecto a la dosificación, tiempo de seguimiento y desenlaces evaluados. La mayoría de los estudios mostraron alto o riesgo de sesgo no clarificado y solamente algunos de los desenlaces pudieron ser evaluados con metaanálisis. Los resultados mostraron que la coenzima Q10 se asoció a una disminución de la mortalidad de cualquier causa en comparación a placebo o control (RR 0.58; IC95% 0.35; 0.95), aunque el resultado fue derivado de 1 solo estudio con moderada calidad de la evidencia. También se observó una reducción del riesgo de hospitalización asociada a insuficiencia cardiaca (RR 0.62; IC95%: 0.49; 0.78) (2 estudios) con moderada calidad de la evidencia. Muy baja calidad de la evidencia asocia el tratamiento con coenzima Q10 con mejoría en la FEVI (DM 1.77: IC95% 0.09; 3.44) y no hubo resultados concluyentes respecto al aumento en la capacidad para el ejercicio. Tampoco hubo diferencia entre los grupos en la incidencia de eventos adversos (RR 0.70; IC95%: 0.45; 1.10) (2 estudios). La conclusión de los autores es que se requiere más estudios bien diseñados para evaluar la eficacia y seguridad del tratamiento con coenzima Q10 agregada al tratamiento convencional de la insuficiencia cardiaca115.
La trimetazidine inhibe la 3-cetoacil coenzima A tiolasa contribuye a preservar el metabolismo energético de las células expuestas a la hipoxia o isquemia, previene una disminución de las concentraciones de ATP intracelular, asegurando de esta manera el funcionamiento adecuado de las bombas iónicas y del flujo transmembranario de sodio-potasio, al mismo tiempo que se mantiene la homeostasis celular116. Una RS publicada por Zhao et al. en 2015 tuvo como objetivo evaluar el impacto de trimetazidina en el manejo de la insuficiencia cardiaca. Los autores incluyeron 16 estudios clínicos (2,004 participantes), 8 calificados con bajo riesgo de sesgo y 6 con moderado a alto riesgo de sesgo. La dosis de trimetazidina fueron en un rango de 60 a 140 mg/día de 0.5 a 24 meses de tratamiento. Los resultados del metaanálisis mostraron que el tratamiento con trimetazidina se asoció a un aumento en la duración del ejercicio (DMP 37.35 minutos; IC95%: 25.58; 49.13)116. Por su parte, Zhpu et al.117 condujeron una RS con metaanálisis e incluyeron 19 ECAs, de los cuales la mitad aproximadamente tuvieron una evaluacion de Jadad de 4, y el restante entre 1-3. La mayoría de los estudios reportaron el cambio en la FEVI, 8 el cambio en la clase funcional NYHA, 6 reportaron duración del ejercicio, 3 mortalidad y 4 hospitalizaciones. Los resultados de los metaanálisis mostraron que adicionar trimetazidina a la terapia convencional se asoció a una mejoría del FEVI (DMP 7.29%; IC95% 6.49: 8.09) y una disminución de los volúmenes telesistólico y telediastólico del ventrículo izquierdo (DMP –17.09mL; IC95% –20.15: –14.04) y (DMP –11.24mL; IC95% –14.06: –8.42), respectivamente. También se observó una mejoría en cuanto al cambio de la clase funcional NYHA en comparación a placebo (DMP –0.55; IC95% –0.81: –0.28), sin embargo, no se encontró diferencias en la duración del ejercicio (DMP 18.58 segundos; IC95% –6.88: –44.05) ni respecto a la mortalidad de cualquier causa (RR 0.47; IC95% 0.12; 1.78)117. Los valores de BNP y CRP también mostraron una disminución significativa en el grupo con trimetazidina en comparación a placebo (DMP –157.08 pg/mL; IC95% –176.55: –137.62) y (DMP –1.86 mg/L; IC95% –2.81: –0.90), respectivamente117.
Las GPC de ESC 2021 sugieren el uso de trimetazidina en pacientes ICFEr, especialmente pacientes con angina independientemente del tratamiento con BB o IVA5.
La vitamina D también se ha propuesto como un suplemento que pudiera ser benéfico en el tratamiento de la insuficiencia cardiaca crónica. Una RS publicada por Wang et al.118 en 2019, los autores incluyeron 10 ECAs, de los cuales la mayoría fueron calificados como con bajo o moderado riesgo de sesgo. Los resultados del metaanálisis mostraron que la terapia con vitamina D mejoró la HRQoL, pero falló en demostrar un beneficio en el cambio de los valores de BNP, NT-proBNP y la duración del ejercicio (6MWD)118.
Pregunta 27: ¿Cuáles son las recomendaciones y las limitantes para el empleo de antiarrítmicos en el manejo de los pacientes con insuficiencia cardiaca crónica?
Recomendación:
– La amiodarona puede ser considerada como el antiarrítmico de elección para intentar el control del ritmo en los pacientes con insuficiencia cardiaca con FEVI reducida que presenten fibrilación auricular.
– La amiodarona puede ser recomendada después de una cardioversión eléctrica exitosa para conservar el ritmo sinusal en pacientes con insuficiencia cardiaca con FEVI reducida.
– En pacientes con insuficiencia cardiaca con FEVI reducida se puede considerar el empleo de amiodarona para disminuir la recurrencia de arritmias ventriculares, y mejorar los síntomas y la función ventricular.
– Es recomendable vigilar periódicamente la función tiroidea, pulmonar y ocular en los pacientes que utilicen amiodarona en forma crónica.
– El uso de amiodarona no disminuye el riesgo de muerte súbita cardiaca en los pacientes con insuficiencia cardiaca con FEVI reducida.
– No existe suficiente evidencia científica para sustentar el uso de amiodarona para disminuir la morbimortalidad en los pacientes con insuficiencia cardiaca con FEVI preservada o ligeramente reducida.
– La propafenona, la flecainida, la disopiramida y el sotalol no deben ser recomendados para el manejo de la fibrilación auricular, debido a la falta de evidencia que sustente la seguridad de estos fármacos en los pacientes con insuficiencia cardiaca.
Nivel de evidencia 1, grado de recomendación B (recomendación condicionada a realizar estudios de investigación robustos).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
Las arritmias en pacientes con insuficiencia cardiaca constituyen un factor de riesgo importante asociado a morbilidad y mortalidad. Una proporción importante de las causas de hospitalización por insuficiencia cardiaca se deben a arritmias supraventriculares, como la fibrilación auricular, la cual constituye una causa importante de ECVA y tromboembolismo, y muchas veces tiene un curso silente hasta que se presentan las complicaciones119. Las arritmias ventriculares, a su vez, son causa de muerte súbita cardiaca; y, por último, las bradiarritmias también son comunes e incluyen la disfunción nodal, síndrome bradi-taquicardia y otras enfermedades de conducción. En general, el manejo farmacológico de la fibrilación auricular comprende dos estrategias, la primera involucra permitir que la fibrilación auricular persista, pero con un control de la frecuencia ventricular. La otra estrategia consiste en usar medicamentos antiarrítmicos en cardioversión y tratar de mantener un ritmo sinusal120. Los estudios clínicos han fallado en demostrar una superioridad muy clara de una estrategia sobre la otra en cuanto a mortalidad cardiovascular (27% en el grupo control vs. 25% en el grupo de ritmo). De igual manera los desenlaces secundarios como mortalidad por cualquier causa, empeoramiento de la insuficiencia cardiaca o EVC120. Los lineamientos fijados por la Sociedad Mexicana de Cardiología en 202219 sugieren, debido a que del 30 al 50% de los pacientes con insuficiencia cardiaca pueden presentar fibrilación auricular, es importante explorar de manera intencionada la presencia de fibrilación auricular en todos los pacientes con insuficiencia cardiaca. Con respecto al manejo de la frecuencia cardiaca, es de mayor valor reestablecer el ritmo sinusal que el control de la frecuencia, por sí misma. En este caso, los medicamentos antiarrítmicos son la primera línea de tratamiento, como la amiodarona, como la opción preferible para el restablecimiento del ritmo19. La fibrilación auricular se clasifica en paroxística (episodios autolimitados de < 7 días de duración), persistente (episodios no autolimitados que duran 7 días y hasta 6 meses), persistentes de largo plazo (duración de más de 1 año) y permanentes (refractarios al tratamiento)119.
Una revisión publicada por Reddy et al.121 en 2022 hace recomendaciones sobre el manejo farmacológico de la fibrilación auricular. Los BB son medicamentos usados ampliamente en pacientes ICFEr y se han asociado a una reducción de la mortalidad en alrededor del 35%, sin embargo, una RS publicada recientemente121 que analizó 18,254 participantes demostró que la reducción de la mortalidad y la disminución de las hospitalizaciones solamente se observó en pacientes con ritmo sinusal, y no así, en pacientes con fibrilación auricular. Sin embargo, algunas limitantes del análisis fue que los pacientes no fueron catalogados dentro de los distintos fenotipos de fibrilación auricular. Se observó además una disminución del riesgo de desarrollar fibrilación auricular durante el tiempo de seguimiento de los estudios en los pacientes con BB (33% menor riesgo)121. Todo esto parece indicar que la falta de eficacia de los BB se mostró predominantemente en los pacientes con fibrilación auricular permanente, no así en los paroxísticos. Algunos estudios han mostrado que los BB son igualmente eficaces a dosis bajas o altas en el control de la frecuencia cardiaca. Sin embargo, no hay estudios clínicos controlados para evaluar los BB en fibrilación auricular permanente. La conclusión es que es deseable optimizar la dosis de BB a la dosis máxima recomendada en pacientes con fibrilación auricular paroxística o ritmo sinusal y ajustar la dosis de BB menos agresivamente en pacientes con fibrilación auricular permanente121.
La digoxina tiene la ventaja de disminuir la actividad del nodo auriculoventricular sin tener efectos inotrópicos negativos, y es una opción en pacientes en los cuales los BB no son bien tolerados. Los estudios con digoxina han demostrado disminuir el riesgo de hospitalización, pero no tienen efecto en la mortalidad. Algunos estudios llevados a cabo en pacientes ICFEr avanzada con fibrilación auricular refractaria al tratamiento tuvieron pobres desenlaces. Sin embargo, el estudio RATE-AF-Trial mostró en pacientes con ICFEr y fibrilación auricular permanente que el tratamiento con digoxina fue seguro y en algunos casos tuvo mejor eficacia que el BB121.
El tratamiento con iECA y BRA disminuyen la incidencia de fibrilación auricular, posiblemente como resultado de la disminución de la remodelación ventricular. Sucubitrilo/valsartán tiene mayor eficacia sobre los iECA y BRA y es el manejo de elección en los pacientes ICFEr sin importar el estado basal de la fibrilación auricular121.
Los iSGLT-2 tienen efecto benéfico en pacientes ICFEr sin importar el estado de fibrilación auricular, mejorando síntomas, hospitalización y mortalidad, sin embargo, no disminuyen la incidencia de fibrilación auricular mostrado en el análisis del estudio DAPA HF pero si en una RS con iSGLT-2 sin importar en el fenotipo de insuficiencia cardiaca121.
La anticoagulación en pacientes con fibrilación auricular disminuye la incidencia de EVC en alrededor de 2/3, sin embargo, con un mayor riesgo de sangrado. La warfarina o dosis bajas de rivaroxabán han mostrado disminución del riesgo de EVC por lo que no se pudo demostrar beneficio en pacientes con ritmo sinusal. El uso de aspirina ha mostrado ser deletérea en pacientes con ICFEr y no deben de ser combinados en el uso de otros anticoagulantes121.
Para el control farmacológico del ritmo cardiaco, un estudio clínico controlado evaluó amiodarona como medicamento para el control del ritmo, que mostró ser más eficaz en lograr ritmo sinusal comparado a control de la frecuencia cardiaca (la fibrilación auricular disminuyó de 54% en el estado basal a 27% a 4 años comparado con ningún cambio en los pacientes bajo control de la frecuencia cardiaca. A pesar del control del ritmo cardiaco, no hubo diferencia en la mortalidad, hospitalización ni en la clase funcional NYHA. El manejo farmacológico para el control del ritmo se asoció con mayor hospitalización por fibrilación auricular y bradicardia y 6 veces mayor riesgo de cardioversión. Este estudio sugiere que el tratamiento farmacológico de control del ritmo no debería ser la primera línea de tratamiento en pacientes ICFEr y fibrilación auricular secundaria. Una RS no demostró mejoría en las hospitalizaciones asociadas a insuficiencia cardiaca o en la mortalidad con el manejo farmacológico del control del ritmo cardiaco121.
Una RS publicada por Zaki et al.120 tuvo como objetivo evaluar la eficacia de amiodarona en comparación a digoxina. Los autores incluyeron 7 estudios clínicos y los resultados del metaanálisis mostraron en el desenlace de frecuencia cardiaca que la amiodarona mostró un mejor efecto que la digoxina, sin embargo, la reducción en la frecuencia cardiaca en pacientes con fibrilación ventricular no mostró diferencias (DM –5.44; IC95%: -9.53; –1.34). Por otro lado, la digoxina mostró una disminución en la mortalidad de cualquier causa comparada con amiodarona (RM 2.01; IC95%: 1.18; 3.41). No hubo una diferencia en la incidencia de eventos adversos entre el grupo con amiodarona y digoxina. El análisis de los autores mostró que el 70% (amiodarona) y 68% (digoxina) lograron un adecuado control de la frecuencia cardiaca. Las conclusiones de los autores son que la amiodarona puede ser usada como primera línea de tratamiento en cardioversión a ritmo sinusal en pacientes con fibrilación auricular120.
La muerte súbita cardiaca es un desenlace fatal que se presenta en los pacientes de insuficiencia cardiaca, sobre todo en pacientes con una FEVI < 35%, al generarse mecanismos fisiopatológicos que provocan isquemia miocárdica, prolongación del intervalo QTc, desequilibrio hidroelectrolítico, entre otros2. El consenso mexicano sobre insuficiencia cardiaca sugiere que la combinación de sacubitrilo/valsartán en combinación con BB y agentes antialdosterónicos reducen el riesgo de muerte súbita cardiaca.
Una RS publicada en 2018 por Al-Gobari et al. evaluó la eficacia de las distintas alternativas farmacológicas para disminuir el riesgo de muerte súbita cardiaca en pacientes ICFEr. Los autores incluyeron 41 revisiones de la literatura y los metaanálisis mostraron que distintas clases terapéuticas disminuyen la muerte súbita cardiaca. Los BB disminuyen la incidencia de muerte súbita cardiaca (RM 0.69; IC95%: 0.62; 0.77), los ARM también disminuyen el riesgo (RR 0.81; IC95% 0.67; 0.98), BRA/neprisilina (RR 0.81; IC95%: 0.69; 0.95). Donde la evidencia no fue tan clara, el uso de amiodarona mostró una disminución del riesgo de muerte súbita cardiaca pero no de muerte por cualquier causa, con una baja calidad de la evidencia. Los iECA, los BRA y las estatinas no mostraron una disminución del riesgo de muerte súbita cardiaca122.
Pregunta 28: ¿Cuáles son los esquemas de dosificación y titulación de los fármacos modificadores de la enfermedad en los pacientes con insuficiencia cardiaca crónica?
Recomendación:
– El tratamiento óptimo de la insuficiencia cardiaca debe considerarse desde una visión cualitativa y cuantitativa.
– Siempre que sea posible, se deben titular los medicamentos a las dosis máximas toleradas por los pacientes.
– Es recomendable utilizar la propuesta del primer posicionamiento mexicano en insuficiencia cardiaca para la titulación de dosis de INRA, IECA, BRA y BB.
– Los iSGLT2 (dapagliflozina, empagliflozina) no requieren titulación de dosis para el manejo de la insuficiencia cardiaca.
Nivel de evidencia 1+, grado de recomendación A (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
La mayoría de los estudios clínicos en fármacos de primera línea para el manejo de pacientes ICFEr establecen el manejo inicial a dosis bajas. Si el paciente tolera adecuadamente el medicamento a dosis bajas, el protocolo establece un aumento en la titulación de la dosis ("uptitration") para alcanzar una meta establecida. Incluso, aunque haya una adecuada respuesta, el protocolo establece necesario alcanzar la dosis establecida. Debido a ello y a que, la eficacia de las distintas clases terapéuticas se ha establecido a esas dosis, es importante llegar a las dosis clínicamente recomendadas. No hay evidencia que demuestre que dosis inferiores en pacientes que no toleraron las dosis altas pueden brindar beneficios equiparables4 (Fig. 6 y 7).
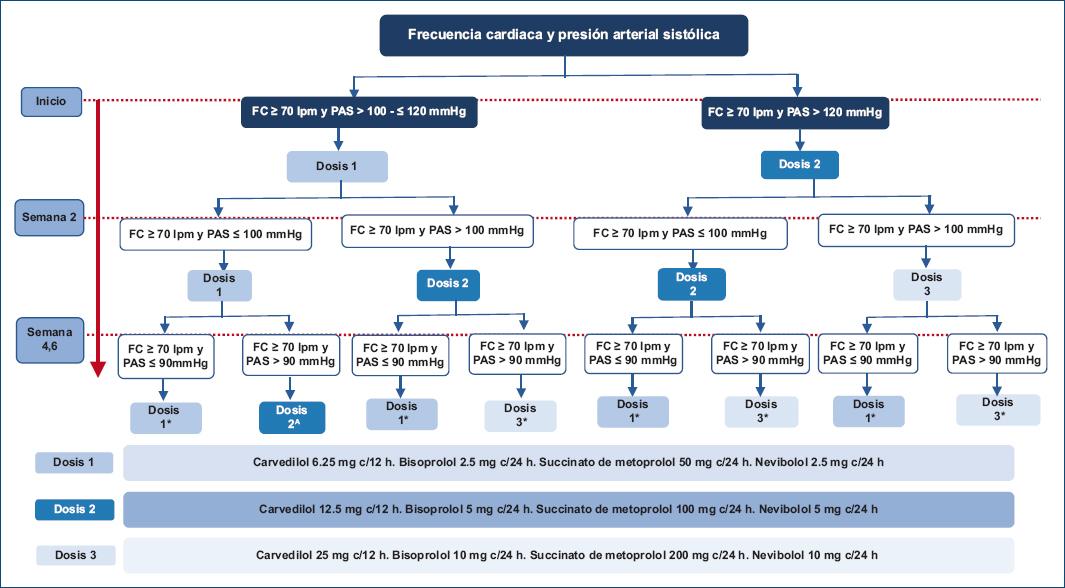
Figura 6 Titulación y optimización de dosis de betabloqueadores de acuerdo con las cifras de presión arterial sistólica (PAS) y de frecuencia cardiaca (FC) (modificada con permiso de: Magaña S, Cigarroa L, Chávez M, Rayo C, Galvan O, Aguilera M. First Mexican statement in heart failure. Cardiovasc Metab Sci. 2021;32(Suppl 1):s8-s85).
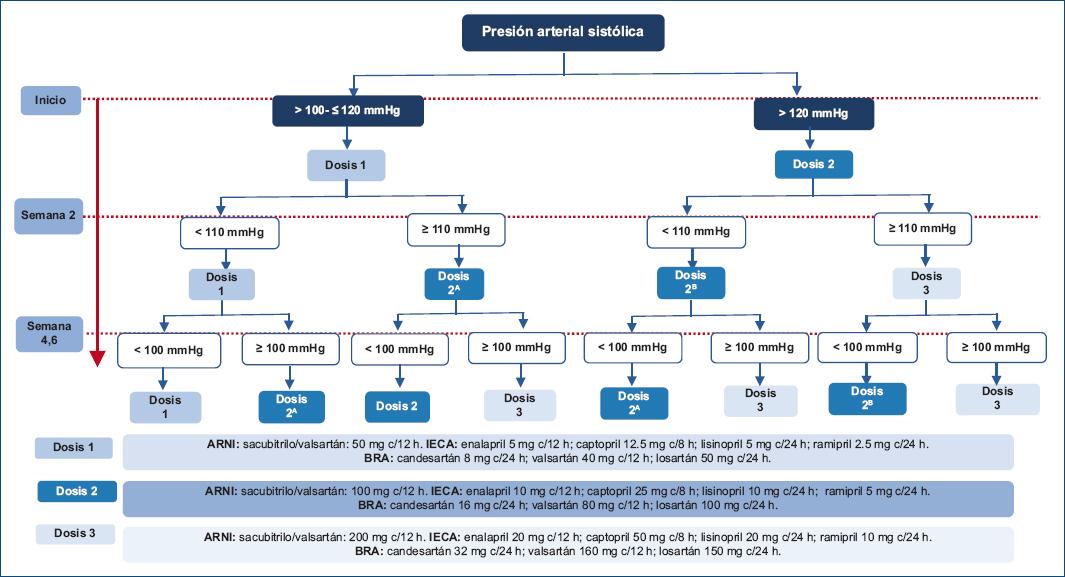
Figura 7 Titulación y optimización de dosis de antagonistas del sistema renina-angiotensina (ARNI) según las cifras de presión arterial sistólica basales (modificado con permiso de: Magaña S, Cigarroa L, Chávez M, Rayo C, Galvan O, Aguilera M. First Mexican statement in Heart Failure. Cardiovasc Metab Sci. 2021;32(Suppl 1):s8-s85).
Las GPC AHA/ACC 2022 recomiendan iniciar las dosis de estos medicamentos de control a dosis bajas, e ir incrementando la dosis conforme el paciente vaya tolerando adecuadamente hasta alcanzar las dosis clínicamente recomendadas. Es importante que los médicos se esfuercen por alcanzar y mantener esas dosificaciones. Es importante que los pacientes se mantengan vigilados de su frecuencia cardiaca, presión arterial, función renal, equilibrio hidroelectrolítico y síntomas, especialmente en este periodo de incremento de la dosis. Los BB, por ejemplo, proveen una respuesta dosis dependiente en cuanto a los valores de FEVI, reducción del riesgo de hospitalización y reducción de la mortalidad por cualquier causa. La frecuencia e intensidad de la titulación de los distintos medicamentos debe de individualizarse en cada paciente4.
Las GPC ESC 2021 por su parte, recomiendan en todos los pacientes ICFEr el seguimiento estrecho en intervalos no mayores a 6 meses, para revisar síntomas, signos vitales, resultados de laboratorios y la función renal, aquellos pacientes en los cuales se está incrementando la posología, el intervalo de visitas al consultorio debe ser menor. La realización de ecocardiograma seriado no es necesaria en pacientes estables, sin embargo, es importante llevarlo a cabo cuando el paciente muestra datos de progreso de la enfermedad. Estos lineamientos también recomiendan llevar a cabo un ecocardiograma dentro de 3 a 6 meses de haber llegado a las dosis óptimas después del periodo de "uptitration"5.
El consenso mexicano sobre insuficiencia cardiaca 20212 propone el concepto de lograr el Tratamiento Médico Óptimo cuando la combinación de medicamentos logra que el paciente permanezca libre de síntomas y con una mejoría de la FEVI. La combinación de medicamentos modificadores de la enfermedad considera triple terapia neuroendócrina con antagonistas del SRA, BB y ARM, sin embargo, se pueden agregar algunas alternativas como iSGLT-2, IVA, digoxina, nitratos, hidralazina. En estos lineamientos consideran un incremento de al menos 10% de la FEVI y alcanzar > 40% para considerar una "mejoría en la FEVI"19. Con la finalidad de lograr la dosis óptima es deseable establecer esquemas estructurados para las dosis de inicio y para continuar el incremento de la posología hasta lograr la dosis óptima recomendada2.
Pregunta 29: ¿Cuáles son la eficacia y la seguridad de los desfibriladores automáticos implantables (DAI) para el manejo de las arritmias en los pacientes con insuficiencia cardiaca crónica?
Recomendación:
-
– Debe implantarse un DAI para la prevención secundaria de la muerte súbita y de la taquicardia/fibrilación ventricular rescatada de causa no reversible en pacientes con expectativa de vida > 1 año, ya que reduce de manera significativa la mortalidad.
-
– Debe implantarse un DAI para la prevención primaria de la muerte súbita en pacientes con insuficiencia cardiaca con FEVI reducida (≤ 35%), en clase funcional II-III de la NYHA, con tratamiento médico óptimo por al menos 3 meses y con una expectativa de vida > 1 año, ya que reduce de manera significativa la mortalidad.
-
– Puede considerarse implantar un DAI en presencia de insuficiencia cardiaca con FEVI < 30% en clase funcional I de la NYHA a pesar de recibir tratamiento médico óptimo, en pacientes con una expectativa de vida > 1 año.
-
– Siempre que se considere un implante de DAI deberá evaluarse la necesidad de implantar un resincronizador asociado.
-
– Puede considerarse un DAI subcutáneo como alternativa cuando no existe indicación de estimulación cardiaca.
-
– Debe estratificarse de manera temprana todo paciente posterior a un IAM para definir si es candidato a DAI.
-
– Debe realizarse un estudio electrofisiológico para intentar la inducción de arritmias ventriculares y en caso de ser así deberá implantarse un DAI en pacientes con FEVI intermedia (35-40%) y síncope inexplicable por métodos de estudio no invasivos.
-
– Debe optimizarse la programación del DAI por personal capacitado debido a su impacto en la morbimortalidad, con los objetivos de disminuir las descargas inapropiadas, alargar los periodos de detección de taquicardia ventricular, minimizar en lo posible la estimulación ventricular innecesaria, favorecer la adecuada detección de taquicardias supraventriculares, la detección oportuna de fallas en el sistema y definir la mejor estrategia de estimulación antitaquicardia.
-
– No debe implantarse un DAI en caso de no tener controlados los episodios de arritmia ventricular.
-
– Debe realizarse ablación de taquicardias supraventriculares, incluida la fibrilación auricular, para evitar descargas inapropiadas.
-
– Debe realizarse ablación en los pacientes con insuficiencia cardiaca y fibrilación auricular como método de control de ritmo, por encima de los antiarrítmicos, al disminuir la mortalidad y las hospitalizaciones por insuficiencia cardiaca o empeoramiento de esta, aun en insuficiencia cardiaca avanzada. En presencia de taquicardiomiopatía es una indicación absoluta.
-
– Debe realizarse ablación de taquicardia ventricular recurrente a pesar del uso crónico de amiodarona, ya que es superior al escalamiento de antiarrítmicos.
-
– Considerar la ablación de taquicardia ventricular antes o posterior al implante de DAI para la prevención de episodios de arritmias ventriculares y choques, sin que la ablación sustituya el DAI en caso de cardiopatías no corregibles.
-
– Considerar la ablación de extrasístoles ventriculares que sirven de desencadenante de episodios de taquicardia/fibrilación ventricular como método preventivo.
REVISIÓN DE LA LITERATURA Y ANÁLISIS
Está muy bien demostrado que los pacientes con ICFEr avanzada tienen un riesgo incrementado de muerte por arritmias ventriculares y muerte cardiaca súbita. Derivado de los estudios clínicos publicados hace más de dos décadas que demostraron que el uso de desfibrilador automático implantable (DAI) disminuye la mortalidad en comparación a la terapia médica estándar, las GPC actuales recomiendan su eso en pacientes seleccionados. El primer DAI fue diseñado por el profesor Mirowski en 1967 y su uso se extendió en la década de los 80s y 90s. Los primeros dispositivos algo rudimentarios administraban descargas eléctricas. Los más actuales son dispositivos pequeños que funcionan como antibradicardia (marcapasos) y antitaquicardia, incluido el desfibrilador. Esto como resultado de la generación de pequeños pulsos de bajo voltaje, sin embargo, la función antitaquicardia genera pulsos de mayor voltaje (choques) que pueden ser percibidas por el paciente e incluso ser dolorosas123.
Las GPC AHA/ACC 2022 hacen énfasis en que los estudios pivote que se realizaron hace más de dos décadas para evaluar la efectividad de los DAI son poco probable que sean repetidos, por su complejidad. Inicialmente los DAI fueron evaluados en pacientes con paro cardiaco y en los cuales se demostró un beneficio palpable. Posteriormente, estos dispositivos mostraron beneficio en otras poblaciones en riesgo de muerte cardiaca súbita. Estos lineamientos recomiendan considerar en pacientes con enfermedad isquémica cardiaca al menos 40 días post infarto con un FEVI < 35% y NYHA II/III con expectativa razonable de vida de al menos 1 año, la colocación de un DAI para prevenir la muerte cardiaca súbita. Un DAI es una alternativa valiosa en los pacientes con alto riesgo de presentar arritmia ventricular. También se recomienda en pacientes al menos con 40 días post infarto con un FEVI < 30% y NYHA I con expectativa razonable de vida de al menos 1 año y en terapia médica óptima, la colocación de un DAI para prevenir primariamente la muerte cardiaca súbita. Para pacientes con FEVI < 35%, ritmo sinusal, bloqueo de rama izquierda con una duración del QRS > 150 ms y NYHA II, III o IV en terapia médica óptima, la terapia cardiaca de resincronización (TCR) está indicada para reducir la mortalidad total, disminuir hospitalizaciones y mejorar síntomas y HRQoL.
Una RS publicada por Woods et al. en 2015 tuvo como objetivo evaluar la evidencia científica sobre la eficacia y seguridad de los dispositivos implantables, entre ellos el DAI, para informar al Instituto de Excelencia Clínica de Gran Bretaña para el desarrollo de sus lineamientos124. Los autores desarrollaron un "metaanálisis en red" en donde identificaron 22 estudios clínicos, de los cuales 13 aportaron información para hacer un análisis a nivel de los pacientes individuales. Se aleatorizaron 13,350 pacientes. El desenlace primario fue la disminución del riesgo de mortalidad por cualquier causa. Las características de los pacientes mostraron que los pacientes que fueron incluidos para colocarles un TCR-P o TCR-D mostraban duración del QRS prolongados y habitualmente mostraban bloqueo de rama izquierda en comparación a aquellos que recibieron terapia médica óptima o DAI. La mayoría de los pacientes fueron NYHA II o III y con FEVI < 35%124. Los autores realizaron un modelo multivariado para determinar las asociaciones de los distintos dispositivos con el desenlace y como las características de los pacientes influyen en las mismas. Los resultados mostraron que a una menor FEVI se incrementó la eficacia de los TRC-D pero disminuyó la eficacia de los TRC-P y DAI. Los resultados finales mostraron que en todos los subgrupos de pacientes (FEVI < 35% y QRS > 120 ms) el TRC-D se asoció a una disminución de la mortalidad, con un rango de 28% (CR 0.72; IC95% 0.51; 1.01) a 53% (CR 0.47; IC95% 0.34; 0.66) entre los distintos subgrupos. CRT-D es más efectivo en los pacientes con QRS > 150 ms y bloqueo de rama izquierda. Respecto a DAI, el beneficio en la mortalidad es mayor en hombres, y menos aparente en pacientes de mayor edad. En todos los grupos de hombres, el beneficio fue de 24 a 48% en la disminución del riesgo relativo de muerte, sin embargo, en las mujeres el beneficio fue menos evidente y en 9 de 10 subgrupos no hubo diferencia estadísticamente significativa124. No hubo evidencia de que la clase NYHA sea un factor diferenciador en la respuesta, así como la etiología de la FEVI disminuida. Las conclusiones de esta revisión son que tanto los DAI, como los TRC-P y TRC-D reducen la mortalidad por cualquier causa comparados con la terapia médica óptima sola. El metaanálisis y la meta-regresión mostraron que los pacientes con QRS > 150 ms, bloqueo de rama izquierda y de sexo femenino se beneficiaron más de TRC-P y TRC-D, y aquellos hombres de < 60 años se beneficiaron más de la DAI. El dispositivo TRC-D fue el más efectivo de los tratamientos si no se consideran características de los pacientes con una reducción relativa de la mortalidad del 42% (IC95% 32; 50%), seguido del DAI 29% (IC95% 20-37%) y el TRC-P del 28% (15-40%)124.
Una RS publicada por Friedman et al.125 tuvo como objetivo determinar si la decisión de colocar un DAI de acuerdo con la clase funcional NYHA se asociaba a una diferencia en la mortalidad. Los autores incluyeron 4 ECAs con 2,763 pacientes (68% NYHA II y 52% recibieron un DAI). En un análisis multivariado se determinó que la colocación de un DAI en pacientes NYHA II disminuyó el riesgo relativo de muerte en 45% (CR 0.55; IC95% 0.35; 0.85), mientras que no se pudo observar una disminución del riesgo de muerte en clase funcional NYHA III (CR 0.76; IC95% 0.48; 1.24)125.
Una RS publicada por Bazoukis et al.126 evaluaron el impacto de la terapia DAI en la mortalidad. Los pacientes que reciben la colocación de un DAI pueden recibir tratamiento apropiado ("shock" o marcapaso anti-taquicardia como resultado de una arritmia fatal como la fibrilación o la taquicardia ventriculares). Sin embargo, algunos factores como las arritmias auriculares o errores de detección pueden provocar activación del DAI inapropiada. La frecuencia de "shocks" apropiados es de 10-20% en comparación a 20-70% de "shocks" inapropiados126. Los autores incluyeron 17 estudios clínicos (21,764 pacientes) en los cuales se informaron la ocurrencia de "shocks" apropiados o inapropiados. Los resultados del metaanálisis mostraron que las intervenciones DAI apropiadas ("shocks" o marcapasos anti-taquicardia) se asoció a un incremento del riesgo de mortalidad por cualquier causa (CR 2.00; IC95%: 1.52; 2.63) así como los "shocks" inapropiados (CR 1.30; IC95% 1.07; 1.58)126. El monitoreo remoto de los DAI provee la habilidad de colectar información valiosa acerca de la función cardiaca y el ritmo. El monitoreo informa sobre el ritmo cardiaco en reposo, la actividad física de pacientes, variabilidad del ritmo cardiaco, intensidad de los ruidos cardiacos e impedancia intratorácica. Una RS publicada en 2022 por McGee et al.127 tuvo como objetivo evaluar las tecnologías de monitoreo cardiaco y los autores incluyeron 11 estudios clínicos. Los resultados del metaanálisis mostraron que no hubo diferencias en la mortalidad (8 estudios) (RR 1.02; IC95%: 0.85; 1.23) ni en la re-hospitalización por insuficiencia cardiaca (RR 1.07; IC95% 0.97; 1.20), por lo que la conclusión de los autores es que todavía no hay suficiente evidencia para demostrar un claro beneficio del monitoreo remoto en estos pacientes127.
En pacientes con insuficiencia cardiaca avanzada, el trasplante cardiaco sería la opción ideal, pero desafortunadamente la accesibilidad sigue siendo una gran barrera para el tratamiento de estos casos y el trasplante cardiaco es una opción muy limitada que se reserva sólo a pacientes con IC avanzada128. La asistencia mecánica circulatoria, particularmente la de dispositivos de asistencia ventricular izquierda (DAVI) implantables de forma permanente, están siendo una alternativa importante para estos casos. Se ha calculado que la supervivencia a un año de estos pacientes presenta un rango de 56 a 87% y de alrededor de 47% a 4 años. La muerte cardiaca súbita y las arritmias pueden presentarse en estos pacientes128. Una RS publicada por Vakil et al. en 2016 evaluó la efectividad de los DAI en pacientes con DAVI e incluyeron 6 estudios observacionales (937 pacientes). Los pacientes tenían en promedio 53 años y el 80% eran del sexo masculino. Se encontró un flujo continuo en el 39% de los pacientes y un FEVI promedio de 16 ± 6%. En un periodo de seguimiento de 7 meses, murieron 241 pacientes (26% de los cuales 16% tenían DAI vs. 32% en los pacientes control). El uso de un DAI se asoció a una reducción relativa de 39% de la mortalidad por cualquier causa. (RR 0.61; IC95%: 046; 0.82). Este beneficio no se observó en pacientes DAVI con flujo continuo128.
Otra RS publicada por Paschallis et al.129 en 2021 tuvo como objetivo revisar la evidencia científica de la efectividad de la terapia combinada con un DAI y con DAVI con flujo continuo. Los autores incluyeron 10 estudios con 7,074 pacientes. La causa de insuficiencia cardiaca fue cardiomiopatía isquémica en 47.6% de los pacientes y el promedio de edad de los pacientes 54.7% años y 73.1% fueron del sexo masculino. Los resultados del metaanálisis mostraron que la incorporación de un DAI no se asoció a una disminución de la mortalidad (RM 0.85; IC95% 0.64; 1.12), aunque cuando el análisis se ajustó al retirar el estudio INTERMACS (Registro para el Apoyo Circulatorio Mecánico Asistido)129 si se pudo observar una disminución del riesgo relativo de muerte (RM 0.77; IC95% 0.6; 0.99). Cuando se sub estratificaron los pacientes de estudios realizados en EE.UU. se observó un incremento de la mortalidad con DAI (RM 1.2; IC95% 1.02; 1.33) y una disminución en los estudios europeos (RM 0.58; IC95%: 0.4; 0.83). El uso de DAI no se asoció a riesgo de insuficiencia cardiaca derecha (RM 1.17; IC95% 0.74; 1.83), o a infección mayor (RM 1.43; IC95% 0.93; 2.2)129.
Pregunta 30: ¿Cuáles son la eficacia y la seguridad de la terapia de resincronización cardiaca en los pacientes con insuficiencia cardiaca crónica?
Recomendación:
-
– Debe implantarse un TRC en pacientes con insuficiencia cardiaca con FEVI ≤ 35%, en ritmo sinusal, en clase funcional II-III de la NYHA, con QRS ancho ≥ 150 ms y bloqueo de rama izquierda con tratamiento médico óptimo por al menos 3 meses y con una expectativa de vida > 1 año, ya que reduce de manera significativa la morbimortalidad y las hospitalizaciones por insuficiencia cardiaca, y mejora la función cardiaca y la CVRS.
-
– Considerar implantar un TRC en los pacientes con insuficiencia cardiaca con FEVI ≤ 35%, en ritmo sinusal, en clase funcional II-III de la NYHA, con QRS ancho de 130-149 ms y bloqueo de rama izquierda con tratamiento médico óptimo por al menos 3 meses y con una expectativa de vida > 1 año, ya que reduce de manera significativa la mortalidad y las hospitalizaciones por insuficiencia cardiaca, y mejora la CVRS.
-
– Considerar implantar un TRC en pacientes con insuficiencia cardiaca con FEVI ≤ 35%, en ritmo sinusal, en clase funcional II-III de la NYHA, con QRS ancho ≥ 150 ms y no bloqueo de rama izquierda con tratamiento médico óptimo por al menos 3 meses y con una expectativa de vida > 1 año, ya que reduce de manera significativa la morbimortalidad y las hospitalizaciones por insuficiencia cardiaca, y mejora la función cardiaca y la CVRS.
-
– Puede considerarse implantar un TRC en pacientes con insuficiencia cardiaca con FEVI ≤ 35%, en ritmo sinusal, en clase funcional II-III de la NYHA, con QRS ancho de 130-149 ms y no bloqueo de rama izquierda con tratamiento médico óptimo por al menos 3 meses y con una expectativa de vida > 1 año.
-
– Puede considerarse implantar un TRC en pacientes con insuficiencia cardiaca con fracción de expulsión reducida (FEVI ≤ 30%), en ritmo sinusal, en clase funcional I de la NYHA, con QRS ancho ≥ 150 ms y bloqueo de rama izquierda con tratamiento médico óptimo por al menos 3 meses y con una expectativa de vida > 1 año, ya que reduce el empeoramiento de la insuficiencia cardiaca y mejora la función cardiaca.
-
– Siempre que se considere un implante de TRC deberá evaluarse la necesidad de un DAI asociado.
-
– Puede considerarse implantar un TRC en pacientes candidatos a recibirlo y en ritmo de fibrilación auricular no candidatos al control del ritmo, y debe mantenerse una estimulación biventricular > 90-95%.
-
– Debe realizarse ablación del nodo auriculoventricular en pacientes con fibrilación auricular y TRC en caso de no tener > 90-95% de estimulación biventricular por no lograr un adecuado control de la frecuencia cardiaca.
-
– Debe realizarse ablación del nodo auriculoventricular e implante de TRC en pacientes con insuficiencia cardiaca con FEVI < 40% y fibrilación auricular no candidatos a control del ritmo en los cuales no se logra un control adecuado de la frecuencia cardiaca.
-
– Puede considerarse ablación del nodo auriculoventricular e implante de TRC en pacientes con insuficiencia cardiaca con FEVI del 40-49% y fibrilación auricular no candidatos a control del ritmo en los cuales no se logra un control adecuado de la frecuencia cardiaca.
-
– Puede considerarse la estimulación del sistema de conducción, sea del haz de His o del área de la rama izquierda, como una alternativa en pacientes candidatos a TRC o cuando esta no resulta efectiva o no es posible.
-
– Debe implantarse un TRC o realizar estimulación del sistema de conducción en los pacientes con cardiomiopatía inducida por marcapasos.
-
– Puede considerarse, con FEVI > 35%, realizar estimulación del sistema de conducción en pacientes con riesgo de desarrollar cardiomioparía inducida por marcapasos y con una expectativa de estimulación ventricular > 20%, con el fin de prevenir una insuficiencia cardiaca secundaria. En caso de bloqueo de rama izquierda también puede considerarse TRC.
-
– Debe valorarse la FEVI de manera periódica en pacientes con alto porcentaje de estimulación ventricular que no es posible disminuir con una adecuada programación.
REVISIÓN DE LA LITERATURA Y ANÁLISIS
La terapia de resincronización cardiaca (TRC) fue conceptualizada en la década de los 90s por el Dr. Mower al utilizar un marcapaso biventricular para mejorar la función cardiaca, mejorar la capacidad funcional y la supervivencia. El desarrollo tecnológico de los dispositivos TRC ha pasado por la emergencia de varias generaciones. La primera generación que consistía en la estimulación biventricular, con un estimulador guía en ventrículo izquierdo y sin programación de intervalo V-V, resultaba a menudo en una captura anodal en ventrículo derecho. Un incremento del estímulo del ventrículo izquierdo resultaba en un patrón de activación ventricular dominado por el ventrículo derecho. Esto en muchas ocasiones derivaba de una afectación miocárdica del ventrículo izquierdo130. La segunda generación se componía de estimuladores bipolar en ventrículo izquierdo, y la posibilidad de programación del intervalo V-V. Esta generación de TRC disminuyó la frecuencia de captura anodal del ventrículo derecho y la programación del intervalo V-V permitió una disminución de la propagación del impulso miocárdico130. La tercera generación de dispositivos TRC consistió en una optimización de los intervalos AV y VV usando un electrocardiograma de 12 canales para lograr un máximo de estrechamiento y positividad del complejo QRS para lograr una despolarización óptima y poder fusionarla con el QRS espontáneo. Estos TRC adaptativos se adaptan continuamente al sensor y marcapaso del intervalo AV para ajustarse a las variaciones del intervalo AV intrínseco130. Los dispositivos de 4ª generación utilizan un dispositivo cuadripolar hacia ventrículo izquierdo con estimulación de sitios múltiples. La estimulación utilizando múltiples puntos en el VD o VI ha demostrado que marcapasos de sitios múltiples es posible y esta mejora la FEVI y el volumen telesistólico del ventrículo izquierdo130.
Las GPC AHA/ACC y ESC hacen énfasis en que los dispositivos TRC se han desarrollado como una terapia altamente efectiva en pacientes con ICFEr y bloqueo de LBBB, en algunas subpoblaciones de pacientes no han podido demostrar una respuesta significativa. Esto derivado de la baja capacidad de estimular el tejido enfermo y la dificultad de reclutar el sistema de conducción especializado a través de la estimulación epicárdica.
Las indicaciones actuales derivadas de estos lineamientos para los dispositivos TRC son pacientes con FEVI < 35%, ritmo sinusal, bloqueo de rama izquierda con una duración de QRS > 150 ms y NYHA clase II, III o pacientes ambulatorios IV en terapia médica óptima. En los pacientes con esas mismas características, pero sin bloqueo de rama izquierda también es una posibilidad terapéutica. En los pacientes con bloqueo cardiaco completo o de alto grado y FEVI 36 a 50%, la terapia TRC es una terapia razonable. En pacientes con FEVI < 35%, ritmo sinusal, bloqueo de rama izquierda con una duración de QRS de 120 a 149 ms y NYHA clase II, III o pacientes ambulatorios IV en terapia médica óptima la terapia TRC es una terapia razonable. En pacientes con fibrilación auricular y FEVI < 35% en terapia médica óptima los dispositivos TRC han demostrado beneficios en mortalidad, mejoría de síntomas y de HRQoL. Otros pacientes candidatos son aquellos en los que no tienen un bloqueo de rama izquierda o que tienen una causa isquémica de ICFEr4,5.
Woods et al. demostraron en su RS con "metaanálisis en red" que a una menor FEVI se incrementó la eficacia de los TRC-D pero disminuyó la eficacia de los TRC-P y DAI. Los resultados finales mostraron que en todos los subgrupos de pacientes (FEVI < 35% y QRS > 120 ms) el TRC-D se asoció a una disminución de la mortalidad, con un rango de 28% (CR 0.72; IC95% 0.51; 1.01) a 53% (CR 0.47; IC95% 0.34; 0.66) entre los distintos subgrupos. CRT-D es más efectivo en los pacientes con QRS > 150 ms y bloqueo de rama izquierda124. No hubo evidencia de que la clase NYHA sea un factor diferenciador en la respuesta, así como la etiología de la FEVI disminuida. Las conclusiones de esta revisión son que tanto los TRC-P y TRC-D reducen la mortalidad por cualquier causa comparados con la terapia médica óptima sola. El metaanálisis y la meta-regresión mostraron que los pacientes con QRS > 150 ms, bloqueo de rama izquierda y de sexo femenino se beneficiaron más de TRC-P y TRC-D, y aquellos hombres de < 60 años se beneficiaron más de la DAI. El dispositivo TRC-D fue el más efectivo de los tratamientos si no se consideran características de los pacientes con una reducción relativa de la mortalidad del 42% (IC95% 32; 50%), seguido del DAI 29% (IC95% 20-37%) y el TRC-P del 28% (15-40%)124.
Una RS publicada por Patel et al. en 2021131 tuvo como objetivo evaluar la evidencia científica respecto a los beneficios en pacientes con cardiomiopatía no isquémica a los que se les colocó un dispositivo TRC-D en comparación a los que se les colocó un marcapasos CRT-P. Los autores incluyeron 8 estudios clínicos, de los cuales solo hubo 1 ECA y 7 estudios observacionales. Los resultados del metaanálisis mostraron que no hubo diferencia significativa en mortalidad de cualquier causa (CR ajustado 0.92; IC95%: 0.83; 1.03) con bajo nivel de evidencia131.
Una RS publicada por Bazoukis et al. en 2021 evaluaron si los estudios de ecocardiografía podían ser útiles para determinar mejor a los pacientes respondedores de los no respondedores a terapia TRC. La medición de la deformación longitudinal global (GLS, por sus siglas en inglés), una medida de deformación del miocardio puede depender de la FEVI aunque se pueden presentar alteraciones menores en pacientes con una fracción de eyección normal. Los autores incluyeron 12 estudios clínicos (1,004 pacientes) y los resultados de los metaanálisis mostraron que los pacientes con una mejor respuesta tenían mejores resultados de GLS en reposo en comparación a los no respondedores (GLS DM –2.13; IC95%: –3.03; –1.23) y de igual manera se demostró que los respondedores mejoraron las cifras de GLS en mayor medida que los pacientes que no respondieron adecuadamente a la TRC (GLS DM -3.20; IC95%: –4.95; –1.45). Las conclusiones de los autores es que esta modalidad ecocardiográfica puede ayudar a hacer una mejor selección de los pacientes candidatos a TRC132. Juggan et al.133 en una RS cuyo objetivo fue el de evaluar si la edad avanzada en pacientes receptores de TRC respondían de una manera distinta respecto a los pacientes de menor edad. Los resultados mostraron que no hubo diferencias en cuanto a eficacia y seguridad entre ambas poblaciones133.
Hu et al.134 por su parte, publicaron una RS que tuvo como objetivo evaluar las distintas alternativas de imagen para la colocación de dispositivos TRC. Los autores incluyeron 8 estudios clínicos con 1,075 participantes, la mitad fueron aleatorizados para ser implantados con apoyo imagenológico y la otra mitad sin ese apoyo. Los resultados del metaanálisis mostraron que los pacientes a los que se les colocó el dispositivo TRC guiados por imagen mostraron una mejor respuesta y colocación del cable estimulador en VI que el grupo control (RR 1.33, IC95% 1.21; 1.47) y (RR 1.39; IC95%; 1.01; 1.92). Una mejoría en la FEVI significativa en el grupo guiado por imagen (DMP 3.25%; IC95%; 1.80; 4.70)134. Estos mismos hallazgos fueron replicados por Mehta et al. en 2022 en donde reportó mejores desenlaces en pacientes en los que su dispositivo TRC fue colocado guiado mediante estudios de imagen135.
Ye et al. en 2020136 reportan en una RS en la cual se evaluó la incorporación de rehabilitación cardiaca en pacientes receptores con dispositivos TRC. Los autores incluyeron 7 estudios clínicos que incluyeron 661 pacientes no encontraron diferencias significativas en los pacientes en cuanto a mortalidad de cualquier causa, sin embargo, los pacientes en rehabilitación cardiaca mostraron una mejor capacidad para el ejercicio (duración DMP 102.34s; IC95%: 67.06; 137.62) aunque hubo una marcada heterogeneidad entre los estudios136. La FEVI también se incrementó de manera estadísticamente significative en los pacientes bajo rehabilitación cardiaca (DMP 3.89%; IC95% 1.50; 6.28%) y en la HRQoL (DMP –5.34; IC95% –10.12; 0.056) evaluado con la MLHFQ136.
Pregunta 31: ¿Cuáles son las consideraciones para el manejo terapéutico en los pacientes con insuficiencia cardiaca crónica e hipertensión arterial sistémica?
Recomendación:
– Los cambios en el estilo de vida son parte esencial del manejo no farmacológico de los pacientes con ICFEr que tienen hipertensión arterial.
– Los antihipertensivos, como los IECA, los BRA, los BB y los antagonistas del calcio dihidropiridínicos, y los diuréticos para el tratamiento de la hipertensión, pueden reducir la incidencia de insuficiencia cardiaca.
– Los antagonistas del calcio no dihidropiridínicos (diltiazem y verapamilo) están contraindicados porque han demostrado desenlaces que incrementan la mortalidad por insuficiencia cardiaca.
– Los bloqueadores alfa no tienen efecto en la sobrevida de los pacientes con ICFEr e hipertensión arterial.
– Los objetivos de presión arterial son inciertos tanto en la insuficiencia cardiaca con FEVI reducida como en la insuficiencia cardiaca con FEVI preservada.
– En los pacientes con ICFEp con hipertrofia ventricular izquierda es de suma importancia evitar la hipotensión arterial.
Nivel de evidencia 1+, grado de recomendación A (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
La hipertensión arterial sistémica sigue siendo una de las enfermedades crónico-degenerativas más prevalentes en nuestro medio. El consenso mexicano sobre insuficiencia cardiaca 2022 recomienda instaurar un tratamiento temprano de la hipertensión para disminuir el riesgo de progresión a insuficiencia cardiaca. Hacen hincapié en que las terapias de control neuroendocrino (iECA, BRA, iRNA, BB y diuréticos) tienen un efecto positivo en la disminución de las cifras de presión arterial. En paciente ICFEr que no logran las metas terapéuticas recomendadas internacionalmente con terapia farmacológica óptima, se pueden considerar antagonistas de calcio dihidropiridina o una combinación de nitratos con hidralazina. No se recomiendan de los antagonistas de calcio como el verapamilo o el diltiacem tienen efectos inotrópicos negativos por lo que no se recomiendan (Fig. 8). Una RS publicada por Ho et al.137 concluyó que el tratamiento intensivo de la hipertensión arterial puede prevenir la ocurrencia de EVC en pacientes mayores (1.7 años; IC95% 1.0; 2.9 se requieren para prevenir 1 EVC en 200 pacientes tratados. El estudio SPRINT (Systolic Blood Pressure Intervention Trial)138 mostró (140 mmHg sistólica basal, 121 mmHg sistólica al final del estudio) requirió 5.9 años para lograr disminuir 1 evento en 200 pacientes137. Los resultados del estudio SPRINT han mostrado en pacientes en estadio A, con hipertensión, pero sin daño estructural cardiaco, lograr una meta de tratamiento por debajo de 120 mmHg sistólica logra una disminución del 38% del desarrollo de insuficiencia cardiaca139. El mismo estudio SPRINT, en un análisis de subgrupos, demostró que en pacientes estadio B, el tratamiento intensivo de la hipertensión arterial puede ayudar a involucionar el daño cardiaco logrando cifras por debajo de 130 mmHg de presión arterial sistólica. Las GPC de AHA/ACC recomiendan una meta menor a 130/80 mmHg para pacientes hipertensos con riesgo aumentado de desarrollar insuficiencia cardiaca139. Hay evidencia sólida respecto a que el ejercicio físico realizado de manera cotidiana y preferentemente de manera organizada y supervisada es eficiente para disminuir las cifras de presión arterial, tanto sistólicas como diastólicas140. En pacientes estadio C ICFEp, las GPC AHA/ACC recomiendan una meta menor a 130/80 mmHg para pacientes hipertensos, sin embargo, no hay suficiente evidencia en esta población de pacientes que hayan evaluado los distintos esquemas de manejo farmacológico139.
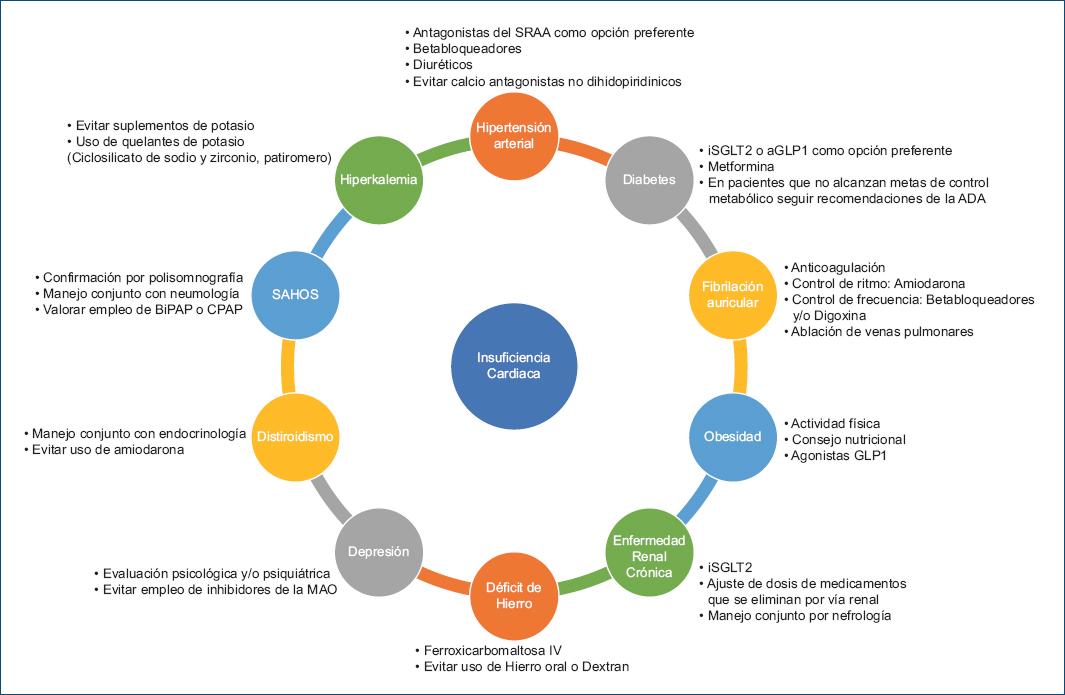
Figura 8 Manejo de la comorbilidad en pacientes con insuficiencia cardiaca crónica. ADA: American Diabetes Association; aGLP1: agonistas del receptor del péptido similar al glucagón 1; BiPAP: presión positiva de dos niveles en la vía respiratoria; CPAP: presión positiva continua en la vía respiratoria; iSGLT2: inhibidores del cotransportador sodio-glucosa tipo 2; IV: intravenoso; MAO: monoaminooxidasa; SAHOS: síndrome de apnea hipopnea obstructiva de sueño; SRAA: sistema renina-angiotensina-aldosterona.
Una RS publicada por Saiz et al.141 en 2022 con la colaboración Cochrane tuvo como objetivo determinar si metas de presión arterial menores (135/85 mmHg o menos) se asocian a una disminución de la mortalidad y morbilidad comparadas con metas de presión arterial estándar (140 a 160 mmHg/90 a 100 mmHg o menos) en el tratamiento de personas con hipertensión arterial y antecedentes de enfermedad cardiovascular (IAM, angina, EVC, enfermedad vascular periférica). Los autores incluyeron 7 ECAs que incluyeron 9,595 participantes, con un promedio de seguimiento de 3.7 años. Los resultados mostraron que no se pudo encontrar una diferencia significativa en la mortalidad (RR 1.05; IC95%: 0.91; 1.23) moderada calidad de la evidencia, mortalidad cardiovascular (RR 1.03; IC95%: 0.82; 1.29) moderada calidad de la evidencia. No hubo tampoco diferencias en la incidencia de eventos adversos (RR 1.01; IC95%: 0.94; 1.08) baja calidad de la evidencia. Hubo una necesidad de usar más medicamentos en el grupo con un meta menor de presión arterial (DM 0.56, IC95% 0.16; 0.96)141. Verdecchia et al.142 publicaron una RS de ECAs para evaluar las diferentes estrategias de manejo de la hipertensión arterial, compararon una estrategia más intensiva vs. una estrategia menos intensiva (7.6/4.5 mmHg de diferencia entre ambas), y los autores analizaron 18 ECAs con 53,405 pacientes en donde se evaluó el riesgo de EVC, AIM, insuficiencia cardiaca y muerte cardiovascular, El estudio SPRINT138 nuevamente influyó mucho en los resultados estadísticos. Los autores concluyeron que la evidencia punta a una superioridad de las estrategias más intensivas para la prevención de eventos cardiovasculares142.
Algunos de las alternativas recientes de tratamiento han demostrado tener efectos benéficos en cuanto al control de la presión arterial se refiere. Los iRNA son una nueva clase de agentes cardiovasculares que han mostrado tener un efecto hipotensor poderoso, incluso similar o superior a los BRA. Sin embargo, todavía se necesitan más estudios de investigación para conocer sus beneficios en todo el espectro de pacientes con insuficiencia cardiaca139. Los iSGLT-2 tienen dentro de sus beneficios farmacológicos el de disminuir el riesgo de insuficiencia cardiaca y otros efectos protectores renales, cardiacos y de disminución del peso corporal, por lo que se recomiendan en esta población de pacientes139. Para pacientes en estadio C, la terapia farmacológica óptima en la que se encuentran iECA, iRNA, BRA, BB, iSGLT-2; tienen la capacidad de reducir el riesgo de mortalidad y de mejorar el control de la presión arterial en pacientes con ICFEr139.
En pacientes en estadio D, una presión arterial alta presenta una oportunidad de titular la posología de la terapia farmacológica óptima (iECA, iRNA, BRA, ARM, BB, iSGLT-2), aunque de una manera cuidadosa139.
Pregunta 32: ¿Cuáles son las consideraciones para el manejo terapéutico en los pacientes con insuficiencia cardiaca crónica y diabetes?
Recomendación:
– En los pacientes con insuficiencia cardiaca y diabetes, los iSGLT2 (canagliflozina, dapagliflozina, empagliflozina, ertugliflozina, sotagliflozina) son la opción preferente como fármacos reductores de la glucosa y para disminuir los eventos cardiovasculares mayores, la mortalidad por causa cardiovascular, la insuficiencia renal y las rehospitalizaciones por insuficiencia cardiaca.
– La metformina se debe recomendar junto con un iSGLT2 para mejorar el control glucémico de los pacientes con insuficiencia cardiaca y diabetes.
– Los agonistas del receptor del péptido similar al glucagón tipo 1 (GLP-1) pueden considerarse como adyuvantes de los iSGLT2 y la metformina para el control metabólico en pacientes con insuficiencia cardiaca y diabetes.
– En pacientes con ICFEp, la semaglutida ha demostrado mejorar los síntomas y la capacidad funcional, por lo que su empleo queda a juicio del médico tratante en estos pacientes.
– En pacientes con insuficiencia cardiaca, los inhibidores de la dipeptidil peptidasa 4 y las insulinas pueden ser considerados como manejo adyuvante de la diabetes, pero solo después del uso de iSGLT2, agonistas GLP-1 y metformina.
– Las tiazolidinedionas (glitazonas) están contraindicadas como manejo de la diabetes en pacientes con insuficiencia cardiaca, ya que su empleo incrementa el riesgo de desenlaces adversos, incluyendo la muerte de causa cardiovascular.
Nivel de evidencia 1+, grado de recomendación A (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
La diabetes es otra de las comorbilidades que se manifiestan con frecuencia en pacientes con insuficiencia cardiaca. Las GPC de AHA/ACC 2022, las GPC ADA 2022143,144 y las GPC ESC144 entre otros lineamientos internacionales, recomiendan el uso de iSGLT-2 como agentes de primera línea en el tratamiento de la hiperglicemia en pacientes con diabetes e insuficiencia cardiaca o en riesgo de desarrollar insuficiencia cardiaca. El uso de iSGLT-2 en pacientes con diabetes e insuficiencia cardiaca se asocia a una disminución en el riesgo de eventos cardiovasculares mayores, incluyendo muerte cardiovascular y hospitalizaciones por insuficiencia cardiaca (Fig. 8). El resultado de 2 ECAs en pacientes ICFEr mostraron una reducción del riesgo relativo de mortalidad de cualquier causa del 13%, muerte cardiovascular del 14%, hospitalización del 26% y de agravamiento del daño renal de 38% con iSGLT-24. Los beneficios son consistentes cuando se hicieron los análisis de subgrupos por edad, sexo y en pacientes con o sin diabetes4.
Los arGLP-1 (receptors agonists to Glucagon-like peptide-1) reducen el riesgo de EVC, IAM o muertes cardiovasculares, pero no la incidencia de insuficiencia cardiaca. No se ha podido demostrar que los arGLP-1 tengan un efecto benéfico en mejorar la FEVI y mejorar la frecuencia cardiaca; sin embargo, aumentaron la incidencia de eventos cardiacos graves en un estudio clínico controlado. Tampoco han demostrado disminuir las hospitalizaciones por insuficiencia cardiaca, en comparación a placebo5.
Una RS publicada por Hasan et al.145 en 2023 tuvo como objetivo evaluar la evidencia sobre los beneficios de los iSGLT-2 en pacientes con insuficiencia cardiaca con o sin diabetes. Los autores incluyeron 13 ECAs con un total de 75,287 participantes. Los resultados de los metaanálisis mostraron una disminución significativa en el riesgo de hospitalización por insuficiencia cardiaca del 32% (RR 0.68; IC95%: 0.63; 0.74) con diabetes y del 25% sin diabetes (RR 0.75; IC95%: 0.62; 0.89). También hubo una disminución de la mortalidad en pacientes con diabetes (RR 0.87; 0.77; 0.99), aunque en los pacientes sin diabetes esta no fue estadísticamente significativa (RR 0.93; IC95% 0.70; 1.23). Los iSGLT-2 mostraron una disminución de los eventos adversos (RR 0,94; IC95%: 0.90; 0.98) en pacientes con diabetes145.
Pregunta 33: ¿Cuáles son las consideraciones para el manejo terapéutico en los pacientes con insuficiencia cardiaca crónica y déficit de hierro?
Recomendación:
– Se recomienda la administración de hierro intravenoso en pacientes sintomáticos con insuficiencia cardiaca con FEVI reducida y deficiencia de hierro demostrada, para aliviar los síntomas de la insuficiencia cardiaca y mejorar la calidad de vida.
– La administración de hierro intravenoso (carboximaltosa o derisomaltosa férrica) debe ser considerada en pacientes sintomáticos con insuficiencia cardiaca con FEVI reducida y ligeramente reducida cuando se demuestre deficiencia de hierro, para reducir el riesgo de hospitalización por insuficiencia cardiaca.
– En el momento actual no hay evidencia suficiente para recomendar la administración de hierro intravenoso en pacientes con insuficiencia cardiaca con FEVI preservada, por lo que su uso deberá restringirse al manejo de problemas hematológicos o del metabolismo del hierro, y no como parte del manejo de la insuficiencia cardiaca.
Nivel de evidencia 1+, grado de recomendación A (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
La deficiencia de hierro es común en pacientes con insuficiencia cardiaca y es independientemente asociada a un riesgo incrementado de hospitalizaciones y de mortalidad por cualquier causa. La deficiencia de hierro se define como una concentración < 100 ng/mL o 100-299 ng/mL con una saturación de transferrina < 20%. El estado proinflamatorio de algunos pacientes con insuficiencia cardiaca afecta el metabolismo del hierro, que también puede verse disminuido en su absorción. Las GPC ESC 2021 recomiendan en todos los pacientes se lleve a cabo la determinación de deficiencia de hierro y la búsqueda de anemia, concentración de ferritina sérica y de saturación de transferrina. No recomiendan el uso de eritropoyetina debido al riesgo incrementado de eventos trombóticos5. Se recomienda, por otro lado, la suplementación con carboximeltosa férrica endovenoso en pacientes sintomáticos con una FEVI < 45% para mejorar su sintomatología y en pacientes recientemente hospitalizados por insuficiencia cardiaca y una FEVI < 50% (Fig. 8).
Una RS publicada en 2022 por Tan et al. incluyó 4 ECAs en donde se reportó que la suplementación de hierro oral mejora los valores de la FEVI (DM 1.52%; IC95%: 0.69; 2.36) y de la ferritina sérica (DM 1.64; IC95%: 0.26; 3.02), sin embargo, no hubo diferencias en la evaluación de 6MWT, NT-proBNP; y de los niveles de hemoglobina146.
Mei et al. en 2022147, por su parte, evaluaron a través de un metaanálisis en red, el impacto de la suplementación de hierro endovenosa en comparación a la oral en pacientes con insuficiencia cardiaca. Los autores incluyeron 16 ECAs, los resultados muestran que la suplementación con hierro endovenoso no disminuyó el riesgo de muerte de cualquier causa (RR 0.69; IC95%: 0.39; 1.23) o mortalidad cardiovascular (RR 0.89; IC95%: 0.66; 1.20). Después de 12 semana se observó una disminución de las hospitalizaciones por insuficiencia cardiaca con la suplementación endovenosa de hierro (RR 0.58; IC95%: 0.34; 0.97). Se observó una mejoría de la evaluación de 6MWT (DM 44.44; IC95%: 6.10; 82.79) y KCCQ (DM 5.96; IC95%; 3.19; 9.83). Los suplementos orales mejoraron la hospitalización por insuficiencia cardiaca (RR 0.36; IC95%: 0.14; 0.96) y de muerte por cualquier causa (RR 0.34; IC95%: 0.12; 0.95), aunque no mejoran el 6MWT (DM 29.76; IC95%: –47.36; 106.83) ni el KCCQ (DM 0.10; –10.95; 11.15)147.
Pregunta 34: ¿Cuáles son las consideraciones para el manejo terapéutico en los pacientes con insuficiencia cardiaca crónica y enfermedad renal crónica?
Recomendación:
– En pacientes con insuficiencia cardiaca crónica, el tratamiento adecuado de la congestión es fundamental para evitar la progresión de la enfermedad renal.
– Se debe evitar la hipotensión arterial grave (presión sistólica < 80 mmHg) en pacientes con insuficiencia cardiaca y enfermedad renal crónica.
– En pacientes con insuficiencia cardiaca y enfermedad renal crónica se debe incrementar la vigilancia de los niveles séricos de potasio.
– No hay evidencia que sustente el uso de iSGLT2 en pacientes con insuficiencia cardiaca y TFGe < 15 ml/min.
– No hay evidencia que sustente el uso de sacubitrilo/valsartán, IECA o BRA en pacientes con insuficiencia cardiaca y TFGe < 15 ml/min.
– El uso de digoxina en pacientes con insuficiencia cardiaca con FEVI reducida y enfermedad renal crónica debe ser evaluado en conjunto con nefrología, y evitarse cuando hay hiperpotasemia o la TFGe es < 15 ml/min.
– En pacientes con insuficiencia cardiaca y enfermedad renal crónica grave se deberá considerar siempre el manejo conjunto con nefrología para estructurar el tratamiento y la toma de decisiones complejas.
– En pacientes con diabetes y enfermedad renal crónica, los iSGLT2 (dapagliflozina o empagliflozina) se recomiendan para reducir el riesgo de hospitalización por insuficiencia cardiaca y de muerte por causa cardiovascular.
– En pacientes con diabetes y enfermedad renal crónica, la finerenona se recomienda para reducir el riesgo de hospitalización por insuficiencia cardiaca.
Nivel de evidencia 1+, grado de recomendación A (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
La insuficiencia cardiaca y la enfermedad renal crónica (ERC) con frecuencia coexisten y además comparten algunos de los factores de riesgo como diabetes o HAS. La ERC empeora la insuficiencia cardiaca contribuyendo a la sobrecarga hídrica, hipertensión y afectación vascular; y la insuficiencia cardiaca empeora la función renal por su desequilibrio neurohumoral y estado pro-inflamatorio (Fig. 8). Las GPC ESC 2021 hacen énfasis en que al iniciar el manejo con iRNA o iSGLT-2 se puede notar una disminución del filtrado glomerular, pero esto es transitorio, y se recupera pronto por lo que no está indicado suspender el tratamiento. Se puede considerar aceptable un incremento de la creatinina sérica < 50% por arriba del estado basal, mientras se mantenga < 3 mg/dL o una disminución de < 10% FGR mientras que se mantenga > 25 mL/min/1.73m25. Estos lineamientos establecen que el uso de BB reducen la mortalidad en pacientes ICFEr con ERC moderada o moderada/severa, aunque no hay evidencia suficiente en pacientes con ERC grave. Sacubitrilo/valsartán disminuye la progresión del daño renal y mejora algunos parámetros cardiovasculares. Los iSGLT-2 disminuyen la progresión de la ERC. Hay pocos estudios en pacientes con ERC grave (< 30 mL/min/1.73m2)5.
Una RS publicada en 2022 por Ravindran et al.148 tuvo como objetivo evaluar el beneficio de los iSGLT-2 en pacientes con ERC e insuficiencia cardiaca, en pacientes con diabetes y sin diabetes. Los autores evaluaron los efectos protectores cardiovasculares y renales con los SGLT-2i en tres grandes ECAs con una cohorte de pacientes con y sin diabetes. Los resultados concluyen que existe una reducción significativa de las hospitalizaciones por insuficiencia cardíaca y de muerte cardiovascular y por todas las causas. Además, los iSGLT-2 impiden la progresión y la muerte por ERC148. Una RS publicada por Spanella et al.149 en 2020 tuvo como objetivo evaluar el impacto de sacubitrilo/valsartán en la progresión de la ERC. Los autores incluyeron 10 ECAs con 16,456 participantes y los resultados de los metaanálisis mostraron que sacubitrilo/valsartán se asoció a un menor riesgo de ERC (RM 0.70; IC95%: 0.57; 0.85), cuando se llevaron a cabo análisis de subgrupos se encontró la misma asociación, pero con mayor fuerza en pacientes mayores y en pacientes ICFEp149.
Pregunta 35: ¿Cuáles son las consideraciones para el manejo terapéutico en los pacientes con insuficiencia cardiaca crónica y obesidad?
Recomendación:
– Como parte de las medidas no farmacológicas, mantener un peso corporal cercano al ideal se recomienda para todo paciente con insuficiencia cardiaca crónica, para disminuir los síntomas y mejorar la capacidad funcional.
– En este momento no existe evidencia suficiente del beneficio de la reducción de peso para disminuir la muerte o los episodios de empeoramiento en pacientes con insuficiencia cardiaca con FEVI reducida o ligeramente reducida que tengan obesidad.
– En pacientes con insuficiencia cardiaca con FEVI preservada y obesidad, el uso de semaglutida puede ser recomendado para disminuir los síntomas y mejorar la capacidad funcional y los parámetros de CVRS medidos con el KCCQ.
Nivel de evidencia 1+, grado de recomendación A (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
Las GPC de la ESC 20215 establecen que la obesidad es un factor de riesgo bien establecido para hipertensión y distintas enfermedades cardiovasculares, así como para la insuficiencia cardiaca. Es importante considerar, que un paciente con aumento del IMC (índice de masa corporal) tiene peor pronóstico si tiene una mayor proporción de tejido graso y cierto grado de sarcopenia, que un paciente con una composición corporal con una mayor proporción de masa muscular. La circunferencia abdominal es un mejor indicador que el IMC de un riesgo cardiovascular incrementado5 (Fig. 8).
La obesidad se considera una causa muy importante de ICFEp, por lo que es muy importante implementar estrategias para disminuir el peso corporal, como el ejercicio físico habitual y la restricción dietética5.
La paradoja de la obesidad se describe como aquella situación en la que pacientes ICFEp con obesidad moderada o sobrepeso tienen mejor pronostico que los pacientes con un peso corporal dentro de percentiles normales. Li et al.150 demostraron en una RS con 69,273 participantes con ICFEp que el riesgo de muestre se incrementa 10% (HR 0.90, IC95%: 0.84; 0.95) por cada 5 unidades de incremento del IMC, pero la asociación mostró una forma de U con el nadir del riesgo en el IMC 32-34 kg/m2. Se observó una relación lineal del IMC con el riesgo de hospitalización por cualquier causa150.
Una RS publicada por Shoar et al.151 concluyo que en pacientes ICFEr la cirugía bariátrica se asoció a una disminución del IMC significativa (DM 12.9 IMC, IC95%: 5.1; 23) con una correlación directa con la mejoría clínica de la insuficiencia cardiaca (r = 0.61, p < 0.0001) pero que no se pudo correlacionar con mejoría de la clase funcional NYHA (r = 0.17, p = 0.4)151.
Los iSGLT-2 son una clase terapéutica que ha ganado mucha atención recientemente por diversos beneficios que ofrecen a pacientes con diabetes o incluso en pacientes sin diabetes. Entre estos beneficios, la pérdida ponderal ha generado mucho interés por la importancia que tienen el sobrepeso y la obesidad en la fisiopatología de distintas enfermedades metabólicas y cardiovasculares. Una RS publicada recientemente por Wang et al.152 demostró que el tratamiento de pacientes con insuficiencia cardiaca con iSGLT-2 se asoció a una disminución ponderal significativa (DM –1.36 kg, IC95%: –1.68; –1.03)152.
Pregunta 36: ¿Cuáles son la eficacia y la seguridad de las distintas técnicas intervencionistas para el manejo de los pacientes con insuficiencia cardiaca crónica?
Recomendación:
– En pacientes con insuficiencia cardiaca crónica y angina, la intervención coronaria percutánea (ICP) está recomendada como parte del manejo de la enfermedad isquémica del corazón para mejorar los síntomas y la capacidad funcional.
– No existe evidencia suficiente para sustentar el uso sistemático de la ICP en pacientes con disfunción ventricular izquierda o insuficiencia cardiaca para reducir la mortalidad por causa cardiovascular o las hospitalizaciones por insuficiencia cardiaca.
– En pacientes con insuficiencia mitral secundaria grave e insuficiencia cardiaca con FEVI reducida se recomienda la optimización del tratamiento farmacológico antes de cualquier tratamiento intervencionista.
– En pacientes con insuficiencia cardiaca crónica con FEVI reducida, la reparación transcatéter de la insuficiencia mitral secundaria ha demostrado que es benéfica en pacientes con síntomas persistentes a pesar del tratamiento farmacológico optimizado.
– Son candidatos para reparación transcatéter de la válvula mitral los pacientes que demuestren tener una anatomía adecuada mediante ecocardiograma transesofágico, FEVI del 20-50%, diámetro sistólico final del ventrículo izquierdo ≤ 70 mm y presión sistólica de la arteria pulmonar ≤ 70 mmHg.
– Se recomienda la cirugía de la válvula tricúspide en pacientes con insuficiencia tricúspide grave que requieren cirugía cardiaca del lado izquierdo. También se debe considerar en pacientes con insuficiencia tricúspide moderada y dilatación del anillo que requieren cirugía cardíaca del lado izquierdo, y en pacientes sintomáticos con insuficiencia tricúspide grave aislada.
Nivel de evidencia 1+, grado de recomendación A (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
El consenso mexicano sobre insuficiencia cardiaca 20222 establece la importancia de las terapias intervencionistas en pacientes con insuficiencia cardiaca en escenarios específicos.
La revascularización miocárdica es un procedimiento extendido para el manejo de la miocardiopatía isquémica. El consenso mexicano sobre insuficiencia cardiaca sugiere la realización de la revascularización miocárdica en pacientes con angina inestable que permanecen sintomáticos a pesar del manejo farmacológico óptimo y llevado a cabo por un equipo interdisciplinario con amplia experiencia en centros especializados. Es importante realizar una valuación de la viabilidad miocárdica antes del manejo invasivo con métodos como la ecocardiografía bajo estrés, la MRI, medicina nuclear y PET-CT.
Una RS publicada por Laconelli et al.153 en 2023 tuvo como objetivo evaluar el impacto de la revascularización coronaria en pacientes con insuficiencia cardiaca. Los autores incluyeron 5 ECAs que incluyeron 2,842 participantes (la mayoría < 65 años, 85% hombres, 67% con FEVI < 35%). Los resultados del metaanálisis mostraron que la revascularización coronaria se asoció a una disminución de la mortalidad por cualquier causa en un 12% (CR 0.88; IC95%: 0.79; 0.99) y de mortalidad cardiovascular en 20% (CR 0.87; IC95%: 0.70; 0.93), sin embargo, no se asoció a una menor hospitalización por cualquier causa (CR 0.88; IC95%: 0.74; 1.01)153. No hubo suficiente evidencia para mostrar si la cirugía de injerto de derivación de arterias coronarias (CABG, por sus siglas en inglés) o la intervención coronaria percutánea (PCI, por sus siglas en inglés) obtuvieron resultados distintos. Los estudios no fueron cegados, lo que disminuyó la calidad de la evidencia, aunque en general, los estudios fueron calificados con bajo riesgo de sesgo153.
Otra RS publicada por Pei et al. en 2021154 tuvo como objetivo evaluar si la cirugía las diferencias en resultados de la CABG y la PCI en pacientes con insuficiencia cardiaca. Los autores incluyeron 18 estudios que incluyeron 11,686 participantes (2 ECAs, 1 estudio de casos y controles y 16 estudios de registros de bases de datos). Los resultados de los metaanálisis de estos estudios descriptivos, en su mayoría, mostraron que no hubo diferencias en la mortalidad a los 30 días entre ambos grupos (CR 1.18; IC95%: 0.89; 1.56), aunque si se observó una disminución del riesgo de muerte a largo plazo con ambos procedimientos (CR 0.70; IC95%: 0.61; 0.80). Tampoco se observó diferencia entre CABG y PCI en la incidencia de IAM (CR 0.42; IC95%: 0.16; 1.11)154.
Otra intervención en pacientes con insuficiencia cardiaca es la denominada reparación de la válvula mitral transcatéter (RVMT) con el sistema Mitraclip® para los pacientes con insuficiencia mitral grave de alto riesgo para cirugía155. La insuficiencia mitral (IM) grave se asocia con una progresiva dilatación del ventrículo izquierdo dando como resultado la aparición de insuficiencia cardiaca (IC). Los pacientes sintomáticos tienen una tasa de mortalidad anual superior al 5% cuando no se interviene155. La remodelación de las paredes del ventrículo y la pérdida de su geometría normal con la subsecuente dilatación del anillo mitral se presenta con frecuencia en pacientes ICFEr. El consenso mexicano sobre insuficiencia cardiaca2 sugieren que en pacientes ICFEr candidatos a RVMT con Mitraclip® se lleve a cabo una evaluación cuidadosa en centros especializados para decidir la conveniencia del procedimiento por todos los miembros del equipo de tratamiento.
Una RS recientemente publicada por Martínez Gómez et al.156 tuvo como objetivo evaluar la evidencia científica sobre el desempeño de la RVMT con Mitraclip®. Los autores incluyeron 40 estudios que incluyeron 254 participantes con regurgitación mitral moderada a grave (grado 4 en el 91% de los casos). Los autores reportaron un éxito en 238 pacientes (93.7%) con una disminución significativa de la regurgitación mitral (grado < 2 en 91.8%). Se presentaron complicaciones no fatales en el 9.1% de los casos y mortalidad en el 12%. Los análisis Kaplan-Meier estimaron una mortalidad global de 39.1% a los 12 meses de seguimiento con persistencia de la reducción de la regurgitación mitral (grado < 2 en el 81.3% de los casos)156.
Otra RS publicada por Oh et al.157 comparó la efectividad de la RVMT con Mitraclip® en comparación a la cirugía de remplazo de la válvula mitral (RVM). Los autores incluyeron 9 estudios (1,873 en total, 533 con RVMT con Mitraclip® y 644 RVM). Los autores encontraron que los pacientes a los que se les llevó a cabo la RVMT con Mitraclip® tenían más comorbilidades. La RVMT con Mitraclip® demostró menor estancia hospitalaria (–3.86 días), aunque se observó mayor regurgitación mitral moderada a severa residual al momento del alta (RM 2.81; ic95% 1.39; 5.69) y a los 5 años (RM 2.46; IC95%: 1.54; 3.94), y mayor necesidad de reintervención (RM 5.28; IC95%: 3.43; 8.11). La mortalidad general fue comparable entre los dos grupos (CR 2.06; IC95%: 0.98; 4.29) en un periodo de seguimiento de 4.8 años157.
Otra condición que requiere procedimientos intervencionistas para su manejo es la estenosis aórtica. El consenso mexicano en insuficiencia cardiaca establece que los pacientes con disfunción ventricular izquierda y estenosis aórtica con gradiente y flujo bajos son especialmente complejos en su manejo. Sugieren la realización de un ecocardiograma de estrés con estimulación con dobutamina a dosis bajas para evaluar la reserva contráctil en estos pacientes. En estos pacientes, la colocación de un implante percutáneo de válvula aórtica (TAVI, por sus siglas en inglés) es una opción para ser considerada. Es importante considerar que la selección de los pacientes debe de hacerse en una clínica altamente especializada por el equipo interdisciplinario.
Una RS publicada por Liu et al.158 tuvo como objetivo evaluar la efectividad clínica del TAVI. Los autores incluyeron 3 ECAs de buena calidad metodológica. Los pacientes tenían en promedio 83-85 años, con Clase Funcional NYHA III o IV en el 83.8% al 94.2% con comorbilidades frecuentes. Los autores reportaron en un estudio con 358 pacientes no operables, que TAVI fue superior a la terapia médica respecto a la mortalidad por cualquier causa a 1 año (CR 0.58; IC95%: 0.36; 0.92), a dos años (CR 0.50; IC95%: 0.39; 0.65), 3 años (CR 0.53; IC95%: 0.41; 0.68) y 5 años (CR 0.50; IC95%: 0.39; 0.65). Sin embargo, el TAVI tuvo un riesgo incrementado de sangrado mayor y de EVC a 2 años. También mostró mayor riesgo de complicaciones vasculares mayores a 3 años (CR 8; 0.27 IC95%: 2.92; 23.44). Los resultados de los metaanálisis no mostraron diferencias en comparación al remplazo aórtico en mortalidad de cualquier causa a los dos años (CR 1.03; IC95%: 0.82; 1.29) y a cinco años (CR 0.97; IC95%: 0.83; 1.12)158.
Pregunta 37: ¿Cuáles son la eficacia y la seguridad del trasplante cardiaco para el manejo de los pacientes con insuficiencia cardiaca crónica avanzada?
Recomendación:
– Para pacientes seleccionados con insuficiencia cardiaca avanzada a pesar del tratamiento médico óptimo (farmacológico y con dispositivos cuando esté indicado), el trasplante cardiaco está indicado para mejorar la sobrevida y la calidad de vida.
– En caso de hipertensión pulmonar grave irreversible, IMC > 35 kg/m2, enfermedad arterial periférica grave, enfermedad oncológica grave o enfermedad sistémica con involucro multiorgánico, el trasplante cardiaco está contraindicado.
– El trasplante de corazón sigue siendo el tratamiento de referencia para la insuficiencia cardiaca avanzada en ausencia de contraindicaciones.
– Se puede considerar la asistencia mecánica de la circulación (AMC) de largo plazo en pacientes con insuficiencia cardiaca avanzada refractaria a tratamiento médico óptimo y a la terapia con dispositivos como puente al trasplante cardiaco para mejorar los síntomas, reducir el riesgo de hospitalización por insuficiencia cardiaca y el riesgo de muerte prematura.
Nivel de evidencia 1+, grado de recomendación A (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
El trasplante cardiaco inició hace más de 5 décadas por el Dr. Christiaan Barnard en Sudáfrica y en México a finales de la década de los 80s por el Dr. Rubén Argüero Sánchez2.
Las GPC AHA/ACC 2022 recomiendan considerar el trasplante cardiaco en pacientes seleccionados con insuficiencia cardiaca avanzada a pesar de encontrarse bajo terapia médica óptima, con el objetivo de prolongar la sobrevida y la HRQoL de los pacientes receptores del mismo4. La evidencia que apoya el hecho de que el trasplante cardiaco prolonga la sobrevida está extraída de estudios de cohortes. Las bases de datos internacionales, de la Sociedad Internacional del Corazón y Pulmones (ISHL, por sus siglas en inglés) y la UNOS (United Network of Organ Sharing) han documentado que el promedio de sobrevida de los receptores de un trasplante cardiaco es de > 12 años, mientras que la media de sobrevida en pacientes con insuficiencia cardiaca avanzada solamente con terapia farmacológica es de alrededor de 2 años. Con el continuo mejoramiento de los protocolos de trasplante cardiaco, los porcentajes de rechazo se han reportado en alrededor del 15%. Las metas de la mayoría de los programas en el mundo es disminuir la mortalidad de los pacientes en espera y un uso óptimo de los dispositivos de apoyo circulatorio. Por ello, las GPC establecen porcentajes de sobrevida a 1, 3 y 5 años de 90%, 84% y 79%, respectivamente. La HRQoL mejora de manera sensible y el estado funcional NYHA también.
El consenso mexicano de insuficiencia cardiaca 20212 recomienda seleccionar a los candidatos para recibir un trasplante cardiaco a aquellos pacientes con un daño miocárdico grave y avanzado (FEVI < 30%) que no responde al esquema terapéutico óptimo a dosis máximas toleradas, haber descartado causas tratables del daño al miocardio y haber considerado otras alternativas de apoyo cardiaco. La evaluación del paciente puede ser apoyada por escalas funcionales como NYHA, HFSS (Heart Failure Survival Score) y SHFS (Seattle Heart Failure Score). Algunos datos clínicos que pueden respaldar la decisión de indicación de un paciente para trasplante cardiaco son las hospitalizaciones frecuentes debido a la progresión de síntomas, afectación hepática y/o renal, arritmias ventriculares malignas, y afectación funcional progresiva (Tabla 7).
Tabla 7 Contraindicaciones relativas y absolutas del trasplante cardiaco
| Contraindicaciones relativas | Contraindicaciones absolutas |
|---|---|
| Obesidad, índice de masa corporal > 35 kg/m2 | Enfermedad sistémica con expectativa de vida menor de 1 año independientemente de la insuficiencia cardiaca |
| Infección por virus de la inmunodeficiencia humana | Enfermedad maligna con riesgo alto de recurrencias |
| Aterosclerosis cerebrovascular leve o moderada sin limitación física importante | Diabetes con daño irreversible de órgano diana |
| Daño renal bajo protocolo de reemplazo de órgano | Hipertensión pulmonar grave irreversible |
| Cirrosis hepática bajo protocolo de reemplazo de órgano | Neumopatía obstructiva crónica grave |
| Edad > 65 años, cada centro de trasplante establecerá sus propios criterios de selección | Estado séptico refractario a tratamiento |
| Enfermedad neurológica avanzada | |
| Edad avanzada con expectativa de vida menor de 3 años |
Modificada con permiso de: Magaña S, Cigarroa L, Chávez M, Rayo C, Galvan O, Aguilera M. First Mexican statement in heart failure. Cardiovasc Metab Sci. 2021;32(Suppl 1):s8-s85.
Hsich et al. en 2020159 publican una revisión de los pacientes que recibieron un trasplante cardiaco y que se encontraban registrados en la base de datos de SRTR (Scientific Registry of Tansplant Recipients) que incluyó 30,606 pacientes del 2004 al 2018. Los autores analizaron los factores asociados a la mortalidad y reportaron 3 grupos de pacientes en donde hubo un mayor riesgo de muerte en pacientes post trasplantados. El sexo de los pacientes, no mostraron diferencia en el riesgo de mortalidad. En la fase temprana, la mortalidad ocurría dentro de la primera semana de trasplantados y disminuía en el transcurso del primer mes. La fase "constante" mostró una tasa de mortalidad de 4% al año y la fase "tardía" el riesgo de mortalidad se fue incrementando con el tiempo con un pronóstico mejor en mujeres que en hombres en esta última fase. Los factores de riesgo asociados a un incremento de la mortalidad en la fase temprana fueron la función renal, función hepática, enfermedad congénita, oxigenación extracorpórea, soporte circulatorio mecánico y apoyo ventilatorio mecánico al momento del trasplante. Durante la fase "constante" los factores de riesgo más importantes fueron la edad del paciente, raza afroamericana, cardiomiopatía isquémica y para la etapa "tardía" la edad, el IMC y el antecedente de diabetes159.
Aleksova et al.160 publicaron una RS que tuvo como objetivo evaluar las Escalas de Riesgo en pacientes Post trasplantados validados en estudios publicados. Los autores incluyeron 21 estudios que incluyeron a su vez 16 escalas clinimétricas. Los resultados de la revisión fueron que la escala IMPACT fue la más empleada, validad en el uso de dos grandes bases de datos de pacientes trasplantados y tuvo una buena capacidad de discriminar la supervivencia a los 3 meses160.
Pregunta 38: ¿Cuál es la eficacia y seguridad de los dispositivos de asistencia mecánica de la circulación como alternativa del trasplante en el manejo de los pacientes con insuficiencia cardiaca crónica avanzada?
Recomendación:
– En pacientes seleccionados con insuficiencia cardiaca avanzada, con síntomas, clase funcional IV de la NYHA, que se encuentren dependientes de un inotrópico intravenoso continuo o de AMC de corta duración, la implantación de AMC de largo plazo es eficaz para mejorar el estado funcional, la calidad de vida y la supervivencia.
– Se debe considerar la AMC de largo plazo en pacientes con insuficiencia cardiaca avanzada, a pesar del tratamiento médico óptimo y de terapias con dispositivos, no elegibles para trasplante cardiaco u otras opciones quirúrgicas, sin disfunción ventricular derecha grave, para reducir el riesgo de muerte y mejorar los síntomas.
– La AMC de corta duración debe usarse en pacientes con perfiles INTERMACS 1 o 2 como puente a la decisión, puente a la recuperación, puente a puente para AMC de largo plazo o puente para trasplante cardiaco urgente.
– El daño renal irreversible, el daño hepático irreversible, el daño neurológico irreversible y la limitación psicosocial grave se consideran contraindicaciones absolutas para la instalación de una AMC.
Nivel de evidencia 1+, grado de recomendación A (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
Los Dispositivos de Asistencia Mecánica de la Circulación (MCS, por sus siglas en inglés) han evolucionado los últimos años como una estrategia terapéutica para restaurar la perfusión sistémica en pacientes con insuficiencia cardiaca avanzada con la finalidad de prolongar la vida y la capacidad funcional. Estos dispositivos pueden ser empleados en el muy corto plazo (horas a días) y en el largo plazo (meses a años)4. Las GPC AHA/ACC 2022 recomiendan considerar un dispositivo MCS en pacientes ICFEr avanzada con clase funcional NYHA IV y sintomáticos dependientes de inotrópicos endovenosos continuos, la implantación de un dispositivo de asistencia ventricular izquierda (LVAD, por sus siglas en inglés) es efectiva para mejorar el estado funcional, la HRQoL y la supervivencia4. En pacientes con ICFEr avanzada y compromiso hemodinámico y shock, un dispositivo MCS, incluyendo dispositivos de asistencia ventricular percutáneos o extracorpóreos, son una opción razonable como "puente" para una opción más definitiva4.
El consenso mexicano en insuficiencia cardiaca2 hacen énfasis en la utilidad de emplear la clasificación INTERMACS para definir aquellos pacientes que pueden verse beneficiados de un dispositivo MCS. Hay un beneficio claro de los pacientes clasificados INTERMACS 1, 2 y 3. Las indicaciones para el uso de un dispositivo MCS son el "puente" para la recuperación, "puente" para el trasplante cardiaco, "puente" para una decisión y finalmente como terapia destino2. Los pacientes candidatos como "puente" para la recuperación son aquellos cuya condición aguda o crónica ocasiona un deterioro hemodinámico que requiere la colocación de un dispositivo MCS en lo que el ventrículo vuelve a ganar funcionalidad para que el dispositivo pueda ser retirado. Algunos dispositivos que cumplen esta función son el Centrimag®, la membrana de oxigenación extracorpórea (ECMO®, por sus siglas en inglés) y el soporte de vida extracorpórea (ECLS, por sus siglas en inglés). En los casos de los que la función del ventrículo no se recupere, el paciente podrá ser considerado para trasplante cardiaco2. Los dispositivos MCS pueden también colocarse en los pacientes "puente para trasplante". Es importante considerar el acceso al trasplante cardiaco en cada programa para considerar el mejor dispositivo MCS. Los pacientes "puente para decisión" son aquellos que se encuentran en condiciones críticas con daño orgánico importante y/o con estado neurológico desconocido y debido a ello no está claro si son candidatos para un MCS. En estos casos se recomiendan emplear dispositivos de uso corto para proveer soporte circulatorio mecánico mientras las condiciones del paciente se vuelvan más favorables. La indicación de terapia de destino se refiere a aquellos pacientes ICFEr avanzada que no son candidatos a implante cardiaco inicialmente. Actualmente solo hay tres dispositivos aprobados por la FDA (Food and Drug Administration, por sus siglas en inglés) de EE. UU., Heart Mate II®, HeartWare® y el Heart Mate 3®; los cuales pueden funcionar incluso por varios años2.
Una RS publicada en 2021 por McNamara et al. en 2021161 tuvo como objetivo evaluar la supervivencia de los dispositivos LVAD de flujo continuo. Los autores incluyeron 63 estudios clínicos que tomaron en cuenta 9,280 participantes. Los resultados de la revisión muestran que el registro más grande de pacientes reportó una supervivencia de 82% (12 meses), 72% (24 meses) y 57% (48 meses). Los eventos adversos más frecuentes fueron sangrado gastrointestinal, infección asociada al dispositivo, eventos neurológicos y falla cardiaca derecha. La HRQoL utilizando el KCCQ mejoró significativamente en los pacientes receptores de LVAD161. Una RS publicada por Zhang et al.162 en 2021 tuvo como objetivo comparar los desenlaces de pacientes receptores de LVAD de flujo continuo en comparación a los pacientes receptores de un trasplante cardiaco162. Los autores incluyeron 12 estudios clínicos. Los resultados de los metaanálisis es que no hubo diferencias entre los pacientes LVAD y los pacientes postrasplantes cardiaco en cuanto a la mortalidad a 1 año (RM 1.08; IC95%: 0.97; 1.21), a 2 años (RM 1.01; IC95%: 0.91; 1.12), a 3 años (RM 1.02; IC95%: 0.69; 1.51) y a 5 años (RM 1.02; IC95%: 0.93; 1.11). La comparación de los eventos adversos tampoco encontró diferencias en el sangrado o la infección, pero si un riesgo incrementado de EVC (RM 5.09; IC95%: 1.74; 14.84) en los pacientes receptores de LVAD162. Zhang et al.163 evaluaron la efectividad de las técnicas mínimamente invasivas en comparación a la técnica convencional. Los autores incluyeron 10 estudios clínicos y los resultados de los metaanálisis es que no hubo diferencias en la mortalidad a los 30 días (RM 0.57; IC95%: 0.29; 1.14), 6 meses (RM 0.66; IC95%: 0.41 1.05), disfunción neurológica (RM 1.10; IC95%: 0.69; 1.76), infección grave (RM 0.68; IC95%: 0.36; 1.28), y trombosis (RM 1.49; IC95%: 0.63; 3.52). Las técnicas mínimamente invasivas se asociaron a menor riesgo de sangrado grave (RM 0.39; IC95%: 0.22; 0.68), falla cardiaca derecha grave (RM 0.43; IC95%: 0.23; 0.81) y menos utilización de hemoderivados (DME –0.53)163.
Una RS publicada por den Uil et al. en 2017 evaluó la eficacia de los dispositivos MCS a corto plazo como "tera puente" para pacientes candidatos a trasplante cardiaco. Los autores incluyeron 39 estudios, la mayoría de ellos basados en bases de datos de registros de pacientes, que incluyeron 4,151 participantes. El rango de duración de los dispositivos fueron 1.6 a 25 días, dependiendo el tipo de dispositivo. La proporción de pacientes en "terapia puente a terapia definitiva" fueron 3 al 30% y la mayoría de los pacientes tenían cardiomiopatía terminal (12-35%)164. Thiele et al. evaluó la efectividad de los dispositivos MCS en pacientes en shock cardiogénico. Los autores incluyeron 4 ECAs (148 pacientes), en todos los estudios se utilizó un balón de contrapulsación aórtico de control. No hubo diferencia en la mortalidad a 30 días (RR 1.01; IC95% 0.70; 1.44) entre los grupos MCS y el grupo control. Hubo una disminución de las cifras de lactato arterial (DM –1.36 mmol/L, IC95% –2.52; 0.19) pero el índice cardiaco no mostró diferencias (DM 0.32; IC95%; –0.24; 0.87). No hubo diferencias en la incidencia de isquemia en miembros pélvicos, aunque si hubo una mayor frecuencia de sangrados en los dispositivos MCS en comparación al grupo control (RR 2.50; IC95%: 1.55; 4.04)165.
Pregunta 39: ¿Cuáles son los datos clínicos y paraclínicos para identificar un evento de empeoramiento de insuficiencia cardiaca crónica?
Recomendación:
– Se recomienda vigilar la clase funcional, el peso corporal, la presión arterial, las variaciones en el peso corporal, la presencia de congestión pulmonar, el edema periférico y datos clínicos como lipotimia o síncope en toda consulta de evaluación en pacientes con insuficiencia cardiaca crónica con miras a detectar eventos de empeoramiento.
– Se recomienda que todo paciente con insuficiencia cardiaca crónica y su entorno reciban capacitación sobre datos de alarma (deterioro de la clase funcional, retención de líquidos, lipotimia, síncope, dolor torácico), con el propósito de identificar tempranamente eventos de empeoramiento y solicitar auxilio médico en forma inmediata.
– Siempre que sea posible se deberán utilizar cuestionarios clinimétricos, como el KCCQ, para identificar la evolución clínica de los pacientes con insuficiencia cardiaca crónica y evaluar posibles eventos de empeoramiento o progresión de la enfermedad.
– Las elevaciones de las concentraciones sanguíneas de péptidos natriuréticos y de antígeno carbohidrato Ca-125 son útiles para precisar eventos de empeoramiento, por lo que es recomendable utilizar estos parámetros en el seguimiento estructurado de los pacientes con insuficiencia cardiaca crónica.
– Es recomendable solicitar niveles séricos de creatinina, nitrógeno ureico y transaminasas hepáticas como parte del seguimiento y de la evaluación de los pacientes con insuficiencia cardiaca crónica, ya que su elevación puede considerarse como marcador bioquímico de compromiso extracardiaco y se asocia con episodios de empeoramiento.
Nivel de evidencia 1+, grado de recomendación A (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
El consenso mexicano de insuficiencia cardiaca define un evento de empeoramiento de la insuficiencia cardiaca como aquel que se caracteriza por síntomas y signos manifestados como congestión pulmonar o sistémica con o sin disminución de la FEVI y es habitualmente resultado de una sobrecarga hemodinámica o daño cardiaco agudo2. Es vital reconocer el compromiso hemodinámico en estos pacientes y atenderlos de manera urgente. Los datos clínicos más relevantes son disnea progresiva, retención hídrica, crepitación pulmonar y edema periférico, datos de bajo gasto como hipotensión arterial, anuria y diaforesis. Habitualmente, es importante considerar todos los datos clínicos y resultados de estudios de gabinete para poder establecer el diagnóstico de empeoramiento de la insuficiencia cardiaca2. Es importante que los servicios de urgencias tengan gente capacitada para el manejo integral de estos pacientes. Los estudios de gabinete y laboratorio que deben de estar disponibles son un electrocardiograma, radiografías de tórax, biomarcadores como péptidos natriuréticos y troponinas, ecocardiograma y ultrasonido pulmonar2 (Fig. 9).
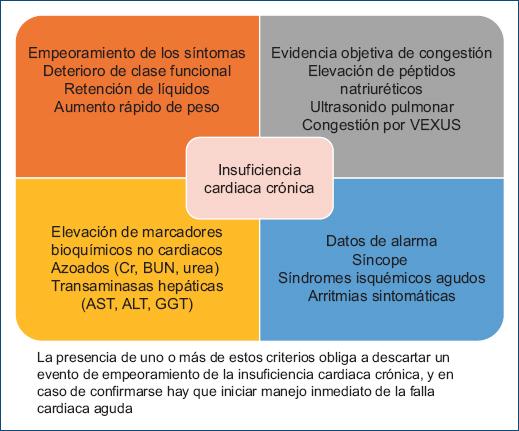
Figura 9 Reconocimiento temprano de episodios de empeoramiento en la insuficiencia cardiaca crónica.
Las GPC de la AHA/ACC 20224 recomiendan en los pacientes con descompensación una evaluación integral por un equipo multidisciplinario en una clínica especializada. La elevación de las presiones de llenado cardiacas derecha e izquierda normalmente se incrementan proporcionalmente a la descompensación de la insuficiencia, aunque un 25% de los pacientes no muestran esa correlación. La elevación de los BNP, son útiles en el contexto de los pacientes hospitalizados, sin embargo, su precisión diagnóstica disminuye con la obesidad y la sepsis. Es importante en todo momento descartar estados de hipoperfusión, y la determinación de lactato sérico nos es útil en estos casos. La evaluación de trastornos del ritmo es crucial en estos pacientes, debido a la frecuencia de empeoramiento de la insuficiencia cardiaca por esas causas. El establecimiento del volumen corporal óptimo es una de las metas más importantes en estos pacientes, debido a que tienen un riesgo elevado de re-hospitalización4.
Pregunta 40: ¿Cuál es el protocolo de atención para dar continuidad al tratamiento de los pacientes después de un evento de empeoramiento de su insuficiencia cardiaca crónica?
Recomendación:
– Se debe considerar que todo paciente con insuficiencia cardiaca crónica, después de un episodio de empeoramiento, se encuentra en un periodo vulnerable de la enfermedad que puede prolongarse hasta 6 meses tras el evento agudo.
– En los pacientes hospitalizados por un evento de empeoramiento de su insuficiencia cardiaca crónica se debe garantizar que antes del egreso hospitalario se inicie o se optimice el tratamiento modificador de la enfermedad (INRA/IECA, BB, ARM, iSGLT2).
– Es imprescindible que después del alta hospitalaria todos los pacientes reciban una evaluación clínica (presencial o remota) en un tiempo no mayor de 14 días con el propósito de conocer el estado clínico, identificar datos de congestión residual y continuar la optimización del manejo farmacológico.
– Las citas subsecuentes se deberán programar dependiendo del estado clínico y del nivel de riesgo de cada paciente en forma individual.
– Siempre que sea posible, los pacientes en periodo vulnerable deben ser referidos a un programa estructurado de manejo de la insuficiencia cardiaca para su seguimiento y control.
Nivel de evidencia 1+, grado de recomendación A (recomendación fuerte).
REVISIÓN DE LA LITERATURA Y ANÁLISIS
Las GPC AHA/ACC 20224 recomiendan en los pacientes con empeoramiento de la insuficiencia cardiaca ingresados en un hospital para su atención, la continuación de la terapia farmacológica óptima en la medida de lo posible. En los pacientes con una disminución de la función renal o una disminución de la presión arterial asintomática durante la hospitalización, no se recomienda descontinuar los diuréticos ni el resto de los medicamentos dentro de la terapia farmacológica óptima. En los pacientes ICFEr, la terapia farmacológica óptima debe de reiniciarse una vez que se ha conseguido la estabilización del paciente, incluso, en los pacientes a los que se les descontinuó la terapia durante su manejo inicial4. En el estudio OPTIMIZE-HF (Organized Program to Initiate Lifesaving Treatment in Hospitalized Patients with Heart Failure)166 se reportó que la suspensión de los BB se asoció a una mayor mortalidad. De la misma manera, la interrupción de los BRA, también se asociaron a una mayor mortalidad después del alta hospitalaria. Otros estudios sugieren que el beneficio de valsartán se mantienen incluso en pacientes con hipotensión arterial. Algunos reportes sugieren también un efecto benéfico de la espironolactona y los BB en pacientes con insuficiencia cardiaca y empeoramiento de la función renal. El uso de BB en el alta se ha asociado a una disminución de la mortalidad a los 30 días y de readmisión a los 4 años, sin embargo, se sugiere tener precaución en pacientes que requirieron soporte con inotrópicos. El inicio de BRA en estos pacientes se asocia a una reducción de la mortalidad a los 30 días y a 1 año y de readmisión a los 30 días. Algunos estudios señalan que son pocos los pacientes que reciben terapia farmacológica óptima (BB [18.7%], BRA [10.8%] o iRNA [2.0%]). Estudios han demostrado que hay una disminución gradual de la mortalidad o de la re-hospitalización en pacientes con triple terapia, doble terapia y monoterapia, en orden decreciente4.
La terapia de descongestión es una parte importante del manejo hospitalario de los pacientes con descompensación aguda de la insuficiencia cardiaca. La GPC AHA/ACC 20224 recomienda valorar el inicio de diuréticos de asa endovenosos para mejorar los síntomas y la mortalidad. Las dosis de los medicamentos deben de ser tituladas con la finalidad de resolver la evidencia clínica de congestión para conseguir la mejoría clínica de los pacientes. Es primordial establecer un plan de disminución de los diuréticos en los pacientes que se han dado de alta para de esta manera disminuir el riesgo de re-hospitalización. Cuando la diuresis es inadecuada se puede considerar un incremento de la dosis de los diuréticos de asa o agregar un segundo diurético. Aunque es universal la recomendación del uso de diuréticos de asa en pacientes con empeoramiento de la insuficiencia cardiaca, no hay estudios clínicos controlados que hayan evaluado su eficacia4.
Una revisión descriptiva publicada por Njoroge et al. en 2021167 concluye que no existen terapias novedosas con suficiente evidencia científica para ser autorizados por la mayoría de los ministerios de salud para el tratamiento de la insuficiencia crónica descompensada167. Es importante mejorar el entendimiento de todos los procesos fisiopatológicos de esta condición de empeoramiento a un nivel celular y molecular, lo que podría brindarnos futuros blancos terapéuticos que pudieran mejorar la mortalidad y disminuir las tasas de readmisión de estos pacientes, fueron las conclusiones de los autores167.
Actualización
Se planea la actualización de la Guía de Práctica Clínica para incorporar nueva evidencia científica a las recomendaciones en un periodo de 3 a 4 años.
Información importante
Esta Guía de Práctica Clínica y los documentos que sean publicados con base en ella representan herramientas originadas por el consenso de expertos clínicos acerca de las terapias y toma de decisiones vigentes para el manejo de la insuficiencia cardiaca. Este documento ha sido publicado para que los especialistas consideren las recomendaciones clínicas y las incorporen a la toma de decisiones de su práctica clínica cotidiana. Sin embargo, estas recomendaciones no se encuentran por arriba del criterio clínico independiente de cada médico y de las condiciones individuales de cada paciente.











 nueva página del texto (beta)
nueva página del texto (beta)