Introducción
Cuando se ocluye una arteria coronaria, se producen cambios perjudiciales en los capilares y arteriolas cardiacas. Después del alivio de la oclusión, el flujo de sangre al tejido isquémico aún puede verse impedido, un fenómeno conocido como no reflujo1. Por lo tanto, el fenómeno de falta de reflujo se define como una perfusión miocárdica inadecuada en un segmento dado de la circulación coronaria sin evidencia angiográfica de obstrucción vascular mecánica2.
Se sospecha clínicamente que no hay reflujo si, a pesar de la reperfusión exitosa, hay recurrencia del dolor, hipotensión y persistencia de las anomalías de las ondas ST y T3. Cuanto más prolongada la isquemia, más probable es que ocurra el fenómeno de no reflujo4. La incidencia del fenómeno de reflujo varía ampliamente según los estudios disponibles, la complejidad del paciente y los métodos de diagnóstico utilizados5. Usando el criterio de grado de flujo TIMI (thrombolysis in myocardial infarction) ≤ 2 sin obstrucción macrovascular, la incidencia de falta de reflujo durante la intervención coronaria percutánea (ICP) ha oscilado entre el 7 y el 25% en algunos estudios5-7.
Antecedentes
Los estudios que investigaron la relación entre el perfil inflamatorio y el fenómeno de no reflujo mostraron que los pacientes de edad avanzada (> 65 años) tienen tasas más altas de no reflujo, debido a un estado proinflamatorio más pronunciado8. Se han identificado otros factores como la hipertensión, el tabaquismo, la dislipidemia, la diabetes, la insuficiencia renal y otros procesos inflamatorios que presagian un mayor riesgo de no reflujo9-11. Al mostrar que la presencia de fibrilación auricular se asocia con un aumento del doble del riesgo de desarrollar reflujo en pacientes con infarto de miocardio con elevación del segmento ST (IAMCEST), Kaya et al.12 confirmaron el concepto de que una mayor carga trombótica se asocia con un mayor riesgo de ausencia de reflujo.
Como observaron Krug y Kloner2,13, cuanto más tiempo permanecía ocluida la arteria, era menos probable que recuperara el flujo normal, por lo que un tiempo puerta-balón menor se asocia con menos lesión miocárdica y una menor incidencia de no reflujo9.
Mecanismos fisiopatológicos
El fenómeno de no reflujo fue descrito por primera vez por Krug et al.13 y más tarde Kloner et al. demostraron en modelos animales experimentales que la isquemia prolongada altera la perfusión y conduce al daño de la microvasculatura arterial, que es proporcionalmente mayor con periodos de isquemia más largos2.
El no reflujo está relacionado con una alteración funcional y estructural de la microcirculación coronaria y podemos enumerar cuatro mecanismos fisiopatológicos principales: embolización aterotrombótica distal, daño isquémico, daño por reperfusión y susceptibilidad individual al daño microvascular.
Todos estos factores interactúan entre sí; una placa aterosclerótica compleja puede conducir a fenómenos de embolización distal tanto en la fase aguda como durante la angioplastia, lo que lleva a un aumento de la resistencia vascular distal y microinfartos adicionales que promueven la liberación de sustancias proinflamatorias y vasoconstrictoras14,15. El daño isquémico da como resultado la muerte de los cardiomiocitos, las células endoteliales y la formación de edema intersticial con producción deficiente de óxido nítrico y la subsiguiente obstrucción de la microcirculación favorecida por la liberación de factores de crecimiento endotelial vascular, que aumentan la permeabilidad vascular16,17. La lesión por reperfusión, por otro lado, es causada por la restauración abrupta del flujo sanguíneo a nivel de la microcirculación dañada, causa daño directo a los cardiomiocitos con una afluencia de neutrófilos inflamatorios durante la reperfusión que promueve la producción de citocinas inflamatorias, radicales libres de oxígeno, sustancias vasoactivas y enzimas proteolíticas18,19.
Estos eventos dan como resultado una cicatrización deficiente del área infartada y una remodelación adversa20. El tamaño del infarto es un determinante importante del pronóstico de los pacientes y se asocia con eventos clínicos y mortalidad cardiovascular21.
El fenómeno de no reflujo se correlaciona significativamente con malos resultados clínicos y representa un predictor independiente de muerte e infarto de miocardio9. La embolización distal es una de las causas más intuitivas de no reflujo. El material tromboembólico puede originarse a partir de trombos coronarios epicárdicos y de placas fisuradas durante la ICP primaria22. La lesión isquémica produce cambios morfológicos de las células endoteliales (protuberancias y cuerpos unidos a la membrana), que pueden contribuir a la obliteración luminal. La consiguiente pérdida del tono vascular provoca la extravasación de eritrocitos, lo que da como resultado un edema intersticial que comprime aún más la circulación microvascular13.
La reperfusión después de la isquemia representa una etapa traumática para la microcirculación coronaria, con plaquetas y neutrófilos infiltrándose extensamente en ella y formando agregados que obstruyen los capilares y, en consecuencia, bloquean el flujo23.
Metodología
- Objetivo primario. Crear un modelo de regresión multivariante que prediga la aparición del fenómeno de no reflujo en pacientes con IAMCEST en el Instituto Nacional de Cardiología Ignacio Chávez del 2006 al 2021.
- Objetivos secundarios. Determinar la prevalencia, los factores de riesgo y el impacto en la mortalidad del fenómeno de no reflujo en pacientes con IAMCEST en el Instituto Nacional de Cardiología Ignacio Chávez del 2006 al 2021.
- Criterios de inclusión. En resumen, los pacientes eran elegibles para la inclusión si cumplían con los siguientes criterios: edad ≥ 18 años, infarto agudo de miocardio, menos de 12 horas desde el inicio de los síntomas y que hubieran sido llevados a angioplastia coronaria percutánea primaria.
- Criterios de exclusión. Pacientes a los que no se les realizó angioplastia, pacientes con más de 12 horas desde el inicio de los síntomas.
Para el presente estudio el fenómeno de no reflujo se definió como grados de flujo sanguíneo TIMI 0-1 posteriores a la ICP primaria en ausencia de estenosis residual posterior al procedimiento ≥ 25%, cierre abrupto del vaso, disección, perforación, trombo de la lesión diana original o espasmo epicárdico.
El punto final primario fue la mortalidad hospitalaria. Los criterios de valoración secundarios fueron evaluar las características clínicas, las opciones de tratamiento previas al procedimiento y las características angiográficas que pueden predecir el fenómeno de no reflujo.
Análisis estadístico
Las características basales y angiográficas de los pacientes se compararon mediante la prueba t de Student o la prueba de suma de rangos de Kruskal-Wallis para variables continuas y la prueba de χ2 de Pearson para variables categóricas, según correspondiera. Los resultados se presentan como porcentajes para las variables categóricas, media ± desviación estándar (DE) o mediana y rango percentil intercuartílico (RIC) para las variables continuas. Se realizó un análisis de regresión logística multivariante para identificar los predictores independientes de mortalidad hospitalaria en los pacientes que presentaban el fenómeno de no reflujo en comparación con los pacientes sin reflujo durante la ICP primaria. Se realizó otro análisis de regresión logística multivariante para identificar los predictores independientes del fenómeno de no reflujo. Los resultados se presentan como razones de probabilidad (OR, odds ratio) e intervalo de confianza del 95% (IC 95%). Las covariables constantes incluidas en los análisis fueron: sexo, edad, factores de riesgo cardiovascular (antecedentes de diabetes, antecedentes de hipertensión, tabaquismo), historia clínica de cardiopatía isquémica (infarto de miocardio previo, ICP anterior e injerto de derivación de arteria coronaria anterior), historia clínica de trastornos cardiovasculares (enfermedad arterial periférica previa, ictus previo y/o accidente isquémico transitorio previo) y gravedad de la presentación clínica (IAMCEST, clase Killip ≥ 2, presión arterial sistólica y frecuencia cardiaca). Para todos los análisis, la significación estadística se definió como un valor de p < 0.05. La evaluación estadística se realizó mediante IBM SPSS Statistic 26 (Armonk, NY: IBM Corp.).
Resultados
En la tabla 1 se presentan los resultados: en la primera columna se encuentra las variables estudiadas y la dimensional, según corresponda; en la segunda columna el grupo de estudio, los pacientes que presentaron fenómeno de no reflujo, es decir, flujo final TIMI ≤ 2, que de aquí en adelante se llamará grupo de estudio; en la tercera columna los pacientes con flujo TIMI 3, que de aquí en adelante se llamará grupo control, y en la última columna se presenta el grado de significancia estadística (valor de p) para cada variable. La prueba estadística utilizada para comparar los grupos se describe en la metodología.
Tabla 1 Características basales de los pacientes
| Flujo TIMI ≤ 2 (n = 413) | Flujo TIMI = 3 (n = 2,050) | Valor de p | |
|---|---|---|---|
| n (%) | |||
| Edad media (RIC), años | 60 (53-69.5) | 59 (51-66) | 0.001 |
| Mujeres | 73 (17.7) | 286 (14.0) | 0.051 |
| IMC media (RIC), kg/m2 | 26.98 (24.85-29.41) | 27.16 (24.97-29.41) | 0.441 |
| Inicio de síntomas a SU, media (RIC), min | 270 (174-410) | 247 (140-386) | 0.001 |
| SU a balón, media (RIC), min | 75 (60-95) | 80 (60-97) | 0.434 |
| Antecedentes | |||
| Angina | 24 (5.8) | 178 (8.7) | 0.052 |
| Infarto de miocardio | 48 (11.6) | 378 (18.4) | 0.001 |
| Insuficiencia cardiaca | 15 (3.6) | 66 (3.2) | 0.668 |
| Diabetes | 164 (39.7) | 687 (33.5) | 0.016 |
| Hipertensión | 195 (47.2) | 997 (48.6) | 0.599 |
| Evento cerebrovascular | 3 (0.7) | 41 (2) | 0.075 |
| Enfermedad arterial periférica | 0 (0) | 19 (0.9) | 0.059 |
| Hiperlipidemia | 119 (28.8) | 684 (33.4) | 0.072 |
| Fumador activo | 133 (32.2) | 701 (34.2) | 0.435 |
| Fumador inactivo | 116 (28.1) | 590 (28.8) | 0.776 |
| ICP | 28 (6.8) | 243 (11.9) | 0.003 |
| CRC | 3 (0.7) | 32 (1.6) | 0.191 |
| Tratamiento previo | |||
| Aspirina | 60 (14.5) | 441 (21.5) | 0.001 |
| Inhibidores de la ECA | 74 (18.3) | 442 (22.2) | 0.085 |
| Bloqueadores de los RA | 46 (11.4) | 282 (14.2) | 0.153 |
| Estatinas | 54 (13.1) | 357 (17.4) | 0.030 |
| Presentación | |||
| Pulso, media (RIC), latidos/min | 80 (70-92) | 80 (70-90) | 0.987 |
| Presión arterial sistólica, media (RIC), mmHg | 128 (112-150) | 132 (120-150) | < 0.001 |
| Presión arterial sistólica, media (RIC), mmHg | 80 (70-90) | 80 (70-90) | 0.033 |
| Presión arterial media, media (RIC), mmHg | 96.6 (85.3-110) | 99 (87.3-113) | 0.004 |
| Killip y Kimball clase > 1 | 153 (37) | 541 (26.4) | < 0.001 |
| Infarto de miocardio anterior | 229 (55.4) | 980 (47.8) | 0.005 |
| Datos de angiografía-inicial | |||
| Arteria responsable | 0.002 | ||
| Tronco coronario izquierdo | 5 (1.2) | 9 (0.4) | |
| Descendente anterior | 231 (55.9) | 960 (47.8) | |
| Circunfleja | 30 (7.3) | 249 (12.1) | |
| Coronaria derecha | 146 (35.4) | 801 (39.1) | |
| Otra | 1 (0.2) | 11 (0.5) | |
| Flujo TIMI inicial, grado | < 0.001 | ||
| 0 | 314 (76.0) | 1393 (68) | |
| 1 | 49 (11.9) | 171 (8.3) | |
| 2 | 35 (8.5) | 334 (16.3) | |
| 3 | 15 (3.6) | 152 (7.4) | |
| TMP inicial, grado | < 0.001 | ||
| 0 | 58 (14.1) | 92 (4.5) | |
| 1 | 96 (23.3) | 91 (4.4) | |
| 2 | 144 (34.9) | 434 (21.2) | |
| 3 | 115 (27.8) | 1433 (69.9) | |
| Uso de inhibidores de la GP IIb/IIIa | 213 (51.6) | 717 (35) | < 0.001 |
| Estado a los 30 días | |||
| Muerto | 69 (16.7) | 88 (4.29) | < 0.001 |
TIMI: thrombolysis in myocardial infarction; RIC: rango intercuartil; IMC: índice de masa corporal; SU: servicio de urgencias; ICP: intervención coronaria percutánea; CRC: cirugía de revascularización coronaria; ECA: enzima convertidora de angiotensina; RA: receptor de angiotensina; TMP: TIMI myocardial perfusion; GP: glucoproteína.
Las variables se encuentran agrupadas en características generales, historia médica previa, tratamiento médico previo, variables a la presentación en el servicio de urgencias, datos angiográficos y finalmente estado a los 30 días.
La edad promedio en el grupo de estudio fue de 60 años, con un rango intercuartil (RIC) de 53 a 69.5 años y la edad promedio del grupo control fue de 59 años, RIC de 51 a 66 años, con un valor de p de 0.001. El 17.7% de los pacientes eran de sexo femenino en el grupo de estudio y el 14% en el grupo control, con un valor de p de 0.051. El tiempo promedio de inicio de los síntomas a la llegada al servicio de urgencias fue de 270 minutos en el grupo de estudio, con un RIC de 174 a 410 minutos, y en el grupo control fue de 247 minutos, RIC de 140 a 386 minutos, con un valor de p de 0.001. El tiempo desde la llegada a urgencias al paso de la guía (balón), fue de 75 minutos en el grupo de estudio y 80 minutos en el grupo control, valor de p de 0.434.
En tratamiento médico previo el 14.5% de los pacientes en el grupo de estudio reportaron uso de aspirina y el 21.5% en el grupo control, con un valor de p 0.001. El 18.3% de los pacientes usaban inhibidores de la enzima convertidora de angiotensina en el grupo de estudio y el 22.2% en el grupo control, con un valor de p de 0.085. El 11.4% de los pacientes en el grupo de estudio reportaron usar antagonista de los receptores de angiotensina II y el 14.2% de los pacientes en el grupo control reportaron usarlos, con un valor de p de 0.153. Finalmente, el 13.1% de los pacientes reportaron usar estatinas en el grupo control y el 17.4% de los pacientes en el grupo control, con un valor de p de 0.030.
En las variables de historial médico: el 5.8% de los pacientes en el grupo de estudio reportaron angina y el 8.7% de los pacientes en el grupo control, con un valor de p de 0.052; el 11.6% de los pacientes tuvieron un infarto previo en el grupo de estudio y el 18.4% en el grupo control, con un valor de p de 0.001 y, finalmente, el 6.8% de los pacientes en el grupo de estudio tuvieron una angioplastia previa y el 11.9% de los pacientes en el grupo control, con un valor de p de 0.003.
En las variables a la presentación en el servicio de urgencias: la frecuencia cardiaca media fue de 80 latidos por minuto (lpm) en el grupo de estudio, con un RIC de 70 a 92 lpm, y en el grupo control fue de 80 lpm con un RIC de 70 a 90 lpm, con un valor de p de 0.987; la presión arterial sistólica media fue de 128 milímetros de mercurio (mmHg) en el grupo de estudio, con un RIC de 112 a 150 mmHg, y en el grupo control fue de 132 mmHg con un RIC de 120 a 150 mmHg, con un valor de p < 0.001; el 37% de los pacientes en el grupo de estudio tuvieron una clasificación en la escala de Killip y Kimball > 1 y el 26.4% en el grupo control, con un valor de p ≤ 0.001; en el grupo de estudio el 55.44% de los pacientes tuvieron un infarto anterior y el 47.8% de los pacientes en el grupo control, con un valor de p de 0.005.
Las características en la angiografía coronaria tuvieron la siguiente distribución: en el grupo de estudio el 55.9% de los pacientes tuvieron la arteria descendente anterior como la arteria responsable del infarto, el 35.4% a la coronaria derecha y el 7.3% a la circunfleja, en el grupo control en el 47.8% la arteria responsable fue la descendente anterior, en el 39.1% fue la coronaria derecha y en el 12.1% la circunfleja, con un valor de p de 0.002.
El flujo final según la clasificación de TIMI fue en el grupo de estudio grado 0 en el 76% de los pacientes, grado 1 en el 11.9%, grado 2 en el 8.5% y grado 3 en el 3.6%, y en el grupo control fue grado 0 en el 68%, grado 1 en el 8.3%, grado 2 en el 16.3% y grado 3 en el 7.4%, con un valor de p ≤ 0.001.
La perfusión miocárdica, según la clasificación TIMI myocardial perfusion (TMP), fue grado 0 en el 14.1% de los pacientes en el grupo de estudio, grado 1 en el 23.3%, grado 2 en el 34.9% y grado 3 en el 27.8%, y en el grupo control fue grado 0 en el 4.5% de los pacientes, grado 1 en el 4.4%, grado 2 en el 21.2% y grado 3 en el 69.9%, con un valor de p ≤ 0.001. Finalmente, a los 30 días el 16.7% de los pacientes en el grupo de estudio y el 4.29% en el grupo control habían fallecido, con un valor de p ≤ 0.001.
Los pacientes en el grupo de estudio recibieron un inhibidor de la glucoproteína IIb/IIIa en un 51.6% de los casos, mientras que en el grupo control un 35.0% de los casos recibieron inhibidor de la glucoproteína IIb/IIIa, valor de p ≤ 0.001.
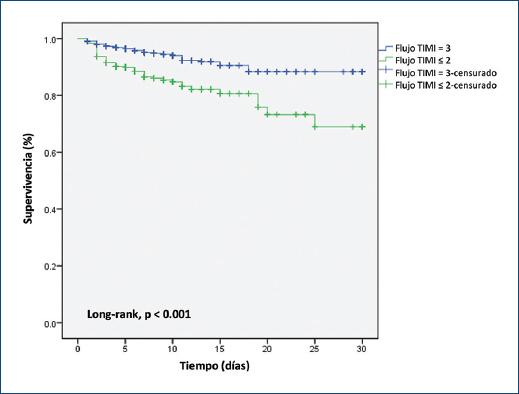
En la figura 1 se presentan las curvas de supervivencia de los grupos (Kaplan-Meier), en azul el grupo control, es decir, el grupo con flujo TIMI 3, y en color verde se grafica el grupo de estudio, es decir, el grupo con flujo TIMI ≤ 2. En el eje de ordenadas se encuentra el porcentaje de supervivencia y en el de abscisas el tiempo, expresado en días. Con una separación de las curvas desde el día 3 que continúan separándose hasta el día 30 y valor de p < 0.001 para la prueba de significancia estadística (long-rank test).
En la tabla 2 se presentan las complicaciones intrahospitalarias.
En la tabla 3 se resume el modelo de regresión logística univariante, en el que se identificaron las variables que predijeron la aparición del fenómeno de no reflujo. Las variables incluidas en este modelo fueron seleccionadas a partir de las variables con diferencia entre grupos en el análisis relacional. Las variables fueron dicotomizadas, en el caso de las variables continúas, según lo descrito en la literatura. En la tabla 2 se muestran el coeficiente b, el error estándar, la OR, los IC 95% y el valor de p. Resaltan, entre otras, que la angioplastia coronaria transcutánea percutánea previa y el infarto agudo de miocardio previo fueron factores protectores con una OR de 0.541 y 0.582, y un IC 95% de 0.361 a 0.812 y 0.422 a 0.802, con un valor de p de 0.003 y 0.001, respectivamente; que el tiempo puerta-balón mayor a 60 minutos no fue estadísticamente significativo, con una OR de 0.923 y un IC 95% de 0.717 a 1.187, con un valor de p de 0.532, al igual que la tasa de filtrado glomerular comprendida entre 30 a 60 ml/min/1.73 m2, con una OR de 1.265 y un IC 95% de 0.964 a 1.661, con un valor de p de 0.091. Por último, el lactato mayor a 2.5 mmol/l tampoco resultó ser una variable predictora del fenómeno de no reflujo, con una OR de 1.311, un IC 95% de 0.924 a 1.859 y un valor de p de 0.131.
Tabla 2 Complicaciones
| Flujo TIMI ≤ 2 (n = 413) | Flujo TIMI = 3 (n = 2,050) | Valor de p | |
|---|---|---|---|
| n (%) | |||
| Choque cardiogénico | 59 (14.3) | 57 (2.8 | < 0.001 |
| Edema pulmonar | 17 (4.1) | 26 (1.3) | < 0.001 |
| Evento cerebrovascular | 4 (1) | 6 (0.3) | 0.071 |
| Bloqueo AV* | 29 (7.0) | 66 (4.2) | 0.020 |
| Fibrilación atrial/aleteo atrial | 23 (5.6) | 53 (2.6) | 0.002 |
| Taquicardia ventricular/fibrilación ventricular | 74 (17.9) | 152 (7.4) | 0.001 |
| Sangrado mayor | 10 (2.4) | 17 (0.8) | 0.009 |
| Trombosis subaguda | 3 (0.7) | 19 (0.9) | 0.999 |
*Segundo y tercer grado. TIMI: thrombolysis in myocardial infarction; AV: atrioventricular.
Tabla 3 Modelo de regresión logística univariante
| b | EE | OR | IC 95% | p | ||
|---|---|---|---|---|---|---|
| Inf. | Sup. | |||||
| Edad > 65 años | 0.276 | 0.113 | 1.318 | 1.056 | 1.647 | 0.015 |
| Diabetes | 0.268 | 0.111 | 1.307 | 1.051 | 1.624 | 0.016 |
| ACTP previa | 0.615 | 0.207 | 0.541 | 0.361 | 0.812 | 0.003 |
| IAM previo | 0.542 | 0.164 | 0.582 | 0.422 | 0.802 | 0.001 |
| PAS < 100 mmHg | 0.62 | 0.197 | 1.858 | 1.262 | 2.736 | 0.002 |
| KK ≥ 2 | 0.496 | 0.114 | 1.641 | 1.314 | 2.051 | < 0.001 |
| Tiempo de retraso > 240 min | 0.35 | 0.111 | 1.419 | 1.144 | 1.761 | 0.001 |
| Puerta balón > 60 min | 0.08 | 0.129 | 0.923 | 0.717 | 1.187 | 0.532 |
| Infarto anterior | 0.307 | 0.108 | 1.359 | 1.099 | 1.681 | 0.005 |
| Glucosa > 180 mg/dl | 0.385 | 0.109 | 1.471 | 1.187 | 1.819 | < 0.001 |
| Leucocitos > 10 x 109 | 0.401 | 0.121 | 1.493 | 1.177 | 1.894 | 0.001 |
| TFG de 30 a 60 ml/min/1.73 m2 | 0.235 | 0.139 | 1.265 | 0.964 | 1.661 | 0.091 |
| TFG < 30 ml/min/1.73 m2 | 0.698 | 0.252 | 2.009 | 1.225 | 3.295 | 0.006 |
| Albúmina < 3.5 g/l | 0.329 | 0.126 | 1.39 | 1.087 | 1.777 | 0.009 |
| pH < 7.2 | 1.163 | 0.373 | 3.199 | 1.541 | 6.642 | 0.002 |
| HCO3 < 18 mmol/l | 0.487 | 0.118 | 1.628 | 1.293 | 2.051 | < 0.001 |
| Lactato > 2.5 mmol/l | 0.27 | 0.178 | 1.311 | 0.924 | 1.859 | 0.131 |
| PCR | 0.003 | 0.001 | 1.003 | 1.001 | 1.004 | 0.004 |
IC: intervalo de confianza; b: coeficiente b; EE: error estándar; OR: odds ratio; Inf.: inferior; Sup.: superior; ACTP: angioplastia coronaria transcutánea percutánea; IAM: infarto agudo de miocardio; PAS: presión arterial sistólica; KK: Killip y Kimball; min: minutos; TFG: tasa de filtrado glomerular; PCR: proteína C reactiva.
En la tabla 4 se resume el modelo de regresión logística multivariante, en el que se incluyeron todas las variables identificadas en el modelo de regresión logística univariante (Tabla 2) y fueron eliminadas sucesivamente hasta obtener el modelo que se muestra en la tabla 3. La bondad del modelo, calculada por medio del R2 de Nagelkerke, fue de 0.047.
Tabla 4 Modelo de regresión logística multivariante
| b | EE | OR | IC 95% | p | ||
|---|---|---|---|---|---|---|
| Inf. | Sup. | |||||
| Edad > 65 años | 0.285 | 0.134 | 1.331 | 1.023 | 1.729 | 0.033 |
| Tiempo de retraso > 240 min | 0.265 | 0.116 | 1.304 | 1.038 | 1.638 | 0.023 |
| IAM previo | 0.504 | 0.176 | 0.604 | 0.427 | 0.853 | 0.004 |
| IAM anterior | 0.343 | 0.114 | 1.411 | 1.127 | 1.763 | 0.003 |
| Glucosa > 180 mg/dl | 0.233 | 0.115 | 1.262 | 1.007 | 1.581 | 0.043 |
| Leucocitos > 10 x109 | 0.338 | 0.129 | 1.402 | 1.091 | 1.804 | 0.009 |
| Albúmina < 3.5 g/dl | 0.244 | 0.133 | 1.277 | 0.984 | 1.657 | 0.661 |
| HCO3- < 18 mmol/l | 0.396 | 0.125 | 1.485 | 1.163 | 1.898 | 0.002 |
IC: intervalo de confianza; b: coeficiente b; EE: error estándar; OR: odds ratio; Inf.: inferior; Sup.: superior; min: minutos; IAM: infarto agudo de miocardio.
Discusión
Desde 1994 se han reportado estudios que indican incidencias tan bajas como el 2.0%7, mientras que algunos más recientes indican un porcentaje del 2.5%24. Sin embargo, se considera que la incidencia se sitúa en un rango amplio que va desde el 2.0 hasta el 50%5,7,24,25. Esto sugiere que el fenómeno de no reflujo continúa siendo una complicación frecuente en las angioplastias primarias. Desde el año 2006 hasta el 2021 se realizaron 2,463 angioplastias primarias en el Instituto Nacional de Cardiología, y la incidencia del fenómeno de no reflujo fue del 16.7%.
Estudios publicados reportan que el fenómeno de no reflujo es más frecuente en pacientes mayores de 65 años6,24,26-28. La edad promedio en este estudio fue más baja, con medias de 60 y 59 años, para el grupo de no reflujo y el grupo control, respectivamente. A pesar de que ambas medias son similares, se observó una mayor dispersión de la edad en los pacientes que presentaron no reflujo.
El porcentaje de mujeres que presentaron no reflujo fue mayor que en el grupo control, aunque esta diferencia no alcanzó significación estadística. Resalta que la proporción de mujeres fue menor que la de los hombres en ambos grupos. Las causas van más allá del alcance de esta investigación.
El tiempo de retraso prehospitalario, comprendido desde el inicio de los síntomas hasta la llegada del paciente al servicio de urgencias, ha sido reportado en numerosos estudios como un factor asociado al desarrollo del fenómeno de no reflujo. Por ejemplo, Aggarwa et al.29 reportaron una asociación del fenómeno de no reflujo con pacientes reperfundidos ≥ 6 horas desde el inicio de los síntomas, un hallazgo similar reportado por Nair-Rajesh et al.30, con un tiempo de reperfusión promedio de 6.3 horas ± 2.76 horas en los pacientes que presentaron no reflujo, comparado con 4.50 ± 2.86 horas en el grupo con flujo final normal (p < 0.001). Este hallazgo probablemente refleje la fisiopatología subyacente del fenómeno de no reflujo, como fue descrito por Klooner et al.2. El tiempo de retraso prehospitalario en este estudio fue en promedio 270 minutos (4.50 horas), y fue mayor y con mayor dispersión en los pacientes que desarrollaron no reflujo que en los pacientes del grupo control. En los análisis univariante y multivariante, se utilizó el punto de corte preestablecido de > 240 minutos (4 horas), en este último se encontró un riesgo relativo de 1.3 (IC 95%: 1.03-1.6). Si bien, como se mencionó arriba, un retraso prehospitalario mayor a 6 horas se ha asociado como un factor de riesgo para desarrollar no reflujo, comparado con otros estudios, el retraso prehospitalario en este estudio se encuentra muy por arriba de la media reportada. Oyanati et al.31 reportaron un tiempo de retraso promedio de 104 minutos (RIC: 56-204), en una cohorte de 603 pacientes en la región de Hokkaido, Japón. Goldbert et al.32, en un análisis del registro GRACE, reportó un retraso medio y mediano de 4.7 (282 minutos) y 2.3 horas (138 minutos), respectivamente. También encontró que aproximadamente el 41% de los pacientes con IAMCEST acudieron a los 94 hospitales del estudio dentro de las 2 horas siguientes al inicio de los síntomas coronarios agudos.
En los pacientes del grupo control el tiempo de retraso prehospitalario fue superior al punto de corte de 120 minutos establecido por las guías33,34. Incluso el RIC inferior se encuentra en 140 minutos, lo que indica que en menos del 25% de los pacientes la ICP fue realizada en menos de 120 minutos. Por otro lado, el tiempo puerta-balón no fue estadísticamente diferente entre los grupos, y aunque fue mayor a 60 minutos, lo recomendado por la guía de la Sociedad Europea de Cardiología33, el tiempo fue similar al reportado por Armstrong et al.35. Esto sugiere que, en términos generales, la duración total de la isquemia estuvo mayormente influenciada por el tiempo de retraso prehospitalario. No obstante, es esencial dirigir mayores esfuerzos hacia la reducción del tiempo puerta-balón, ya que periodos inferiores, dentro de una ventana de 90 minutos, están correlacionados con resultados más favorables a largo plazo36.
Se observó que el antecedente de diabetes mellitus fue más prevalente en el grupo de estudio, con un 39.7% de los pacientes afectados en comparación con el 33.5% en el grupo control, con un valor de p de 0.016. Aunque no se indagó si la diabetes estaba controlada o no. Además, el antecedente de angioplastia previa también fue menos común en los pacientes con fenómeno de no reflujo, presentándose en solo el 6.8% de los casos, en comparación con el 11.9% en el grupo control, con un valor de p de 0.003.
En las características clínicas de los pacientes a su llegada al servicio de urgencias destacan dos variables. La primera, la tensión arterial sistólica, que fue menor en los pacientes del grupo de estudio, con una media de 128 mmHg, y una media de 132 mmHg en el grupo control, con un valor de p ≤ 0.001. Nuevamente una asociación reportada en estudios previos29,37,38, como un dato indirecto de contractibilidad, o reserva miocárdica. La segunda característica fue la clasificación de Killip y Kimball, una clasificación que evalúa la presencia de insuficiencia cardiaca secundaria al infarto agudo de miocardio39, con grados mayores a 1 directamente asociados a una mayor mortalidad subsecuente39-41. El grupo de estudio tuvo una mayor proporción de pacientes en las categorías > 1, siendo esta del 37%, en comparación con el 26.4% en el grupo control, con un valor de p < 0.001.
La arteria responsable del infarto en grupo de estudio en el 55.9% de los infartos fue la descendente anterior, contra el 47.8% de los infartos en el grupo control, con un valor de p para esta categoría de 0.002. El flujo inicial clasificado según la escala de TIMI, con una mayor mortalidad en todos los flujos ≤ 26, fue de TIMI 0 en el 76% de los casos del grupo de estudio contra 68% de los pacientes del grupo control, y fue TIMI 3 en el 3.6% de los casos en el grupo de estudio contra 7.4% en el grupo control. Lo cual, probablemente, traduce una mayor carga trombótica inicial, lo cual pueda justificar que la mitad de los pacientes del grupo de estudio recibieron un inhibidor de la glucoproteína IIb/IIIa como terapia de rescate.
La mortalidad fue cuatro veces mayor en los pacientes con no reflujo con respecto a los pacientes del grupo con flujo normal. Lo cual se ve representado en la figura 1, en donde las curvas de supervivencia se separan desde el día dos y continúan con la misma tendencia hasta el día 30. Y como se muestra en la tabla 2, las complicaciones postinfarto fueron mayores en los pacientes que desarrollaron no reflujo, en particular el choque cardiogénico fue casi 20 veces mayor en el grupo de no reflujo comparado con el grupo control, y también experimentaron más episodios de sangrado mayor.
A medida que nuestro entendimiento de la fisiopatología de la inflamación, daño celular, isquemia y necrosis vaya avanzando también surgirán nuevas formas de tratamiento, ya sea intervenciones, fármacos o una combinación de ambos, podremos disminuir las complicaciones causadas por el fenómeno de no reflujo en el ICP primario, que como se presenta en este estudio, tiene desenlaces fatales. En la opinión de este autor, las condiciones demográficas, sociales y socioculturales seguirán impidiendo que los pacientes acudan siempre en ventana terapéutica, será labor de los médicos encontrar estrategias que mejoren los desenlaces clínicos.











 nueva página del texto (beta)
nueva página del texto (beta)