Introducción
Los aneurismas y los divertículos ventriculares en su mayoría tienen un origen congénito y su etiología aún no se encuentra bien dilucidada, pero se considera que podría estar relacionada con la persistencia anormal del mesocardio ventral luego de la cuarta semana de vida embrionaria. Sin embargo, también se han documentado casos adquiridos durante la vida fetal o neonatal, debido a infecciones virales, anomalías coronarias o vasculitis que pueden generar debilidad local de la pared ventricular.
Su diagnóstico se realiza casi siempre mediante técnicas no invasivas, como la ecocardiografía o, en caso de dudas, con tomografía computarizada (TC) o resonancia magnética (RM).
A la fecha, dichas patologías se han manejado de forma quirúrgica, pero en este artículo pretendemos informar de la importancia y la efectividad del manejo endovascular, haciendo énfasis en su carácter menos invasivo y mórbido. El objetivo de esta investigación es dar a conocer otras opciones de manejo de divertículos ventriculares, diferentes a las opciones quirúrgicas, usando materiales alternativos, que no se usan muy a menudo en la práctica diaria.
Material y métodos
Caso clínico
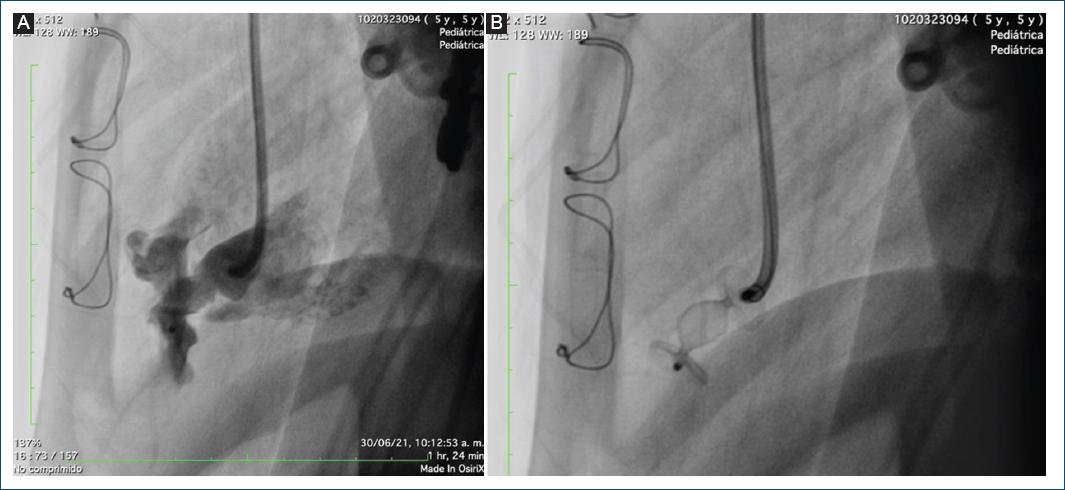
Se trata de un paciente remitido a una institución de alto nivel de complejidad en la ciudad de Medellín, Antioquia, Colombia, a los 20 días de vida, producto de un embarazo a término, con adaptación neonatal espontánea, peso y talla adecuados para la edad gestacional, con paraclínicos infecciosos normales y diagnóstico prenatal de aneurisma ventricular izquierdo (AVI) de 1.6 mm de diámetro, confirmado por ecocardiografía y RM cardiaca posnatal, con ausencia de endocardio asociado, hipocinesia grave, con función ventricular normal y extrasistolia ventricular leve, unifocal, bigeminada, con una carga arrítmica total no significativa del 0.6%. El caso fue llevado a reunión médico-quirúrgica, en la que se decidió realizar un cateterismo diagnóstico, el cual mostró arterias coronarias normales, con divertículo del ventrículo izquierdo (DVI) gigante (Fig. 1).
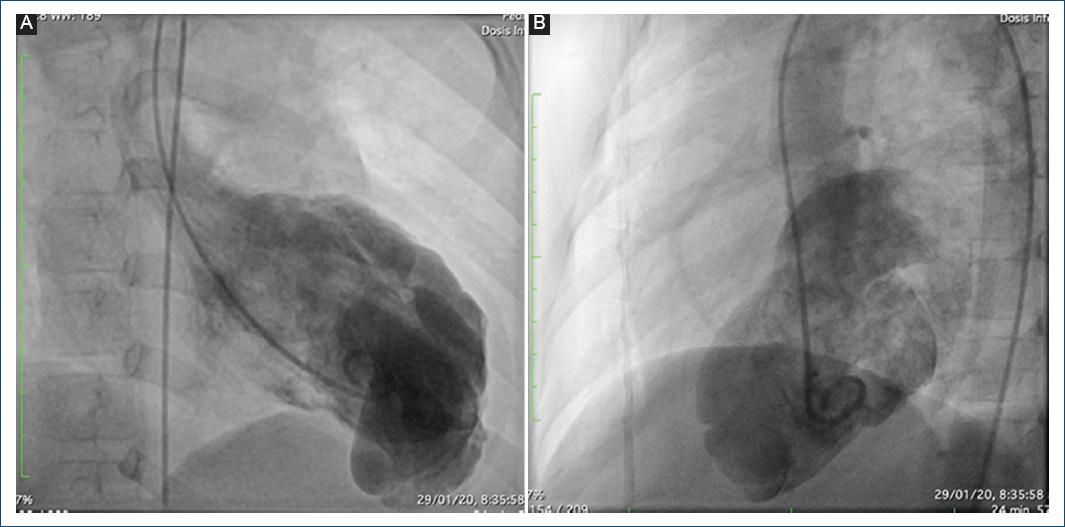
Figura 1 A: ventriculografía que muestra un aneurisma en el ápex cardiaco. B: vista lateral del aneurisma.
Para entonces el paciente se encontraba completamente asintomático, razón por la cual se decidió continuar manejo sistemático con imágenes no invasivas.
A los 3 años de vida se realizaron imágenes de control con RM, encontrando el AVI conocido comprometiendo la pared septal del ventrículo izquierdo, con diámetro de 16 × 11 mm, con adelgazamiento de la pared miocárdica e hipocinesia en esta región, sin comunicación con el ventrículo derecho. El ecocardiograma mostró función ventricular izquierda conservada, con fracción de eyección del ventrículo izquierdo (FEVI) del 63%, sin dilatación del ventrículo izquierdo, y aneurisma apical de 16 × 15 mm de diámetro. Con estos resultados, se decidió realizar estudio hemodinámico, en el cual se observó un ventrículo de morfología izquierda posterior, con segmento apical con divertículo gigante, con trabéculas en su interior e hipocinesia asociada. La diferenciación angiográfica entre aneurisma y divertículo es difícil, requiriendo para su correcta caracterización un estudio histológico. Sin embargo, al presentar una disminución progresiva de la FEVI hasta el 50%, se decidió llevar al paciente a corrección quirúrgica del aneurisma o del divertículo.
Durante el procedimiento quirúrgico se realizó esternotomía media, con canulación aórtica y en la aurícula derecha, se inició circulación extracorpórea, pinzamiento aórtico y paso de cardioplejia del nido por la raíz hasta asistolia, se luxó el corazón y se realizó ventriculotomía longitudinal, evidenciando un DVI en el ápex, con abundante zona fibrótica epicárdica y endocárdica de 4 × 3 cm de diámetro.
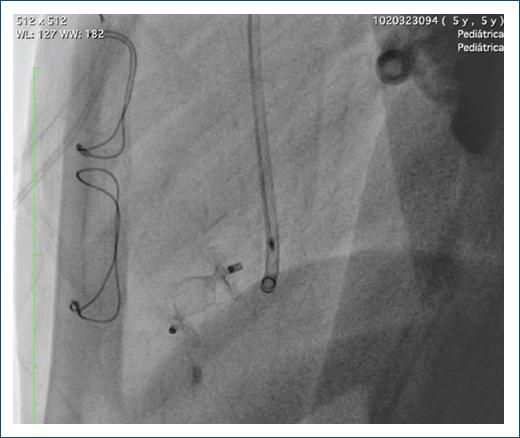
Se procedió a realizar escisión de tejido fibrótico intramiocárdico, localizando los bordes del DVI, y se realizó reparación con exclusión del divertículo con parche de pericardio heterólogo. Se cerró la ventriculotomía por planos, se despinzó y se retornó a ritmo sinusal, sin complicaciones (Fig. 2).
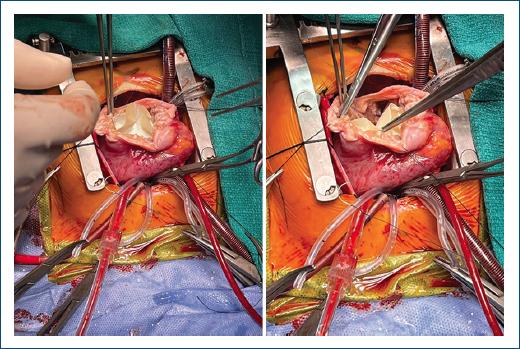
Figura 2 Exclusión del divertículo en el ápex del ventrículo izquierdo con parche de pericardio heterólogo.
Se realizó ecocardiografía de control, en la cual se evidenció el aneurisma excluido (Fig. 3). Sin embargo, al año de seguimiento, mediante ecocardiografía se evidenció un defecto residual en el parche, con dos fugas residuales de 1.5 y 2.5 mm, con cortocircuito bidireccional en la punta del ventrículo izquierdo hacia la bolsa residual pericárdica, con función ventricular sistólica conservada, discinesia e hipocinesia de la punta ventricular izquierda (en el sitio del parche quirúrgico) (Fig. 4).
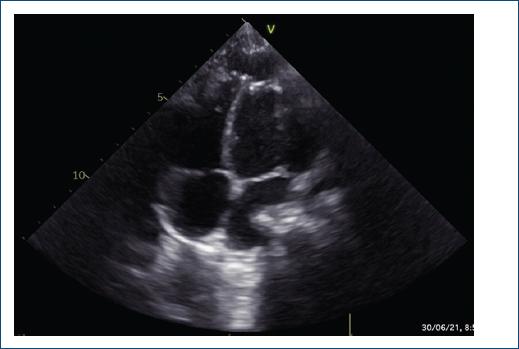
Figura 3 Ecocardiografía que muestra el aneurisma ventricular izquierdo excluido, con el parche de pericardio en posición, sin fugas residuales.
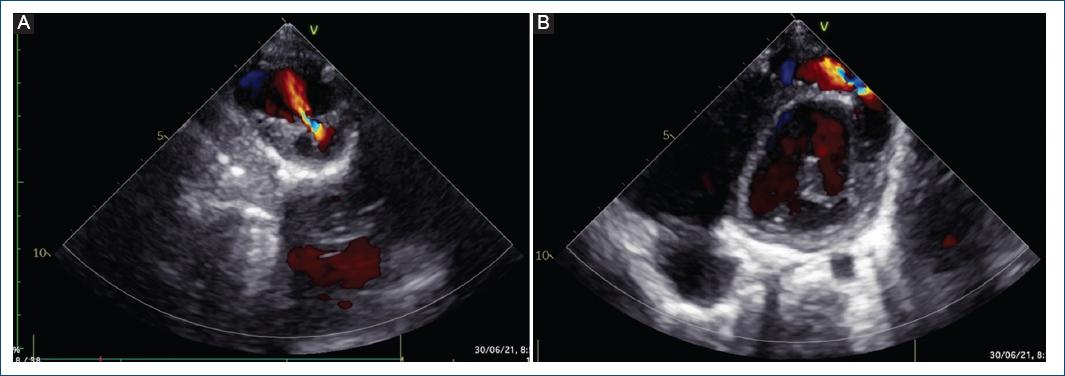
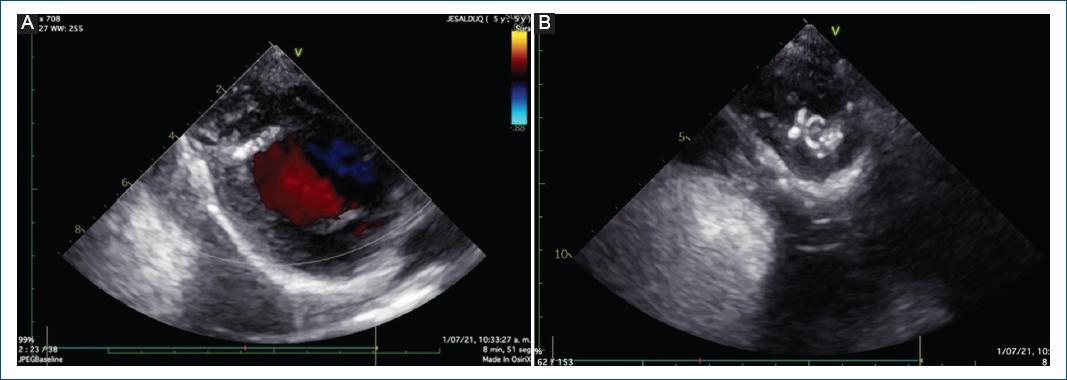
Figura 4 Ecocardiografía transtorácica. A: eje corto paraesternal, con evidencia de fuga residual en el parche de pericardio. B: eje apical de cuatro cámaras mirando al ápex, con evidencia de fuga residual.
Se realizó RM, en la cual fue posible visualizar el parche en el ápex comunicando con la bolsa apical residual de 25 × 15 mm, con flujo bidireccional en su interior; la zona de comunicación era anterolateral y medía 4 × 3.5 mm. La función sistólica del ventrículo izquierdo estaba levemente disminuida, incluyendo la bosal apical que tenía flujo. La FEVI era del 44% y la fracción de eyección del ventrículo derecho del 57%.
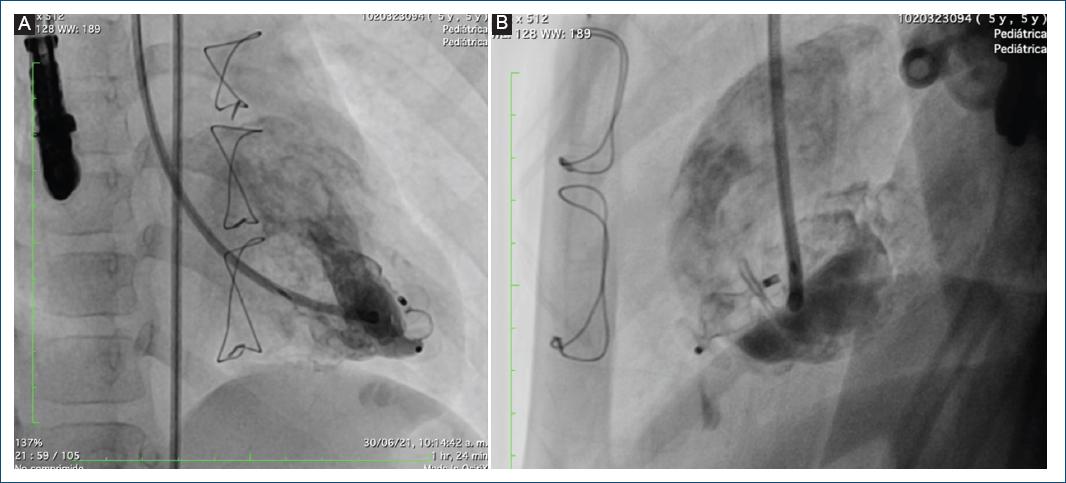
Se llevó de nuevo el caso a junta médico-quirúrgica, donde se consideró el cierre del defecto por vía endovascular (Fig. 5). Para ello, se avanzó una guía hidrófila dentro del divertículo y sobre esta se pasó un catéter non taper hasta el cuerpo del divertículo. Se realizó angiografía en proyecciones oblicua derecha y lateral, observando el gran divertículo con un boca proximal tipo túnel.
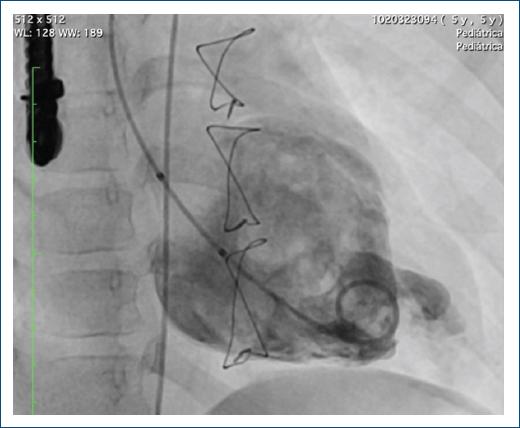
Figura 5 Ventriculografía izquierda con ventrículo de morfología izquierda, posterior, con segmento apical con divertículo gigante, con trabéculas en su interior, con fuga residual del parche de pericardio, visualizada previamente en la ecocardiografía.
Para aclarar la anatomía, se pasó una guía Whisper 0.014 y sobre esta se llevó un balón Tyshak de 10 × 20 mm, el cual se infla en forma manual, observando que la boca del divertículo medía 4 mm.
Se decidió ocluir con un Amplatzer Vascular Plug II (AVP II) de 10 mm, un dispositivo oclusor cilíndrico autoexpandible que se ajusta a la forma del vaso con una malla flexible de alambres de nitinol con marcas de platino en ambos extremos, sin material trombogénico en su interior (Fig. 6).
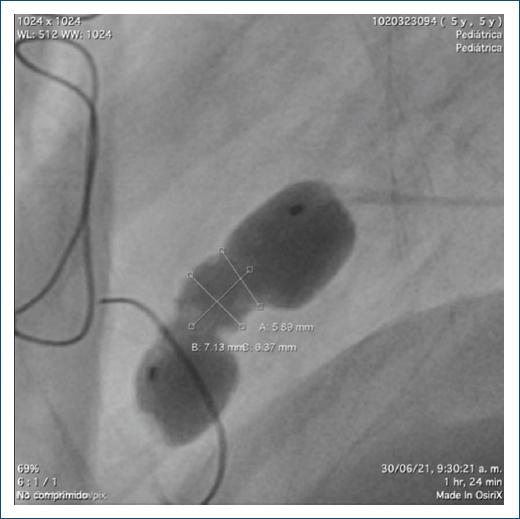
Figura 6 Medidas del balón y decisión de implantación de un dispositivo Amplatzer Vascular Plug, teniendo en cuenta la necesidad de un dispositivo con cintura por la configuración de la lesión en túnel.
Se pasó un introductor Flexor 6 Fr hasta el ventrículo izquierdo, luego se avanzó al catéter non taper distal en el divertículo y se pasó un guía de soporte Amplatz 0.035, sobre la cual se pasó un catéter guía JR 6 Fr. Se avanzó un AVP II de 10 mm, liberando el extremo distal y el tambor central en la cavidad del divertículo y en la boca distal, y por último se liberó el disco proximal (Fig. 7). Se realizó una maniobra de Minessotta wiggle para evaluar la estabilidad del dispositivo, que permaneció estable, y finalmente se liberó (Fig. 8). La angiografía de control mostró el dispositivo en posición con oclusión del divertículo (Fig. 9).
El procedimiento se realizó con ecocardiografía transesofágica y transtorácica en forma simultánea, demostrando en la imagen final la desaparición del flujo dentro del divertículo. Se observó la bolsa pericárdica apical izquierda sin cortocircuito residual. En la punta del ventrículo izquierdo se observó una bolsa pericárdica residual ocluida completamente por el dispositivo Amplatzer Vascular Plug II de 10 mm, con función ventricular sistólica conservada y excursión sistólica del anillo tricúspide de 21 mm (Fig. 10).
Discusión
Las enfermedades relacionadas con la expansión y el crecimiento congénitos del ventrículo izquierdo incluyen el DVI y el AVI congénitos1. Ambas son anormalidades raras en el desarrollo, que se caracterizan por la presencia de abombamiento y adelgazamiento local de la pared del corazón. Ocurren con mayor frecuencia en el ventrículo izquierdo, y rara vez se han informado en el ventrículo derecho o en ambos ventrículos2. El divertículo corresponde a una evaginación de un ventrículo que se contrae de manera sincrónica con esa cámara e histológicamente contiene las tres capas de la pared ventricular (endocardio, miocardio y pericardio), mientras que el aneurisma es una protuberancia ventricular que es acinética o discinética, y en la histología es tejido predominantemente fibroso sin miocardio organizado2. Se estima que ocurren con una frecuencia de en torno a 1 por cada 200,000 nacidos vivos, del 0.013-0.76% de los pacientes sometidos a examen ecocardiográfico y del 0.4% de las autopsias después de la muerte de causa cardiaca3,4. Sin embargo, es posible que se desconozca la verdadera prevalencia de estas patologías, teniendo en cuenta la posibilidad de su curso asintomático5,6. Es importante diferenciarlos en la práctica clínica, ya que difieren en tipo histológico, características clínicas, proceso natural y esquema de tratamiento1.
Desde que O'Bryan7 describió por primera vez el DVI en 1838 ha habido pocos reportes en la literatura, menos de 1000, la mayoría de ellos en recién nacidos y niños. El DVI está causado por la reducción o eliminación del tejido miocárdico local o el reemplazo del tejido miocárdico normal por tejido fibroso, que da como resultado un abultamiento anormal de los tejidos miocárdicos bajo una presión ventricular izquierda alta1. Se cree que esto ocurre como resultado de un desarrollo deficiente del tubo endocárdico durante la cuarta semana de desarrollo embriológico, y a menudo se combina con otras malformaciones congénitas, como anomalías del esternón, del pericardio, del diafragma y del corazón (defectos del tabique interventricular y auricular)5,6. Una de las manifestaciones más graves de esta asociación es la pentalogía de Cantrell, una serie de defectos de la pared toracoabdominal con ectopia cardiaca y onfalocele2,5.
Los divertículos pueden clasificarse histológicamente en tipo muscular y tipo fibroso, según la cantidad de fibras de miocardio involucradas. Los divertículos fibrosos contienen tejido conectivo compuesto de reticulina, con fibras musculares escasas o ausentes, se encuentran principalmente debajo de la válvula aórtica o la válvula mitral, tienen un cuello más ancho, con una pared delgada y sin función contráctil, y se acompañan de pocas malformaciones cardiacas o extracardiacas1,8. El DVI muscular a menudo se encuentra en el vértice del ventrículo izquierdo y contiene tres capas de estructura miocárdica, formando una cavidad real y comunicada con la cavidad del ventrículo izquierdo a través de un cuello corto, y su pared puede moverse sincrónicamente con la pared del ventrículo normal. En el periodo diastólico, la sangre ingresa al divertículo desde el ventrículo izquierdo y el divertículo se agranda, mientras que en el período sistólico la sangre fluye desde el divertículo hacia el ventrículo izquierdo y el divertículo se vuelve más pequeño1.
Actualmente, la corrección de la malformación combinada con la resección del DVI al mismo tiempo ha sido ampliamente reconocida para los DVI con síntomas o con malformaciones cardiacas; sin embargo, no hay consenso sobre si realizar o no tratamiento quirúrgico de las DVI aisladas asintomáticas1,9. Algunos estudios sugieren que todos los pacientes con DVI requieren tratamiento quirúrgico para reducir los riesgos de trombosis ventricular izquierda, arritmia ventricular, ruptura de la pared ventricular y hemorragia masiva3. Sin embargo, otros creen que el tratamiento quirúrgico radical de todos los DVI puede dañar la estructura del ventrículo izquierdo debido a la resección de los músculos normales de la pared ventricular, lo que puede provocar insuficiencia cardiaca e incluso la muerte1.
Se recomienda considerar el tratamiento quirúrgico para los DVI musculares simples que se acompañan de síntomas, como compresión del tracto de salida, de la pared ventricular y de la arteria coronaria, para los DVI que se expanden gradualmente y para el fibrodivertículo, porque este generalmente se encuentra debajo de la válvula aórtica o la válvula mitral y puede afectar la estructura de las valvas, llevando a insuficiencia valvular. Además, el fibrodivertículo, debido a que su base suele ser más ancha que la del divertículo muscular y carece de función contráctil, es más propenso a romperse1. La técnica de corrección quirúrgica del defecto está determinada por el tamaño de la protuberancia y el volumen diastólico final del ventrículo izquierdo5.
Es crucial distinguir el DVI de otras formas de evaginación ventricular, como el aneurisma y el pseudoaneurisma. El diagnóstico se puede hacer por el hallazgo de contractilidad de la evaginación, por la histopatología, por el tamaño del cuello de conexión y por otras malformaciones congénitas que lo acompañan1,5. El DVI se contrae sincrónicamente con la pared ventricular y está conectado al ventrículo por un cuello estrecho, mientras que el aneurisma es una bolsa acinética o discinética con un cuello ancho, carece de músculo miocárdico y tiene una sola capa de tejido fibroelástico5,8, y el pseudoaneurisma representa una ruptura cardiaca contenida por pericardio adherente o trombo y forma una cavidad no contráctil10.
En comparación con el DVI congénito, el AVI congénito pertenece a las cardiopatías congénitas con displasia del endocardio o miocardio. El sustrato para su aparición es la isquemia miocárdica local durante la embriogénesis5. En la mayoría de los casos, su pared es de tejido conectivo, que conduce a hipo- o acinesia grave de la pared y asincronía de la contracción4,5. El aneurisma tiene una base ancha, en general más grande que el divertículo. Además, su tamaño puede aumentar, requiriendo un cuidado especial para los pacientes con esta patología11. Esta malformación suele ser aislada; las anomalías extracardiacas solo se observan en el 3.1% de los pacientes5.
Estos defectos pueden causar una amplia gama de síntomas, desde ninguno (el 42% de los pacientes con aneurismas y en el 63% de los pacientes con divertículos están asintomáticos) hasta soplo cardiaco, dolor precordial, disnea con el ejercicio, arritmias, embolias, rotura e incluso muerte súbita12. En más de la mitad de los casos, estos defectos se diagnostican accidentalmente durante una ecocardiografía, una TC o una RM. La sospecha inicial suele basarse en las características imagenológicas, pero se requiere la confirmación histológica8. La ecocardiografía es el método de diagnóstico más utilizado, y es necesario mejorar la disponibilidad de la ecocardiografía fetal, ya que hasta el 62.5% de los casos pueden diagnosticarse en el examen prenatal3,13. Técnicas de imagen como la RM han adquirido un papel importante, al ser una técnica no invasiva que confirma la presencia del defecto y da información sobre la caracterización tisular, el tamaño y la extensión de las formaciones saculares. La detección de realce tardío con secuencias potenciadas en T1 permite caracterizar el tejido fibroso o necrótico, siendo de gran utilidad para el diagnóstico diferencial entre divertículo y aneurisma5.
El pronóstico y las secuelas a largo plazo varían según el tipo de protuberancia. En un estudio se halló que en los primeros 8,5 meses desde el nacimiento el 40% de los niños con AVI desarrollaron complicaciones, mientras que no se registraron complicaciones graves en los niños con DVI en un seguimiento de 10 años14.











 nueva página del texto (beta)
nueva página del texto (beta)