Introducción
Al comienzo de la pandemia de COVID-19 se informó que la población pediátrica era menos afectada por la enfermedad, tanto en frecuencia como en gravedad. Sin embargo, desde abril de 2020 comenzaron reportes de gravedad, caracterizados por fenómenos inflamatorios sistémicos, condición denominada síndrome inflamatorio multisistémico pediátrico (PIMS, pediatric inflammatory multisystem syndrome). Este se caracteriza por compromiso cardíaco, hasta en un 80% de los casos como lesión miocárdica con significativa elevación de biomarcadores (troponinas séricas I/T, péptido natriurético tipo B [BNP] o fracción N terminal del propéptido natriurético tipo B [NT-proBNP], al igual que diversos grados de disfunción ventricular, pericarditis, derrame pericárdico, valvulitis, arritmias y lesiones coronarias que van desde la dilatación hasta aneurismas. La evaluación cardiovascular de los pacientes con PIMS se ha sistematizado basándose en la presentación clínica, la lesión miocárdica (miocarditis, valvulitis, pericarditis), el choque cardiogénico y las alteraciones coronarias. En México no existen datos que permitan hacer comparaciones y establecer pautas en el manejo. Mediante este estudio se busca exponer las alteraciones cardiovasculares en los pacientes diagnosticados con PIMS durante la pandemia por SARS-CoV-2, con el fin de comprender la enfermedad, su evolución y el manejo óptimo al diagnóstico.
Método
Diseño del estudio
Estudio analítico, transversal, retrospectivo, de todos los casos con PIMS diagnosticados en el Instituto Nacional de Pediatría de la Ciudad de México, un centro hospitalario de tercer nivel en el que se diagnosticaron y trataron pacientes graves menores de 18 años con el diagnóstico, desde marzo de 2020 hasta diciembre de 2021.
Los casos de PIMS fueron identificados en la sala de urgencias y se ingresaron bajo normas de bioseguridad al área COVID-19, y de acuerdo con la gravedad se distribuyeron en cuidado pediátrico, terapia intermedia y cuidados intensivos pediátricos de COVID-19.
Los criterios de inclusión fueron los casos de PIMS que cumplían los criterios de la Organización Mundial de la Salud (OMS) (Tabla 1) y contaban con un ecocardiograma al momento del diagnóstico. Los criterios de exclusión fueron aquellos pacientes con PIMS atendidos en otra institución y aquellos con diagnóstico de enfermedad de Kawasaki (EK), síndrome de activación de macrófagos o choque séptico estafilocócico o estreptocócico.
Tabla 1 Criterios de síndrome inflamatorio multisistémico pediátrico según la Organización Mundial de la Salud (OMS)1
| Parámetros | OMS |
|---|---|
| Terminología | Afección inflamatoria multisistémica en niños y adolescentes |
| Edad | 0-19 años |
| Hallazgos clínicos | Fiebre > 3 días y al menos dos de los criterios siguientes |
| Erupción cutánea o conjuntivitis no purulenta bilateral o signos de inflamación mucocutánea (boca, manos o pies) | |
| Hipotensión o choque | |
| Datos de disfunción miocárdica, pericarditis, valvulitis o anomalías coronarias (incluidos hallazgos ecocardiográficos o valores elevados de troponina/NT-proBNP) | |
| Evidencia de coagulopatía (alteración de TP, TTPa o valores elevados de dímero D) | |
| Síntomas gastrointestinales agudos (diarrea, vómitos o dolor abdominal) | |
| Hallazgos de laboratorio | Elevación de marcadores inflamatorios, cualquiera de los siguientes |
| Proteína C reactiva | |
| Velocidad de sedimentación globular | |
| Procalcitonina | |
| Evidencia de infección por SARS-CoV-2 | Evidencia de COVID-19 (RT-PCR, pruebas antigénicas o serología positivas) o contacto probable con un caso de COVID-19 |
NT-proBNP: fracción N terminal del propéptido natriurético tipo B; RT-PCR: reacción en cadena de la polimerasa-transcriptasa inversa; TP: tiempo de protrombina; TTPa: tiempo de tromboplastina parcial activada (modificada de García-Salido et al.1).
Recolección de datos
Del archivo clínico físico y electrónico del Instituto Nacional de Pediatría se analizaron los expedientes de los pacientes con diagnóstico de PIMS desde marzo de 2020 hasta diciembre de 2021. Se creó en primer lugar una base de datos en Excel con todas las variables demográficas y antropométricas, características clínicas y antecedentes patológicos, hallazgos de laboratorio, marcadores inflamatorios, enzimas cardiacas y alteraciones cardiovasculares: miocarditis, pericarditis, derrame pericárdico, arritmias, lesiones coronarias (z-score ≥ 2) y disfunción ventricular (fracción de eyección del ventrículo izquierdo [FEVI] < 55%, método de Simpson biplanar). De estos pacientes se analizaron las características clínicas, el tiempo al diagnóstico, los estudios de laboratorio y gabinete, el tratamiento utilizado y las asociaciones entre los antecedentes demográficos, clínicos y paraclínicos con la presentación de las alteraciones cardiovasculares, el choque y la mortalidad de los pacientes con PIMS.
Análisis estadístico
Una vez concluida la recolección de datos en Excel, estos se exportaron al programa estadístico SPSS versión 22 para su análisis a través de medidas de tendencia central y dispersión para las variables cuantitativas, y de frecuencias, proporciones y χ2 para las variables cualitativas. El aspecto analítico se evaluó con diferencia de medias por t de Student en las dicotómicas y ANOVA en las politómicas si la distribución era normal; en casos de distribución no normal se evalúo por medio de U de Mann-Whitney y Kruskal-Wallis.
Resultados
De acuerdo con los criterios de la OMS, se registraron 77 pacientes con diagnóstico de PIMS que fueron atendidos en el Instituto Nacional de Pediatría de la Ciudad de México desde marzo de 2020 hasta diciembre de 2021, con una edad media al ingreso de 86 ± 61.81 meses. El sexo masculino fue el más afectado, representando el 61% del total de los pacientes. De todos los pacientes admitidos, la edad escolar fue el grupo más afectado, que corresponde al 33.8%, seguido de los adolescentes con el 27.3%. Respecto a la antropometría, el peso bajo en el grupo de estudio fue dominante, con el 68.8% (Tabla 2).
Tabla 2 Características demográficas, presentación clínica y marcadores de laboratorio en pacientes con síndrome inflamatorio multisistémico pediátrico
| Características | n = 77 |
|---|---|
| Edad, meses | 86 ± 61.81 |
| Lactantes (%) | 17 (22.1) |
| Preescolares (%) | 13 (16.9) |
| Escolares (%) | 26 (33.8) |
| Adolescentes (%) | 21 (27.3) |
| Sexo masculino (%) | 47 (61) |
| Peso (kg) | 27.60 ± 17.72 |
| Talla (cm) | 1.17 ± 0.31 |
| IMC (kg/m2) | 17.51 ± 4.16 |
| Peso normal (%) | 21 (27.3) |
| Peso bajo (%) | 53 (68.8) |
| Sobrepeso (%) | 2 (2.6) |
| Obesidad (%) | 1 (1.3) |
| Estancia hospitalaria (días) | 11.21 ± 14.01 |
| Fallecidos (%) | 8 (10.4) |
| Presentación clínica | |
| Fiebre (%) | 74 (96) |
| Duración fiebre (días) | 5.38 ± 3.2 |
| Temperatura fiebre (grados) | 38.9 ± 0.75 |
| Tos (%) | 20 (26) |
| Rinorrea (%) | 12 (15.6) |
| Disnea (%) | 18 (23.4) |
| Exantema (%) | 48 (62.3) |
| Conjuntivitis (%) | 60 (78) |
| Eritema (%) | 37 (48) |
| Edema (%) | 34 (44) |
| Ganglio cervical (%) | 20 (26) |
| Queilitis (%) | 47 (61) |
| Dolor abdominal (%) | 46 (59.7) |
| Diarrea (%) | 35 (32.5) |
| Vómito (%) | 33 (42.9) |
| Artralgia (%) | 10 (13) |
| Choque (%) | 23 (30) |
| Trombosis (%) | 1 (1.3) |
| Neurológico (%) | 26 (33.8) |
| Comorbilidad | |
| Sanos (%) | 52 (67.5) |
| Oncológica (%) | 6 (7.8) |
| Neurológica (%) | 6 (7.8) |
| Metabólica (%) | 4 (5.2) |
| Pulmonar (%) | 5 (6.5) |
| Inmunológica (%) | 2 (2.6) |
| Vascular (%) | 2 (2.6) |
| Marcadores de laboratorio | |
| Leucocitos (ml) | 14,961.17 ± 25,109.84 |
| Hemoglobina (g/dl) | 12.20 ± 2.01 |
| Hematocrito (%) | 36.33 ± 5.98 |
| Plaquetas (ml) | 243,720 ± 195,671 |
| Proteína C reactiva (mg/dl) | 12.81 ± 13.56 |
| Procalcitonina (ng/ml) | 18.05 ± 31.78 |
| VSG (mm/h) | 39.81 ± 23.45 |
| Ferritina (ng/dl) | 1390 ± 2555.79 |
| Dímero D (mg/ml) | 19.21 ± 116.44 |
| Fibrinógeno (mg/dl) | 413.68 ± 166.57 |
| NT-proBNP (pg/ml) | 6295.46 ± 10.166 |
| Troponina I (pg/ml) | 91.66 ± 154.08 |
| RT-PCR positiva, n (%) | 24 (31.2) |
| Serología positiva, n (%) | 7 (9.1) |
IMC: índice de masa corporal; NT-proBNP: fracción N terminal del propéptido natriurético tipo B; RT-PCR: reacción en cadena de la polimerasa-transcriptasa reversa; VSG: velocidad de sedimentación globular.
En 36% de la población se documentó como contacto positivo con personas infectadas por SARS-CoV-2 y prueba de reacción en cadena de la polimerasa-transcriptasa inversa (RT-PCR) positiva en 24 pacientes. Las manifestaciones clínicas principales y los marcadores de laboratorio se resumen en la tabla 2. La mayoría de los pacientes (67.5%) eran previamente sanos; hubo 25 pacientes con comorbilidad relacionada con problemas oncológicos y neurológicos con igual distribución del 7.8%, seguida de afecciones pulmonares en el 6.5% y metabólicas en el 5.2%; además, se observó que dos pacientes con historia de enfermedad de Kawasaki en estadio I presentaron PIMS (Tabla 2). La mortalidad fue del 10.4%, que corresponde a ocho pacientes.
Del total de los pacientes, el 17% presentaron alteraciones electrocardiográficas, siendo las principales taquicardia sinusal en el 17.1%, taquicardia ventricular sin respuesta a maniobras de desfibrilación produciendo el fallecimiento en el 2.9%, y taquicardia supraventricular que requirió primero cardioversión farmacológica y posteriormente cardioversión eléctrica con retorno a ritmo sinusal en el 2.9%. En dos pacientes se documentaron extrasístoles ventriculares aisladas, un paciente con QT largo y un paciente con bradicardia sinusal. También se observó alternancia eléctrica en un paciente con derrame pericárdico y elevación del segmento ST e infradesnivel del PR.
Respecto a la función ventricular, en el 77% de los pacientes se encontró conservada. Los que presentaron disfunción ventricular se estratificaron de acuerdo con la cuantificación por método de Simpson biplanar (dos vistas ortogonales): el 13.5% presentaron disfunción ventricular leve, el 6.8% disfunción moderada y el 2.7% disfunción grave (Fig. 1).
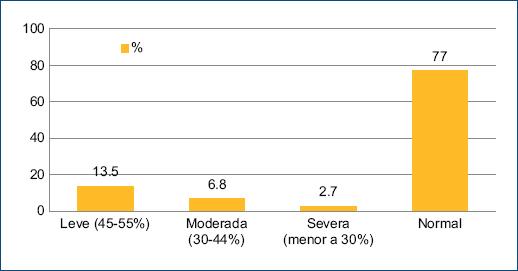
Figura 1 Función ventricular en los pacientes con síndrome inflamatorio multisistémico pediátrico al ingreso.
En la evaluación de las arterias coronarias se identificó que el 77.9% mantuvieron las coronarias normales. La anomalía coronaria más frecuente fue el aneurisma pequeño en seis pacientes; en cuatro de ellos la descendente anterior estuvo comprometida, seguida por el tronco de la coronaria izquierda y la coronaria derecha. El 5.2% presentaron ectasia; dos pacientes desarrollaron aneurisma moderado 1 con afección de la coronaria derecha y la descendente anterior, y otro paciente con compromiso aislado de la coronaria derecha. Finalmente, el 1.3% desarrollaron aneurisma gigante de la coronaria derecha con z-score +16.47 (Figs. 2 y 3). Además de los hallazgos ecocardiográficos citados, en 15 pacientes (20.5%) se identificaron datos de miocarditis y el 25.7% cursaron con derrame pericárdico sin fisiología de tamponade.
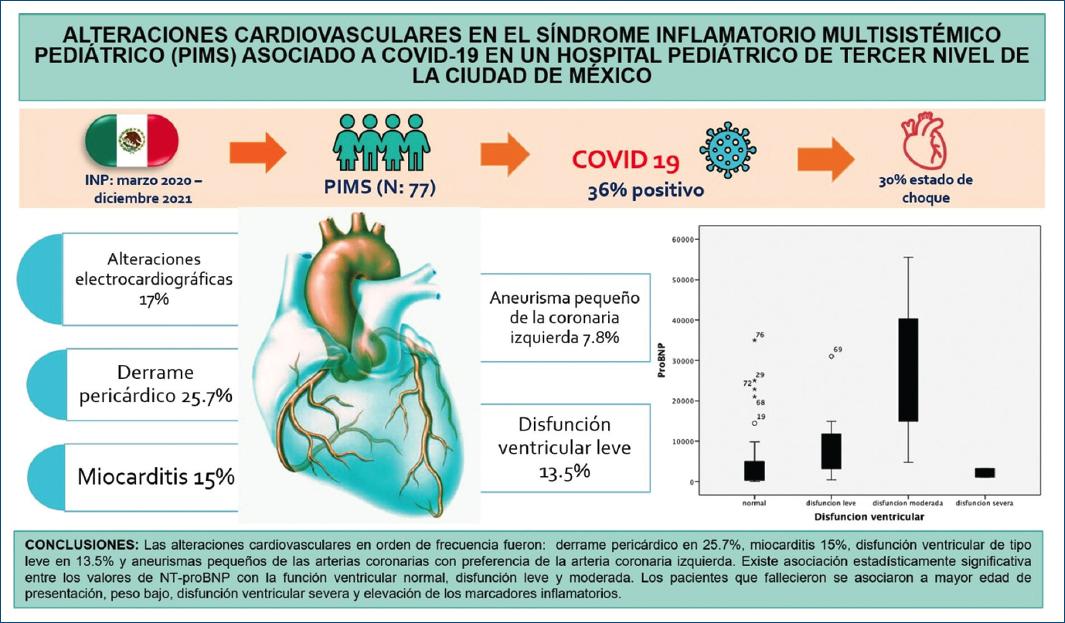
Figura 2 Alteraciones cardiovasculares en los pacientes con síndrome inflamatorio multisistémico pediátrico.
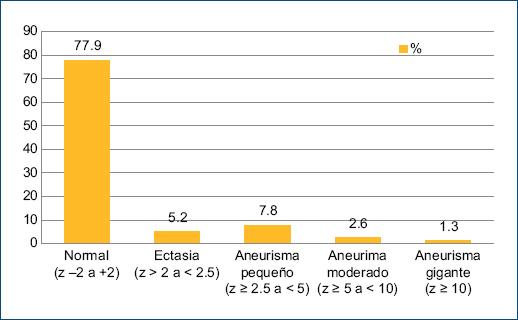
Figura 3 Alteraciones coronarias en los pacientes con síndrome inflamatorio multisistémico pediátrico.
Se correlacionaron la disfunción ventricular y los valores de NT-proBNP determinando diferencias estadísticamente significativas: la función ventricular normal presentó un valor medio de NT-proBNP de 4547.20 ± 7357.041 pg/ml, en la disfunción ventricular leve hubo un valor medio de NT-proBNP de 9148.67 ± 9636.383 pg/ml, y para la disfunción ventricular moderada el valor medio de NT-proBNP fue de 27577.50 ± 20936.94 pg/ml. Los pacientes con disfunción moderada tuvieron un NT-proBNP significativamente mayor en comparación con aquellos con disfunción leve, y estos a su vez con los que mantuvieron una función ventricular preservada (ANOVA p < 0.05 y Kruskal-Wallis p = 0.007) (Figs. 2 y 4).
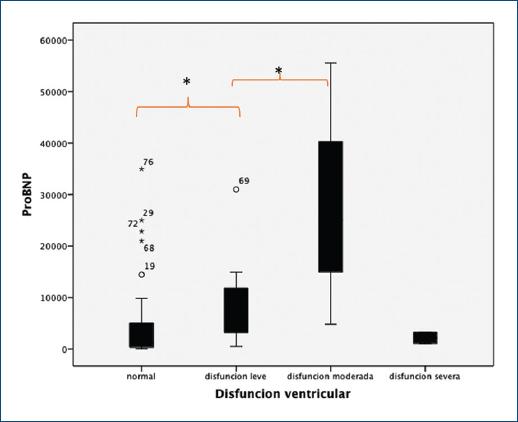
Figura 4 Valores de propéptido natriurético tipo B (NT-proBNP) y disfunción ventricular. ANOVA p < 0.05, Kruskal-Wallis p = 0.007.
Se analizaron los niños que presentaron choque en contraste con aquellos que no lo presentaron (Tabla 3) y se estableció que los pacientes con choque tenían una relación estadísticamente significativa con mayor estancia hospitalaria (p < 0.001), edad escolar de presentación (p < 0.001) y peso bajo (p = 0.002). Las manifestaciones clínicas que demostraron significancia estadística se documentan en la tabla 3. Los resultados mostraron correlación entre el estado de choque y valores más elevados de los marcadores de laboratorio (plaquetas 144217.29 ± 139321.6 μl [p < 0.001], procalcitonina 27.37 ± 38.37 ng/ml [p = 0.05] y ferritina 1937.87 ± 2562.63 [p < 0.001]).
Tabla 3 Niños con choque asociado a síndrome inflamatorio multisistémico pediátrico
| Variables | Niños sin choque | Niños con choque | p |
|---|---|---|---|
| Días de estancia | 6.80 ± 4.47 | 21.57 ± 21.68 | < 0.001 |
| Edad (meses) | 70.48 ± 56.02 | 121.61 ± 61 | 0.001 |
| Duración de fiebre (días) | 5.85 ± 3.47 | 4.26 ± 2.2 | 0.029† |
| Peso (kg) | 23.19 ± 15.20 | 37.92 ± 19,20 | 0.001 |
| IMC (kg/m2) | 16.58 ± 3.32 | 19.69 ± 5.12 | 0.002 |
| Frecuencia cardiaca | 138 ± 21.32 | 144.48 ± 16.07 | 0.171 |
| Frecuencia respiratoria | 31.30 ± 9.3 | 37.47 ± 12.13 | 0.018 |
| PAS (mmHg) | 101.59 ± 12.52 | 86.91 ± 16.43 | < 0.001 |
| PAD (mmHg) | 62.31 ± 11.71 | 53.61 ± 12.20 | 0.004 |
| SaO2 (%) | 93.24 ± 4.87 | 89.70 ± 6.81 | 0.012 |
| Hematocrito (%) | 36.50 ± 5.64 | 35.95 ± 6.83 | 0.712 |
| Leucocitos (ml) | 12,216.67 ± 7053.85 | 21,404.78 ± 44,680.44 | 0.143 |
| Segmentados (ml) | 8744.63 ± 4920 | 10,905.3 ± 8480.33 | 0.164 |
| Plaquetas (ml) | 285,816 ± 201,850 | 144,217.39 ± 139,321.06 | 0.001 |
| Proteína C reactiva (mg/dl) | 10.38 ± 8.65 | 18.66 ± 20.29 | 0.077 |
| Procalcitonina (ng/ml) | 9.46 ± 21.63 | 27.37 ± 38.37 | 0.009† |
| VSG (mm/h) | 42.61 ± 23.84 | 31.84 ± 20.87 | 0.085 |
| Ferritina (ng/dl) | 1083.31 ± 2531.22 | 1937.87 ± 2562.63 | < 0.001† |
| Troponina (ng/ml) | 40.77 ± 71.71 | 185.8 ± 214.16 | < 0.001 |
| NT-proBNP (pg/ml) | 3925 ± 7572 | 11,864.7 ± 13178.87 | 0.003 |
| FEVI (%) | 58.1 ± 8.4 | 49.6 ± 9.1 | < 0.001* |
| z-score coronaria izquierda | 0.44 ± 1.42 | 0.51 ± 1.55 | 0.02 |
| z-score descendente anterior | 0.29 ± 1.84 | 0.40 ± 1.56 | 0.82 |
| z-score circunfleja | 0.061 ± 1.24 | 0.18 ± 1.01 | 0.73 |
| z-score coronaria derecha | 0.54 ± 2.81 | 1.15 ± 2.05 | 0.36 |
*t de Student.
†U de Mann-Whitney. FEVI: fracción de eyección del ventrículo izquierdo; IMC: índice de masa corporal; NT-proBNP: fracción N terminal del propéptido natriurético tipo B; PAD: presión arterial diastólica; PAS: presión arterial sistólica; SaO2: saturación de oxígeno; VSG: velocidad de sedimentación globular.
La función ventricular en los pacientes con choque era significativamente menor en comparación con aquellos sin choque (FEVI 49.6 ± 9.1% vs. 58.1 ± 8.4%; t de Student p < 0.001); también presentaron elevación del NT-proBNP (11864.7 ± 13178.87 pg/ml; p = 0.003) y alteración de la arteria coronaria izquierda (p = 0.02) (Tabla 3).
Al comparar los pacientes vivos y fallecidos (Tabla 4), se estableció que la edad de los fallecidos fue significativamente mayor que la de los sobrevivientes (p < 0.001), y se encontraron algunas diferencias estadísticamente significativas en quienes fallecieron con relación a peso bajo (p = 0.006), duración de los días de fiebre (p = 0.046) y comorbilidad (cuatro pacientes oncológicos, tres previamente sanos y un paciente con lupus eritematoso sistémico). Todos los fallecidos presentaron elevación de los marcadores inflamatorios, alteración del tronco de la coronaria izquierda (p = 0.02) y disfunción ventricular con significancia estadística (p < 0.001). Los pacientes fallecidos también presentaron mayor frecuencia de miocarditis (p = 0.008), dada por el compromiso inflamatorio en comparación con los pacientes sobrevivientes.
Tabla 4 Comparación de los días de fiebre, signos, marcadores inflamatorios y ecocardiográficos en los pacientes con síndrome inflamatorio multisistémico pediátrico vivos frente a fallecidos
| Vivos media (DE) | Fallecidos media (DE) | p | |
|---|---|---|---|
| Edad (meses) | 77.17 ± 57.29 | 159.75 ± 51.18 | < 0.001 |
| Estancia (días) | 10.20 ± 12.52 | 19.88 ± 22.64 | 0.064 |
| Duración de fiebre (días) | 5.67 ± 3.17 | 2.88 ± 2.64 | 0.019 |
| Peso (kg) | 17.01 ± 2.04 | 15.09 ± 5.33 | 0.006 |
| IMC (kg/m2) | 17.21 ± 4.16 | 20.06 ± 3.40 | 0.026† |
| Frecuencia cardiaca (lpm) | 140.78 ± 20.77 | 134.88 ± 10.62 | 0.21 |
| PAS (mmHg) | 97.68 ± 14,54 | 93.13 ± 21.35 | 0.428 |
| PAD (mmHg) | 59.93 ± 12.62 | 58.25 ± 11.52 | 0.709 |
| SaO2 (%) | 92.42 ± 5.45 | 90.13 ± 7.79 | 0.286 |
| Hematocrito (%) | 35.95 ± 5.51 | 39.65 ± 8.90 | 0.099 |
| Leucocitos (ml) | 15,461.88 ± 26,216.15 | 10,642.50 ± 12,049.57 | 0.377 |
| Segmentados (ml) | 9433.61 ± 5416.48 | 9014.13 ± 11614 | 0.858 |
| Proteína C reactiva (mg/dl) | 13.17 ± 13.78 | 9.26 ± 11.36 | 0.42 |
| Procalcitonina (ng/ml) | 13.90 ± 27.39 | 38.77 ± 44.86 | 0.042 |
| VSG (mm/h) | 39.50 ± 23.81 | 44 ± 19.39 | 0.682 |
| Ferritina (ng/dl) | 1057.26 ± 1873.96 | 3722.50 ± 4908.43 | < 0.001† |
| Troponina (ng/ml) | 70.47 ± 123.32 | 221.42 ± 251.53 | 0.009 |
| NT-proBNP (pg/ml) | 5419.98 ± 8208.11 | 12752.13 ± 19032.61 | 0.05 |
| FEVI (%) | 57.13 ± 7.43 | 42.25 ± 13.92 | < 0.001 |
| z-score tronco coronaria izquierda | 1.52 ± 0.19 | 0.57 ± 0.41 | 0.155 |
| z-score descendente anterior | 1.77 ± 0.22 | 0.03 ± 0.025 | < 0.001 |
| z-score circunfleja | 1.19 ± 0.15 | 0.05 ± 0.04 | < 0.001 |
| z-score coronaria derecha | 1.42 ± 0.18 | 1.13 ± 0.8 | 0.048 |
| Miocarditis (%) | 10 ± 15.4 | 5 ± 62.5 | 0.008* |
χ2.
†U de Mann-Whitney. DE: desviación estándar; FEVI: fracción de eyección del ventrículo izquierdo; IMC: índice de masa corporal; NT-proBNP: fracción N terminal del propéptido natriurético tipo B; PAD: presión arterial diastólica; PAS: presión arterial sistólica; SaO2: saturación de oxígeno; VSG: velocidad de sedimentación globular.
Discusión
Se encuentran similitudes y algunas diferencias en las manifestaciones cardiovasculares de los pacientes con PIMS respecto a otros centros pediátricos nacionales e internacionales. En nuestro centro, el sexo más afectado fue el masculino con el 61%, valor semejante al estudio de Haghighi AB et al.2, que identificó el mismo sexo predominante en el 57% de su población; la edad más afectada es variable en diversas publicaciones, en este estudio la media de edad al ingreso fue de 86 ± 61.81 meses similar a lo observado por Valverde et al.3 cuyo estudio multicéntrico (Europa) identificó que en el 67% del total de la población, la edad media de presentación fue de 7.1 años (86 meses) mientras para Minocha PK et al.4 en un estudio de New York, reporta una edad media de presentación menor con 2.8 años (32 meses).
Dentro de las manifestaciones clínicas se evidenció que 74 (96%) pacientes cursaron con fiebre. Como mencionan Sperotto et al.5, existe una diferencia en relación a la presentación de las demás características clínicas y algunas semejanzas con la enfermedad de Kawasaki; la conjuntivitis y el exantema fueron los signos con mayor frecuencia en este estudio, que corresponden al 78% y al 62.3% respectivamente. Los síntomas gastrointestinales se ubicaron en segundo lugar con dolor abdominal en el 59.7% y diarrea en un 32.5% de los casos, contrastando nuestros resultados con Canturutti et al.6, quienes encontraron que los síntomas gastrointestinales fueron predominantes en el 72% de sus pacientes, y para Belhadjer et al.7 en el 80% de los casos.
La comorbilidad en nuestra población fue de tipo oncológico y neurológico, y en tercer lugar enfermedades pulmonares, ligeramente diferente de otros estudios, en los cuales las patologías pulmonares crónicas presentaban mayor vulnerabilidad para contraer PIMS. De acuerdo con Gil Guevara et al.8, en México se identificó que un 45.3% de los casos tenían alguna condición subyacente, como obesidad (25%), cáncer (9%), alteraciones neuromusculares (8%) y enfermedades respiratorias (7%). Por otra parte, en el mismo estudio se mencionó la obesidad como factor de riesgo, tanto en población adulta como pediátrica, para la infección por SARS-CoV-2; sin embargo, en nuestra población se demostró que el 68.8% cursaba con bajo peso, por lo cual se puede considerar que los extremos en el índice de masa corporal son factores de riesgo para PIMS.
De los pacientes que cursaron con choque y muerte, cuatro tenían comorbilidad oncológica y uno antecedente inmunológico, que en forma parcial representa lo mencionado por Felsenstein et al.9, en cuanto a que el asma o alguna condición que comprometa el sistema inmunitario pueden asociarse a mayor mortalidad por PIMS.
Los marcadores inflamatorios estuvieron alterados durante la fase aguda, con elevación del valor medio de NT-proBNP de 6295,46 ± 10.166 pg/ml. Mannarino et al.10 encontraron valores similares y estadísticamente significativos. En un metaanálisis, Zhao et al.11 determinaron que los niveles de BNP eran más altos en pacientes con PIMS que en pacientes con COVID-19 no grave, pero no hubo diferencia significativa en los resultados de BNP, troponinas y AST.
En los hallazgos ecocardiográficos se identificó que el 25.7% de los pacientes presentaron derrame pericárdico, el 15% miocarditis, el 13.5% disfunción ventricular moderada y el 7.8% aneurisma pequeño coronario; resultados similares a los de Mannarino et al.10 en Italia, quienes reportaron disfunción ventricular moderada a grave en el 16% de los casos. Pérez et al.12, en Colombia, observaron que la alteración coronaria fue la lesión cardiovascular más frecuente, en 35% de los casos, que incluían ectasia y aneurisma pequeño, seguido por derrame pericárdico en el 25% de los pacientes. Respecto al compromiso coronario, Belhadjer et al.7 y Verdoni et al.13 han observado ectasia coronaria como lesión más frecuente, diferente de nuestros resultados, en los que la dilatación coronaria ocupó el segundo lugar con el 5.2% y la lesión predominante se presentó con aneurismas coronarios pequeños en el 7.8%; en cuatro de ellos la descendente anterior estuvo comprometida, un paciente presentó aneurisma en el tronco de la coronaria izquierda antes de su bifurcación y un paciente en la coronaria derecha. Wong et al.14, al igual que en nuestro estudio, informaron que a nivel coronario siete pacientes mostraron algún grado de dilatación, de los cuales la coronaria principal izquierda, la descendente anterior y la circunfleja se encontraron afectadas en el 10.4%, el 16.4% y el 4.4%, respectivamente, lo cual permite distinguir que la arteria coronaria izquierda es la más afectada. Gil Guevara et al.8, en un estudio en población mexicana, reportó aneurisma coronario en el 6.7% de sus casos.
Wong et al.14 concluyo que el derrame pericárdico sin necesidad de drenaje es frecuente, representando el 31.3%, similar al nuestro, que se registró en el 25.7%.
La asociación entre choque y elevación de los valores de NT-proBNP en comparación con quienes no tuvieron choque también se confirmó en nuestros resultados. Se obtuvieron valores de NT-proBNP en pacientes con choque de 11864.7 ± 13178.87 pg/ml y en pacientes sin choque de 3925 ± 7572 pg/ml (p = 0.003), similar a lo reportado por Clark et al.15, quienes encontraron valores de 11411 ± 2143 pg/ml y 2273 ± 638 pg/ml, respectivamente (p = 0.001).
En la correlación entre los valores de NT-proBNP y la función ventricular, Ruvinsky et al.16 determinaron que existe una alta correlación del NT-proBNP y las alteraciones ecocardiográficas. Se demostraron diferencias estadísticamente significativas en la función ventricular normal, la disfunción leve y la disfunción moderada: 4547.20 ± 7357.041 pg/ml, 9148.67 ± 9636.383 pg/ml y 27577.50 ± 20936.94 pg/ml, respectivamente (ANOVA p < 0.05 y Kruskal-Wallis p = 0.007).
La edad de los pacientes que fallecieron con PIMS fue significativamente mayor que la de aquellos que sobrevivieron (p < 0.001), y se encontraron algunas diferencias estadísticamente significativas en cuanto a peso bajo (p = 0.006), elevación de los marcadores inflamatorios (procalcitonina [p = 0.042], ferritina [p = 0.05], NT-proBNP [p = 0.055] y troponina I [p = 0.009]) y disfunción ventricular (p < 0.001). Teniendo en cuenta estos resultados, existe limitación en la literatura para determinar cuáles fueron las asociaciones implícitas en la mortalidad. Valverde et al.3 informaron un fallecimiento que se relacionó con taquicardia ventricular y disfunción grave, mientras que para Clark et al.15 las dos defunciones que ocurrieron fueron secundarias a limitaciones de los recursos disponibles. Por su parte, Haghighi et al.2 mencionan que la mortalidad se encuentra relacionada probablemente con las complicaciones cardiovasculares demostradas, con elevación de los marcadores inflamatorios y disfunción ventricular. Pérez et al.12 analizaron los riesgos en sobrevivientes y fallecidos, y demostraron que la mortalidad se relacionó con factores cardiovasculares como disfunción diastólica (p = 0.02), derrame pericárdico (p = 0.01) y arritmias cardiacas (p = 0.03). González et al.17, en un estudio de cohorte multinacional, encontraron que los pacientes que desarrollaron PIMS tuvieron menor mortalidad que aquellos infectados por SARS-CoV-2 sin PIMS, y se asoció a edad menor de 2 años y comorbilidad pulmonar y cardiaca17.
Nuestro estudio demuestra las alteraciones cardiovasculares en pacientes con PIMS durante la fase aguda de la enfermedad y la relación de mayor gravedad-mortalidad en los pacientes de mayor edad con disfunción ventricular y elevación de biomarcadores pero aún faltan estudios para valorar la evolución cardiovascular a largo plazo en estos pacientes.
Limitaciones
Entre las limitaciones del estudio se encuentra que se realizó en un solo centro hospitalario de tercer nivel de la Ciudad de México, por lo que no refleja el comportamiento del PIMS en toda la nación. Además, al tratarse de un estudio retrospectivo se han perdido algunas variables. Así mismo, desde la declaración de la pandemia el acceso al área COVID-19 fue restringido, con pérdida de numerosos estudios electrocardiográficos, así como también de los valores del NT-proBNP, porque se determinaba de forma extrahospitalaria, lo cual limitó un mayor estudio y seguimiento.
Conclusiones
Las alteraciones cardiovasculares observadas fueron, en orden de frecuencia, derrame pericárdico (25.7%), miocarditis (15%), disfunción ventricular de tipo leve (13.5%) y aneurismas pequeños de las arterias coronarias, con preferencia de la arteria coronaria izquierda y la descendente anterior. Hubo diferencia estadísticamente significativa en los pacientes que fallecieron, con mayor edad de presentación, peso bajo, disfunción ventricular grave y elevación de los marcadores inflamatorios, por lo cual se considera que la menor edad puede ser un factor protector para el desarrollo de PIMS. Existe una asociación estadísticamente significativa entre NT-proBNP y función ventricular normal, disfunción leve y moderada; no se encontró correlación con la disfunción ventricular grave, probablemente porque la muestra fue reducida y en ese momento este biomarcador se determinaba en un laboratorio externo al hospital.
Los pacientes con PIMS requieren un diagnóstico y un tratamiento oportunos. La valoración por un cardiólogo pediatra permite evaluar las complicaciones cardiovasculares que conllevan una alta mortalidad. Mediante el presente estudio se ha podido extraer el conocimiento y el aprendizaje de los pacientes con PIMS y las alteraciones cardiovasculares en la fase aguda de la enfermedad, y compararlos con los hallazgos disponibles en la literatura internacional. Sin embargo, aún quedan interrogantes para conocer el alcance de la infección por SARS-CoV-2 a largo plazo y las posibles consecuencias orgánicas que pueda tener.











 nueva página del texto (beta)
nueva página del texto (beta)


