Introducción
En los últimos años, en el mercado global hay una tendencia al alza en el uso de los nanomateriales por lo que los analistas económicos confían en su continuidad, ya que en el año 2019, se estimaron ventas por más de 8 mil millones de dólares estadounidenses, cuyo beneficio se verá reflejado en una tasa de crecimiento anual de alrededor del 13% para el 2027 (Dikshit et al., 2021). Entre todos los tipos de nanomateriales, las nanopartículas (NPs) son las que más se producen (Miu & Dinischiotu, 2022); un ejemplo de estas últimas son las que se basan en materiales inorgánicos compuestos por metales y óxidos metálicos como el óxido de plata, el óxido de zinc, etc. Entre todas las NPs sintetizadas, las de plata (NPs de Ag) son las más utilizadas y exhiben su dominio en varios productos de consumo en (más del 25%), (Dikshit et al., 2021).
Las NPs han sido utilizadas en diversos campos como en: la nanomedicina para protección de la salud humana por sus propiedades de potencial antimicrobiano, antiparasitario, antiproliferativo, proapoptótico, prooxidativo o antioxidante según el contexto, además de su actividad antiinflamatoria, etc.); la agricultura, conocidas como de precisión para una liberación controlada de agroquímicos y un número específico de biomoléculas, para una absorción de nutrientes más eficiente, detección y control de enfermedades de las plantas, etc.; la ciencia y la tecnología de los alimentos, para el (procesamiento, almacenamiento y envasado); la bioingeniería para funcionar como (biocatalizadores, fotocatalizadores y biosensores, etc.); la cosmetología para (protección solar, antienvejecimiento, crecimiento capilar, aporte de compuestos bioactivos y nanoemulsión, etc.), entre otros (Hano & Abbasi, 2021).
Sin embargo, el motivo principal por el que el potencial nanotecnológico se vería limitado es por la preocupación de seguridad cuando las NPs están en contacto con humanos y con animales (Miu & Dinischiotu, 2022).
Pero, aun con lo expuesto, avances recientes en nanotecnología prometen un desarrollo fortalecido a las NPs, con una vida útil mejorada, solubilidad en agua y toxicidad sistémica reducida en los huéspedes. Con la salvedad de que para su síntesis fisicoquímica, se usan productos químicos potencialmente peligrosos y de alto costo (Devatha & Thalla, 2018). Además de las desventajas en términos de consumo de energía y el uso y liberación de sustancias químicas contaminantes (Miu & Dinischiotu, 2022). En la aplicación de la metodología física se utilizan aerosoles, radiación ultravioleta y descomposición térmica, con alta temperatura y presión; para la aplicación de la metodología química, la substancia requerida es el borohidruro de sodio, un reactivo caro y tóxico, así como otros estabilizadores dispersantes y disolventes orgánicos (Ying et al., 2022).
Por lo anterior, la síntesis verde (SV) a diferencia de la síntesis fisicoquímica mencionada; es una alternativa atractiva al emplear organismos vivos; su metodología consiste de tres tipos: síntesis intracelular (endógena), síntesis extracelular (exógena) y el uso de productos bioquímicos específicos (Figura 1), (Miu & Dinischiotu, 2022).
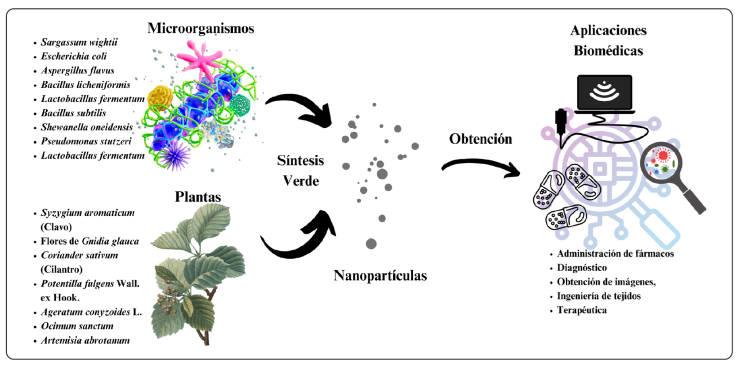
Figura, creatividad personal.
Figura 1 Síntesis verde de NPs de microorganismos/plantas para aplicaciones biomédicas.
Recién, la SV de NPs ha suscitado más atención tanto en la industria como en el mundo académico, debido al uso de componentes biológicos, es una estrategia simple, rentable y relativamente reproducible cuyo resultado son materiales más estables (Devatha & Thalla, 2018). Sin embargo, existen algunas desventajas, por ejemplo, problemas en la extracción de las materias primas, que no están ampliamente disponibles, el tiempo de reacción en general es largo y la calidad de los productos finales no siempre es la esperada, esto, porque el tamaño y la forma de las NPs sintetizadas por diferentes extractos son muy variables, y el tener un contenido determinado de propiedades las hace insuficientes. Los informes actuales muestran grandes diferencias en el tamaño de las partículas, lo que hace que la tecnología verde no sea la adecuada para la producción a gran escala o que el control del tamaño de las partículas durante la producción sea un gran desafío (Ying et al., 2022). La comprensión del mecanismo de biosíntesis es otro factor limitante, lo que dificulta obtener una reacción química precisa que explique el proceso (Ying et al., 2022).
La SV de NPs tiene un enfoque bottom-up (Gautam, Sharma, Tyagi, Kumar & Singh, 2022), en donde la selección de un solvente verde o amigable con el medio ambiente (ej., agua, etanol o sus mezclas), un agente reductor no tóxico y una sustancia segura para su estabilidad, son los tres requisitos más importantes (Hano & Abbasi, 2021). La SV inicia con la combinación de precursores de sales de metales nobles y biomateriales, estos, contienen la siguiente variedad de compuestos: proteínas, alcaloides, flavonoides, azúcares reductores y polifenoles que actúan como agentes reductores de los iones metálicos a un estado de valencia más bajo, al tiempo que funcionan como estabilizadores de las NPs (Ying et al., 2022). La reducción del precursor de la sal metálica a sus respectivas NPs se confirma al observar el cambio de color en la solución coloidal (Dikshit et al., 2021).
Síntesis de nanopartículas por medio de microorganismos
Una situación favorable para la síntesis de NPs es a través del uso de microorganismos, como bacterias, hongos y levaduras.
Estos son capaces de sintetizar NPs al reducir los iones metálicos a sus formas metálicas correspondientes, estabilizarlas y formar partículas a escala nanométrica. Esta síntesis tiene varias ventajas sobre los métodos tradicionales, porque requiere de energía más baja, el uso de precursores ecológicos económicos, y la producción de partículas de tamaño estrecho y formas únicas (Singh, Kim, Zhang & Yang, 2016). Además de que son capaces de sintetizar una amplia gama de NPs de plata, oro, platino, cobre, óxido de hierro y selenio (Jadoun et al., 2022). El proceso está influido por los siguientes factores: los tipos de microorganismo y de iones metálicos utilizados, las condiciones de crecimiento y el pH del medio de reacción.
En la Tabla I se presentan diversas síntesis de NPs y los diferentes microorganismos que se utilizan, uno de los más involucrados es la bacteria Escherichia coli. Esta bacteria se emplea en la biosíntesis extracelular de las NPs de Ag y CuO. En el caso de las de plata, el tamaño de partícula varía en el rango de 5 a 25 nm. Destaca la actividad antimicrobiana de la bacteria antes citada al producir NPs con una mayor eficacia contra diversas bacterias patógenas, como Salmonella typhi, Bacillus subtilis, Klebsiella pneumoniae y Vibrio cholerae (Radulescu, Surdu, Ficai, Grumezescu & Andronescu, 2023).
Tabla I Ejemplos de microorganismos utilizados en la Síntesis verde de NPs.
| Tipo de NP | Microorganismos | Técnicas de síntesis | Precursores metálicos | Tamaño de la partícula | Resultados | Referencias |
|---|---|---|---|---|---|---|
| Ag | Sargassum wightii | Biosíntesis extracelular | AgNO3 | 18 nm | Las proteínas presentes en Sargassum wightii le dan estabilidad a las NPs. | (El-Sheekh, Deyab, Hassan & Abu Ahmed, 2022) |
| Ag | Escherichia coli | Biosíntesis extracelular Reducción de iones Ag+ | AgNO3 | 5 a 25 nm | El microorganismo presenta una mayor actividad antimicrobiana contra Salmonella typhi, Bacillus subtilis, Klebsiella pneumonia y Vibrio cholerae. | (Divya, Kurian, Vijayan & Manakulan, 2016) |
| Ag | Aspergillus flavus | Biosíntesis extracelular | AgNO3 | 10 a 35 nm | Su función es como un agente estabilizador. | (Soltani-Horand, Vahari, Soltani- Horand, Adibpour & Jafarizadeh- Malmiri, 2020) |
| Au | Bacillus licheniformis | Biosíntesis | AuCl | 10 a 40 nm | La bacteria produce péptidos que reducen el cloruro de oro I a NPs de oro. | (Tikariha, Banerjee, Dev & Singh, 2017) |
| Au | Lactobacillus fermentum | Reducción | HAuCl4 | 30 a 50 nm | El ácido láctico producido por la bacteria actúa como un agente reductor. | (Kumar, Vazhacharicka, Mathew & Joy, 2015) |
| ZnO | Bacillus subtilis | Precipitación biológica | ZnCl2 | 20 a 30 nm | La producción de proteínas extracelulares actúa como un agente reductor y estabilizador de las NPs. | (Sabir et al., 2020) |
| Fe2O3 | Shewanella oneidensis | Reducción microbiana | FeCl3 | 10-100 nm | La presencia de grupos amino y carboxilo en la superficie de la bacteria actúan como agentes reductores y estabilizadores de las NPs. | (Mohamed et al., 2021) |
| Ag2O | Lactobacillus fermentum | Síntesis enzimática | AgNO3 | 5-20 nm | La enzima nitrito reductasa presente en la superficie de la bacteria actúa como agente reductor de los iones de plata. | (Garmasheva, Kovalenko, Voychuk, Ostapchuk, Livins´ka & Oleschenko, 2016) |
| CuO | Escherichia coli | Biosíntesis | CuSO4 | 10-20 nm | La presencia de grupos sulfhídrico en la superficie de la bacteria actúan como agentes reductores de los iones de cobre. | (Ghorbani, Fazeli & Fallahi, 2015) |
Es importante mencionar que, si bien, E. coli es utilizada en la síntesis de NPs por reducir iones metálicos y participar en la estabilización de las partículas, la elección del microorganismo también depende de la aplicación específica que se dará a las NPs y las propiedades deseadas, como tamaño, forma y actividad (Kulkarni et al., 2023).
Síntesis de nanopartículas por medio de plantas
La síntesis de NPs a partir del uso de plantas es una técnica emergente y sostenible que utiliza los compuestos orgánicos e inorgánicos de sus extractos para reducir los iones metálicos y producir NPs metálicas (Tabla II), (Chopra et al., 2022; Peralta-Videa, et al., 2016).
Tabla II Ejemplos de plantas utilizadas en la Síntesis verde de NPs.
| Tipos de NP | Plantas | Técnicas de síntesis | Precursores metálico | Tamaño de la partícula | Resultados | Referencias |
|---|---|---|---|---|---|---|
| Au | Clavo | Reducción química | HAuCl4 | 50-70 nm | La presencia de compuestos fenólicos y flavonoides en la planta ayudan a la reducción del cloruro de oro y a la formación de NPs estables. | (Fizer, Mariychuk & Fizer, 2022) |
| Au | Flores de Gnidia glauca | Síntesis verde utilizando un extracto de planta | HAuCl4.3H2O | 10-40 nm | La planta actúa como agente reductor y estabilizador en la síntesis de NPs. | (Ghosh & Patil, 2016) |
| Ag | Coriander sativum (cilantro) | Síntesis verde | AgNO3 | 10-35 nm | Los compuestos fitoquímicos presentes en la planta, como los alcaloides, los flavonoides y los ácidos orgánicos, actúan como agentes reductores y estabilizadores en la síntesis de NPs. | (Alsubki, Tabassum, Abudawood, Rabaan, Alsobaie & Ansar, 2021) |
| Ag | Potentilla fulgens Wall ex Hook.. | Síntesis verde | AgNO3 | 5-50 nm | Potentilla fulgens actúa como un agente reductor y estabilizador en la síntesis de las NPs. | (Mittal et al., 2015) |
| NiO | Ageratum conyzoides L. | Síntesis verde | Ni(NO3)2 6H2O | 20-30 nm | Los compuestos fenólicos presentes en la planta actúan como agentes reductores y los grupos funcionales de la superficie como agentes estabilizadores en la síntesis de NPs. | (Wardani, Yulizar, Abdullah & Apriandanu, 2019) |
| TiO2 | Ocimum sanctum | Síntesis verde | TiO2 | 75 - 123 nm | El extracto de las hojas de Ocimum sanctum se utilizó como agente reductor para la bioproducción. | (Ahmad et al., 2022) |
| MgO | Artemisia abrotanum | Método biológico con materiales vegetales | Mg(NO3)2 | 10 nm | El extracto de Artemisia abrotanum forma esferas y es un estabilizador en la síntesis de NPs. | (Dobrucka, 2018) |
Las ventajas de esta técnica son: la producción de NPs de tamaño uniforme, un bajo uso de compuestos químicos tóxicos y el empleo de plantas comunes y bajo costo (Jadoun, Arif, Jangid & Meena, 2021; Kulkarni et al., 2023); las NPs así favorecen a la industria médica, alimentaria y cosmética (Rajeshkumar, 2016; Włodarczyk & Kwarciak-Kozłowska, 2021).
Entre las plantas son elegidas la avena, el té verde, el té negro, la hoja de menta y la albahaca, entre otras (Asimuddin et al., 2020; Suganthy, Ramkumar, Pugazhendhi, Benelli & Archunan, 2018). Las NPs producidas a partir de los extractos han mostrado propiedades antimicrobianas, antioxidantes y antitumorales, lo que las convierte en un área de investigación en constante crecimiento (Sweidan, Rayyan, Mahmoud & Ali, 2023; Yahia, Benabderrahim, Tlili, Bagues & Nagaz, 2020).
En la Tabla II se precisa que una de las plantas más utilizada en la síntesis de NPs es Coriander sativum, conocida con el nombre común de cilantro. Es útil en el proceso de SV de NPs de plata (Ag) con un tamaño de partícula que oscila entre 10 y 35 nm o sea coloidal, estable y no aglomerada. La actividad más influyente en esta síntesis es la capacidad de acción reductora y estabilizadora que le otorgan los alcaloides, los flavonoides y los ácidos orgánicos presentes en los compuestos fitoquímicos del cilantro. El resultado son características fisicoquímicas y tecnológicas adecuadas, por su tamaño homogéneo y un índice de polidispersión bajo (Ritu, Das & Chandra, 2023).
La elección de la planta y sus propiedades fitoquímicas específicas es crucial en la síntesis de NPs, ya que determina en gran medida la calidad y las características de las partículas producidas. En el caso de Coriander sativum, su capacidad para reducir y estabilizar las NPs de plata la convierte en una elección valiosa en la SV de nanomateriales con aplicaciones prometedoras en diversas áreas científicas y tecnológicas.
Factores que afectan la síntesis verde de nanopartículas
La síntesis de NPs al utilizar microorganismos y plantas se ha convertido en una alternativa más sustentable y respetuosa con el medio ambiente a diferencia de las técnicas químicas tradicionales (Bahrulolum et al., 2021). La síntesis de NPs mediante el uso de microorganismos y plantas es un campo de investigación en constante evolución. Diversos factores, como el pH, la concentración del precursor, la temperatura y el tiempo de incubación influyen en este proceso y afectan las propiedades finales de las NPs (Fagier, 2021). La Tabla III muestra algunos ejemplos de factores que pueden perjudicar a la SV de estas a partir del uso de plantas o microorganismos.
Tabla III Factores que afectan a las propiedades de las plantas y los microorganismos en el proceso de síntesis de las NPs.
| Factores | Tipos de NP | Microorganismos/Plantas | Efectos | Referencias |
|---|---|---|---|---|
| pH | Au | Bacillus licheniformis | Un pH neutro o ligeramente alcalino es óptimo para la síntesis de NPs, la diferencia son los pH ácidos que inhiben la síntesis. | (Tikariha et al., 2017) |
| ZnO | Bacillus subtilis | Un pH neutro (próximo a 7) favorece la síntesis de NPs de ZnO más estables y de menor tamaño. | (Sabir et al., 2020) | |
| Ag | Escherichia coli | Hay un incremento de NPs de plata en pH más bajos. Las enzimas reductasas que se producen en la síntesis, se desactivan a medida que las condiciones se vuelven más alcalinas. | (Divya et al., 2016) | |
| Fe2O3 | Shewanella oneidensis | Un pH básico (9.5) favorece la formación de NPs de hematita con una forma más definida y homogénea, diferente a un pH ácido (4.5) que produce NPs menos definidas y más irregulares. | (Mohamed et al., 2021) | |
| Ag2O | Lactobacillus fermentum | Un pH más alto (próximo a 9) favorece la formación de NPs más grandes y aglomeradas. | (Garmasheva et al., 2016) | |
| Au | Syzygium aromaticum (Clavo) | Un pH neutro (7) es óptimo para la síntesis de NPs. | (Fizer et al., 2022) | |
| Au | Flores de Gnidia glauca | Influyen en la reducción del ion áurico (Au3+) y en la formación de NPs de oro. El pH óptimo para la síntesis de NPs de oro es de 7.0. | (Ghosh & Patil, 2016) | |
| Ag | Coriander sativum (Cilantro) | Un pH más bajo favorece la formación de NPs de plata de menor tamaño. | (Alsubki et al., 2021) | |
| NiO | Ageratum conyzoides L. | El pH de la solución influye en la síntesis de NPs y actúa como estabilizador de los iones metálicos. | (Wardani et al., 2019) | |
| Concentración del precursor | Ag | Pseudomonas deceptionensis | Una concentración óptima de nitrato de plata aumenta la producción de NPs de plata. | (Jo et al., 2016) |
| Au | Bacillus licheniformis | La concentración del precursor influye en la formación de NPs y su tamaño, por esto se busca el equilibrio entre una alta concentración (mayor producción de NPs) y una baja concentración (mayor control del tamaño y forma de las NPs). | (Tikariha et al., 2017) | |
| ZnO | Bacillus subtilis | A mayor concentración de la solución de Zn2+ (entre 3 y 5 mM), las NPs de ZnO son más grandes y en su superficie absorben una mayor cantidad de iones Zn2+. | (Sabir et al., 2020) | |
| Ag2O | Lactobacillus fermentum | A una mayor concentración de nitrato de plata se forman NPs más grandes y aglomeradas. | (Garmasheva et al., 2016) | |
| Au | Syzygium aromaticum (Clavo) | En una mayor concentración de la solución precursora las NPs son más grandes. | (Fizer et al., 2022) | |
| Au | Flores de Gnidia glauca | A medida que se aumenta la concentración de extracto de flores, las NPs son de menor tamaño y la forma es más uniforme. | (Ghosh & Patil, 2016) | |
| Ag | Coriander sativum (Cilantro) | En una mayor concentración de la sal de plata y del extracto las NPs son de mayor tamaño. | (Alsubki et al., 2021) | |
| Tiempo de incubación | ZnO | Bacillus subtilis | A mayor tiempo de incubación (24, 48 y 72 horas), las NPs de ZnO son de mayor tamaño y más estables a largo plazo. | (Sabir et al., 2020) |
| Temperatura de incubación | Ag | Escherichia coli | Al aumentar la temperatura a 37 °C, se incrementan tanto la producción de NPs de Ag como la velocidad de reacción, por esto la mayoría de los iones Ag+ se consumen en la formación de los núcleos. | (Divya et al., 2016) |
| Ag | Pseudomonas deceptionensis | Una temperatura de incubación de (37 °C) óptima, favorece la producción de NPs de plata. | (Jo et al., 2016) | |
| Au | Bacillus licheniformis | La temperatura de incubación influye en la tasa de síntesis de NPs y en su tamaño, por lo que es importante mantener una temperatura óptima para el crecimiento del microorganismo y la formación de las NPs. | (Tikariha et al., 2017) | |
| Temperatura de reacción | Au | Syzygium aromaticum (Clavo) | Una temperatura de reacción de 80 °C fue la óptima para la formación de NPs. | (Fizer et al., 2022) |
| Au | Flores de Gnidia glauca | La temperatura de reacción afecta su velocidad y la formación de las NPs. Por consiguiente, a 60 °C se lleva a cabo la síntesis de las NPs. | (Ghosh & Patil, 2016) | |
| Ag | Coriander sativum (Cilantro) | Una temperatura de reacción más baja favorece la formación de NPs de menor tamaño. | (Alsubki et al., 2021) | |
| NiO | Ageratum conyzoides L. | La temperatura influye en la velocidad de la reacción y en la estabilidad de las NPs sintetizadas. | (Wardani et al., 2019) |
En el caso de los microorganismos, las diferentes especies microbianas tienen distintas capacidades para reducir los iones metálicos y producir NPs. De igual forma, las condiciones de cultivo (pH, temperatura y concentración de iones metálicos), influyen en la tasa y la eficacia de la síntesis (Figura 2), (Lahiri et al., 2021). Otras propiedades relevantes que se ven afectadas por estos factores son el tamaño y la forma de las NPs. La forma y el tamaño de ellas intervienen en su actividad biológica, distribución y acumulación en tejidos específicos, como los pulmones, riñones o hígado. Asimismo, suelen presentar un recubrimiento de biomoléculas derivadas de la especie microbiana, lo que repercute en su estabilidad y actividad biomédica. Este recubrimiento puede generar partículas de mayor tamaño. Un incremento en el tamaño de las partículas facilita su eliminación del cuerpo en periodos más cortos, ya que el organismo puede eliminarlas más rápidamente a través de procesos biológicos como la filtración renal o la fagocitosis por parte del sistema inmunológico (Gomathi, Rajeshwari, Kanchaa, Sudha & Parthasarathy, 2019).
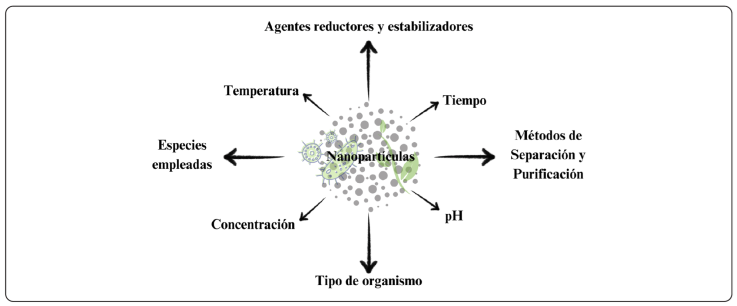
Figura, creatividad personal.
Figura 2 Factores que pueden afectar en las propiedades o el proceso de síntesis de las NPs.
Por otro lado, la amplia gama de biomoléculas producidas por las plantas (polisacáridos, proteínas y ácidos nucleicos) actúan como agentes reductores y estabilizadores de las NPs (Shukla & Iravani, 2018). En los procesos de síntesis con plantas, los factores que inciden en este proceso incluyen la especie vegetal, las condiciones de cultivo, el tipo de extracto vegetal utilizado y el pH del medio.
En lo que respecta al pH, se ha observado que uno neutro o ligeramente alcalino es especialmente propicio para la síntesis exitosa de las NPs. Por ejemplo, en la producción de NPs de oro (Au), este rango de pH promueve la formación de partículas estables y bien formadas. Por otro lado, en el caso de las NPs de plata (Ag), la variación del pH tiene un impacto significativo. Un pH más bajo tiende a incrementar la cantidad de NPs, diferente a las condiciones alcalinas que inhiben la síntesis por la desactivación de las enzimas reductoras cruciales. En lo que se refiere a la síntesis de NPs de óxido de zinc (ZnO), un pH neutro favorece la obtención de partículas de menor tamaño y mayor estabilidad.
La concentración del precursor alta u óptima y baja es otro factor esencial para encontrar el equilibrio en la síntesis de NPs de metales como Ag y Au. Las óptimas permiten maximizar la producción y controlar el tamaño y la forma de las NPs. Este equilibrio es también crucial en la generación de las NPs de ZnO, donde concentraciones más altas de iones Zn2+ influyen en el tamaño y en la cantidad de iones adsorbidos en la superficie de las partículas.
La temperatura es otro factor crítico en la síntesis de producción de NPs de Ag, temperaturas de incubación en torno a los 37 °C aumentan la velocidad de su formación al incrementar la tasa de reacción y consumo de iones Ag+. De manera similar ocurre en las de Au, la temperatura de incubación influye en la tasa de síntesis y el tamaño de las partículas. Además, en la síntesis de NPs de ZnO, los tiempos de incubación son más prolongados, de 24, 48 y 72 h, para lograr partículas de mayor tamaño y estabilidad.
Campos de potencial aplicación biomédica de NPs inorgánicas
El campo biomédico ha sido testigo de notables avances en los últimos años, particularmente en el área de la nanotecnología. Las NPs, con sus propiedades físicas y químicas únicas, se han convertido en candidatas prometedoras para diversas aplicaciones biomédicas. A través de las estrategias de SV se da la producción de NPs con tamaño, forma y propiedades de superficie controlados, que son fundamentales para su aplicación biomédica (Ray & Bandyopadhyay, 2021).
En el ámbito de la biomedicina, estas NPs han mostrado un gran potencial en diversas áreas, incluida la administración dirigida de fármacos, el diagnóstico, la obtención de imágenes, la ingeniería de tejidos y la terapéutica. Ofrecen también una plataforma versátil para la liberación precisa de agentes terapéuticos en sitios específicos del cuerpo. Sus propiedades fisicoquímicas únicas, como la alta relación área superficial/ volumen y la química de superficie ajustable, permiten una encapsulación, una protección y una liberación controlada y eficiente de los fármacos, lo que da como resultado una eficacia terapéutica mejorada y efectos secundarios reducidos (Millot, 2020; Rezić, 2022).
Además, estas NPs han demostrado ser valiosas en diagnóstico e imágenes biomédicas. Sus propiedades ópticas, magnéticas o luminiscentes inherentes las convierten en excelentes agentes de contraste para diversas modalidades de imágenes, incluidas las de resonancia magnética (IRM), las de tomografía computarizada (TC) y las de fluorescencia. Además, el funcionamiento de estas NPs con ligandos o biomoléculas específicos permite obtener imágenes para detectar enfermedades o biomarcadores específicos que facilitan un diagnóstico temprano y el seguimiento preciso de respuestas en un tratamiento (Han, Xu, Taratula & Farsad, 2019).
Su aplicación también se extiende más allá de la administración de fármacos y el diagnóstico, se estudian cada vez más por su potencial en la ingeniería de tejidos, donde pueden servir como andamios, soportes o transportadores para el crecimiento celular y la regeneración de tejidos. Al imitar la matriz extracelular, estas NPs pueden brindar soporte estructural, promover la adhesión celular y facilitar la liberación controlada de factores de crecimiento, mejorando así los procesos de regeneración y reparación de tejidos.
Además, las NPs también han demostrado su potencial en intervenciones terapéuticas. Se pueden diseñar con propiedades antimicrobianas inherentes, para combatir infecciones bacterianas resistentes a los medicamentos, incluso se utilizan para la hipertermia dirigida, la terapia fotodinámica y la administración de genes, lo que ofrece nuevas vías para el tratamiento del cáncer y otras enfermedades (Fathi-Achachelouei et al., 2019; Hasan, Morshed, Memic, Hassan, Webster & Marei, 2018; Matić, Sher, Ferhat & Sher, 2023).
Selvaraj y cols., evaluaron la biosíntesis de las NPs de Ag con extracto metanólico de las algas Sargassum wightii y Valonopsis pachynem. Al realizar un análisis fitoquímico a los extractos de V. pachynem, se identificó la presencia de glucósidos cardíacos, compuestos fenólicos y carbohidratos, en el de S. wightii hubo esteroides, taninos, glucósidos cardíacos, carbohidratos, compuestos fenólicos, azúcares reductores y saponinas. Se probó la actividad antibacteriana de los extractos de algas y de las NPs de Ag sintetizadas a partir de estos contra Micrococcus luteus (bacteria Gram positiva) y Serratia marcescens (bacteria Gram negativa), dos bacterias relacionadas con la endocarditis y las infecciones cutáneas. Los resultados revelaron que una concentración de 150 ppm de las NPs sintetizadas a partir de S. wightii mostraron una máxima actividad antibacteriana contra M. luteus y S. marcescens comparada con las sintetizadas a partir de V. pachynes (Selvaraj et al., 2020).
Por otro lado, Vinoj y cols., evaluaron in vitro el efecto citotóxico de las NPs de Au recubiertas con proteínas de gomoserina Lactosana N-aciladas (AiiA AuNPs), obtenidas a partir de Bacillus licheniformis. Los autores reportan que con el tratamiento de las NPs de Au recubiertas con la proteína AiiA hubo una reducción significativa en la producción de exopolisacáridos, actividades metabólicas e hidrofobicidad de la superficie celular. Además, se observó una potente actividad antibiopelícula contra las especies de Proteus resistentes a múltiples fármacos, en comparación al tratamiento con la proteína AiiA sola. Esta actividad antibiopelícula, se obtuvo con concentraciones de 2 a 8 μM, sin causar daño a los macrófagos. Las NPs de Au recubiertas con AiiA mostraron la capacidad de eliminar bacterias sin dañar a las células huésped (Vinoj, Pati, Sonawane & Vaseeharan, 2015).
En el caso de las NPs sintetizadas a partir de plantas, Rajeshkumar y cols., evaluaron las NPs de Au bifuncionales y sintetizadas con extractos de la planta Syzygium aromaticum (clavo), posteriormente se aplicaron a diversos cultivos de células cancerígenas. Los resultados del estudio indicaron que los radicales libres producidos por las NPs de Au eran los agentes responsables de la actividad anticancerígena observada. Para corroborar la capacidad que tenían para eliminar a los radicales libres, se llevó a cabo un ensayo con óxido nítrico con el fin de medir la eficacia de las NPs de Au en esta tarea. Con ello se demostró que si eran suprimidos de manera dosis-dependiente, es decir, la eficacia de erradicarlos aumentaba proporcionalmente con la dosis de NPs de Au administrada. Esto sugiere un mecanismo potencial para la actividad anticancerígena de estas bifuncionales obtenidas a partir de esta planta (Rajeshkumar, 2016).
Mittal y cols., desarrollaron un método de síntesis de NPs de Ag con extractos de la planta medicinal Potentilla fulgens. Evaluaron las propiedades anticancerígenas y antimicrobianas de las NPs. Los análisis fitoquímicos revelaron que los componentes adsorbidos en la superficie de estas eran principalmente flavonoides. Además, se evaluó su citotoxicidad contra diversas líneas celulares de cáncer, lo que demostró su potencial anticancerígeno. Se llevó a cabo un estudio adicional para evaluar su efecto apoptótico tanto en las células normales como en las cancerígenas. Se realizó un ensayo con azul de tripano y un análisis de citometría de flujo. Los resultados indicaron que las NPs sintetizadas tenían la capacidad de eliminar células cancerígenas en mayor medida en comparación con las células normales. Además, demostraron una actividad antimicrobiana comparable contra bacterias Gram positivas y Gram negativas, lo que indica su potencial en la lucha contra diversas infecciones bacterianas (Mittal et al., 2015).
Adicionalmente, Ahmad y cols., desarrollaron un método de síntesis ecológica de las NPs de TiO2 con extractos de hojas de Ocimum sanctum. Se les incorporó un gel de quitosano (CS) con el objetivo de tratar y curar heridas en pacientes diabéticos y exhibieron propiedades tixotrópicas deseadas y un comportamiento pseudoplástico. Se realizaron estudios in vivo de cicatrización de heridas y análisis histopatológicos de las heridas cicatrizadas, lo que comprobó la notable eficacia del gel CS que contiene las NPs de TiO2 en la cicatrización de heridas en ratas diabéticas. Esta actividad fue confirmada al medir el área de contracción de la herida en relación al tiempo transcurrido desde el inicio del tratamiento (Ahmad et al., 2022).
Conclusiones
El avance en los estudios de la síntesis verde de nanopartículas inorgánicas ha permitido, como se mencionó, el desarrollo de nanoestructuras sustentables que no afectan al medio ambiente, al reducir significativamente el impacto de las sustancias tóxicas y la generación de residuos peligrosos, al tiempo que favorecen la producción de nanopartículas estables y biocompatibles convertidas en herramientas versátiles para la biomedicina, especialmente en el diagnóstico y tratamiento de diversas enfermedades. Esta revisión muestra un área de trabajo interdisciplinaria con la química, la biología y la medicina, que fomenta la investigación y el desarrollo de soluciones terapéuticas y diagnósticas más efectivas y seguras. A medida que se avanza en el conocimiento de este campo, se abren nuevas perspectivas biomédicas. La síntesis verde de nanopartículas inorgánicas da lugar al desarrollo de nuevas tecnologías para el bienestar común. Sin embargo, existen desafíos que deberán superarse con el fin de maximizar el potencial de las nanopartículas inorgánicas.











 nueva página del texto (beta)
nueva página del texto (beta)


