Introducción
El fósforo (P) es un elemento esencial para el óptimo crecimiento y desarrollo de las plantas. La mayoría de las plantas terrestres lo absorben del suelo exclusivamente en forma de ortofosfato inorgánico (Pi) (Vance, Uhde -Stone & Allan, 2003). Sin embargo, la movilidad limitada del Pi en el suelo y su conversión a formas insolubles que las plantas no pueden absorber hacen que la fertilización del Pi sea ineficiente (Vance et al., 2003; López-Arredondo, Leyva-González, González-Morales, López-Bucio & Herrera-Estrella, 2014). Para soportar esta deficiencia, las plantas han desarrollado distintos tipos de respuestas adaptativas para promover la adquisición del Pi (Phosphate Starvation Responses; PSR) (Rubio, Linhares, Solano, Martõn, Iglesias & Leyva, 2001; Wild, Gerasimaite, Jung, Truffault, Pavlovic & Schmidt, 2016; Rico-Reséndiz et al., 2020). Estas respuestas incluyen cambios en el sistema de la arquitectura de la raíz, un aumento en la expresión de sus transportadores para mejorar su captación, el cambio de fosfolípidos hacia lípidos sin P (principalmente sulfolípidos y galactolípidos), así como adaptaciones metabólicas que reducen la demanda de ATP y permiten optimizar el uso interno del Pi (Wild et al., 2016; Castrillo et al., 2017). Las PSR van acompañadas de una reprogramación de la transcripción en todo el genoma (Bustos et al., 2010) y se ha identificado al factor transcripcional Phosphate Starvation Response1 (PHR1) como el regulador maestro de muchos de estos genes. PHR1 reconoce un elemento en cis denominado PHR1-Binding Sequence (P1BS), que contiene la secuencia 5’-GnATATnC-3’ presente en un gran número de genes que se expresan en respuesta a los cambios en la disponibilidad de Pi (Rubio et al., 2001; Wang, Zheng, Zhu, Kong & Liu, 2022) . En Arabidopsis thaliana, PHR1 pertenece a una familia de factores transcripcionales (TF) del tipo MYB-CC, que consta de 15 miembros divididos en dos clados (clados A y B) (Rubio et al., 2001; Wang et al., 2022). Ambos clados tienen en común la presencia de los dominios tipo MYB (para unión al DNA) y dominios Coiled-Coil (CC, para la formación de dímeros). Difieren en su estructura con la presencia de una parte adicional en el extremo N-terminal de la proteína por parte de los miembros del clado A, a diferencia de los miembros del clado B que tienen una extensión hacia el extremo C-terminal (Wang et al., 2022) (Figura 1).
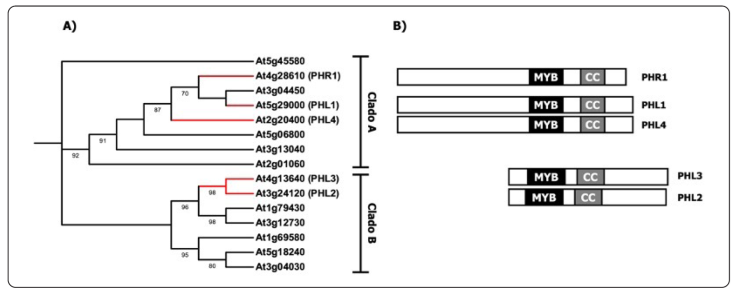
Modificado de Wang et al., 2022.
Figura 1 Relación filogenética de los miembros de la familia MYB-CC en Arabidopsis thaliana. A) Filograma de las proteínas MYB-CC en Arabidopsis thaliana, estos se agrupan en dos clados distintos y, B) Diagrama que muestra la estructura de la proteína y en la que se resalta la presencia de los dominios tipo MYB (para unión a DNA) y dominios Coiled-Coil (CC, para la formación de dímeros). Las proteínas que pertenecen al clado A presentan una extensión hacia el extremo N-terminal de la proteína, en lo opuesto los miembros del clado B tienen una extensión hacia el extremo C-terminal.
Además de PHR1 se han identificado a otros cuatro miembros de la familia MYB-CC denominados PHR1-like (PHL1-4) que también participan en la regulación de la homeostasis del Pi. Sin embargo, a pesar de que existe un efecto sinérgico entre estos miembros, PHR1 representa el TF principal que regula la expresión de más del 80% de los genes que se expresan durante la deficiencia de Pi (Bustos et al., 2010; Barragán-Rosillo, Peralta-Alvarez, Ojeda-Rivera, Arzate-Mejía, Recillas-Targa & Herrera-Estrella, 2021). La mutante por pérdida de función phr1 presenta una disminución en la expresión de genes que se inducen por su deficiencia, o sea, una disminución en el contenido del Pi total, así como una reducción en la acumulación de las antocianinas. Además, la mutante phr1 tiene una menor biomasa y la relación del crecimiento de brotes y raíces son significativamente menores en comparación con la planta tipo silvestre (WT) (Rubio et al., 2001). Por el contrario, la sobreexpresión de PHR1 da como resultado una mayor acumulación del Pi y por lo tanto síntomas de toxicidad (Nilsson, Muller & Nielsen, 2007).
Algunos otros miembros de la familia MYB-CC como PHL1 desempeñan funciones parcialmente redundantes con respecto a PHR1 (Barragán-Rosillo et al., 2021). La expresión de genes relacionados a la PSR en el mutante phl1 que crecen en deficiencia de Pi, tienen una reducción en comparación con la expresión en la planta silvestre, pero este efecto es menor cuando se compara con el mutante de phr1. Al analizar la expresión en la doble mutante phr1phl1, se observa que sus niveles disminuyen aún más en comparación con el mutante phr1 (Bustos et al., 2010). Estos resultados indican que hay una redundancia parcial de funciones entre PHL1 y PHR1, pero también sugieren que existe un efecto aditivo en la función de ambos factores de transcripción. Además, dado que aún en la doble mutante no se abate completamente la expresión de algunos de estos genes, es posible suponer la presencia de otros mecanismos que controlan a la PSR (Bustos et al., 2010).
Se han identificado ortólogos de PHR1 que participan en la homeostasis celular del P en diversas especies de plantas (Wang et al., 2022). En el arroz, por ejemplo, el ortólogo de Arabidopsis, denominado OsPHR2, desempeña un papel crucial por aumentar la expresión de sus transportadores, convirtiéndolo en tóxico y dar origen a plantas más pequeñas con clorosis o necrosis en los márgenes de las hojas (Zhou et al., 2008). Estos datos sugieren que las proteínas PHR1 tienen un papel universal y predominante en la regulación de las respuestas al estrés por P. La diversidad funcional dentro de la familia revela la complejidad de sus mecanismos y plantea nuevas preguntas sobre cómo se coordinan estas proteínas para garantizar la adaptación eficaz ante este estrés nutrimental.
Cascada de señalización de PHR1
En las plantas de Arabidopsis crecidas en condiciones de deficiencia del Pi, PHR1 induce la acumulación de miR399, un RNA no codificante que se une al transcrito de PHOSPHATE 2 (PHO2) provocando su degradación (Liu, Huang, Tseng, Lai, Lin & Lin, 2012; Motte & Beeckman, 2017). En condiciones normales, la actividad de PHO2, que actúa como una enzima E2-conjugadora de ubicuitina, es responsable de la degradación de los transportadores del Pi a través del proteasoma (Liu et al., 2012). De esta manera, la acumulación de miR399 y la regulación negativa de PHO2 liberan el control negativo de los transportadores, lo que resulta en un aumento en la captación de Pi y su translocación a diferentes partes de la planta. Adicionalmente, la degradación de PHO2 mediada por miR399 es regulada por un RNA largo no codificante denominado Induced by Phosphate Starvation1 (IPS1). IPS1 es inducido por PHR1 y su transcrito es capaz de secuestrar a miR399, evita la degradación de PHO2 y mantiene la homeostasis del Pi, al modular la estabilidad de los transportadores de la familia PHT1 (PHOSPHATE TRANSPORTER1) (Rubio et al., 2001; Franco-Zorrilla, Valli, Todesco, Mateos, Puga & Rubio-Somoza, 2007) (Figura 2 y Figura 3).
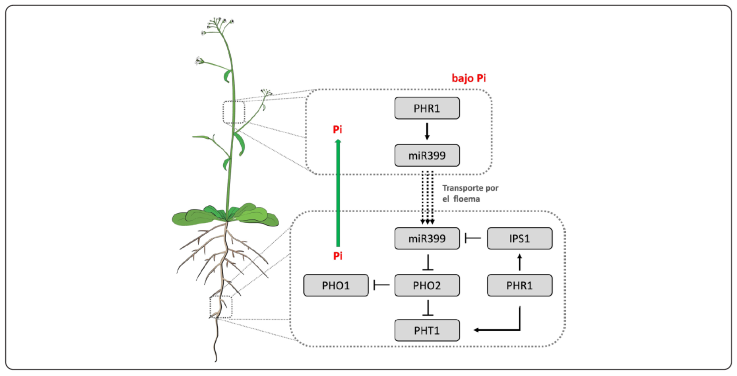
Figura creatividad de J.M. González-Coronel.
Figura 2 Homeostasis de Pi en Arabidopsis thaliana. En condiciones de deficiencia de Pi, se induce la expresión de miR399 en la parte aérea, desde donde es transportado hacia la raíz para inactivar a PHO2. La regulación de PHO2 previene la degradación de los transportadores PHO1 y PHT1, que aumentan la captación y translocación de Pi. La deficiencia de Pi también induce la expresión de IPS1, que se une a miR399 para modular su actividad.
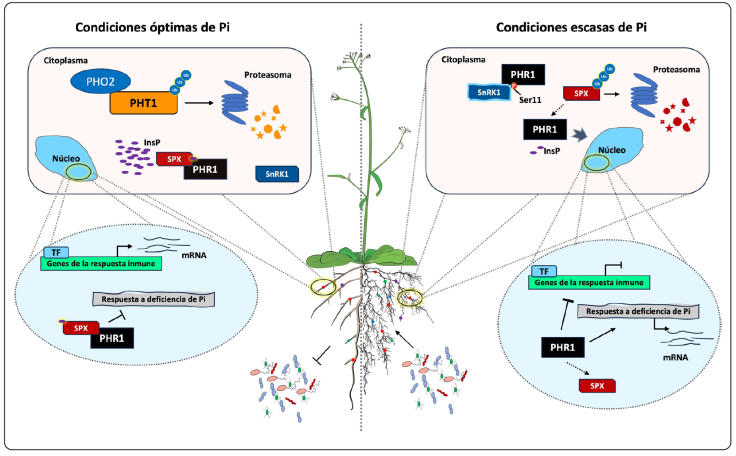
Figura 3 Función de PHR1 en el balance entre la respuesta inmune de la planta y la homeostasis de Pi. En condiciones óptimas de Pi, la microbiota asociada a las plantas se forma mediante la modulación del sistema inmunológico de las plantas. SPX1 se une a PHR1 debido a cambios conformacionales inducidos por la unión de InsPs, impidiendo su asociación con el elemento P1BS en el promotor de los genes de la PSR y se activan los mecanismos de defensa para prevenir la colonización por microorganismos. En condiciones de deficiencia de Pi, PHR1 se libera de SPX y se une a los promotores de los genes de la PSR para activar su expresión y al mismo tiempo reprimir ciertos genes de defensa para permitir que se establezca la interacción con microorganismos que ayuden a mejorar la captación de Pi (Modificado de Motte & Beeckman, 2017).
¿Cómo se regula la actividad de PHR1?
Regulación a nivel transcripcional
En las plantas de Arabidopsis, no ocurren cambios significativos en los niveles de PHR1 en respuesta a la disponibilidad de Pi y este comportamiento es extensivo a sus homólogos en otras especies vegetales (Valdés-López & Hernández, 2008; Zhou et al., 2008). El análisis del promotor y la región 5’ UTR de PHR1 permitió identificar a tres elementos de respuesta a las auxinas que unen a dos TF, ARF7 y ARF9 para regular positivamente su expresión génica. Mutantes sencillos o dobles de arf7 y arf9 muestran una reducción de más del 50% en la expresión de los genes como IPS1, At4, PHT1;1, ACP5 y RNS1 que son blancos directos de PHR1, al enfatizar el papel de estos TF como reguladores positivos de su expresión (Huang et al., 2018).
Modificaciones post-traduccionales
Las modificaciones postraduccionales (PTM) se producen en uno o más aminoácidos y son catalizadas por enzimas que reconocen secuencias específicas. Una de las PTM que ocurre en las células eucariotas es la SUMOilación, que implica la unión de una proteína modificadora relacionada con la ubicuitina o SUMO (Small-Ubiquitin-related Modifier), (Miura, Lee, Jin, Yoo, Miura & Hasegawa, 2009; Han, Lai & Yang, 2021). En Arabidopsis, la proteína E3-ligasa de SUMO denominada SIZ1 (SAP and MIZ/SP-RING zinc finger domain-containing protein1) se encarga de SUMOilar a PHR1 in vitro en los residuos de lisina de las posiciones 261 y 372 (Miura, Rus & Sharkhuu, 2005; Miura et al., 2009; Rojas-Triana, Bustos, Espinosa-Ruiz, Prat, Paz-Ares & Rubio, 2013). La mutante siz1 presenta un retraso en el crecimiento de la raíz primaria en comparación con las plantas del tipo silvestre en condiciones limitantes de Pi, que se reestablece con una suplementación del faltante (Miura et al., 2005; Catala et al., 2007); pero también, en condiciones de deficiencia de Pi, los niveles de acumulación de los transcritos de diversos genes de la PSR presentes en esta mutante, son similares a los de plantas WT, solo en el caso de los transcritos de AtIPS1 y AtRNS1 (Ribonuclease1), su acumulación disminuye (Miura et al., 2005; Miura et al., 2009). Estos resultados sugieren que la SUMOilación afecta la actividad de PHR1 solo en algunos promotores, lo que posiblemente tiene que ver con la interacción con proteínas auxiliares (Miura et al., 2005; Miura et al., 2009).
La modificación covalente de proteínas desempeña un papel fundamental en la regulación de su actividad e influye en su localización y en su capacidad para interactuar con otras proteínas (Hao et al., 2023). Se ha observado que las alteraciones en la fosforilación de las proteínas son una respuesta a la deficiencia del Pi en las raíces de las plantas (Li, Xu, Fan, Zhang, Hou & Yang, 2014; Yang, Xie, Yang, Liu & Lin, 2019). Recientemente, Trejo-Fregoso y colaboradores (2022) demostraron que PHR1 es fosforilado en el residuo de serina (S) en la posición 11 por las cinasas de la familia SnRK1. De acuerdo con la base de datos PhosPhat v4.0 (https://phosphat.uni-hohenheim.de/), este residuo está contenido en una región de 21 aminoácidos que abarca, desde S11 a S32, distintos restos de serina y treonina que son susceptibles a ser fosforilados. La fosforilación de la S11 ejerce un impacto negativo en la actividad transcripcional de PHR1, evaluada mediante la expresión transitoria de un gen reportero bajo el control de un promotor inducible por deficiencia de Pi (Trejo-Fregoso et al., 2022). El residuo S19, ubicado en la misma región que S11, también presenta una firma de fosforilación reconocida por las cinasas de la familia SnRK1 y podría ser susceptible a una regulación (Trejo-Fregoso et al., 2022).
Otra forma de controlar la actividad transcripcional de PHR1 en respuesta a los niveles de Pi, es a través de su interacción con las proteínas que contienen un dominio SPX (SIG1-PHO81-XPR1) (Ried et al., 2021). En Arabidopsis, se han identificado cuatro proteínas SPX denominadas SPX1-4, y cada una desempeña un papel específico en la percepción y en la regulación de la disponibilidad del Pi, lo que es fundamental para la supervivencia y el crecimiento de la planta en diversos entornos (Puga, Mateos, Charukesi, Wang, Franco-Zorrilla & de Lorenzo, 2014). En el núcleo, AtSPX1 y AtSPX2 reprimen la actividad de PHR1 por interacción física y evitan que se una al elemento P1BS de los genes que son inducidos en respuesta a la deficiencia de Pi (Duan, Yi, Dang, Huang, Wu & Wu, 2008; Puga et al., 2014). La interacción entre PHR1 y SPX1/2 depende de la concentración celular de Pi, siendo más fuerte en condiciones de suficiencia de este elemento. Además, la transcripción de SPX1/2 es inducida por PHR1 durante su escasez lo que indica la existencia de un mecanismo de regulación con retroalimentación negativa entre SPX1/2 y PHR1 (Puga et al., 2014). La interacción entre PHR1 y las proteínas con dominio SPX se conservan en otras especies vegetales, como el arroz, en donde OsSPX1/2 interactúa con OsPHR2 en el núcleo para evitar la unión de OsPHR2 al elemento P1BS (Zhou et al., 2008; Wang et al., 2014). Las proteínas SPX4 en Arabidopsis y OsSPX4 y OsSPX6 en el arroz interactúan con PHR1 en el citoplasma para inhibir la translocación nuclear de PHR1 cuando hay suficiente Pi (Lv et al., 2014; Zhong et al., 2018), pero cuando es escaso OsSPX4 y OsSPX6 son degradados por acción del sistema ubicuitina -proteasoma, liberando así a OsPHR2 (Lv et al., 2014; Zhong et al., 2018). La interacción de PHR1 con las proteínas SPX requiere de la participación de los polifosfatos de inositol (InsP) incluyendo el fitato (InsP6), InsP7 y a InsP8. Este último posee la mayor afinidad por las proteínas SPX y su presencia depende del contenido de Pi intracelular (Park, Jeong, Huang, Park & Chua, 2023). Los InsP6-8 tienen la capacidad de unirse a las proteínas SPX y estabilizar su unión con PHR1 para secuestrarlo (Puga et al., 2014; Park et al., 2023). En consecuencia, la señalización en deficiencia de Pi que depende de PHR1 se activa cuando los niveles de InsP6- 8 son bajos y las proteínas SPX lo liberan (Puga et al., 2014). Aunado a ello provoca que las proteínas SPX sean degradadas en el proteasoma, lo que permite que PHR1 se libere y se active la PSR (Figura 3), (Puga et al., 2014).
PHR1 está involucrado en la homeostasis entre la nutrición y la respuesta inmune de la planta
En la naturaleza, las plantas enfrentan varios tipos de estrés, tanto bióticos como abióticos, y es crucial que sean capaces de integrarlos para responder de manera efectiva y adaptarse a su entorno (Haqcuard, 2016; Isidra-Arellano, Delaux & Valdés-López, 2021). Durante la deficiencia de Pi, las plantas presentan adaptaciones morfológicas, bioquímicas y metabólicas para incrementar su captación y su reutilización y algunas de ellas están coordinadas por el regulador transcripcional PHR1. Por otro lado, la interacción con la microbiota de la rizosfera ofrece ventajas significativas para aumentar la disponibilidad de este elemento; es el caso de ciertas bacterias y hongos que liberan enzimas que descomponen los compuestos fosfatados insolubles (Motte & Beeckman, 2017). La interacción entre las raíces y los diversos microorganismos que habitan en la rizosfera es compleja; se han identificado organismos patógenos, benéficos y neutros. Aunque el mecanismo de reconocimiento de las diferentes interacciones aún no se conoce completamente, en el caso de los organismos patógenos se ha identificado un patrón de respuesta que conduce a la activación del sistema inmune de las plantas permitiéndoles combatir esta agresión. Inicialmente, algunas moléculas producidas y secretadas por las bacterias (patrones moleculares asociados a los microbios, MAMPs) son reconocidas por receptores específicos, lo que desencadena una respuesta de defensa. Sin embargo, estas mismas moléculas también son producidas por bacterias que podrían contribuir al aumento de la absorción de los nutrientes. Para aprovechar este beneficio, es crucial permitir la asociación de estas bacterias, lo que requiere una coordinación entre la respuesta al estrés nutricional y la respuesta inmune (Tzipilevich, Russ, Dangl & Benfey, 2021).
Trabajos realizados por Hacquard y colaboradores (2016) analizaron el patrón de expresión en las raíces de Arabidopsis colonizadas por hongos del género Colletotrichum, comparando la respuesta al usar una especie benéfica (C. tofieldiae, Ct) y una patógena (C. incanum, Ci) cuando crecían en diferentes concentraciones de Pi y en condiciones de deficiencia, estos autores observaron que la asociación con la especie benéfica se veía favorecida, al reducirse las respuestas de defensa y la respuesta inmune se activaba contra la especie patógena. La forma como las plantas coordinan la activación de las PSR con la reducción de la respuesta de defensa comenzó a quedar clara a partir de los trabajos de Castrillo y colaboradores (2017), quienes al utilizar una comunidad bacteriana sintética (SynCom) asociada a las raíces de Arabidopsis, vieron el efecto que esta comunidad tenía sobre la transcripción cuando las plantas crecían en suficiencia y deficiencia de Pi. Los resultados mostraron que la presencia de las bacterias incrementaba la expresión de los genes que componen la PSR. Al comparar las plantas de tipo silvestre con las plantas mutantes phr1, apreciaron una disminución en la expresión de los genes asociados a la PSR, pero un aumento en la de los genes involucrados a la función inmune. Estos resultados fueron sustentados experimentalmente al constatar que las plantas phr1 eran menos susceptibles a la infección por la bacteria patógena Pseudomonas syringae lo que respalda la sugerencia de que PHR1 regula negativamente a la respuesta inmune (Castrillo et al., 2017; Motte & Beeckman, 2017).
Datos publicados a partir de análisis transcriptómicos y de ChIP-seq han identificado genes involucrados en la respuesta inmune que dependen directa o indirectamente de PHR1. La Figura 4 muestra un grupo de genes de plantas WT de Arabidopsis que están relacionados a la respuesta inmune y que se encuentran desregulados en las plantas phr1. Se pueden reconocer tanto genes regulados positivamente como negativamente, y en ambos grupos se encuentra la presencia del motivo P1BS que los define como blancos potenciales de PHR1 y que además fueron identificados en un ChIP -seq. Estos datos sugieren que PHR1 regula de forma positiva y negativa la expresión de algunos genes que están involucrados en la respuesta inmune y se especula que esta acción prioriza el establecimiento de la PSR y la asociación con la microbiota que permite estimular la adquisición de Pi en condiciones donde este nutrimento es limitante (Chan, Ya-Yun & Tzyy-Jen, 2021).

Figura 4 Genes identificados en Arabidopsis que están
relacionados a la respuesta inmune y que se encuentran regulados
positiva o negativamente. En ambos grupos se encuentran genes
identificados en análisis transcriptómicos que modifican su expresión
con base en la presencia/ausencia de PHR1, este grupo de genes a su vez
fue validado con los resultados obtenidos de un ChiP-seq, que
identificaría blancos potenciales de PHR1 (los que contienen la
secuencia que corresponde al motivo P1BS [  ]), (Modificado de
Bustos et al.,
2010; Castrillo et
al., 2017).
]), (Modificado de
Bustos et al.,
2010; Castrillo et
al., 2017).
Conclusiones
En general, las plantas tienen dificultades para hacer frente a la escasez de Pi y a los patógenos al mismo tiempo. Cuando los recursos de Pi se agotan, PHR1 suprime algunas de las respuestas inmunológicas y prioriza las respuestas a la deficiencia nutrimental al permitir la colonización de la microbiota benéfica que ayuda a captarlo. Esto respalda la idea de que las raíces de las plantas están, por definición, acompañadas por una asociación constante de microorganismos capaces de responder a su escasez (Castrillo et al., 2017; Finkel, Salas-González, Castrillo, Spaepen, Law & Teixeira, 2019). Esta información ha ayudado a comprender que PHR1 representa un punto de convergencia que coordina e integra diferentes vías de señalización y la comprensión de estos mecanismos permitirá el desarrollo de estrategias novedosas para mejorar la resistencia a las enfermedades.











 nueva página del texto (beta)
nueva página del texto (beta)


