Introducción
Las algas marinas pardas del género Sargassum división Phaeophyta, clase Pheophyceae, orden Fucales, familia Sargassaceae, son de amplia distribución en las costas de Europa, Asia, África, Australia, América del Norte y América del Sur (Thinh, Menshova, Ermakova, Anastyuk, Ly & Zvyagintseva, 2013). El hábitat de la mayoría de las especies de Sargassum sp. es sobre las rocas (bentónicas) y muy pocas, en plataformas de marea (pelágicas). Las especies bentónicas crecen entre la parte alta de la zona submareal y la parte baja de la zona intermareal (Norris, 2010). La temporada de crecimiento, los ciclos de reproducción altos y el periodo de crecimiento rápido de los sargazos ocurre en la primavera e inicio del verano (Redmond, Kim, Yarish, Pietrak & Bricknell, 2014).
Los sargazos de las aguas templadas del Océano Pacífico mexicano que están en las zonas rocosas someras, forman “bosques” de gran interés ecológico, medicinal y biotecnológico (Andrade-Sorcia et al., 2014; Pacheco-Ruíz, Zertuche-González, Chee-Barragán & Blanco-Betancourt, 1998; Perumal, Sowmiya, Prasanna Kumar, Ravikumar, Deepak & Balasubramani, 2018). S. sinicola es una de las especies bentónicas que predomina en el Golfo de California, su abundancia es de un 80% muy diferente a las otras algas pardas con las que cohabita. La macroalga se localiza en el Golfo de Santa Clara, costa noroeste de Sonora hasta Cabo San Lucas en Baja California Sur (Norris, 2010; Aguilar-Rosas, Aguilar-Rosas, Mateo-Cid & Mendoza-González, 2002) y la especie está desde Puerto Peñasco, Sonora, a la Isla San Esteban, Baja California Sur, incluida la laguna de Agiabampo, Sonora, y el sistema lagunar Altata-Ensenada en el Pabellón, Sinaloa. Es abundante en los litorales de la Península de Baja California, en las bahías de Guaymas y de Kino, Sonora; (Aguilar-Rosas, Ochoa Izaguire, Aguilar-Rosas, Tovalín Hernández & Páez Osuna, 2009; Andrade-Sorcia et al., 2014; Mateo-Cid, Mendoza-González, Aguilar-Rosas & Aguilar-Rosas, 2017).
Los sargazos se consumen en las poblaciones asiáticas desde hace largo tiempo, ya sean secas o frescas en sopas, platos vegetarianos gourmet, ensaladas y sazonadoras. Desde el siglo pasado se establecieron cultivos de sargazo para garantizar la demanda de los consumidores. En Corea se cultivan S. fusiforme y S. fulvellum y otras especies en desarrollo (Zhao, Zhao, Yao, Lu, Ang & Duan, 2009; Redmond et al., 2014). En China se cultivan S. fulvellum, S. fusiforme, S. horneri, S. thunbergii y S. muticum (Xie, Liu, Jia, Chen & Yang, 2013). El interés por encontrar diferentes usos a las especies pelágicas invasivas del Océano Atlántico y de utilizar especies bentónicas de sargazo, ha suscitado el ánimo por su estudio con el fin de cultivar estas algas en los Estados Unidos de América. Entre las especies bénticas propuestas para esto se encuentran: S. filipendula, S. cymosum, S. polyceratium, S. agardhianum, S. obtusifolium y S. aquifolium. Otras especies son ahora una industria marítima de rápido crecimiento en Nueva Inglaterra, EUA (Kim, Stekoll & Yarish, 2019).
Para que las especies mexicanas de sargazo se aprovechen y se cultiven, es necesario efectuar un análisis químico para evaluar sus propiedades. Por lo anterior, el objetivo de este trabajo fue determinar el efecto de la temporalidad en la composición química de Sargassum sinicola de Guaymas, Sonora, México.
Materiales y métodos
Recolección y preparación de las algas
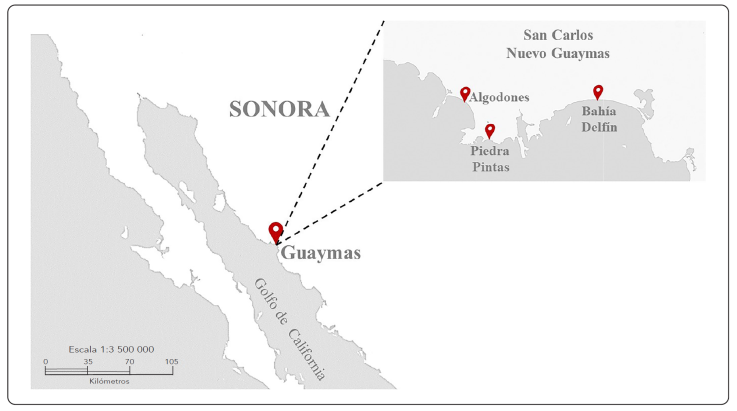
Las algas se colectaron durante el mes de junio de los años 2017 a 2019; además, en el año 2017, en los meses de marzo, mayo y junio, para observar la variación estacional del contenido proximal del sargazo. Los muestreos se realizaron en San Carlos Nuevo Guaymas (Figura 1) en las localidades de San Francisco, Bahía Delfín (27.9591° N, 110.9857° O), Algodones (27.9621° N, 111.0997° O) y Piedras Pintas (27.9389° N, 111.0871° W). En cada lugar se muestrearon de 20-25 kg de algas a la deriva, que fueron transportadas en bolsas de plástico al laboratorio de análisis; se eliminaron las epífitas y el material de interés se identificó con base en las claves taxonómicas de McCourt (1984) y Norris (2010). Las algas se lavaron tres veces con agua corriente sumergiéndolas en agua durante 10 min y se secaron a la sombra hasta alcanzar una humedad ≤ 4 %, determinada por el método 945.09 de la AOAC (2000). Enseguida se tamizaron para eliminar posible arena remanente, se molieron en un molino de aspas (Nutribulet Serie 900, Homeland Housewares, LLC, China); nuevamente se tamizaron con malla de 60 y se envasaron en recipientes de plástico a 25 °C, hasta su posterior análisis.
Análisis proximal
El análisis proximal del alga molida se hizo con los métodos de la AOAC (2000). La humedad se determinó por el método oficial 945.09 (AOAC). El extracto etéreo se obtuvo con equipo Soxhlet, método oficial 920.39 (AOAC). La proteína total se estimó por el método micro-Kjeldahl 976.05 (AOAC). El contenido de proteína se calculó con el factor de conversión 6.25 de acuerdo con Di Filippo-Herrera, Hernández-Carmona, Muñoz-Ochoa, Arvizu-Higuera & Rodríguez-Montesinos (2018) y con el factor 5.38 como sugieren Lourenço, Barbarino, De-Paula, Pereira & Marquez, (2002). El contenido de cenizas se determinó utilizando el método de ignición a 500 °C mufla 923.03 (AOAC). La fibra cruda se obtuvo por el método oficial 962.09 (AOAC). Todos los análisis se hicieron por triplicado, con tres observaciones por réplica. Los carbohidratos se determinaron por diferencia restando la suma de todos los demás componentes al 100% (AOAC, 2000).
Análisis de los macro y microelementos
Para el análisis de los minerales se llevó a cabo una digestión ácida de las muestras y un posterior análisis por espectroscopía de absorción atómica (Agilent Technologies 240FS-AA; Santa Clara, CA, USA). Se analizaron Na, K, Ca, Mg Fe, Zn, Cu y Mn, de acuerdo con las técnicas de la AOAC (2000).
Análisis estadístico
Los resultados se expresan con la media ± desviación estándar (DE). Para el análisis de los datos se utilizó el paquete estadístico NCSS versión 2020 (NCSS, LLC, Utah, USA). Se realizó un análisis de varianza (ANOVA de una vía, p < 0.05) utilizando la prueba de Tukey-Kramer para comparación de medias.
Resultados y discusión
Análisis Proximal
Los valores encontrados en el análisis proximal de S. sinicola recolectado en los años 2017, 2018 y 2019, se muestran en la Tabla I. Se observaron diferencias significativas en el contenido de las proteínas y las cenizas. El contenido de los carbohidratos totales también varió, ya que este parámetro se obtuvo restando la suma de todos los componentes al 100%.
Tabla I Análisis proximal de Sargassum sinicola recolectado en diferentes años. (Media ± Desv. Std.)
| Análisis (%) | Años de colecta | ||
|---|---|---|---|
| 2017 | 2018 | 2019 | |
| Humedad del alga seca | 3.21 ± 0.20 | 2.98 ± 0.03 | 3.0 ± 0.03 |
| Materia seca | 96.79± 0.20 | 97.03 ± 0.02 | 97.00± 0.03 |
| Extracto etéreo | 2.0 ± 0.10 | 1.97 ± 0.40 | 1.99 ± 0.20 |
| Proteína (N x6.25) | 11.2 ± 0.10* | 12.6 ± 0.09* | 10.8± 0.20* |
| Proteína (N x5.38) | 9.64 ± 0.1* | 10.84 ± 0.09* | 9.30 ± 0.20* |
| Cenizas | 38.33± 0.02* | 37.56± 0.05* | 38.91± 0.05* |
| Fibra cruda | 11.86± 0.40 | 11.90± 0.22 | 12.00± 0.16 |
| Carbohidratos totales | 34.96± 0.02 | 34.75± 0.03 | 34.8± 0.01 |
*Indica diferencias significativas entre los años de colecta (ANOVA p< 0.05, Tukey-Kramer).
La proteína representa aproximadamente el 80% del nitrógeno presente en las macroalgas marinas. No obstante, la concentración de la proteína varía dependiendo del tipo de alga: el grupo de las algas cafés a las que pertenece S. sinicola, tiene el porcentaje más bajo de proteína (3% a 15%); las algas rojas presentan entre el 9% y 26% y las verdes hasta un 47% (de Souza Celente, Sui & Acharya, 2023; Vásquez, Martínez & Bernal, 2019; Dawczynski, Schubert & Jahreis, 2007). En nuestro estudio la proteína se calculó por el método de Kjeldahl con dos factores de conversión, el de 6.25 que es el más utilizado (Di Filippo-Herrera et al., 2018; Matanjun, Mohamed, Mustapha & Muhammad, 2009) y el de 5.38 recomendado por Lourenço et al. (2002) quienes realizaron un estudio específico sobre los aminoácidos y las proteínas de las algas pardas. Independiente del factor utilizado, las concentraciones de proteína encontradas en este trabajo, están en el rango de la composición proteica reportada para diferentes especies de sargazos, que va del 8% al 13% (Kumar, Sahoo & Levine, 2015). El contenido de proteína de S. sinicola obtenido en nuestro trabajo al utilizar el factor de conversión de 6.25, fue similar al encontrado por Liu et al. (2020) para S. fusiforme que es una especie ampliamente cultivada en Asia para consumo humano y a los de S. wightii, S. mangarevense, S. henslowianum y S. echinocarpum de los autores Zubia, Payri, Deslandes & Guezennec (2003) y Wong & Cheung (2001). Sucedió lo mismo al emplear el factor 5.38, las cantidades resultantes fueron similares a las de Sargassum vulgare de los estudios de Lourenço et al. (2002). Por otro lado, Carrillo Domínguez, Casas Valdez, Ramos-Ramos, Pérez-Gil & Sánchez Rodríguez (2002) reportaron un contenido de 6.97 ± 0.02 % para S. sinicola colectado durante el mes de mayo, más al sur del Golfo, en Bahía de la Paz, en las costas de Baja California sur. Las condiciones ambientales (salinidad, temperatura externa y temperatura del agua, época del año, humedad relativa y precipitación externas), la ubicación geográfica y la época de colecta, influyen en la composición química de las algas pardas (Balboa, Gallego-Fábrega, Moure & Domínguez, 2016; Toth et al., 2020).
El porcentaje del extracto etéreo encontrado en este trabajo fluctuó entre el 1.93% y el 2.1%, diferente a los datos de Carrillo Domínguez et al. (2002) y Rodriguez Bernal (1995) que fue de 0.6% y de 1.63% para la misma especie, respectivamente. Estos autores reportaron una concentración de cenizas similar al encontrado en este trabajo (~ 37-39 %). En la ceniza los minerales residuales de la biomasa de las algas, son: Na, K, S, Ca, y Mg. De acuerdo con Balboa et al. (2016), Kumar et al. (2015) y Murakami et al. (2011), el contenido de cenizas en los sargazos fluctúa entre el 13.2% y el 41.8%, influenciado por la radiación solar, la concentración salina, la variación estacional y la región geográfica.
El porcentaje de fibra cruda fue alto (de11.46% a 12.16%), cantidad suficiente para promover la peristalsis y la salud intestinal. También se observó un alto contenido de otros carbohidratos (≈ 35 %), característico de los sargazos (Balboa et al., 2016). Entre estos últimos componentes destacan el alginato y el fucoidan, ambos con propiedades nutracéuticas que es necesario analizar a mayor profundidad para esta especie (Di Filippo-Herrera et al., 2018).
La Tabla II presenta las variaciones en composición observadas en los diferentes meses de colecta del año 2017. Los porcentajes del extracto etéreo fueron menores (p<0.05) en mayo y junio, que los encontrados en las algas recolectadas en el mes de marzo. En general, se ha visto que el contenido de lípidos del extracto etéreo, aumenta al disminuir la temperatura del agua; esto debido a los mecanismos de protección de la planta (Nomura et al., 2013). Otras especies de sargazo como S. echinocarpum S. fusiforme y S. obtusifolium presentan porcentajes de extracto etéreo similares a las encontradas para S. sinicola (Meinita, Harwanto, Sohn, Kim & Choi, 2021; Kumar et al., 2015). Aunque los sargazos contienen una pequeña cantidad de lípidos, algunos de ellos son importantes para la salud, como los ácidos grasos poliinsaturados y los ácidos grasos omega 3 (Balboa et al., 2016). Sin embargo, es necesario saber si estos se encuentran presentes en S. sinicola.
Tabla II Variaciones estacionales en la composición proximal de Sargassum sinicola colectado en el año 2017. (Media ± Desv. Std.)
| Análisis (%) | Meses de colecta | ||
|---|---|---|---|
| marzo | mayo | junio | |
| Humedad del alga seca | 3.01 ± 0.20 | 3.18 ± 0.03 | 3.21 ± 0.20 |
| Materia seca | 96.9± 0.20 | 96.8 ± 0.02 | 96.79 ± 0.20 |
| Extracto etéreo | 3.1 ± 0.04* | 2.15 ± 0.04 | 2.00 ± 010 |
| Proteína (N x5.38) | 10.15 ± 0.1* | 9.30 ± 0.09* | 9.64 ± 0.10* |
| Cenizas | 34.4 ± 0.02* | 37.8± 0.02* | 38.33 ± 0.02* |
| Fibra cruda | 13.1 ± 0.21* | 11.0± 0.16* | 11.86 ± 0.40* |
* Indica diferencias significativas entre los meses de colecta de colecta (ANOVA p< 0.05, Tukey-Kramer).
Las concentraciones más altas de proteína se observaron en el mes de marzo, coincidiendo con la fase de desarrollo de las algas (Kumar et al., 2015). Factores externos como la temperatura ambiente, la concentración de nutrientes y la salinidad del agua, también influyen en el contenido proteico. Un ejemplo son las variaciones de proteína encontradas en S. vulgare (9.2-19.9%), influenciadas por factores extrínsecos (Marinho-Soriano, Fonseca, Carneiro & Moreira, 2006). Por lo general, a mayores temperaturas, menor contenido de proteína (Murakami et al., 2011). Tendencias similares fueron observadas en Sargassum hemiphyllum (9- 10 %) por Chan, Cheung & Ang (1997) y en S. horneri (6.3-10.5%) por Balboa et al. (2016). El contenido de proteínas es importante para la valoración de un recurso, tanto para la alimentación de los humanos, como para la del ganado. En el caso de Sargassum spp. del Golfo de California, existen estudios en los que las algas pardas se incluyen como parte de la alimentación de las cabras y las ovejas, siendo un buen suplemento por su contenido de fibra y de proteína (Marín et al., 2009; Cervantes, 2019).
Los valores más altos de ceniza se encontraron en los meses de mayo y junio. El contenido de cenizas en las algas pardas varía considerablemente con la exposición a la radiación solar y a la salinidad del agua de mar. Además, depende del estado fisiológico del alga y de la región geográfica donde habita (Kumar et al., 2015). Sargazos con alta cantidad de ceniza, pueden utilizarse como fertilizantes de suelos y si ese es el propósito de uso, es importante colectarlas en esta época del año. Por el contrario, si la cantidad de ceniza es baja, son adecuadas para la alimentación animal (Balboa et al., 2016).
Análisis de los macro y microelementos
El análisis de los macroelementos en las algas colectadas en diferentes años (Tabla III), presentó diferencias (p<0.05) en el contenido de sodio. Éstas pueden deberse a residuos de arena y agua de mar. Los resultados variaron entre 21.85 mg/g a 23 mg/g siendo similares a los de Rodríguez Bernal (1995) y menores a los de Carrillo Domínguez et al. (2002) ambos, para S. sinicola de Baja California Sur. Una alta concentración de sodio limita el uso del sargazo como fertilizante o como alimento para el ganado. El lavado con agua, la inmersión en agua por varias horas y algunos tratamientos químicos, como el uso de formaldehido al 2 %, seguido de HCl al 0.2 M, disminuyen significativamente el contenido de sodio en las algas, mejorando su potencial de uso (Salgado-Hernández et al., 2023; Fertah, Belfkira, Dahmane, Taourirte & Brouillette, 2017).
Tabla III Análisis de los macroelementos de Sargassum sinicola extraídos en los años 2017, 2018 y 2019. (Media ± Desv. Std.)
| Análisis (mg/g) | 2017 | 2018 | 2019 |
|---|---|---|---|
| Na | 22.2 ± 0.08 | 21.98 ± 0.13 | 23.0 ± 0.03* |
| K | 39.2 ± 0.23 | 40.01 ± 0.01 | 38.92 ± 0.03 |
| Ca | 32.0 ± 0.11* | 32.97 ± 0.04* | 31.02 ± 0.12* |
| Mg | 12.20 ± 0.10* | 12.16 ± 0.09* | 10.8 ± 0.20* |
* Indica diferencias significativas entre los años de colecta (ANOVA p< 0.05, Tukey-Kramer).
En este trabajo el contenido de potasio se situó en el rango de 38.9 mg/g a 40.3 mg/g, diferente al de Carrillo Domínguez et al. (2002) al ser de 55.9 mg/g. El potasio es un macronutriente esencial necesario para el crecimiento y las actividades metabólicas de las algas marinas. En todos los organismos vivos debe existir un balance entre las concentraciones de sodio y potasio (Na+/K+) que debe ser menor a 1.5 (Cofrades et al., 2010). En diferentes géneros de algas cafés las relaciones Na+/ K+ estuvieron entre 0.33 y 1.26 Rupérez (2002). En nuestro trabajo las relaciones Na+/K+ se dieron entre 0.55 y 0.59, que, desde el punto de vista nutricional, son relaciones balanceadas que pueden contribuir al equilibrio de la presión sanguínea. Dietas altas en sodio y bajas en potasio se relacionan con la hipertensión arterial. (Rupérez, 2002).
El contenido de calcio observado en nuestro trabajo fue de alrededor de 32 mg/g, diferente (p< 0.05), en los distintos años de colecta. En los diferentes géneros que conforman a las algas cafés existe una manifiesta variación estacional en la concentración de este mineral que va de 7 mg/g a 68 mg/g en los diferentes géneros que conforman a las algas cafés (Kumar et al., 2015; Balboa et al., 2016; Marín et al., 2009). En varias especies del género Sargassum, el elemento citado disminuye en mayo y aumenta en octubre (Balboa et al., 2016). La bioacumulación de calcio en las algas marinas se ve afectada por el pH, los nutrientes y la salinidad del agua, así como por las variaciones estacionales, la edad, el hábitat del sargazo y por la exposición a las actividades antropogénicas (Kumar et al., 2015) . La concentración de magnesio fue similar a la reportada por Carrillo Domínguez et al. (2002), para la misma especie de S. sinicola de Baja California Sur.
La Tabla IV resume las concentraciones de los micronutrientes analizados. Se observó un alto contenido de hierro, equivalente al encontrado en otras especies de sargazos durante las estaciones cálidas (Balboa et al., 2016) y al reportado por Marín et al. (2009) para Sargassum spp. del Golfo de California Los datos pueden ser de interés para la alimentación humana y animal. Sin embargo, es necesario completar el estudio con un análisis del contenido de metales pesados, ya que los sargazos también captan arsénico, cadmio, plomo y mercurio, entre otros (Nava-Jiménez, Tejeda-Vega, Cortina-Ramírez, Zarazúa-Ortega, Berriozabal-Islas & Sánchez-Hernández, 2022).
Tabla IV Análisis de los microelementos de Sargassum sinicola extraídos en los años 2017, 2018 y 2019. Media ± Desv. Std.)
| Análisis (µg/g) | Años | ||
|---|---|---|---|
| 2017 | 2018 | 2019 | |
| Fe | 220.21 ± 0.08 | 219.98 ± 0.13 | 230.0 ± 0.03* |
| Cu | 9.8± 0.30 | 10.01 ± 0.15 | 11.61± 0.03* |
| Zn | 12.7 ± 0.06* | 11.00 ± 0.04* | 12.57 ± 0.02* |
| Mn | 12.20 ± 0.10 | 12.16 ± 0.09 | 12.18± 0.20 |
* Indica diferencias significativas entre los años de colecta (ANOVA p< 0.05, Tukey-Kramer).
S. sinicola presentó bajo contenido de zinc en comparación con los reportados por Marín et al. (2009) para Sargassum spp. del Golfo de California, (119 µg/g). Sin embargo, fue semejante a S. hemiphyllum (10 µg/g), y para S. miticum colectados durante la misma estación (11µg/g), (Chan et al., 1997; Balboa et al., 2016). En algunos estudios el contenido de Zn en Sargassum spp. decrece a medida que aumenta la temperatura del ambiente (Balboa et al., 2016). Este mismo comportamiento siguen el cobre y el manganeso (Balboa et al., 2016; Kumar et al., 2015).
Conclusiones
El presente trabajo muestra que Sargassum sinicola tiene alto contenido en fibra, porcentajes de proteína similares a los de otras especies de sargazo cultivadas actualmente para consumo humano, bajo contenido en lípidos y alto en potasio, calcio y hierro. Estos valores presentan variaciones estacionales y anuales y en general, son diferentes a la composición química reportada para la misma especie colectada en Baja California Sur. Estos resultados son de interés para estudios posteriores encaminados al uso sustentable de Sargassum sinicola.











 nueva página del texto (beta)
nueva página del texto (beta)