INTRODUCCIÓN
Los microorganismos realizan continuas adapta-ciones metabólicas en respuesta a los cambios ambientales que enfrentan (Stock, Robinson & Goudreau, 2000; Cousin et al., 2013), siendo la fosforilación de proteínas un mecanismo expedito (en comparación con la regulación transcripcional), cuyo carácter de modificación covalente le confiere un tiempo de vida prolongado (Mijakovic,Grangeasse & Turgay, 2016). La fosforilación de proteínas es una modificación post-traduccional (MPT) dinámica y reversible, es decir que el grupo fosfato puede ser incorporado o removido de un péptido mediante la actividad de enzimas especializadas denominadas cinasas y fosfatasas, respectivamente (Macek et al., 2019).
Comúnmente la fosforilación de proteínas conlleva la activación de éstas, promoviendo su actividad enzimática, su localización subcelular o su interacción con otras proteínas. En contraparte, la reacción inversa (desfosforilación) restaura el sistema y lo prepara para responder a un evento de señalización posterior. De acuerdo con lo anterior, es posible asociar la actividad de las enzimas cinasas y fosfatasas como una especie de interruptores moleculares que encienden y apagan elementos celulares en respuesta a diversos estímulos.
Durante varias décadas se consideró que la fosforilación en residuos de serina, treonina y tirosina se encontraba restringida a organismos eucariontes y que en bacterias la MPT predominante correspondía a la fosforilación de residuos de histidina y aspartato, evento canónico de los bien caracterizados sistemas de dos componentes (SDC) (Stock, Robinson & Goudreau, 2000). En los SDC, la proteína cinasa sensora en respuesta a un estímulo resulta autofosforilada (histidina) y posteriormente transfiere el grupo fosfato a la proteína reguladora de respuesta (aspartato), ésta última suele operar como un regulador transcripcional de genes blanco específicos (para consultar una revisión reciente (Jacob-Dubuisson, Mechaly, Bettton & Antoine, 2018)).
No obstante, durante las últimas décadas estudios genómicos evidencian que la prevalencia de genes codificantes de cinasas de serina, treonina y tirosina en procariontes es muy semejante a la de los genes de cinasas de histidina (de los SDC) (Kannan, Taylor, Zhai, Venter & Manning, 2007). Adicionalmente, análisis globales basados en la espectrometría de masas a partir de diferentes organismos modelo procariontes, han demostrado que una fracción significativa de sus proteomas es sujeta a fosforilación en residuos de serina, treonina y tirosina (Macek et al., 2019). Actualmente, diferentes grupos de investigación evalúan las implicaciones de esta MPT en la fisiología procarionte.
A la fecha, la contribución de la señalización a través de la fosforilación en serina y treonina en bacterias se ha asociado con diferentes procesos como son la síntesis de pared y división celular, el metabolismo secundario y la patogénesis (Pereira, Goss & Dworkin, 2011; Dworkin, 2015; Macek et al., 2019; Schastnaya et al., 2021). Las enzimas que realizan esta MPT son las cinasas de serina/treonina (S/T) bacterianas, que forman parte de las cinasas denominadas tipo-Hanks, es decir comparten similitudes catalíticas y estructurales con sus homólogos eucariontes (Pereira et al., 2011). Algunas cinasas S/T procariontes presentan un dominio extracelular que puede ser activado tras el acoplamiento de un ligando, lo que promueve su oligomerización, autofosforilación y la posterior transferencia del grupo fosfato a las proteínas blanco (Manuse, Fleurie, Zucchini, Lesterlin & Grangeasse, 2016). Además, se ha descrito que algunas cinasas S/T fosforilan factores transcripcionales y/o proteínas reguladoras de respuesta de los SDC impactando así en la expresión genética global (Horstmann et al., 2014; Libby, Goss & Dworkin, 2015). Para conocer más de las implicaciones de la fosforilación en S/T y las cinasas tipo-Hanks asociadas referirse a (Bonne Kohler et al., 2020; Nagarajan, Lenoir & Grangeasse, 2022).
La presente revisión se centra en la fosforilación de proteínas en residuos de tirosina y su impacto en la fisiología procarionte.
Cinasas de tirosina bacterianas
La similitud de secuencia de las cinasas S/T bacterianas con sus contrapartes eucariontes facilitó la identificación de genes homólogos en los genomas procariontes. Sin embargo, en el caso de las cinasas de tirosina una aproximación semejante no permite identificar a las enzimas equivalentes en bacterias salvo contadas excepciones, por ejemplo, los trabajos pioneros que caracterizaron a las tirosina cinasas procariontes atípicas, WaaP y MasK (con dominios semejantes a los de cinasas eucariontes), en Pseudomonas aeruginosa (Zhao & Lam, 2002) y Myxococcus xanthus (Thomasson et al., 2002), respectivamente.
Fue hasta finales de la década de los 90 que Grangeasse y colaboradores describieron una nueva enzima en Acinetobacter johnsonii capaz de auto-fosforilarse en tirosina, Ptk (Grangeasse et al., 1997). A partir de este reporte proteínas homólogas a Ptk se describieron en diferentes bacterias y se confirmó la actividad de tirosina cinasa en este grupo de enzimas, distinguiéndose de las cinasas tipo-Hanks eucariontes, tanto por su estructura como por su mecanismo catalítico (Grangeasse, Nessler & Mijakovic, 2012). Por lo anterior y debido a la prevalencia de genes homólogos a ptk en la mayoría de los genomas bacterianos, este grupo de enzimas se unificó como una nueva familia de proteínas denominada cinasas de tirosina bacterianas o BY-cinasas (por sus siglas en inglés, Bacterial tyrosine-kinases) (Chao, Wong & Av-Gay, 2014). Además se desarrolló una base de datos específica denominada BYKdb (https://bykdb.lyon.inserm.fr/BYKdb/) (Jadeau et al., 2008; Jadeau et al., 2012).
La ausencia de homólogos de BY-cinasas en genomas eucariontes o de arqueas sugiere que el ancestro común de las cinasas tipo-Hanks S/T adquirió la capacidad de fosforilar tirosinas posterior a que los grupos Eukarya y Bacteria divergieran, mientras que en Bacteria se desarrolló un mecanismo independiente para fosforilar tirosinas (Grangeasse et al., 2012).
Estructura de las by-cinasas
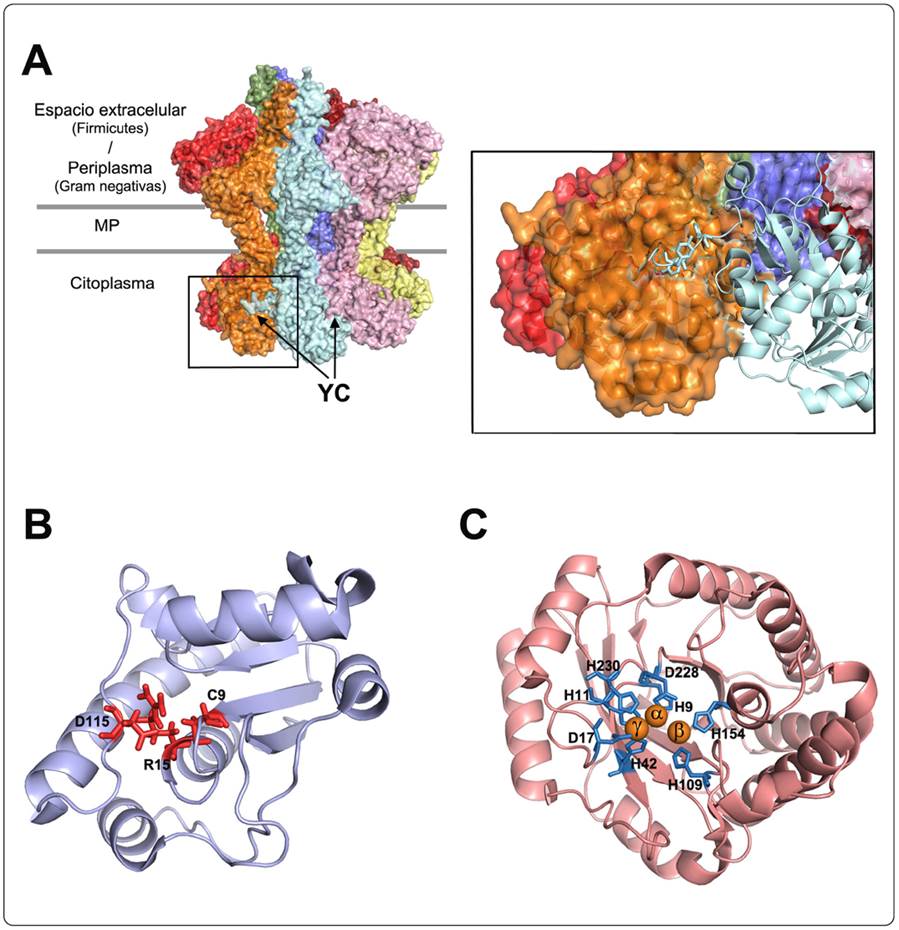
Las BY-cinasas se dividen estructuralmente en 3 regiones, (i) el dominio N-terminal compuesto por dos hélices transmembranales delimitan un bucle que se extiende hacia el espacio periplásmico (Proteobacteria y Actinobacteria), o al espacio extracelular (Firmicutes), se considera que este bucle participa en la percepción de algún estímulo o ligando (Figura 1A). Acorde con lo anterior, mutaciones en un motivo rico en prolinas localizado justo antes del inicio de la segunda hélice transmembranal impactan en la actividad de las BY-cinasas (Grangeasse, Terreux & Nessler, 2010). (ii) El dominio citoplásmico C-terminal, que corresponde al dominio catalítico y contiene los motivos que unen al ATP; Walker A (A/Gx5GK[S/T]) y Walker B (hhhhDxxP), donde x y h corresponden a cualquier residuo y a un residuo hidrofóbico, respectivamente; además de un motivo Walker A’ (hhhhDxDxR) implicado en la unión del cofactor Mg2+. Los motivos Walker son comunes entre las proteínas que unen nucleótidos (Leipe, Koonin & Aravind, 2003), sin embargo, el motivo Walker A de las BY-cinasas solo mantiene bien conservados a los aminoácidos GK[S/T] (Bechet et al., 2009). (iii) El denominado cluster de tirosinas (YC), se localiza en la porción final del extremo C-terminal (últimos 10-20 residuos), y contiene un grupo de 3 a 7 tirosinas, todas éstas substrato de auto-fosforilación (Grangeasse et al., 2012).
Figura, creatividad personal.
Figura 1 Enzimas bacterianas asociadas a fosforilación de tirosinas. (A) Octámero de BY-cinasa Wzc de E. coli (PDB: 7NHR), representación en superficie. Cada subunidad del oligómero se encuentra en diferente color. El YC de la región C-terminal de dos subunidades se indica por las flechas. Izquierda, amplificación del recuadro marcado, la superficie de la subunidad coloreada en cian se retiró para poder visualizar la incorporación de su YC en el sitio catalítico de la subunidad contigua (naranja). Las tirosinas (Y715, Y717 y Y718) de la subunidad en color cian se muestran como barras. (B) Representación en listones de la LMW-PTP Wzb de E. coli (PDB: 2FEK), los residuos catalíticos (C9, R15 y D115) se muestran en barras rojas. (C) Representación en listones de la PHP de Lactococcus lactis subsp. Lactis (PDB: 4GC3), los 3 cationes divalentes (α, β y γ) se muestran como esferas naranjas y los residuos de aspartato e histidina asociados a éstos se indican en barras azules (H9, H11, D17, H42, H109, H154, D228 y H230). La visualización de las estructuras y la preparación de las imágenes se realizaron con PyMol 2.0.
De manera general, en Proteobacteria y Actinobacteria, las BY-cinasas se encuentran codificas por un solo gen que codifica el dominio transmembranal y citosólico de la enzima. En contraste, en Firmicutes los dominios se encuentran codificados por genes independientes, es decir, cada dominio corresponde a péptidos individuales (Grangeasse, Cozzone, Deutscher & Mijakovic, 2007). No obstante, la interacción de ambos péptidos es necesaria para constituir una enzima funcional. Se considera que esta división de los dominios en Firmicutes permite la amplificación de la respuesta, ya que un mismo dominio transmembranal puede interaccionar con más de un dominio citosólico, y a su vez un dominio citosólico con diferentes dominios transmembranales.
En consecuencia, el bucle del dominio transmembranal en Firmicutes y en Actinobacteria es más corto en comparación con el de Proteobacteria. En este último grupo en la parte N-terminal de su dominio citosólico se localiza una región de aproximadamente 20 aminoácidos rica en residuos de arginina y lisina (cluster RK), ausente en el grupo de Firmicutes (Grangeasse et al., 2012).
Las diferencias descritas entre las BY-cinasas llevan a varias hipótesis sobre su evolución dentro del dominio Bacteria, a) una posibilidad es que su ancestro común constaba de un solo péptido que posteriormente se separó en dos en el clado de los Firmicutes, y b) de manera alternativa, es posible que este ancestro estuviera compuesto por dos péptidos, cuyos genes codificantes se fusionaron en el grupo que dio origen a Actinobacteria y a Proteobacteria (Grangeasse et al., 2007).
Por otra parte, los análisis filogenéticos sugieren que las BY-cinasas y las proteínas más relacionadas las ATPasas de arsenito (ArsA) y MinD, divergieron a partir de una ATPasa procarionte común (Grangeasse et al., 2012). Ambos grupos enzimáticos comparten los motivos Walker y la actividad de ATPasa. Las proteínas ArsA son necesarias para expulsar a los iones de arsenito y de antimonito, por otra parte, MinD se ha caracterizado como una ATPasa necesaria para la división celular en bacterias (Rosen, Bhattacharjee, Zhou & Walmsley,1999; Ma, King & Rothfield, 2004).
Mecanismo catalítico de las by-cinasas
A pesar de que aún se desconoce a detalle el mecanismo de acción de las BY-cinasas se piensa que el dominio N-terminal en respuesta a algún estímulo promueve la activación del dominio citosólico. O bien que la fosforilación del YC induce a un cambio conformacional que permite al bucle del dominio N-terminal recibir estímulos externos (Collins et al., 2006; Bechet et al., 2009).
De acuerdo con las estructuras resueltas de las BY-cinasas Etk y Wzc de Escherichia coli y CapAB de Staphylococcus aureus se propone un mecanismo de acción para la familia de las BY-cinasas. Los residuos conservados de lisina y arginina del motivo Walker A, junto con los aspartatos de los motivos Walker B y A’ unen el fosfato del nucleótido y coordinan el Mg2+ (Grangeasse et al., 2010). Un residuo aromático conservado cercano al sitio activo (F547 en Etk) funciona como base para localizar el anillo de la adenina del nucleótido (Lee, Zheng, She & Jia, 2008), y un residuo no polar (F221 en CapA) establece una interacción hidrofóbica con la base del nucleótido y activa el dominio catalítico (Olivares-Illana et al., 2008).
La implementación de versiones de BY-cinasas con mutaciones en el sitio activo reveló la formación de un anillo octamérico, en el que las tirosinas del YC de cada subunidad se encuentran unidas al sitio activo de las subunidades adyacentes, con base en estas evidencias estructurales se propuso que estas enzimas llevan a cabo un proceso de trans-autofosforilación entre las subunidades que componen el oligómero (Bechet et al., 2010; Hajredini & Ghose, 2021) y que el anillo aromático de una de las tirosinas del YC interacciona con los residuos de los motivos Walker B y A´ de la subunidad continua (Figura 1A). En particular, el grupo hidroxilo de la tirosina blanco a fosforilación interactúa con el segundo aspartato del motivo Walker A’, el que probablemente opera como un catalizador ácido en el proceso de trans-autofosforilación (Grangeasse et al., 2012).
El motivo citoplásmico conservado ExxRxxR se ha descrito como importante para estabilizar el estado oligomérico de las BY-cinasas (Olivares-Illana et al., 2008; Bechet et al., 2010; Schwechheimer et al., 2020). Y la fosforilación múltiple del YC de las subunidades del anillo octamérico reduce su estabilidad e induce la disociación de las subunidades y la consiguiente transferencia del grupo fosfato a los substratos endógenos (Nakamoto et al., 2021; Alphonse, Djemil, Piserchio & Ghose, 2022), y/o su desfosforilación por alguna tirosina fosfatasas específica (Temel et al., 2013; Hajredini & Ghose, 2021). Una vez que los dominios citosólicos de las BY-cinasas se encuentran desfosforilados se promueve la oligomerización y el ciclo reinicia (Alphonse et al., 2022).
A diferencia de las cinasas eucariontes, el mecanismo de las BY-cinasas no está ligado al estado de fosforilación de un residuo de tirosina específico, sino a un nivel de fosforilación general del YC. Puesto que la eliminación de una tirosina del YC no afecta la función de la enzima, las alteraciones fisiológicas tienen lugar solo en la ausencia de múltiples residuos de tirosina del YC (Paiment, Hocking & Whitfield, 2002; Morona, Morona, Miller & Paton, 2003).
Fosfatasas de tirosina bacterianas
La actividad de las proteínas cinasas contribuye a la regulación de vías de transducción de señales y de funciones celulares clave en procariontes. La fosforilación tiene un carácter dinámico y las proteínas tirosina fosfatasas (PTP, por sus siglas en inglés) son las enzimas encargadas de regular el efecto de esta MPT, a través de la remoción del grupo fosfato de las proteínas fosforiladas y de las mismas BY-cinasas (Temel et al., 2013).
A la fecha, en bacterias se han identificado numerosas PTP, la mayoría con gran similitud a las enzimas eucariontes (Böhmer, Szedlacsek, Tabernero, Ostman & Den Hertog, 2013). De manera general, las PTP procariontes se categorizan en (i)PTP convencionales de tipo eucariota y fosfatasas de doble especificidad (DSP, por sus siglas en inglés), con actividad contra fosfoserina y fosfotreonina, además de fosfotirosina; (ii) PTP de bajo peso molecular (LMW-PTP, por sus siglas en inglés); y (iii) las fosfatasas polimerasa-histidinol (PHP, por sus siglas en inglés), éste último grupo se encuentra representado por una familia de fosfoesterasas comúnmente presentes en Firmicutes (Bechet et al., 2009).
Mecanismo catalítico de PTP, DSP y LMW-PTP
A pesar de sus diferencias en tamaño, las enzimas PTP convencionales, DSP y LMW-PTP tienen un mecanismo de acción común, éstas comparten el motivo catalítico conservado C(X)5R, localizado en el denominado bucle P, región de unión del grupo fosfato. Los residuos de cisteína y arginina del motivo catalítico son fundamentales para la reacción de desfosforilación (Cirri et al., 1993) (Figura 1B).
La hidrólisis de los ésteres de fosfato de tirosina se lleva a cabo en dos pasos. En primer lugar, tras la formación del complejo enzima-sustrato, la arginina del bucle P interacciona electrostáticamente con la carga negativa de la fosfotirosina, y la cisteína catalítica realiza un ataque nucleofílico hacia el átomo de fósforo del sustrato. La unión del sustrato y la ruptura del enlace éster provoca que el aspartato catalítico (localizado en el bucle D), se aproxime al sitio activo y el aspartato actúe como un ácido en la reacción (Taddei et al., 1994), para la liberación del sustrato desfosforilado al transferirle un protón.
La reacción de sustitución resulta en la unión del grupo fosfato a la cisteína catalítica a través de un enlace covalente tio-fosfato (Zhang et al., 1994). En una segunda reacción de desplazamiento el anión aspartato resultante de la primer reacción, funciona como una base al activar a una molécula de agua para que tenga lugar la hidrólisis del tio-fosfato, se regenere la enzima y se libere fosfato inorgánico (Kolmodin & Åqvist, 2001).
Mecanismo catalítico de las PHP
Las proteínas PHP son parte de la superfamilia amidohidrolasa (AHS, por sus siglas en inglés). Las proteínas AHS incorporan iones metálicos en su sitio activo lo que les permite activar moléculas de agua y realizar el ataque nucleofílico contra los enlaces amida o éster de los sustratos fosforilados (Seibert & Raushel, 2005). Sin embargo, las enzimas PHP se distinguen de las AHS por presentar un plegamiento distorsionado conformado por barriles (β/α)7, además de un sitio activo con 3 cationes divalentes (denominados α, β y γ), unidos a través de residuos de histidina y aspartato conservados (Ghodge et al., 2013) (Figura 1C). El sitio de unión del sustrato en las PHP consta de una región cargada positivamente conformada por cationes divalentes y residuos de arginina que permiten la interacción con el grupo fosfato, además de un centro hidrofóbico con residuos aromáticos (tirosina y/o fenilalanina) que facilitan la unión del anillo imidazol a través de interacciones de apilamiento tipo π (Ghodge & Raushel, 2018).
La reacción enzimática originalmente descrita en las PHP fue la de fosfatasa de ʟ-histidinol fosfato, penúltimo paso en la biosíntesis de la ʟ-histidina (Alifano et al., 1996). Y fue hasta hace dos décadas que la caracterización de los genes asociados con la regulación de la cápsula de Streptococcus pneumoniae evidenció la actividad de fosfotirosina fosfatasa en la proteína CpsB perteneciente a la familia PHP (Morona, Morona, Miller & Paton, 2002). Contrario a las PTP o LMW-PTP, las PHP muestran una actividad óptima a un pH básico y dependen de un ion metálico, por lo general Mn2+.
Péptidos bacterianos que contienen fosfo-tirosinas
Actualmente se desconoce la naturaleza específica de los sustratos de las BY-cinasas, no obstante, estas enzimas deben de distinguir sus proteínas sustrato y los motivos peptídicos que contienen los residuos de tirosina blancos de fosforilación. Cabe mencionar que la ubicación del grupo fosfato en la posición O4 del anillo fenólico de los residuos de tirosina, brinda una característica estructural y energética para los dominios de unión específicos a través de interacciones hidrofóbicas o de tipo π. De acuerdo con estas características los dominios catalíticos de las cinasas y de las fosfatasas específicas para fosfo-tirosinas resultan más profundos (~6 Å), en comparación con los dominios de unión a fosfo-serinas y/o fosfo-treoninas (Hunter, 2014).
La búsqueda de motivos peptídicos en las secuencias reportadas en la base de datos de sitios de fosforilación en bacterias, dbPSP (por sus siglas en inglés) (Pan et al., 2015), no consiguió evidenciar una secuencia consenso conservada en los péptidos que contienen fosfo-tirosinas (situación semejante se presenta en los péptidos que incluyen fosfo-serinas y fosfo-treoninas) (Shi et al., 2020). Sin embargo, de entre los 3,835 registros de fosfo-tirosinas depositados en dbPSP se distingue que éstos localizan preferencialmente a un residuo de glicina en la posición +1 y de lisina en la posición -2, respecto a la fosfo-tirosina (Shi et al., 2020). En concordancia, la implementación de la herramienta Phosphosite logo generator sobre el fosfoproteoma de tirosinas de Shigella flexneri mostró resultados semejantes con una mayor frecuencia de residuos de glicina en las posiciones +1 y -1, y de lisina en la posición -2, respecto a la fosfo-tirosina (Standish et al., 2016). De manera semejante, el análisis de los sitios de fosfo-tirosinas en S. pneumoniae indica una sobre representación de glicina particularmente en las posiciones -3 y -1, respecto a la fosfo-tirosina (Sun et al., 2010). Además, el fosfoproteoma de tirosinas de E. coli muestra una sobre representación de glicina en la posición -1 y de aspartato en la posición +1, respecto a la fosfo-tirosina (Hansen et al., 2013). La comparación iterativa realizada con el algoritmo Motif-X de los fosfo-sitios de E. coli coincide con el enriquecimiento del residuo lisina en diferentes posiciones relativas a la fosfo-tirosina (+3, +4, +5 y -6) (Hansen et al., 2013), lo que sugiere un rol potencial como aceptor de electrones para este amino ácido positivo.
La falta de similitud de los motivos procariontes que contienen fosfo-tirosinas en relación con los motivos eucariontes posiblemente corresponde a las diferencias estructurales y catalíticas de las BY-cinasas respecto a sus contrapartes eucariontes. Por lo tanto, se requiere la identificación y caracterización funcional de más fosfo-sitios procariontes para entender la especificidad de los sustratos de las BY-cinasas.
La fosforilación de tirosinas y su impacto en diferentes funciones celulares
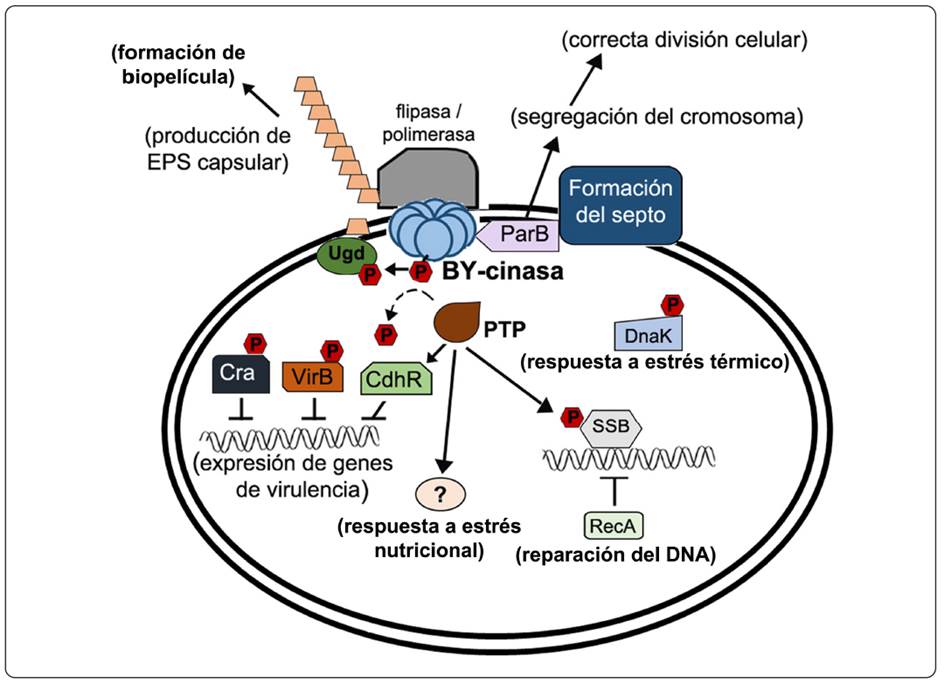
Las primeras descripciones de la fosforilación de tirosinas en bacterias corresponden a los trabajos relacionados con la biogénesis de los polisacáridos capsulares (PC) (Mijakovic et al., 2003; Whitmore & Lamont, 2012). Esto derivado de que la mayoría de los genes codificantes de BY-cinasas y PTP procariontes se encuentran en regiones genómicas implicadas en la biosíntesis de exopolisacáridos (EPS) (Lee & Jia, 2009; Grangeasse et al., 2012) y aunque todavía se desconocen varios aspectos, se considera de manera extendida que la autofosforilación de las BY-cinasas y su consiguiente desfosforilación por parte de las PTP contribuye a la síntesis y exportación de la cápsula bacteriana, y en la formación de biopelícula (Bechet et al., 2010; Schwechheimer et al., 2020) (Figura 2). El estado fosforilado de las BY-cinasas impacta en su capacidad de oligomerizar y se propone que su multimerización, como un octámero, permite que las BY-cinasas operen como una especie de plataforma que localiza a las enzimas flipasa y polimerasa, responsables de la translocación y polimerización de los PC, respectivamente (Bechet et al., 2010). Además, la enzima UDP-glucosa deshidrogenasa (Ugd), que participa en la síntesis de precursores de los PC, se describió como sustrato de las BY-cinasas Wzc y Etk de E.coli. La fosforilación de Ugd modifica su actividad enzimática y la consecuente cantidad de PC en la superficie de la bacteria (Lacour, Bechet, Cozzone, Mijakovic & Grangeasse, 2008).
Figura, creatividad personal.
Figura 2 Fosforilación de tirosinas y regulación de procesos celulares. Octámero de BY-cinasa se indica en azul claro. La enzima fosfatasa (café) se indica como PTP. La formación del oligómero de BY-cinasa funciona como una plataforma para la flipasa y polimerasa de EPS capsular (gris) y se asocia con la localización de la maquinaria responsable de la formación del septo incluyendo ParB. Se indican sustratos a fosforilación en tirosinas descritos en diferentes organismos (Ugd, Cra, VirB, CdhR, SSB y DnaK). Los diferentes procesos celulares en los que éstos contribuyen se escriben entre paréntesis.
En S. aureus, un elegante estudio evidenció una delicada y coordinada regulación durante la biosíntesis de los PC y el peptidoglucano de la pared celular, en la que la actividad de la BY-cinasa CapAB es requerida en distintos pasos del consumo de los precursores lipídicos de los CP (Rausch et al., 2019). De manera semejante se ha descrito que la proteína BY-cinasa CpsCD de S. pneumoniae coordina la síntesis de los PC y el peptidoglucano y que su fosforilación en tirosinas impacta en el tamaño de la cápsula (Nakamoto et al., 2021). Además, en S. pneumoniae se ha reportado que la proteína CpsCD interactúa y modula la movilidad de la proteína ParB (asociada a la segregación del cromosoma) por lo que se propone que la fosforilación de la proteína CpsCD señaliza para coordinar la síntesis de la cápsula y la segregación del cromosoma durante la división celular, lo que garantiza que las células hijas adquieran su envoltura capsular (Henriques, Rodrigues, Carido, Ferreira & Filipe, 2011; Nourikyan et al., 2015). La ausencia de la BY-cinasas CpsCD provoca la acumulación intracelular de PC de bajo peso molecular y condiciona un efecto letal como consecuencia del secuestro de un precursor del peptidoglucano (Nakamoto et al., 2021). La contribución de la fosforilación de tirosinas en la división celular está conservada en S. flexneri donde se ha descrito la fosforilación en tirosinas en la proteína FtsA (Standish et al., 2016), particularmente en un residuo de tirosina previamente identificado como importante para su interacción con FtsZ proteína que interviene en la formación del septo (Pichoff & Lutkenhaus, 2007).
Otro aspecto al que se ha ligado la fosforilación en tirosinas es la respuesta a diferentes tipos de estrés (Figura 2). En Bacillus subtilis se determinó que la proteína de unión al DNA de cadena sencilla, SSB, incrementa significativamente su afinidad por el DNA en su estado tirosina fosforilado, limitando el reclutamiento de RecA (proteína asociada a la reparación del DNA), lo que sugiere que el estado desfosforilado de SSB (a través de la actividad de la tirosina fosfatasa YwqD), es requerido durante la respuesta al daño del material genético (Mijakovic et al., 2006). Además, se ha reportado que la fosforilación de la chaperona DnaK de B. subtilis es requerida durante la respuesta al estrés térmico (Shi, Ravikumar, Derouiche, Macek & Mijakovic, 2016). En Deinococcus radiodurans, se ha descrito que la fosforilación de RecA (proteína implicada en la respuesta SOS) en residuos de tirosina y treonina también impacta en su unión al DNA de doble cadena y en la resistencia del microorganismo a la radiación (Rajpurohit, Bihani, Waldor & Misra, 2016). Por otra parte, en Burkholderia cenocepacia se reportó que la eliminación de la LMW-PTP BPtpA disminuye la capacidad de crecimiento de la bacteria tras su exposición a un estrés nutricional (Andrade, Tavares-Carreon, Khodai-Kalaki & Valvano, 2016), Asimismo, una cepa de B. contaminans mutante de la proteína BY-cinasa BceF tiene una menor tasa de recuperación posterior a un estrés por radiación UV (Ferreira et al., 2013).
Cabe mencionar que la fosforilación de reguladores transcripcionales afecta la expresión de múltiples genes, por ejemplo, en B. subtilis el estado tirosina fosforilado del represor SalA induce un cambio conformacional que deriva en una mayor afinidad por sus sitios blanco (Derouiche et al., 2015). De manera opuesta, en E. coli enterohemorrágica la fosforilación del represor Cra, un regulador transcripcional global implicado en el metabolismo de carbono, parece disminuir su capacidad de unión al DNA, lo que permite la expresión de genes de virulencia en esta bacteria (Robertson, Hazen, Kaper, Rasko & Hansen, 2018). En S. flexneri también se ha reportado que la fosforilación del regulador VirB afecta la expresión de genes de virulencia y su capacidad invasiva (Standish et al., 2016). En Porphyromonas gingivalis se propone que la desfosforilación del regulador transcripcional CdhR (por la LMW-PTP, Ltp1) permite la expresión de la fimbria Mfa1, necesaria para la formación de biopelícula y de comunidades con S. gordonii (Liu, Miller, Wang, Merchant & Lamont, 2017).
Cinasas de tirosina bacterianas que no pertenecen a la familia de las by-cinasas
Como se mencionó, la mayoría de las cinasas de tirosina bacterianas caracterizadas pertenecen a la familia de las BY-cinasas, no obstante, se han descrito algunos otros grupos de enzimas capaces de llevar a cabo la reacción de fosforilación de tirosinas (Tabla I). Entre los primeros reportes de cinasas de tirosina no relacionadas a BY-cinasas se encuentra WaaP de P. aeruginosa, enzima que presenta un mecanismo funcional semejante al de las cinasas eucariontes y cuya actividad es fundamental para la fosforilación de la región central del lipopolisacárido (Zhao & Lam, 2002). Además de MasK de M. xanthus, proteína que también comparte identidad con las cinasas eucariontes y cuya actividad se ha ligado con el control de la motilidad dependiente del pili tipo IV (Thomasson et al., 2002). Recién se describió una nueva familia de cinasas de tirosina denominada Ubk (cinasa bacteriana ubicua, por sus siglas en inglés), estas proteínas tienen baja similitud con las BY-cinasas y cuentan con homólogos en múltiples genomas bacterianos. YdiB de B. subtilis es un representante de la familia Ubk cuya actividad se ha relacionado con la resistencia al estrés oxidativo (Nguyen et al., 2017). La proteína Ubk de S. pneumoniae se describe como esencial para el crecimiento óptimo y la morfogénesis celular de esta bacteria (Pelletier et al., 2019). Por otra parte, en Mycobacterium tuberculosis un grupo de cinasas de serina y treonina de la familia Pkn presentan también actividad cinasa hacia tirosinas (Kusebauch et al., 2014), y aunque estas enzimas se relacionan con diferentes aspectos metabólicos aún se desconoce la contribución específica de su actividad como cinasas de tirosina por lo que son necesarios futuros estudios que ayuden a clarificar la contribución de las diferentes enzimas cinasas y su posible interconexión durante la señalización procarionte asociada a la fosforilación de las tirosinas.
Tabla I Tirosina-cinasas bacterianas.
| Proteínas | Familias | Organismos | Referencias |
|---|---|---|---|
| Ptk | BY-cinasa | A. johnsonni | (Grangeasse et al., 1998) |
| Etk | BY-cinasa | E. coli | (Ilan et al., 1999) |
| Wzc | BY-cinasa | E. coli | (Vincent et al., 1999) |
| CapAB | BY-cinasa | S. aureus | (Olivares-Illana et al., 2008) |
| CpsCD | BY-cinasa | S. pneumoniae | (Morona et al., 2002) |
| WaaP | Kdo/WaaP | P. aeruginosa | (Zhao & Lam, 2002) |
| YdiB | Cinasa bacteriana ubicua (Ubk) | B. subtilis | (Nguyen et al., 2017) |
| MasK | Cinasa de especificidad dual (Serine/Threonine and Tyrosine kinase) | M. xanthus | (Thomasson et al., 2002) |
| PknD | Cinasa de especificidad dual (Serine/Threonine and Tyrosine kinase) | M.tuberculosis | (Kusebauch et al., 2014) |
Comentarios finales
Diversos mecanismos de fosforilación de proteínas ocurren de manera natural en las células bacterianas y resultan necesarios para modular sus procesos fisiológicos en respuesta a los estímulos ambientales, no obstante, el inherente carácter dinámico de las MPT y la intercomunicación entre los diferentes sistemas de fosforilación dificulta la identificación y el análisis cuantitativo de los múltiples sustratos asociados.
En particular, la fosforilación de las tirosinas en bacterias representa una de las MPT más recientemente descritas y por consiguiente se mantiene como un área poco entendida. Al respecto se han conseguido avances considerables en el ámbito estructural y catalítico de las principales enzimas asociadas con la fosforilación en tirosinas, las BY-cinasas. Diferentes evidencias indican que estas enzimas operan como oligómeros acoplando su ensamble/desensamble con su actividad de autocinasa en coordinación con la actividad de sus enzimas fosfatasas específicas. Principalmente estudiadas respecto al metabolismo de polisacáridos extracelulares. Se sugiere que el mecanismo de acción de las BY-cinasas se asemeja a una especie de cronómetro molecular el cual sincroniza la síntesis y exportación de los PC. La coordinación temporal de las BY-cinasas hacia eventos extra-citoplasmáticos es posible que también opere con respecto a los procesos intracelulares que regula la fosforilación en tirosinas, como son la división celular y la respuesta a diferentes condiciones de estrés. En este sentido, la distribución ubicua de las BY-cinasas y su significativa disimilitud respecto a las enzimas tirosina cinasas eucariontes, son aspectos que han incentivado la búsqueda de inhibidores específicos que se pudieran implementar en un contexto infeccioso para limitar la capacidad de proliferación y/o respuesta al estrés de las bacterias patógenas.
Uno de los principales retos que enfrenta el área es el limitado número de fosfopéptidos y además restringidos a pocas especies bacterianas. Por otra parte, los datos proteómicos suelen representar escenarios únicos derivados de una condición particular o un punto temporal del crecimiento celular. Se espera que en un futuro próximo el perfeccionamiento en las técnicas de espectrometría de masas y el enriquecimiento de fosfopéptidos, facilite la detección de MPTs en microorganismos para entender con mayor detalle el papel regulatorio de estas modificaciones, así como su interconectividad durante la regulación del ciclo celular, el crecimiento y la interacción con los hospederos eucariontes.











 nueva página del texto (beta)
nueva página del texto (beta)


