Introducción
Hoy en día el sector industrial a través de sus procesos genera agua residual con desechos químicos que no son tratados de manera adecuada y que terminan en cuerpos de agua como ríos, lagos, mantos acuíferos y el mismo mar contaminándolos. Esto se está convirtiendo en un problema ambiental cada vez más grave, ya que con esto se afectan ecosistemas enteros modificándolos o acabando directamente con los mismos, perjudicando a los organismos de la flora, fauna y los seres humanos. La industria textil y de pesticidas emplean 4-nitrofenol (4-NF) y sus derivados para crear pinturas, colorantes sintéticos, recubrimientos anticorrosivos, herbicidas y pesticidas (Álvarez, 2017).
Se ha reportado que este compuesto está presente en aguas residuales industriales en Bélgica e Italia (Loos et al., 2007), en aguas residuales municipales en Reino Unido (Rodgers et al., 2001), aguas superficiales en Alemania, Japón (Kuch & Ballschmiter, 2001) y Estados Unidos (Fairbairn et al., 2016) y en agua de mar en Norteamérica (Diehl et al., 2012). El 4-NF se obtiene a partir de la reducción de etoxilatos de nonilfenol y se sabe que incluso es más peligroso que sus precursores debido a que presenta riesgos por ser un disruptor endocrino (Kuzikova et al., 2016). También se han evidenciado efectos estrogénicos por presencia de este compuesto (Ying et al., 2002). Según la EPA de Estados Unidos (Environmental Protection Agency por sus siglas en inglés) estableció un límite permitido de >60 μg/L para el 4-NF en agua potable debido a su toxicidad y por su naturaleza contaminante refractaria (Bogireddy et al., 2020). Para la remoción de 4-NF se han empleado muchos métodos como: adsorción, filtración por membrana, osmosis inversa o nanofiltración (Villegas et al., 2016), pero los métodos de adsorción tienen riesgos y es que al cambiar pH, temperatura o concentración inicial la eficiencia de la adsorción se ve afectada. Hay una tecnología para la remoción de 4-NF conocido como catálisis que debido su gran variedad de usos y a su alta eficiencia en reducción o eliminación de contaminantes orgánicos como 4-NF usan radicales libres hidroxilos que son agentes reductores muy fuertes, por ello, esta tecnología ha generado interés en la comunidad científica.
Por otro lado, de entre las propiedades de las nanopartículas (NPs) de metales nobles se encuentran las propiedades catalíticas por su alta actividad química en reacciones de oxidación, lo cual es importante para la reducción de contaminantes orgánicos como el 4-NF; además de su tamaño nanométrico las nanopartículas de oro (AuNPs) poseen propiedades físicas, electrónicas, de fototerapia, y tienen propiedades plasmónicas (Naveen et al., 2017). Por su parte, las nanopartículas de plata (AgNPs) tienen propiedades ópticas, electrónicas, antimicrobianas y plasmónicas (Adewale, et al., 2020) que las hacen potenciales candidatas para ayudar en la descontaminación de aguas residuales, y con esto aportar una mejora a la purificación de aguas residuales para así poder reutilizarse, además de evitar contaminar otros cuerpos de aguas limpias.
Existen diferentes tipos de nanopartículas dependiendo de su origen, que pueden ser orgánicas (se encuentran en la naturaleza) o sintéticas (fabricadas por el hombre). Se distinguen por su dimensión, es decir, dimensión cero si sus tres dimensiones están en la escala nanométrica: Unidimensional (1-D) si dos de sus dimensiones están dentro de la escala nanométrica, Bidimensional (2-D) si una de sus dimensiones están dentro de la escala nanométrica y tercera dimensión (Tooba et al., 2017).
La obtención de las nanopartículas se puede llevar a cabo a través de dos métodos diferentes, el primero es ascendente o químico, donde se usan materiales de tamaño atómico que se hacen crecer a un tamaño nanométrico, y el segundo, el método físico descendente, donde se reduce el material precursor de tamaño grande a tamaño nanométrico (Gaurav et al., 2019).
Recientemente se descubrió una nueva metodología para obtener nanopartículas llamada síntesis verde o de química verde que, a diferencia de los otros métodos mencionados anteriormente que afectan al medio ambiente por sus procesos, este tiene la particularidad de no dañarlo, ya que en este proceso se usan extractos de plantas, frutos, semillas, hongos, etcétera. Por esto y más, la síntesis verde favorece la obtención de nanopartículas y al mismo tiempo no se contamina al medio ambiente, como lo hacen los métodos tradicionales (Mondal et al., 2020). En este trabajo, la reducción de 4-NF a 4-aminofenol (4-AF) se llevará a cabo mediante reducción catalítica porque el 4-AF es menos tóxico que el 4-NF y se utiliza como precursor para la fabricación de paracetamol. Las etapas de síntesis para la fabricación de paracetamol son las siguientes: Nitración de 4-NF, reducción del grupo nitro al grupo amino (4-AP) y acetilación del grupo amino a paracetamol (Mejía & Reddy, 2022).
Desarrollo
En este trabajo mediante la síntesis verde se obtuvieron nanopartículas de oro y plata usando como extracto polvo de semilla de nanche. El nanche es un fruto mexicano, cuyo nombre científico es Byrsonima crassifolia, este se cultiva en los estados sureños desde Michoacán hasta Chiapas, Yucatán y Quintana Roo (sureste) ya que crece bien en la arena y suelos arenosos, alcalinos. En México se genera un total nacional de más de 7 mil toneladas. El nanche tiene forma esférica donde su cascara es de color amarillo, su pulpa color blanco y a veces tiene un sabor dulce o amargo. Esta fruta tiene una semilla hasta el centro de sí misma que es muy dura y de color negro.
Método de obtención
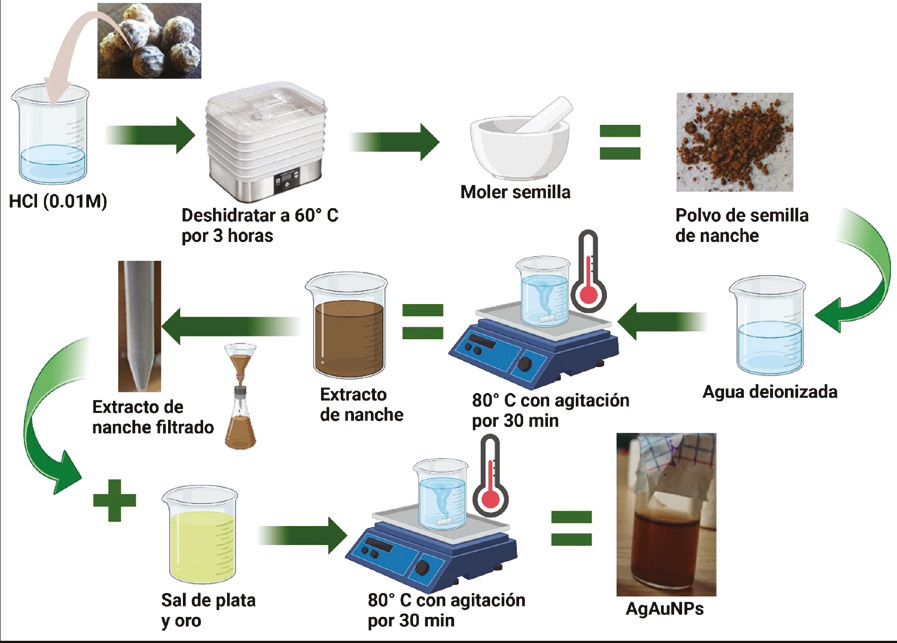
Para la obtención de las nanopartículas de oro y plata se empleó la síntesis verde donde se usó extracto de semilla de nanche, a continuación, la siguiente metodología describe la obtención de las NPs de forma detallada (Figura 1).
Las semillas de nanche se sumergieron en ácido clorhídrico (HCl) (0.01M) para quitar la pulpa, luego se depositaron en un deshidratador a 60 °C por 3 horas. Después, las semillas de nanche se trituraron hasta obtener un polvo fino y se almacenaron en condiciones ambientales. Para preparar el extracto de nanche se agregaron 400 mg de polvo fino en 20 mL de agua desionizada (DI) y se dejó durante 30 min a 80 °C con agitación, por último, se filtraron usando papel de filtro cualitativo.
Preparación de nanopartículas de plata (AgNPs)
Primero se preparó una solución de nitrato de plata (AgNO3; 1 mM) y luego se mezcló con 4 mL de extracto de nanche previamente elaborado para poner dicha solución en un termo-agitador a 80 °C durante 30 min. Al término de esta reacción la solución final cambió de un color transparente a un tono amarillo confirmando la creación de AgNPs.
Preparación de nanopartículas bimetálicas (AgAuNPs)
Para fabricar un sistema bimetálico de Ag y Au primero se generó el extracto de nanche, después se elaboró una solución de nitrato de plata (AgNO3; 1mM) y otra de sal de oro (HAuCl4. 3H2O; 1mM), se añadió 0.2 mL AgNO3 más 0.8 mL HAuCl4. 3H2O en combinación con 4 mL de extracto de nanche y se sometió a 80 °C de temperatura con agitación por 30 min donde el color de la solución cambió pasado ese tiempo a un tono entre amarillo y morado.
Parámetros de catálisis de 4-nitrofenol (4-NF)
Para realizar este proceso es necesario un contaminante (en este caso 4-NF), un reductor (en este caso NaBH4) y un catalizador (en este caso AgNPs y AgAuNPs). Para medir la reducción del contaminante 4-NF por catálisis se utilizó agua desionizada (DI), cierta AgNPs, diferentes cantidades de AgAuNPs, diferentes soluciones de borohidruro de sodio (NaBH4) variando la concentración, también se hicieron 6 soluciones de 4-NF, 5 de estas con agua desionizada a diferente pH, una más con agua de río. La Tabla 1 muestra las cantidades y concentraciones de las soluciones a utilizar en catálisis. Se tomó agua de un río perteneciente al estado de Morelos llamando río Apatlaco, el pH de este río se clasifica entre neutro y medianamente alcalino, al presentar valores entre 7 y 8 unidades. El contenido de materia orgánica en los sedimentos varía entre medio y muy alto. La muestra fue colectada en el sitio El Rayo, ubicado en la corriente principal del río Apatlaco.
Tabla 1 Las cantidades y concentraciones de las soluciones a utilizar durante las reacciones catalíticas
| Medio | Contaminante
4-NF (0.8 mL, 1mM) a diferentes pH |
Concentración y pH
de reductor (0.5 mL; NaBH4) |
Catalizador (1mM) |
| 2.4 mL agua desionizada | Neutro | 50 mM; pH neutro | 0.20 mL AgNPs |
| 0.15 mL AgAuNPs | |||
| 0.20 mL AgAuNPs | |||
| 0.25 mL AgAuNPs | |||
| 100 mM; pH neutro | 0.20 mL AgAuNPs | ||
| 200 mM; pH neutro | 0.20 mL AgAuNPs | ||
| 3 | 200 mM; pH 3 | ||
| 5 | 200 mM; pH 5 | ||
| 9 | 200 mM; pH 9 | ||
| 11 | 200 mM; pH 11 | ||
| 2.4 mL agua de río | Con agua de río | 200 mM en agua de río |
Fuente: Elaboración propia
Discusión y análisis de resultados
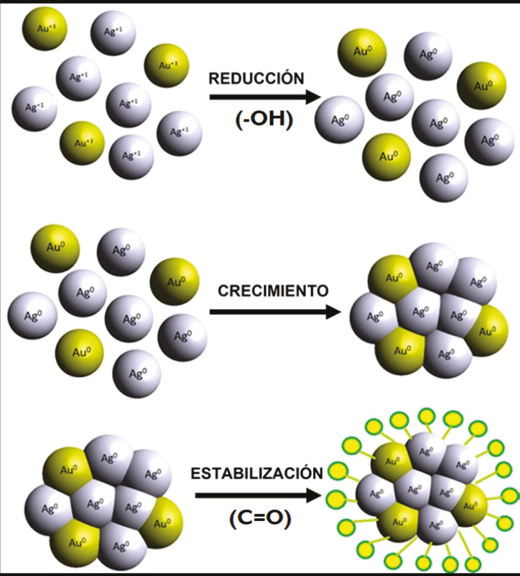
Los espectros de absorbancia UV-Vis (Figura 2a) de las nanopartículas de Ag y AgAu mostraron un pico de resonancia de plasmón superficial (RPS) significativo a 412 nm y 419 nm. Se observa un pico amplio significativo alrededor de 510 nm correspondiente a la RPS de las NP de Au, lo que confirma la fabricación exitosa de nanopartículas bimetálicas en el caso de las NP de AgAu (Bogireddy et al., 2015). El extracto de nanche tiene varios grupos funcionales, pero en este caso, solo interesan los grupos fenólicos (-OH) y carbonilo (C=O), una manera de observar la reacción entre el extracto y las sales metálicas es mediante la caracterización FT-IR, se tomó un espectro FT-IR de polvo de semillas de nanche (antes de la reducción de iones metálicos) y otro espectro FT-IR AgAuNPs (después de la reducción de iones metálicos) y se compararon en un rango de 4500 a 900 cm-1 como se aprecia en la Figura 2b. Es importante destacar el posible mecanismo de reacción de las NPs de oro y plata, ya que los grupos -OH del extracto de nanche reducen los iones de plata de Ag+1 a Ag0 (AgNPs) y Au+3 a Au0 (AuNPs) en el caso de los iones de oro, además el grupo C=O se encarga de darles estabilidad a las AgAuNPs. La Figura 3 presenta el mecanismo de forma visual (Naveen et al., 2017).
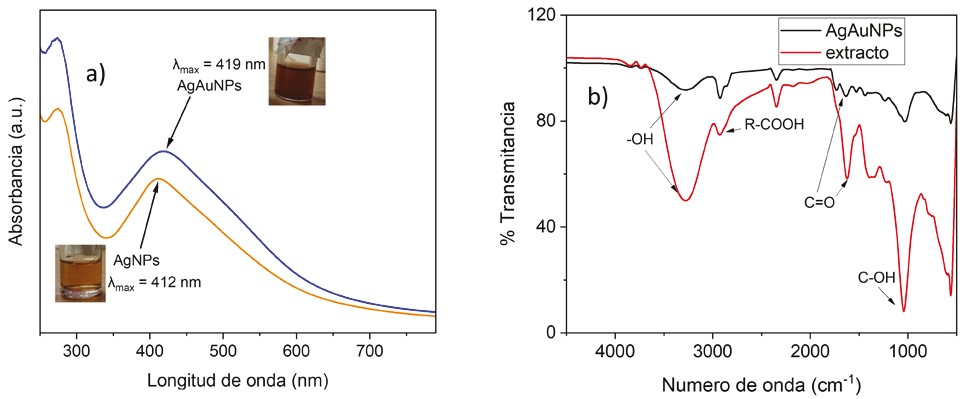
Fuente: Elaboración propia
Figura 2 a) Espectros UV-Vis de absorbancia de Ag NPs y AgAu NPs se registraron en un espectrofotómetro Perkin-Elmer Lambda 950 de doble haz a temperatura ambiente y b) espectros de infra rojo por transformada de Fourier de polvo de nanche y polvo de AgAuNPs a temperatura ambiente, se registraron en un espectrofotómetro FT-IR Varian 660-IR
Reducción de 4-nitrofenol (4-NF)
Para observar la reducción de 4-NF el proceso fue monitoreado mediante espectrofotometría UV-visible en modo de absorbancia. Para medir los espectros de absorbancia se hizo la línea base con agua desionizada para descartar cualquier señal de esta misma, después se mezcló 4-NF con agua desionizada para apreciar la banda máxima del 4-NF, posterior a ello se agregó NaBH4 y se percibió cambio de la banda máxima de 317 nm a 400 nm (ion 4-nitrofenolato) por último, se incorporaron las NPs en la mezcla de 4-NF y NaBH4 donde se observó una disminución en la intensidad del ion 4-nitrofenolato, a la vez que se nota un incremento en 300 nm (4-aminofenol). Este mismo procedimiento se hizo con el agua destilada, de la llave y de río para el análisis del 4-NF. Todos estos análisis se hicieron en un rango de 200 a 800 nm. Esta técnica permite saber la concentración del contaminante antes de la reducción y después de la misma, además se varió la cantidad de catalizador, la concentración de reductor y se varió el pH, también se analizó el proceso de catálisis de 4-NF tomado agua de río para observar si hay algo en esas aguas que influya en el proceso de catálisis.
El 4-NF presenta su banda máxima en 317 nm, que al tener contacto con el agente reductor (NaBH4) presenta un cambio en su banda máxima de 317 a 400 nm, donde este nuevo pico representa un compuesto intermedio de 4-NF llamado ion 4-nitrofenolato (ion 4-NF). Después este compuesto, al mezclarse con las AgAuNPs el ion 4-nitrofenolato se convierte en 4-AF y este compuesto se presenta en 300 nm dentro del espectro de absorbancia UV-Vis en tiempo real o mediciones continuas sin sacar la muestra de espectroscopía (Figura. 4).
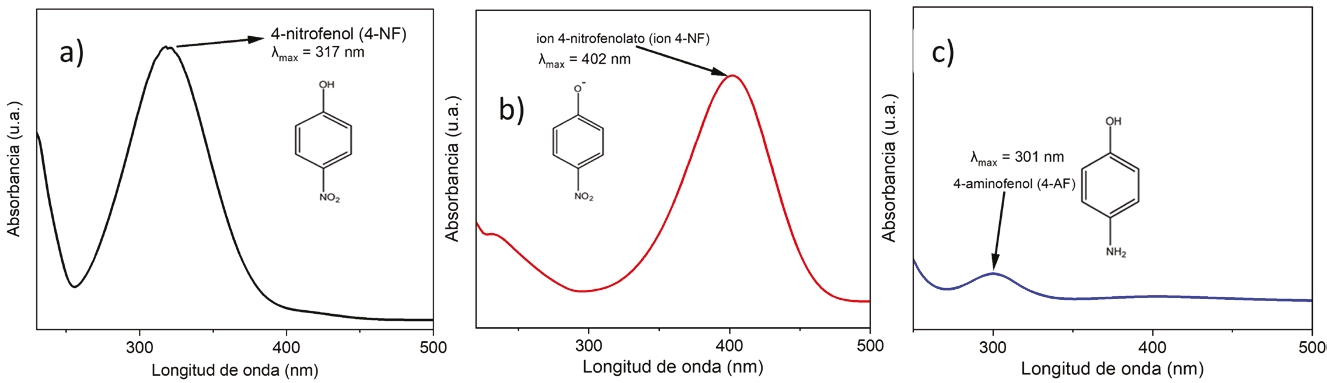
Fuente: Elaboración propia
Figura 4 Actividad catalítica: Espectros de UV-vis de absorbancia de a) 4-nitrofenol, b) ion 4-nitrofenolato y c) 4-aminofenol
La Figura 5 muestra la reducción catalítica del 4-NF (317 nm) donde primero pasa a un estado intermediario de ion 4-nitrofenolato (400 nm) por acción del NaBH4 y con el pasar del tiempo la intensidad de este pico va disminuyendo, posteriormente al tener contacto con las AgAuNPs hay otro cambio en su composición química, pasa de ion 4-nitrofenol a 4-AF, presentando un pico nuevo en 300 nm que incrementa con el tiempo.
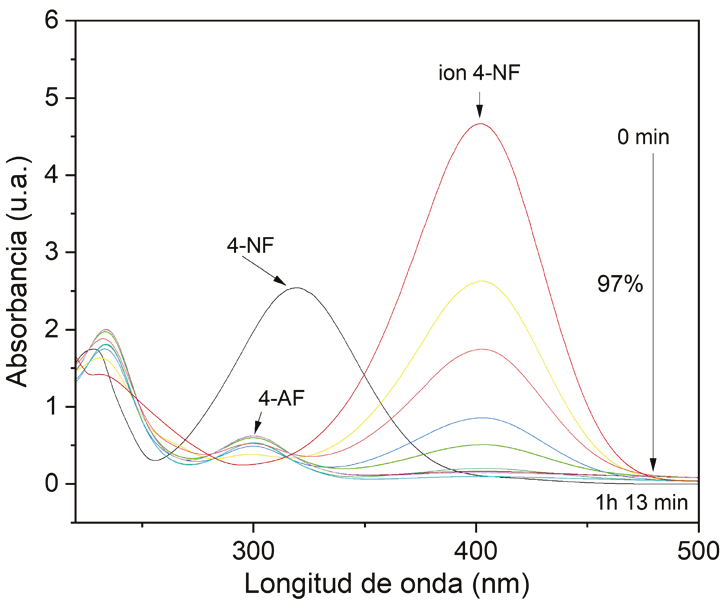
Fuente: Elaboración propia
Figura 5 Espectro UV-Visible de absorbancia en tiempo real de catálisis de 4-NF y NaBH4 (100 mM) en presencia de 0.2 mL de AgAuNPs en agua desionizada
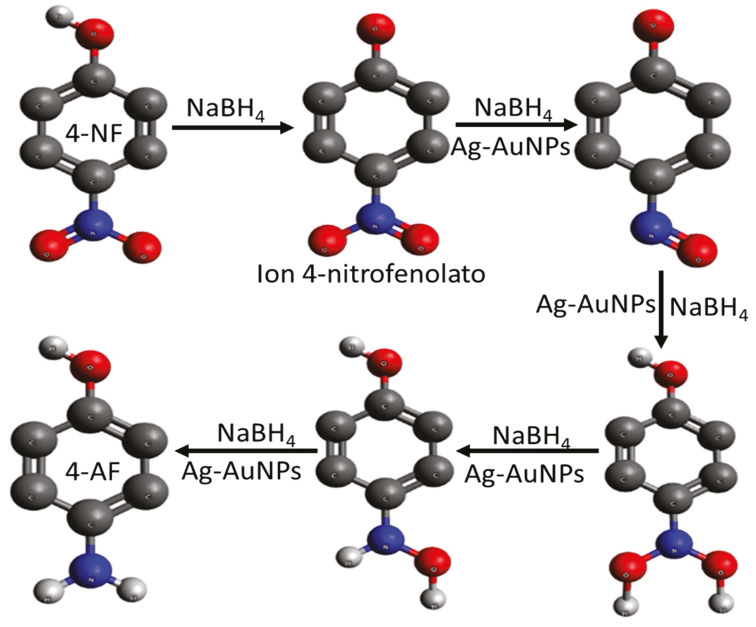
La Figura 6 muestra el posible mecanismo de reducción del 4-NF donde en el primer paso se observa un cambio en la estructura química del 4-NF a un compuesto intermedio del mismo llamado ion 4-nitrofenolato por tener contacto con el reductor NaBH4, ya que este funciona como una fuente de H+. Esto genera la protonación del ion 4-nitrofenolato en la parte donde tiene un enlace C-O. Posteriormente al agregar el catalizador (AgAuNPs) el compuesto de ion 4-nitrofenolato tiene más cambios en su composición química, principalmente en su grupo nitro que cambia a grupo nitroso, convirtiendo la molécula en 4-AF.
La solución de 4-NF tiene un color verde-amarillo, al agregar el agente reductor (NaBH4), la solución de 4-NF cambió su color de verde-amarillo a amarillo-pálido (ion 4-nitrofenolato) y al agregar el catalizador (AgNPs y AgAuNPs) después de un tiempo, la solución se tornó transparente (Figura 7).
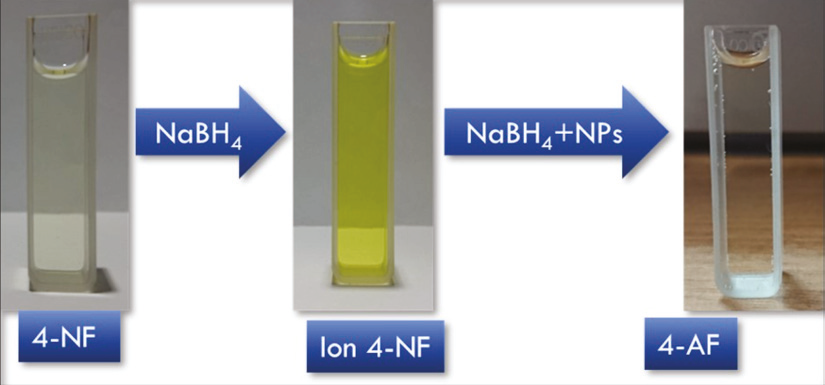
Fuente: Elaboración propia
Figura 7 Proceso de reducción de 4-nitrofenol a 4-aminofenol de forma visual
La siguiente tabla describe los tiempos registrados y el % reducción de 4-NF durante el proceso de reducción, variando los parámetros de catálisis en donde se observa que la solución con menos cantidad de catalizador tiene un tiempo de reducción muy largo, también la solución que solo tiene AgNPs; donde a medida que aumentan el tiempo se reduce, lo mismo pasa con la concentración del agente reductor. Se observa que a pH ácidos la catálisis toma más tiempo. Cabe mencionar que se compararon estos análisis con anteriores trabajos donde se destaca el tiempo de reducción del 4-NF. Lubna Sherin y colaboradores redujeron 4-NF con AgNPs en 60 min (Sherin et al., 2020), Malik et al. (2021) redujeron 4-NF en 45 min con AgAuNPs en este trabajo se redujo 4-NF en tan solo 22 min con AgAuNPs.
Tabla 2 Resultados del proceso de catálisis variando parámetros
| Parámetros | Tiempo de reducción | Reducción de 4-nitrofenol (%) |
| DI + 4-NF + NaBH4 + 0.20 mL AgNPs | 51 min | 43 |
| DI + 4-NF + NaBH4 (50mM) + 0.15mL AgAuNPs | 1h 50 min | 84 |
| DI + 4-NF + NaBH4 (50 mM) + 0.20mL AgAuNPs | 1h 26 min | 99 |
| DI + 4-NF + NaBH4 (50mM) + 0.25mL AgAuNPs | 1h 24 min | 86 |
| DI + 4-NF + NaBH4 (100mM) + 0.20mL AgAuNPs | 1h 13 min | 97 |
| DI + 4-NF + NaBH4 (200mM) + 0.20mL AgAuNPs | 30 min | 96 |
| pH3: DI + 4-NF + NaBH4 (200mM) + 0.20mL AgAuNPs | 1h 30 min | 75 |
| pH5: DI + 4-NF + NaBH4 (200mM) + 0.20mL AgAuNPs | 58 min | 95 |
| pH9: DI + 4-NF + NaBH4 (200mM) + 0.20mL AgAuNPs | 24 min | 98 |
| pH11: DI + 4-NF + NaBH4 (200mM) + 0.20mL AgAuNPs | 19 min | 97 |
| Agua de río + 4-NF + NaBH4 (200mM) + 0.20mL AgAuNPs | 22 min | 96 |
Análisis prospectivo
Es necesario valorar el uso de materia prima a partir de residuos reciclados para producir nanopartículas metálicas. Además, los procedimientos rápidos y simples son esenciales para desarrollar sondas catalíticas reciclables para aumentar la eficiencia catalítica. Suponemos que la próxima investigación de sondas catalíticas que utilizan nanopartículas metálicas basadas en precursores sustentables ampliará la conciencia de la audiencia general y la comunidad científica sobre su aplicación de eliminación de la contaminación debido a su simplicidad, accesibilidad y compatibilidad.
Conclusiones
Los resultados demostraron que usando extracto de semilla de nanche se redujeron los iones metálicos a NPs, además este extracto mantuvo estables a las mismas. Con la variación de parámetros para catálisis las NPs demostraron la total reducción del contaminante 4-NF. También cabe mencionar que un catalizador de partículas bimetálicas (AgAuNPs) favorece más el proceso de catálisis minimizando el tiempo de reducción del 4-NF. Otro punto para destacar es que mientras más concentrado está el agente reductor la catálisis toma menos tiempo. Por otro lado, hay que mencionar que a mayor concentración de catalizador, se reduce más el tiempo de reacción, así como a pH más básico, el proceso es más rápido. Por último, la catálisis en agua de río fue más rápido en comparación con los análisis en agua desionizadas, ya que se observa una reducción de tiempo del proceso en agua de río y en agua de desionizada. Los análisis en aguas reales destacan por mucho respecto a los otros análisis, se tiene una hipótesis de que, en esas aguas hay alguna propiedad que hace acelerar el proceso de la catálisis. Además, con el respeto de limitaciones del estudio todavía falta analizar el agua de acuerdo con las normas que existen antes usar la misma.











 nueva página del texto (beta)
nueva página del texto (beta)